複合体粒子
【課題】 水溶性高分子により水系溶媒中で分散させた酸化チタン複合体に対して、水溶性高分子を変質させることなく結合させたリンカー分子を介して抗体を修飾することで、分散性と触媒活性を失うことなく選択的な結合能を付与した、複合体粒子の提供。
【解決手段】 本発明は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させ、さらにリンカー分子を介して抗体を修飾した、酸化チタン−抗体複合体であることを特徴とする複合体粒子である。この複合体粒子は患部に集積し、診断または超音波照射と併せた治療のための薬剤として利用できる。
【解決手段】 本発明は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させ、さらにリンカー分子を介して抗体を修飾した、酸化チタン−抗体複合体であることを特徴とする複合体粒子である。この複合体粒子は患部に集積し、診断または超音波照射と併せた治療のための薬剤として利用できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を酸化チタン表面に結合させ、さらに該リンカー分子を介して抗体が結合されてなり、超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とする、複合体粒子に関する。
【背景技術】
【0002】
酸化チタンはpH6前後に等電点を有すると言われている。このため、酸化チタン粒子は中性付近の水系溶媒中では凝集を生じてしまい、これを均一に分散させることは極めて難しい。そのため、酸化チタン粒子を水系の分散媒に均一に分散させるため、今まで種々の試みがなされてきた。
【0003】
PEG(ポリエチレングリコール)を分散剤として添加して、分散媒中における酸化チタン粒子の分散性を向上させることが知られている(特許文献1(特開平2−307524号公報)および特許文献2(特開2002−60651号公報)参照)。
【0004】
あるいは酸化チタン微粒子に、ポリアクリル酸等の親水性高分子を、カルボキシル基を介して結合させた、表面改質酸化チタン微粒子も知られている(特許文献3(WO2004/087577)参照)。この技術は、ポリアクリル酸等といったアニオン性ポリマーの使用を念頭としたものである。アニオン性ポリマーのもつカルボキシル基等の官能基により表面電荷を与え、それにより生体内環境に近い中性の生理食塩水においても安定した分散性を示し、かつ紫外線照射時の光触媒活性機能を有するものである。
【0005】
更に、酸化チタンに機能性を付与する検討がなされている。例えば、前記表面改質酸化チタン微粒子に対して、前記親水性高分子の結合に関与していないカルボキシル残基に、目的分子に対して特異的な結合能を有する分子を固定化した、分子識別能を有する二酸化チタン複合体が提案されている(特許文献4(特許第3835700号)参照)。この技術は、アニオン性ポリマーのもつカルボキシル基等の官能基により、分子が固定化されていても表面電荷を与え、安定した分散性を示すものである。一方で、官能基によって与えられる表面電荷は分散性に直接寄与しており、結合に関与していない残基に分子を固定化することで表面電荷は減少する。このことが固定化される分子の量等に対して制限を与える。
【0006】
【特許文献1】特開平2−307524号公報
【特許文献2】特開2002−60651号公報
【特許文献3】WO2004/087577号パンフレット
【特許文献4】特許第3835700号公報
【発明の開示】
【0007】
本発明は、水溶性高分子により水系溶媒中で分散性を保ち、超音波の照射による触媒活性を有する酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を介して抗体を修飾することで、分散性と触媒活性を失うことなく選択的な結合能を付与した酸化チタン−抗体複合体粒子であることを特徴とする複合体粒子、および該複合体粒子を含んでなる抗腫瘍剤の提供をその目的としている。
【0008】
本発明者らは、今般、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させることにより、前記水溶性高分子を変質させることなく、分散性と触媒活性を保ちながら、新たに抗体を付与することが可能である、との知見を得た。
【0009】
すなわち、本発明によれば、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面にリンカー分子を結合し、さらに該リンカー分子を介して抗体を結合させることにより、水溶性高分子を変質させることなく高い分散性を保持し、なおかつ超音波の照射による触媒活性を有し、さらに抗原と結合可能な酸化チタン−抗体複合体粒子であることを特徴とする複合体粒子を作製することができる。複合体粒子が抗原と結合している状態で超音波照射をすることで、ラジカル種と抗原との反応性を高めることが期待できる。抗原が癌細胞もしくは新生血管等の癌近傍組織に由来する場合にあっては、複合体粒子を患部である癌近傍に集積させ、さらに超音波照射を行うことで高い抗腫瘍効果を得ることができる。よって本発明の複合体粒子は抗腫瘍剤としての使用が可能である。該抗腫瘍剤は、患部に集積させ、さらに超音波を照射することにより行われる超音波癌治療を促進する薬剤として好適に利用可能である。
【0010】
そして、本発明の複合体粒子は、
酸化チタン粒子と、
該酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を介して結合されてなる水溶性高分子を含んでなる、酸化チタン複合体と、
該酸化チタン複合体の表面に、さらに結合されてなるリンカー分子を含んでなり、該リンカー分子は、
(1)カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を有し、
(2)a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物であって、
該官能基を介して前記酸化チタンと結合され、
該官能基同士で重合すること無く、
さらに該リンカー分子を介して抗体が結合されてなり、
超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とするものである。
【0011】
また、本発明による分散液は、複合体粒子と、該複合体粒子が分散される溶媒とを含んでなるものである。
【0012】
本発明によれば、水溶性高分子により水系溶媒中で分散性を保ち、超音波の照射による触媒活性を有する酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を介して抗体を修飾することで、分散性と触媒活性を失うことなく選択的な結合能を付与した酸化チタン−抗体複合体であることを特徴とした複合体粒子およびその分散体を提供できる。
【0013】
また、本発明による抗腫瘍剤は、複合体粒子または複合体粒子が分散された分散液を含んでなるものである。
【発明を実施するための最良の形態】
【0014】
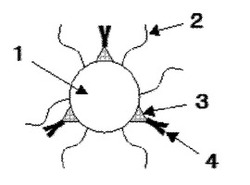
本発明の複合体粒子は、酸化チタン粒子と、水溶性高分子と、リンカー分子と、抗体とからなる酸化チタン−抗体複合体を含む。図1に、複合体粒子の一例を示す。図1に示されるように、複合体粒子は、酸化チタン粒子1の表面に水溶性高分子2およびリンカー分子3を介して抗体4が結合されたものである。酸化チタン粒子1と、水溶性高分子2およびリンカー分子3との結合は、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を介して形成される。
【0015】
すなわち、これらの官能基は酸化チタンとの間で強固な結合を形成するため、酸化チタン粒子の高い触媒活性に関わらず分散性を保持できる。また、リンカー分子を介して抗体の結合を保持することが可能である。なお、本発明における結合形態は、体内における安全性の観点から、体内への投与後24〜72時間後に分散性が確保されている程度の結合形態であればよい。生理条件での分散が安定しており、かつ超音波照射後も水溶性高分子の遊離が無く、正常細胞へのダメージが少ない点で、共有結合であるのが望ましい。
【0016】
カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基は、3官能シラノール基のような相互に三次元的に縮合重合して重合物で酸化チタン粒子の表面を覆い尽くしてしまう官能基とは異なり、官能基同士で重合することが無いため、図1に示されるように酸化チタン粒子の表面に剥き出しの部分を確保することができると考えられる。その結果、表面が重合体で覆われることによって起こりうる失活を抑制しつつ、酸化チタン粒子の触媒活性を十分に発揮させることができる。
【0017】
そして、酸化チタン粒子の表面に結合した水溶性高分子は、電荷あるいは水和の作用によって、酸化チタン粒子の分散が困難とされる中性付近の水系溶媒中であって、本発明の複合体粒子を分散させることができる。抗体を、酸化チタン粒子の表面に結合した水溶性高分子に対して導入する方法については公知である。このような場合は、水溶性高分子と抗体を化学結合するために、水溶性高分子は反応性の高い極性基を含んでなることが必要である。この水溶性高分子に含まれる極性基は、抗体が結合されると失われる。このことにより、水溶性高分子の極性自体に変化が生じる。つまり、酸化チタン粒子の表面に結合した水溶性高分子のもつ電荷あるいは水和の作用によって分散しているバランスが、抗体の結合前後において変化すると考えられる。この酸化チタン粒子の表面に結合した水溶性高分子の変質に伴う電荷あるいは水和のバランスをうまくコントロールすることでのみ達成しうる。一方、本発明における酸化チタン粒子の表面に結合したリンカー分子を介して結合した抗体については、水溶性高分子を変質させることなく結合させることにより、水溶性高分子による高い分散性を保持できる。このため、水溶性高分子の変質によって生じる分散性の変化を考慮することなく、抗体の結合に際して自由度の高い分子設計が可能である。
【0018】
本発明の複合体粒子によれば、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面にリンカー分子を結合し、さらに該リンカー分子を介して抗体を結合させることにより、水溶性高分子を変質させることなく高い分散性を保持する酸化チタン−抗体複合体であることを特徴とする抗腫瘍剤を作製することができる。このように抗体を結合することにより、本発明の複合体粒子が抗原と結合することを可能とする。また、本発明の複合体粒子に対して超音波照射をすることでラジカル種を発生することができる。一般的にラジカル種は高い反応性をもつが寿命が短く、ごく僅かに拡散して近傍の物質と反応する。このため、本発明の複合体粒子が抗原と結合している状態で超音波照射をすることで、ラジカル種と抗原との反応性を高めることが期待できる。抗原が癌細胞もしくは新生血管等の癌近傍組織に由来する場合にあっては、本発明の複合体粒子を患部である癌近傍に集積させ、さらに超音波照射を行うことで高い抗腫瘍効果を得ることができる。よって本発明の複合体粒子は、抗腫瘍剤として使用することができる。そして、本発明の複合体粒子は、投与後に患部へ集積させ、さらに超音波を照射することにより行われる超音波癌治療を促進するための薬剤としての効果を期待できる。
【0019】
また、本発明の複合体粒子によれば、酸化チタン−抗体複合体の酸化チタン表面に対し、リンカー分子を介して光応答性の分子や放射性物質を結合することで、水溶性高分子を変質させることなく高い分散性を保持することができる。特に、放射性物質に関しては、安全性の観点からなるべく少ない工程で用いることが必要であるが、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体に対して、酸化チタン表面に放射性物質を結合した後に、未結合の放射性物質を適当な方法で分離除去するだけの、簡易でかつ少ない工程によって粒子の標識ができる。このため、放射性物質が外部に広がる機会が少なく、安全性の面において優れる。また、これを適当な機器により測定することで粒子のイメージングや定量の測定が可能である。そのため、本発明の複合体粒子は、体内に投与後に体内動態を確認するためのトレーサー実験用材料や、患部に超音波照射することにより行われる診断および治療のための医療用材料としても利用可能である。
【0020】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介して結合されてなることが好ましい。これによって、酸化チタン粒子の表面に強固に結合することが可能であり、また、3官能シラノール基のような相互に三次元的に縮合重合して重合物で酸化チタン粒子の表面を覆い尽くしてしまう官能基とは異なり、官能基同士で重合することが無いため、図1に示されるように酸化チタン粒子の表面に剥き出しの部分を多く確保することができると考えられる。その結果、表面が重合体で覆われることによって起こりうる失活を抑制し、酸化チタン粒子の触媒活性を十分に発揮させることができる。
【0021】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、酸化チタン−抗体複合体を水系溶媒中で分散させることができれば特に限定されない。本発明に用いる水溶性高分子において、電荷を有するものとしては、アニオン性またはカチオン性を有する水溶性高分子、また、電荷を有さずに水和によって分散性を与えるものとしてはノニオン性を有する水溶性高分子が挙げられ、これらの少なくとも一種を含んでなる。
【0022】
本発明の好ましい態様によれば、前記水溶性高分子は重量平均分子量2000〜100000である。水溶性高分子の重量平均分子量はサイズ排除クロマトグラフィーを用いて求めた値である。前記分子量をこの範囲とすることで、水溶性高分子のもつ電荷あるいは水和の作用によって、酸化チタン粒子の分散が困難とされる中性付近の水系溶媒中であって酸化チタン−抗体複合体を分散させることができる。
より好ましい範囲は5000〜100000であり、さらに好ましくは5000〜40000である。
【0023】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、アニオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。アニオン性を有する水溶性高分子は、複数のカルボキシル基を有するものが好適に利用可能であり、例えばカルボキシメチルデンプン、カルボキシメチルデキストラン、カルボキシメチルセルロース、ポリカルボン酸類、およびカルボキシル基単位を有する共重合体(コポリマー)などが挙げられる。具体的には、水溶性高分子の加水分解性および溶解度の観点から、ポリアクリル酸、ポリマレイン酸等のポリカルボン酸類、およびアクリル酸/マレイン酸やアクリル酸/スルフォン酸系モノマーの共重合体(コポリマー)がより好適に使用され、さらに好ましくはポリアクリル酸である。
【0024】
アニオン性を有する水溶性高分子として、ポリアクリル酸を用いる場合、分散性の観点からポリアクリル酸の重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000であり、さらに好ましくは5000〜20000である。
【0025】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、カチオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。カチオン性を有する水溶性高分子は、複数のアミノ基を有するものとしてが好適に利用可能であり、例えばポリアミノ酸、ポリペプチド、ポリアミン類、およびアミン単位を有する共重合体(コポリマー)などが挙げられる。具体的には、水溶性高分子の加水分解性および溶解度の観点から、ポリエチレンイミン、ポリビニルアミン、ポリアリルアミン等のポリアミン類がより好適に使用され、さらに好ましくはポリエチレンイミンである。
【0026】
カチオン性を有する水溶性高分子として、ポリエチレンイミンを用いる場合、分散性の観点からポリエチレンイミンの重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000であり、さらに好ましくは5000〜20000である。
【0027】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、ノニオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。ノニオン性を有する水溶性高分子は、好ましくは水酸基および/またはポリオキシアルキレン基を有する高分子が挙げられる。そのような水溶性高分子の好ましい例としては、ポリエチレングリコール(PEG)、ポリビニルアルコール、ポリエチレンオキシド、デキストランあるいはそれらを含有するコポリマーが挙げられ、より好ましくはポリエチレングリコール(PEG)およびデキストランであり、さらに好ましくはポリエチレングリコールである。
【0028】
ノニオン性を有する水溶性高分子として、ポリエチレングリコールを用いる場合、分散性の観点からポリエチレングリコールの重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000である
【0029】
以上に例示した水溶性高分子は、本発明の複合体粒子の分散性を妨げない範囲内において、これまでに記載した各要素を自由に組み合わせることができる。
【0030】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、酸化チタン粒子表面に結合してなるが、該機能性分子はカルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を有する。
【0031】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物である。
【0032】
上記炭素数よりなるリンカー分子は、前記水溶性高分子と比べて分子の大きさが小さい。また、リンカー分子は酸化チタン表面に結合してなる。このため、本発明の酸化チタン−抗体複合体において、外殻に水溶性高分子が位置するのに対し、より内部の位置にリンカー分子を有する構造をとる。該外殻は本発明の複合体粒子の分散性に対する影響が最も大きい。すなわち外殻に位置する水溶性高分子に対して、内部に位置するリンカー分子が分散性に与える影響は小さくなり、好適に用いることができる。
【0033】
本発明の複合体粒子に結合されたリンカー分子の量は、酸化チタン粒子の質量:1gあたり1.0×10−6〜1.0×10−3 molであり、より好ましくは1.0×10−6〜1.0×10−4 mol/酸化チタン粒子‐gである。
この範囲であると、本発明の複合体粒子は生体内環境に近い、10%タンパク質溶液を溶媒としても分散することができるため、好適に用いることができる。さらに、この範囲であると、本発明の複合体粒子は超音波を照射する際に触媒活性を有し、ラジカル種を発生することができるため、好適に用いることができる。
【0034】
そのようなリンカー分子の例としては、芳香族化合物やアルキル構造をもつ分子等が考えられ、より具体的には、ベンゼン環をもつ分子として、カテコール、メチルカテコール、ターシャリーブチルカテコールドーパ、ドーパミン、ジヒドロキシフェニルエタノール、ジヒドロキシフェニルプロピオン酸、ジヒドロキシフェニル酢酸等の、分子内にカテコールの構造を有する、カテコール類などが挙げられる。また、他の環状分子として、フェロセン、フェロセンカルボン酸、アスコルビン酸、ジハイドロキシシクロブテンジエン、アリザリン、ビナフタレンジオール等が好適に使用できる。さらに、アルキル構造をもつ分子としては、ヘキシル基、オクチル基、ラウリル基、パルミチル基、ステアリル基などのアルキル基を有する分子が挙げられる。あるいは、ヘキセニル基、オクテニル基、オレイル基などのアルケニル基、または、シクロアルキル基などの飽和又は不飽和脂肪族炭化水素基をもつものなどが挙げられる。
【0035】
以上に例示したリンカー分子およびその量は、これまでに記載した各構成要素と好適に組み合わせることができる。
【0036】
本発明の好ましい態様によれば、リンカー分子を介して結合する抗体としては、特に制限はないが、本発明の複合体粒子を積極的に癌部位へ集積させるため、該抗体の抗原が癌細胞もしくは新生血管等の癌近傍組織に由来することが望ましい。あるいは、抗体をFab領域等に低分子化させたフラグメントを用いることも何ら問題はない。
【0037】
また、本発明の複合体粒子を積極的に癌部位へ集積させるため、リンカー分子を介して結合する分子は抗体に限らず、例えば癌細胞もしくは新生血管等の癌近傍組織に由来する部位と相互作用を示すペプチドやアミノ酸配列であってもよい。より具体的には5−アミノレブリン酸、メチオニン、システイン、グリシン等が挙げられる。あるいは、糖鎖を含んでもよい。さらに、結合性を有する核酸を含んでいても良い。核酸としては、特に制限はなく、DNA、RNA等の核酸塩基、PNA等のペプチド核酸、あるいはそれらが高次構造を形成するアプタマー等を用いることもできる。以上に記載したペプチドやアミノ酸配列は、抗体と組み合わせて使用しても良い。また、これらのペプチドやアミノ酸配列はこれまでに記載した各構成要素と好適に組み合わせることができる。
【0038】
本発明の好ましい態様によれば、リンカー分子を介して結合する抗体以外にも、リンカー分子を介してさらに別の機能性分子が結合しても良い。機能性分子の例として光応答性分子が挙げられ、光応答性分子としては蛍光性分子を用いることができる。
【0039】
また、機能性分子の他の例としては放射性化合物が挙げられる。放射性化合物としては同位体元素を含む化合物が挙げられ、例えば14Cを有する14C標識カテコールなどが好適に用いられる。
【0040】
また、機能性分子の他の例としてはラジカル応答性化合物が挙げられる。ラジカル応答性化合物としては、ラジカルと特異的な反応性を示す化学発光性分子や蛍光性分子、またはスピントラップ剤を含んでなる。より具体的には、化学発光性分子や蛍光性分子として、ルミノール、海ホタルルシフェリン類縁体、シュウ酸エステル、アクリジニウム、パラヒドロキシフェニルフルオレセイン、パラアミノフェニルフルオレセイン、ジヒドロローダミン123、ジヒドロローダミン6G、トランス‐1‐(2’‐メトキシビニル)ピレン、ジヒドロキシエチジウム、葉酸、(2’,7’−dichlorodihydrofluorescein diacetate,succinimidyl ester(インビトロジェン)、)、5−or6−(N−Succinimidyloxycarbonyl)−3’,6’−O,O’−diacetylfluorescein、Cy色素(アマシャムバイオサイエンス社製)、プテリンなどであり、スピントラップ剤としては、4,6−Tri−tert−butylnitrosobenzene、2−Methyl−2−nitrosopropane、3,3,5,5−Tetramethyl−1−pyrroline N−Oxide、5,5−Dimethyl−1−pyrroline N−Oxide、5−(Diethylphosphono)−5−methyl−1−pyrroline N−Oxide、N−tert−Butyl−alpha−(4−pyridyl−1−oxide)nitrone、N−tert−Butyl−alpha−phenylnitrone、Nitrosobenzene、5,5−Dimethyl−1−pyrroline N−oxide、4−Hydroxy−2,2,6,6−tetramethylpiperidinyloxy, free radical、2−(5,5−Dimethyl−2−oxo−2λ5−[1,3,2]dioxaphosphinan−2−yl)−2−methyl−3,4−dihydro−2H−pyrrole 1−oxide、5−Diethoxyphosphoryl−5−methyl−1−pyrroline−N−oxideなどである。
【0041】
また、機能性分子の他の例としては、フルオロウラシル、ゲムシタビン、メソトレキセート、シクロホスファミド、塩酸ダウノルビシン、アドリアマイシン、塩酸イダルビシン、ブレオマイシン、マイトマイシン、アクチノマイシン、ビンクリスチン、シスプラチン、カルボプラチン、エトポシド、ネダプラチン、パクリタキセル、ドセタキセル、塩酸イリノテカン等から少なくとも一つの抗がん剤、ペニシリン系、マクロライド系、ニューキノロン系、テトラサイクリン系等の抗菌剤、ラミブジン、ネルフィナビル、インジナビ、サキナビル、インターフェロン、アマンタジン、アシクロビル等のウイルス治療薬、そして、ニュープロレリン、ブセレリン、ゴセレリン、トリプトレリン、ナファレリン等のホルモン疾患治療薬、イブプロフェン等の鎮痛薬等が挙げられる。
【0042】
また、機能性分子の他の例としては、低原子価遷移金属を含む分子が挙げられる。低原子価遷移金属はHarber−Weiss機構によって過酸化水素を分解してヒドロキシラジカルを発生することが知られており(活性酸素種の化学〔季刊 化学総説 No.7〕 日本化学会編)、低原子価遷移金属として、例えば二価の鉄イオンを用いた場合はFenton反応としてよく知られている。また、ヒドロキシラジカルを含む各種のラジカルは細胞障害作用を有している。そのため、リンカー分子を介してこれらの低原子価遷移金属を含む分子が結合していれば、過酸化水素が存在する限りラジカルを発生することが可能となり、細胞障害作用を持続することができる。すなわち、超音波照射を停止した後も、系中に蓄積した過酸化水素と、本発明の複合体粒子に結合した低原子価遷移金属を含む分子とのフェントン反応によって、より酸化力の強いヒドロキシラジカルを発生を継続的に行い、これに伴う持続的な抗腫瘍効果を得ることが可能である。ただし、低原子価遷移金属を含む分子として錯体を用いた場合、フリーのヒドロキシラジカルだけではなく、例えば鉄錯体を用いた場合に生じうるフェリル錯体等、いわゆるCrypto−HO・の形で酸化反応に関与することも考えられる。このような低原子価遷移金属としては、二価の鉄の他に、三価のチタン、二価のクロム、一価の銅などが挙げられる。さらに、このような低原子価遷移金属を含む分子としては、フェロセンカルボン酸、ビシンコニン酸と一価の銅との錯体等が挙げられる。
【0043】
以上の機能性分子はこれまでに記載した各構成要素と好適に組み合わせて、本発明の効果を妨げずに上述した各種の効果を奏することができる。
【0044】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、上記機能性分子と酸化チタン表面に結合する官能基がさらに別のリンカーを介して結合してなる分子であってもなんら問題はない。
【0045】
本発明の好ましい態様によれば、前記リンカーは、例えば生体分子同士を異なる官能基同士で結合する際に用いられるヘテロバイファンクショナルなクロスリンカーなどが考えられる。リンカーの具体例としては、N−ヒドロキシスクシンイミド、N−[α−マレイミドアセトキシ]スクシンイミドエステル、N−[β−マレイミドプロピルオキシ]スクシンイミドエステル、N−β−マレイミドプロピオン酸、N−[β−マレイミドプロピオン酸]ヒドラジド・TFA、1−エチル−3−[3−ジメチルアミノプロピル]カルボジイミドヒドロクロリド、N−ε−マレイミドカプロン酸、N−[ε−マレイミドカプロン酸]ヒドラジド、N−[ε−マレイミドカプロイルオキシ]スクシンイミドエステル、N−[γ−マレイミドブチリルオキシ]スクシンイミドエステル、N−κ−マレイミドウンデカン酸、N−[κ−マレイミドウンデカン酸]ヒドラジド、スクシンイミジル−4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシ−[6−アミドカプロエート]、スクシンイミジル6−[3−(2−ピリジルジチオ)−プロピオンアミド]ヘキサノエート、m−マレイミドベンゾイル−N−ヒドロキシスクシンイミドエステル、4−[4−N−マレイミドフェニル]酪酸ヒドラジド・HCl、3−[2−ピリジルジチオ]プロピオニルヒドラジド、N−[p−マレイミドフェニル]イソシアネート、N−スクシンイミジル[4−アジドフェニル]−1,3’−ジチオプロピオネート、N−スクシンイミジル S−アセチルチオアセテート、N−スクシンイミジルS−アセチルチオプロピオネート、スクシンイミジル 3−[ブロモアセトアミド]プロピオネート、N−スクシンイミジル ヨードアセテート、N−スクシンイミジル[4−イオドアセチル]アミノベンゾエート、スクシンイミジル4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシレート、スクシンイミジル4−[p−マレイミドフェニル]ブチレート、スクシンイミジル6−[(β−マレイミドプロピオンアミド)ヘキサノネート]、4−スクシンイミジルオキシカルボニル−メチル−α[2−ピリジルジチオ]トルエン、N−スクシンイミジル3−[2−ピリジルジチオ]プロピオネート、N−[ε−マレイミドカプロイルオキシ]スルホスクシンイミドエステル、N−[γ−マレイミドブチリルオキシ]スルホスクシンイミドエステル、N−[κ−マレイミドウンデカノイルオキシ]−スルホスクシンイミドエステル、スルホスクシンイミジル−6−[α−メチル−α−(2−ピリジルジチオ)トルアミド]ヘキサノネート、スルホスクシンイミジル6−[3’−(2−ピリジルチチオ)−プロピオンアミド]ヘキサノネート、m−マレイミドベンゾイル−N−ヒドロキシスルホ−スクシンイミドエステル、スルホスクシンイミジル[4−ヨードアセチル]アミノベンゾエート、スルホスクシンイミジル4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシレート、スルホスクシンイミジル4−[p−マレイミドフェニル]ブチレート、N−[ε−トリフルオロアセチルカプロイルオキシ]スクシンイミドエステル、クロロトリアジン、ジクロロトリアジン、トリクロロトリアジン、スクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン、C6−スクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン、スクシンイミジル−4−ヒドラジドテレフタレート−ハイドロクロライド、スクシンイミジル−4−フォルミルベンゾエイト、C6−スクシンイミジル−4−フォルミルベンゾエイト等が挙げられる。また、リンカーはさらに他のリンカー同士が結合されるような複数種類のリンカーから構成されてもよい。以上のリンカーは、これまでに記載した各構成要素と好適に組み合わせることができる。
【0046】
本発明の好ましい態様によれば、酸化チタン粒子と水溶性高分子およびまたはリンカー分子との結合に用いられるジオール基としては、エンジオール基であることが好ましく、より好ましくはα−ジオール基である。これらの官能基を用いることで、優れた酸化チタン粒子への結合を実現することができる。
【0047】
本発明の好ましい態様によれば、酸化チタン粒子が、アナターゼ型酸化チタンまたはルチル型酸化チタンであるのが好ましい。紫外線や超音波の照射による高い触媒活性を利用する場合にはアナターゼ型酸化チタンが好ましく、化粧料のように高い屈折率等の性質を利用する場合にはルチル型酸化チタンが好ましい。酸化チタン粒子としてアナターゼ型酸化チタンまたはルチル型酸化チタンを用いることは、これまでに記載した各構成要素と好適に組み合わせることができ、かつ上述した新たな効果を奏することができる。
【0048】
本発明の好ましい態様によれば、本発明の複合体粒子は20〜200nmの粒子径を有し、より好ましくは50〜200nmであり、さらに好ましくは50〜150nmである。この粒径範囲であると、癌腫瘍への到達を目的として患者の体内に投与されると、ドラッグデリバリーシステムのように、Enhanced Permeability and Retention Effect(EPR効果)により癌組織に効率的に到達して蓄積される。そして、上述の通り、400kHz〜20MHzの超音波の照射によりラジカル種の特異的生成が起こる。したがって、超音波の照射により高い効率で癌組織を殺傷することができる。
【0049】
本発明の別の好ましい態様によれば、抗腫瘍剤が50nm未満(例えば数nm)の粒子径を有する場合、見かけ上のサイズを大きくしてEPR効果を得ることもできる。すなわち、50〜150nmの粒子径を有する二次粒子の形態を有するように半導体粒子同士を多官能リンカーで連結する等の方法にて結合されることで、EPR効果により高い癌治療効果を実現することができる。
【0050】
本発明において半導体粒子の粒子径は、動的光散乱法により測定することができる。具体的には、粒径分布測定装置(ゼータサイザーナノ、マルバーンインスツルメント社製)を用いて、キュミュラント解析で得られる、Z−average sizeで示される値として得ることができる。
【0051】
本発明の複合体粒子を上記の粒子径とすることは、これまでに記載した各構成要素と好適に組み合わせることができ、かつ上述した新たな効果を奏することができる。
【0052】
本発明の複合体粒子として、単一種類の酸化チタン複合体のみならず、複数種類の半導体粒子の混合物あるいは複合物も包含する。具体例としては、酸化チタン粒子と酸化鉄ナノ粒子との複合物、酸化チタン粒子と白金との複合物、およびシリカ被覆された酸化チタン等が挙げられる。
【0053】
本発明の好ましい態様によれば、本発明の複合体粒子が、溶媒に分散されて分散液の形態とされてなるのが好ましい。これにより、本発明の複合体粒子を、点滴、注射、塗布等の種々の方法により、患者の体内に効率的に投与する抗腫瘍剤として用いることができる。分散液の液性は限定されず、pH3〜10の広範囲にわたって高い分散性を実現可能である。なお、体内投与における安全性の観点から、分散液は、pH5〜9であるのが好ましく、より好ましくは5〜8、特に中性の液性を有するのが好ましい。また、本発明の好ましい態様によれば、溶媒は水系溶媒であるのが好ましく、さらに好ましくはpH緩衝液または生理食塩水である。水系溶媒の好ましい塩濃度は2M以下であり、体内投与における安全性の観点から200mM以下がより好ましい。本発明の複合体粒子は分散体に対して、0.001〜1質量%以下含有されることが好ましく、より好ましくは0.001〜0.1質量%である。この範囲内であれば、投与後、24〜72時間後に患部(腫瘍)に効果的に粒子を蓄積させることが可能となる。すなわち、患部(腫瘍)に粒子濃度が蓄積しやすくなるとともに、血中での粒子の分散性も確保されて凝集隗が形成しにくくなるため、投与後に血管の閉塞などの二次的弊害を招くおそれも無い。
【0054】
本発明の複合体粒子は、点滴、注射、塗布等の種々の方法により、患者の体内に投与することができる。特に静脈または皮下による投与経路で用いられる場合は、粒子の大きさによるEPR効果と、血中の滞留性および粒子に結合した抗体と患部に由来する抗原との相互作用を利用して、所謂DDS的な治療により、患者の負担を軽減する観点から好ましい。そして、体内に投与された複合体粒子は、ドラッグデリバリーシステムのように、癌組織に到達して集積される。
【0055】
本発明の複合体粒子は、患部に近い血管や臓器等を経由する投与経路で用いられる場合は、生体内環境での高い分散性および粒子に結合した抗体と患部に由来する抗原との相互作用により、所謂局所DDS的な治療により、患者の負担を軽減する観点から好ましい。そして、体内に投与された複合体粒子は、ドラッグデリバリーシステムのように、癌組織に到達して集積される。
【0056】
本発明の複合体粒子は、超音波または紫外線の、好ましくは超音波の照射を受け、該照射により細胞毒となることができる。この複合体粒子は、体内に投与され、超音波照射を受け、該照射により細胞毒を生成することで、細胞を殺傷することができるが、体内に限らず、試験管内においても殺対象である細胞を殺傷することができる。本発明において、殺対象は特に限定されないが、癌細胞であるのが好ましい。すなわち、本発明の複合体粒子によれば、超音波や紫外線の照射により活性化して癌細胞を殺傷するので、抗腫瘍剤として用いることができる。
【0057】
本発明の好ましい態様によれば、本発明の複合体粒子が集積された癌組織に超音波処理が行われる。使用する超音波の周波数は、400kHz〜20MHzが好ましく、より好ましくは600kHz〜10MHz、さらに好ましくは1MHz〜10MHzである。超音波の照射時間は治療対象である癌組織の位置および大きさを考慮して適宜決定されるべきであり、特に限定されない。こうして、患者の癌組織を超音波により高い効率で殺傷して、高い癌治療効果を実現することができる。超音波は生体内の深部に外部より到達させることが可能で、本発明の複合体粒子と併せて用いることにより、非侵襲の状態で生体内深部に存在するような患部やターゲット部位の治療が実現できる。さらに、患部やターゲット部位に本発明の複合体粒子が集積することにより、周辺の正常細胞に悪影響を及ぼさない程度の微弱な超音波で本発明の複合体粒子を集積させた局所のみに作用させることができる。
【0058】
ところで、これらの半導体粒子が超音波の照射により活性化して細胞を殺傷する効果は、超音波照射によりラジカル種を生成させることにより得ることができる。すなわち、これらの半導体粒子が与える生物的殺傷効果はラジカル種の質的・量的な増加にあり、これらのラジカル種が細胞毒となると考えられる。その理由は以下の通り推察されるが、以下の理由はあくまで仮説であって、本発明は何ら下記説明に限定されるものではない。すなわち、超音波照射のみでは系中には過酸化水素とヒドロキシルラジカルが発生するが、本発明者らの知見によれば、酸化チタンなどの半導体粒子の存在下では、過酸化水素及びヒドロキシルラジカルの生成が促進される。また、これら半導体粒子の存在下、特に酸化チタンの存在下では、スーパーオキサイドアニオンと一重項酸素の生成が促進されるように見受けられる。これらラジカル種の特異的生成は、ナノメートルオーダーの微粒子を用いた場合、超音波照射時の周波数が400kHz〜20MHzの範囲、好ましくは600kHz〜10MHzの範囲、より好ましくは1MHz〜10MHzの範囲で顕著に観察される現象であると考えられる。
【0059】
製造方法
本発明の複合体粒子に用いられる酸化チタン複合体は、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有する水溶性高分子を酸化チタン粒子に結合させることにより、製造することができる。この方法による酸化チタン複合体の製造は、例えば、非プロトン系溶媒中に、酸化チタン粒子と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有するノニオン性水溶性高分子とを分散させ、得られた分散液を80〜220℃で、例えば1〜16時間、加熱することにより行うことができる。なお、好ましい非プロトン系溶媒の例としては、ジメチルホルムアミド,ジオキサン、およびジメチルスルホキシドが挙げられる。
【0060】
本発明の複合体粒子は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させ、さらにリンカー分子を介して抗体を修飾した、酸化チタン−抗体複合体にすることにより、製造することができる。この方法による抗腫瘍剤の製造は、例えば、水溶液中に、酸化チタン複合体と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有するリンカー分子とを分散させ、例えば0℃〜50℃で1〜16時間加熱し、膜分離等で未結合のリンカー分子を除去後、酸化チタン複合体に結合したリンカー分子の有するアミノ基等の官能基を、例えば1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩等のカルボジイミド剤と反応して活性化後、膜分離等で未反応のカルボジイミド剤を除去し、抗体を混合して例えば0℃〜室温で1〜16時間反応し、膜分離等で未反応の抗体を除去することにより行うことができる。
【0061】
あるいは、本発明の複合体粒子は、抗体と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を例えば1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩等のカルボジイミド剤と反応して活性化後、例えば0℃〜室温で1〜16時間反応し、膜分離等で未結合のリンカー分子を除去後、さらに水溶性高分子により水系溶媒中で分散させた酸化チタン複合体を混合して、例えば0℃〜室温で1〜16時間反応し、酸化チタン表面に抗体とリンカー分子の複合体を結合し、膜分離等で未反応の抗体を除去することにより行うことができる。
【実施例】
【0062】
以下に実施例を示す。特に断りのない限り、「%」は質量%を意味する。
【0063】
例1:ポリエチレングリコールを結合した酸化チタン複合体の作製
チタンテトライソプロポキシド3.6gとイソプロパノール3.6gを混合し、氷冷下で60mlの超純水に滴下して加水分解を行った。滴下後に室温で30分間攪拌した。攪拌後、12N硝酸1mlを滴下して80℃で8時間攪拌を行い、ペプチゼーションした。ペプチゼーション終了後0.45μmのフィルターで濾過し、さらに脱塩カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて溶液交換して固形成分1%の酸性酸化チタンゾルを調製した。この酸化チタンゾルを100ml容のバイアル瓶に入れ、超音波発生器MIDSONIC200(カイジョー製)を用いて200kHzで30分間超音波処理を行った。超音波処理を行った後の平均分散粒経を動的光散乱法により測定した。この測定は、超音波処理を行った後の酸化チタンゾルを12Nの硝酸で1000倍に希釈した後、分散液0.1mlを石英測定セルに仕込み、ゼータサイザーナノZS(シスメックス製)を用いて、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は36.4nmであった。蒸発皿を用いて、50℃下で酸化チタンゾル溶液の濃縮を行い、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0064】
次に、ポリオキシエチレン−モノアリル−モノメチルエーテルと無水マレイン酸の共重合体(平均分子量;33659−日本油脂製)1gに水5mlを添加し加水分解後得られた溶液と1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(同仁化学製)を、超純水を用いてそれぞれ濃度が50mg/mlおよび50mMとなるように混合に調整した。調整した溶液に4−アミノサリチル酸(分子量Mn=153.14:MP Biomedicals,Inc.)を濃度50mMになるよう混合して4mlの溶液を得た。この溶液を室温にて72時間振とう撹拌して反応させた。反応後、得られた溶液を透析膜であるスペクトラ/ポア CE 透析用チューブ(分画分子量=3500、Spectrum Laboratories,Inc.)に移して超純水4lに対して室温にて24時間で透析を行った。透析後にすべてナスフラスコに移し替えて一晩凍結乾燥し、得られた粉末に4mlのジメチルホルムアミド(DMF:和光純薬工業製)を添加して混合し、4−アミノサリチル酸結合ポリエチレングリコール溶液とした。
【0065】
次にDMFを用いて4−アミノサリチル酸結合ポリエチレングリコール溶液が終濃度20(vol/vol)%、先に得られたアナタ−ゼ型二酸化チタンゾルが終濃度で固形成分0.25%となるよう調整し、2.5mlの反応溶液とした。この反応溶液を水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、80℃で6時間加熱反応を行った。反応終了後、反応容器温度が50℃以下になるまで冷却し、エバポレータでDMFを除去した後に、蒸留水1mlを添加してポリエチレングリコールを結合した酸化チタン複合体の分散液とした。さらに、HPLC:AKTA purifier(GEヘルスケアバイオサイエンス製)、カラム:HiPrep 16/60 Sephacryl S−300HR(GEヘルスケアバイオサイエンス製)、移動相:リン酸塩緩衝溶液(pH7.4)、流速:0.3ml/min]に付したところ、素通り画分にUV吸収のピークが確認され、この画分を回収した。この分散液を蒸留水で0.05(wt/vol)%水溶液に希釈して72時間静置後、動的光散乱法による分散粒径およびゼータ電位の確認を、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリエチレングリコールを結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて測定した。キュミュラント解析の結果、分散粒径は54.2nmであった。
【0066】
例2:ポリアクリル酸を結合した酸化チタン複合体の作製
例1と同様に、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0067】
この酸性酸化チタンゾル0.6mlをジメチルホルムアミド(DMF)で20mlとなるよう調整して分散させ、平均分子量5000のポリアクリル酸(和光純薬工業製)0.3gを溶解したDMF10mlを添加後、攪拌して混合した。水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、150℃で5時間反応を行った。反応終了後、反応容器温度が50℃以下になるまで反応液を冷却し、反応液に対して2倍量のイソプロパノールを添加した。室温で30分間静置後、2000gにて15min遠心分離により沈殿を回収した。回収した沈殿表面をエタノールで洗浄後、1.5mlの水を加えてポリアクリル酸を結合した酸化チタン複合体の分散液を得た。この分散液を蒸留水で100倍に希釈し、分散粒径およびゼータ電位を動的光散乱法により測定した。この測定は、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリアクリル酸を結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は53.6nm、ゼータ電位は−45.08mVであった。
【0068】
例3:ポリエチレンイミンを結合した酸化チタン複合体の作製
例1と同様に、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0069】
得られた酸化チタンゾル3mlを20mlのジメチルホルムアミド(DMF)に分散させ、平均分子量10000のポリエチレンイミン(和光純薬工業製)450mgを溶解したDMF10mlを添加後、攪拌して混合した。水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、150℃で5時間反応を行った。反応終了後、反応容器温度が50℃以下になるまで反応液を冷却し、反応液に対して2倍量のアセトンを添加した。室温で30分間静置後、2000gにて15min遠心分離により沈殿を回収した。回収した沈殿表面をエタノールで洗浄後、1.5mlの水を加えてポリエチレンイミンを結合した酸化チタン複合体の分散液を得た。この分散液を蒸留水で100倍に希釈し、分散粒径およびゼータ電位を動的光散乱法により測定した。この測定は、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリエチレンイミンを結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は57.5nm、ゼータ電位は47.5mVであった。
【0070】
例4:酸化チタン複合体へのジヒドロキシフェニルプロピオン酸の結合
例1で得られた、酸化チタン複合体とジヒドロキシフェニルプロピオン酸を用いて、超純水中で表1に示す組成で混合し、合計1mlに調製した。それぞれの組成において酸化チタン複合体A〜Cとした。
【0071】
【表1】

【0072】
調整した溶液を室温で4時間静置した。反応後の溶液について可視光域における波長の吸収スペクトルを紫外−可視光分光光度計により確認したところ、吸光度の増大が認められたため、ジヒドロキシフェニルプロピオン酸が結合したと考えられた。また、反応前と反応後の溶液をキャピラリ電気泳動にて以下の条件で、フォトダイオードアレイ検出器の吸収波長214nmのピークを確認することによりジヒドロキシフェニルプロピオン酸の変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d × 67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM ホウ酸緩衝溶液(pH9.0)
・電圧:25kV
・温度:20℃
求めた変化量より、酸化チタン粒子の質量あたり結合したジヒドロキシフェニルプロピオン酸量は表2で表される結果であった。
【0073】
【表2】

【0074】
さらに、この溶液1mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のジヒドロキシフェニルプロピオン酸を除去した。ジヒドロキシフェニルプロピオン酸の除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのジヒドロキシフェニルプロピオン酸がないことを確認した。これらからジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体(酸化チタン複合体A〜C)の作製を確認した。
【0075】
例5:ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体への抗体の結合
例4で得られた、ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体のうち、酸化チタン複合体Bの溶液と1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(同仁化学製)を、超純水を用いてそれぞれ濃度が20mg/mlおよび80mMとなるように混合した。混合した溶液を室温にて10分間反応した。脱塩カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて20mM HEPES緩衝溶液(pH7.4)に溶液交換し、酸化チタン濃度にして20mg/mlの粒子の溶液を得た。これと同一の緩衝液で調製した抗ヒト血清アルブミン(抗HSA)モノクローナル抗体(マウスIgG:MSU−304、コスモバイオ製)を3mg/mlになるように添加し、全量で1mlの溶液とした。4℃で24時間反応後、終濃度が0.5Mとなるようエタノールアミンを添加して、さらに4℃で1時間反応した。この溶液を酸化チタン濃度にして1mg/mlに調製し、HPLC:AKTA purifier(GEヘルスケアバイオサイエンス製)、カラム:HiPrep 16/60 Sephacryl S−500HR(GEヘルスケアバイオサイエンス製)、移動相:リン酸緩衝生理食塩水(pH7.4)、流速:0.3ml/min]に1ml付したところ、素通り画分および結合に用いた抗HSAモノクローナル抗体が単体で確認される画分にUV吸収のピークが確認され、これらの画分を回収した。素通り画分は分離された分子の大きさから抗体分子を結合した酸化チタン−抗体複合体を含む溶液だと考えられた。また、抗HSAモノクローナル抗体が単体で確認される画分については、ブラッドフォード法でタンパク質濃度を測定した結果、反応前後で抗体濃度の減少が確認された。以上のことから、ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体の、ジヒドロキシフェニルプロピオン酸を介して抗体分子を結合した、酸化チタン−抗体複合体が作製できることを確認した。
【0076】
例6:酸化チタン−抗体複合体への蛍光色素の結合
例5で得られた、酸化チタン−抗体複合体を超純水にて固形成分1%の分散液とした。次に、ドーパミン塩酸塩(分子量Mn=153.178:和光純薬工業製)を200mMとなるよう調整した。調整した溶液と分散液を1:9で混合して1mlとし、室温で4時間結合反応を行った。反応後の溶液について可視光域における波長の吸収スペクトルを紫外−可視光分光光度計により確認したところ、それぞれの溶液について増大が認められたため、ドーパミンが結合したと考えられた。また、反応前と反応後の溶液をキャピラリ電気泳動にて以下の条件で付したところ、フォトダイオードアレイ検出器によって吸収波長214nmのピークを確認することによりドーパミンの変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d×67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM 酢酸ナトリウム緩衝溶液(pH4.8)
・電圧:25kV
・温度:20℃
求めた変化量よりドーパミンは酸化チタン粒子の質量あたり4.0×10−5 ドーパミン−g/酸化チタン粒子−gであった。このことからリンカー分子全体としては、酸化チタン粒子の質量あたり9.0×10−5 リンカー分子−mol/酸化チタン粒子‐gであった。
【0077】
さらに、この溶液1.0mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のドーパミンを除去した。ドーパミンの除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのドーパミンがないことを確認した。これらからドーパミンを結合した酸化チタン−抗体複合体の作製を確認した。次にこのドーパミンを結合した酸化チタン−抗体複合体を終濃度で0.3%、またNHS−Rhodamine(ピアース製)を終濃度で1mMとなるように20mMホウ酸緩衝液中で混合調整した。この溶液を4℃、遮光下で24時間静置した。この溶液2.5mlに対してバッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて水3.5mlで回収して未反応のNHS−Rhodamineを除去した。NHS−Rhodamineの除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのNHS−Rhodamineがないことを確認した。得られた溶液を蛍光分光光度計にてスペクトル解析を行い、励起波長555nm、蛍光波長575nmで蛍光を示すことを確認した。これらのことから、ドーパミンを結合した酸化チタン−抗体複合体へ、ドーパミンを介して蛍光分子を結合した、蛍光分子結合酸化チタン−抗体複合体の作製を確認した。
【0078】
例7:酸化チタン複合体の分散性評価
例1で得られた酸化チタン複合体(酸化チタン複合体Dとする)および例4で得られた酸化チタン複合体A〜Cを、それぞれリン酸緩衝生理食塩水に対して、固形成分0.05%になるように添加し、1時間、室温にて静置した。その後、例1と同様にゼータサイザーナノZSを用いて分散粒径およびゼータ電位を動的光散乱法により測定した。結果を表3に示す。酸化チタン複合体A〜Dにおいて、分散粒径およびゼータ電位に大きな変化がないことが確認された。
【0079】
【表3】

【0080】
例8:酸化チタン−抗体複合体の分散性評価
例5で得られた酸化チタン−抗体複合体を、リン酸緩衝生理食塩水に対して、固形成分0.05%になるように添加し、1時間、室温にて静置した。その後、例1と同様にゼータサイザーナノZSを用いて分散粒径およびゼータ電位を動的光散乱法により測定した。その結果、分散粒径は52.5nmでゼータ電位は−4.48mVであり、例7の結果と比べて大きな変化がないことが確認された。
【0081】
例9:酸化チタン複合体の超音波照射による一重項酸素生成能の評価
例1で得られた酸化チタン複合体(酸化チタン複合体Dとする)および例4で得られた酸化チタン複合体A〜Cを、それぞれリン酸緩衝生理食塩水に対して、固形成分0.05%になるように調製した。また、コントロールとしてリン酸緩衝生理食塩水のみを調製した。各溶液3mlに対して、一重項酸素の生成を測定する試薬のSinglet Oxygen Sensor Green Reagent(Molecular Probes社)をマニュアルに従い混合して試験溶液とした。超音波照射装置(オージー技研製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、0.4W/cm2で50% duty cycle運転で3分間超音波を照射し、測定サンプルとして照射前後の溶液を400μlずつ採取した。各測定サンプルについて一重項酸素生成に起因する、Ex=488nm、Em=525nmにおける蛍光強度を蛍光分光光度計(RF−5300PC;島津製作所製)により測定した。その結果は、図2に示される通りであった。図2に示されるように、コントロールと比べて酸化チタン複合体A〜Dは、超音波照射により一重項酸素をより効率的に生成することが確認された。また、酸化チタン粒子の質量あたり結合したリンカー量が多いほど、一重項酸素の生成は抑制されると考えられた。
【0082】
例10:酸化チタン−抗体複合体の抗原結合評価
SPRセンサによる抗原への結合確認のため、SPRセンサ装置(BIACORE1000,BIAcore製)にセンサチップC1(BIAcore製)をセットし、メーカーのマニュアルに従ってヒト血清アルブミン(HSA:和光純薬工業製)の固定化反応を行った。BIAcore amine coupling kit(BIAcore製)に含まれる50μlのNHS−EDC混合溶液を5μl/minで流してセンサチップ表面のカルボキシル基をスクシニル化した後に、10mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH5.0)に1g/lになるよう溶解したHSAの溶液を50μl、流速5μl/minでロードして反応を行った。反応後、BIAcore amine coupling kitに含まれる1mol/lのエタノールアミンを50μl、流速5μl/minでロードして、結合に関与しなかったスクシニル基のブロッキング処理を行った。これによって約0.8ng/mm2のHSA結合が得られた。次に、例5で得られた酸化チタン−抗体複合体の分散液および抗ヒト血清アルブミン(抗HSA)モノクローナル抗体(マウスIgG:MSU−304、コスモバイオ製)をそれぞれ各濃度に調製したものを流速30μl/minで60μlロードした。センサグラムの反応確認後、100mmol/lのglycine−NaOH緩衝溶液(pH12.0)を30μl/minで30μlロードし、センサからの解離反応を行った。センサグラムの解析はBiomolecular Interaction Analysis(BIA)evaluation software(version 3.5,BIAcore製)を用いて行った。バックグラウンドとして例1で得られた酸化チタン複合体を同様にロードして得た結果を差し引いた。それらの結果は、図3に示される通りであった。図中の記号は、A:0.05%酸化チタン−抗体複合体、B:0.005%酸化チタン−抗体複合体、C:0.0005%酸化チタン−抗体複合体、D:5μg/ml抗ヒト血清アルブミン(抗HSA)モノクローナル抗体、E:1μg/ml抗HSAモノクローナル抗体をそれぞれ表す。これらの結果から酸化チタン−抗体複合体は抗原に対して強く結合することが示された。
【0083】
例11:酸化チタン複合体へのジヒドロキシフェニルプロピオン酸の結合2
例1で得られた、酸化チタン複合体およびジヒドロキシフェニルプロピオン酸を用いて、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)、2)20mmol/lのMES緩衝溶液(同仁化学製;pH=6.0)、3)20mmol/lのHEPES緩衝溶液(同仁化学製;pH=8.1)中で、酸化チタン複合体が終濃度2%、またジヒドロキシフェニルプロピオン酸が終濃度で50mmol/lとなるよう混合し、合計0.8mlに調製した。
【0084】
調製した溶液を40℃で25時間攪拌した。それぞれの溶液について紫外−可視光域(200−600nm)における吸収スペクトルを紫外−可視光分光光度計により確認した。ジヒドロキシフェニルプロピオン酸のみを混合した溶液について、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中においては、調整後0時間と比べてほとんど変化がなかったのに対し、2)20mmol/lのMES緩衝溶液(pH=6.0)および3)20mmol/lのHEPES緩衝溶液(pH=8.1)中においては、調整後0時間と比べて吸収スペクトルの変化が確認され、目視によっても薄赤色に変色していることが確認された。これらのことから、ジヒドロキシフェニルプロピオン酸はpH=6.0以上において変化を生じ、不安定であると考えられた。また、酸化チタン複合体およびジヒドロキシフェニルプロピオン酸を混合した溶液について、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中においては、調整後0時間と比べて吸収スペクトルの変化が確認され、目視によっても濃茶色に変色していることが確認された。ジヒドロキシフェニルプロピオン酸のみにおいては大きな変化がなかったことから、この変化は酸化チタン複合体にジヒドロキシフェニルプロピオン酸が結合、電荷移動を生じたためと考えられた。
【0085】
次に、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中において、調整後0時間と25時間攪拌後の溶液をキャピラリ電気泳動にて以下の条件で、フォトダイオードアレイ検出器の吸収波長214nmのピークを確認することによりジヒドロキシフェニルプロピオン酸の変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d × 67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM ホウ酸緩衝溶液(pH9.0)
・電圧:25kV
・温度:20℃
求めた変化量より、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中における酸化チタン粒子の質量あたり結合したジヒドロキシフェニルプロピオン酸量は7.7×10−4 ジヒドロキシフェニルプロピオン酸‐mol/酸化チタン粒子‐gであった。
【0086】
例12:超音波照射による細胞殺傷試験
例5で得られた酸化チタン−抗体複合体を、1×105cells/mlのJurkat細胞を含む、10%血清入りRPMI1640培地(Invitrogen製)3mlに1/10量添加して、終濃度0.05%および0%となるように試験溶液を調整した。各試験溶液に、超音波照射装置(オージー技研(株)製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、15秒間超音波照射(0.5W/cm2、50%パルス)を行なった。MTTアッセイ(同仁化学製)でメーカーの手順書に従い細胞数を計測し、照射前の細胞数を細胞生存率100%として、各試験溶液における細胞生存率を算出した。その結果、終濃度0.05%においては細胞生存率75.8%、また、終濃度0%において細胞生存率99.2%となった。これらのことから、酸化チタン−抗体複合体の超音波照射による細胞殺傷効果が確認された。
【0087】
例13:酸化チタン複合体へのフェロセンカルボン酸およびドーパミンの結合
フェロセンカルボン酸(和光純薬工業製)および塩酸ドーパミン(和光純薬工業製)を1mMとなるようジメチルホルムアミド(DMF;和光純薬工業製)に溶解した。また、同様にDMFを用いて200mM Benzotriazole−1−yl−oxy−trispyrrolidinophosphonium hexafluorophosphate(PyBop;メルク製)、200mM 1−ヒドロキシベンゾトリアゾール(HoBt;同仁化学製)、20mM N,N−ジイソプロピルエチルアミン(DIEA;和光純薬工業製)をそれぞれ調製した。これらのうち、フェロセンカルボン酸と塩酸ドーパミンは元濃度の1/4、またその他は元濃度の1/10となるよう混合してDMFで20mlに溶液調整した。この混合溶液を緩やかに攪拌しながら、室温で20時間反応を行った。
【0088】
反応溶液の一部を超純水で10倍に希釈し、この溶液を逆相クロマトグラフィ(HPLCシステム:Prominence(島津製作所製)、カラム:Chromolith RP−18e 100−3mm(メルク製)、移動相:A メタノール(和光純薬工業製)B 0.1%トリフルオロ酢酸水溶液(和光純薬工業製)、流速:2ml/min)を用いて解析した。紫外線検出器で波長210nmに設定し、インジェクション(0.02ml)後、1〜10minにおいてメタノールが100%となるようグラジエント溶出を行った結果、フェロセンカルボン酸と塩酸ドーパミンの複合体と考えられるピークを確認した。また、フェロセンカルボン酸および塩酸ドーパミンそれぞれ単独のピークは検出限界以下であった。これらのことから、フェロセンカルボン酸と塩酸ドーパミンの複合体の生成を確認した。
【0089】
反応溶液の残りを減圧下で10倍に濃縮し、反応濃縮溶液とした。例1で得られた、酸化チタン複合体を超純水にて固形成分1%に調整し、そこに反応濃縮溶液を1/10量混合して、全量で1mlとした。この混合溶液を緩やかに攪拌しながら、室温で1時間反応を行った。反応後、沈殿成分を遠心分離(1500g、10min)して上澄みを回収し、この溶液1mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のフェロセンカルボン酸と塩酸ドーパミンの複合体およびDMFを除去した。この溶液について可視光域(400nm)における波長の吸収スペクトルを紫外−可視光分光光度計(UV1600;島津製作所製)により確認したところ増大が認められたため、フェロセンカルボン酸と塩酸ドーパミンの複合体が結合したと考えられた。これらからフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体の作製を確認した。
【0090】
例14:酸化チタン−抗体複合体へのフェロセンカルボン酸およびドーパミンの結合
例13において、例1で得られた酸化チタン複合体の代わりに、例5で得られた酸化チタン−抗体複合体を用いた以外はまったく同様にしてフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン−抗体複合体を作製した。
【0091】
例15:フェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体の超音波照射によるヒドロキシラジカル生成能の評価
例13で得られたフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体(酸化チタン複合体Eとする)を、リン酸緩衝生理食塩水(pH7.4)に対して、固形成分0.05%になるように調製した。また、コントロールとしてリン酸緩衝生理食塩水(pH7.4)のみを用いた。各溶液3mlを用意して試験溶液とした。超音波照射装置(オージー技研製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、3分間超音波照射(0.4W/cm2、50%パルス)を行い、照射後に各溶液に対して、ヒドロキシラジカルの生成を測定する試薬のヒドロキシフェニルフルオレセイン(HPF、第一化学薬品製)をマニュアルに従い混合し、室温で15分および30分静置、各静置時間における測定サンプルとして照射前後の溶液を400μlずつ採取した。各測定サンプルについてヒドロキシラジカル生成に起因する、Ex=490nm、Em=515nmにおける蛍光強度を蛍光分光光度計(RF−5300PC;島津製作所製)により測定した。その結果は、図4に示される通りであった。図4に示されるように、コントロールと比べて酸化チタン複合体Eは、超音波照射によりヒドロキシラジカルを効率的に生成することが確認された。また、酸化チタン複合体Eは静置時間に伴って蛍光値が増大することから、持続的にヒドロキシラジカルを生成すると考えられた。
【0092】
例16:ドーパミンを介した酸化チタン複合体への抗体の結合
抗αフェトプロテイン(抗AFP)抗体(マウスIgG:NB013、日本バイオテスト研究所製)0.1mgをCoupling buffer(pH5.5;Catalog No.153−6054、バイオラッド製)を用いて1.8mlに調製し、そこに25mg/1.2mlの過ヨウ素酸ナトリウム(和光純薬工業製)水溶液を0.2ml加えて室温にて1時間反応後、超純水を加えて2.5mlとした溶液に対してバッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて20mM MES緩衝溶液(pH5.5)で3.2ml回収して未反応の過ヨウ素酸ナトリウムを除去し、Amicon Ultra−15(MWCO=5000;ミリポア製)で遠心分離(1500g、15min)して0.7mlに濃縮し、酸化された抗体溶液を得た。また、200mMの塩酸ドーパミン(和光純薬工業製)水溶液0.5mlと70mMのスクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン(SANH;PIERCE製)水溶液0.1mlを混合し、100mM HEPES緩衝溶液(pH8.1)および超純水で総量1mlに調製し、室温にて1時間反応後、薄層クロマトグラフィーによりSANHとドーパミンの結合を確認、SANHとドーパミンの複合体溶液を得た。これら、酸化された抗体溶液0.7mlとSANHとドーパミンの複合体溶液0.1mlとCoupling buffer(pH5.5;Catalog No.153−6054、バイオラッド製)0.2mlを混合して、4℃にて16時間反応後、バッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いてPBS緩衝液(リン酸生理食塩水)で溶出し、抗体とSANHとドーパミンの複合体と、未反応のSANHとドーパミンの複合体を除去した。こうして、抗体とSANHとドーパミンの複合体を得た。次に、例1で得られた、5(wt/vol)%の酸化チタン複合体2mlと、抗体とSANHとドーパミンの複合体1mlを混合し、4℃にて16時間反応後、44.5 mm PBCC membrane (MWCO=300000;Catalog No.PBMK04310、ミリポア製)および攪拌式セルModel8050(Catalog No.5122、ミリポア製)を用いて、メーカーのプロトコルに従い10psiで334mlの溶液交換に伴う、未結合の抗体とSANHとドーパミンの複合体除去を行った。このようにして酸化チタン−抗AFP抗体複合体粒子の分散液を得た。
【0093】
次に、SPRセンサによる抗原への結合確認のため、SPRセンサ装置(BIACORE1000,BIAcore製)にセンサチップC1(BIAcore製)をセットし、メーカーのマニュアルに従ってαフェトプロテイン(AFP:日本バイオテスト研究所製)の固定化反応を行った。移動相にはリン酸緩衝液の混合溶液(10mM リン酸緩衝液(pH7.4)、150mM NaCl、0.05(wt/vol)% Tween20)を用いた。BIAcore amine coupling kit(BIAcore製)に含まれる200μlのNHS−EDC混合溶液を30μl/minで流してセンサチップ表面のカルボキシル基をスクシニル化した後に、90mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH5.0)に100μg/mlになるよう溶解したAFPの溶液を180μl、流速30μl/minでロードして反応を行った。反応後、BIAcore amine coupling kitに含まれる1mol/lのエタノールアミンを150μl、流速30μl/minでロードして、結合に関与しなかったスクシニル基のブロッキング処理を行った。これによって150RUのレスポンスが得られた。作製した0.025(wt/vol)%の酸化チタン−抗AFP抗体複合体粒子の分散液および10μg/mlの抗αフェトプロテイン(抗AFP)抗体(マウスIgG:NB013、日本バイオテスト研究所製)をそれぞれ各濃度に調製したものを流速30μl/minで90μlロードした。センサグラムの反応確認後、100mmol/lのglycine−NaOH緩衝溶液(pH12.0)を30μl/minで100μlロードし、センサからの解離反応を行った。センサグラムの解析はBiomolecular Interaction Analysis(BIA)evaluation software(version 3.5,BIAcore製)を用いて行った。バックグラウンドとして例1で得られた酸化チタン複合体を同様にロードして得た結果を差し引いた。それらの結果、抗AFP抗体では15RU、酸化チタン−抗AFP抗体複合体粒子においては50RUのレスポンスを得た。これらの結果から酸化チタン−抗AFP抗体複合体粒子は抗原に対して強く結合することが示された。以上により、ドーパミンを介した酸化チタン複合体への抗AFP抗体を結合した、酸化チタン−抗体複合体が作製できることを確認した。
【図面の簡単な説明】
【0094】
【図1】本発明の複合体粒子の一例を示す図である。
【図2】例9において各種粒子について測定された、超音波照射による一重項酸素の発生に起因する、一重項酸素検出用蛍光試薬を介した蛍光強度を示す図である。
【図3】例10において酸化チタン−抗体複合体について測定された、抗原に対する結合評価である。
【図4】例15において酸化チタン複合体Eについて測定された、超音波照射後のヒドロキシラジカルの発生に起因する、ヒドロキシラジカル検出用蛍光試薬を介した蛍光強度を示す図である。
【技術分野】
【0001】
本発明は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を酸化チタン表面に結合させ、さらに該リンカー分子を介して抗体が結合されてなり、超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とする、複合体粒子に関する。
【背景技術】
【0002】
酸化チタンはpH6前後に等電点を有すると言われている。このため、酸化チタン粒子は中性付近の水系溶媒中では凝集を生じてしまい、これを均一に分散させることは極めて難しい。そのため、酸化チタン粒子を水系の分散媒に均一に分散させるため、今まで種々の試みがなされてきた。
【0003】
PEG(ポリエチレングリコール)を分散剤として添加して、分散媒中における酸化チタン粒子の分散性を向上させることが知られている(特許文献1(特開平2−307524号公報)および特許文献2(特開2002−60651号公報)参照)。
【0004】
あるいは酸化チタン微粒子に、ポリアクリル酸等の親水性高分子を、カルボキシル基を介して結合させた、表面改質酸化チタン微粒子も知られている(特許文献3(WO2004/087577)参照)。この技術は、ポリアクリル酸等といったアニオン性ポリマーの使用を念頭としたものである。アニオン性ポリマーのもつカルボキシル基等の官能基により表面電荷を与え、それにより生体内環境に近い中性の生理食塩水においても安定した分散性を示し、かつ紫外線照射時の光触媒活性機能を有するものである。
【0005】
更に、酸化チタンに機能性を付与する検討がなされている。例えば、前記表面改質酸化チタン微粒子に対して、前記親水性高分子の結合に関与していないカルボキシル残基に、目的分子に対して特異的な結合能を有する分子を固定化した、分子識別能を有する二酸化チタン複合体が提案されている(特許文献4(特許第3835700号)参照)。この技術は、アニオン性ポリマーのもつカルボキシル基等の官能基により、分子が固定化されていても表面電荷を与え、安定した分散性を示すものである。一方で、官能基によって与えられる表面電荷は分散性に直接寄与しており、結合に関与していない残基に分子を固定化することで表面電荷は減少する。このことが固定化される分子の量等に対して制限を与える。
【0006】
【特許文献1】特開平2−307524号公報
【特許文献2】特開2002−60651号公報
【特許文献3】WO2004/087577号パンフレット
【特許文献4】特許第3835700号公報
【発明の開示】
【0007】
本発明は、水溶性高分子により水系溶媒中で分散性を保ち、超音波の照射による触媒活性を有する酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を介して抗体を修飾することで、分散性と触媒活性を失うことなく選択的な結合能を付与した酸化チタン−抗体複合体粒子であることを特徴とする複合体粒子、および該複合体粒子を含んでなる抗腫瘍剤の提供をその目的としている。
【0008】
本発明者らは、今般、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させることにより、前記水溶性高分子を変質させることなく、分散性と触媒活性を保ちながら、新たに抗体を付与することが可能である、との知見を得た。
【0009】
すなわち、本発明によれば、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面にリンカー分子を結合し、さらに該リンカー分子を介して抗体を結合させることにより、水溶性高分子を変質させることなく高い分散性を保持し、なおかつ超音波の照射による触媒活性を有し、さらに抗原と結合可能な酸化チタン−抗体複合体粒子であることを特徴とする複合体粒子を作製することができる。複合体粒子が抗原と結合している状態で超音波照射をすることで、ラジカル種と抗原との反応性を高めることが期待できる。抗原が癌細胞もしくは新生血管等の癌近傍組織に由来する場合にあっては、複合体粒子を患部である癌近傍に集積させ、さらに超音波照射を行うことで高い抗腫瘍効果を得ることができる。よって本発明の複合体粒子は抗腫瘍剤としての使用が可能である。該抗腫瘍剤は、患部に集積させ、さらに超音波を照射することにより行われる超音波癌治療を促進する薬剤として好適に利用可能である。
【0010】
そして、本発明の複合体粒子は、
酸化チタン粒子と、
該酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を介して結合されてなる水溶性高分子を含んでなる、酸化チタン複合体と、
該酸化チタン複合体の表面に、さらに結合されてなるリンカー分子を含んでなり、該リンカー分子は、
(1)カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を有し、
(2)a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物であって、
該官能基を介して前記酸化チタンと結合され、
該官能基同士で重合すること無く、
さらに該リンカー分子を介して抗体が結合されてなり、
超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とするものである。
【0011】
また、本発明による分散液は、複合体粒子と、該複合体粒子が分散される溶媒とを含んでなるものである。
【0012】
本発明によれば、水溶性高分子により水系溶媒中で分散性を保ち、超音波の照射による触媒活性を有する酸化チタン複合体に対して、水溶性高分子を変質させることなくリンカー分子を介して抗体を修飾することで、分散性と触媒活性を失うことなく選択的な結合能を付与した酸化チタン−抗体複合体であることを特徴とした複合体粒子およびその分散体を提供できる。
【0013】
また、本発明による抗腫瘍剤は、複合体粒子または複合体粒子が分散された分散液を含んでなるものである。
【発明を実施するための最良の形態】
【0014】
本発明の複合体粒子は、酸化チタン粒子と、水溶性高分子と、リンカー分子と、抗体とからなる酸化チタン−抗体複合体を含む。図1に、複合体粒子の一例を示す。図1に示されるように、複合体粒子は、酸化チタン粒子1の表面に水溶性高分子2およびリンカー分子3を介して抗体4が結合されたものである。酸化チタン粒子1と、水溶性高分子2およびリンカー分子3との結合は、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を介して形成される。
【0015】
すなわち、これらの官能基は酸化チタンとの間で強固な結合を形成するため、酸化チタン粒子の高い触媒活性に関わらず分散性を保持できる。また、リンカー分子を介して抗体の結合を保持することが可能である。なお、本発明における結合形態は、体内における安全性の観点から、体内への投与後24〜72時間後に分散性が確保されている程度の結合形態であればよい。生理条件での分散が安定しており、かつ超音波照射後も水溶性高分子の遊離が無く、正常細胞へのダメージが少ない点で、共有結合であるのが望ましい。
【0016】
カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基は、3官能シラノール基のような相互に三次元的に縮合重合して重合物で酸化チタン粒子の表面を覆い尽くしてしまう官能基とは異なり、官能基同士で重合することが無いため、図1に示されるように酸化チタン粒子の表面に剥き出しの部分を確保することができると考えられる。その結果、表面が重合体で覆われることによって起こりうる失活を抑制しつつ、酸化チタン粒子の触媒活性を十分に発揮させることができる。
【0017】
そして、酸化チタン粒子の表面に結合した水溶性高分子は、電荷あるいは水和の作用によって、酸化チタン粒子の分散が困難とされる中性付近の水系溶媒中であって、本発明の複合体粒子を分散させることができる。抗体を、酸化チタン粒子の表面に結合した水溶性高分子に対して導入する方法については公知である。このような場合は、水溶性高分子と抗体を化学結合するために、水溶性高分子は反応性の高い極性基を含んでなることが必要である。この水溶性高分子に含まれる極性基は、抗体が結合されると失われる。このことにより、水溶性高分子の極性自体に変化が生じる。つまり、酸化チタン粒子の表面に結合した水溶性高分子のもつ電荷あるいは水和の作用によって分散しているバランスが、抗体の結合前後において変化すると考えられる。この酸化チタン粒子の表面に結合した水溶性高分子の変質に伴う電荷あるいは水和のバランスをうまくコントロールすることでのみ達成しうる。一方、本発明における酸化チタン粒子の表面に結合したリンカー分子を介して結合した抗体については、水溶性高分子を変質させることなく結合させることにより、水溶性高分子による高い分散性を保持できる。このため、水溶性高分子の変質によって生じる分散性の変化を考慮することなく、抗体の結合に際して自由度の高い分子設計が可能である。
【0018】
本発明の複合体粒子によれば、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面にリンカー分子を結合し、さらに該リンカー分子を介して抗体を結合させることにより、水溶性高分子を変質させることなく高い分散性を保持する酸化チタン−抗体複合体であることを特徴とする抗腫瘍剤を作製することができる。このように抗体を結合することにより、本発明の複合体粒子が抗原と結合することを可能とする。また、本発明の複合体粒子に対して超音波照射をすることでラジカル種を発生することができる。一般的にラジカル種は高い反応性をもつが寿命が短く、ごく僅かに拡散して近傍の物質と反応する。このため、本発明の複合体粒子が抗原と結合している状態で超音波照射をすることで、ラジカル種と抗原との反応性を高めることが期待できる。抗原が癌細胞もしくは新生血管等の癌近傍組織に由来する場合にあっては、本発明の複合体粒子を患部である癌近傍に集積させ、さらに超音波照射を行うことで高い抗腫瘍効果を得ることができる。よって本発明の複合体粒子は、抗腫瘍剤として使用することができる。そして、本発明の複合体粒子は、投与後に患部へ集積させ、さらに超音波を照射することにより行われる超音波癌治療を促進するための薬剤としての効果を期待できる。
【0019】
また、本発明の複合体粒子によれば、酸化チタン−抗体複合体の酸化チタン表面に対し、リンカー分子を介して光応答性の分子や放射性物質を結合することで、水溶性高分子を変質させることなく高い分散性を保持することができる。特に、放射性物質に関しては、安全性の観点からなるべく少ない工程で用いることが必要であるが、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体に対して、酸化チタン表面に放射性物質を結合した後に、未結合の放射性物質を適当な方法で分離除去するだけの、簡易でかつ少ない工程によって粒子の標識ができる。このため、放射性物質が外部に広がる機会が少なく、安全性の面において優れる。また、これを適当な機器により測定することで粒子のイメージングや定量の測定が可能である。そのため、本発明の複合体粒子は、体内に投与後に体内動態を確認するためのトレーサー実験用材料や、患部に超音波照射することにより行われる診断および治療のための医療用材料としても利用可能である。
【0020】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介して結合されてなることが好ましい。これによって、酸化チタン粒子の表面に強固に結合することが可能であり、また、3官能シラノール基のような相互に三次元的に縮合重合して重合物で酸化チタン粒子の表面を覆い尽くしてしまう官能基とは異なり、官能基同士で重合することが無いため、図1に示されるように酸化チタン粒子の表面に剥き出しの部分を多く確保することができると考えられる。その結果、表面が重合体で覆われることによって起こりうる失活を抑制し、酸化チタン粒子の触媒活性を十分に発揮させることができる。
【0021】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、酸化チタン−抗体複合体を水系溶媒中で分散させることができれば特に限定されない。本発明に用いる水溶性高分子において、電荷を有するものとしては、アニオン性またはカチオン性を有する水溶性高分子、また、電荷を有さずに水和によって分散性を与えるものとしてはノニオン性を有する水溶性高分子が挙げられ、これらの少なくとも一種を含んでなる。
【0022】
本発明の好ましい態様によれば、前記水溶性高分子は重量平均分子量2000〜100000である。水溶性高分子の重量平均分子量はサイズ排除クロマトグラフィーを用いて求めた値である。前記分子量をこの範囲とすることで、水溶性高分子のもつ電荷あるいは水和の作用によって、酸化チタン粒子の分散が困難とされる中性付近の水系溶媒中であって酸化チタン−抗体複合体を分散させることができる。
より好ましい範囲は5000〜100000であり、さらに好ましくは5000〜40000である。
【0023】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、アニオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。アニオン性を有する水溶性高分子は、複数のカルボキシル基を有するものが好適に利用可能であり、例えばカルボキシメチルデンプン、カルボキシメチルデキストラン、カルボキシメチルセルロース、ポリカルボン酸類、およびカルボキシル基単位を有する共重合体(コポリマー)などが挙げられる。具体的には、水溶性高分子の加水分解性および溶解度の観点から、ポリアクリル酸、ポリマレイン酸等のポリカルボン酸類、およびアクリル酸/マレイン酸やアクリル酸/スルフォン酸系モノマーの共重合体(コポリマー)がより好適に使用され、さらに好ましくはポリアクリル酸である。
【0024】
アニオン性を有する水溶性高分子として、ポリアクリル酸を用いる場合、分散性の観点からポリアクリル酸の重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000であり、さらに好ましくは5000〜20000である。
【0025】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、カチオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。カチオン性を有する水溶性高分子は、複数のアミノ基を有するものとしてが好適に利用可能であり、例えばポリアミノ酸、ポリペプチド、ポリアミン類、およびアミン単位を有する共重合体(コポリマー)などが挙げられる。具体的には、水溶性高分子の加水分解性および溶解度の観点から、ポリエチレンイミン、ポリビニルアミン、ポリアリルアミン等のポリアミン類がより好適に使用され、さらに好ましくはポリエチレンイミンである。
【0026】
カチオン性を有する水溶性高分子として、ポリエチレンイミンを用いる場合、分散性の観点からポリエチレンイミンの重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000であり、さらに好ましくは5000〜20000である。
【0027】
本発明の好ましい態様によれば、本発明に用いる水溶性高分子は、ノニオン性を有する水溶性高分子が、本発明の複合体粒子を水系溶媒中で分散させることができればいずれも使用可能である。ノニオン性を有する水溶性高分子は、好ましくは水酸基および/またはポリオキシアルキレン基を有する高分子が挙げられる。そのような水溶性高分子の好ましい例としては、ポリエチレングリコール(PEG)、ポリビニルアルコール、ポリエチレンオキシド、デキストランあるいはそれらを含有するコポリマーが挙げられ、より好ましくはポリエチレングリコール(PEG)およびデキストランであり、さらに好ましくはポリエチレングリコールである。
【0028】
ノニオン性を有する水溶性高分子として、ポリエチレングリコールを用いる場合、分散性の観点からポリエチレングリコールの重量平均分子量は2000〜100000であるのが好ましく、より好ましくは5000〜40000である
【0029】
以上に例示した水溶性高分子は、本発明の複合体粒子の分散性を妨げない範囲内において、これまでに記載した各要素を自由に組み合わせることができる。
【0030】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、酸化チタン粒子表面に結合してなるが、該機能性分子はカルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を有する。
【0031】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物である。
【0032】
上記炭素数よりなるリンカー分子は、前記水溶性高分子と比べて分子の大きさが小さい。また、リンカー分子は酸化チタン表面に結合してなる。このため、本発明の酸化チタン−抗体複合体において、外殻に水溶性高分子が位置するのに対し、より内部の位置にリンカー分子を有する構造をとる。該外殻は本発明の複合体粒子の分散性に対する影響が最も大きい。すなわち外殻に位置する水溶性高分子に対して、内部に位置するリンカー分子が分散性に与える影響は小さくなり、好適に用いることができる。
【0033】
本発明の複合体粒子に結合されたリンカー分子の量は、酸化チタン粒子の質量:1gあたり1.0×10−6〜1.0×10−3 molであり、より好ましくは1.0×10−6〜1.0×10−4 mol/酸化チタン粒子‐gである。
この範囲であると、本発明の複合体粒子は生体内環境に近い、10%タンパク質溶液を溶媒としても分散することができるため、好適に用いることができる。さらに、この範囲であると、本発明の複合体粒子は超音波を照射する際に触媒活性を有し、ラジカル種を発生することができるため、好適に用いることができる。
【0034】
そのようなリンカー分子の例としては、芳香族化合物やアルキル構造をもつ分子等が考えられ、より具体的には、ベンゼン環をもつ分子として、カテコール、メチルカテコール、ターシャリーブチルカテコールドーパ、ドーパミン、ジヒドロキシフェニルエタノール、ジヒドロキシフェニルプロピオン酸、ジヒドロキシフェニル酢酸等の、分子内にカテコールの構造を有する、カテコール類などが挙げられる。また、他の環状分子として、フェロセン、フェロセンカルボン酸、アスコルビン酸、ジハイドロキシシクロブテンジエン、アリザリン、ビナフタレンジオール等が好適に使用できる。さらに、アルキル構造をもつ分子としては、ヘキシル基、オクチル基、ラウリル基、パルミチル基、ステアリル基などのアルキル基を有する分子が挙げられる。あるいは、ヘキセニル基、オクテニル基、オレイル基などのアルケニル基、または、シクロアルキル基などの飽和又は不飽和脂肪族炭化水素基をもつものなどが挙げられる。
【0035】
以上に例示したリンカー分子およびその量は、これまでに記載した各構成要素と好適に組み合わせることができる。
【0036】
本発明の好ましい態様によれば、リンカー分子を介して結合する抗体としては、特に制限はないが、本発明の複合体粒子を積極的に癌部位へ集積させるため、該抗体の抗原が癌細胞もしくは新生血管等の癌近傍組織に由来することが望ましい。あるいは、抗体をFab領域等に低分子化させたフラグメントを用いることも何ら問題はない。
【0037】
また、本発明の複合体粒子を積極的に癌部位へ集積させるため、リンカー分子を介して結合する分子は抗体に限らず、例えば癌細胞もしくは新生血管等の癌近傍組織に由来する部位と相互作用を示すペプチドやアミノ酸配列であってもよい。より具体的には5−アミノレブリン酸、メチオニン、システイン、グリシン等が挙げられる。あるいは、糖鎖を含んでもよい。さらに、結合性を有する核酸を含んでいても良い。核酸としては、特に制限はなく、DNA、RNA等の核酸塩基、PNA等のペプチド核酸、あるいはそれらが高次構造を形成するアプタマー等を用いることもできる。以上に記載したペプチドやアミノ酸配列は、抗体と組み合わせて使用しても良い。また、これらのペプチドやアミノ酸配列はこれまでに記載した各構成要素と好適に組み合わせることができる。
【0038】
本発明の好ましい態様によれば、リンカー分子を介して結合する抗体以外にも、リンカー分子を介してさらに別の機能性分子が結合しても良い。機能性分子の例として光応答性分子が挙げられ、光応答性分子としては蛍光性分子を用いることができる。
【0039】
また、機能性分子の他の例としては放射性化合物が挙げられる。放射性化合物としては同位体元素を含む化合物が挙げられ、例えば14Cを有する14C標識カテコールなどが好適に用いられる。
【0040】
また、機能性分子の他の例としてはラジカル応答性化合物が挙げられる。ラジカル応答性化合物としては、ラジカルと特異的な反応性を示す化学発光性分子や蛍光性分子、またはスピントラップ剤を含んでなる。より具体的には、化学発光性分子や蛍光性分子として、ルミノール、海ホタルルシフェリン類縁体、シュウ酸エステル、アクリジニウム、パラヒドロキシフェニルフルオレセイン、パラアミノフェニルフルオレセイン、ジヒドロローダミン123、ジヒドロローダミン6G、トランス‐1‐(2’‐メトキシビニル)ピレン、ジヒドロキシエチジウム、葉酸、(2’,7’−dichlorodihydrofluorescein diacetate,succinimidyl ester(インビトロジェン)、)、5−or6−(N−Succinimidyloxycarbonyl)−3’,6’−O,O’−diacetylfluorescein、Cy色素(アマシャムバイオサイエンス社製)、プテリンなどであり、スピントラップ剤としては、4,6−Tri−tert−butylnitrosobenzene、2−Methyl−2−nitrosopropane、3,3,5,5−Tetramethyl−1−pyrroline N−Oxide、5,5−Dimethyl−1−pyrroline N−Oxide、5−(Diethylphosphono)−5−methyl−1−pyrroline N−Oxide、N−tert−Butyl−alpha−(4−pyridyl−1−oxide)nitrone、N−tert−Butyl−alpha−phenylnitrone、Nitrosobenzene、5,5−Dimethyl−1−pyrroline N−oxide、4−Hydroxy−2,2,6,6−tetramethylpiperidinyloxy, free radical、2−(5,5−Dimethyl−2−oxo−2λ5−[1,3,2]dioxaphosphinan−2−yl)−2−methyl−3,4−dihydro−2H−pyrrole 1−oxide、5−Diethoxyphosphoryl−5−methyl−1−pyrroline−N−oxideなどである。
【0041】
また、機能性分子の他の例としては、フルオロウラシル、ゲムシタビン、メソトレキセート、シクロホスファミド、塩酸ダウノルビシン、アドリアマイシン、塩酸イダルビシン、ブレオマイシン、マイトマイシン、アクチノマイシン、ビンクリスチン、シスプラチン、カルボプラチン、エトポシド、ネダプラチン、パクリタキセル、ドセタキセル、塩酸イリノテカン等から少なくとも一つの抗がん剤、ペニシリン系、マクロライド系、ニューキノロン系、テトラサイクリン系等の抗菌剤、ラミブジン、ネルフィナビル、インジナビ、サキナビル、インターフェロン、アマンタジン、アシクロビル等のウイルス治療薬、そして、ニュープロレリン、ブセレリン、ゴセレリン、トリプトレリン、ナファレリン等のホルモン疾患治療薬、イブプロフェン等の鎮痛薬等が挙げられる。
【0042】
また、機能性分子の他の例としては、低原子価遷移金属を含む分子が挙げられる。低原子価遷移金属はHarber−Weiss機構によって過酸化水素を分解してヒドロキシラジカルを発生することが知られており(活性酸素種の化学〔季刊 化学総説 No.7〕 日本化学会編)、低原子価遷移金属として、例えば二価の鉄イオンを用いた場合はFenton反応としてよく知られている。また、ヒドロキシラジカルを含む各種のラジカルは細胞障害作用を有している。そのため、リンカー分子を介してこれらの低原子価遷移金属を含む分子が結合していれば、過酸化水素が存在する限りラジカルを発生することが可能となり、細胞障害作用を持続することができる。すなわち、超音波照射を停止した後も、系中に蓄積した過酸化水素と、本発明の複合体粒子に結合した低原子価遷移金属を含む分子とのフェントン反応によって、より酸化力の強いヒドロキシラジカルを発生を継続的に行い、これに伴う持続的な抗腫瘍効果を得ることが可能である。ただし、低原子価遷移金属を含む分子として錯体を用いた場合、フリーのヒドロキシラジカルだけではなく、例えば鉄錯体を用いた場合に生じうるフェリル錯体等、いわゆるCrypto−HO・の形で酸化反応に関与することも考えられる。このような低原子価遷移金属としては、二価の鉄の他に、三価のチタン、二価のクロム、一価の銅などが挙げられる。さらに、このような低原子価遷移金属を含む分子としては、フェロセンカルボン酸、ビシンコニン酸と一価の銅との錯体等が挙げられる。
【0043】
以上の機能性分子はこれまでに記載した各構成要素と好適に組み合わせて、本発明の効果を妨げずに上述した各種の効果を奏することができる。
【0044】
本発明の好ましい態様によれば、本発明に用いるリンカー分子は、上記機能性分子と酸化チタン表面に結合する官能基がさらに別のリンカーを介して結合してなる分子であってもなんら問題はない。
【0045】
本発明の好ましい態様によれば、前記リンカーは、例えば生体分子同士を異なる官能基同士で結合する際に用いられるヘテロバイファンクショナルなクロスリンカーなどが考えられる。リンカーの具体例としては、N−ヒドロキシスクシンイミド、N−[α−マレイミドアセトキシ]スクシンイミドエステル、N−[β−マレイミドプロピルオキシ]スクシンイミドエステル、N−β−マレイミドプロピオン酸、N−[β−マレイミドプロピオン酸]ヒドラジド・TFA、1−エチル−3−[3−ジメチルアミノプロピル]カルボジイミドヒドロクロリド、N−ε−マレイミドカプロン酸、N−[ε−マレイミドカプロン酸]ヒドラジド、N−[ε−マレイミドカプロイルオキシ]スクシンイミドエステル、N−[γ−マレイミドブチリルオキシ]スクシンイミドエステル、N−κ−マレイミドウンデカン酸、N−[κ−マレイミドウンデカン酸]ヒドラジド、スクシンイミジル−4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシ−[6−アミドカプロエート]、スクシンイミジル6−[3−(2−ピリジルジチオ)−プロピオンアミド]ヘキサノエート、m−マレイミドベンゾイル−N−ヒドロキシスクシンイミドエステル、4−[4−N−マレイミドフェニル]酪酸ヒドラジド・HCl、3−[2−ピリジルジチオ]プロピオニルヒドラジド、N−[p−マレイミドフェニル]イソシアネート、N−スクシンイミジル[4−アジドフェニル]−1,3’−ジチオプロピオネート、N−スクシンイミジル S−アセチルチオアセテート、N−スクシンイミジルS−アセチルチオプロピオネート、スクシンイミジル 3−[ブロモアセトアミド]プロピオネート、N−スクシンイミジル ヨードアセテート、N−スクシンイミジル[4−イオドアセチル]アミノベンゾエート、スクシンイミジル4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシレート、スクシンイミジル4−[p−マレイミドフェニル]ブチレート、スクシンイミジル6−[(β−マレイミドプロピオンアミド)ヘキサノネート]、4−スクシンイミジルオキシカルボニル−メチル−α[2−ピリジルジチオ]トルエン、N−スクシンイミジル3−[2−ピリジルジチオ]プロピオネート、N−[ε−マレイミドカプロイルオキシ]スルホスクシンイミドエステル、N−[γ−マレイミドブチリルオキシ]スルホスクシンイミドエステル、N−[κ−マレイミドウンデカノイルオキシ]−スルホスクシンイミドエステル、スルホスクシンイミジル−6−[α−メチル−α−(2−ピリジルジチオ)トルアミド]ヘキサノネート、スルホスクシンイミジル6−[3’−(2−ピリジルチチオ)−プロピオンアミド]ヘキサノネート、m−マレイミドベンゾイル−N−ヒドロキシスルホ−スクシンイミドエステル、スルホスクシンイミジル[4−ヨードアセチル]アミノベンゾエート、スルホスクシンイミジル4−[N−マレイミドメチル]−シクロヘキサン−1−カルボキシレート、スルホスクシンイミジル4−[p−マレイミドフェニル]ブチレート、N−[ε−トリフルオロアセチルカプロイルオキシ]スクシンイミドエステル、クロロトリアジン、ジクロロトリアジン、トリクロロトリアジン、スクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン、C6−スクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン、スクシンイミジル−4−ヒドラジドテレフタレート−ハイドロクロライド、スクシンイミジル−4−フォルミルベンゾエイト、C6−スクシンイミジル−4−フォルミルベンゾエイト等が挙げられる。また、リンカーはさらに他のリンカー同士が結合されるような複数種類のリンカーから構成されてもよい。以上のリンカーは、これまでに記載した各構成要素と好適に組み合わせることができる。
【0046】
本発明の好ましい態様によれば、酸化チタン粒子と水溶性高分子およびまたはリンカー分子との結合に用いられるジオール基としては、エンジオール基であることが好ましく、より好ましくはα−ジオール基である。これらの官能基を用いることで、優れた酸化チタン粒子への結合を実現することができる。
【0047】
本発明の好ましい態様によれば、酸化チタン粒子が、アナターゼ型酸化チタンまたはルチル型酸化チタンであるのが好ましい。紫外線や超音波の照射による高い触媒活性を利用する場合にはアナターゼ型酸化チタンが好ましく、化粧料のように高い屈折率等の性質を利用する場合にはルチル型酸化チタンが好ましい。酸化チタン粒子としてアナターゼ型酸化チタンまたはルチル型酸化チタンを用いることは、これまでに記載した各構成要素と好適に組み合わせることができ、かつ上述した新たな効果を奏することができる。
【0048】
本発明の好ましい態様によれば、本発明の複合体粒子は20〜200nmの粒子径を有し、より好ましくは50〜200nmであり、さらに好ましくは50〜150nmである。この粒径範囲であると、癌腫瘍への到達を目的として患者の体内に投与されると、ドラッグデリバリーシステムのように、Enhanced Permeability and Retention Effect(EPR効果)により癌組織に効率的に到達して蓄積される。そして、上述の通り、400kHz〜20MHzの超音波の照射によりラジカル種の特異的生成が起こる。したがって、超音波の照射により高い効率で癌組織を殺傷することができる。
【0049】
本発明の別の好ましい態様によれば、抗腫瘍剤が50nm未満(例えば数nm)の粒子径を有する場合、見かけ上のサイズを大きくしてEPR効果を得ることもできる。すなわち、50〜150nmの粒子径を有する二次粒子の形態を有するように半導体粒子同士を多官能リンカーで連結する等の方法にて結合されることで、EPR効果により高い癌治療効果を実現することができる。
【0050】
本発明において半導体粒子の粒子径は、動的光散乱法により測定することができる。具体的には、粒径分布測定装置(ゼータサイザーナノ、マルバーンインスツルメント社製)を用いて、キュミュラント解析で得られる、Z−average sizeで示される値として得ることができる。
【0051】
本発明の複合体粒子を上記の粒子径とすることは、これまでに記載した各構成要素と好適に組み合わせることができ、かつ上述した新たな効果を奏することができる。
【0052】
本発明の複合体粒子として、単一種類の酸化チタン複合体のみならず、複数種類の半導体粒子の混合物あるいは複合物も包含する。具体例としては、酸化チタン粒子と酸化鉄ナノ粒子との複合物、酸化チタン粒子と白金との複合物、およびシリカ被覆された酸化チタン等が挙げられる。
【0053】
本発明の好ましい態様によれば、本発明の複合体粒子が、溶媒に分散されて分散液の形態とされてなるのが好ましい。これにより、本発明の複合体粒子を、点滴、注射、塗布等の種々の方法により、患者の体内に効率的に投与する抗腫瘍剤として用いることができる。分散液の液性は限定されず、pH3〜10の広範囲にわたって高い分散性を実現可能である。なお、体内投与における安全性の観点から、分散液は、pH5〜9であるのが好ましく、より好ましくは5〜8、特に中性の液性を有するのが好ましい。また、本発明の好ましい態様によれば、溶媒は水系溶媒であるのが好ましく、さらに好ましくはpH緩衝液または生理食塩水である。水系溶媒の好ましい塩濃度は2M以下であり、体内投与における安全性の観点から200mM以下がより好ましい。本発明の複合体粒子は分散体に対して、0.001〜1質量%以下含有されることが好ましく、より好ましくは0.001〜0.1質量%である。この範囲内であれば、投与後、24〜72時間後に患部(腫瘍)に効果的に粒子を蓄積させることが可能となる。すなわち、患部(腫瘍)に粒子濃度が蓄積しやすくなるとともに、血中での粒子の分散性も確保されて凝集隗が形成しにくくなるため、投与後に血管の閉塞などの二次的弊害を招くおそれも無い。
【0054】
本発明の複合体粒子は、点滴、注射、塗布等の種々の方法により、患者の体内に投与することができる。特に静脈または皮下による投与経路で用いられる場合は、粒子の大きさによるEPR効果と、血中の滞留性および粒子に結合した抗体と患部に由来する抗原との相互作用を利用して、所謂DDS的な治療により、患者の負担を軽減する観点から好ましい。そして、体内に投与された複合体粒子は、ドラッグデリバリーシステムのように、癌組織に到達して集積される。
【0055】
本発明の複合体粒子は、患部に近い血管や臓器等を経由する投与経路で用いられる場合は、生体内環境での高い分散性および粒子に結合した抗体と患部に由来する抗原との相互作用により、所謂局所DDS的な治療により、患者の負担を軽減する観点から好ましい。そして、体内に投与された複合体粒子は、ドラッグデリバリーシステムのように、癌組織に到達して集積される。
【0056】
本発明の複合体粒子は、超音波または紫外線の、好ましくは超音波の照射を受け、該照射により細胞毒となることができる。この複合体粒子は、体内に投与され、超音波照射を受け、該照射により細胞毒を生成することで、細胞を殺傷することができるが、体内に限らず、試験管内においても殺対象である細胞を殺傷することができる。本発明において、殺対象は特に限定されないが、癌細胞であるのが好ましい。すなわち、本発明の複合体粒子によれば、超音波や紫外線の照射により活性化して癌細胞を殺傷するので、抗腫瘍剤として用いることができる。
【0057】
本発明の好ましい態様によれば、本発明の複合体粒子が集積された癌組織に超音波処理が行われる。使用する超音波の周波数は、400kHz〜20MHzが好ましく、より好ましくは600kHz〜10MHz、さらに好ましくは1MHz〜10MHzである。超音波の照射時間は治療対象である癌組織の位置および大きさを考慮して適宜決定されるべきであり、特に限定されない。こうして、患者の癌組織を超音波により高い効率で殺傷して、高い癌治療効果を実現することができる。超音波は生体内の深部に外部より到達させることが可能で、本発明の複合体粒子と併せて用いることにより、非侵襲の状態で生体内深部に存在するような患部やターゲット部位の治療が実現できる。さらに、患部やターゲット部位に本発明の複合体粒子が集積することにより、周辺の正常細胞に悪影響を及ぼさない程度の微弱な超音波で本発明の複合体粒子を集積させた局所のみに作用させることができる。
【0058】
ところで、これらの半導体粒子が超音波の照射により活性化して細胞を殺傷する効果は、超音波照射によりラジカル種を生成させることにより得ることができる。すなわち、これらの半導体粒子が与える生物的殺傷効果はラジカル種の質的・量的な増加にあり、これらのラジカル種が細胞毒となると考えられる。その理由は以下の通り推察されるが、以下の理由はあくまで仮説であって、本発明は何ら下記説明に限定されるものではない。すなわち、超音波照射のみでは系中には過酸化水素とヒドロキシルラジカルが発生するが、本発明者らの知見によれば、酸化チタンなどの半導体粒子の存在下では、過酸化水素及びヒドロキシルラジカルの生成が促進される。また、これら半導体粒子の存在下、特に酸化チタンの存在下では、スーパーオキサイドアニオンと一重項酸素の生成が促進されるように見受けられる。これらラジカル種の特異的生成は、ナノメートルオーダーの微粒子を用いた場合、超音波照射時の周波数が400kHz〜20MHzの範囲、好ましくは600kHz〜10MHzの範囲、より好ましくは1MHz〜10MHzの範囲で顕著に観察される現象であると考えられる。
【0059】
製造方法
本発明の複合体粒子に用いられる酸化チタン複合体は、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有する水溶性高分子を酸化チタン粒子に結合させることにより、製造することができる。この方法による酸化チタン複合体の製造は、例えば、非プロトン系溶媒中に、酸化チタン粒子と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有するノニオン性水溶性高分子とを分散させ、得られた分散液を80〜220℃で、例えば1〜16時間、加熱することにより行うことができる。なお、好ましい非プロトン系溶媒の例としては、ジメチルホルムアミド,ジオキサン、およびジメチルスルホキシドが挙げられる。
【0060】
本発明の複合体粒子は、水溶性高分子により水系溶媒中で分散させた酸化チタン複合体の酸化チタン表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を結合させ、さらにリンカー分子を介して抗体を修飾した、酸化チタン−抗体複合体にすることにより、製造することができる。この方法による抗腫瘍剤の製造は、例えば、水溶液中に、酸化チタン複合体と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基から選択される少なくとも1種の官能基を有するリンカー分子とを分散させ、例えば0℃〜50℃で1〜16時間加熱し、膜分離等で未結合のリンカー分子を除去後、酸化チタン複合体に結合したリンカー分子の有するアミノ基等の官能基を、例えば1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩等のカルボジイミド剤と反応して活性化後、膜分離等で未反応のカルボジイミド剤を除去し、抗体を混合して例えば0℃〜室温で1〜16時間反応し、膜分離等で未反応の抗体を除去することにより行うことができる。
【0061】
あるいは、本発明の複合体粒子は、抗体と、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくともひとつの官能基を介してリンカー分子を例えば1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩等のカルボジイミド剤と反応して活性化後、例えば0℃〜室温で1〜16時間反応し、膜分離等で未結合のリンカー分子を除去後、さらに水溶性高分子により水系溶媒中で分散させた酸化チタン複合体を混合して、例えば0℃〜室温で1〜16時間反応し、酸化チタン表面に抗体とリンカー分子の複合体を結合し、膜分離等で未反応の抗体を除去することにより行うことができる。
【実施例】
【0062】
以下に実施例を示す。特に断りのない限り、「%」は質量%を意味する。
【0063】
例1:ポリエチレングリコールを結合した酸化チタン複合体の作製
チタンテトライソプロポキシド3.6gとイソプロパノール3.6gを混合し、氷冷下で60mlの超純水に滴下して加水分解を行った。滴下後に室温で30分間攪拌した。攪拌後、12N硝酸1mlを滴下して80℃で8時間攪拌を行い、ペプチゼーションした。ペプチゼーション終了後0.45μmのフィルターで濾過し、さらに脱塩カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて溶液交換して固形成分1%の酸性酸化チタンゾルを調製した。この酸化チタンゾルを100ml容のバイアル瓶に入れ、超音波発生器MIDSONIC200(カイジョー製)を用いて200kHzで30分間超音波処理を行った。超音波処理を行った後の平均分散粒経を動的光散乱法により測定した。この測定は、超音波処理を行った後の酸化チタンゾルを12Nの硝酸で1000倍に希釈した後、分散液0.1mlを石英測定セルに仕込み、ゼータサイザーナノZS(シスメックス製)を用いて、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は36.4nmであった。蒸発皿を用いて、50℃下で酸化チタンゾル溶液の濃縮を行い、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0064】
次に、ポリオキシエチレン−モノアリル−モノメチルエーテルと無水マレイン酸の共重合体(平均分子量;33659−日本油脂製)1gに水5mlを添加し加水分解後得られた溶液と1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(同仁化学製)を、超純水を用いてそれぞれ濃度が50mg/mlおよび50mMとなるように混合に調整した。調整した溶液に4−アミノサリチル酸(分子量Mn=153.14:MP Biomedicals,Inc.)を濃度50mMになるよう混合して4mlの溶液を得た。この溶液を室温にて72時間振とう撹拌して反応させた。反応後、得られた溶液を透析膜であるスペクトラ/ポア CE 透析用チューブ(分画分子量=3500、Spectrum Laboratories,Inc.)に移して超純水4lに対して室温にて24時間で透析を行った。透析後にすべてナスフラスコに移し替えて一晩凍結乾燥し、得られた粉末に4mlのジメチルホルムアミド(DMF:和光純薬工業製)を添加して混合し、4−アミノサリチル酸結合ポリエチレングリコール溶液とした。
【0065】
次にDMFを用いて4−アミノサリチル酸結合ポリエチレングリコール溶液が終濃度20(vol/vol)%、先に得られたアナタ−ゼ型二酸化チタンゾルが終濃度で固形成分0.25%となるよう調整し、2.5mlの反応溶液とした。この反応溶液を水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、80℃で6時間加熱反応を行った。反応終了後、反応容器温度が50℃以下になるまで冷却し、エバポレータでDMFを除去した後に、蒸留水1mlを添加してポリエチレングリコールを結合した酸化チタン複合体の分散液とした。さらに、HPLC:AKTA purifier(GEヘルスケアバイオサイエンス製)、カラム:HiPrep 16/60 Sephacryl S−300HR(GEヘルスケアバイオサイエンス製)、移動相:リン酸塩緩衝溶液(pH7.4)、流速:0.3ml/min]に付したところ、素通り画分にUV吸収のピークが確認され、この画分を回収した。この分散液を蒸留水で0.05(wt/vol)%水溶液に希釈して72時間静置後、動的光散乱法による分散粒径およびゼータ電位の確認を、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリエチレングリコールを結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて測定した。キュミュラント解析の結果、分散粒径は54.2nmであった。
【0066】
例2:ポリアクリル酸を結合した酸化チタン複合体の作製
例1と同様に、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0067】
この酸性酸化チタンゾル0.6mlをジメチルホルムアミド(DMF)で20mlとなるよう調整して分散させ、平均分子量5000のポリアクリル酸(和光純薬工業製)0.3gを溶解したDMF10mlを添加後、攪拌して混合した。水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、150℃で5時間反応を行った。反応終了後、反応容器温度が50℃以下になるまで反応液を冷却し、反応液に対して2倍量のイソプロパノールを添加した。室温で30分間静置後、2000gにて15min遠心分離により沈殿を回収した。回収した沈殿表面をエタノールで洗浄後、1.5mlの水を加えてポリアクリル酸を結合した酸化チタン複合体の分散液を得た。この分散液を蒸留水で100倍に希釈し、分散粒径およびゼータ電位を動的光散乱法により測定した。この測定は、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリアクリル酸を結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は53.6nm、ゼータ電位は−45.08mVであった。
【0068】
例3:ポリエチレンイミンを結合した酸化チタン複合体の作製
例1と同様に、最終的に固形成分20%の酸性酸化チタンゾルを調製した。
【0069】
得られた酸化チタンゾル3mlを20mlのジメチルホルムアミド(DMF)に分散させ、平均分子量10000のポリエチレンイミン(和光純薬工業製)450mgを溶解したDMF10mlを添加後、攪拌して混合した。水熱反応容器のHU−50(三愛科学製)に溶液を移し変え、150℃で5時間反応を行った。反応終了後、反応容器温度が50℃以下になるまで反応液を冷却し、反応液に対して2倍量のアセトンを添加した。室温で30分間静置後、2000gにて15min遠心分離により沈殿を回収した。回収した沈殿表面をエタノールで洗浄後、1.5mlの水を加えてポリエチレンイミンを結合した酸化チタン複合体の分散液を得た。この分散液を蒸留水で100倍に希釈し、分散粒径およびゼータ電位を動的光散乱法により測定した。この測定は、ゼータサイザーナノZSを用いて、ゼータ電位測定セルにポリエチレンイミンを結合した酸化チタン複合体の分散液0.75mlを仕込み、溶媒の各種パラメーターを水と同値に設定し、25℃にて行った。その結果、分散粒径は57.5nm、ゼータ電位は47.5mVであった。
【0070】
例4:酸化チタン複合体へのジヒドロキシフェニルプロピオン酸の結合
例1で得られた、酸化チタン複合体とジヒドロキシフェニルプロピオン酸を用いて、超純水中で表1に示す組成で混合し、合計1mlに調製した。それぞれの組成において酸化チタン複合体A〜Cとした。
【0071】
【表1】

【0072】
調整した溶液を室温で4時間静置した。反応後の溶液について可視光域における波長の吸収スペクトルを紫外−可視光分光光度計により確認したところ、吸光度の増大が認められたため、ジヒドロキシフェニルプロピオン酸が結合したと考えられた。また、反応前と反応後の溶液をキャピラリ電気泳動にて以下の条件で、フォトダイオードアレイ検出器の吸収波長214nmのピークを確認することによりジヒドロキシフェニルプロピオン酸の変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d × 67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM ホウ酸緩衝溶液(pH9.0)
・電圧:25kV
・温度:20℃
求めた変化量より、酸化チタン粒子の質量あたり結合したジヒドロキシフェニルプロピオン酸量は表2で表される結果であった。
【0073】
【表2】

【0074】
さらに、この溶液1mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のジヒドロキシフェニルプロピオン酸を除去した。ジヒドロキシフェニルプロピオン酸の除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのジヒドロキシフェニルプロピオン酸がないことを確認した。これらからジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体(酸化チタン複合体A〜C)の作製を確認した。
【0075】
例5:ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体への抗体の結合
例4で得られた、ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体のうち、酸化チタン複合体Bの溶液と1−エチル−3−(3−ジメチルアミノプロピル)カルボジイミド塩酸塩(同仁化学製)を、超純水を用いてそれぞれ濃度が20mg/mlおよび80mMとなるように混合した。混合した溶液を室温にて10分間反応した。脱塩カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて20mM HEPES緩衝溶液(pH7.4)に溶液交換し、酸化チタン濃度にして20mg/mlの粒子の溶液を得た。これと同一の緩衝液で調製した抗ヒト血清アルブミン(抗HSA)モノクローナル抗体(マウスIgG:MSU−304、コスモバイオ製)を3mg/mlになるように添加し、全量で1mlの溶液とした。4℃で24時間反応後、終濃度が0.5Mとなるようエタノールアミンを添加して、さらに4℃で1時間反応した。この溶液を酸化チタン濃度にして1mg/mlに調製し、HPLC:AKTA purifier(GEヘルスケアバイオサイエンス製)、カラム:HiPrep 16/60 Sephacryl S−500HR(GEヘルスケアバイオサイエンス製)、移動相:リン酸緩衝生理食塩水(pH7.4)、流速:0.3ml/min]に1ml付したところ、素通り画分および結合に用いた抗HSAモノクローナル抗体が単体で確認される画分にUV吸収のピークが確認され、これらの画分を回収した。素通り画分は分離された分子の大きさから抗体分子を結合した酸化チタン−抗体複合体を含む溶液だと考えられた。また、抗HSAモノクローナル抗体が単体で確認される画分については、ブラッドフォード法でタンパク質濃度を測定した結果、反応前後で抗体濃度の減少が確認された。以上のことから、ジヒドロキシフェニルプロピオン酸を結合した酸化チタン複合体の、ジヒドロキシフェニルプロピオン酸を介して抗体分子を結合した、酸化チタン−抗体複合体が作製できることを確認した。
【0076】
例6:酸化チタン−抗体複合体への蛍光色素の結合
例5で得られた、酸化チタン−抗体複合体を超純水にて固形成分1%の分散液とした。次に、ドーパミン塩酸塩(分子量Mn=153.178:和光純薬工業製)を200mMとなるよう調整した。調整した溶液と分散液を1:9で混合して1mlとし、室温で4時間結合反応を行った。反応後の溶液について可視光域における波長の吸収スペクトルを紫外−可視光分光光度計により確認したところ、それぞれの溶液について増大が認められたため、ドーパミンが結合したと考えられた。また、反応前と反応後の溶液をキャピラリ電気泳動にて以下の条件で付したところ、フォトダイオードアレイ検出器によって吸収波長214nmのピークを確認することによりドーパミンの変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d×67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM 酢酸ナトリウム緩衝溶液(pH4.8)
・電圧:25kV
・温度:20℃
求めた変化量よりドーパミンは酸化チタン粒子の質量あたり4.0×10−5 ドーパミン−g/酸化チタン粒子−gであった。このことからリンカー分子全体としては、酸化チタン粒子の質量あたり9.0×10−5 リンカー分子−mol/酸化チタン粒子‐gであった。
【0077】
さらに、この溶液1.0mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のドーパミンを除去した。ドーパミンの除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのドーパミンがないことを確認した。これらからドーパミンを結合した酸化チタン−抗体複合体の作製を確認した。次にこのドーパミンを結合した酸化チタン−抗体複合体を終濃度で0.3%、またNHS−Rhodamine(ピアース製)を終濃度で1mMとなるように20mMホウ酸緩衝液中で混合調整した。この溶液を4℃、遮光下で24時間静置した。この溶液2.5mlに対してバッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて水3.5mlで回収して未反応のNHS−Rhodamineを除去した。NHS−Rhodamineの除去はキャピラリ電気泳動にて上記と同様に確認し、フリーのNHS−Rhodamineがないことを確認した。得られた溶液を蛍光分光光度計にてスペクトル解析を行い、励起波長555nm、蛍光波長575nmで蛍光を示すことを確認した。これらのことから、ドーパミンを結合した酸化チタン−抗体複合体へ、ドーパミンを介して蛍光分子を結合した、蛍光分子結合酸化チタン−抗体複合体の作製を確認した。
【0078】
例7:酸化チタン複合体の分散性評価
例1で得られた酸化チタン複合体(酸化チタン複合体Dとする)および例4で得られた酸化チタン複合体A〜Cを、それぞれリン酸緩衝生理食塩水に対して、固形成分0.05%になるように添加し、1時間、室温にて静置した。その後、例1と同様にゼータサイザーナノZSを用いて分散粒径およびゼータ電位を動的光散乱法により測定した。結果を表3に示す。酸化チタン複合体A〜Dにおいて、分散粒径およびゼータ電位に大きな変化がないことが確認された。
【0079】
【表3】

【0080】
例8:酸化チタン−抗体複合体の分散性評価
例5で得られた酸化チタン−抗体複合体を、リン酸緩衝生理食塩水に対して、固形成分0.05%になるように添加し、1時間、室温にて静置した。その後、例1と同様にゼータサイザーナノZSを用いて分散粒径およびゼータ電位を動的光散乱法により測定した。その結果、分散粒径は52.5nmでゼータ電位は−4.48mVであり、例7の結果と比べて大きな変化がないことが確認された。
【0081】
例9:酸化チタン複合体の超音波照射による一重項酸素生成能の評価
例1で得られた酸化チタン複合体(酸化チタン複合体Dとする)および例4で得られた酸化チタン複合体A〜Cを、それぞれリン酸緩衝生理食塩水に対して、固形成分0.05%になるように調製した。また、コントロールとしてリン酸緩衝生理食塩水のみを調製した。各溶液3mlに対して、一重項酸素の生成を測定する試薬のSinglet Oxygen Sensor Green Reagent(Molecular Probes社)をマニュアルに従い混合して試験溶液とした。超音波照射装置(オージー技研製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、0.4W/cm2で50% duty cycle運転で3分間超音波を照射し、測定サンプルとして照射前後の溶液を400μlずつ採取した。各測定サンプルについて一重項酸素生成に起因する、Ex=488nm、Em=525nmにおける蛍光強度を蛍光分光光度計(RF−5300PC;島津製作所製)により測定した。その結果は、図2に示される通りであった。図2に示されるように、コントロールと比べて酸化チタン複合体A〜Dは、超音波照射により一重項酸素をより効率的に生成することが確認された。また、酸化チタン粒子の質量あたり結合したリンカー量が多いほど、一重項酸素の生成は抑制されると考えられた。
【0082】
例10:酸化チタン−抗体複合体の抗原結合評価
SPRセンサによる抗原への結合確認のため、SPRセンサ装置(BIACORE1000,BIAcore製)にセンサチップC1(BIAcore製)をセットし、メーカーのマニュアルに従ってヒト血清アルブミン(HSA:和光純薬工業製)の固定化反応を行った。BIAcore amine coupling kit(BIAcore製)に含まれる50μlのNHS−EDC混合溶液を5μl/minで流してセンサチップ表面のカルボキシル基をスクシニル化した後に、10mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH5.0)に1g/lになるよう溶解したHSAの溶液を50μl、流速5μl/minでロードして反応を行った。反応後、BIAcore amine coupling kitに含まれる1mol/lのエタノールアミンを50μl、流速5μl/minでロードして、結合に関与しなかったスクシニル基のブロッキング処理を行った。これによって約0.8ng/mm2のHSA結合が得られた。次に、例5で得られた酸化チタン−抗体複合体の分散液および抗ヒト血清アルブミン(抗HSA)モノクローナル抗体(マウスIgG:MSU−304、コスモバイオ製)をそれぞれ各濃度に調製したものを流速30μl/minで60μlロードした。センサグラムの反応確認後、100mmol/lのglycine−NaOH緩衝溶液(pH12.0)を30μl/minで30μlロードし、センサからの解離反応を行った。センサグラムの解析はBiomolecular Interaction Analysis(BIA)evaluation software(version 3.5,BIAcore製)を用いて行った。バックグラウンドとして例1で得られた酸化チタン複合体を同様にロードして得た結果を差し引いた。それらの結果は、図3に示される通りであった。図中の記号は、A:0.05%酸化チタン−抗体複合体、B:0.005%酸化チタン−抗体複合体、C:0.0005%酸化チタン−抗体複合体、D:5μg/ml抗ヒト血清アルブミン(抗HSA)モノクローナル抗体、E:1μg/ml抗HSAモノクローナル抗体をそれぞれ表す。これらの結果から酸化チタン−抗体複合体は抗原に対して強く結合することが示された。
【0083】
例11:酸化チタン複合体へのジヒドロキシフェニルプロピオン酸の結合2
例1で得られた、酸化チタン複合体およびジヒドロキシフェニルプロピオン酸を用いて、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)、2)20mmol/lのMES緩衝溶液(同仁化学製;pH=6.0)、3)20mmol/lのHEPES緩衝溶液(同仁化学製;pH=8.1)中で、酸化チタン複合体が終濃度2%、またジヒドロキシフェニルプロピオン酸が終濃度で50mmol/lとなるよう混合し、合計0.8mlに調製した。
【0084】
調製した溶液を40℃で25時間攪拌した。それぞれの溶液について紫外−可視光域(200−600nm)における吸収スペクトルを紫外−可視光分光光度計により確認した。ジヒドロキシフェニルプロピオン酸のみを混合した溶液について、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中においては、調整後0時間と比べてほとんど変化がなかったのに対し、2)20mmol/lのMES緩衝溶液(pH=6.0)および3)20mmol/lのHEPES緩衝溶液(pH=8.1)中においては、調整後0時間と比べて吸収スペクトルの変化が確認され、目視によっても薄赤色に変色していることが確認された。これらのことから、ジヒドロキシフェニルプロピオン酸はpH=6.0以上において変化を生じ、不安定であると考えられた。また、酸化チタン複合体およびジヒドロキシフェニルプロピオン酸を混合した溶液について、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中においては、調整後0時間と比べて吸収スペクトルの変化が確認され、目視によっても濃茶色に変色していることが確認された。ジヒドロキシフェニルプロピオン酸のみにおいては大きな変化がなかったことから、この変化は酸化チタン複合体にジヒドロキシフェニルプロピオン酸が結合、電荷移動を生じたためと考えられた。
【0085】
次に、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中において、調整後0時間と25時間攪拌後の溶液をキャピラリ電気泳動にて以下の条件で、フォトダイオードアレイ検出器の吸収波長214nmのピークを確認することによりジヒドロキシフェニルプロピオン酸の変化量を求めた。
・装置:P/ACE MDQ(ベックマンコールター製)
・キャピラリ:フューズドシリカキャピラリ 50μm i.d × 67cm(effective length 50cm)(ベックマンコールター製)
・移動相:50mM ホウ酸緩衝溶液(pH9.0)
・電圧:25kV
・温度:20℃
求めた変化量より、1)20mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH=3.6)中における酸化チタン粒子の質量あたり結合したジヒドロキシフェニルプロピオン酸量は7.7×10−4 ジヒドロキシフェニルプロピオン酸‐mol/酸化チタン粒子‐gであった。
【0086】
例12:超音波照射による細胞殺傷試験
例5で得られた酸化チタン−抗体複合体を、1×105cells/mlのJurkat細胞を含む、10%血清入りRPMI1640培地(Invitrogen製)3mlに1/10量添加して、終濃度0.05%および0%となるように試験溶液を調整した。各試験溶液に、超音波照射装置(オージー技研(株)製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、15秒間超音波照射(0.5W/cm2、50%パルス)を行なった。MTTアッセイ(同仁化学製)でメーカーの手順書に従い細胞数を計測し、照射前の細胞数を細胞生存率100%として、各試験溶液における細胞生存率を算出した。その結果、終濃度0.05%においては細胞生存率75.8%、また、終濃度0%において細胞生存率99.2%となった。これらのことから、酸化チタン−抗体複合体の超音波照射による細胞殺傷効果が確認された。
【0087】
例13:酸化チタン複合体へのフェロセンカルボン酸およびドーパミンの結合
フェロセンカルボン酸(和光純薬工業製)および塩酸ドーパミン(和光純薬工業製)を1mMとなるようジメチルホルムアミド(DMF;和光純薬工業製)に溶解した。また、同様にDMFを用いて200mM Benzotriazole−1−yl−oxy−trispyrrolidinophosphonium hexafluorophosphate(PyBop;メルク製)、200mM 1−ヒドロキシベンゾトリアゾール(HoBt;同仁化学製)、20mM N,N−ジイソプロピルエチルアミン(DIEA;和光純薬工業製)をそれぞれ調製した。これらのうち、フェロセンカルボン酸と塩酸ドーパミンは元濃度の1/4、またその他は元濃度の1/10となるよう混合してDMFで20mlに溶液調整した。この混合溶液を緩やかに攪拌しながら、室温で20時間反応を行った。
【0088】
反応溶液の一部を超純水で10倍に希釈し、この溶液を逆相クロマトグラフィ(HPLCシステム:Prominence(島津製作所製)、カラム:Chromolith RP−18e 100−3mm(メルク製)、移動相:A メタノール(和光純薬工業製)B 0.1%トリフルオロ酢酸水溶液(和光純薬工業製)、流速:2ml/min)を用いて解析した。紫外線検出器で波長210nmに設定し、インジェクション(0.02ml)後、1〜10minにおいてメタノールが100%となるようグラジエント溶出を行った結果、フェロセンカルボン酸と塩酸ドーパミンの複合体と考えられるピークを確認した。また、フェロセンカルボン酸および塩酸ドーパミンそれぞれ単独のピークは検出限界以下であった。これらのことから、フェロセンカルボン酸と塩酸ドーパミンの複合体の生成を確認した。
【0089】
反応溶液の残りを減圧下で10倍に濃縮し、反応濃縮溶液とした。例1で得られた、酸化チタン複合体を超純水にて固形成分1%に調整し、そこに反応濃縮溶液を1/10量混合して、全量で1mlとした。この混合溶液を緩やかに攪拌しながら、室温で1時間反応を行った。反応後、沈殿成分を遠心分離(1500g、10min)して上澄みを回収し、この溶液1mlに対してバッファー交換用自然落下型カラムNAP−10(GEヘルスケアバイオサイエンス製)を用いて水1.5mlで回収して未反応のフェロセンカルボン酸と塩酸ドーパミンの複合体およびDMFを除去した。この溶液について可視光域(400nm)における波長の吸収スペクトルを紫外−可視光分光光度計(UV1600;島津製作所製)により確認したところ増大が認められたため、フェロセンカルボン酸と塩酸ドーパミンの複合体が結合したと考えられた。これらからフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体の作製を確認した。
【0090】
例14:酸化チタン−抗体複合体へのフェロセンカルボン酸およびドーパミンの結合
例13において、例1で得られた酸化チタン複合体の代わりに、例5で得られた酸化チタン−抗体複合体を用いた以外はまったく同様にしてフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン−抗体複合体を作製した。
【0091】
例15:フェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体の超音波照射によるヒドロキシラジカル生成能の評価
例13で得られたフェロセンカルボン酸と塩酸ドーパミンの複合体結合酸化チタン複合体(酸化チタン複合体Eとする)を、リン酸緩衝生理食塩水(pH7.4)に対して、固形成分0.05%になるように調製した。また、コントロールとしてリン酸緩衝生理食塩水(pH7.4)のみを用いた。各溶液3mlを用意して試験溶液とした。超音波照射装置(オージー技研製、ULTRASONIC APPARATUS ES-2:1MHz)を用いて、3分間超音波照射(0.4W/cm2、50%パルス)を行い、照射後に各溶液に対して、ヒドロキシラジカルの生成を測定する試薬のヒドロキシフェニルフルオレセイン(HPF、第一化学薬品製)をマニュアルに従い混合し、室温で15分および30分静置、各静置時間における測定サンプルとして照射前後の溶液を400μlずつ採取した。各測定サンプルについてヒドロキシラジカル生成に起因する、Ex=490nm、Em=515nmにおける蛍光強度を蛍光分光光度計(RF−5300PC;島津製作所製)により測定した。その結果は、図4に示される通りであった。図4に示されるように、コントロールと比べて酸化チタン複合体Eは、超音波照射によりヒドロキシラジカルを効率的に生成することが確認された。また、酸化チタン複合体Eは静置時間に伴って蛍光値が増大することから、持続的にヒドロキシラジカルを生成すると考えられた。
【0092】
例16:ドーパミンを介した酸化チタン複合体への抗体の結合
抗αフェトプロテイン(抗AFP)抗体(マウスIgG:NB013、日本バイオテスト研究所製)0.1mgをCoupling buffer(pH5.5;Catalog No.153−6054、バイオラッド製)を用いて1.8mlに調製し、そこに25mg/1.2mlの過ヨウ素酸ナトリウム(和光純薬工業製)水溶液を0.2ml加えて室温にて1時間反応後、超純水を加えて2.5mlとした溶液に対してバッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いて20mM MES緩衝溶液(pH5.5)で3.2ml回収して未反応の過ヨウ素酸ナトリウムを除去し、Amicon Ultra−15(MWCO=5000;ミリポア製)で遠心分離(1500g、15min)して0.7mlに濃縮し、酸化された抗体溶液を得た。また、200mMの塩酸ドーパミン(和光純薬工業製)水溶液0.5mlと70mMのスクシンイミジル−4−ヒドラジノニコチネート−アセトンヒドラゾン(SANH;PIERCE製)水溶液0.1mlを混合し、100mM HEPES緩衝溶液(pH8.1)および超純水で総量1mlに調製し、室温にて1時間反応後、薄層クロマトグラフィーによりSANHとドーパミンの結合を確認、SANHとドーパミンの複合体溶液を得た。これら、酸化された抗体溶液0.7mlとSANHとドーパミンの複合体溶液0.1mlとCoupling buffer(pH5.5;Catalog No.153−6054、バイオラッド製)0.2mlを混合して、4℃にて16時間反応後、バッファー交換用自然落下型カラムPD−10(GEヘルスケアバイオサイエンス製)を用いてPBS緩衝液(リン酸生理食塩水)で溶出し、抗体とSANHとドーパミンの複合体と、未反応のSANHとドーパミンの複合体を除去した。こうして、抗体とSANHとドーパミンの複合体を得た。次に、例1で得られた、5(wt/vol)%の酸化チタン複合体2mlと、抗体とSANHとドーパミンの複合体1mlを混合し、4℃にて16時間反応後、44.5 mm PBCC membrane (MWCO=300000;Catalog No.PBMK04310、ミリポア製)および攪拌式セルModel8050(Catalog No.5122、ミリポア製)を用いて、メーカーのプロトコルに従い10psiで334mlの溶液交換に伴う、未結合の抗体とSANHとドーパミンの複合体除去を行った。このようにして酸化チタン−抗AFP抗体複合体粒子の分散液を得た。
【0093】
次に、SPRセンサによる抗原への結合確認のため、SPRセンサ装置(BIACORE1000,BIAcore製)にセンサチップC1(BIAcore製)をセットし、メーカーのマニュアルに従ってαフェトプロテイン(AFP:日本バイオテスト研究所製)の固定化反応を行った。移動相にはリン酸緩衝液の混合溶液(10mM リン酸緩衝液(pH7.4)、150mM NaCl、0.05(wt/vol)% Tween20)を用いた。BIAcore amine coupling kit(BIAcore製)に含まれる200μlのNHS−EDC混合溶液を30μl/minで流してセンサチップ表面のカルボキシル基をスクシニル化した後に、90mmol/lの酢酸−酢酸ナトリウム緩衝溶液(pH5.0)に100μg/mlになるよう溶解したAFPの溶液を180μl、流速30μl/minでロードして反応を行った。反応後、BIAcore amine coupling kitに含まれる1mol/lのエタノールアミンを150μl、流速30μl/minでロードして、結合に関与しなかったスクシニル基のブロッキング処理を行った。これによって150RUのレスポンスが得られた。作製した0.025(wt/vol)%の酸化チタン−抗AFP抗体複合体粒子の分散液および10μg/mlの抗αフェトプロテイン(抗AFP)抗体(マウスIgG:NB013、日本バイオテスト研究所製)をそれぞれ各濃度に調製したものを流速30μl/minで90μlロードした。センサグラムの反応確認後、100mmol/lのglycine−NaOH緩衝溶液(pH12.0)を30μl/minで100μlロードし、センサからの解離反応を行った。センサグラムの解析はBiomolecular Interaction Analysis(BIA)evaluation software(version 3.5,BIAcore製)を用いて行った。バックグラウンドとして例1で得られた酸化チタン複合体を同様にロードして得た結果を差し引いた。それらの結果、抗AFP抗体では15RU、酸化チタン−抗AFP抗体複合体粒子においては50RUのレスポンスを得た。これらの結果から酸化チタン−抗AFP抗体複合体粒子は抗原に対して強く結合することが示された。以上により、ドーパミンを介した酸化チタン複合体への抗AFP抗体を結合した、酸化チタン−抗体複合体が作製できることを確認した。
【図面の簡単な説明】
【0094】
【図1】本発明の複合体粒子の一例を示す図である。
【図2】例9において各種粒子について測定された、超音波照射による一重項酸素の発生に起因する、一重項酸素検出用蛍光試薬を介した蛍光強度を示す図である。
【図3】例10において酸化チタン−抗体複合体について測定された、抗原に対する結合評価である。
【図4】例15において酸化チタン複合体Eについて測定された、超音波照射後のヒドロキシラジカルの発生に起因する、ヒドロキシラジカル検出用蛍光試薬を介した蛍光強度を示す図である。
【特許請求の範囲】
【請求項1】
酸化チタン粒子と、
該酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を介して結合されてなる水溶性高分子を含んでなる、酸化チタン複合体と、
該酸化チタン複合体の表面に、さらに結合されてなるリンカー分子を含んでなり、該リンカー分子は、
(1)カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を有し、
(2)a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物であって、
該官能基を介して前記酸化チタンと結合され、
該官能基同士で重合すること無く、
さらに該リンカー分子を介して抗体が結合されてなり、
超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とする、複合体粒子。
【請求項2】
前記リンカー分子の結合量は前記酸化チタン粒子の質量あたり、1×10−6〜1×10−3 mol/酸化チタン粒子‐gであることを特徴とする、請求項1に記載の複合体粒子。
【請求項3】
前記リンカー分子はカテコール類であることを特徴とする、請求項1または2に記載の複合体粒子。
【請求項4】
前記リンカー分子は、ドーパミン、ジヒドロキシフェニルプロピオン酸からなる群から選択される少なくとも一種である、請求項3に記載の複合体粒子。
【請求項5】
前記水溶性高分子は重量平均分子量5000〜40000であることを特徴とする、請求項1〜4のいずれか1項に記載の複合体粒子。
【請求項6】
前記水溶性高分子は、ポリエチレングリコール、ポリアクリル酸、ポリエチレンイミンの群から選択される少なくとも一種を含んでなることを特徴とする、請求項1〜5のいずれか一項に記載の複合体粒子。
【請求項7】
20〜200nmの粒子径を有する、請求項1〜6のいずれか一項に記載の複合体粒子。
【請求項8】
前記リンカー分子を介してさらに蛍光分子が結合されてなる、請求項1〜7のいずれか一項に記載の複合体粒子。
【請求項9】
前記リンカー分子を介してさらに低原子価遷移金属を含む分子が結合されてなる、請求項1〜8のいずれか一項に記載の複合体粒子。
【請求項10】
請求項1〜9のいずれか一項に記載の複合体粒子と、該複合体粒子が分散される溶媒とを含んでなる、分散液。
【請求項11】
前記溶媒が、水系溶媒である、請求項10に記載の分散液。
【請求項12】
前記溶媒のpHが5〜8である、請求項10または11に記載の分散液。
【請求項13】
前記溶媒が、生理食塩水である、請求項10〜12のいずれか一項に記載の分散液。
【請求項14】
前記複合体粒子が、0.001〜1質量%含有される、請求項10〜13のいずれか一項に記載の分散液。
【請求項15】
請求項1〜9のいずれか一項に記載の複合体粒子を含んでなる、抗腫瘍剤。
【請求項16】
請求項10〜14のいずれか一項に記載の分散液を含んでなる、抗腫瘍剤。
【請求項1】
酸化チタン粒子と、
該酸化チタン粒子の表面に、カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を介して結合されてなる水溶性高分子を含んでなる、酸化チタン複合体と、
該酸化チタン複合体の表面に、さらに結合されてなるリンカー分子を含んでなり、該リンカー分子は、
(1)カルボキシル基、アミノ基、ジオール基、サリチル酸基、およびリン酸基の群から選択される少なくとも一つの官能基を有し、
(2)a)炭素数6〜40よりなる飽和又は不飽和の鎖状炭化水素基、b)置換基を有するか有しない飽和又は不飽和の5〜6員環複素環式基、又はc)置換基を有するか有しない飽和又は不飽和の5〜6員環環状炭化水素基を含んでなる化合物であって、
該官能基を介して前記酸化チタンと結合され、
該官能基同士で重合すること無く、
さらに該リンカー分子を介して抗体が結合されてなり、
超音波の照射による触媒活性を有する酸化チタン−抗体複合体であることを特徴とする、複合体粒子。
【請求項2】
前記リンカー分子の結合量は前記酸化チタン粒子の質量あたり、1×10−6〜1×10−3 mol/酸化チタン粒子‐gであることを特徴とする、請求項1に記載の複合体粒子。
【請求項3】
前記リンカー分子はカテコール類であることを特徴とする、請求項1または2に記載の複合体粒子。
【請求項4】
前記リンカー分子は、ドーパミン、ジヒドロキシフェニルプロピオン酸からなる群から選択される少なくとも一種である、請求項3に記載の複合体粒子。
【請求項5】
前記水溶性高分子は重量平均分子量5000〜40000であることを特徴とする、請求項1〜4のいずれか1項に記載の複合体粒子。
【請求項6】
前記水溶性高分子は、ポリエチレングリコール、ポリアクリル酸、ポリエチレンイミンの群から選択される少なくとも一種を含んでなることを特徴とする、請求項1〜5のいずれか一項に記載の複合体粒子。
【請求項7】
20〜200nmの粒子径を有する、請求項1〜6のいずれか一項に記載の複合体粒子。
【請求項8】
前記リンカー分子を介してさらに蛍光分子が結合されてなる、請求項1〜7のいずれか一項に記載の複合体粒子。
【請求項9】
前記リンカー分子を介してさらに低原子価遷移金属を含む分子が結合されてなる、請求項1〜8のいずれか一項に記載の複合体粒子。
【請求項10】
請求項1〜9のいずれか一項に記載の複合体粒子と、該複合体粒子が分散される溶媒とを含んでなる、分散液。
【請求項11】
前記溶媒が、水系溶媒である、請求項10に記載の分散液。
【請求項12】
前記溶媒のpHが5〜8である、請求項10または11に記載の分散液。
【請求項13】
前記溶媒が、生理食塩水である、請求項10〜12のいずれか一項に記載の分散液。
【請求項14】
前記複合体粒子が、0.001〜1質量%含有される、請求項10〜13のいずれか一項に記載の分散液。
【請求項15】
請求項1〜9のいずれか一項に記載の複合体粒子を含んでなる、抗腫瘍剤。
【請求項16】
請求項10〜14のいずれか一項に記載の分散液を含んでなる、抗腫瘍剤。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公開番号】特開2010−59143(P2010−59143A)
【公開日】平成22年3月18日(2010.3.18)
【国際特許分類】
【出願番号】特願2008−333364(P2008−333364)
【出願日】平成20年12月26日(2008.12.26)
【出願人】(000010087)TOTO株式会社 (3,889)
【Fターム(参考)】
【公開日】平成22年3月18日(2010.3.18)
【国際特許分類】
【出願日】平成20年12月26日(2008.12.26)
【出願人】(000010087)TOTO株式会社 (3,889)
【Fターム(参考)】
[ Back to top ]

