複合生薬抽出物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物
【課題】複合生薬抽出物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物を提供する。
【解決手段】ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物。前記組成物は、2型糖尿病モデル動物のインシュリン分泌を増加させて、インシュリン抵抗性を改善させて、強力な血糖降下活性及び糖尿性合併症抑制活性を示す。又、天然植物性成分であって、安全性が確保されているため、糖尿性疾患の予防または改善及び糖尿病合併症抑制に有用に使用できる。
【解決手段】ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物。前記組成物は、2型糖尿病モデル動物のインシュリン分泌を増加させて、インシュリン抵抗性を改善させて、強力な血糖降下活性及び糖尿性合併症抑制活性を示す。又、天然植物性成分であって、安全性が確保されているため、糖尿性疾患の予防または改善及び糖尿病合併症抑制に有用に使用できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、複合生薬抽出物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物に関し、より具体的には、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物に関する。
【背景技術】
【0002】
糖尿病は、21世紀最大の疾病とされており、現在、世界的に患者は1億7000万名おり、毎年320万名が糖尿病で命を失っている。国内でも糖尿病患者が過去20年間で12倍以上に増加して、2025年には、国民4人当たり1人が糖尿病患者になる可能性が高いため、国家的な次元の対策が切実に求められている。50代以上男性の30%、女性の20%以上が糖尿病に進行する可能性がある‘糖尿病前段階(pre-diabetes)’という調査結果は、糖尿病の深刻性を意味する。
【0003】
糖尿病は、遺伝的要因と共に、後天的要因である肥満、食生活、運動不足及びストレスなどにより影響を受ける疾病であって、膵臓細胞で分泌されるインシュリンの分泌障害及び作用不足により誘発された代謝障害と定義されており、ブドウ糖の過剰生産、体脂肪の分解及び蛋白質の浪費を伴い、グルカゴンの分泌が異常に亢進されて代謝上の混乱を引き起こす(Abrams, J.J., Ginsberg, H, et al., Metabolism of cholesterol and plasma triglyceride in nonketoticdiabetes mellitus. Diabetes, 31, pp903-910, 1982)。
【0004】
したがって、糖尿病は、生体内代謝調節機能に異常をきたし、高血糖症が現れて、尿中に糖が排泄されて、適切な治療と管理が成されないと循環器系などの合併症を伴う慢性的な代謝性疾患である(Mandrup-Poulsen, T., British Medical Journal., 316, pp1221-1225, 1998; Wilson, P. W. F. et al., Am. J. Med., 80, pp3-9, 1986)。
【0005】
糖尿病は、その発病原因及び症状の治療方法によって、大きくインシュリン依存型糖尿病(insulin dependent diabetes mellitus, IDDM)とインシュリン非依存型糖尿病(non-insulin dependent diabetes mellitus, NIDDM)とに分類できる。韓国の場合、糖尿病患者の95%以上がインシュリン非依存型糖尿病患者である。糖尿病は、それ自体が大きい疾患というよりは、長期間この疾患にかかっていることにより発病する合併症、例えば、糖尿病性神経症(neuropathy)、網膜症(retinopathy)、白内障(cataract)、腎臓病(nephropathy)などにより、患者たちが正常な生を営めないだけではなく、致命的となる可能性があるため、社会的に大きい問題とされている。
【0006】
糖尿病治療の最も重要な目標は、血糖値をなるべく正常数値に近く調節することであるが、空腹時血糖と共に食後血糖調節が、糖尿病症状の改善と合併症の予防及び治療において重要であり、治療方法として、薬物療法、食餌療法及び運動療法がある(Ref. Jenkins, D.J.A., Woever et.al., starchy food and glycemic index, Diabetes care, 11, pp149-159, 1988)。
【0007】
ところが、よく使用される薬物療法は、インシュリン及び化学的経口血糖降下剤などの化学物質を使用しており、薬物服用による副作用と患者の耐性が絶えず問題となっており、このため、天然物を利用した糖尿病治療剤の開発は、非常に重要な意味を有する。
【0008】
ゴーヤ(Momordica charantia L.)は、ウリ科(cucurbitaceae)の蔓植物であって、学名は、momordica charantiaであり、キュウリのように長いものを‘ニガウリ(bitter melon)’とも呼ぶ。原産地は、確実には知られていないが、インドを始めとした熱帯アジア地域と推定される。
【0009】
ゴーヤ成分の中、特に注目を浴びているものは、チャランチン(Charantin)と植物-インシュリン(plant-Insulin)であって、チャランチンは、インシュリンを分泌する膵臓の機能を活発にする脂溶性成分であり、植物-インシュリンは、体内でインシュリンと等しい作用をするペプチドの一種であって、ゴーヤの実と種に多く入っている(Ref. D. Sathishsekar and S. Subramanian, Biol. pharm. Bull. 28(6) pp978-983, 2005)。
【0010】
冬虫夏草(Cordyceps sinensis SACC.)は、冬虫夏草菌の子実体とそこに寄生する昆虫のコウモリガ幼虫死体との複合体である。冬虫夏草の成分としては、水分10.84%、脂肪8.4%、蛋白質25.32%、組織維18.53%、炭水化物28.90%、灰分4.10%を含有する。この他に、キナ酸(guinic acid)の異性体であるコルデーセプス酸(cordycepic acid)約7%を含有する。冬虫夏草は、強壮作用、免疫系に対する作用、血中コレステロール低下作用及びニコチンアミド(nicotinamide)とストレプトゾトシン(streptozotocin)で誘導した糖尿に対して血糖降下作用がある(Ref. Lo H.C., etal. Life sci., 74, pp2897-2908, 2004)。
【0011】
一方、上記のような生薬を、1種または2種以上を原料として、それぞれ配合を変えて得られた抽出物を有効成分とする糖尿病予防及び改善効果がある複合抽出物が明かされている。
【0012】
しかしながら、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参から構成された複合生薬抽出物に対する糖尿病予防及び治療効果に対しては、何の開示や教示もされていない。
【0013】
本発明は、血糖降下などの機能性効果があると既に知られているゴーヤ抽出物と冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参をもって、マウスの糖尿病誘発による体重変化、食餌効率、空腹時血糖及びグルコース負荷を実験し、生薬を単独使用するより、本発明の複合生薬抽出物を使用することが、抗糖尿効果にさらに優れていることを確認し、本発明を完成した。
【先行技術文献】
【非特許文献】
【0014】
【非特許文献1】Abrams, J.J., Ginsberg, H, et al., Metabolism of cholesterol and plasma triglyceride in nonketoticdiabetes mellitus. Diabetes, 31, pp903-910, 1982
【非特許文献2】Mandrup-Poulsen, T., British Medical Journal., 316, pp1221-1225, 1998; Wilson, P. W. F. et al., Am. J. Med., 80, pp3-9, 1986
【非特許文献3】Jenkins, D.J.A., Woever et.al., starchy food and glycemic index, Diabetes care, 11, pp149-159, 1988
【非特許文献4】D. Sathishsekarand S. Subramanian, Biol. pharm. Bull. 28(6) pp978-983, 2005
【非特許文献5】Lo H.C., etal. Life sci., 74, pp2897-2908, 2004
【発明の開示】
【発明が解決しようとする課題】
【0015】
本発明は、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物を提供することを目的とする。
【課題を解決するための手段】
【0016】
本発明は、上記目的を達成するために、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物を提供する。
【0017】
以下、本発明を詳細に説明する。
【0018】
本発明において、血糖調節は、特に言及しない限り、血糖降下を意味する。
【0019】
本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比の熱水抽出物から構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物を提供する。
【0020】
本発明のゴーヤは、水溶性エタノール抽出物から減圧乾燥後、粉末として得られることを特徴とする。具体的な例として、ゴーヤの実と種を粉砕して粉末にした後、95%エタノールに48時間還流した後、抽出液を常温で減圧乾燥し、黄色粉末状活性成分を取得したものを使用する。
【0021】
本発明の冬虫夏草は、白きょう菌冬虫夏草を利用するもので、白きょう菌冬虫夏草の白きょう菌菌糸体及び子実体から熱水抽出(hot-water extract)法で抽出して精製した後、凍結乾燥して冬虫夏草抽出物を取得したものを使用する。
【0022】
前記ゴーヤエタノール抽出物、冬虫夏草抽出物の混合比率が4:1〜4であることが好ましく、本発明の血糖降下活性に重要な意味を有する。
【0023】
前記地骨皮(Lycii Radicis cortex)は、クコの根皮であって、成分としては、ベタイン、ダウコステリン、アスコルビン酸がある。また、灰分では、Si、K、Na、Ca、Mg、Fe、D、S、Znなどが確認されて、解熱作用、血圧降下及び血糖降下作用がある(Ref. Funagama S. etal, Fetrahedron Lett. 21, pp1355-1356, 1980)。
【0024】
前記桑白皮(Mori cortex Radicis)は、桑の木または桑の木科の根皮であって、成分としては、mulberrin(C25H26O6, 0.15%)、mulberrochromene(C25H24O6, 0.2%)、cyclomulberrin(C25H24O6, 0.02%)、cyclomulberrochromene(C25H22O6, 0.016%)などがあり、利尿、血圧降下作用、血糖降下作用がある(Ref. Hikino. H etal. plant Med. 159 pp 160(1985))。
【0025】
前記鬼剪羽(EuonymiLignum Suberalatum)は、ニシキギ科のニシキギの幹に矢のように生えたコルクを切って干したもので、成分としては、コルクのタンニン質と、根皮にはグッタペルカに似たゴム質がある。これは、癌細胞の侵入と転移過程に活性を抑制して、アロキサン(alloxan)で誘導した糖尿(rabbit)に対して血糖や尿糖を下げて、体重を増加させる作用がある(Ref. Kitanaka S. etal. chem.pharm.Bull44, pp615-617, 1996)。
【0026】
前記葛根(PuerariaeRadix)は、葛(豆科)の周皮を除去した根であって、成分としては、イソフラボン化合物である4,7−ジヒドロキシイソフラボン、アミドゼイン−7−グリコシドなどとクマリンを有しており、解熱鎮静作用、循環系に対する作用とブドウ糖の活性を増加させる血糖降下作用がある(Ref. Hsu H.H etal. planta Med. 68, pp999-1003 (2002))。
【0027】
前記黄精(polygonati Rhizoma)は、シベリアアマドコロ、ナルコユリまたは眞黄精(ユリ科)の根茎の外皮をむいて蒸したもので、コンバラリン、コンバラマリンなど、少ない量のアルカロイド、アスパラギン、マンニトを始めとしたMn、Cu、Fe、Mg、Zn、Moを含んでいる。滋養強壮作用とストレプトゾトシン(streptozotocin)糖尿を誘発させたマウスの血糖を下げる作用がある(Ref. Kato A. Miura T., planta Med. 60 pp201-203 (1994))。
【0028】
前記白朮(AtractylodisRhizoma Alba)は、オケラまたは唐白朮(キク科)の根茎または周皮を除去したものである。成分としては、根茎に約1.5%精油とカロリン、イヌリンゴム質、サポニン、クマリンなどを含んでおり、鎮胃、利尿、鎮静作用と血糖降下作用がある(Ref. Konno C. etal. planta Med. 51, pp102 (1985))
【0029】
前記麥門冬(Liriopis Tuber)は、ユリ科の根の膨大部である。乾いた塊根の約71%は、単糖(約10%)と分子量の少ない多糖類(粘液43%)である。また、β-シトステロール、ルスコゲニンなどを含有している。解熱鎮咳、抗炎症作用があり、水抽出物には、持続的な血糖降下作用がある(Ref. Lin YC etal. Am.J. Chin Med 31, pp354-579(2003))。
【0030】
前記山茱萸(CorniFructus)は、ミズキ科に属するサンシュユの果肉であって、種を除去したものである。没食子酸、リンゴ酸、酒石酸とモルロニシドとサポニン成分のロガニンが主成分であって、利尿、血圧降下、滋養強壮及び血糖降下作用がある(Ref. Jeng H etal. Am.J. Chin Med. 25, pp301-306 (1997))
【0031】
前記ウコギ科に属する高麗人参(GinseugRadix Alba)は、根であって、側根とコルク層を除去したものである。根には、配糖体、精油、アミノ酸、アルカロイド、炭水化物、樹脂、微量元素などが含まれ、滋養強壮作用、免疫増強作用、中枢神経系、心血管系作用、血糖降下作用、脂質代謝作用、抗癌作用、脳下垂体副腎皮質系などに作用をする(Ref. Yokozawa T. etal. Chem.pharm.Bull 33, pp869-872 (1985))。
【0032】
本発明の組成物の場合、ゴーヤエタノール抽出物、冬虫夏草抽出物及び、前記地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸及び高麗人参の熱水抽出物から成り、前記熱水抽出物が地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比で構成される、複合生薬抽出物を使用することを特徴とする。
【0033】
具体的な例として、地骨皮250g、桑白皮280g、鬼剪羽200g、葛根250g、黄精230g、白朮100g、麥門冬100g、山茱萸100g、高麗人参100gを細切した後、常温で20lの水に2時間漬けておいてから、80℃で3時間加熱し、2回目は、15lの水で1.5時間加熱して、3回目は、水15lで1時間加熱、このように3回繰り返して加熱して得た抽出液を、80℃で減圧濃縮して熱水抽出物を得たものを使用した。
【0034】
本発明による複合生薬抽出物は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び熱水抽出物から構成されて、これらの混合比率が4:1〜4:2〜5の重量比であることを特徴とする。
【0035】
本発明による前記メドハギ抽出物の発酵物は、メドハギ抽出物20〜40重量%にアスペルギルス・オリゼー(Aspergillus oryzae)菌株を接種して固体発酵させたことを特徴とし、また、前記メドハギ抽出物は、水、エタノールまたはこれらの混合溶媒で抽出後、エタノール沸騰点(78.3℃)以上に高温殺菌して得られることを特徴とする。
【0036】
前記メドハギは、根を含んだメドハギ植物全体をきれいに洗浄した後、細かく細切する。前記細切時、甘くて風味に優れた梨、リンゴ、柿、枸杞子からなる群から選択された1種以上の実または果物をさらに添加して製造することができ、前記実または果物は、味が苦くて辛いメドハギの嗜好性を増進させて、老若男女のだれもが飲用できるような飲料や茶を製造することができる。
【0037】
前記細切されたメドハギ、枸杞子の実やリンゴなどの果物を粉末形態に粉砕した後、エタノールを添加して静置及び熟成させる段階を経る。特にメドハギは、機能性ウェルビーイング漢方薬として利用されているが、エタノールで熟成させた後に抽出しないと、その効能が低下する問題がある。したがって、一般茶や飲料を製造する方法と異なって、メドハギの効能を増加させるために、エタノールで5日〜10日程度静置保管して、自然熟成させる過程が必要である。
【0038】
前記回収されたメドハギ抽出物は、熟成過程でエタノールが蒸発して一部消滅するが、まだエタノール成分が含まれてアルコール気が残っているため、飲料として不適な側面があり、その味が苦い短所がある。したがって、本発明者らは、このような問題点を解決するために、残存エタノールを除去するために、エタノール沸騰点(78.3℃)以上にて5時間程度高温殺菌して、前記残存アルコールを蒸留消滅させながら殺菌して、前記メドハギ抽出物を取得した。
【0039】
具体的な例として、メドハギを細かく細切した後、95%エタノールを添加して10日間静置及び熟成させる。前記熟成されたメドハギ抽出液を、ふるいまたは網紗の布で、固形化された不純物を分離ろ過し、メドハギ抽出液を回収した後、エタノール沸騰点(78.3℃)以上にて5時間高温殺菌して、残存アルコールを蒸留消滅させながら殺菌し、メドハギ抽出液を取得した。前記取得したメドハギ抽出物を20g量り取って均質に混合した後、種菌のコウジカビのアスペルギルス・オリゼー(Aspergillus oryzae)KFRI 00888(ATCC 22887)菌株0.1%を接種させた後、温度30〜32℃、湿度70〜85%の培養室で36〜42時間固体培養して、本発明による組成物を製造した。この際、培養を促進するためにビオチン(biotin)0.001%を添加して、メドハギ抽出物の発酵物を製造した。
【0040】
前記メドハギ抽出物は、発酵工程を通じて、原料内の有効成分が多様な有用性成分に転移すると考えられており、特に発酵を通じて多様な酵素成分が生成され、蛋白質の低分子化が起こり、また、ビタミンが合成され、機能性成分が活性型に転移されるなど、その有用性が極大化される。血中ブドウ糖の代謝が円滑に成されなくて発生する糖尿病は、固体発酵産物内の転移された活性成分が体内エネルギー代謝を促進させて、酵素及び細胞機能を活性化させることにより、糖尿病改善及び予防に役立てる。
【0041】
本発明における糖尿病とは、1型糖尿病または2型糖尿病であり、糖尿病合併症は、神経性合併症、糖尿病性網膜症、腎不全症、性機能障害、皮膚疾患、高血圧、動脈硬化症、脳卒中、心臓病、または壊疽である。即ち、本発明における糖尿病または糖尿病合併症の治療または予防用組成物は、糖尿病哺乳動物の膵臓からインシュリン分泌を増加させて、膵臓インシュリン含量を増加させて、空腹時、血糖を上昇させて、耐糖能(glucose tolerance)を改善させることを特徴とする。
【0042】
本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物を有効成分として含有する薬学組成物を提供する。
【0043】
本発明の抽出物を含む薬学組成物は、薬学的組成物の製造に通常に使用する適切な担体、賦形剤及び希釈剤をさらに含むことができる。前記担体、賦形剤及び希釈剤としては、ソルビトール、マンニトール、キシリトール、エリスリトール、マルチトール、澱粉、アカシアゴム、アルギネート、ゼラチン、カルシウムホスフェート、カルシウムシリケート、セルロース、メチルセルロース、微晶質セルロース、ポリビニールピロリドン、水、メチルヒドロキシベンゾエート、プロピルヒドロキシベンゾエート、タルク、マグネシウムステアレート及び鉱物油が挙げられる。
【0044】
本発明の抽出物を含む組成物は、それぞれ通常の方法により、散剤、顆粒剤、錠剤、カプセル剤、懸濁液、エマルジョン、シロップ及びエアロゾルなどの経口型剤形、外用剤、坐剤及び滅菌注射溶液の形態に剤形化して使用できる。
【0045】
詳細には、製剤化する場合は、普段使用する充填剤、増量剤、結合剤、湿潤剤、崩解剤、界面活性剤などの希釈剤または賦形剤を使用して調製できる。経口投与のための固形製剤には、錠剤、丸剤、散剤、顆粒剤及びカプセル剤などが含まれて、このような固形製剤は、前記抽出物またはこれの粉末に少なくとも一つ以上の賦形剤、例えば、澱粉、カルシウムカーボネート(calcium carbonate)及びゼラチンなどを混ぜて調製できる。また、単純な賦形剤の他に、マグネシウムステアレート及びタルクのような潤滑剤も使用できる。経口のための液状製剤としては、懸濁剤、内溶液剤、油剤及びシロップ剤などが該当するが、よく使用される単純希釈剤の水及びリキードパラフィンの他に様々な賦形剤、例えば、湿潤剤、甘味剤、芳香剤及び保存剤などが含まれる。非経口投与のための製剤には、滅菌された水溶液、非水性溶剤、懸濁剤、油剤、凍結乾燥製剤及び坐剤が含まれる。非水性溶剤、懸濁剤としては、プロピレングリコール(propylene glycol)、ポリエチレングリコール及びオリーブオイルのような植物性オイル及びエチルオレートのような注射可能なエステルなどが使用できる。坐剤の基剤としては、witepsol、マクロゴル、tween61、カカオジ、ラウリンジ及びグリセロゼラチンなどが使用できる。
【0046】
本発明の抽出物の好ましい投与量は、患者の状態及び体重、疾病の程度、薬物形態、投与経路及び期間によって異なるが、当業者により適宜選択できる。しかし、好ましい効果のために、本発明の抽出物は、0.01〜20g/kg、好ましくは0.01〜10g/kgの量を一日1回乃至数回に分けて投与できる。組成物において、本発明の抽出物または複合生薬粉末は、全体組成物の総重量に対して0.1〜50重量%の含量で配合できる。
【0047】
本発明の薬学組成物は、ラット、マウス、家畜、人間などの哺乳動物に多様な経路で投与できる。投与のあらゆる方式が予想できるが、例えば、経口、直腸または静脈、筋肉、皮下、子宮内硬膜及び脳血管内(Intracerebroventricular)注射により投与できる。
【0048】
また、本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物を有効成分として含有する血糖降下用健康食品を提供する。
【0049】
前記抽出物を食品に使用する場合は、それをそのまま使用するか、他の食品または食品成分と共に使用することができ、通常の方法によって適宜使用できる。有効成分の混合量は、その使用目的(予防、健康または治療的処置)によって適宜決定できる。一般に、食品または飲料の製造時には、前記ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物が、原料に対して10乃至90重量%、好ましくは、30乃至70重量%の量で添加される。
【0050】
しかしながら、健康増進、あるいは健康管理を目的とする長期間の摂取の場合は、前記範囲以下の量であってもよく、有効成分は、安全性面で何の問題もないため、前記範囲以上の量でも使用可能であることは確実である。前記食品の種類には特に制限がない。前記物質を添加できる食品の例としては、肉類、ソーセージ、チョコレート、キャンディー類、スナック類、お菓子類、ピザ、麺類、ガム類、アイスクリーム類を含む酪農製品、各種スープ、飲料、お茶、ドリンク剤、アルコール飲料及びビタミン複合剤などがあって、通常の意味での健康食品を全て含む。
【発明の効果】
【0051】
本発明による糖尿病または糖尿病合併症の治療または予防用組成物は、2型糖尿病モデル動物のインシュリン分泌を増加させて、インシュリン抵抗性を改善させて、強力な血糖降下活性及び糖尿病性合併症抑制活性を示し、また、天然植物性成分であって、安全性が確保されているため、糖尿病性疾患の予防または改善及び糖尿病合併症抑制に有用に使用できる。
【発明を実施するための最良の形態】
【0052】
本発明を詳細に記述する前に、特定具体例の変形例が行われ得るが、添付の特許請求の範囲の範疇内に含まれるため、本発明は、以下記述する本発明の特定な具体例に限定されないことを理解すべきである。また、使用された用語は、特定具体例を説明するためのものであって、限定するものではない。その代わり、本発明の範囲は、添付した特許請求の範囲により確立される。
【0053】
本明細書と添付の特許請求の範囲に使用する単数形態は、明確に指示しない限り、複数形態も含むことを理解すべきである。特に定義しない限り、本明細書に使用された全ての専門科学用語は、当業者が普遍的に理解しているものと同じ意味を有する。
【0054】
(製造例)
(1)ゴーヤ抽出物の製造
ゴーヤの実(1kg)と種(1kg)を、不純物を除去して、水で土と埃を洗った後、100乃至400メッシュの大きさの粒子に粉砕して、粉末にした。これを20lの95%エタノールにて48時間還流した後、抽出液を常温で減圧乾燥し、30gの黄色粉末状活性成分を取得した。
【0055】
(2)冬虫夏草抽出物の製造
白きょう菌冬虫夏草1kgを、不純物を除去した後、水で土と埃を洗って細切した後、水20lに常温で2時間漬けておいてから80℃で3時間加熱して、2回目は、水15lにて1.5時間加熱し、3回目は、水15lにて1時間加熱した。
【0056】
前記3回繰り返して加熱して得た抽出液を80℃で減圧濃縮して精製した後、凍結乾燥して、冬虫夏草抽出物10gを取得した。
【0057】
(3)熱水抽出物の製造
地骨皮250g、桑白皮280g、鬼剪羽200g、葛根250g、黄精230g、白朮100g、麥門冬100g、山茱萸100g、高麗人参100gから不純物を除去した後、水で土と埃を洗って細切した後、1610gを水20lに常温で2時間漬けておいてから、80℃で3時間加熱し、2回目は、15lの水にて1.5時間加熱して、3回目は、水15lにて1時間加熱した。
【0058】
前記3回繰り返して加熱して得た抽出液を、80℃で減圧濃縮して熱水抽出物250gを得た。
【0059】
(4)メドハギ発酵物の製造
メドハギ1kgをきれいに洗浄した後、細かく細切して、20lの95%エタノールを添加して10日間静置及び熟成させる。前記熟成されたメドハギ抽出液を、20〜50メッシュのふるいまたは網紗の布で、固形化された不純物を分離し、メドハギ抽出液を回収した後、エタノール沸騰点(78.3℃)以上にて5時間高温殺菌して、残存アルコールを蒸留消滅させながら殺菌し、メドハギ抽出液を取得した。
【0060】
前記取得したメドハギ抽出物を20g量り取り均質に混合した後、種菌のコウジカビのアスペルギルス・オリゼー(Aspergillus oryzae)KFRI 00888(ATCC 22887)菌株0.1%を接種させた後、温度30〜32℃、湿度70〜85%の培養室で36〜42時間固体培養して、本発明による組成物を製造した。この際、培養を促進するためにビオチン(biotin)0.001%を添加した。
【0061】
(実施例)糖尿病または糖尿病合併症の治療または予防用組成物の製造
前記方法により抽出したゴーヤエタノール抽出物30g、冬虫夏草抽出物10g、熱水抽出物250g及び発酵物10gを40℃以下で混合機で均質に混合して、300gの糖尿病または糖尿病合併症の治療または予防用組成物を製造した。
【0062】
(試験例1)急性毒性試験
1.試験系
(1)種及び系統:特定病原菌不在(SPF)マウス
(2)供給源:吉林獣医大学研究センター実験動物肉腫育種課
(3)試験系の選択理由
マウスは、毒性試験に適した実験動物であって、急性毒性試験に広く使用されている。本系統のマウスは、豊富な試験基礎資料が蓄積されていて、試験結果の解釈及び評価時、このような資料を利用することが可能である。
(4)週齢及び体重範囲
【0063】
【表1】

【0064】
(5)検疫及び馴化
動物入手後、外観を肉眼で検査し、7日間試験を施す動物室で馴化させた後、一般症状を観察して、健康な動物のみを試験に提供した。
【0065】
2.飼育環境
(1)環境条件
本試験は、温度23±30℃、相対湿度55±15%、照明時間12時間(午前8時〜午後8時)及び照度150〜300Luxに設定された韓国化学研究所安全性研究センター中動物洞の2号室で行われた。試験者らはみんな高圧蒸気滅菌(121℃、20分)された作業服、頭巾、マスク及び手袋などを着用して作業を行った。
【0066】
(2)飼育環境モニタリング
試験期間中、動物室の温湿度は、自動温湿度測定器により毎時間測定されて、照度などの環境条件は、定期的(3ヶ月に1回)に測定された。環境測定の結果、試験に影響を及ぼすと思われるような変動はなかった。
【0067】
(3)飼育箱、飼育密度及び飼育箱の識別試験期間の間、ステンレス製網飼育箱(220w×420L×200H mm)を利用して、馴化期間には4匹ずつ、投与と観察期間中は5匹ずつを収容した。試験期間中、飼育箱には、試験番号及び動物番号を記入した個体識別カード(媒体対照群:白色、T1:黄色)を付した。
【0068】
(4)飼料及び飲水
i)飼料の給与方法
飼料は、実験動物用固形飼料(吉林飼料公司)を放射線(2.0Mrad)滅菌して、自由に摂取させた。また、当該研究所実験動物室と供給会社で微生物及び汚染物質確認試験を施したところ、本試験に影響を及ぼすような要因は発見されなかった。
ii)飲水の給与方法及び汚染物質の確認
飲水は、上水道水を紫外線殺菌器で消毒した後、自由に摂取させた。飲水に対しては、給与前に予め一般水質検査を行って、検査の結果、試験に影響を及ぼすような要因は発見されなかった。
【0069】
3.投与量及び試験群の構成
(1)投与量設定
本試験物質は、植物抽出物製剤であって、予備試験の結果、限界容量である2000mg/kgの容量で死亡動物が観察されなかったため、限界容量試験の一環として最高容量を2000mg/kgにして、媒体のみを投与する媒体対照群をおいた。但し、中国衛生部の‘毒性試験条例’には、限界容量に対する基準がないため、日本厚生省の‘医薬品非臨床試験ガイドライン解説(1997)’を参考した。
(2)試験群の構成、投与濃度及び容量
【0070】
【表2】

【0071】
(3)群分離及び動物識別
動物の群分離は、以下のように行った。まず、馴化期間中、健康だと判定された動物の体重を測定した後、5g間隔で区分しておいた。そして、雌・雄それぞれの平均体重に近い個体を雌雄それぞれ10匹ずつを選択した。5g間隔で区分されて選択された雌雄それぞれ10匹を雌・雄各群に5匹ずつ均等に入るように、体重を利用した無作為法を利用して分配した。動物の個体識別は、皮毛色素マーキング法及び個体識別カード表示法で行った。
【0072】
4.試験物質の投与
(1)投与液の調製法
投与直前に、注射用生理食塩水を媒体として試験物質を2000mg/20ml/kgに調製した。媒体対照群(vehicle control)の動物には、媒体の0.5%CMCのみを投与した。
【0073】
(2)投与経路及び投与方法
投与前日一晩中絶食させた後、経口投与用ゾンデ(sonde)を装着した注射器を利用して、調製試験物質を強制経口投与した。
【0074】
(3)投与経路の選択理由
臨床予定経路として経口投与を選択した。
【0075】
(4)投与回数及び投与期間
投与当日午前に個体別に単回投与した。
【0076】
(5)投与液量の計算
投与当日の測定された体重を基準にして投与液量(20ml/kg)を計算した。
【0077】
5.観察及び検査項目
(1)一般症状及び死亡動物の観察
投与当日は、投与後1時間から6時間までは毎時間、投与翌日から14日までは毎日1回以上一般症状及び死亡動物の有無を観察した。
【0078】
(2)体重測定
試験に使用された全ての動物に対して、投与開始前と投与後1、3、7及び14日に体重を測定した。
【0079】
(3)剖検所見
全体生存動物をCO2ガスで麻酔して開腹して、放血致死させた後、肉眼で全ての内部臓器を観察した。
【0080】
6.統計学的方法
吉林獣医大学毒性研究センターのSOPによって統計処理を行った。
【0081】
7.結果
一般症状を観察した結果、全ての試験群では観察期間の間、何の異常症状も観察されず、雌・雄の全ての試験群において、投与後、1、3、7及び14日目、正常的な体重増加が観察された。
【0082】
また、死亡率及びLD50値(動物の半数致死量)を調べた結果、雌・雄の媒体対照群及び2000mg/kg投与群において、試験期間を通じて死亡動物は観察されず、雌・雄動物に対する本試験物質のLD50値は、それぞれ2000mg/kgを上回って、剖検結果も同様に、雌雄の全ての試験群において、肉眼で異常のある剖検所見は観察されなかった。
【0083】
本発明による糖尿病または糖尿病合併症の治療または予防用組成物に対する単回経口投与毒性試験を、雌雄SD系統のマウスを利用して行った結果、試験期間の間、死亡率、一般症状、体重変化及び剖検所見において、試験物質の投与に起因した変化は観察されなかった。
【0084】
(試験例2)長期毒性試験
1.試験薬
本発明による試料は、糖尿病または糖尿病合併症の治療または予防用組成物であって、粉末1gは、生薬10.6gに該当し、蒸留水を溶剤として必要な濃度に製造して使用した。
【0085】
2.実験動物
マウスは、体重が95〜102g、性別は、雌・雄同数の西安医科大学実験動物センター提供SD系マウス(批准番号07−005号)を利用した。
【0086】
分類は、SD系マウス160匹を無作為に4群に分類、各群40匹雌雄同数とした。高容量群は、試験薬3.0gを15.0%濃度の懸濁液にして(臨床容量の50倍)20ml/kgを経口投与して、中容量群は、試験薬1.5gを7.5%濃度の懸濁液にして、20ml/kgを経口投与して、低容量群は、試験薬0.3gを1.5%濃度の懸濁液にして、20ml/kgを経口投与した。対照群は、蒸留水のみを投与した。
【0087】
飼育は、空調施設、飼育温度18〜24℃、相対湿度45〜70%にして、 換風機を利用して換気をして、1日12時間ずつ照明を与えた。飼料は、西安医科大学実験動物センターで製造した標準固体飼料で飼育して、一般家庭用水で飲水を供給するが、性別を区分して飼育した。
【0088】
飼育箱当たり5匹を飼育して、3日毎に飼育箱を掃除して、上記条件に1週間適応させた後、実験を行った。
【0089】
マウスを試験動物に選定した理由は、この動物が毒性試験に適した実験動物であって、急性毒性試験に広く使用されており、特に、SD系は、試験基礎資料が十分確保され得るため、試験結果の解釈及び評価時、このような資料を利用することが可能であるためである。
【0090】
3.実験方法(投与方法)
毎日1回経口投与して、投与3ヶ月後、試験動物に対して関連検査を行う。
【0091】
4.試験項目
(1)一般的状況及び体重
試験に使用された全ての動物に対して神経状態、活動状態、分泌物、飲食習慣、排泄物、毛髪、皮膚などの状態を観察して、2週毎に体重を測定し、変化によって容量を調節した。
【0092】
(2)血液学的検査
試験に使用された全ての動物に対して、投与3ヶ月後、各群別に大腿動脈から採血して、血蛋白(Hb)、赤血球(RBC)、白血球(WBC)及び血小板(Pt)を検査した。
【0093】
(3)血液生化学的検査
試験に使用された全ての動物に対して、投与3ヶ月後、大腿動脈から採血して、血液内の各種物質の濃度(ALT, AST, ALP, TP, ALB, BUN, Crea, T-BIL, GLU)を検査した。
【0094】
(4)尿検査
試験に使用された全ての動物に対して、検査期間にマウス代謝ケースを使用して尿を収集し、色相、尿糖、尿蛋白、赤血球、白血球などを検査した。
【0095】
(5)心電図
試験に使用された全ての動物に対して、検査期間に標準心電図を検査した。
【0096】
(6)解剖(主要臓器係数)
試験に使用された全ての動物に対して、検査期間に心臓、肝、脾臓、肺、腎臓、胸腺、副腎、睾丸、卵巣など、九つの臓器を測定した。
【0097】
(7)組織病理学的検査
試験に使用された全ての動物に対して、心臓、肝、脾臓、肺、腎臓、胃頭部、十二指腸、空腸、結腸、膀胱、腸間膜リンパ節、睾丸、副睾丸、卵巣、子宮、胸骨(骨髄)、大脳、垂体、副腎、胸腺、甲状腺など、21個組織を検査した。
【0098】
5.結果
一般的な状態及び体重変化を観察した結果、投与13週後、一般的な状態は良好であり、毛髪、神経状態、活動状態、目、鼻の分泌物も正常であった。24時間の食餌習慣も正常であって、体重は段々増加したが、対照群と比較時、変化程度には有意差がなかった。
【0099】
血液学的影響及び血液生化学的影響を調べるために、投与3ヶ月後、及び回復後、それぞれペントバルビタール(pentobarbital)を皮下注射して麻酔させた後、大腿動脈から採血して、血液検査及び生化学的検査を行った。その結果、血液学的影響は、下記表1から確認できるように、投与群の検査数値に特別な変化がなく、対照群と比較し著しい差はなかった。
【0100】
【表3】

【0101】
血液生化学的影響は、アミノトランスフェラーゼ(aminotransferase)、肝機能、腎機能、血糖を調査した結果、下記表2の結果からも確認できるように、高容量投与群の血糖は著しく降下して、対照群に比べて著しい差を確認して、その他の項目別生化学的検査値は正常であって、対照群と統計学的差はなかった。
【0102】
【表4】

【0103】
尿に対する影響を調べた結果、下記表3の結果のように、各試験動物の尿状態は正常であって、尿糖、尿蛋白など、全て陰性であって、顕微鏡検査結果、赤血球と白血球も発見されなかった。これは、試験薬物がマウスの尿に対して何の影響もないことを確認したことである。
【0104】
【表5】

【0105】
試験薬物投与3ヶ月後、心電図に対する影響を調べた結果、試験動物の心拍率、S−波、T−波など、各波は、対照群と差がなかった。また、試験薬物の投与後、試験動物を解剖して、肉眼で心臓、肝、脾臓、肺、腎臓、胃、空腸、結腸、膀胱、胆嚢、副腎、胸腺、睾丸、子宮、脳、垂体、腹腔、胸腔などの主要臓器及び体腔の色相、形態、病巣などを観察した結果、臓器及び体腔の色相と形態には異常がなく、病巣も観察されなかった。
【0106】
前記解剖された試験動物の心臓、肝、脾臓、肺、腎臓、副腎、胸腺、睾丸、卵巣などを採取して、臓器の大きさによって重量を測った後、臓器係数を測定した(g/100g体重、またはmg/100g体重)。
【0107】
その結果、下記表4の結果からも確認できるように、各臓器係数は、全て正常範囲内に含まれることを確認した。
【0108】
【表6】

【0109】
組織病理学的検査のためにマウス臓器を採取して、その中、対照群及び高容量投与群は各6匹から、中容量群と低容量群も各6匹から採取した。
【0110】
臓器組織は、心臓、肝、脾臓、肺、腎臓、胃、十二指腸、空腸、結腸、腸間膜リンパ節、副腎、胸腺、甲状腺、睾丸、副睾丸、卵巣、子宮、胸骨(骨髄)、大脳、垂体と、さらに本試験薬物が血糖降下作用があるため、膵臓腺の組織を追加して、計21個組織を採取した。
【0111】
前記組織は、10%ホルムアルデヒド溶液で固定し、パラフィン切片を作って、HEで染色した後、顕微鏡で試験群と対照群を比較しながら観察した結果、図1及び図2からも確認できるように、試験群の臓器組織は、構造上明確であり、試験薬物投与時の充血、浮腫、変性、怪死、細胞浸潤などの病理学的変化は観察されなかった。
【0112】
したがって、本試験薬物は、病理学的影響が現れなかったことを確認して、試験薬物は、マウスに対する13週間の反復投与結果、特異な毒性反応はなく、安全な服用量は、体重で換算し、3.0g/kg体重/dayであることを確認することができた。
【0113】
(試験例3)血糖降下効果の測定
前記実施例で製造された糖尿病または糖尿病合併症の治療または予防用組成物(以下、試験薬物と称する)の血糖降下効果を測定するために、下記のような実験を行った。
【0114】
実験動物は、大韓実験動物センターから入手したマウスに、0.85%食塩水(Saline)に溶解させたストレプトゾトシン(Streptozotoxin;STZ, Sigma.co.,USA)を5日間反復投与して、人為的に糖尿病を誘発した後、前記試験薬物を投与して、血糖の変化を比較観察して、本発明の組成物の治療効果を調べた。
【0115】
1.実験方法
実験動物は、大韓実験動物センターから入手して、清浄室内で温度22±2℃、湿度55±5%、照明12L/12Dの条件下で管理した。
【0116】
試験動物は、計4群に分けて、具体的に、第1対照群は、ストレプトゾトシンを投与しなかった対照群として、第2対照群は、ストレプトゾトシンを60mg/kgを3乃至5回腹腔投与して、第3対照群は、ストレプトゾトシンと共に、偽薬として0.85%食塩水(Saline)を投与して、実験群は、前記第3対照群に投与した試料に、本発明による試験薬物を267mg/ml/kgを投与した。
【0117】
試験薬物は、投与当日から23日まで投与して、4日毎に血糖、尿糖、体重を測定した。
【0118】
血糖の測定は、マウスの尻尾静脈から採血して、血糖値を簡易血糖計(アキュトレンド、緑十字)で測定して、測定技術上、最高血中濃度500mg/dlまでのみ測定した。
【0119】
2.結果
本発明による糖尿病または糖尿病合併症の治療または予防用組成物(以下、試験薬物と称する)に対するマウス個体別血糖値を測定した結果、下記表5で確認した結果、血糖値300mg/dl以上を糖尿病マウスと判定する時、第2対照群では、試験の終わった10匹の中9匹が、第3対照群では、10匹の中8匹が糖尿病と判定されたが、試験薬物を投与した実験群では、ストレプトゾトシンマウスの糖尿病発病が抑制されたことを確認することができた。
【0120】
【表7】

【0121】
(試験例4)インシュリン非依存型糖尿病(NIDD)に対する効果
2型(インシュリン依存型)糖尿病に対する試験薬の効果を測定するために、2007年12月〜2008年9月の期間中、中国陝西省西安市と中国吉林省長春市一帯に居住する51名のインシュリン非依存型(NIDD)糖尿病患者に対して、本試験薬を投与して、臨床治療効果を観察した。
【0122】
1.対象者選定
1)選定患者基準(1998年WHO標準):血糖を測定して、下記(1)乃至(3)の条件中の一つのみに符合すれば、糖尿病患者と診断する。
(1)空腹時血糖≧7.8mmol/l(140mg/100ml)、または食後血糖≧11.1mmol/l(200mg/100ml)
(2)空腹時血糖は、7.8mmol/lより低いが、ブドウ糖75gでOGTTを行った時、血糖が≧11.1mmol/l(200mg/100ml)
(3)OGTT 1時間後血糖が≧11.1mmol/lであるか、または、OGTT2時間後血糖が≧11.1mmol/l、または空腹時血糖が≧7.8mmol/l
【0123】
2)試験対象者選定基準
前記1)項の基準に適合する者でも、次の各号の一つに該当すれば、除外する。
(1)試験薬の投薬前より血糖は正常より高いが、食餌療法や運動療法などで空腹時血糖が7.8mmol/l(140mg/100ml)より高いか、食後2時間後の血糖が11.1mmol/l(200mg/100ml)より低い場合
(2)食餌療法規定や薬物服用規定を守らなくて、薬効に影響を与える者
(3)合併症が深刻な者、あるいは他の病歴者
(4)糖尿病が最近1ヶ月内に発病した者または酸中毒及び感染者
(5)治療を中断した者、薬効が判断できないか、資料が不完全な者
(6)インシュリン依存型糖尿病(IDD)患者
(7)15歳以下であるか、妊婦あるいは産婦
【0124】
3)一般
【0125】
【表8】

【0126】
2.試験方法
1)一般的観察
(1)一般的な身体検査
(2)血、糖尿検査及び血、尿ルチン検査
(3)一部患者に対して心臓、腎臓、肝、血中脂質検査
【0127】
2)薬効観察
(1)病歴を詳細に確認して、食餌、運動、心理、糖尿病に対する知識などを確認する。
(2)空腹及び食後2時間後、血糖検査(投薬後10乃至15日毎に観察する)
(3)耐糖能(glucose tolerance)実験(OGTT)
(4)インシュリン分泌(insulin release)実験(INSRT)
(5)アミノフルクトース(Amino Fructose)測定
【0128】
薬物投与期間は、基本60日を単位とし、上記の(1)項の血糖検査及び(2)項の耐糖能(glucose tolerance)は必ず行って、その他の項目は、患者状況によって行うが、試験薬物の服用後、10乃至15日毎に空腹時血糖、尿糖、または食後2時間後、血糖と尿糖を測定した。
【0129】
薬物服用開始後、患者は、下記の基準により食餌療法を行って、投与60日後に、治療前の記録と比較して評価した。
【0130】
【表9】

【0131】
3)治療及び観察
(1)薬物投与方法:3回/日、4カプセル/回、食前30分乃至食後30分の間に経口で服用した。以後、血糖降下の程度によって容量を調節し、基本維持量は、3〜4カプセル/日として服用した。
(2)治療期間:60日を治療周期として、10乃至15日間隔で空腹時及び食後2時間後の血糖及び尿糖を検査した。
【0132】
4)薬効判定標準
中国糖尿病会議標準及び中和人民共和国衛生部標準によって、
(1)著しい効果
○治療後、症状は基本的になくなって、
○空腹時血糖<7.2mmol/l(130mg/100ml)、
○食後2時間後の血糖<8.3mmol/l(150mg/100ml)
○24時間内の尿糖量<10(g)
○血糖値及び24時間内の尿糖量が、治療前より30%降下した場合、著しい効果と判定した。
【0133】
(2)有効:
○治療後、一般的な症状は改善されて、
○空腹時血糖<8.3mmol/l(150mg/100ml)、
○食後2時間後の血糖<10mmol/l(180mg/100ml)
○24時間内の尿糖量<25(g)
○または、血糖量及び24時間内の尿糖量が、治療前より10%降下した場合、有効と判定した。
【0134】
(3)無効:
○治療後、症状は改善されず、血糖及び尿糖降下作用が上記の基準外である場合、無効と判定した。
【0135】
3.試験結果
投薬前・後の血糖変化を調べた結果を下記表6乃至7に示した。
【0136】
【表10】

【0137】
【表11】

【0138】
上記表6乃至7から確認できるように、治療後、血糖降下値(mmol/l)を見ると、3.1mmol/l以上降下した症例は、計51名の中49名であって、96.08%に血糖降下効果があることを確認した。
【0139】
【表12】

【0140】
【表13】

【0141】
また、被験者を対象に投薬前後の症状を確認した結果も、治療後、大部分は、治療前に比べて、典型的な症状である咽の渇き、食欲過多、過尿現象がなくなって、特に無力感などが著しく改善されたことを確認して、本発明による試験薬物は、2型糖尿病に明確な治療効果(血糖降下作用)と、糖尿による三多一無症状の改善効果があることを確認することができた。
【0142】
(健康補助食品組成物の剤形例1)ドリンク剤
実施例の糖尿病または糖尿病合併症の治療または予防用組成物100mg、液状オリゴ糖25gを混合した後、精製水200mlを加えて、80mlずつビニールパックに充填し、130℃で4〜5秒間滅菌して液剤を製造する。
【0143】
(薬学組成物の剤形例1)錠剤
実施例の糖尿病または糖尿病合併症の治療または予防用組成物100mg、玉蜀黍澱粉100mg、乳糖50mg、ステアリン酸マグネシウム2mgを混合した後、通常の錠剤の製造方法によって打錠して錠剤を製造する。
【0144】
(薬学組成物剤形例2)カプセル剤
実施例の糖尿病または糖尿病合併症の治療または予防用100mg、結晶性セルロース3mg、ラクトース14.8mg、マグネシウムステアレート0.2mgを混合した後、通常のカプセル剤の製造方法によって上記の成分を混合して、ゼラチンカプセルに充填してカプセル剤を製造する。
【図面の簡単な説明】
【0145】
【図1】本発明による抽出物の長期投与に対する膵臓組織の毒性有無を確認した結果である。(A:高容量群、B:中容量群、C:低容量群、D:対照群)
【図2】本発明による抽出物の長期投与に対する肝組織の毒性有無を確認した結果である。(A:高容量群、B:中容量群、C:低容量群、D:対照群)
【技術分野】
【0001】
本発明は、複合生薬抽出物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物に関し、より具体的には、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物に関する。
【背景技術】
【0002】
糖尿病は、21世紀最大の疾病とされており、現在、世界的に患者は1億7000万名おり、毎年320万名が糖尿病で命を失っている。国内でも糖尿病患者が過去20年間で12倍以上に増加して、2025年には、国民4人当たり1人が糖尿病患者になる可能性が高いため、国家的な次元の対策が切実に求められている。50代以上男性の30%、女性の20%以上が糖尿病に進行する可能性がある‘糖尿病前段階(pre-diabetes)’という調査結果は、糖尿病の深刻性を意味する。
【0003】
糖尿病は、遺伝的要因と共に、後天的要因である肥満、食生活、運動不足及びストレスなどにより影響を受ける疾病であって、膵臓細胞で分泌されるインシュリンの分泌障害及び作用不足により誘発された代謝障害と定義されており、ブドウ糖の過剰生産、体脂肪の分解及び蛋白質の浪費を伴い、グルカゴンの分泌が異常に亢進されて代謝上の混乱を引き起こす(Abrams, J.J., Ginsberg, H, et al., Metabolism of cholesterol and plasma triglyceride in nonketoticdiabetes mellitus. Diabetes, 31, pp903-910, 1982)。
【0004】
したがって、糖尿病は、生体内代謝調節機能に異常をきたし、高血糖症が現れて、尿中に糖が排泄されて、適切な治療と管理が成されないと循環器系などの合併症を伴う慢性的な代謝性疾患である(Mandrup-Poulsen, T., British Medical Journal., 316, pp1221-1225, 1998; Wilson, P. W. F. et al., Am. J. Med., 80, pp3-9, 1986)。
【0005】
糖尿病は、その発病原因及び症状の治療方法によって、大きくインシュリン依存型糖尿病(insulin dependent diabetes mellitus, IDDM)とインシュリン非依存型糖尿病(non-insulin dependent diabetes mellitus, NIDDM)とに分類できる。韓国の場合、糖尿病患者の95%以上がインシュリン非依存型糖尿病患者である。糖尿病は、それ自体が大きい疾患というよりは、長期間この疾患にかかっていることにより発病する合併症、例えば、糖尿病性神経症(neuropathy)、網膜症(retinopathy)、白内障(cataract)、腎臓病(nephropathy)などにより、患者たちが正常な生を営めないだけではなく、致命的となる可能性があるため、社会的に大きい問題とされている。
【0006】
糖尿病治療の最も重要な目標は、血糖値をなるべく正常数値に近く調節することであるが、空腹時血糖と共に食後血糖調節が、糖尿病症状の改善と合併症の予防及び治療において重要であり、治療方法として、薬物療法、食餌療法及び運動療法がある(Ref. Jenkins, D.J.A., Woever et.al., starchy food and glycemic index, Diabetes care, 11, pp149-159, 1988)。
【0007】
ところが、よく使用される薬物療法は、インシュリン及び化学的経口血糖降下剤などの化学物質を使用しており、薬物服用による副作用と患者の耐性が絶えず問題となっており、このため、天然物を利用した糖尿病治療剤の開発は、非常に重要な意味を有する。
【0008】
ゴーヤ(Momordica charantia L.)は、ウリ科(cucurbitaceae)の蔓植物であって、学名は、momordica charantiaであり、キュウリのように長いものを‘ニガウリ(bitter melon)’とも呼ぶ。原産地は、確実には知られていないが、インドを始めとした熱帯アジア地域と推定される。
【0009】
ゴーヤ成分の中、特に注目を浴びているものは、チャランチン(Charantin)と植物-インシュリン(plant-Insulin)であって、チャランチンは、インシュリンを分泌する膵臓の機能を活発にする脂溶性成分であり、植物-インシュリンは、体内でインシュリンと等しい作用をするペプチドの一種であって、ゴーヤの実と種に多く入っている(Ref. D. Sathishsekar and S. Subramanian, Biol. pharm. Bull. 28(6) pp978-983, 2005)。
【0010】
冬虫夏草(Cordyceps sinensis SACC.)は、冬虫夏草菌の子実体とそこに寄生する昆虫のコウモリガ幼虫死体との複合体である。冬虫夏草の成分としては、水分10.84%、脂肪8.4%、蛋白質25.32%、組織維18.53%、炭水化物28.90%、灰分4.10%を含有する。この他に、キナ酸(guinic acid)の異性体であるコルデーセプス酸(cordycepic acid)約7%を含有する。冬虫夏草は、強壮作用、免疫系に対する作用、血中コレステロール低下作用及びニコチンアミド(nicotinamide)とストレプトゾトシン(streptozotocin)で誘導した糖尿に対して血糖降下作用がある(Ref. Lo H.C., etal. Life sci., 74, pp2897-2908, 2004)。
【0011】
一方、上記のような生薬を、1種または2種以上を原料として、それぞれ配合を変えて得られた抽出物を有効成分とする糖尿病予防及び改善効果がある複合抽出物が明かされている。
【0012】
しかしながら、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参から構成された複合生薬抽出物に対する糖尿病予防及び治療効果に対しては、何の開示や教示もされていない。
【0013】
本発明は、血糖降下などの機能性効果があると既に知られているゴーヤ抽出物と冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参をもって、マウスの糖尿病誘発による体重変化、食餌効率、空腹時血糖及びグルコース負荷を実験し、生薬を単独使用するより、本発明の複合生薬抽出物を使用することが、抗糖尿効果にさらに優れていることを確認し、本発明を完成した。
【先行技術文献】
【非特許文献】
【0014】
【非特許文献1】Abrams, J.J., Ginsberg, H, et al., Metabolism of cholesterol and plasma triglyceride in nonketoticdiabetes mellitus. Diabetes, 31, pp903-910, 1982
【非特許文献2】Mandrup-Poulsen, T., British Medical Journal., 316, pp1221-1225, 1998; Wilson, P. W. F. et al., Am. J. Med., 80, pp3-9, 1986
【非特許文献3】Jenkins, D.J.A., Woever et.al., starchy food and glycemic index, Diabetes care, 11, pp149-159, 1988
【非特許文献4】D. Sathishsekarand S. Subramanian, Biol. pharm. Bull. 28(6) pp978-983, 2005
【非特許文献5】Lo H.C., etal. Life sci., 74, pp2897-2908, 2004
【発明の開示】
【発明が解決しようとする課題】
【0015】
本発明は、ゴーヤ、冬虫夏草、地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする血糖降下活性及び糖尿性合併症の抑制活性を有する糖尿病または糖尿病合併症の治療または予防用組成物を提供することを目的とする。
【課題を解決するための手段】
【0016】
本発明は、上記目的を達成するために、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物を提供する。
【0017】
以下、本発明を詳細に説明する。
【0018】
本発明において、血糖調節は、特に言及しない限り、血糖降下を意味する。
【0019】
本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比の熱水抽出物から構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物を提供する。
【0020】
本発明のゴーヤは、水溶性エタノール抽出物から減圧乾燥後、粉末として得られることを特徴とする。具体的な例として、ゴーヤの実と種を粉砕して粉末にした後、95%エタノールに48時間還流した後、抽出液を常温で減圧乾燥し、黄色粉末状活性成分を取得したものを使用する。
【0021】
本発明の冬虫夏草は、白きょう菌冬虫夏草を利用するもので、白きょう菌冬虫夏草の白きょう菌菌糸体及び子実体から熱水抽出(hot-water extract)法で抽出して精製した後、凍結乾燥して冬虫夏草抽出物を取得したものを使用する。
【0022】
前記ゴーヤエタノール抽出物、冬虫夏草抽出物の混合比率が4:1〜4であることが好ましく、本発明の血糖降下活性に重要な意味を有する。
【0023】
前記地骨皮(Lycii Radicis cortex)は、クコの根皮であって、成分としては、ベタイン、ダウコステリン、アスコルビン酸がある。また、灰分では、Si、K、Na、Ca、Mg、Fe、D、S、Znなどが確認されて、解熱作用、血圧降下及び血糖降下作用がある(Ref. Funagama S. etal, Fetrahedron Lett. 21, pp1355-1356, 1980)。
【0024】
前記桑白皮(Mori cortex Radicis)は、桑の木または桑の木科の根皮であって、成分としては、mulberrin(C25H26O6, 0.15%)、mulberrochromene(C25H24O6, 0.2%)、cyclomulberrin(C25H24O6, 0.02%)、cyclomulberrochromene(C25H22O6, 0.016%)などがあり、利尿、血圧降下作用、血糖降下作用がある(Ref. Hikino. H etal. plant Med. 159 pp 160(1985))。
【0025】
前記鬼剪羽(EuonymiLignum Suberalatum)は、ニシキギ科のニシキギの幹に矢のように生えたコルクを切って干したもので、成分としては、コルクのタンニン質と、根皮にはグッタペルカに似たゴム質がある。これは、癌細胞の侵入と転移過程に活性を抑制して、アロキサン(alloxan)で誘導した糖尿(rabbit)に対して血糖や尿糖を下げて、体重を増加させる作用がある(Ref. Kitanaka S. etal. chem.pharm.Bull44, pp615-617, 1996)。
【0026】
前記葛根(PuerariaeRadix)は、葛(豆科)の周皮を除去した根であって、成分としては、イソフラボン化合物である4,7−ジヒドロキシイソフラボン、アミドゼイン−7−グリコシドなどとクマリンを有しており、解熱鎮静作用、循環系に対する作用とブドウ糖の活性を増加させる血糖降下作用がある(Ref. Hsu H.H etal. planta Med. 68, pp999-1003 (2002))。
【0027】
前記黄精(polygonati Rhizoma)は、シベリアアマドコロ、ナルコユリまたは眞黄精(ユリ科)の根茎の外皮をむいて蒸したもので、コンバラリン、コンバラマリンなど、少ない量のアルカロイド、アスパラギン、マンニトを始めとしたMn、Cu、Fe、Mg、Zn、Moを含んでいる。滋養強壮作用とストレプトゾトシン(streptozotocin)糖尿を誘発させたマウスの血糖を下げる作用がある(Ref. Kato A. Miura T., planta Med. 60 pp201-203 (1994))。
【0028】
前記白朮(AtractylodisRhizoma Alba)は、オケラまたは唐白朮(キク科)の根茎または周皮を除去したものである。成分としては、根茎に約1.5%精油とカロリン、イヌリンゴム質、サポニン、クマリンなどを含んでおり、鎮胃、利尿、鎮静作用と血糖降下作用がある(Ref. Konno C. etal. planta Med. 51, pp102 (1985))
【0029】
前記麥門冬(Liriopis Tuber)は、ユリ科の根の膨大部である。乾いた塊根の約71%は、単糖(約10%)と分子量の少ない多糖類(粘液43%)である。また、β-シトステロール、ルスコゲニンなどを含有している。解熱鎮咳、抗炎症作用があり、水抽出物には、持続的な血糖降下作用がある(Ref. Lin YC etal. Am.J. Chin Med 31, pp354-579(2003))。
【0030】
前記山茱萸(CorniFructus)は、ミズキ科に属するサンシュユの果肉であって、種を除去したものである。没食子酸、リンゴ酸、酒石酸とモルロニシドとサポニン成分のロガニンが主成分であって、利尿、血圧降下、滋養強壮及び血糖降下作用がある(Ref. Jeng H etal. Am.J. Chin Med. 25, pp301-306 (1997))
【0031】
前記ウコギ科に属する高麗人参(GinseugRadix Alba)は、根であって、側根とコルク層を除去したものである。根には、配糖体、精油、アミノ酸、アルカロイド、炭水化物、樹脂、微量元素などが含まれ、滋養強壮作用、免疫増強作用、中枢神経系、心血管系作用、血糖降下作用、脂質代謝作用、抗癌作用、脳下垂体副腎皮質系などに作用をする(Ref. Yokozawa T. etal. Chem.pharm.Bull 33, pp869-872 (1985))。
【0032】
本発明の組成物の場合、ゴーヤエタノール抽出物、冬虫夏草抽出物及び、前記地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸及び高麗人参の熱水抽出物から成り、前記熱水抽出物が地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比で構成される、複合生薬抽出物を使用することを特徴とする。
【0033】
具体的な例として、地骨皮250g、桑白皮280g、鬼剪羽200g、葛根250g、黄精230g、白朮100g、麥門冬100g、山茱萸100g、高麗人参100gを細切した後、常温で20lの水に2時間漬けておいてから、80℃で3時間加熱し、2回目は、15lの水で1.5時間加熱して、3回目は、水15lで1時間加熱、このように3回繰り返して加熱して得た抽出液を、80℃で減圧濃縮して熱水抽出物を得たものを使用した。
【0034】
本発明による複合生薬抽出物は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び熱水抽出物から構成されて、これらの混合比率が4:1〜4:2〜5の重量比であることを特徴とする。
【0035】
本発明による前記メドハギ抽出物の発酵物は、メドハギ抽出物20〜40重量%にアスペルギルス・オリゼー(Aspergillus oryzae)菌株を接種して固体発酵させたことを特徴とし、また、前記メドハギ抽出物は、水、エタノールまたはこれらの混合溶媒で抽出後、エタノール沸騰点(78.3℃)以上に高温殺菌して得られることを特徴とする。
【0036】
前記メドハギは、根を含んだメドハギ植物全体をきれいに洗浄した後、細かく細切する。前記細切時、甘くて風味に優れた梨、リンゴ、柿、枸杞子からなる群から選択された1種以上の実または果物をさらに添加して製造することができ、前記実または果物は、味が苦くて辛いメドハギの嗜好性を増進させて、老若男女のだれもが飲用できるような飲料や茶を製造することができる。
【0037】
前記細切されたメドハギ、枸杞子の実やリンゴなどの果物を粉末形態に粉砕した後、エタノールを添加して静置及び熟成させる段階を経る。特にメドハギは、機能性ウェルビーイング漢方薬として利用されているが、エタノールで熟成させた後に抽出しないと、その効能が低下する問題がある。したがって、一般茶や飲料を製造する方法と異なって、メドハギの効能を増加させるために、エタノールで5日〜10日程度静置保管して、自然熟成させる過程が必要である。
【0038】
前記回収されたメドハギ抽出物は、熟成過程でエタノールが蒸発して一部消滅するが、まだエタノール成分が含まれてアルコール気が残っているため、飲料として不適な側面があり、その味が苦い短所がある。したがって、本発明者らは、このような問題点を解決するために、残存エタノールを除去するために、エタノール沸騰点(78.3℃)以上にて5時間程度高温殺菌して、前記残存アルコールを蒸留消滅させながら殺菌して、前記メドハギ抽出物を取得した。
【0039】
具体的な例として、メドハギを細かく細切した後、95%エタノールを添加して10日間静置及び熟成させる。前記熟成されたメドハギ抽出液を、ふるいまたは網紗の布で、固形化された不純物を分離ろ過し、メドハギ抽出液を回収した後、エタノール沸騰点(78.3℃)以上にて5時間高温殺菌して、残存アルコールを蒸留消滅させながら殺菌し、メドハギ抽出液を取得した。前記取得したメドハギ抽出物を20g量り取って均質に混合した後、種菌のコウジカビのアスペルギルス・オリゼー(Aspergillus oryzae)KFRI 00888(ATCC 22887)菌株0.1%を接種させた後、温度30〜32℃、湿度70〜85%の培養室で36〜42時間固体培養して、本発明による組成物を製造した。この際、培養を促進するためにビオチン(biotin)0.001%を添加して、メドハギ抽出物の発酵物を製造した。
【0040】
前記メドハギ抽出物は、発酵工程を通じて、原料内の有効成分が多様な有用性成分に転移すると考えられており、特に発酵を通じて多様な酵素成分が生成され、蛋白質の低分子化が起こり、また、ビタミンが合成され、機能性成分が活性型に転移されるなど、その有用性が極大化される。血中ブドウ糖の代謝が円滑に成されなくて発生する糖尿病は、固体発酵産物内の転移された活性成分が体内エネルギー代謝を促進させて、酵素及び細胞機能を活性化させることにより、糖尿病改善及び予防に役立てる。
【0041】
本発明における糖尿病とは、1型糖尿病または2型糖尿病であり、糖尿病合併症は、神経性合併症、糖尿病性網膜症、腎不全症、性機能障害、皮膚疾患、高血圧、動脈硬化症、脳卒中、心臓病、または壊疽である。即ち、本発明における糖尿病または糖尿病合併症の治療または予防用組成物は、糖尿病哺乳動物の膵臓からインシュリン分泌を増加させて、膵臓インシュリン含量を増加させて、空腹時、血糖を上昇させて、耐糖能(glucose tolerance)を改善させることを特徴とする。
【0042】
本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物を有効成分として含有する薬学組成物を提供する。
【0043】
本発明の抽出物を含む薬学組成物は、薬学的組成物の製造に通常に使用する適切な担体、賦形剤及び希釈剤をさらに含むことができる。前記担体、賦形剤及び希釈剤としては、ソルビトール、マンニトール、キシリトール、エリスリトール、マルチトール、澱粉、アカシアゴム、アルギネート、ゼラチン、カルシウムホスフェート、カルシウムシリケート、セルロース、メチルセルロース、微晶質セルロース、ポリビニールピロリドン、水、メチルヒドロキシベンゾエート、プロピルヒドロキシベンゾエート、タルク、マグネシウムステアレート及び鉱物油が挙げられる。
【0044】
本発明の抽出物を含む組成物は、それぞれ通常の方法により、散剤、顆粒剤、錠剤、カプセル剤、懸濁液、エマルジョン、シロップ及びエアロゾルなどの経口型剤形、外用剤、坐剤及び滅菌注射溶液の形態に剤形化して使用できる。
【0045】
詳細には、製剤化する場合は、普段使用する充填剤、増量剤、結合剤、湿潤剤、崩解剤、界面活性剤などの希釈剤または賦形剤を使用して調製できる。経口投与のための固形製剤には、錠剤、丸剤、散剤、顆粒剤及びカプセル剤などが含まれて、このような固形製剤は、前記抽出物またはこれの粉末に少なくとも一つ以上の賦形剤、例えば、澱粉、カルシウムカーボネート(calcium carbonate)及びゼラチンなどを混ぜて調製できる。また、単純な賦形剤の他に、マグネシウムステアレート及びタルクのような潤滑剤も使用できる。経口のための液状製剤としては、懸濁剤、内溶液剤、油剤及びシロップ剤などが該当するが、よく使用される単純希釈剤の水及びリキードパラフィンの他に様々な賦形剤、例えば、湿潤剤、甘味剤、芳香剤及び保存剤などが含まれる。非経口投与のための製剤には、滅菌された水溶液、非水性溶剤、懸濁剤、油剤、凍結乾燥製剤及び坐剤が含まれる。非水性溶剤、懸濁剤としては、プロピレングリコール(propylene glycol)、ポリエチレングリコール及びオリーブオイルのような植物性オイル及びエチルオレートのような注射可能なエステルなどが使用できる。坐剤の基剤としては、witepsol、マクロゴル、tween61、カカオジ、ラウリンジ及びグリセロゼラチンなどが使用できる。
【0046】
本発明の抽出物の好ましい投与量は、患者の状態及び体重、疾病の程度、薬物形態、投与経路及び期間によって異なるが、当業者により適宜選択できる。しかし、好ましい効果のために、本発明の抽出物は、0.01〜20g/kg、好ましくは0.01〜10g/kgの量を一日1回乃至数回に分けて投与できる。組成物において、本発明の抽出物または複合生薬粉末は、全体組成物の総重量に対して0.1〜50重量%の含量で配合できる。
【0047】
本発明の薬学組成物は、ラット、マウス、家畜、人間などの哺乳動物に多様な経路で投与できる。投与のあらゆる方式が予想できるが、例えば、経口、直腸または静脈、筋肉、皮下、子宮内硬膜及び脳血管内(Intracerebroventricular)注射により投与できる。
【0048】
また、本発明は、ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物を有効成分として含有する血糖降下用健康食品を提供する。
【0049】
前記抽出物を食品に使用する場合は、それをそのまま使用するか、他の食品または食品成分と共に使用することができ、通常の方法によって適宜使用できる。有効成分の混合量は、その使用目的(予防、健康または治療的処置)によって適宜決定できる。一般に、食品または飲料の製造時には、前記ゴーヤエタノール抽出物、冬虫夏草抽出物及び地骨皮、桑白皮、鬼剪羽、葛根、黄精、白朮、麥門冬、山茱萸、高麗人参を含む熱水抽出物で構成される複合生薬抽出物が、原料に対して10乃至90重量%、好ましくは、30乃至70重量%の量で添加される。
【0050】
しかしながら、健康増進、あるいは健康管理を目的とする長期間の摂取の場合は、前記範囲以下の量であってもよく、有効成分は、安全性面で何の問題もないため、前記範囲以上の量でも使用可能であることは確実である。前記食品の種類には特に制限がない。前記物質を添加できる食品の例としては、肉類、ソーセージ、チョコレート、キャンディー類、スナック類、お菓子類、ピザ、麺類、ガム類、アイスクリーム類を含む酪農製品、各種スープ、飲料、お茶、ドリンク剤、アルコール飲料及びビタミン複合剤などがあって、通常の意味での健康食品を全て含む。
【発明の効果】
【0051】
本発明による糖尿病または糖尿病合併症の治療または予防用組成物は、2型糖尿病モデル動物のインシュリン分泌を増加させて、インシュリン抵抗性を改善させて、強力な血糖降下活性及び糖尿病性合併症抑制活性を示し、また、天然植物性成分であって、安全性が確保されているため、糖尿病性疾患の予防または改善及び糖尿病合併症抑制に有用に使用できる。
【発明を実施するための最良の形態】
【0052】
本発明を詳細に記述する前に、特定具体例の変形例が行われ得るが、添付の特許請求の範囲の範疇内に含まれるため、本発明は、以下記述する本発明の特定な具体例に限定されないことを理解すべきである。また、使用された用語は、特定具体例を説明するためのものであって、限定するものではない。その代わり、本発明の範囲は、添付した特許請求の範囲により確立される。
【0053】
本明細書と添付の特許請求の範囲に使用する単数形態は、明確に指示しない限り、複数形態も含むことを理解すべきである。特に定義しない限り、本明細書に使用された全ての専門科学用語は、当業者が普遍的に理解しているものと同じ意味を有する。
【0054】
(製造例)
(1)ゴーヤ抽出物の製造
ゴーヤの実(1kg)と種(1kg)を、不純物を除去して、水で土と埃を洗った後、100乃至400メッシュの大きさの粒子に粉砕して、粉末にした。これを20lの95%エタノールにて48時間還流した後、抽出液を常温で減圧乾燥し、30gの黄色粉末状活性成分を取得した。
【0055】
(2)冬虫夏草抽出物の製造
白きょう菌冬虫夏草1kgを、不純物を除去した後、水で土と埃を洗って細切した後、水20lに常温で2時間漬けておいてから80℃で3時間加熱して、2回目は、水15lにて1.5時間加熱し、3回目は、水15lにて1時間加熱した。
【0056】
前記3回繰り返して加熱して得た抽出液を80℃で減圧濃縮して精製した後、凍結乾燥して、冬虫夏草抽出物10gを取得した。
【0057】
(3)熱水抽出物の製造
地骨皮250g、桑白皮280g、鬼剪羽200g、葛根250g、黄精230g、白朮100g、麥門冬100g、山茱萸100g、高麗人参100gから不純物を除去した後、水で土と埃を洗って細切した後、1610gを水20lに常温で2時間漬けておいてから、80℃で3時間加熱し、2回目は、15lの水にて1.5時間加熱して、3回目は、水15lにて1時間加熱した。
【0058】
前記3回繰り返して加熱して得た抽出液を、80℃で減圧濃縮して熱水抽出物250gを得た。
【0059】
(4)メドハギ発酵物の製造
メドハギ1kgをきれいに洗浄した後、細かく細切して、20lの95%エタノールを添加して10日間静置及び熟成させる。前記熟成されたメドハギ抽出液を、20〜50メッシュのふるいまたは網紗の布で、固形化された不純物を分離し、メドハギ抽出液を回収した後、エタノール沸騰点(78.3℃)以上にて5時間高温殺菌して、残存アルコールを蒸留消滅させながら殺菌し、メドハギ抽出液を取得した。
【0060】
前記取得したメドハギ抽出物を20g量り取り均質に混合した後、種菌のコウジカビのアスペルギルス・オリゼー(Aspergillus oryzae)KFRI 00888(ATCC 22887)菌株0.1%を接種させた後、温度30〜32℃、湿度70〜85%の培養室で36〜42時間固体培養して、本発明による組成物を製造した。この際、培養を促進するためにビオチン(biotin)0.001%を添加した。
【0061】
(実施例)糖尿病または糖尿病合併症の治療または予防用組成物の製造
前記方法により抽出したゴーヤエタノール抽出物30g、冬虫夏草抽出物10g、熱水抽出物250g及び発酵物10gを40℃以下で混合機で均質に混合して、300gの糖尿病または糖尿病合併症の治療または予防用組成物を製造した。
【0062】
(試験例1)急性毒性試験
1.試験系
(1)種及び系統:特定病原菌不在(SPF)マウス
(2)供給源:吉林獣医大学研究センター実験動物肉腫育種課
(3)試験系の選択理由
マウスは、毒性試験に適した実験動物であって、急性毒性試験に広く使用されている。本系統のマウスは、豊富な試験基礎資料が蓄積されていて、試験結果の解釈及び評価時、このような資料を利用することが可能である。
(4)週齢及び体重範囲
【0063】
【表1】

【0064】
(5)検疫及び馴化
動物入手後、外観を肉眼で検査し、7日間試験を施す動物室で馴化させた後、一般症状を観察して、健康な動物のみを試験に提供した。
【0065】
2.飼育環境
(1)環境条件
本試験は、温度23±30℃、相対湿度55±15%、照明時間12時間(午前8時〜午後8時)及び照度150〜300Luxに設定された韓国化学研究所安全性研究センター中動物洞の2号室で行われた。試験者らはみんな高圧蒸気滅菌(121℃、20分)された作業服、頭巾、マスク及び手袋などを着用して作業を行った。
【0066】
(2)飼育環境モニタリング
試験期間中、動物室の温湿度は、自動温湿度測定器により毎時間測定されて、照度などの環境条件は、定期的(3ヶ月に1回)に測定された。環境測定の結果、試験に影響を及ぼすと思われるような変動はなかった。
【0067】
(3)飼育箱、飼育密度及び飼育箱の識別試験期間の間、ステンレス製網飼育箱(220w×420L×200H mm)を利用して、馴化期間には4匹ずつ、投与と観察期間中は5匹ずつを収容した。試験期間中、飼育箱には、試験番号及び動物番号を記入した個体識別カード(媒体対照群:白色、T1:黄色)を付した。
【0068】
(4)飼料及び飲水
i)飼料の給与方法
飼料は、実験動物用固形飼料(吉林飼料公司)を放射線(2.0Mrad)滅菌して、自由に摂取させた。また、当該研究所実験動物室と供給会社で微生物及び汚染物質確認試験を施したところ、本試験に影響を及ぼすような要因は発見されなかった。
ii)飲水の給与方法及び汚染物質の確認
飲水は、上水道水を紫外線殺菌器で消毒した後、自由に摂取させた。飲水に対しては、給与前に予め一般水質検査を行って、検査の結果、試験に影響を及ぼすような要因は発見されなかった。
【0069】
3.投与量及び試験群の構成
(1)投与量設定
本試験物質は、植物抽出物製剤であって、予備試験の結果、限界容量である2000mg/kgの容量で死亡動物が観察されなかったため、限界容量試験の一環として最高容量を2000mg/kgにして、媒体のみを投与する媒体対照群をおいた。但し、中国衛生部の‘毒性試験条例’には、限界容量に対する基準がないため、日本厚生省の‘医薬品非臨床試験ガイドライン解説(1997)’を参考した。
(2)試験群の構成、投与濃度及び容量
【0070】
【表2】

【0071】
(3)群分離及び動物識別
動物の群分離は、以下のように行った。まず、馴化期間中、健康だと判定された動物の体重を測定した後、5g間隔で区分しておいた。そして、雌・雄それぞれの平均体重に近い個体を雌雄それぞれ10匹ずつを選択した。5g間隔で区分されて選択された雌雄それぞれ10匹を雌・雄各群に5匹ずつ均等に入るように、体重を利用した無作為法を利用して分配した。動物の個体識別は、皮毛色素マーキング法及び個体識別カード表示法で行った。
【0072】
4.試験物質の投与
(1)投与液の調製法
投与直前に、注射用生理食塩水を媒体として試験物質を2000mg/20ml/kgに調製した。媒体対照群(vehicle control)の動物には、媒体の0.5%CMCのみを投与した。
【0073】
(2)投与経路及び投与方法
投与前日一晩中絶食させた後、経口投与用ゾンデ(sonde)を装着した注射器を利用して、調製試験物質を強制経口投与した。
【0074】
(3)投与経路の選択理由
臨床予定経路として経口投与を選択した。
【0075】
(4)投与回数及び投与期間
投与当日午前に個体別に単回投与した。
【0076】
(5)投与液量の計算
投与当日の測定された体重を基準にして投与液量(20ml/kg)を計算した。
【0077】
5.観察及び検査項目
(1)一般症状及び死亡動物の観察
投与当日は、投与後1時間から6時間までは毎時間、投与翌日から14日までは毎日1回以上一般症状及び死亡動物の有無を観察した。
【0078】
(2)体重測定
試験に使用された全ての動物に対して、投与開始前と投与後1、3、7及び14日に体重を測定した。
【0079】
(3)剖検所見
全体生存動物をCO2ガスで麻酔して開腹して、放血致死させた後、肉眼で全ての内部臓器を観察した。
【0080】
6.統計学的方法
吉林獣医大学毒性研究センターのSOPによって統計処理を行った。
【0081】
7.結果
一般症状を観察した結果、全ての試験群では観察期間の間、何の異常症状も観察されず、雌・雄の全ての試験群において、投与後、1、3、7及び14日目、正常的な体重増加が観察された。
【0082】
また、死亡率及びLD50値(動物の半数致死量)を調べた結果、雌・雄の媒体対照群及び2000mg/kg投与群において、試験期間を通じて死亡動物は観察されず、雌・雄動物に対する本試験物質のLD50値は、それぞれ2000mg/kgを上回って、剖検結果も同様に、雌雄の全ての試験群において、肉眼で異常のある剖検所見は観察されなかった。
【0083】
本発明による糖尿病または糖尿病合併症の治療または予防用組成物に対する単回経口投与毒性試験を、雌雄SD系統のマウスを利用して行った結果、試験期間の間、死亡率、一般症状、体重変化及び剖検所見において、試験物質の投与に起因した変化は観察されなかった。
【0084】
(試験例2)長期毒性試験
1.試験薬
本発明による試料は、糖尿病または糖尿病合併症の治療または予防用組成物であって、粉末1gは、生薬10.6gに該当し、蒸留水を溶剤として必要な濃度に製造して使用した。
【0085】
2.実験動物
マウスは、体重が95〜102g、性別は、雌・雄同数の西安医科大学実験動物センター提供SD系マウス(批准番号07−005号)を利用した。
【0086】
分類は、SD系マウス160匹を無作為に4群に分類、各群40匹雌雄同数とした。高容量群は、試験薬3.0gを15.0%濃度の懸濁液にして(臨床容量の50倍)20ml/kgを経口投与して、中容量群は、試験薬1.5gを7.5%濃度の懸濁液にして、20ml/kgを経口投与して、低容量群は、試験薬0.3gを1.5%濃度の懸濁液にして、20ml/kgを経口投与した。対照群は、蒸留水のみを投与した。
【0087】
飼育は、空調施設、飼育温度18〜24℃、相対湿度45〜70%にして、 換風機を利用して換気をして、1日12時間ずつ照明を与えた。飼料は、西安医科大学実験動物センターで製造した標準固体飼料で飼育して、一般家庭用水で飲水を供給するが、性別を区分して飼育した。
【0088】
飼育箱当たり5匹を飼育して、3日毎に飼育箱を掃除して、上記条件に1週間適応させた後、実験を行った。
【0089】
マウスを試験動物に選定した理由は、この動物が毒性試験に適した実験動物であって、急性毒性試験に広く使用されており、特に、SD系は、試験基礎資料が十分確保され得るため、試験結果の解釈及び評価時、このような資料を利用することが可能であるためである。
【0090】
3.実験方法(投与方法)
毎日1回経口投与して、投与3ヶ月後、試験動物に対して関連検査を行う。
【0091】
4.試験項目
(1)一般的状況及び体重
試験に使用された全ての動物に対して神経状態、活動状態、分泌物、飲食習慣、排泄物、毛髪、皮膚などの状態を観察して、2週毎に体重を測定し、変化によって容量を調節した。
【0092】
(2)血液学的検査
試験に使用された全ての動物に対して、投与3ヶ月後、各群別に大腿動脈から採血して、血蛋白(Hb)、赤血球(RBC)、白血球(WBC)及び血小板(Pt)を検査した。
【0093】
(3)血液生化学的検査
試験に使用された全ての動物に対して、投与3ヶ月後、大腿動脈から採血して、血液内の各種物質の濃度(ALT, AST, ALP, TP, ALB, BUN, Crea, T-BIL, GLU)を検査した。
【0094】
(4)尿検査
試験に使用された全ての動物に対して、検査期間にマウス代謝ケースを使用して尿を収集し、色相、尿糖、尿蛋白、赤血球、白血球などを検査した。
【0095】
(5)心電図
試験に使用された全ての動物に対して、検査期間に標準心電図を検査した。
【0096】
(6)解剖(主要臓器係数)
試験に使用された全ての動物に対して、検査期間に心臓、肝、脾臓、肺、腎臓、胸腺、副腎、睾丸、卵巣など、九つの臓器を測定した。
【0097】
(7)組織病理学的検査
試験に使用された全ての動物に対して、心臓、肝、脾臓、肺、腎臓、胃頭部、十二指腸、空腸、結腸、膀胱、腸間膜リンパ節、睾丸、副睾丸、卵巣、子宮、胸骨(骨髄)、大脳、垂体、副腎、胸腺、甲状腺など、21個組織を検査した。
【0098】
5.結果
一般的な状態及び体重変化を観察した結果、投与13週後、一般的な状態は良好であり、毛髪、神経状態、活動状態、目、鼻の分泌物も正常であった。24時間の食餌習慣も正常であって、体重は段々増加したが、対照群と比較時、変化程度には有意差がなかった。
【0099】
血液学的影響及び血液生化学的影響を調べるために、投与3ヶ月後、及び回復後、それぞれペントバルビタール(pentobarbital)を皮下注射して麻酔させた後、大腿動脈から採血して、血液検査及び生化学的検査を行った。その結果、血液学的影響は、下記表1から確認できるように、投与群の検査数値に特別な変化がなく、対照群と比較し著しい差はなかった。
【0100】
【表3】

【0101】
血液生化学的影響は、アミノトランスフェラーゼ(aminotransferase)、肝機能、腎機能、血糖を調査した結果、下記表2の結果からも確認できるように、高容量投与群の血糖は著しく降下して、対照群に比べて著しい差を確認して、その他の項目別生化学的検査値は正常であって、対照群と統計学的差はなかった。
【0102】
【表4】

【0103】
尿に対する影響を調べた結果、下記表3の結果のように、各試験動物の尿状態は正常であって、尿糖、尿蛋白など、全て陰性であって、顕微鏡検査結果、赤血球と白血球も発見されなかった。これは、試験薬物がマウスの尿に対して何の影響もないことを確認したことである。
【0104】
【表5】

【0105】
試験薬物投与3ヶ月後、心電図に対する影響を調べた結果、試験動物の心拍率、S−波、T−波など、各波は、対照群と差がなかった。また、試験薬物の投与後、試験動物を解剖して、肉眼で心臓、肝、脾臓、肺、腎臓、胃、空腸、結腸、膀胱、胆嚢、副腎、胸腺、睾丸、子宮、脳、垂体、腹腔、胸腔などの主要臓器及び体腔の色相、形態、病巣などを観察した結果、臓器及び体腔の色相と形態には異常がなく、病巣も観察されなかった。
【0106】
前記解剖された試験動物の心臓、肝、脾臓、肺、腎臓、副腎、胸腺、睾丸、卵巣などを採取して、臓器の大きさによって重量を測った後、臓器係数を測定した(g/100g体重、またはmg/100g体重)。
【0107】
その結果、下記表4の結果からも確認できるように、各臓器係数は、全て正常範囲内に含まれることを確認した。
【0108】
【表6】

【0109】
組織病理学的検査のためにマウス臓器を採取して、その中、対照群及び高容量投与群は各6匹から、中容量群と低容量群も各6匹から採取した。
【0110】
臓器組織は、心臓、肝、脾臓、肺、腎臓、胃、十二指腸、空腸、結腸、腸間膜リンパ節、副腎、胸腺、甲状腺、睾丸、副睾丸、卵巣、子宮、胸骨(骨髄)、大脳、垂体と、さらに本試験薬物が血糖降下作用があるため、膵臓腺の組織を追加して、計21個組織を採取した。
【0111】
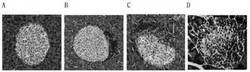
前記組織は、10%ホルムアルデヒド溶液で固定し、パラフィン切片を作って、HEで染色した後、顕微鏡で試験群と対照群を比較しながら観察した結果、図1及び図2からも確認できるように、試験群の臓器組織は、構造上明確であり、試験薬物投与時の充血、浮腫、変性、怪死、細胞浸潤などの病理学的変化は観察されなかった。
【0112】
したがって、本試験薬物は、病理学的影響が現れなかったことを確認して、試験薬物は、マウスに対する13週間の反復投与結果、特異な毒性反応はなく、安全な服用量は、体重で換算し、3.0g/kg体重/dayであることを確認することができた。
【0113】
(試験例3)血糖降下効果の測定
前記実施例で製造された糖尿病または糖尿病合併症の治療または予防用組成物(以下、試験薬物と称する)の血糖降下効果を測定するために、下記のような実験を行った。
【0114】
実験動物は、大韓実験動物センターから入手したマウスに、0.85%食塩水(Saline)に溶解させたストレプトゾトシン(Streptozotoxin;STZ, Sigma.co.,USA)を5日間反復投与して、人為的に糖尿病を誘発した後、前記試験薬物を投与して、血糖の変化を比較観察して、本発明の組成物の治療効果を調べた。
【0115】
1.実験方法
実験動物は、大韓実験動物センターから入手して、清浄室内で温度22±2℃、湿度55±5%、照明12L/12Dの条件下で管理した。
【0116】
試験動物は、計4群に分けて、具体的に、第1対照群は、ストレプトゾトシンを投与しなかった対照群として、第2対照群は、ストレプトゾトシンを60mg/kgを3乃至5回腹腔投与して、第3対照群は、ストレプトゾトシンと共に、偽薬として0.85%食塩水(Saline)を投与して、実験群は、前記第3対照群に投与した試料に、本発明による試験薬物を267mg/ml/kgを投与した。
【0117】
試験薬物は、投与当日から23日まで投与して、4日毎に血糖、尿糖、体重を測定した。
【0118】
血糖の測定は、マウスの尻尾静脈から採血して、血糖値を簡易血糖計(アキュトレンド、緑十字)で測定して、測定技術上、最高血中濃度500mg/dlまでのみ測定した。
【0119】
2.結果
本発明による糖尿病または糖尿病合併症の治療または予防用組成物(以下、試験薬物と称する)に対するマウス個体別血糖値を測定した結果、下記表5で確認した結果、血糖値300mg/dl以上を糖尿病マウスと判定する時、第2対照群では、試験の終わった10匹の中9匹が、第3対照群では、10匹の中8匹が糖尿病と判定されたが、試験薬物を投与した実験群では、ストレプトゾトシンマウスの糖尿病発病が抑制されたことを確認することができた。
【0120】
【表7】

【0121】
(試験例4)インシュリン非依存型糖尿病(NIDD)に対する効果
2型(インシュリン依存型)糖尿病に対する試験薬の効果を測定するために、2007年12月〜2008年9月の期間中、中国陝西省西安市と中国吉林省長春市一帯に居住する51名のインシュリン非依存型(NIDD)糖尿病患者に対して、本試験薬を投与して、臨床治療効果を観察した。
【0122】
1.対象者選定
1)選定患者基準(1998年WHO標準):血糖を測定して、下記(1)乃至(3)の条件中の一つのみに符合すれば、糖尿病患者と診断する。
(1)空腹時血糖≧7.8mmol/l(140mg/100ml)、または食後血糖≧11.1mmol/l(200mg/100ml)
(2)空腹時血糖は、7.8mmol/lより低いが、ブドウ糖75gでOGTTを行った時、血糖が≧11.1mmol/l(200mg/100ml)
(3)OGTT 1時間後血糖が≧11.1mmol/lであるか、または、OGTT2時間後血糖が≧11.1mmol/l、または空腹時血糖が≧7.8mmol/l
【0123】
2)試験対象者選定基準
前記1)項の基準に適合する者でも、次の各号の一つに該当すれば、除外する。
(1)試験薬の投薬前より血糖は正常より高いが、食餌療法や運動療法などで空腹時血糖が7.8mmol/l(140mg/100ml)より高いか、食後2時間後の血糖が11.1mmol/l(200mg/100ml)より低い場合
(2)食餌療法規定や薬物服用規定を守らなくて、薬効に影響を与える者
(3)合併症が深刻な者、あるいは他の病歴者
(4)糖尿病が最近1ヶ月内に発病した者または酸中毒及び感染者
(5)治療を中断した者、薬効が判断できないか、資料が不完全な者
(6)インシュリン依存型糖尿病(IDD)患者
(7)15歳以下であるか、妊婦あるいは産婦
【0124】
3)一般
【0125】
【表8】

【0126】
2.試験方法
1)一般的観察
(1)一般的な身体検査
(2)血、糖尿検査及び血、尿ルチン検査
(3)一部患者に対して心臓、腎臓、肝、血中脂質検査
【0127】
2)薬効観察
(1)病歴を詳細に確認して、食餌、運動、心理、糖尿病に対する知識などを確認する。
(2)空腹及び食後2時間後、血糖検査(投薬後10乃至15日毎に観察する)
(3)耐糖能(glucose tolerance)実験(OGTT)
(4)インシュリン分泌(insulin release)実験(INSRT)
(5)アミノフルクトース(Amino Fructose)測定
【0128】
薬物投与期間は、基本60日を単位とし、上記の(1)項の血糖検査及び(2)項の耐糖能(glucose tolerance)は必ず行って、その他の項目は、患者状況によって行うが、試験薬物の服用後、10乃至15日毎に空腹時血糖、尿糖、または食後2時間後、血糖と尿糖を測定した。
【0129】
薬物服用開始後、患者は、下記の基準により食餌療法を行って、投与60日後に、治療前の記録と比較して評価した。
【0130】
【表9】

【0131】
3)治療及び観察
(1)薬物投与方法:3回/日、4カプセル/回、食前30分乃至食後30分の間に経口で服用した。以後、血糖降下の程度によって容量を調節し、基本維持量は、3〜4カプセル/日として服用した。
(2)治療期間:60日を治療周期として、10乃至15日間隔で空腹時及び食後2時間後の血糖及び尿糖を検査した。
【0132】
4)薬効判定標準
中国糖尿病会議標準及び中和人民共和国衛生部標準によって、
(1)著しい効果
○治療後、症状は基本的になくなって、
○空腹時血糖<7.2mmol/l(130mg/100ml)、
○食後2時間後の血糖<8.3mmol/l(150mg/100ml)
○24時間内の尿糖量<10(g)
○血糖値及び24時間内の尿糖量が、治療前より30%降下した場合、著しい効果と判定した。
【0133】
(2)有効:
○治療後、一般的な症状は改善されて、
○空腹時血糖<8.3mmol/l(150mg/100ml)、
○食後2時間後の血糖<10mmol/l(180mg/100ml)
○24時間内の尿糖量<25(g)
○または、血糖量及び24時間内の尿糖量が、治療前より10%降下した場合、有効と判定した。
【0134】
(3)無効:
○治療後、症状は改善されず、血糖及び尿糖降下作用が上記の基準外である場合、無効と判定した。
【0135】
3.試験結果
投薬前・後の血糖変化を調べた結果を下記表6乃至7に示した。
【0136】
【表10】

【0137】
【表11】

【0138】
上記表6乃至7から確認できるように、治療後、血糖降下値(mmol/l)を見ると、3.1mmol/l以上降下した症例は、計51名の中49名であって、96.08%に血糖降下効果があることを確認した。
【0139】
【表12】

【0140】
【表13】

【0141】
また、被験者を対象に投薬前後の症状を確認した結果も、治療後、大部分は、治療前に比べて、典型的な症状である咽の渇き、食欲過多、過尿現象がなくなって、特に無力感などが著しく改善されたことを確認して、本発明による試験薬物は、2型糖尿病に明確な治療効果(血糖降下作用)と、糖尿による三多一無症状の改善効果があることを確認することができた。
【0142】
(健康補助食品組成物の剤形例1)ドリンク剤
実施例の糖尿病または糖尿病合併症の治療または予防用組成物100mg、液状オリゴ糖25gを混合した後、精製水200mlを加えて、80mlずつビニールパックに充填し、130℃で4〜5秒間滅菌して液剤を製造する。
【0143】
(薬学組成物の剤形例1)錠剤
実施例の糖尿病または糖尿病合併症の治療または予防用組成物100mg、玉蜀黍澱粉100mg、乳糖50mg、ステアリン酸マグネシウム2mgを混合した後、通常の錠剤の製造方法によって打錠して錠剤を製造する。
【0144】
(薬学組成物剤形例2)カプセル剤
実施例の糖尿病または糖尿病合併症の治療または予防用100mg、結晶性セルロース3mg、ラクトース14.8mg、マグネシウムステアレート0.2mgを混合した後、通常のカプセル剤の製造方法によって上記の成分を混合して、ゼラチンカプセルに充填してカプセル剤を製造する。
【図面の簡単な説明】
【0145】
【図1】本発明による抽出物の長期投与に対する膵臓組織の毒性有無を確認した結果である。(A:高容量群、B:中容量群、C:低容量群、D:対照群)
【図2】本発明による抽出物の長期投与に対する肝組織の毒性有無を確認した結果である。(A:高容量群、B:中容量群、C:低容量群、D:対照群)
【特許請求の範囲】
【請求項1】
ゴーヤエタノール抽出物、冬虫夏草抽出物、地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比の熱水抽出物から構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項2】
前記複合生薬抽出物が、ゴーヤエタノール抽出物、冬虫夏草抽出物及び熱水抽出物の混合比率が4:1〜4:2〜5の重量比であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項3】
前記複合生薬抽出物が、組成物の全重量に対して0.1〜50重量%含まれることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項4】
前記ゴーヤ抽出物が、エタノール抽出物を減圧乾燥後、粉末として得られることを特徴とする、請求項2に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項5】
前記メドハギ抽出物の発酵物が、メドハギ抽出物20〜40重量%にアスペルギルス・オリゼー(Aspergillus oryzae)菌株を接種して固体発酵させたことを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項6】
前記メドハギ抽出物の発酵物が、組成物の全重量に対して0.01〜20重量%含まれることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項7】
前記メドハギ抽出物が、水、エタノールまたはこれらの混合溶媒で抽出後、エタノール沸騰点(78.3℃)以上に高温殺菌して得られることを特徴とする、請求項5に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項8】
前記糖尿病が、1型糖尿病または2型糖尿病であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項9】
前記糖尿病合併症が、神経合併症、糖尿病網膜症、腎不全症、性機能障害、皮膚疾患、高血圧、動脈硬化症、脳卒中、心臓病または壊疽であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項1】
ゴーヤエタノール抽出物、冬虫夏草抽出物、地骨皮1:桑白皮1〜10:鬼剪羽1〜10:葛根1〜10:黄精1〜10:白朮1〜5:麥門冬1〜5:山茱萸1〜5:高麗人参1〜5の重量組成比の熱水抽出物から構成される複合生薬抽出物、及びメドハギ抽出物の発酵物を有効成分とする糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項2】
前記複合生薬抽出物が、ゴーヤエタノール抽出物、冬虫夏草抽出物及び熱水抽出物の混合比率が4:1〜4:2〜5の重量比であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項3】
前記複合生薬抽出物が、組成物の全重量に対して0.1〜50重量%含まれることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項4】
前記ゴーヤ抽出物が、エタノール抽出物を減圧乾燥後、粉末として得られることを特徴とする、請求項2に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項5】
前記メドハギ抽出物の発酵物が、メドハギ抽出物20〜40重量%にアスペルギルス・オリゼー(Aspergillus oryzae)菌株を接種して固体発酵させたことを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項6】
前記メドハギ抽出物の発酵物が、組成物の全重量に対して0.01〜20重量%含まれることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項7】
前記メドハギ抽出物が、水、エタノールまたはこれらの混合溶媒で抽出後、エタノール沸騰点(78.3℃)以上に高温殺菌して得られることを特徴とする、請求項5に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項8】
前記糖尿病が、1型糖尿病または2型糖尿病であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【請求項9】
前記糖尿病合併症が、神経合併症、糖尿病網膜症、腎不全症、性機能障害、皮膚疾患、高血圧、動脈硬化症、脳卒中、心臓病または壊疽であることを特徴とする、請求項1に記載の糖尿病または糖尿病合併症の治療または予防用組成物。
【図1】


【図2】




【図2】


【公開番号】特開2011−32272(P2011−32272A)
【公開日】平成23年2月17日(2011.2.17)
【国際特許分類】
【出願番号】特願2010−174274(P2010−174274)
【出願日】平成22年8月3日(2010.8.3)
【出願人】(510211701)ダイ ハン ファーム.シーオー.,エルティーディー. (1)
【氏名又は名称原語表記】DAI HAN PHARM.CO.,LTD.
【Fターム(参考)】
【公開日】平成23年2月17日(2011.2.17)
【国際特許分類】
【出願日】平成22年8月3日(2010.8.3)
【出願人】(510211701)ダイ ハン ファーム.シーオー.,エルティーディー. (1)
【氏名又は名称原語表記】DAI HAN PHARM.CO.,LTD.
【Fターム(参考)】
[ Back to top ]

