試験紙及びその製造方法
【課題】貯蔵性が高く、かつ検出感度の高い試験紙を作成する。
【解決手段】
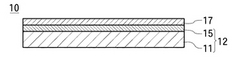
本発明の試験紙10は、検知剤が含有された担体15の表面が保護膜17で覆われており、担体15は保護膜17及び支持体11によって空気から遮断されているため、検知剤が酸化されやすい物質であっても、担体15が変色又は退色しない。従って、本発明の試験紙は貯蔵性に優れている。保護膜17は水溶性フィルムで構成されているので、検出物質の水溶液が保護膜17に接触すると、保護膜17が溶解又は膨潤して担体15に検出物質の水溶液が接触し、その水溶液に検出物質が含まれる場合は、担体15中の検知剤が検出物質と反応して変色する。
【解決手段】
本発明の試験紙10は、検知剤が含有された担体15の表面が保護膜17で覆われており、担体15は保護膜17及び支持体11によって空気から遮断されているため、検知剤が酸化されやすい物質であっても、担体15が変色又は退色しない。従って、本発明の試験紙は貯蔵性に優れている。保護膜17は水溶性フィルムで構成されているので、検出物質の水溶液が保護膜17に接触すると、保護膜17が溶解又は膨潤して担体15に検出物質の水溶液が接触し、その水溶液に検出物質が含まれる場合は、担体15中の検知剤が検出物質と反応して変色する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は特定の化学物質を検出する試験紙とその製造方法に関する。
【背景技術】
【0002】
従来より、特定の化学物質と反応して変色する検知剤は広く用いられている。
例えば、検知剤である塩化第二鉄(FeCl3)は通常は黄色を呈しているが、サリチル酸と反応して紫色に変色する。
【0003】
人間がアスピリンを摂取すると、アスピリンは体内で代謝され、その代謝物であるサリチル酸が尿や唾液に排出される。従って、患者の尿や唾液を含む試料を塩化第二鉄に接触させたときに、塩化第二鉄が変色するか否かで、患者がアスピリンを摂取したかどうかの判定をすることができる。
【0004】
従来のサリチル酸検出方法は、塩化第二鉄の水溶液を作成し、その水溶液に試料を入れて変色反応を観察していた。しかしながら、塩化第二鉄は酸化されやすく、塩化第二鉄の水溶液は短時間で変色してしまうので、検出試験の度に塩化第二鉄水溶液を作成する必要があり、工程が煩雑であった。
【非特許文献1】石澤不二雄 他6名、「サリチル酸検知管の開発」、中毒研究、日本中毒学会、2004年4月号(Vol.17/No2)、p.149−154
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は上記課題を解決するためになされたものであり、その目的は、長時間保存可能であって、かつ、簡易に検出物質を検知可能な試験紙を提供するものである。
【課題を解決するための手段】
【0006】
上記課題を解決するために請求項1記載の発明は、支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体には、検出物質と反応して変色する検知剤が含有され、前記保護膜は水溶性物質で構成され、前記検出物質が水に溶解した検出物質の水溶液を、前記保護膜に接触させると、前記保護膜が溶解し、前記検出物質の水溶液が前記担体と接触するように構成された試験紙である。
請求項2記載の発明は、請求項1記載の試験紙であって、前記保護膜はオブラートである試験紙である。
請求項3記載の発明は、請求項2記載の試験紙であって、前記保護膜の膜厚は10μm以上20μm以下である試験紙である。
請求項4記載の発明は、請求項1乃至請求項3のいずれか1項記載の試験紙であって、前記検知剤は塩化第二鉄であり、前記検出物質はサリチル酸である試験紙である。
請求項5記載の発明は、請求項1乃至請求項4のいずれか1項記載の試験紙であって、前記担体の構成物質は、セルロースを主成分とする試験紙である。
請求項6記載の発明は、請求項1乃至請求項5のいずれか1項記載の試験紙であって、前記支持体は樹脂フィルムである試験紙である。
請求項7記載の発明は、支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体に検知剤が含有された試験紙を製造する試験紙の製造方法であって、前記支持体上に配置された前記担体に、前記検知剤が溶解した検知剤溶液を含浸させた後、前記担体の表面に水溶性フィルムを配置し、前記水溶性フィルムを前記担体に含浸された前記検知剤溶液に接触させて、保護膜を形成する試験紙の製造方法である。
請求項8記載の発明は、請求項7記載の試験紙の製造方法であって、前記保護膜の形成は、前記担体の表面に前記水溶性フィルムを配置した後、前記水溶性フィルムを乾燥させる試験紙の製造方法である。
請求項9記載の発明は、サリチル酸と反応して変色する試験紙を製造する請求項7又は請求項8のいずれか1項記載の製造方法であって、前記検知剤として塩化第二鉄を用い、前記塩化第二鉄を、前記検知剤溶液100mlあたり、2.5gを越え、かつ10g未満の範囲で添加する試験紙の製造方法である。
【0007】
本発明は上記のように構成されており、担体に含有された検知剤の色あせを避けるために、担体表面に保護膜が配置され、担体が空気から遮断されている。
検査対象が尿等の水溶液(試料)であるため、保護膜の材質は試料に浸した時にすぐに溶解するような水溶性の材料である必要がある。従って、合成樹脂は不適当である。
【0008】
そのような水溶性の膜剤としてはオブラート、ゼラチン、水溶性でんぷんがあるが、保護膜の材料にオブラートを使うと、乾燥後長時間が経過しても黄色のまま色あせない(化学反応を起こさない)。またオブラートは膜厚が10μm以上20μm以下という超薄膜のため試料に浸すとすぐ溶け、その結果試験紙はサリチル酸と即座に反応できることから、シートを覆う膜としてはオブラートが最適である。
担体に検知剤溶液をしみこませてから、担体が乾かないうちにオブラートを貼付すると、担体の表面全体に均一にオブラートが付着する。
【0009】
また、支持体を用いず、例えばセルロースろ紙からなる担体に検知剤溶液をしみこませた後、その担体の両面をオブラートのような保護膜で覆うことも考えられるが、濡れた担体の両面にオブラートを貼付することは技術的に難しく、手間がかかる上、乾燥時にろ紙が波をうちオブラート膜が破れてしまうおそれがある。従って、本発明は担体を支持体上に配置することが好ましい。
【0010】
尚、オブラートを担体に貼付した直後は、オブラートが水分を吸収して糊状になっているため、余分な水分を除去するために全体を乾燥させるが、ドライヤー等で加熱して強制的に乾燥するとオブラートが急激に収縮して膜が破れ、表面全体が覆われなくなる可能性があるので、室温(5℃以上35℃以下)に放置して自然乾燥することが必要である。
【発明の効果】
【0011】
検知剤が含有された担体は両面が支持体と保護膜で覆われており、支持体と保護膜によって空気が遮断されるので、検知剤が酸化されやすい物質であっても、検知剤が変色しない。従って、試験紙の貯蔵性が高い。保護膜は水に溶解するので、保護膜の表面に水を含有する検出物質の水溶液を接触させるだけで、保護膜が溶解または膨潤し、検出物質の水溶液が担体に接触するようになる。従って、本発明の試験紙は検出試験の前に保護膜を取り外す必要がない。本発明の試験紙は、体液を遠心分離やろ過等の前処理をせずにそのまま試料液として用いることができる。
【発明を実施するための最良の形態】
【0012】
図1の符号10は本発明の試験紙の一例を示しており、この試験紙10は積層体12を有している。積層体12は、シート状の支持体11と、支持体11の表面に配置された担体層15とを有しており、積層体12の担体層15側の表面には保護膜17が配置されている。
【0013】
本発明に用いる保護膜17はオブラートのような水溶性フィルムで構成されている。オブラートの製造工程の一例について説明すると、先ず、馬鈴薯でんぷん等のでんぷんを水に分散させ、その分散液を煮沸し、攪拌すると、でんぷんが加熱されてアルファ化し、でんぷんが水を吸収して分散液が糊状になる。糊状の分散液をロールの側面に塗布して分散液の塗布膜を形成し、塗布層を押し伸ばしながら塗布層を加熱して分散液中の水分を乾燥除去し、膜厚が10μm以上20μm以下のでんぷんの薄膜を形成する。
【0014】
得られたでんぷんの薄膜を湿度が一定に保たれた室内に所定時間置き(エージング)、所定形状に切り出すと、アルファ化されたでんぷんの膜が得られる。このでんぷん膜は、でんぷんをアルファ化させなかった場合に比べて吸水性や、膨潤性や、水溶性が高い。従って、このでんぷん膜は水溶性フィルムの1種である。尚、でんぷんのアルファ化は加熱だけではなく、酸処理、酵素変性等の他の処理方法で、でんぷんをアルファ化させることもできる。
【0015】
次に、この試験紙の製造工程の一例について説明する。
図2(a)の符号12は本発明に用いる積層体の一例を示している。積層体12は例えばTLC(Thin Layer Chromatography,薄層クロマトグラフィー)用のセルロースシートで構成されており、このセルロースシートは、樹脂フィルムからなる支持体11と、支持体11表面に形成されたセルロース層とからなる担体13とで構成されている。
【0016】
検知剤である塩化第二鉄を水に溶解させて検知剤溶液を作成し、該検知剤溶液を積層体12の担体13側の表面に塗布する。
担体13を構成するセルロース層は吸水性を有するので、検知剤溶液は担体13表面から内部に浸透する。支持体11を構成する樹脂フィルムは吸水性を有さないので、検知剤溶液が担体13と支持体11との界面に到達しても、支持体11には吸収されず、検知剤溶液は担体13内部で保持される。
【0017】
図2(b)の符号15は検知剤溶液が内部に保持された状態の担体を示している。担体13を構成するセルロースと、支持体11を構成する樹脂(例えばポリエステル樹脂)は、検知剤である塩化第二鉄に対する反応性が低いので、塩化第二鉄は担体15中で変色せず、黄色のままである。従って、この担体15は黄色に呈色されている。
【0018】
次に、検知剤溶液が保持された担体15が乾かないうちに、上記水溶性フィルムを担体15表面に貼付すると、水溶性フィルムが担体15中に含浸された検知剤溶液と接触する。
【0019】
上述したように、オブラートのような水溶性フィルムは吸水性や膨潤性が非常に高く、水溶性フィルムが検知剤溶液と接触すると、水溶性フィルムの少なくとも表面部分が溶解して糊状となり、水溶性フィルムが担体15の表面に接着する。
【0020】
次に、水溶性フィルムが接着された状態の積層体を室温で自然乾燥し、水溶性フィルムから余分な水分を蒸発、除去する。水溶性フィルムから水分が蒸発する時には、水溶性フィルムは担体15に接着したまま反り返ろうとするが、担体15は樹脂フィルムからなる支持体11に保持されるので、積層体12は反り返らない。
【0021】
水溶性フィルムから余分な水分が除去されると、水溶性フィルムは、担体15の表面に接着されたまま糊状から固体状に戻り、担体15の表面に、固体状の水溶性フィルムからなる保護膜17が形成される。このとき、担体15内部に保持された水の一部も蒸発除去されるが、検知剤は除去されずに担体15内部に残る。
保護膜17が形成された状態の積層体12を所定形状(例えば、幅3cm長さ4cmの長方形形状)に切断すると、本発明の試験紙10が得られる。
【0022】
上述したように、担体15の内部から検知剤は除去されないので、担体15内部には検知剤が含有されており、担体15は検知剤の色(ここでは黄色)に呈色されている。
【0023】
上述した保護膜17と、支持体11を構成する樹脂フィルムは、それぞれ空気遮断性を有しており、従って担体15の表面と裏面は空気遮断性の膜で覆われ、担体15が空気にさらされない。従って、担体15に含有される検知剤が、塩化第二鉄のような酸化されやすい物質であっても、検知剤が酸化せず、担体15の色が変色せず、本発明の試験紙10は貯蔵性が高い。
【0024】
次に、試験紙10を使用例を説明すると、尿や唾液等の体液を採取し、その体液をそのまま検出物質の水溶液として用い、体液中に試験紙10を浸漬させるか、試験紙10の保護膜17側の表面に体液を滴下し、保護膜17に体液を接触させる。体液は水を主成分としており、上述したように保護膜17は吸水性が高いので、保護膜17は体液に溶解又は膨潤し、いずれの場合も担体15に体液が接触する。
【0025】
体液中にサリチル酸が含有されない場合は、担体15に含有される塩化第二鉄は変色せず、黄色のままである。従って、担体15は黄色に呈色されたままである。
【0026】
体液中にサリチル酸が含有される場合は、サリチル酸のフェノール性水酸基がFe3+と反応し、塩化第二鉄が緑色、青色あるいは紫色の錯塩となる。従って、担体15が黄色から、緑色、青色あるいは紫色に変色する。
【0027】
このように、本発明の試験紙10は、試料である体液を保護層17に接触させ、担体15の色が変わるかどうかを目視で観察するだけで、検出物質の水溶液である体液中に検出物質であるサリチル酸が含有されるかどうか調べることができる。
【実施例】
【0028】
<試験紙の特徴>
塩化第二鉄5gを蒸留水に溶解して100mlの検知剤溶液を作成した。この検知剤溶液を用いて、上記図2(a)、(b)に示した工程で試験紙10を作成し、サリチル酸の検出試験に用いる前の色を調べた。マンセルの標準色表に基づいた試験紙10の色相、明度、彩度を下記表1に示す。
【0029】
【表1】

【0030】
<塩化第二鉄の濃度>
塩化第二の鉄の添加量が異なる4種類の検知剤溶液を作成した。各検知剤溶液の塩化第二鉄の添加量を下記表2に記載する。
【0031】
【表2】

【0032】
上記表2中の添加量は、検知剤溶液100ml中に含有される塩化第二鉄の重量(g)を示している。これら4種類の検知剤溶液を用いて、図2(a)、(b)に示した工程で4種類の試験紙10を作成し、サリチル酸水溶液に試験紙10を浸漬して、担体15が変色するかどうかを目視で確認した。その観察結果を上記表1に記載した。
【0033】
上記表1から明らかなように、塩化第二鉄の添加量が2.5gの場合はサリチル酸の検出感度が低く、サリチル酸濃度が低い水溶液では担体15の色が変わらなかった。
【0034】
塩化第二鉄の添加量が5g以上であると、水溶液中のサリチル酸濃度が100mg/lと低くても担体15が変色したが、塩化第二鉄の添加量が10g以上になると、担体15の色そのものが塩化第二鉄で濃く着色されてしまった。
水溶液中のサリチル酸濃度が低く、担体15の変色程度が小さい場合には、担体15が濃く着色されていると、担体15が変色したかどうかの判定が困難になるの。
【0035】
従って、サリチル酸濃度の低い水溶液の検出に本発明の試験紙10を用いる場合には、検知剤溶液100ml当たりの塩化第二鉄の添加量を2.5gを超え、かつ10g未満の範囲にすればよいことがわかる。
【0036】
<担体の材質>
塩化第二鉄5gを蒸留水に溶解して100mlの検知剤溶液を作成した。この検知剤溶液を異なる種類の担体にしみこませて乾燥し、試験紙を作成した。担体の材質を下記表3に記載する。
【0037】
【表3】

【0038】
尚、上記表3中「TLCセルロールプレート+オブラート」以外のものは、担体表面に保護膜が形成されておらず、担体表面が露出している。
普通のろ紙(セルロースろ紙)に検知剤溶液をしみこませた試験紙は、作製直後は黄色で、サリチル酸との反応により紫色に着色し検査が可能であったが、作成後数時間で黄色が色あせ、使用不可能になった。
【0039】
石英ろ紙、ガラスウールろ紙を用いた場合は、作製直後にろ紙が褐色に変色し使用不可能であった。これは、石英ろ紙、ガラスウールろ紙にしみこんだ塩化第二鉄が化学変化を起こしたためである。また、ポリフロンろ紙は検知剤溶液が内部にしみこまず、試験紙を作成することが不可能であった。
【0040】
TLC用プラスチック蛍光剤入りシリカゲルシートを用いた場合も、石英ろ紙を用いた場合と同様に、作成後すぐに変色してしまった。
TLCプラスチックシリカゲルシートを用いた試験紙は、サリチル酸と反応し着色するが、検出物質の水溶液として尿を用いた場合、サリチル酸が含まれない場合であっても変色し、擬陽性反応を示すため不都合である。
【0041】
TLC用プラスチックセルロースシートを用いると、セルロースろ紙と同様検査が可能な試験紙が作製できるが、これも作製後数時間で色あせてしまう。これは担体15表面が露出しているので、空気の影響で塩化第二鉄が酸化されたためと考えられる。
【0042】
これに対し、TLC用プラスチックセルロースシートを用い、更に担体15の表面にオブラートを貼付して保護膜17を形成した本発明の試験紙10は、サリチル酸を検出可能であるだけではなく、作成後24時間以上経過しても担体15の色が退色しなかった。
【0043】
尚、TLCプラスチックシリカゲルシートは、樹脂フィルム表面にシリカゲル膜が形成されたものであり、TLC蛍光剤入りシリカゲルプレートは、樹脂フィルム表面に蛍光剤入りシリカゲル膜が形成されたものであり、TLCセルロースシートは、上記図2(a)に示した積層体12である。
【0044】
<保護膜の材料>
合成樹脂、ゼラチン、水溶性でんぷんを水に溶解させた塗布液を作成した。
図2(a)、(b)に示す工程で、積層体12の担体15に検知剤溶液をしみこませた後、上記塗布液を担体表面に塗布、乾燥して保護膜17を形成した。
【0045】
【表4】

【0046】
保護膜の材料のうち、合成樹脂は水に不溶であったため、保護膜を形成することができなかった。ゼラチンと水溶性でんぷんは水に可溶であるので保護膜17が形成できた。しかも、ゼラチンや水溶性でんぷんの保護膜17は検出物質の水溶液に溶解し、検出物質の水溶液中のサリチル酸を検出可能であった。
【0047】
しかしながら、ゼラチンや水溶性でんぷんを用いると、保護膜17にオブラートを用いた場合に比べて保護膜17の膜厚が厚く、保護膜17が乾燥するのに時間がかかるため、オブラートを用いた場合よりも試験紙の製造に要する時間が長くなる。また、ゼラチンや水溶性でんぷんを用いた保護膜17は、検出物質の水溶液に溶解するのに時間がかかるためサリチル酸の検出に時間がかかる。従って、水溶性でんぷんやゼラチンを保護膜17に用いることはできるが、それらの保護膜17はオブラートよりも劣る。
【0048】
次に、本発明の実施形態の他の例について説明するが、本発明はこれに限定されるものではない。
保護膜17は、担体15を空気から保護する機能を有し、かつ、サリチル酸の溶媒(水)と接触してすぐ溶ける膜であれば特に限定されるものではないが、現状ではオブラートが最も適している。
【0049】
支持体11の種類も特に限定されないが、支持体11が可撓性を有する樹脂フィルムである場合は、試験紙10全体が可撓性を有するので、試験紙10の使用の際の取り扱いが容易である。可撓性を有する樹脂フィルムは特に限定されるものではなく、例えば、ポリビニル樹脂、ポリイミド樹脂、ポリ塩化ビニル樹脂等の可撓性樹脂が1種類以上含有されたものを用いることができる。
【0050】
また、支持体11としては可撓性を有しない剛性材料で構成されたものを用いてもよい、そのような剛性材料としてはポリカーボネート樹脂、エポキシ樹脂等の剛性樹脂、ガラス、セラミック等の剛性無機材料がある。
【0051】
支持体11の色は特に限定されないが、支持体11の色は担体15の背景色となるため、担体15色の変化を確実に判定するためには、支持体11の色は白色か透明であることが好ましい。
【0052】
担体15は、検知剤を溶解する溶媒(例えば水)の吸収性を有し、検知剤と化学的に反応しないものであれば特に限定されるものではない。担体15は、更に体液中の検出物質以外の成分(例えばウロクロームやウロビリン等の尿素色素)で着色されないものが好ましく、現状ではセルロースが最も適している。
【0053】
検知剤を溶解する溶媒も水に限定されるものではなく、検知剤15が溶解可能なものであって、担体15の構成物質や、保護膜17の構成物質や、検知剤と化学的に反応しないものであれば、有機溶媒を用いることも可能である。
【0054】
塩化第二鉄は、サリチル酸以外にも、アセトアミノフェン、サリチル酸メチル、塩酸モルヒネ、フェノール、クレゾール、アスピリンと反応して青色〜紫色に変色し、更に、フェノチアジン誘導体(例えばクロルプロマジン)や、ピラゾロン誘導体(例えばアンチピリン)と反応して赤色及び赤茶色に変色するので、塩化第二鉄を検知剤に用いた場合には、本発明の試験紙10をこれらの物質の検出に用いることもできる。また、サリチル酸と反応し、変色する検知剤としては、塩化第二鉄以外にも、4−アミノアンチピリンを用いることができる。
【0055】
本発明の試験紙を用いて体液中の検出物質を検出する場合には、体液をそのまま検出物質の水溶液として用いてもよいし、体液を水等の溶媒で希釈したものを検出物質の水溶液として用いてもよい。
【産業上の利用可能性】
【0056】
本発明の試験紙はアスピリンの代謝物であるサリチル酸の定性試験を簡易に行うことが可能であり、試料の前処理も不溶なので、誤飲や自殺目的で患者がアスピリンを服用したかどうかの予備試験に用いることができる。
【図面の簡単な説明】
【0057】
【図1】本発明の試験紙の一例を示す断面図
【図2】(a)、(b):本発明の試験紙の製造工程の一例を示す断面図
【符号の説明】
【0058】
10……試験紙 11……支持体 13……担体 15……検知剤が含有された担体 17……保護膜
【技術分野】
【0001】
本発明は特定の化学物質を検出する試験紙とその製造方法に関する。
【背景技術】
【0002】
従来より、特定の化学物質と反応して変色する検知剤は広く用いられている。
例えば、検知剤である塩化第二鉄(FeCl3)は通常は黄色を呈しているが、サリチル酸と反応して紫色に変色する。
【0003】
人間がアスピリンを摂取すると、アスピリンは体内で代謝され、その代謝物であるサリチル酸が尿や唾液に排出される。従って、患者の尿や唾液を含む試料を塩化第二鉄に接触させたときに、塩化第二鉄が変色するか否かで、患者がアスピリンを摂取したかどうかの判定をすることができる。
【0004】
従来のサリチル酸検出方法は、塩化第二鉄の水溶液を作成し、その水溶液に試料を入れて変色反応を観察していた。しかしながら、塩化第二鉄は酸化されやすく、塩化第二鉄の水溶液は短時間で変色してしまうので、検出試験の度に塩化第二鉄水溶液を作成する必要があり、工程が煩雑であった。
【非特許文献1】石澤不二雄 他6名、「サリチル酸検知管の開発」、中毒研究、日本中毒学会、2004年4月号(Vol.17/No2)、p.149−154
【発明の開示】
【発明が解決しようとする課題】
【0005】
本発明は上記課題を解決するためになされたものであり、その目的は、長時間保存可能であって、かつ、簡易に検出物質を検知可能な試験紙を提供するものである。
【課題を解決するための手段】
【0006】
上記課題を解決するために請求項1記載の発明は、支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体には、検出物質と反応して変色する検知剤が含有され、前記保護膜は水溶性物質で構成され、前記検出物質が水に溶解した検出物質の水溶液を、前記保護膜に接触させると、前記保護膜が溶解し、前記検出物質の水溶液が前記担体と接触するように構成された試験紙である。
請求項2記載の発明は、請求項1記載の試験紙であって、前記保護膜はオブラートである試験紙である。
請求項3記載の発明は、請求項2記載の試験紙であって、前記保護膜の膜厚は10μm以上20μm以下である試験紙である。
請求項4記載の発明は、請求項1乃至請求項3のいずれか1項記載の試験紙であって、前記検知剤は塩化第二鉄であり、前記検出物質はサリチル酸である試験紙である。
請求項5記載の発明は、請求項1乃至請求項4のいずれか1項記載の試験紙であって、前記担体の構成物質は、セルロースを主成分とする試験紙である。
請求項6記載の発明は、請求項1乃至請求項5のいずれか1項記載の試験紙であって、前記支持体は樹脂フィルムである試験紙である。
請求項7記載の発明は、支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体に検知剤が含有された試験紙を製造する試験紙の製造方法であって、前記支持体上に配置された前記担体に、前記検知剤が溶解した検知剤溶液を含浸させた後、前記担体の表面に水溶性フィルムを配置し、前記水溶性フィルムを前記担体に含浸された前記検知剤溶液に接触させて、保護膜を形成する試験紙の製造方法である。
請求項8記載の発明は、請求項7記載の試験紙の製造方法であって、前記保護膜の形成は、前記担体の表面に前記水溶性フィルムを配置した後、前記水溶性フィルムを乾燥させる試験紙の製造方法である。
請求項9記載の発明は、サリチル酸と反応して変色する試験紙を製造する請求項7又は請求項8のいずれか1項記載の製造方法であって、前記検知剤として塩化第二鉄を用い、前記塩化第二鉄を、前記検知剤溶液100mlあたり、2.5gを越え、かつ10g未満の範囲で添加する試験紙の製造方法である。
【0007】
本発明は上記のように構成されており、担体に含有された検知剤の色あせを避けるために、担体表面に保護膜が配置され、担体が空気から遮断されている。
検査対象が尿等の水溶液(試料)であるため、保護膜の材質は試料に浸した時にすぐに溶解するような水溶性の材料である必要がある。従って、合成樹脂は不適当である。
【0008】
そのような水溶性の膜剤としてはオブラート、ゼラチン、水溶性でんぷんがあるが、保護膜の材料にオブラートを使うと、乾燥後長時間が経過しても黄色のまま色あせない(化学反応を起こさない)。またオブラートは膜厚が10μm以上20μm以下という超薄膜のため試料に浸すとすぐ溶け、その結果試験紙はサリチル酸と即座に反応できることから、シートを覆う膜としてはオブラートが最適である。
担体に検知剤溶液をしみこませてから、担体が乾かないうちにオブラートを貼付すると、担体の表面全体に均一にオブラートが付着する。
【0009】
また、支持体を用いず、例えばセルロースろ紙からなる担体に検知剤溶液をしみこませた後、その担体の両面をオブラートのような保護膜で覆うことも考えられるが、濡れた担体の両面にオブラートを貼付することは技術的に難しく、手間がかかる上、乾燥時にろ紙が波をうちオブラート膜が破れてしまうおそれがある。従って、本発明は担体を支持体上に配置することが好ましい。
【0010】
尚、オブラートを担体に貼付した直後は、オブラートが水分を吸収して糊状になっているため、余分な水分を除去するために全体を乾燥させるが、ドライヤー等で加熱して強制的に乾燥するとオブラートが急激に収縮して膜が破れ、表面全体が覆われなくなる可能性があるので、室温(5℃以上35℃以下)に放置して自然乾燥することが必要である。
【発明の効果】
【0011】
検知剤が含有された担体は両面が支持体と保護膜で覆われており、支持体と保護膜によって空気が遮断されるので、検知剤が酸化されやすい物質であっても、検知剤が変色しない。従って、試験紙の貯蔵性が高い。保護膜は水に溶解するので、保護膜の表面に水を含有する検出物質の水溶液を接触させるだけで、保護膜が溶解または膨潤し、検出物質の水溶液が担体に接触するようになる。従って、本発明の試験紙は検出試験の前に保護膜を取り外す必要がない。本発明の試験紙は、体液を遠心分離やろ過等の前処理をせずにそのまま試料液として用いることができる。
【発明を実施するための最良の形態】
【0012】
図1の符号10は本発明の試験紙の一例を示しており、この試験紙10は積層体12を有している。積層体12は、シート状の支持体11と、支持体11の表面に配置された担体層15とを有しており、積層体12の担体層15側の表面には保護膜17が配置されている。
【0013】
本発明に用いる保護膜17はオブラートのような水溶性フィルムで構成されている。オブラートの製造工程の一例について説明すると、先ず、馬鈴薯でんぷん等のでんぷんを水に分散させ、その分散液を煮沸し、攪拌すると、でんぷんが加熱されてアルファ化し、でんぷんが水を吸収して分散液が糊状になる。糊状の分散液をロールの側面に塗布して分散液の塗布膜を形成し、塗布層を押し伸ばしながら塗布層を加熱して分散液中の水分を乾燥除去し、膜厚が10μm以上20μm以下のでんぷんの薄膜を形成する。
【0014】
得られたでんぷんの薄膜を湿度が一定に保たれた室内に所定時間置き(エージング)、所定形状に切り出すと、アルファ化されたでんぷんの膜が得られる。このでんぷん膜は、でんぷんをアルファ化させなかった場合に比べて吸水性や、膨潤性や、水溶性が高い。従って、このでんぷん膜は水溶性フィルムの1種である。尚、でんぷんのアルファ化は加熱だけではなく、酸処理、酵素変性等の他の処理方法で、でんぷんをアルファ化させることもできる。
【0015】
次に、この試験紙の製造工程の一例について説明する。
図2(a)の符号12は本発明に用いる積層体の一例を示している。積層体12は例えばTLC(Thin Layer Chromatography,薄層クロマトグラフィー)用のセルロースシートで構成されており、このセルロースシートは、樹脂フィルムからなる支持体11と、支持体11表面に形成されたセルロース層とからなる担体13とで構成されている。
【0016】
検知剤である塩化第二鉄を水に溶解させて検知剤溶液を作成し、該検知剤溶液を積層体12の担体13側の表面に塗布する。
担体13を構成するセルロース層は吸水性を有するので、検知剤溶液は担体13表面から内部に浸透する。支持体11を構成する樹脂フィルムは吸水性を有さないので、検知剤溶液が担体13と支持体11との界面に到達しても、支持体11には吸収されず、検知剤溶液は担体13内部で保持される。
【0017】
図2(b)の符号15は検知剤溶液が内部に保持された状態の担体を示している。担体13を構成するセルロースと、支持体11を構成する樹脂(例えばポリエステル樹脂)は、検知剤である塩化第二鉄に対する反応性が低いので、塩化第二鉄は担体15中で変色せず、黄色のままである。従って、この担体15は黄色に呈色されている。
【0018】
次に、検知剤溶液が保持された担体15が乾かないうちに、上記水溶性フィルムを担体15表面に貼付すると、水溶性フィルムが担体15中に含浸された検知剤溶液と接触する。
【0019】
上述したように、オブラートのような水溶性フィルムは吸水性や膨潤性が非常に高く、水溶性フィルムが検知剤溶液と接触すると、水溶性フィルムの少なくとも表面部分が溶解して糊状となり、水溶性フィルムが担体15の表面に接着する。
【0020】
次に、水溶性フィルムが接着された状態の積層体を室温で自然乾燥し、水溶性フィルムから余分な水分を蒸発、除去する。水溶性フィルムから水分が蒸発する時には、水溶性フィルムは担体15に接着したまま反り返ろうとするが、担体15は樹脂フィルムからなる支持体11に保持されるので、積層体12は反り返らない。
【0021】
水溶性フィルムから余分な水分が除去されると、水溶性フィルムは、担体15の表面に接着されたまま糊状から固体状に戻り、担体15の表面に、固体状の水溶性フィルムからなる保護膜17が形成される。このとき、担体15内部に保持された水の一部も蒸発除去されるが、検知剤は除去されずに担体15内部に残る。
保護膜17が形成された状態の積層体12を所定形状(例えば、幅3cm長さ4cmの長方形形状)に切断すると、本発明の試験紙10が得られる。
【0022】
上述したように、担体15の内部から検知剤は除去されないので、担体15内部には検知剤が含有されており、担体15は検知剤の色(ここでは黄色)に呈色されている。
【0023】
上述した保護膜17と、支持体11を構成する樹脂フィルムは、それぞれ空気遮断性を有しており、従って担体15の表面と裏面は空気遮断性の膜で覆われ、担体15が空気にさらされない。従って、担体15に含有される検知剤が、塩化第二鉄のような酸化されやすい物質であっても、検知剤が酸化せず、担体15の色が変色せず、本発明の試験紙10は貯蔵性が高い。
【0024】
次に、試験紙10を使用例を説明すると、尿や唾液等の体液を採取し、その体液をそのまま検出物質の水溶液として用い、体液中に試験紙10を浸漬させるか、試験紙10の保護膜17側の表面に体液を滴下し、保護膜17に体液を接触させる。体液は水を主成分としており、上述したように保護膜17は吸水性が高いので、保護膜17は体液に溶解又は膨潤し、いずれの場合も担体15に体液が接触する。
【0025】
体液中にサリチル酸が含有されない場合は、担体15に含有される塩化第二鉄は変色せず、黄色のままである。従って、担体15は黄色に呈色されたままである。
【0026】
体液中にサリチル酸が含有される場合は、サリチル酸のフェノール性水酸基がFe3+と反応し、塩化第二鉄が緑色、青色あるいは紫色の錯塩となる。従って、担体15が黄色から、緑色、青色あるいは紫色に変色する。
【0027】
このように、本発明の試験紙10は、試料である体液を保護層17に接触させ、担体15の色が変わるかどうかを目視で観察するだけで、検出物質の水溶液である体液中に検出物質であるサリチル酸が含有されるかどうか調べることができる。
【実施例】
【0028】
<試験紙の特徴>
塩化第二鉄5gを蒸留水に溶解して100mlの検知剤溶液を作成した。この検知剤溶液を用いて、上記図2(a)、(b)に示した工程で試験紙10を作成し、サリチル酸の検出試験に用いる前の色を調べた。マンセルの標準色表に基づいた試験紙10の色相、明度、彩度を下記表1に示す。
【0029】
【表1】

【0030】
<塩化第二鉄の濃度>
塩化第二の鉄の添加量が異なる4種類の検知剤溶液を作成した。各検知剤溶液の塩化第二鉄の添加量を下記表2に記載する。
【0031】
【表2】

【0032】
上記表2中の添加量は、検知剤溶液100ml中に含有される塩化第二鉄の重量(g)を示している。これら4種類の検知剤溶液を用いて、図2(a)、(b)に示した工程で4種類の試験紙10を作成し、サリチル酸水溶液に試験紙10を浸漬して、担体15が変色するかどうかを目視で確認した。その観察結果を上記表1に記載した。
【0033】
上記表1から明らかなように、塩化第二鉄の添加量が2.5gの場合はサリチル酸の検出感度が低く、サリチル酸濃度が低い水溶液では担体15の色が変わらなかった。
【0034】
塩化第二鉄の添加量が5g以上であると、水溶液中のサリチル酸濃度が100mg/lと低くても担体15が変色したが、塩化第二鉄の添加量が10g以上になると、担体15の色そのものが塩化第二鉄で濃く着色されてしまった。
水溶液中のサリチル酸濃度が低く、担体15の変色程度が小さい場合には、担体15が濃く着色されていると、担体15が変色したかどうかの判定が困難になるの。
【0035】
従って、サリチル酸濃度の低い水溶液の検出に本発明の試験紙10を用いる場合には、検知剤溶液100ml当たりの塩化第二鉄の添加量を2.5gを超え、かつ10g未満の範囲にすればよいことがわかる。
【0036】
<担体の材質>
塩化第二鉄5gを蒸留水に溶解して100mlの検知剤溶液を作成した。この検知剤溶液を異なる種類の担体にしみこませて乾燥し、試験紙を作成した。担体の材質を下記表3に記載する。
【0037】
【表3】

【0038】
尚、上記表3中「TLCセルロールプレート+オブラート」以外のものは、担体表面に保護膜が形成されておらず、担体表面が露出している。
普通のろ紙(セルロースろ紙)に検知剤溶液をしみこませた試験紙は、作製直後は黄色で、サリチル酸との反応により紫色に着色し検査が可能であったが、作成後数時間で黄色が色あせ、使用不可能になった。
【0039】
石英ろ紙、ガラスウールろ紙を用いた場合は、作製直後にろ紙が褐色に変色し使用不可能であった。これは、石英ろ紙、ガラスウールろ紙にしみこんだ塩化第二鉄が化学変化を起こしたためである。また、ポリフロンろ紙は検知剤溶液が内部にしみこまず、試験紙を作成することが不可能であった。
【0040】
TLC用プラスチック蛍光剤入りシリカゲルシートを用いた場合も、石英ろ紙を用いた場合と同様に、作成後すぐに変色してしまった。
TLCプラスチックシリカゲルシートを用いた試験紙は、サリチル酸と反応し着色するが、検出物質の水溶液として尿を用いた場合、サリチル酸が含まれない場合であっても変色し、擬陽性反応を示すため不都合である。
【0041】
TLC用プラスチックセルロースシートを用いると、セルロースろ紙と同様検査が可能な試験紙が作製できるが、これも作製後数時間で色あせてしまう。これは担体15表面が露出しているので、空気の影響で塩化第二鉄が酸化されたためと考えられる。
【0042】
これに対し、TLC用プラスチックセルロースシートを用い、更に担体15の表面にオブラートを貼付して保護膜17を形成した本発明の試験紙10は、サリチル酸を検出可能であるだけではなく、作成後24時間以上経過しても担体15の色が退色しなかった。
【0043】
尚、TLCプラスチックシリカゲルシートは、樹脂フィルム表面にシリカゲル膜が形成されたものであり、TLC蛍光剤入りシリカゲルプレートは、樹脂フィルム表面に蛍光剤入りシリカゲル膜が形成されたものであり、TLCセルロースシートは、上記図2(a)に示した積層体12である。
【0044】
<保護膜の材料>
合成樹脂、ゼラチン、水溶性でんぷんを水に溶解させた塗布液を作成した。
図2(a)、(b)に示す工程で、積層体12の担体15に検知剤溶液をしみこませた後、上記塗布液を担体表面に塗布、乾燥して保護膜17を形成した。
【0045】
【表4】

【0046】
保護膜の材料のうち、合成樹脂は水に不溶であったため、保護膜を形成することができなかった。ゼラチンと水溶性でんぷんは水に可溶であるので保護膜17が形成できた。しかも、ゼラチンや水溶性でんぷんの保護膜17は検出物質の水溶液に溶解し、検出物質の水溶液中のサリチル酸を検出可能であった。
【0047】
しかしながら、ゼラチンや水溶性でんぷんを用いると、保護膜17にオブラートを用いた場合に比べて保護膜17の膜厚が厚く、保護膜17が乾燥するのに時間がかかるため、オブラートを用いた場合よりも試験紙の製造に要する時間が長くなる。また、ゼラチンや水溶性でんぷんを用いた保護膜17は、検出物質の水溶液に溶解するのに時間がかかるためサリチル酸の検出に時間がかかる。従って、水溶性でんぷんやゼラチンを保護膜17に用いることはできるが、それらの保護膜17はオブラートよりも劣る。
【0048】
次に、本発明の実施形態の他の例について説明するが、本発明はこれに限定されるものではない。
保護膜17は、担体15を空気から保護する機能を有し、かつ、サリチル酸の溶媒(水)と接触してすぐ溶ける膜であれば特に限定されるものではないが、現状ではオブラートが最も適している。
【0049】
支持体11の種類も特に限定されないが、支持体11が可撓性を有する樹脂フィルムである場合は、試験紙10全体が可撓性を有するので、試験紙10の使用の際の取り扱いが容易である。可撓性を有する樹脂フィルムは特に限定されるものではなく、例えば、ポリビニル樹脂、ポリイミド樹脂、ポリ塩化ビニル樹脂等の可撓性樹脂が1種類以上含有されたものを用いることができる。
【0050】
また、支持体11としては可撓性を有しない剛性材料で構成されたものを用いてもよい、そのような剛性材料としてはポリカーボネート樹脂、エポキシ樹脂等の剛性樹脂、ガラス、セラミック等の剛性無機材料がある。
【0051】
支持体11の色は特に限定されないが、支持体11の色は担体15の背景色となるため、担体15色の変化を確実に判定するためには、支持体11の色は白色か透明であることが好ましい。
【0052】
担体15は、検知剤を溶解する溶媒(例えば水)の吸収性を有し、検知剤と化学的に反応しないものであれば特に限定されるものではない。担体15は、更に体液中の検出物質以外の成分(例えばウロクロームやウロビリン等の尿素色素)で着色されないものが好ましく、現状ではセルロースが最も適している。
【0053】
検知剤を溶解する溶媒も水に限定されるものではなく、検知剤15が溶解可能なものであって、担体15の構成物質や、保護膜17の構成物質や、検知剤と化学的に反応しないものであれば、有機溶媒を用いることも可能である。
【0054】
塩化第二鉄は、サリチル酸以外にも、アセトアミノフェン、サリチル酸メチル、塩酸モルヒネ、フェノール、クレゾール、アスピリンと反応して青色〜紫色に変色し、更に、フェノチアジン誘導体(例えばクロルプロマジン)や、ピラゾロン誘導体(例えばアンチピリン)と反応して赤色及び赤茶色に変色するので、塩化第二鉄を検知剤に用いた場合には、本発明の試験紙10をこれらの物質の検出に用いることもできる。また、サリチル酸と反応し、変色する検知剤としては、塩化第二鉄以外にも、4−アミノアンチピリンを用いることができる。
【0055】
本発明の試験紙を用いて体液中の検出物質を検出する場合には、体液をそのまま検出物質の水溶液として用いてもよいし、体液を水等の溶媒で希釈したものを検出物質の水溶液として用いてもよい。
【産業上の利用可能性】
【0056】
本発明の試験紙はアスピリンの代謝物であるサリチル酸の定性試験を簡易に行うことが可能であり、試料の前処理も不溶なので、誤飲や自殺目的で患者がアスピリンを服用したかどうかの予備試験に用いることができる。
【図面の簡単な説明】
【0057】
【図1】本発明の試験紙の一例を示す断面図
【図2】(a)、(b):本発明の試験紙の製造工程の一例を示す断面図
【符号の説明】
【0058】
10……試験紙 11……支持体 13……担体 15……検知剤が含有された担体 17……保護膜
【特許請求の範囲】
【請求項1】
支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、
前記担体には、検出物質と反応して変色する検知剤が含有され、
前記保護膜は水溶性物質で構成され、
前記検出物質が水に溶解した検出物質の水溶液を、前記保護膜に接触させると、前記保護膜が溶解し、前記検出物質の水溶液が前記担体と接触するように構成された試験紙。
【請求項2】
前記保護膜はオブラートである請求項1記載の試験紙。
【請求項3】
前記保護膜の膜厚は10μm以上20μm以下である請求項2記載の試験紙。
【請求項4】
前記検知剤は塩化第二鉄であり、前記検出物質はサリチル酸である請求項1乃至請求項3のいずれか1項記載の試験紙。
【請求項5】
前記担体の構成物質は、セルロースを主成分とする請求項1乃至請求項4のいずれか1項記載の試験紙。
【請求項6】
前記支持体は樹脂フィルムである請求項1乃至請求項5のいずれか1項記載の試験紙。
【請求項7】
支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体に検知剤が含有された試験紙を製造する試験紙の製造方法であって、
前記支持体上に配置された前記担体に、前記検知剤が溶解した検知剤溶液を含浸させた後、
前記担体の表面に水溶性フィルムを配置し、前記水溶性フィルムを前記担体に含浸された前記検知剤溶液に接触させて、保護膜を形成する試験紙の製造方法。
【請求項8】
前記保護膜の形成は、前記担体の表面に前記水溶性フィルムを配置した後、前記水溶性フィルムを乾燥させる請求項7記載の試験紙の製造方法。
【請求項9】
サリチル酸と反応して変色する試験紙を製造する請求項7又は請求項8のいずれか1項記載の製造方法であって、
前記検知剤として塩化第二鉄を用い、
前記塩化第二鉄を、前記検知剤溶液100mlあたり、2.5gを越え、かつ10g未満の範囲で添加する試験紙の製造方法。
【請求項1】
支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、
前記担体には、検出物質と反応して変色する検知剤が含有され、
前記保護膜は水溶性物質で構成され、
前記検出物質が水に溶解した検出物質の水溶液を、前記保護膜に接触させると、前記保護膜が溶解し、前記検出物質の水溶液が前記担体と接触するように構成された試験紙。
【請求項2】
前記保護膜はオブラートである請求項1記載の試験紙。
【請求項3】
前記保護膜の膜厚は10μm以上20μm以下である請求項2記載の試験紙。
【請求項4】
前記検知剤は塩化第二鉄であり、前記検出物質はサリチル酸である請求項1乃至請求項3のいずれか1項記載の試験紙。
【請求項5】
前記担体の構成物質は、セルロースを主成分とする請求項1乃至請求項4のいずれか1項記載の試験紙。
【請求項6】
前記支持体は樹脂フィルムである請求項1乃至請求項5のいずれか1項記載の試験紙。
【請求項7】
支持体と、前記支持体上に配置された担体と、前記担体上に配置された保護膜とを有し、前記担体に検知剤が含有された試験紙を製造する試験紙の製造方法であって、
前記支持体上に配置された前記担体に、前記検知剤が溶解した検知剤溶液を含浸させた後、
前記担体の表面に水溶性フィルムを配置し、前記水溶性フィルムを前記担体に含浸された前記検知剤溶液に接触させて、保護膜を形成する試験紙の製造方法。
【請求項8】
前記保護膜の形成は、前記担体の表面に前記水溶性フィルムを配置した後、前記水溶性フィルムを乾燥させる請求項7記載の試験紙の製造方法。
【請求項9】
サリチル酸と反応して変色する試験紙を製造する請求項7又は請求項8のいずれか1項記載の製造方法であって、
前記検知剤として塩化第二鉄を用い、
前記塩化第二鉄を、前記検知剤溶液100mlあたり、2.5gを越え、かつ10g未満の範囲で添加する試験紙の製造方法。
【図1】


【図2】




【図2】


【公開番号】特開2006−300739(P2006−300739A)
【公開日】平成18年11月2日(2006.11.2)
【国際特許分類】
【出願番号】特願2005−123095(P2005−123095)
【出願日】平成17年4月21日(2005.4.21)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成17年3月20日 日本法医学会発行の「日本法医学雑誌 第59巻・第1号」に発表
【出願人】(390010364)光明理化学工業株式会社 (18)
【Fターム(参考)】
【公開日】平成18年11月2日(2006.11.2)
【国際特許分類】
【出願日】平成17年4月21日(2005.4.21)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成17年3月20日 日本法医学会発行の「日本法医学雑誌 第59巻・第1号」に発表
【出願人】(390010364)光明理化学工業株式会社 (18)
【Fターム(参考)】
[ Back to top ]

