質量分析スペクトル分析方法
【課題】
生体試料のクロマトグラフィー質量分析では、類似の条件下で測定を行ったとしても、多成分の混合による分離の不足や測定間での強度およびクロマトグラフィーでの保持時間のばらつき、または前処理等で生じる試料自体のばらつきなどにより、各成分の対応付けが困難となる。
【解決手段】
本発明では、複数のクロマトグラフィー質量分析データ間の成分対応付けを行うために、対応付けを行う成分のMSスペクトルのイオン情報(質量,価数,強度,同位体ピーク分布,保持時間)と対応付けを行う成分と類似の質量,時間帯に検出された別成分のMSスペクトル情報も利用する。別成分の情報としては、質量,価数,強度,同位体ピーク分布,保持時間などがあり、一致の程度をスコアとして評価する。対応付けを行う成分だけでなく、類似の時間帯に検出された成分情報もあわせて判定に利用することで、対応付けの精度を向上させる。
生体試料のクロマトグラフィー質量分析では、類似の条件下で測定を行ったとしても、多成分の混合による分離の不足や測定間での強度およびクロマトグラフィーでの保持時間のばらつき、または前処理等で生じる試料自体のばらつきなどにより、各成分の対応付けが困難となる。
【解決手段】
本発明では、複数のクロマトグラフィー質量分析データ間の成分対応付けを行うために、対応付けを行う成分のMSスペクトルのイオン情報(質量,価数,強度,同位体ピーク分布,保持時間)と対応付けを行う成分と類似の質量,時間帯に検出された別成分のMSスペクトル情報も利用する。別成分の情報としては、質量,価数,強度,同位体ピーク分布,保持時間などがあり、一致の程度をスコアとして評価する。対応付けを行う成分だけでなく、類似の時間帯に検出された成分情報もあわせて判定に利用することで、対応付けの精度を向上させる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、質量分析データ解析方法および質量分析システムに関するものである。
【背景技術】
【0002】
質量分析法には、成分をイオン化してそのまま分析する方法(MS分析法)と、特定成分のイオン(プリカーサーイオン)を質量選択し、それを解離させて生成した解離イオンを質量分析するタンデム質量分析法がある。タンデム質量分析法には、解離イオンの中から、特定の質量対電荷比を持つイオン(プリカーサーイオン)を選択し、更に、そのプリカーサーイオンを解離し、その際生成した解離イオンの質量分析を行うといったように、解離・質量分析を多段に行う機能(n段目の計測:以降MSn)がある。尚、プリカーサーイオンは親イオンとも称される。MSnを実施することにより、プリカーサーイオンの断片情報から成分の構造が解析でき、断片情報を用いたタンパク質データベース検索や断片間の質量から構造を解読するde novo sequencing法などから、成分が何であるかを特定できる。
【0003】
複数の成分が多数混在しているような試料の測定には、クロマトグラフィーと質量分析計とを組み合わせたシステムが用いられる。このシステムでは、測定する物質は、クロマトグラフィーによって物質のカラムへの吸着度の違い等から時間で分離され、質量分析計によって質量で分離される。糖鎖の異性体や1つのアミノ酸と同質量を持つ2つのアミノ酸の組み合わせなどを持つ化合物の場合、質量的に分離することは困難であるが、それらの物質は物質の化学的性質,物理的性質によりクロマトグラフィーによってほとんどが時間的に分離される。クロマトグラフィーを用いた場合では、同じ試料を同じ分析条件下で測定しても、数分のイオンの検出時間誤差が現われるのが通常である。また、生体試料のように、非常に多くの成分が混在したクルードな試料においては、検出時間の一様なずれだけではなく、同一質量の成分間の検出順番の入れ替わりが発生することがある。
【0004】
測定した質量分析データは分析終了後、データ解析が実施される。複数の質量分析データからの同一成分抽出には様々な方法が用いられている。
【0005】
WO05/050188(特許文献1)には、質量分析の同一成分の抽出方法として、タンデム質量分析データを解析した結果であるMSnスペクトルを利用し同一成分を抽出する方法が開示されている。複数の試料に対して、それぞれタンデム質量分析を実施する。それぞれの測定で得られたタンデム質量分析データに対して、データベース検索を実施する。データベース検索の結果、得られた成分に対して、各試料間で同一なものを抽出する。本方法では、データベース検索の結果から同一成分を抜き出しているため、一致判定の精度は高い。しかし、タンデム質量分析を実施した成分に対してのみを、抽出の対象としているため、タンデム質量分析されていない成分については、一致判定が出来ない。生体試料などの成分が数万〜数十万含まれるクルードな試料に対しては、現状の質量分析装置の性能では、1度の測定で検出される全ての成分に対してタンデム質量分析を行うことは困難である。更に、各測定間で、成分の強度や保持時間がばらつくため、ある測定ではタンデム質量分析されていた成分が、次の測定では、タンデム質量分析されていないといったことが起こりうる。このような場合、一方にしか構造情報が無いため、対応付けの精度は大きく低下する。また、成分が微量にしか含まれない場合には、タンデム質量分析を行っても構造を特定できない、または誤った特定をする場合があり、このような場合にも、正しい一致判定が出来ない。
【0006】
また、同一成分の抽出は、通常、各成分の定量分析を目的として行われ、成分の定量にはMSスペクトルの強度が用いられる。このため、定量精度を上げるには、各成分に対してより多くのMSスペクトルを取得する必要がある。一方、タンデム質量分析を行うことでMSスペクトルの取得数が減少するので、結果的に定量精度は低下する。
【0007】
このため、タンデム質量分析を行わず、MSスペクトルのみから同一成分を抽出する方法も検討されている。
【0008】
【特許文献1】WO05/050188
【発明の開示】
【発明が解決しようとする課題】
【0009】
生体試料のクロマトグラフィー質量分析では、同一装置、同一のクロマトグラフィー分離条件で、の条件下で測定を行ったとしても、多成分の混合による分離の不足や測定間での強度およびクロマトグラフィーでの保持時間のばらつき、または前処理等で生じる試料自体のばらつきなどにより、各成分の対応付けが困難となる。
【0010】
本発明は、類似の条件下で、複数の試料に対して測定した複数の質量分析データに対して、同一成分を高精度に抽出可能な質量分析データ解析方法を提供することにある。
【課題を解決するための手段】
【0011】
本発明の一つの特徴は、質量分析データ解析方法において、複数の成分の混合物からなる複数の試料に対して測定して得られた複数のクロマトグラフィー質量分析データの質量分析データ解析方法において、
特定のある成分の情報と、該特定のある成分とある一定範囲内の質量であって、かつ、ある一定範囲内の時間帯に同様の条件下で検出された他の成分の情報とを用いて、異なるクロマトグラフィー質量分析データ間の対応関係を求め、その一致の割合又は状況から、複数のクロマトグラフィー質量分析データ間の同一成分を求めることである。
【発明の効果】
【0012】
本発明では、複数の試料に対して測定した複数の質量分析データに対して、同一成分を高精度に抽出可能な質量分析データ解析方法を提供することができる。
【発明を実施するための最良の形態】
【0013】
本発明は、例えば生体試料など、試料中に多くの成分が混在する場合において、液体またはガスクロマトグラフィーなどによって分離した質量分析データに対して、複数の測定データ間の成分の対応付けを行う方法に関するものである。以下に本発明の実施例を示す。
【実施例1】
【0014】
図1を参照して本発明の質量分析データ解析方法を説明する。本発明では、複数のクロマトグラフィー質量分析データの解析を目的とする。想定する解析対象の質量分析データとしては、例えば、バイオマーカー探索の際の、基準となる試料群と比較したい試料群のように複数の質量分析データが考えられる。基準となる試料群と、比較したい試料群間の各成分の対応付けを精度高く行うことが出来れば、その後の定量分析で各成分の量比を求め、量比に変動があるものをバイオマーカー候補として抽出できる。
【0015】
本発明では、少なくとも2つ以上の質量分析データ(A,B,C・・・)を読み込み、それぞれに対して、MSスペクトル処理,マスクロマトグラム処理,不純物・ノイズ除去を実施した後、同一成分の判定を実施する。MSスペクトル処理としては、一定の強度閾値によるノイズの除去,ピーク判定,同位体ピーク判定,モノアイソトピックピークの抽出が含まれる。次に、マスクロマトグラム処理を行い、各質量ピーク強度の時間軸変化を評価する。
【0016】
ここでは、各成分のマスクロマトグラム面積を評価する。次に、マスクロマトグラムの形状から、ノイズおよび不純物のデータを除去する。例えば、1MSスペクトルのみ瞬間的に検出される成分や、測定の開始から終了まで長時間にわたって検出され続けるような成分はノイズ,不純物として除去される。次に、各測定データから得られた成分リストを元に、同一成分の判定を実施する。
【0017】
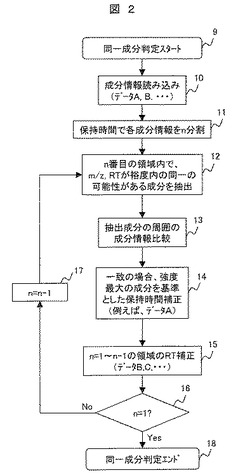
同一成分の判定に関して、図2を用いて説明する。図1(2〜5)で導出された各成分情報を元に、時間軸で各測定データの成分をn分割する。ここでの分割数は、ユーザが自由に設定可能である。例えば、60分の測定データを10分割するとすれば、分析開始である0分〜6分,6分〜12分,・・・と6分毎に、各測定で各時間に検出された成分を分類していく。次に、同一の可能性がある成分を抽出する。n番目の領域内で、質量対電荷比(m/z)および保持時間(RT)が一定の裕度内で一致する成分を抽出する。ここでの裕度は、ユーザが分析の条件に応じて、設定可能である。ここでは、m/z裕度:1.0Da,RT裕度:2.0分とした。ここで抽出された成分は、同一成分である可能性があるが、生体試料などのクルードな試料では、誤った一致判定をしている可能性がある。
そこで、抽出した成分の周囲(図3に示すm/zとRTの2次元マップにおいて)の成分情報を比較する。図3において、各点は、それぞれの時間に特定の質量で検出された成分をプロットしている。ここでは、試料Aの成分αの判定を行うものとする。成分αに関しては、試料Bでは、同じような時間帯に、同じ質量のβとγが検出されていたとする。この場合、試料Bのβおよびγどちらが一致する成分かを判定するのは困難である。そこで、α,β,γの周辺の成分情報を利用して、一致成分の判定を行う。図3では、αのある一定の範囲(m/zおよびRTの)に4種類の成分が確認できる。この4種類の成分は、試料Bにも検出されているため、この4種類の成分を元に判定を行う。試料Aでは、成分1,3がαよりも早い時間(RT)に検出され、成分2,4が遅い時間(RT)に検出されている。一方、試料Bのβでは、成分1,3がβよりも早い時間に検出され、成分2,4が遅い時間に検出されているのに対し、γでは、成分1〜4全てがγよりも早い時間に検出される。このためβの方が一致率が高くなり、同一成分として抽出される。また、一致数が同じ成分がある場合には、周囲の一致成分の同位体ピーク分布の一致率を判定する。検出される成分は同位体ピーク分布を持つため、この情報を利用する。但し、ここでは、同位体ピーク分布を判定する成分は、一定の強度閾値以上の強度を持つ成分のみとする。これは、図4に示すように、強度の大きさによって分布のパターンが変化するためである。強度の高いピークの場合は、ほぼ同じ同位体分布パターンが得られるが、強度が低くなった場合には、質量分析計の検出誤差が大きくなり、同位体分布パターンが測定ごとにばらつくことが知られている。このため、一定以上の強度を持つ成分に対してのみ、同位体ピーク分布の判定を実施する。
【0018】
次に、図2において、抽出成分の周囲の成分情報を比較し、一致する成分がある場合には、基準とする測定データを決定する。ここでは、Aの成分が強度最大であったとすると、Aの補正データを基準として、BおよびCの測定データを補正する。次に、nの補正の結果を元に、1〜n−1の領域に対して補正を行う。ここでは、全成分を一様にnの補正結果と同様に補正する。例えば、領域nで最大の強度を持つ成分αがあり、測定データAの成分αの保持時間を基準として、測定データBの成分αは+0.5分、Cの成分αは−0.2分のずれがあったとする。この場合、Bの成分αは、Aの成分αにあわせるため、保持時間を0.5分マイナス側にシフトし、Cの成分αは、保持時間を0.2分プラス側にシフトする。同様に、ここでは、1〜n−1の領域の全成分に対して、Bでは保持時間を−0.5分補正し、Cでは+0.2分補正する。
【0019】
この処理を全ての領域に対して、一方向(開始〜終了あるいは、終了〜開始)に実施する。ここで、一致判定は、分析終了時間から開始時間の方向で補正していくことが望ましい。図5に測定時間と保持時間のずれの関係を示す。図5から、分析の後半になるほど保持時間のずれは小さくなることがわかる。これは、分析開始時には、試料のカラムへの吸着状況や不純物の流出など測定毎のばらつきが大きく現われるのに対し、分析終了時には溶媒濃度が常に同じ条件になるよう設定されているためである。
【0020】
上記の処理を全領域にわたって実施することにより、同一成分判定を終了し、図1−図7において、結果を出力する。出力する結果を図6に示す。出力結果には、同一と判定された成分の番号,RT(基準としたデータの保持時間),m/z,各測定データの成分のマスクロマトグラム面積、および一致判定の成分数が含まれる。また、これらのリストは、生データとリンクしており、成分番号をクリックすることで生データのピーク情報を表示することが可能である。これにより、本発明で求めたリストから定量解析を行い、バイオマーカー候補が抽出された後に、一致成分数および生データから、成分対応付けの信頼性を評価することが可能である。
【実施例2】
【0021】
次に本発明の第2の実施例を示す。本実施例の質量分析システムを図7に示す。同定したタンパク質由来のペプチドに関するデータを格納する内部データベース27,試料であるペプチドを分離する前処理系19,ペプチドをイオン化するイオン化部20,イオンを質量対電荷比m/zに応じて分離する質量分析部21,分離されたイオンを検出しマススペクトルを生成するイオン検出部22,マススペクトル等のデータを整理及び処理するデータ処理部23,分析結果である質量分析データを表示する表示部24,これらの構成部の処理を制御する制御部25、及び、ユーザがデータ及び命令を入力するための入力部26を有する。
【0022】
前処理系19は、液体クロマトグラフィー(LC)を有し、試料を時間的に分離する。
ここでは、液体クロマトグラフ(LC)の代わりにガスクロマトグラフが用いられてもよい。
【0023】
MS1質量分析では、ペプチドはイオン化部20によってイオン化され、質量分析部21に送られる。イオンは質量分析部21によって、質量対電荷比m/zに応じて分離される。ここで、mはイオン質量、zはイオンの帯電価数である。イオン検出部22によって、MS1マススペクトルが生成される。
【0024】
MS2質量分析では、MS1マススペクトルから選択されたプリカーサーイオンを解離する。本例では、プリカーサーイオンの解離方法として、プリカーサーイオンをヘリウムなどのバッファーガスに衝突させて解離させる衝突解離(Collision Induced Dissociation)法を用いる。本例では、内部に中性ガスを充填したコリジョンセル21A(collision cell)が設けられている。
【0025】
質量分析部21は、特定の質量対電荷比(m/z)又は特定の質量対電荷比(m/z)の領域のプリカーサーイオンを捕獲し、それをまとめてコリジョンセル21Aに投入する。特定のプリカーサーイオンを捕獲するには、例えば、排除すべきイオンが共鳴状態となるように、所定の周波数の共鳴電圧をトラップ電圧に重畳印加させる。
【0026】
プリカーサーイオンは、コリジョンセル21Aに内の中性ガスと衝突し、解離する。プリカーサーイオンを中性ガスと衝突させるには、プリカーサーイオンに共鳴する周波数の電圧を印加する。尚、質量分析部21に中性ガスを充満させて、質量分析部内でプリカーサーイオンを中性ガスに衝突させ、解離させてもよい。その場合、コリジョンセル21Aは不要になる。
【0027】
プリカーサーイオンの解離方法として、プリカーサーイオンに低エネルギーの電子を照射し、多量の低エネルギー電子を捕獲させることにより解離させる電子捕獲解離(Electron Capture Dissociation)法,プリカーサーイオンに陰イオンビームを照射し、電子を移動させることにより解離させる電子移動解離(Electron Transfer Dissociation)法等を用いてもよい。
【0028】
コリジョンセルによって解離されたプリカーサーイオンは質量分析部によって、質量対電荷比m/zに応じて分離される。分離されたイオンは、イオン検出部によって検出され、MS2マススペクトルが生成される。MS2マススペクトルは、データ処理部23によって処理され、その分析結果である質量分析データは表示部24にて表示される。データ処理部による処理は後処理と称される。
【0029】
この一連の質量分析過程、即ち、試料のイオン化,イオン化した試料の質量分析部21への輸送及び入射,プリカーサーイオンの解離及び分離,プリカーサーイオン検出,データ処理等の処理は、制御部25が制御する。
【0030】
図8を参照して、本発明による質量分析システムにおける分析処理を説明する。ステップS29にて、測定を開始する。ステップS30にて、MS1質量分析を行う。ステップS31からステップ42まで、MS1質量分析により得られたMS1(n≧1)質量スペクトルに対して、リアルタイムデータ解析を実施する。ステップS32にて、ピーク判定を行う。即ち、MS1(n≧1)質量スペクトルのピークを検出する。ステップS33にて、同位体・価数判定を行う。即ち、MS1(n≧1)質量スペクトルのピークから、同位体のピークを除去する。こうして得られた同位体を含まないピーク(モノアイソトピックピーク)の数をNpiとする。ステップS34にて、Npi本のピークから、順に1つのピークを選択し、その強度を閾値と比較する。このピークの強度が閾値以上の場合にはステップS35に進み、このピークの強度が閾値未満の場合にはステップS41に進み、次のピークに対して同様の判定を行う。ステップS35にて、このピークのイオンに関して、液体クロマトグラフの保持時間(RT),質量対電荷比(m/z),価数(z)及び同位体パターンを内部データベースに格納された情報と照合する。
【0031】
ステップS36にて、このピークのイオンの情報と内部データベースの情報が一致するか否かを判定する。一致する場合は、ステップS38に進み、一致しない場合は、ステップS37に進む。ステップS38では、一致したイオンは一致リストとしてメモリー上に格納する。次に、ステップS39にて一致リストのイオンの現在の保持時間から内部データベースの保持時間情報を補正する。ここで、補正を行うには、少なくとも3個以上のイオン情報があることが望ましい。1つ或いは2つの場合には、ノイズや不純物などに対して、誤った判定をすることがあり、できるだけ多くの情報を照合して補正を行うことが望ましい。ここでの補正に用いる最低一致イオン数はユーザが指定可能である。ここで内部データベースに格納されているデータを図9に示す。ここでは、補正後の保持時間が格納されており、これ以降の保持時間で検出されるイオンに対しては、補正値を用いて照合を実施する。また、分析の各時間帯において検出される一致イオンによってその時間以降の内部データベースの保持時間は随時書き換えられていく。一方、内部データベースと一致しないイオンについては、ステップS37にて、MS2質量分析のプリカーサーイオンの候補リストに加える。
【0032】
ステップS40にて、全ピークに対して内部データベースとの照合が終了したか否かを判定する。終了した場合はステップS42に進み、終了していない場合は、ステップS41に進む。ステップS41にて、次のピークに進む。ステップS42にて、MS2質量分析のためのプリカーサーイオンを決定する。こうして決定したプリカーサーイオンに対して順にMS2質量分析を実行する(ステップS43)。
【0033】
ステップS44にて、分析が終了か否かを判定する。終了でない場合は、ステップS30に戻る。終了である場合は、ステップS45にて、測定を終了する。ステップS42からステップS42までのリアルタイムデータ解析を実現するには、ステップS32からステップS42までの処理を、10ミリ秒以内で、好ましくは、1ミリ秒以内で実行する必要がある。
【0034】
以上のように本発明では、対応付けを行う成分だけでなく、類似の時間帯に検出された成分情報もあわせて判定に利用することで、対応付けの精度向上が図れる。また、本発明では、MSスペクトルやトータルイオンクロマトグラムなど複数の成分情報が含まれるデータを基に保持時間補正を行わず、各成分ごとに対応付けを実施するため、同じ時間帯に検出される強度の高い成分に影響されがちな微量成分の対応付けも可能である。また、本発明では、MSスペクトルを判定に用いるため、定量分析精度を損なうことなく、MS/MS分析が行われていない全ての成分に対して対応付けが可能である。
【0035】
以上、本発明の例を説明したが、本発明は上述の例に限定されるものではなく、特許請求の範囲に記載された発明の範囲にて様々な変更が可能であることは当業者により容易に理解されよう。
【図面の簡単な説明】
【0036】
【図1】本発明の質量分析データ解析システムの流れを示す図である。
【図2】本発明の同一成分判定の流れを示す図である。
【図3】本発明の周囲のイオン情報を用いた成分対応付けの概念図である。
【図4】強度と同位体ピークの分布の関係を示す図である。
【図5】保持時間と各保持時間でのずれの関係を示す図である
【図6】本発明の質量分析データ解析結果の出力内容を示す図である。
【図7】本発明の第2の実施例である質量分析システムの構成を示す図である。
【図8】本発明の第2の実施例である質量分析システムの流れを示す図である。
【図9】本発明の第2の実施例である質量分析システムで用いる内部データベースの格納データを示した図である。
【符号の説明】
【0037】
1 データ解析の開始
2 データの読込
3 MSスペクトル処理
4 マスクロマトグラム処理
5 不純物、ノイズ除去
6 同一成分判定
7 結果の出力
8 データ解析の終了
9 同一成分判定の開始
10 成分情報読込
11 保持時間で各成分情報をn分割
12 n番目の領域内で(m/z,RT)が裕度内の同一の可能性がある成分を抽出
13 抽出成分の周囲の成分情報比較
14 強度最大の成分を基準とした保持時間補正
15 n=1〜n−1の領域のRT補正
16 n=1の判定
17 n=n−1
18 同一成分判定の終了
19 前処理系
20 イオン化部
21 質量分析部
22 イオン検出部
23 データ処理部
24 表示部
25 制御部
26 ユーザ入力部
27 内部データベース
28 質量分析システム
29 測定の開始
30 MS1分析
31 リアルタイムデータ解析
32 ピーク判定
33 同位体・価数判定
34 プリカーサーイオンの強度判定
35 内部DB照合
36 一致判定
37 候補イオンに追加
38 一致リストに格納
39 一致リストから内部DBの保持時間情報補正
40 照合終了判定
41 次のピークへ
42 MS2プリカーサーイオンの決定
43 MS2分析
44 分析終了判定
45 測定の終了
【技術分野】
【0001】
本発明は、質量分析データ解析方法および質量分析システムに関するものである。
【背景技術】
【0002】
質量分析法には、成分をイオン化してそのまま分析する方法(MS分析法)と、特定成分のイオン(プリカーサーイオン)を質量選択し、それを解離させて生成した解離イオンを質量分析するタンデム質量分析法がある。タンデム質量分析法には、解離イオンの中から、特定の質量対電荷比を持つイオン(プリカーサーイオン)を選択し、更に、そのプリカーサーイオンを解離し、その際生成した解離イオンの質量分析を行うといったように、解離・質量分析を多段に行う機能(n段目の計測:以降MSn)がある。尚、プリカーサーイオンは親イオンとも称される。MSnを実施することにより、プリカーサーイオンの断片情報から成分の構造が解析でき、断片情報を用いたタンパク質データベース検索や断片間の質量から構造を解読するde novo sequencing法などから、成分が何であるかを特定できる。
【0003】
複数の成分が多数混在しているような試料の測定には、クロマトグラフィーと質量分析計とを組み合わせたシステムが用いられる。このシステムでは、測定する物質は、クロマトグラフィーによって物質のカラムへの吸着度の違い等から時間で分離され、質量分析計によって質量で分離される。糖鎖の異性体や1つのアミノ酸と同質量を持つ2つのアミノ酸の組み合わせなどを持つ化合物の場合、質量的に分離することは困難であるが、それらの物質は物質の化学的性質,物理的性質によりクロマトグラフィーによってほとんどが時間的に分離される。クロマトグラフィーを用いた場合では、同じ試料を同じ分析条件下で測定しても、数分のイオンの検出時間誤差が現われるのが通常である。また、生体試料のように、非常に多くの成分が混在したクルードな試料においては、検出時間の一様なずれだけではなく、同一質量の成分間の検出順番の入れ替わりが発生することがある。
【0004】
測定した質量分析データは分析終了後、データ解析が実施される。複数の質量分析データからの同一成分抽出には様々な方法が用いられている。
【0005】
WO05/050188(特許文献1)には、質量分析の同一成分の抽出方法として、タンデム質量分析データを解析した結果であるMSnスペクトルを利用し同一成分を抽出する方法が開示されている。複数の試料に対して、それぞれタンデム質量分析を実施する。それぞれの測定で得られたタンデム質量分析データに対して、データベース検索を実施する。データベース検索の結果、得られた成分に対して、各試料間で同一なものを抽出する。本方法では、データベース検索の結果から同一成分を抜き出しているため、一致判定の精度は高い。しかし、タンデム質量分析を実施した成分に対してのみを、抽出の対象としているため、タンデム質量分析されていない成分については、一致判定が出来ない。生体試料などの成分が数万〜数十万含まれるクルードな試料に対しては、現状の質量分析装置の性能では、1度の測定で検出される全ての成分に対してタンデム質量分析を行うことは困難である。更に、各測定間で、成分の強度や保持時間がばらつくため、ある測定ではタンデム質量分析されていた成分が、次の測定では、タンデム質量分析されていないといったことが起こりうる。このような場合、一方にしか構造情報が無いため、対応付けの精度は大きく低下する。また、成分が微量にしか含まれない場合には、タンデム質量分析を行っても構造を特定できない、または誤った特定をする場合があり、このような場合にも、正しい一致判定が出来ない。
【0006】
また、同一成分の抽出は、通常、各成分の定量分析を目的として行われ、成分の定量にはMSスペクトルの強度が用いられる。このため、定量精度を上げるには、各成分に対してより多くのMSスペクトルを取得する必要がある。一方、タンデム質量分析を行うことでMSスペクトルの取得数が減少するので、結果的に定量精度は低下する。
【0007】
このため、タンデム質量分析を行わず、MSスペクトルのみから同一成分を抽出する方法も検討されている。
【0008】
【特許文献1】WO05/050188
【発明の開示】
【発明が解決しようとする課題】
【0009】
生体試料のクロマトグラフィー質量分析では、同一装置、同一のクロマトグラフィー分離条件で、の条件下で測定を行ったとしても、多成分の混合による分離の不足や測定間での強度およびクロマトグラフィーでの保持時間のばらつき、または前処理等で生じる試料自体のばらつきなどにより、各成分の対応付けが困難となる。
【0010】
本発明は、類似の条件下で、複数の試料に対して測定した複数の質量分析データに対して、同一成分を高精度に抽出可能な質量分析データ解析方法を提供することにある。
【課題を解決するための手段】
【0011】
本発明の一つの特徴は、質量分析データ解析方法において、複数の成分の混合物からなる複数の試料に対して測定して得られた複数のクロマトグラフィー質量分析データの質量分析データ解析方法において、
特定のある成分の情報と、該特定のある成分とある一定範囲内の質量であって、かつ、ある一定範囲内の時間帯に同様の条件下で検出された他の成分の情報とを用いて、異なるクロマトグラフィー質量分析データ間の対応関係を求め、その一致の割合又は状況から、複数のクロマトグラフィー質量分析データ間の同一成分を求めることである。
【発明の効果】
【0012】
本発明では、複数の試料に対して測定した複数の質量分析データに対して、同一成分を高精度に抽出可能な質量分析データ解析方法を提供することができる。
【発明を実施するための最良の形態】
【0013】
本発明は、例えば生体試料など、試料中に多くの成分が混在する場合において、液体またはガスクロマトグラフィーなどによって分離した質量分析データに対して、複数の測定データ間の成分の対応付けを行う方法に関するものである。以下に本発明の実施例を示す。
【実施例1】
【0014】
図1を参照して本発明の質量分析データ解析方法を説明する。本発明では、複数のクロマトグラフィー質量分析データの解析を目的とする。想定する解析対象の質量分析データとしては、例えば、バイオマーカー探索の際の、基準となる試料群と比較したい試料群のように複数の質量分析データが考えられる。基準となる試料群と、比較したい試料群間の各成分の対応付けを精度高く行うことが出来れば、その後の定量分析で各成分の量比を求め、量比に変動があるものをバイオマーカー候補として抽出できる。
【0015】
本発明では、少なくとも2つ以上の質量分析データ(A,B,C・・・)を読み込み、それぞれに対して、MSスペクトル処理,マスクロマトグラム処理,不純物・ノイズ除去を実施した後、同一成分の判定を実施する。MSスペクトル処理としては、一定の強度閾値によるノイズの除去,ピーク判定,同位体ピーク判定,モノアイソトピックピークの抽出が含まれる。次に、マスクロマトグラム処理を行い、各質量ピーク強度の時間軸変化を評価する。
【0016】
ここでは、各成分のマスクロマトグラム面積を評価する。次に、マスクロマトグラムの形状から、ノイズおよび不純物のデータを除去する。例えば、1MSスペクトルのみ瞬間的に検出される成分や、測定の開始から終了まで長時間にわたって検出され続けるような成分はノイズ,不純物として除去される。次に、各測定データから得られた成分リストを元に、同一成分の判定を実施する。
【0017】
同一成分の判定に関して、図2を用いて説明する。図1(2〜5)で導出された各成分情報を元に、時間軸で各測定データの成分をn分割する。ここでの分割数は、ユーザが自由に設定可能である。例えば、60分の測定データを10分割するとすれば、分析開始である0分〜6分,6分〜12分,・・・と6分毎に、各測定で各時間に検出された成分を分類していく。次に、同一の可能性がある成分を抽出する。n番目の領域内で、質量対電荷比(m/z)および保持時間(RT)が一定の裕度内で一致する成分を抽出する。ここでの裕度は、ユーザが分析の条件に応じて、設定可能である。ここでは、m/z裕度:1.0Da,RT裕度:2.0分とした。ここで抽出された成分は、同一成分である可能性があるが、生体試料などのクルードな試料では、誤った一致判定をしている可能性がある。
そこで、抽出した成分の周囲(図3に示すm/zとRTの2次元マップにおいて)の成分情報を比較する。図3において、各点は、それぞれの時間に特定の質量で検出された成分をプロットしている。ここでは、試料Aの成分αの判定を行うものとする。成分αに関しては、試料Bでは、同じような時間帯に、同じ質量のβとγが検出されていたとする。この場合、試料Bのβおよびγどちらが一致する成分かを判定するのは困難である。そこで、α,β,γの周辺の成分情報を利用して、一致成分の判定を行う。図3では、αのある一定の範囲(m/zおよびRTの)に4種類の成分が確認できる。この4種類の成分は、試料Bにも検出されているため、この4種類の成分を元に判定を行う。試料Aでは、成分1,3がαよりも早い時間(RT)に検出され、成分2,4が遅い時間(RT)に検出されている。一方、試料Bのβでは、成分1,3がβよりも早い時間に検出され、成分2,4が遅い時間に検出されているのに対し、γでは、成分1〜4全てがγよりも早い時間に検出される。このためβの方が一致率が高くなり、同一成分として抽出される。また、一致数が同じ成分がある場合には、周囲の一致成分の同位体ピーク分布の一致率を判定する。検出される成分は同位体ピーク分布を持つため、この情報を利用する。但し、ここでは、同位体ピーク分布を判定する成分は、一定の強度閾値以上の強度を持つ成分のみとする。これは、図4に示すように、強度の大きさによって分布のパターンが変化するためである。強度の高いピークの場合は、ほぼ同じ同位体分布パターンが得られるが、強度が低くなった場合には、質量分析計の検出誤差が大きくなり、同位体分布パターンが測定ごとにばらつくことが知られている。このため、一定以上の強度を持つ成分に対してのみ、同位体ピーク分布の判定を実施する。
【0018】
次に、図2において、抽出成分の周囲の成分情報を比較し、一致する成分がある場合には、基準とする測定データを決定する。ここでは、Aの成分が強度最大であったとすると、Aの補正データを基準として、BおよびCの測定データを補正する。次に、nの補正の結果を元に、1〜n−1の領域に対して補正を行う。ここでは、全成分を一様にnの補正結果と同様に補正する。例えば、領域nで最大の強度を持つ成分αがあり、測定データAの成分αの保持時間を基準として、測定データBの成分αは+0.5分、Cの成分αは−0.2分のずれがあったとする。この場合、Bの成分αは、Aの成分αにあわせるため、保持時間を0.5分マイナス側にシフトし、Cの成分αは、保持時間を0.2分プラス側にシフトする。同様に、ここでは、1〜n−1の領域の全成分に対して、Bでは保持時間を−0.5分補正し、Cでは+0.2分補正する。
【0019】
この処理を全ての領域に対して、一方向(開始〜終了あるいは、終了〜開始)に実施する。ここで、一致判定は、分析終了時間から開始時間の方向で補正していくことが望ましい。図5に測定時間と保持時間のずれの関係を示す。図5から、分析の後半になるほど保持時間のずれは小さくなることがわかる。これは、分析開始時には、試料のカラムへの吸着状況や不純物の流出など測定毎のばらつきが大きく現われるのに対し、分析終了時には溶媒濃度が常に同じ条件になるよう設定されているためである。
【0020】
上記の処理を全領域にわたって実施することにより、同一成分判定を終了し、図1−図7において、結果を出力する。出力する結果を図6に示す。出力結果には、同一と判定された成分の番号,RT(基準としたデータの保持時間),m/z,各測定データの成分のマスクロマトグラム面積、および一致判定の成分数が含まれる。また、これらのリストは、生データとリンクしており、成分番号をクリックすることで生データのピーク情報を表示することが可能である。これにより、本発明で求めたリストから定量解析を行い、バイオマーカー候補が抽出された後に、一致成分数および生データから、成分対応付けの信頼性を評価することが可能である。
【実施例2】
【0021】
次に本発明の第2の実施例を示す。本実施例の質量分析システムを図7に示す。同定したタンパク質由来のペプチドに関するデータを格納する内部データベース27,試料であるペプチドを分離する前処理系19,ペプチドをイオン化するイオン化部20,イオンを質量対電荷比m/zに応じて分離する質量分析部21,分離されたイオンを検出しマススペクトルを生成するイオン検出部22,マススペクトル等のデータを整理及び処理するデータ処理部23,分析結果である質量分析データを表示する表示部24,これらの構成部の処理を制御する制御部25、及び、ユーザがデータ及び命令を入力するための入力部26を有する。
【0022】
前処理系19は、液体クロマトグラフィー(LC)を有し、試料を時間的に分離する。
ここでは、液体クロマトグラフ(LC)の代わりにガスクロマトグラフが用いられてもよい。
【0023】
MS1質量分析では、ペプチドはイオン化部20によってイオン化され、質量分析部21に送られる。イオンは質量分析部21によって、質量対電荷比m/zに応じて分離される。ここで、mはイオン質量、zはイオンの帯電価数である。イオン検出部22によって、MS1マススペクトルが生成される。
【0024】
MS2質量分析では、MS1マススペクトルから選択されたプリカーサーイオンを解離する。本例では、プリカーサーイオンの解離方法として、プリカーサーイオンをヘリウムなどのバッファーガスに衝突させて解離させる衝突解離(Collision Induced Dissociation)法を用いる。本例では、内部に中性ガスを充填したコリジョンセル21A(collision cell)が設けられている。
【0025】
質量分析部21は、特定の質量対電荷比(m/z)又は特定の質量対電荷比(m/z)の領域のプリカーサーイオンを捕獲し、それをまとめてコリジョンセル21Aに投入する。特定のプリカーサーイオンを捕獲するには、例えば、排除すべきイオンが共鳴状態となるように、所定の周波数の共鳴電圧をトラップ電圧に重畳印加させる。
【0026】
プリカーサーイオンは、コリジョンセル21Aに内の中性ガスと衝突し、解離する。プリカーサーイオンを中性ガスと衝突させるには、プリカーサーイオンに共鳴する周波数の電圧を印加する。尚、質量分析部21に中性ガスを充満させて、質量分析部内でプリカーサーイオンを中性ガスに衝突させ、解離させてもよい。その場合、コリジョンセル21Aは不要になる。
【0027】
プリカーサーイオンの解離方法として、プリカーサーイオンに低エネルギーの電子を照射し、多量の低エネルギー電子を捕獲させることにより解離させる電子捕獲解離(Electron Capture Dissociation)法,プリカーサーイオンに陰イオンビームを照射し、電子を移動させることにより解離させる電子移動解離(Electron Transfer Dissociation)法等を用いてもよい。
【0028】
コリジョンセルによって解離されたプリカーサーイオンは質量分析部によって、質量対電荷比m/zに応じて分離される。分離されたイオンは、イオン検出部によって検出され、MS2マススペクトルが生成される。MS2マススペクトルは、データ処理部23によって処理され、その分析結果である質量分析データは表示部24にて表示される。データ処理部による処理は後処理と称される。
【0029】
この一連の質量分析過程、即ち、試料のイオン化,イオン化した試料の質量分析部21への輸送及び入射,プリカーサーイオンの解離及び分離,プリカーサーイオン検出,データ処理等の処理は、制御部25が制御する。
【0030】
図8を参照して、本発明による質量分析システムにおける分析処理を説明する。ステップS29にて、測定を開始する。ステップS30にて、MS1質量分析を行う。ステップS31からステップ42まで、MS1質量分析により得られたMS1(n≧1)質量スペクトルに対して、リアルタイムデータ解析を実施する。ステップS32にて、ピーク判定を行う。即ち、MS1(n≧1)質量スペクトルのピークを検出する。ステップS33にて、同位体・価数判定を行う。即ち、MS1(n≧1)質量スペクトルのピークから、同位体のピークを除去する。こうして得られた同位体を含まないピーク(モノアイソトピックピーク)の数をNpiとする。ステップS34にて、Npi本のピークから、順に1つのピークを選択し、その強度を閾値と比較する。このピークの強度が閾値以上の場合にはステップS35に進み、このピークの強度が閾値未満の場合にはステップS41に進み、次のピークに対して同様の判定を行う。ステップS35にて、このピークのイオンに関して、液体クロマトグラフの保持時間(RT),質量対電荷比(m/z),価数(z)及び同位体パターンを内部データベースに格納された情報と照合する。
【0031】
ステップS36にて、このピークのイオンの情報と内部データベースの情報が一致するか否かを判定する。一致する場合は、ステップS38に進み、一致しない場合は、ステップS37に進む。ステップS38では、一致したイオンは一致リストとしてメモリー上に格納する。次に、ステップS39にて一致リストのイオンの現在の保持時間から内部データベースの保持時間情報を補正する。ここで、補正を行うには、少なくとも3個以上のイオン情報があることが望ましい。1つ或いは2つの場合には、ノイズや不純物などに対して、誤った判定をすることがあり、できるだけ多くの情報を照合して補正を行うことが望ましい。ここでの補正に用いる最低一致イオン数はユーザが指定可能である。ここで内部データベースに格納されているデータを図9に示す。ここでは、補正後の保持時間が格納されており、これ以降の保持時間で検出されるイオンに対しては、補正値を用いて照合を実施する。また、分析の各時間帯において検出される一致イオンによってその時間以降の内部データベースの保持時間は随時書き換えられていく。一方、内部データベースと一致しないイオンについては、ステップS37にて、MS2質量分析のプリカーサーイオンの候補リストに加える。
【0032】
ステップS40にて、全ピークに対して内部データベースとの照合が終了したか否かを判定する。終了した場合はステップS42に進み、終了していない場合は、ステップS41に進む。ステップS41にて、次のピークに進む。ステップS42にて、MS2質量分析のためのプリカーサーイオンを決定する。こうして決定したプリカーサーイオンに対して順にMS2質量分析を実行する(ステップS43)。
【0033】
ステップS44にて、分析が終了か否かを判定する。終了でない場合は、ステップS30に戻る。終了である場合は、ステップS45にて、測定を終了する。ステップS42からステップS42までのリアルタイムデータ解析を実現するには、ステップS32からステップS42までの処理を、10ミリ秒以内で、好ましくは、1ミリ秒以内で実行する必要がある。
【0034】
以上のように本発明では、対応付けを行う成分だけでなく、類似の時間帯に検出された成分情報もあわせて判定に利用することで、対応付けの精度向上が図れる。また、本発明では、MSスペクトルやトータルイオンクロマトグラムなど複数の成分情報が含まれるデータを基に保持時間補正を行わず、各成分ごとに対応付けを実施するため、同じ時間帯に検出される強度の高い成分に影響されがちな微量成分の対応付けも可能である。また、本発明では、MSスペクトルを判定に用いるため、定量分析精度を損なうことなく、MS/MS分析が行われていない全ての成分に対して対応付けが可能である。
【0035】
以上、本発明の例を説明したが、本発明は上述の例に限定されるものではなく、特許請求の範囲に記載された発明の範囲にて様々な変更が可能であることは当業者により容易に理解されよう。
【図面の簡単な説明】
【0036】
【図1】本発明の質量分析データ解析システムの流れを示す図である。
【図2】本発明の同一成分判定の流れを示す図である。
【図3】本発明の周囲のイオン情報を用いた成分対応付けの概念図である。
【図4】強度と同位体ピークの分布の関係を示す図である。
【図5】保持時間と各保持時間でのずれの関係を示す図である
【図6】本発明の質量分析データ解析結果の出力内容を示す図である。
【図7】本発明の第2の実施例である質量分析システムの構成を示す図である。
【図8】本発明の第2の実施例である質量分析システムの流れを示す図である。
【図9】本発明の第2の実施例である質量分析システムで用いる内部データベースの格納データを示した図である。
【符号の説明】
【0037】
1 データ解析の開始
2 データの読込
3 MSスペクトル処理
4 マスクロマトグラム処理
5 不純物、ノイズ除去
6 同一成分判定
7 結果の出力
8 データ解析の終了
9 同一成分判定の開始
10 成分情報読込
11 保持時間で各成分情報をn分割
12 n番目の領域内で(m/z,RT)が裕度内の同一の可能性がある成分を抽出
13 抽出成分の周囲の成分情報比較
14 強度最大の成分を基準とした保持時間補正
15 n=1〜n−1の領域のRT補正
16 n=1の判定
17 n=n−1
18 同一成分判定の終了
19 前処理系
20 イオン化部
21 質量分析部
22 イオン検出部
23 データ処理部
24 表示部
25 制御部
26 ユーザ入力部
27 内部データベース
28 質量分析システム
29 測定の開始
30 MS1分析
31 リアルタイムデータ解析
32 ピーク判定
33 同位体・価数判定
34 プリカーサーイオンの強度判定
35 内部DB照合
36 一致判定
37 候補イオンに追加
38 一致リストに格納
39 一致リストから内部DBの保持時間情報補正
40 照合終了判定
41 次のピークへ
42 MS2プリカーサーイオンの決定
43 MS2分析
44 分析終了判定
45 測定の終了
【特許請求の範囲】
【請求項1】
複数の成分の混合物からなる試料をクロマトグラフィーで分離し、前記分離された混合物の質量分析を行う質量分析装置で測定された質量分析データより、所望の成分を含む第一の試料の質量分析データと、前記所望の成分を含む第二の試料の質量分析データとを用い、前記所望の成分を観察する質量分析データの解析方法であって、
前記第一の質量分析データのうち前記所望の成分のデータと、前記所望の成分の質量と所定の範囲内の質量を有しかつ前記所望の成分のクロマトグラフィーの保持時間と所定の範囲内の保持時間を有する比較成分のデータとを特定し、
前記第二の質量分析データのうち前記比較成分のデータを特定し、前記第二の質量分析データの前記比較成分のデータより前記第二の質量分析データの前記所望の成分のデータを特定することを特徴とする質量分析データの解析方法。
【請求項2】
請求項1に記載された質量分析データの解析方法であって、
前記比較成分は複数の成分であり、前記第二の質量分析データの各比較成分が所定の裕度内で一致した割合または状況に基づき、第二の質量分析データの所望の成分のデータを特定することを特徴とする質量分析データの解析方法。
【請求項3】
請求項1または2に記載された質量分析データの解析方法であって、
前記第二の質量分析データの比較成分のデータは、前記第一の質量分析データの比較成分の質量,価数,ピーク強度,同位体ピークの検出分布、又は、クロマトグラフィーの保持時間の少なくともいずれかを用いて特定されることを特徴とする質量分析データの解析方法。
【請求項4】
請求項1ないし3のいずれかに記載された質量分析データの解析方法であって、
前記所定の範囲の質量及び所定の範囲の保持時間は、各質量分析データの解析ごとに指定することを特徴とする質量分析データの解析方法。
【請求項5】
請求項1ないし4のいずれかに記載された質量分析データの解析方法であって、
前記所望の成分のデータについて、第一及び第二の質量分析データの質量,価数,強度,保持時間,同位体の分布を比較したリストを出力することを特徴とする質量分析データの解析方法。
【請求項6】
請求項1ないし5のいずれかに記載された質量分析データの解析方法であって、
前記第一の試料の質量分析データの比較成分と、前記第二の試料の質量分析データの比較成分とを比較し、比較成分のピーク強度の強い一方の質量分析データの比較成分の保持時間を基準とし、他方の質量分析データの比較成分の保持時間を補正することを特徴とする質量分析データの解析方法。
【請求項7】
請求項6に記載された質量分析データの解析方法であって、
前記比較成分の保持時間の補正に基づき前記他方の質量分析データに検出された全成分の保持時間を補正することを特徴とする質量分析データの解析方法。
【請求項8】
複数の成分の混合物からなる試料をクロマトグラフィーで分離し、前記分離された混合物の質量分析を行う質量分析装置と、前記質量分析装置で測定された質量分析データより、所望の成分を含む第一の試料の質量分析データと、前記所望の成分を含む第二の試料の質量分析データとを用い、前記所望の成分を観察する質量分析データの解析装置とを有する質量分析システムであって、
前記解析装置は、前記第一の質量分析データのうち前記所望の成分のデータと、前記所望の成分の質量と所定の範囲内の質量を有しかつ前記所望の成分のクロマトグラフィーの保持時間と所定の範囲内の保持時間を有する比較成分のデータとを特定し、前記第二の質量分析データのうち前記比較成分のデータを特定し、前記第二の質量分析データの前記比較成分のデータより前記第二の質量分析データの前記所望の成分のデータを特定することを特徴とする質量分析システム。
【請求項9】
複数の成分よりなる試料を解離させる第一のイオン化工程と、前記第一のイオン化工程によりイオン化された試料のうち特定の質量対電荷比(m/Z)を有するイオン種を選択し、分離する第一の分離工程と、前記第一の分離工程により分離されたイオン種をさらに解離させる第二のイオン化工程と、前記第二のイオン化工程によりイオン化された試料のうち特定の質量対電荷比を有するイオン種を選択し、分離する第二の分離工程とを有し、同様の選択、分離及び解離を多段階繰り返して試料を分析するタンデム型質量分析システムであって、
過去に分析した試料のイオン情報を格納する内部データベースを有し、前記内部データベースは、最新の分析された試料のイオン情報により更新されることを特徴とする質量分析システム。
【請求項1】
複数の成分の混合物からなる試料をクロマトグラフィーで分離し、前記分離された混合物の質量分析を行う質量分析装置で測定された質量分析データより、所望の成分を含む第一の試料の質量分析データと、前記所望の成分を含む第二の試料の質量分析データとを用い、前記所望の成分を観察する質量分析データの解析方法であって、
前記第一の質量分析データのうち前記所望の成分のデータと、前記所望の成分の質量と所定の範囲内の質量を有しかつ前記所望の成分のクロマトグラフィーの保持時間と所定の範囲内の保持時間を有する比較成分のデータとを特定し、
前記第二の質量分析データのうち前記比較成分のデータを特定し、前記第二の質量分析データの前記比較成分のデータより前記第二の質量分析データの前記所望の成分のデータを特定することを特徴とする質量分析データの解析方法。
【請求項2】
請求項1に記載された質量分析データの解析方法であって、
前記比較成分は複数の成分であり、前記第二の質量分析データの各比較成分が所定の裕度内で一致した割合または状況に基づき、第二の質量分析データの所望の成分のデータを特定することを特徴とする質量分析データの解析方法。
【請求項3】
請求項1または2に記載された質量分析データの解析方法であって、
前記第二の質量分析データの比較成分のデータは、前記第一の質量分析データの比較成分の質量,価数,ピーク強度,同位体ピークの検出分布、又は、クロマトグラフィーの保持時間の少なくともいずれかを用いて特定されることを特徴とする質量分析データの解析方法。
【請求項4】
請求項1ないし3のいずれかに記載された質量分析データの解析方法であって、
前記所定の範囲の質量及び所定の範囲の保持時間は、各質量分析データの解析ごとに指定することを特徴とする質量分析データの解析方法。
【請求項5】
請求項1ないし4のいずれかに記載された質量分析データの解析方法であって、
前記所望の成分のデータについて、第一及び第二の質量分析データの質量,価数,強度,保持時間,同位体の分布を比較したリストを出力することを特徴とする質量分析データの解析方法。
【請求項6】
請求項1ないし5のいずれかに記載された質量分析データの解析方法であって、
前記第一の試料の質量分析データの比較成分と、前記第二の試料の質量分析データの比較成分とを比較し、比較成分のピーク強度の強い一方の質量分析データの比較成分の保持時間を基準とし、他方の質量分析データの比較成分の保持時間を補正することを特徴とする質量分析データの解析方法。
【請求項7】
請求項6に記載された質量分析データの解析方法であって、
前記比較成分の保持時間の補正に基づき前記他方の質量分析データに検出された全成分の保持時間を補正することを特徴とする質量分析データの解析方法。
【請求項8】
複数の成分の混合物からなる試料をクロマトグラフィーで分離し、前記分離された混合物の質量分析を行う質量分析装置と、前記質量分析装置で測定された質量分析データより、所望の成分を含む第一の試料の質量分析データと、前記所望の成分を含む第二の試料の質量分析データとを用い、前記所望の成分を観察する質量分析データの解析装置とを有する質量分析システムであって、
前記解析装置は、前記第一の質量分析データのうち前記所望の成分のデータと、前記所望の成分の質量と所定の範囲内の質量を有しかつ前記所望の成分のクロマトグラフィーの保持時間と所定の範囲内の保持時間を有する比較成分のデータとを特定し、前記第二の質量分析データのうち前記比較成分のデータを特定し、前記第二の質量分析データの前記比較成分のデータより前記第二の質量分析データの前記所望の成分のデータを特定することを特徴とする質量分析システム。
【請求項9】
複数の成分よりなる試料を解離させる第一のイオン化工程と、前記第一のイオン化工程によりイオン化された試料のうち特定の質量対電荷比(m/Z)を有するイオン種を選択し、分離する第一の分離工程と、前記第一の分離工程により分離されたイオン種をさらに解離させる第二のイオン化工程と、前記第二のイオン化工程によりイオン化された試料のうち特定の質量対電荷比を有するイオン種を選択し、分離する第二の分離工程とを有し、同様の選択、分離及び解離を多段階繰り返して試料を分析するタンデム型質量分析システムであって、
過去に分析した試料のイオン情報を格納する内部データベースを有し、前記内部データベースは、最新の分析された試料のイオン情報により更新されることを特徴とする質量分析システム。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【公開番号】特開2009−156722(P2009−156722A)
【公開日】平成21年7月16日(2009.7.16)
【国際特許分類】
【出願番号】特願2007−335523(P2007−335523)
【出願日】平成19年12月27日(2007.12.27)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【Fターム(参考)】
【公開日】平成21年7月16日(2009.7.16)
【国際特許分類】
【出願日】平成19年12月27日(2007.12.27)
【出願人】(501387839)株式会社日立ハイテクノロジーズ (4,325)
【Fターム(参考)】
[ Back to top ]

