透過電子顕微鏡観察用試料の電子染色法。
【課題】
現在、ウラン染色の代替え技術としていろいろ研究されている方法の何れも、細胞組織内への染色処理液の浸透力が弱く、且つ染色性が悪く、コントラストも低いので実用化が難しい。
【解決手段】
エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液(濃度好ましくは0.05〜10.0%)に浸漬し、これを洗浄後、鉛染色液に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
現在、ウラン染色の代替え技術としていろいろ研究されている方法の何れも、細胞組織内への染色処理液の浸透力が弱く、且つ染色性が悪く、コントラストも低いので実用化が難しい。
【解決手段】
エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液(濃度好ましくは0.05〜10.0%)に浸漬し、これを洗浄後、鉛染色液に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、エポキシ樹脂(エポン)などの高分子に包埋した組織塊から超薄切片を作製し、それをアリザリンと鉛を使って電子染色する方法に関するものである。
【背景技術】
【0002】
透過電子顕微鏡の試料作製における電子染色は、電子散乱を促し、得られ像にコントラストを付けるための重要なプロセスである。電子染色は従来ウランや鉛などの重金属染色が主に行われ、一部タンニン酸やルテニウムレッド等の試薬を使用した染色方法もなされている。
透過電子顕微鏡観察用試料の作製方法の中で、ウランと鉛を用いた一般的電子染色法を紹介すると次の通りである。エポキシ樹脂包埋した組織の超薄切片を、まず酢酸ウラニール水溶液(1〜10%前後)に数分〜30分間浸漬する。続いて蒸留水で洗浄後、それらを鉛水溶液に1〜10分浸漬し、これらを洗浄・乾燥して透過電子顕微鏡観察用とする。
近年、国際的な社会情勢から、ウランの使用を規制する法律が検討されている。近い将来、ウランの入手や使用上の厳しい規制によりウランを使用する電子染色法が使用不可能になることが予想される。そこで、ウラン、鉛電子染色法に替わる同等又は優れた電子染色方法を開発すべく研究を進めている。
【0003】
現在紹介されている代替え方法として、非特許文献1〜非特許文献2などがある。
【非特許文献1】医学・生物学電子顕微鏡観察法 P.91〜P.94 日本電子顕微鏡学会関東支部編 丸善(株)
【非特許文献2】よくわかる電子顕微鏡技術 P.80〜P.93 医学・生物学電子顕微鏡技術研究会編 (株)朝倉書店
【発明の開示】
【発明が解決しようとする課題】
【0004】
前記非特許文献1〜非特許文献2に紹介のプロセスは各種電子染色法の実例である。
【課題を解決するための手段】
【0005】
本発明は、ウランの代替え染色剤として考えたものであり、その特徴とする技術条件は、次の(1)、(2)にある。
(1).エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液に浸漬し、これを洗浄後、鉛染色液(鉛水溶液とも言う)に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
(2).アリザリン水溶液の濃度を好ましくは0.05〜10.0%にしたことを特徴とする(1)に記載の透過電子顕微鏡試料の電子染色法。
【発明の効果】
【0006】
本発明の透過電子顕微鏡観察用電子染色の方法は、上記構成の如くアリザリン水溶液と鉛染色液による2重染色であり、これによってアリザリン水溶液と鉛水溶液の細胞組織内浸透速度は均等で且つ早く、細胞組織の細胞膜、核質、核膜、ミトコンドリア、粗面小胞体、滑面小胞体およびグリコーゲン顆粒が良好に染色され、透過電子顕微鏡下でそれらの微細構造が明瞭な高コントラストで観察することが出来るものである。
【発明を実施するための最良の形態】
【0007】
而して、本発明において対象とする細胞組織の超薄切片は、各種動物の各種臓器、骨格筋等である。
本発明において、アリザリン水溶液の効能を確実にする好ましい濃度範囲、温度範囲、浸漬時間は、次の通りである。
有効なアリザリン水溶液の濃度範囲は、 細胞組織への好ましい浸透力を得て且つ染色による汚染を最小限にすることを考慮した結果、0.05%〜10%が好ましい。温度範囲は、染色液の温度が高いほうが染色効果は上るが、アリザリンの分解が早まり染色効果も低下するため、15℃〜50℃とした。適正な浸漬時間は、30分〜90分が良い。
本発明において、鉛染色液は、強アルカリ性で高い染色性を発揮し、さらにアリザリンと増強しあい、より高い染色効果が得られるので、pH11〜pH13が好ましい。又、高温になると汚染が生じるので15℃〜30℃の温度範囲で、しかも浸漬時間は、汚染との関連において1分〜10分が好ましい。
本発明において、アリザリン染色の汚染発生を最小限に抑えるために、アリザリン水溶液で電子染色した超薄切片を再蒸留水または蒸留水を使用して洗浄する。また、鉛水溶液に浸漬後も、超薄切片を再蒸留水または蒸留水を使用して洗浄する。
【実施例1】
【0008】
本発明の実施例を詳細に紹介する。
表1に記載材料の試料1〜11の透過電子顕微鏡試料の作製手順は以下の通りである。灌流固定(試料1〜5、試料7〜10)又は浸漬固定(試料6)した細胞組織塊を細切し、カコジル酸緩衝2%パラホルムアルデヒドと2.5%グルタールアルデヒド混合液に4℃2時間浸漬追固定し、カコジル酸緩衝液で洗浄し、2%四酸化オスミウムに4℃で2時間後固定する。続いて4℃上昇エタノール系列で脱水を十分にする。続いてQY−1とエタノール1:1混合液中に15分間浸漬し、QY−1で15分間2回浸漬置換した後、エポキシ樹脂に包埋、重合させる。
又、試料11の包埋処理方法は、灌流固定した細胞組織塊を上述と同様にパラホルムアルデヒド、グルタールアルデヒド混合液と四酸化オスミウムで浸漬固定した。カコジル酸緩衝液で洗浄後、蒸留水で10分間洗浄を2回行い、室温で0.1%タンニン酸(ファーマフーズ社製)に30分浸漬(ブロック染色)した。次に、2%四酸化オスミウムに4℃1時間後固定し、カコジル酸緩衝液で洗浄した。以下、上述の方法と同じ手順で脱水エポン包埋した。
【0009】
【表1】

【0010】
【表2】

【0011】
【表3】

【0012】
【表4】

【0013】
【表5】

【0014】
【表6】

【0015】
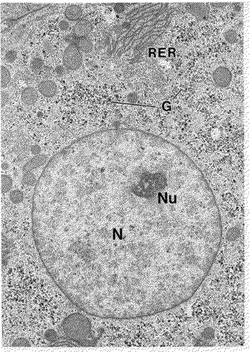
試料1では、肝細胞の核Nやグリコーゲン顆粒G、粗面小胞体RER、核小体Nu等が高(強い)コントラストで染色され、鮮明に観察できた。
試料2では、微絨毛Mvをもつ小腸吸収上皮細胞とその核、粘液顆粒を持つ杯細胞GCおよび細胞境界CJなどが鮮明に観察できた。試料3では、小腸微絨毛の単位膜に包まれたアクチンAc、微絨毛の細胞膜の外表に付着する微細な糖蛋白(糖衣)Gcも明瞭に観察できた。
試料4では、肝細胞の核N、ミトコンドリアM、粗面小胞体RERなどが良好に染色でき、細胞境界CJも明瞭に観察できた。試料5では、腎小体の毛細血管内空BCとその内皮細胞が良好に染色でき明瞭に観察できた。試料6では、腎小体と同様に、心筋細胞が良好に染色でき、介在板IDのデスモゾームDESとギャップジャンクションGAP、ミトコンドリアMを明瞭に観察できた。
このように本発明による試料1〜6は、染色性が良好で、コントラストも高
く明瞭で、電子顕微鏡観察や得られた像の解読判断を迅速且つ正確なものにした。
これに比し試料7、10、11は、いずれも染色性が悪く、コントラストも弱く電子顕微鏡観察や得られた像の解読が困難又は不可なものであった。また試料8は核NとミトコンドリアMが薄く、試料9は毛細血管内空BCとその内皮細胞Eが薄く、電子顕微鏡観察や得られた像の解読がやや困難なものであった。
今回示した実施例は、アリザリン水溶液に室温で1時間程染色した例であり、優れた染色効果があった。より多くの人達に活用してもらうためには、染色時間をもっと短縮できないかなどの課題が残されている。さらに、安定した染色効果を得るための染色装置の開発も必要となる。また、包埋剤、例えばLRホワイトやK4Mなどで本染色法が活用できるかという課題もある。
【産業上の利用可能性】
【0016】
本発明は、アリザリン水溶液と酢酸鉛水溶液などの鉛染料液を使用した2重電子染色法である。写真で示したごとく、各種細胞の微細構造が鮮明に捉えられ、像の解読が容易である。また、アリザリン水溶液と鉛染料液の入手が容易で安価でもあり、これらの染色液の作製も比較的簡単なことから、さらなる実験を積み重ねることによって、この染色法の一般化をはかることは、さほど難しいことではなく、エポキシ樹脂以外の他の包埋剤についても同様である。また、電子染色装置の開発も今後の検討課題である。
【図面の簡単な説明】
【0017】
【図1】本発明の実施例に於ける試料1の透過電子顕微鏡写真である。
【図2】本発明の実施例に於ける試料2の透過電子顕微鏡写真である。
【図3】本発明の実施例に於ける試料3の透過電子顕微鏡写真である。
【図4】本発明の実施例に於ける試料4の透過電子顕微鏡写真である。
【図5】本発明の実施例に於ける試料5の透過電子顕微鏡写真である。
【図6】本発明の実施例に於ける試料6の透過電子顕微鏡写真である。
【図7】本発明の実施例に於ける試料7の透過電子顕微鏡写真である。
【図8】本発明の実施例に於ける試料8の透過電子顕微鏡写真である。
【図9】本発明の実施例に於ける試料9の透過電子顕微鏡写真である。
【図10】本発明の実施例に於ける試料10の透過電子顕微鏡写真である。
【図11】本発明の実施例に於ける試料11の透過電子顕微鏡写真である。
【符号の説明】
【0018】
N 核
G グリコーゲン顆粒
RER 粗面小胞体
M ミトコンドリア
Nu 核小体
BC 毛細血管内腔
Mv 微絨毛
GC 杯細胞
CJ 細胞境界
Ac アクチンフィラメント
GC 糖蛋白(糖衣)
ID 介在板
DES デスモゾーム
GAP ギャップ結合
E 内皮細胞
【技術分野】
【0001】
本発明は、エポキシ樹脂(エポン)などの高分子に包埋した組織塊から超薄切片を作製し、それをアリザリンと鉛を使って電子染色する方法に関するものである。
【背景技術】
【0002】
透過電子顕微鏡の試料作製における電子染色は、電子散乱を促し、得られ像にコントラストを付けるための重要なプロセスである。電子染色は従来ウランや鉛などの重金属染色が主に行われ、一部タンニン酸やルテニウムレッド等の試薬を使用した染色方法もなされている。
透過電子顕微鏡観察用試料の作製方法の中で、ウランと鉛を用いた一般的電子染色法を紹介すると次の通りである。エポキシ樹脂包埋した組織の超薄切片を、まず酢酸ウラニール水溶液(1〜10%前後)に数分〜30分間浸漬する。続いて蒸留水で洗浄後、それらを鉛水溶液に1〜10分浸漬し、これらを洗浄・乾燥して透過電子顕微鏡観察用とする。
近年、国際的な社会情勢から、ウランの使用を規制する法律が検討されている。近い将来、ウランの入手や使用上の厳しい規制によりウランを使用する電子染色法が使用不可能になることが予想される。そこで、ウラン、鉛電子染色法に替わる同等又は優れた電子染色方法を開発すべく研究を進めている。
【0003】
現在紹介されている代替え方法として、非特許文献1〜非特許文献2などがある。
【非特許文献1】医学・生物学電子顕微鏡観察法 P.91〜P.94 日本電子顕微鏡学会関東支部編 丸善(株)
【非特許文献2】よくわかる電子顕微鏡技術 P.80〜P.93 医学・生物学電子顕微鏡技術研究会編 (株)朝倉書店
【発明の開示】
【発明が解決しようとする課題】
【0004】
前記非特許文献1〜非特許文献2に紹介のプロセスは各種電子染色法の実例である。
【課題を解決するための手段】
【0005】
本発明は、ウランの代替え染色剤として考えたものであり、その特徴とする技術条件は、次の(1)、(2)にある。
(1).エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液に浸漬し、これを洗浄後、鉛染色液(鉛水溶液とも言う)に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
(2).アリザリン水溶液の濃度を好ましくは0.05〜10.0%にしたことを特徴とする(1)に記載の透過電子顕微鏡試料の電子染色法。
【発明の効果】
【0006】
本発明の透過電子顕微鏡観察用電子染色の方法は、上記構成の如くアリザリン水溶液と鉛染色液による2重染色であり、これによってアリザリン水溶液と鉛水溶液の細胞組織内浸透速度は均等で且つ早く、細胞組織の細胞膜、核質、核膜、ミトコンドリア、粗面小胞体、滑面小胞体およびグリコーゲン顆粒が良好に染色され、透過電子顕微鏡下でそれらの微細構造が明瞭な高コントラストで観察することが出来るものである。
【発明を実施するための最良の形態】
【0007】
而して、本発明において対象とする細胞組織の超薄切片は、各種動物の各種臓器、骨格筋等である。
本発明において、アリザリン水溶液の効能を確実にする好ましい濃度範囲、温度範囲、浸漬時間は、次の通りである。
有効なアリザリン水溶液の濃度範囲は、 細胞組織への好ましい浸透力を得て且つ染色による汚染を最小限にすることを考慮した結果、0.05%〜10%が好ましい。温度範囲は、染色液の温度が高いほうが染色効果は上るが、アリザリンの分解が早まり染色効果も低下するため、15℃〜50℃とした。適正な浸漬時間は、30分〜90分が良い。
本発明において、鉛染色液は、強アルカリ性で高い染色性を発揮し、さらにアリザリンと増強しあい、より高い染色効果が得られるので、pH11〜pH13が好ましい。又、高温になると汚染が生じるので15℃〜30℃の温度範囲で、しかも浸漬時間は、汚染との関連において1分〜10分が好ましい。
本発明において、アリザリン染色の汚染発生を最小限に抑えるために、アリザリン水溶液で電子染色した超薄切片を再蒸留水または蒸留水を使用して洗浄する。また、鉛水溶液に浸漬後も、超薄切片を再蒸留水または蒸留水を使用して洗浄する。
【実施例1】
【0008】
本発明の実施例を詳細に紹介する。
表1に記載材料の試料1〜11の透過電子顕微鏡試料の作製手順は以下の通りである。灌流固定(試料1〜5、試料7〜10)又は浸漬固定(試料6)した細胞組織塊を細切し、カコジル酸緩衝2%パラホルムアルデヒドと2.5%グルタールアルデヒド混合液に4℃2時間浸漬追固定し、カコジル酸緩衝液で洗浄し、2%四酸化オスミウムに4℃で2時間後固定する。続いて4℃上昇エタノール系列で脱水を十分にする。続いてQY−1とエタノール1:1混合液中に15分間浸漬し、QY−1で15分間2回浸漬置換した後、エポキシ樹脂に包埋、重合させる。
又、試料11の包埋処理方法は、灌流固定した細胞組織塊を上述と同様にパラホルムアルデヒド、グルタールアルデヒド混合液と四酸化オスミウムで浸漬固定した。カコジル酸緩衝液で洗浄後、蒸留水で10分間洗浄を2回行い、室温で0.1%タンニン酸(ファーマフーズ社製)に30分浸漬(ブロック染色)した。次に、2%四酸化オスミウムに4℃1時間後固定し、カコジル酸緩衝液で洗浄した。以下、上述の方法と同じ手順で脱水エポン包埋した。
【0009】
【表1】

【0010】
【表2】

【0011】
【表3】

【0012】
【表4】

【0013】
【表5】

【0014】
【表6】

【0015】
試料1では、肝細胞の核Nやグリコーゲン顆粒G、粗面小胞体RER、核小体Nu等が高(強い)コントラストで染色され、鮮明に観察できた。
試料2では、微絨毛Mvをもつ小腸吸収上皮細胞とその核、粘液顆粒を持つ杯細胞GCおよび細胞境界CJなどが鮮明に観察できた。試料3では、小腸微絨毛の単位膜に包まれたアクチンAc、微絨毛の細胞膜の外表に付着する微細な糖蛋白(糖衣)Gcも明瞭に観察できた。
試料4では、肝細胞の核N、ミトコンドリアM、粗面小胞体RERなどが良好に染色でき、細胞境界CJも明瞭に観察できた。試料5では、腎小体の毛細血管内空BCとその内皮細胞が良好に染色でき明瞭に観察できた。試料6では、腎小体と同様に、心筋細胞が良好に染色でき、介在板IDのデスモゾームDESとギャップジャンクションGAP、ミトコンドリアMを明瞭に観察できた。
このように本発明による試料1〜6は、染色性が良好で、コントラストも高
く明瞭で、電子顕微鏡観察や得られた像の解読判断を迅速且つ正確なものにした。
これに比し試料7、10、11は、いずれも染色性が悪く、コントラストも弱く電子顕微鏡観察や得られた像の解読が困難又は不可なものであった。また試料8は核NとミトコンドリアMが薄く、試料9は毛細血管内空BCとその内皮細胞Eが薄く、電子顕微鏡観察や得られた像の解読がやや困難なものであった。
今回示した実施例は、アリザリン水溶液に室温で1時間程染色した例であり、優れた染色効果があった。より多くの人達に活用してもらうためには、染色時間をもっと短縮できないかなどの課題が残されている。さらに、安定した染色効果を得るための染色装置の開発も必要となる。また、包埋剤、例えばLRホワイトやK4Mなどで本染色法が活用できるかという課題もある。
【産業上の利用可能性】
【0016】
本発明は、アリザリン水溶液と酢酸鉛水溶液などの鉛染料液を使用した2重電子染色法である。写真で示したごとく、各種細胞の微細構造が鮮明に捉えられ、像の解読が容易である。また、アリザリン水溶液と鉛染料液の入手が容易で安価でもあり、これらの染色液の作製も比較的簡単なことから、さらなる実験を積み重ねることによって、この染色法の一般化をはかることは、さほど難しいことではなく、エポキシ樹脂以外の他の包埋剤についても同様である。また、電子染色装置の開発も今後の検討課題である。
【図面の簡単な説明】
【0017】
【図1】本発明の実施例に於ける試料1の透過電子顕微鏡写真である。
【図2】本発明の実施例に於ける試料2の透過電子顕微鏡写真である。
【図3】本発明の実施例に於ける試料3の透過電子顕微鏡写真である。
【図4】本発明の実施例に於ける試料4の透過電子顕微鏡写真である。
【図5】本発明の実施例に於ける試料5の透過電子顕微鏡写真である。
【図6】本発明の実施例に於ける試料6の透過電子顕微鏡写真である。
【図7】本発明の実施例に於ける試料7の透過電子顕微鏡写真である。
【図8】本発明の実施例に於ける試料8の透過電子顕微鏡写真である。
【図9】本発明の実施例に於ける試料9の透過電子顕微鏡写真である。
【図10】本発明の実施例に於ける試料10の透過電子顕微鏡写真である。
【図11】本発明の実施例に於ける試料11の透過電子顕微鏡写真である。
【符号の説明】
【0018】
N 核
G グリコーゲン顆粒
RER 粗面小胞体
M ミトコンドリア
Nu 核小体
BC 毛細血管内腔
Mv 微絨毛
GC 杯細胞
CJ 細胞境界
Ac アクチンフィラメント
GC 糖蛋白(糖衣)
ID 介在板
DES デスモゾーム
GAP ギャップ結合
E 内皮細胞
【特許請求の範囲】
【請求項1】
エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液に浸漬し、これを洗浄後、鉛染色液に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
【請求項2】
アリザリン水溶液の濃度を好ましくは0.05〜10.0%にしたことを特徴とする請求項1に記載の透過電子顕微鏡試料の電子染色法。
【請求項1】
エポキシ樹脂に包埋・重合し薄切した細胞組織を電子染色するに際して、超薄切片をアリザリン水溶液に浸漬し、これを洗浄後、鉛染色液に浸漬し、これを洗浄することを特徴とする透過電子顕微鏡試料の電子染色法。
【請求項2】
アリザリン水溶液の濃度を好ましくは0.05〜10.0%にしたことを特徴とする請求項1に記載の透過電子顕微鏡試料の電子染色法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2006−38660(P2006−38660A)
【公開日】平成18年2月9日(2006.2.9)
【国際特許分類】
【出願番号】特願2004−219627(P2004−219627)
【出願日】平成16年7月28日(2004.7.28)
【出願人】(304028726)国立大学法人 大分大学 (181)
【Fターム(参考)】
【公開日】平成18年2月9日(2006.2.9)
【国際特許分類】
【出願日】平成16年7月28日(2004.7.28)
【出願人】(304028726)国立大学法人 大分大学 (181)
【Fターム(参考)】
[ Back to top ]

