造影剤を含む生体吸収性癒着防止材
【課題】 患者を切開することなく、その配置状態を確認可能な生体吸収性癒着防止材を提供する。
【解決手段】 本発明の生体吸収性癒着防止材は、生体吸収性材料から形成された生体吸収性癒着防止材であって、前記生体吸収性材料が、造影剤を含む。本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。
【解決手段】 本発明の生体吸収性癒着防止材は、生体吸収性材料から形成された生体吸収性癒着防止材であって、前記生体吸収性材料が、造影剤を含む。本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、造影剤を含む生体吸収性癒着防止材に関する。
【背景技術】
【0002】
臨床分野において、生体組織の癒着を防止するために、患部とその周辺組織とを物理的に隔離する癒着防止材が使用されている。他方、前記癒着防止材は、所定の期間内に前述のような癒着防止の機能を発揮した後、分解されて生体に吸収されることが望ましい。このような分解吸収性の性質を示す材料としては、例えば、ラクチドおよびカプロラクトン等を構成モノマーとする重合体および共重合体等が使用されている(特許文献1)。
【0003】
しかしながら、前記癒着防止材を生体内に埋入後、前記所定期間を経過するまでに、生体内での固定が解除されたり、分解によって破損するおそれがある。しかしながら、生体内における前記癒着防止材の状態は、患者を切開して確認する以外に手段がなく、この確認処理は、患者にとって大きな苦痛を伴うものであり、医師にとっても大きな労力となる。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2006−297064号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
そこで、本発明は、前記癒着防止材を患者の体内に埋入した後、切開することなく、前記癒着防止材の状態を確認することが可能な新たな癒着防止材の提供を目的とする。
【課題を解決するための手段】
【0006】
本発明の生体吸収性癒着防止材は、生体吸収性材料から形成された生体吸収性癒着防止材であって、前記生体吸収性材料が、造影剤を含むことを特徴とする。
【発明の効果】
【0007】
本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。このように、本発明は、医療分野において極めて有用である。
【図面の簡単な説明】
【0008】
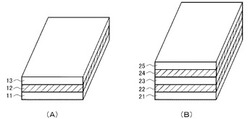
【図1】図1(A)および(B)は、本発明の生体吸収性癒着防止材の構成例を示す概略斜視図である。
【図2】図2は、実施例1の生体吸収性癒着防止材の断面を示す顕微鏡写真である。
【図3】図3は、実施例1の造影剤含有積層フィルムの造影能を示す写真である。
【発明を実施するための形態】
【0009】
本発明の生体吸収性癒着防止材は、前述のように、生体吸収性材料から形成された癒着防止材であって、前記生体吸収性材料が、造影剤を含むことを特徴とする。
【0010】
本発明の生体吸収性癒着防止材は、前記生体吸収性材料が、前記造影剤を含んでいればよく、その他の構成や形状等は、特に制限されない。本発明の生体吸収性癒着防止材は、例えば、その一部に前記造影剤が含まれてもよいし、全体に前記造影剤が含まれてもよい。
【0011】
前記造影剤は、特に制限されず、例えば、画像診断法の種類に応じて適宜選択できる。前記画像診断法は、特に制限されず、例えば、X線画像診断法、核磁気共鳴画像(MRI:Magnetic Resonance Imaging)診断法等があげられる。前記造影剤は、例えば、1種類でもよいし、2種類以上を併用してもよい。後者の場合、例えば、X線画像診断用の造影剤を2種類以上併用してもよいし、MRI診断用の造影剤を2種類以上併用してもよいし、X線画像診断用の造影剤とMRI診断用の造影剤とを併用してもよい。
【0012】
前記造影剤は、特に制限されず、例えば、アミドトリゾ酸、イオキサグル酸、イオキシラン、イオタラム酸、イオトロクス酸メグルミン、イオトロラン、イオパノ酸、イオパミドール、イオプロミド、イオヘキソール、イオメプロール、イオポダートナトリウム、メトリゾ酸、ヨーダミド、ヨードキサム酸、ヨード化ケシ油脂肪酸エチルエステル等のヨード造影剤、硫酸バリウム等があげられ、好ましくは、硫酸バリウムである。これらの造影剤は、例えば、前記X線画像診断法による検出に適している。前記造影剤は、例えば、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせや割合は、特に制限されず、適宜設定可能である。
【0013】
前記造影剤は、これらの他に、例えば、常磁性を示す金属、または前記常磁性を示す金属を含む化合物があげられる。前記金属は、例えば、MRI画像診断による検出に適している。前記金属は、例えば、近傍の原子核との相互作用により造影性を示すものがあげられる。前記近傍の原子核は、例えば、水素原子核があげられる。前記金属の具体例は、ガドリニウム、鉄があげられる。前記鉄は、例えば、超常磁性酸化鉄等があげられる。前記金属を含む化合物は、例えば、クエン酸鉄アンモニウム等があげられる。前記造影剤は、例えば、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせや割合は、特に制限されず、適宜設定できる。
【0014】
前記生体吸収性材料における前記造影剤の濃度は、特に制限されず、例えば、造影剤の種類に応じて適宜設定できる。前記生体吸収性癒着防止材の前記造影剤を含む層において、例えば、10〜50重量%、好ましくは、30〜40重量%である。
【0015】
前記生体吸収性材料は、例えば、生体吸収性ポリマーを含むのが好ましい。前記生体吸収性ポリマーは、特に制限されない。
【0016】
前記生体吸収性ポリマーの分子量は、特に制限されず、例えば、5,000〜2,000,000であり、好ましくは、10,000〜1,500,000であり、より好ましくは、100,000〜1,000,000である。前記生体吸収性ポリマーは、例えば、ホモポリマーでも、コポリマーでもよい。前記コポリマーは、例えば、ランダムポリマー、ブロックポリマー、グラフトポリマー等でもよい。
【0017】
前記生体吸収性ポリマーは、特に制限されず、例えば、脂肪族ポリエステル、ポリビニルアルコール、ポリエチレングリコール、ポリカーボネート、ポリアミド等があげられ、好ましくは、脂肪族ポリエステルである。前記生体吸収性ポリマーを構成するモノマーは、特に制限されず、例えば、乳酸、ラクチド、ラクトン、グリコリド、グリコール酸、トリメチレンカーボネート、エチレンオキサイド、パラジオキサノン等があげられる。前記ホモポリマーは、例えば、いずれかのモノマーから合成でき、または、前記コポリマーは、例えば、これらの組み合わせにより合成できる。前記生体吸収性ポリマーがコポリマーの場合、前記モノマーの組み合わせおよびそれらの割合は、特に制限されない。前記モノマーの組み合わせは、例えば、ラクチドとラクトン、グリコリドとラクトン等があげられ、好ましくは、ラクチドとラクトンである。前記ラクチドは、特に制限されず、例えば、L−ラクチド、D−ラクチドおよびそれらの混合物(D,L−ラクチド)を使用できる。前記ラクチドは、例えば、乳酸から合成してもよい。前記乳酸は、特に制限されず、例えば、L−乳酸、D−乳酸およびそれらの混合物(D,L−乳酸)を使用できる。前記ラクトンは、例えば、ブチロラクトン、バレロラクトン、カプロラクトン等があげられ、カプロラクトンが好ましい。前記ラクトンは、具体的には、例えば、γ−ブチロラクトン、δ−バレロラクトン、ε−カプロラクトン等があげられる。
【0018】
前記生体吸収性ポリマーは、例えば、コラーゲン、ヒアルロン酸、エラスチン、キトサン、キチン、コンドロイチン硫酸、セルロース等の天然高分子でもよい。前記天然高分子は、特に制限されず、例えば、生体の組織や細胞等からの抽出物でもよいし、形質転換体による産生物でもよいし、合成物でもよい。前記天然高分子は、例えば、前記抽出物、産生物または合成物を、さらに、修飾または誘導体化したものでもよい。
【0019】
前記生体吸収性ポリマーは、例えば、前述のポリマーのうち、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせおよび割合は、特に制限されず、適宜設定可能である。
【0020】
前記生体吸収性材料は、前述の造影剤および生体吸収性ポリマー以外に、例えば、他の成分を含んでもよい。前記他の成分は、特に制限されず、例えば、ヒドロキシアパタイト、チタン等があげられる。
【0021】
前記生体吸収性癒着防止材の形状は、特に制限されず、例えば、シート状、管状が好ましく、より好ましくはシート状である。
【0022】
前記生体吸収性癒着防止材は、例えば、単層体でもよいし、積層体でもよく、好ましくは、積層体である。前記積層体は、例えば、前記造影剤を含む層(造影剤含有層)の積層体でもよいし、前記造影剤を含む層と、前記造影剤を含まない層(造影剤非含有層)との積層体でもよい。前記造影剤含有層は、具体的には、造影剤を含有する前記生体吸収性ポリマーの層であり、前記造影剤非含有層は、具体的には、造影剤を含有しない前記生体吸収性ポリマーの層である。前記造影剤含有層および前記造影剤非含有層は、例えば、それぞれ、多孔性でもよいし、非多孔性でもよく、好ましくは非多孔性である。
【0023】
前記生体吸収性癒着防止材が前記積層体の場合、その層数は何ら制限されない。前記層数の下限は、例えば、2層であり、好ましくは、3層であり、より好ましくは、5層であり、上限は、例えば、10層、9層であり、好ましくは、7層である。前記層数の範囲は、例えば、2〜10層であり、好ましくは、3〜7層であり、より好ましくは、5〜7層である。
【0024】
また、前記積層体は、例えば、組成および/または形状等が同じ層の積層体でもよいし、組成および/または形状等が異なる層の積層体でもよい。後者の場合、例えば、各層に含まれる造影剤の種類および濃度、生体吸収性ポリマーの種類および濃度、その他の組成も、特に制限されない。
【0025】
前記積層体が、前記造影剤含有層と前記造影剤非含有層とを含む場合、各層の数および積層順は特に制限されない。前記造影剤含有層における前記造影剤の濃度は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。前記造影剤非含有層は、例えば、実質的に造影剤を含まない層があげられる。実質的に造影剤を含まない層とは、例えば、造影剤を含まない層、または、造影剤が含まれる場合でも、造影剤が検出できない層(造影剤濃度が検出限界以下である層)、造影剤としての機能を奏さない程度の濃度である層等があげられる。
【0026】
前記積層体の構成は、特に制限されない。前記生体吸収性癒着防止材は、例えば、シート状の場合、積層方向の最下層と最上層とが、前記造影剤非含有層であり、前記最下層と前記最上層との間に位置する中層(介在層ともいう)が、前記造影剤含有層を含むことが好ましい。前記最下層と前記最上層との間における中層の層数は、特に制限されず、複数の中層を有する場合、例えば、少なくとも一層が、前記造影剤含有層であればよい。前記最下層は、例えば、適用部位(患部)に接触する側の最外層であり、前記最上層は、例えば、前記最下層とは反対側の最外層である。前記造影剤非含有層は、例えば、前記造影剤含有層より強度に優れる。そこで、このように、例えば、体内の組織と接触する最下層および最上層を前記造影剤非含有層とすれば、前記癒着防止材の物理的強度をさらに向上できる。このため、例えば、前記体内の組織または体液の浸食による、癒着防止材の分解の影響を遅延できる。これによって、前記癒着防止材の形状を、例えば、より長期間、維持可能である。また、前記最下層と前記最上層との間に、前記造影剤含有層を配置すれば、例えば、前記体液の浸食による前記造影剤含有層の分解を抑制できる。これによって、例えば、前記癒着防止材の造影性を、より長期間維持できる。
【0027】
前記積層体は、例えば、前記造影剤含有層を介して、2層の造影剤非含有層が積層された構成があげられる。具体的には、図1(A)に示すように、前記積層体が、3層構造であり、最下層11と最上層13とが、前記造影剤非含有層であり、中層12が、前記造影剤含有層であることが好ましい。
【0028】
また、前記積層体は、例えば、前記造影剤含有層と前記造影剤非含有層とが、1層ずつ交互に積層された構造があげられ、その最下層とその最上層とが、前記造影剤非含有層であることが好ましい。前記積層体の積層数は、特に制限されず、例えば、5層構造または7層構造が好ましい。5層構造の前記積層体の一例を、図1(B)に示す。この積層体は、前記造影剤含有層22、24と前記造影剤非含有層21、23、25とが、1層ずつ交互に積層された構造であり、その最下層21とその最上層25とが、前記造影剤非含有層である。
【0029】
このように、前記造影剤含有層と前記造影剤非含有層とが交互に積層された積層体の場合、各造影剤含有層における造影剤の濃度は、特に制限されず、例えば、全て同じ濃度でもよいし、異なる濃度でもよい。具体例として、前記積層体が、例えば、最下層から最上層の順に、第1層(造影剤非含有層)−第2層(造影剤含有層)−第3層(造影剤非含有層)−第4層(造影剤含有層)−第5層(造影剤非含有層)−第6層(造影剤含有層)−第7層(造影剤非含有層)となる場合、前記第2層、第4層および第6層における造影剤濃度は、例えば、同じでもよいし、異なっていてもよい。前記造影剤濃度が異なる場合、例えば、前記第2層および第6層における各造影剤濃度は、前記第4層における造影剤濃度よりも、低くてもよいし、高くてもよい。前者の場合、前記第4層における造影剤濃度が高いため、例えば、比較的長期間、より高い造影性を維持できる。また、後者の場合、前記第2層および第6層における各造影剤濃度が高いため、例えば、前記第2層および第6層の分解前後で、造影性の差が大きくなる。このため、より容易に、癒着防止材の分解の進行程度を確認できる。
【0030】
前記生体吸収性癒着防止材の生体内における使用方法は、特に制限されない。前記癒着防止材は、例えば、そのままシート状の形態で使用してもよいし、筒状に捲回した形態で使用してもよい。後者は、例えば、腱、神経、卵管等に使用する場合に、好ましい。前記生体は、特に制限されず、例えば、哺乳動物等があげられる。前記哺乳動物は、特に制限されず、例えば、ヒト、サル、イヌ、ネコ、ウマ、ウシ、ヒツジ、ヤギ、ブタ、マウス、ラット、ウサギ、ハムスター等があげられる。
【0031】
本発明の生体吸収性癒着防止材の製造方法は、特に制限されず、造影剤を使用する以外は、公知の方法を採用できる。本発明の生体吸収性癒着防止材の一例として、前記造影剤含有層と前記造影剤非含有層とを含む積層体を製造する方法を、以下に示す。なお、以下の方法は、一例であり、本発明はこれに制限されない。
【0032】
まず、前記生体吸収性ポリマーと溶媒とを混合して、ポリマー液を調製する。前記溶媒は、例えば、前記生体吸収性ポリマーを溶解可能であるものが好ましく、例えば、ジクロロメタン、クロロホルム、1,4−ジオキサン、アセトン、トルエン、ベンゼン、メチルエチルケトン、ジメチルカーボネート、ジメチルホルムアミド、ヘキサフルオロイソプロパノール等の有機溶媒、水等の水系溶媒があげられる。前記溶媒は、例えば、いずれか1種類でもよいし、2種類以上の混合溶媒でもよい。また、前記溶媒は、例えば、前記有機溶媒と前記水系溶媒との混合溶媒でもよい。前記混合溶媒において、組み合わせる溶媒の割合は、特に制限されない。前記ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、例えば、1〜10w/v%であり、好ましくは、3〜7w/v%である。
【0033】
そして、前記ポリマー液に前記造影剤を添加して、造影剤含有ポリマー液を調製する。前記造影剤含有ポリマー液において、前記生体吸収性ポリマー100重量%に対する前記造影剤の割合は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。
【0034】
つぎに、シート状の基材を準備する。前記シート状の基材は、例えば、シリコンシートがあげられる。前記基材の大きさは、特に制限されず、例えば、製造する癒着防止材の大きさに応じて適宜設定できる。
【0035】
さらに、前記基材を、まず、前記造影剤を含まないポリマー液中に浸漬する。前記浸漬時間は、特に制限されず、例えば、1〜10秒間であり、好ましくは、1〜5秒間である。前記浸漬温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬後、前記基材を、前記ポリマー液から引き上げて、乾燥する。これにより、前記基材の表面上に、前記造影剤非含有層が形成される。前記乾燥時間は、特に制限されず、例えば、10〜60分間であり、好ましくは、20〜40分間である。前記乾燥温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬および乾燥の工程は、例えば、1回でもよいし、所望の厚みとなるまで、数回繰り返してもよい。前記造影剤非含有層の厚みは、特に制限されず、例えば、10〜100μmである。
【0036】
続いて、前記造影剤非含有層を形成した基材を、前記造影剤含有ポリマー液中に浸漬する。前記浸漬時間は、特に制限されず、例えば、1〜10秒間であり、好ましくは、1〜5秒間である。前記浸漬温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬後、前記基材を、前記ポリマー液から引き上げて、乾燥する。これにより、前記造影剤非含有層上に、前記造影剤含有層が形成される。前記乾燥時間は、特に制限されず、例えば、10〜60分間であり、好ましくは、20〜40分間である。前記乾燥温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬および乾燥の工程は、例えば、1回でもよいし、所望の厚みとなるまで、数回繰り返してもよい。前記造影剤含有層の厚みは、特に制限されず、例えば、10〜100μmである。
【0037】
そして、再度、前記基材を、前記造影剤を含まないポリマー液に浸漬し、同様にして、前記造影剤非含有層を形成する。これによって、造影剤非含有層−造影剤含有層−造影剤非含有層という3層構造の積層体が形成できる。そして、前記積層体を、前記基材から剥離することにより、本発明の生体吸収性癒着防止材が得られる。前記造影剤非含有層および前記造影剤含有層の形成工程の回数および順序は、何ら制限されず、所望の癒着防止材の構成に応じて適宜決定できる。前記癒着防止材の厚みは、特に制限されず、例えば、50〜400μmである。
【0038】
本発明の生体吸収性癒着防止材の製造方法は、この他に、例えば、熱プレスを利用する方法もあげられる。前記造影剤非含有層は、例えば、前記生体吸収性ポリマーを熱プレスしてシート化し、前記造影剤含有層は、例えば、前記生体吸収性ポリマーと造影剤との混合物を熱プレスしてシート化する。そして、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを積層し、さらに、熱プレスすることで、前記癒着防止材を形成できる。
【0039】
また、本発明の生体吸収性癒着防止材の製造方法は、例えば、キャスト法を利用する方法もあげられる。前記造影剤非含有層は、具体的には、例えば、以下のように作製する。まず、前記生体吸収性ポリマーと溶媒とを混合して、ポリマー液を調製する。前記溶媒は、特に制限されず、前述と同様のものがあげられる。前記ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、例えば、1〜10w/v%であり、好ましくは、3〜7w/v%である。つぎに、前記ポリマー液を、鋳型に流し入れ、前記溶媒を揮発させることで、前記生体吸収性ポリマーをシート化する。また、前記造影剤含有層は、例えば、前記生体吸収性ポリマーと前記造影剤とを混合し、さらに、前記混合物と溶媒とを混合して、造影剤含有ポリマー液を調製する。前記溶媒は、特に制限されず、前述と同様のものがあげられる。前記造影剤含有ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、前記生体吸収性ポリマー液と同様である。また、前記生体吸収性ポリマー100重量%に対する前記造影剤の割合は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。そして、前記造影剤含有ポリマー液を、鋳型に流し入れ、前記溶媒を揮発させることで、前記混合物をシート化する。そして、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを積層し、さらに、熱プレスすることで、前記癒着防止材を形成できる。
【0040】
また、本発明の生体吸収性癒着防止材は、例えば、前記熱プレス法と前記キャスト法とを併用して製造することもできる。例えば、前記造影剤非含有層および前記造影剤含有層の一方を熱プレス法で作製し、他方をキャスト法で作製し、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを熱プレスで積層してもよい。具体例として、例えば、前記造影剤非含有層を前記熱プレスで作製し、前記造影剤含有層をキャスト法で作製する組合せがあげられる。
【0041】
本発明の生体吸収性癒着防止材は、例えば、さらに、補強材を含んでもよい。前記補強材を備えることによって、本発明の生体吸収性癒着防止材は、例えば、その分解性を損なうことなく、前記癒着防止材全体の物理的強度を、さらに向上できる。
【0042】
前記補強材の種類は、特に制限されず、例えば、生体吸収性材料から形成されていることが好ましい。前記生体吸収性材料は、特に制限されず、前述のとおりである。前記補強材の形状は、特に制限されず、例えば、メッシュ状のシートが好ましい。本発明の生体吸収性癒着防止材において、前記補強材の位置は、特に制限されず、例えば、前記造影剤含有層に内包されていることが好ましい。前記造影剤含有層に前記補強材を内包することによって、例えば、前記体液の浸食による前記造影剤含有層の分解を、さらに抑制できる。このため、例えば、本発明の生体吸収性癒着防止材の造影性を、より長期間維持できる。
【0043】
前記補強材の配置方法は、特に制限されない。例えば、予め、前記メッシュ状のシートを補強材として準備し、前記基材上または、前記基材上に形成された造影剤非含有層の上に、前記シートを配置する。そして、前記シートを配置した状態を維持したまま、前記基材を、造影剤含有ポリマー液中に浸漬する。これによって、前記シートのメッシュの間隙に前記造影剤含有ポリマー液が浸透する。浸漬後、前述と同様にして、乾燥処理を施すことによって、前記補強材を内包する前記造影剤含有層を形成できる。
【0044】
前記生体吸収性癒着防止材は、例えば、長い積層体を作製後、所望の長さに切断して製造してもよいし、所望の長さの癒着防止材を直接製造してもよい。なお、本発明の生体吸収性癒着防止材は、前述の浸漬成型法、熱プレス法、キャスト法に限られず、例えば、押出成型、射出成型等の方法を用いて成型してもよい。また、前記生体吸収性癒着防止材の製造方法は、例えば、さらに、滅菌工程等の他の工程を含んでもよい。
【0045】
前記生体吸収性癒着防止材は、例えば、その下面(前記最下層の露出表面)および上面(前記最上層の露出表面)の少なくとも一方に、表面改質処理を施してもよい。前記表面改質処理は、特に制限されず、例えば、親水化処理および疎水化処理等があげられる。前記親水化処理および前記疎水化処理は、特に制限されず、従来公知の方法を採用できる。
【0046】
前記生体吸収性癒着防止材は、例えば、生体内に配置して使用できる。前記配置方法は、特に制限されず、目的の部位に応じて適宜設定できる。前記生体吸収性癒着防止材は、例えば、生体内の組織と共に縫合してもよい。前記縫合により、例えば、前記生体吸収性癒着防止材を、さらに確実に、生体内の組織に固定できる。また、前記生体吸収性癒着防止材は、例えば、複雑で狭小な組織への適用が容易であることから、内視鏡等を用いて、目的部位に配置してもよい。
【0047】
本発明の癒着防止方法は、生体に、前記本発明の生体吸収性癒着防止材を配置する工程と、所望の時点に、前記生体における造影剤を検出することにより、前記生体吸収性癒着防止材を確認することを特徴とする。本発明の方法は、例えば、本発明の生体吸収性癒着防止材の確認方法ともいえる。前記確認工程によれば、前記造影剤の検出により、前記生体吸収性癒着防止材の形状、残存率等を確認できる。
【0048】
本発明の医療用デバイスは、本発明の生体吸収性癒着防止材を含むことを特徴とする。前記医療用デバイスは、本発明の生体吸収性癒着防止材以外に、例えば、内視鏡等を含んでもよい。
【実施例】
【0049】
つぎに、本発明の実施例について説明する。ただし、本発明は、下記実施例により制限されない。
【0050】
(実施例1)
造影剤として硫酸バリウムを含むシート状の生体吸収性癒着防止材を作製した。
【0051】
(1)生体吸収性癒着防止材の作製
生体吸収性ポリマーとして、L−ラクチドとε−カプロラクトンとのコポリマー(以下、「P(LA/CL)」ともいう。)を使用した。前記P(LA/CL)は、分子量が360,000であり、L−ラクチド含有率が69モル%であった。前記P(LA/CL)を、150℃で15分間熱プレスし、非多孔性フィルム状の造影剤非含有層1を作製した。前記造影剤非含有層1の厚みは、120μmとした。
【0052】
他方、前記P(LA/CL)と硫酸バリウムとを重量比100:40となるように混合した。前記混合物を3.5w/v%となるようにジクロロメタンに混合し、造影剤含有ポリマー液を調製した。そして、前記造影剤含有ポリマー液を用いて、キャスト法により、前記混合物をフィルム化した。前記キャスト法は、鋳型に前記造影剤含有ポリマー液を流し入れ、前記ジクロロメタンを揮発させることで行った。これによって、非多孔性フィルム状の造影剤含有層を作製した。前記造影剤含有層2の厚みは、30μmとした。
【0053】
そして、前記造影剤非含有層1、前記造影剤含有層2、前記造影剤非含有層1、前記造影剤含有層2および前記造影剤非含有層1を、この順序で積層し、5層構造の積層フィルムを、130℃で2分間熱プレスした。このようにして、前記造影剤非含有層と前記造影剤含有層とが交互に積層された、シート状の生体吸収性癒着防止材を作製した(以下、「造影剤含有積層フィルム」ともいう。)。前記造影剤含有積層フィルムの厚みは、240μmであった。
【0054】
(2)造影剤含有積層フィルムの評価
前記造影剤含有積層フィルムについて、その断面を顕微鏡で確認した。この結果を、図2に示す。図2は、前記造影剤含有積層フィルムの断面観察(×200)の結果を示す写真である。図2に示すように、前記造影剤含有積層フィルムは、最下層から順に、前記造影剤非含有層と前記造影剤含有層とが交互に積層された、全5層の積層体であることが確認できた。
【0055】
つぎに、前記造影剤含有積層フィルムについて、造影能を確認した。この結果を、図3に示す。図3(a)は、通常条件(自然条件下)で撮影した写真であり、図3(b)は、X線CT撮影した写真である。図3(b)に示すように、前記造影剤含有積層フィルムは、X線CT撮影によりフィルムの形状が明確に写し出されていた。この結果から、前記造影剤含有積層フィルムは、造影能を有することが確認できた。
【0056】
以上、実施形態を参照して本願発明を説明したが、本願発明は、上記実施形態に限定されるものではない。本願発明の構成や詳細には、本願発明のスコープ内で当業者が理解しうる様々な変更をすることができる。
【0057】
この出願は、2011年3月30日に出願された日本出願特願2011−075659を基礎とする優先権を主張し、その開示の全てをここに取り込む。
【産業上の利用可能性】
【0058】
以上のように、本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。このように、本発明は、医療分野において極めて有用である。
【符号の説明】
【0059】
11 最下層
12 中層
13 最上層
21 最下層(造影剤非含有層)
22、24 造影剤含有層
23 造影剤非含有層
25 最上層(造影剤非含有層)
【技術分野】
【0001】
本発明は、造影剤を含む生体吸収性癒着防止材に関する。
【背景技術】
【0002】
臨床分野において、生体組織の癒着を防止するために、患部とその周辺組織とを物理的に隔離する癒着防止材が使用されている。他方、前記癒着防止材は、所定の期間内に前述のような癒着防止の機能を発揮した後、分解されて生体に吸収されることが望ましい。このような分解吸収性の性質を示す材料としては、例えば、ラクチドおよびカプロラクトン等を構成モノマーとする重合体および共重合体等が使用されている(特許文献1)。
【0003】
しかしながら、前記癒着防止材を生体内に埋入後、前記所定期間を経過するまでに、生体内での固定が解除されたり、分解によって破損するおそれがある。しかしながら、生体内における前記癒着防止材の状態は、患者を切開して確認する以外に手段がなく、この確認処理は、患者にとって大きな苦痛を伴うものであり、医師にとっても大きな労力となる。
【先行技術文献】
【特許文献】
【0004】
【特許文献1】特開2006−297064号公報
【発明の概要】
【発明が解決しようとする課題】
【0005】
そこで、本発明は、前記癒着防止材を患者の体内に埋入した後、切開することなく、前記癒着防止材の状態を確認することが可能な新たな癒着防止材の提供を目的とする。
【課題を解決するための手段】
【0006】
本発明の生体吸収性癒着防止材は、生体吸収性材料から形成された生体吸収性癒着防止材であって、前記生体吸収性材料が、造影剤を含むことを特徴とする。
【発明の効果】
【0007】
本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。このように、本発明は、医療分野において極めて有用である。
【図面の簡単な説明】
【0008】
【図1】図1(A)および(B)は、本発明の生体吸収性癒着防止材の構成例を示す概略斜視図である。
【図2】図2は、実施例1の生体吸収性癒着防止材の断面を示す顕微鏡写真である。
【図3】図3は、実施例1の造影剤含有積層フィルムの造影能を示す写真である。
【発明を実施するための形態】
【0009】
本発明の生体吸収性癒着防止材は、前述のように、生体吸収性材料から形成された癒着防止材であって、前記生体吸収性材料が、造影剤を含むことを特徴とする。
【0010】
本発明の生体吸収性癒着防止材は、前記生体吸収性材料が、前記造影剤を含んでいればよく、その他の構成や形状等は、特に制限されない。本発明の生体吸収性癒着防止材は、例えば、その一部に前記造影剤が含まれてもよいし、全体に前記造影剤が含まれてもよい。
【0011】
前記造影剤は、特に制限されず、例えば、画像診断法の種類に応じて適宜選択できる。前記画像診断法は、特に制限されず、例えば、X線画像診断法、核磁気共鳴画像(MRI:Magnetic Resonance Imaging)診断法等があげられる。前記造影剤は、例えば、1種類でもよいし、2種類以上を併用してもよい。後者の場合、例えば、X線画像診断用の造影剤を2種類以上併用してもよいし、MRI診断用の造影剤を2種類以上併用してもよいし、X線画像診断用の造影剤とMRI診断用の造影剤とを併用してもよい。
【0012】
前記造影剤は、特に制限されず、例えば、アミドトリゾ酸、イオキサグル酸、イオキシラン、イオタラム酸、イオトロクス酸メグルミン、イオトロラン、イオパノ酸、イオパミドール、イオプロミド、イオヘキソール、イオメプロール、イオポダートナトリウム、メトリゾ酸、ヨーダミド、ヨードキサム酸、ヨード化ケシ油脂肪酸エチルエステル等のヨード造影剤、硫酸バリウム等があげられ、好ましくは、硫酸バリウムである。これらの造影剤は、例えば、前記X線画像診断法による検出に適している。前記造影剤は、例えば、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせや割合は、特に制限されず、適宜設定可能である。
【0013】
前記造影剤は、これらの他に、例えば、常磁性を示す金属、または前記常磁性を示す金属を含む化合物があげられる。前記金属は、例えば、MRI画像診断による検出に適している。前記金属は、例えば、近傍の原子核との相互作用により造影性を示すものがあげられる。前記近傍の原子核は、例えば、水素原子核があげられる。前記金属の具体例は、ガドリニウム、鉄があげられる。前記鉄は、例えば、超常磁性酸化鉄等があげられる。前記金属を含む化合物は、例えば、クエン酸鉄アンモニウム等があげられる。前記造影剤は、例えば、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせや割合は、特に制限されず、適宜設定できる。
【0014】
前記生体吸収性材料における前記造影剤の濃度は、特に制限されず、例えば、造影剤の種類に応じて適宜設定できる。前記生体吸収性癒着防止材の前記造影剤を含む層において、例えば、10〜50重量%、好ましくは、30〜40重量%である。
【0015】
前記生体吸収性材料は、例えば、生体吸収性ポリマーを含むのが好ましい。前記生体吸収性ポリマーは、特に制限されない。
【0016】
前記生体吸収性ポリマーの分子量は、特に制限されず、例えば、5,000〜2,000,000であり、好ましくは、10,000〜1,500,000であり、より好ましくは、100,000〜1,000,000である。前記生体吸収性ポリマーは、例えば、ホモポリマーでも、コポリマーでもよい。前記コポリマーは、例えば、ランダムポリマー、ブロックポリマー、グラフトポリマー等でもよい。
【0017】
前記生体吸収性ポリマーは、特に制限されず、例えば、脂肪族ポリエステル、ポリビニルアルコール、ポリエチレングリコール、ポリカーボネート、ポリアミド等があげられ、好ましくは、脂肪族ポリエステルである。前記生体吸収性ポリマーを構成するモノマーは、特に制限されず、例えば、乳酸、ラクチド、ラクトン、グリコリド、グリコール酸、トリメチレンカーボネート、エチレンオキサイド、パラジオキサノン等があげられる。前記ホモポリマーは、例えば、いずれかのモノマーから合成でき、または、前記コポリマーは、例えば、これらの組み合わせにより合成できる。前記生体吸収性ポリマーがコポリマーの場合、前記モノマーの組み合わせおよびそれらの割合は、特に制限されない。前記モノマーの組み合わせは、例えば、ラクチドとラクトン、グリコリドとラクトン等があげられ、好ましくは、ラクチドとラクトンである。前記ラクチドは、特に制限されず、例えば、L−ラクチド、D−ラクチドおよびそれらの混合物(D,L−ラクチド)を使用できる。前記ラクチドは、例えば、乳酸から合成してもよい。前記乳酸は、特に制限されず、例えば、L−乳酸、D−乳酸およびそれらの混合物(D,L−乳酸)を使用できる。前記ラクトンは、例えば、ブチロラクトン、バレロラクトン、カプロラクトン等があげられ、カプロラクトンが好ましい。前記ラクトンは、具体的には、例えば、γ−ブチロラクトン、δ−バレロラクトン、ε−カプロラクトン等があげられる。
【0018】
前記生体吸収性ポリマーは、例えば、コラーゲン、ヒアルロン酸、エラスチン、キトサン、キチン、コンドロイチン硫酸、セルロース等の天然高分子でもよい。前記天然高分子は、特に制限されず、例えば、生体の組織や細胞等からの抽出物でもよいし、形質転換体による産生物でもよいし、合成物でもよい。前記天然高分子は、例えば、前記抽出物、産生物または合成物を、さらに、修飾または誘導体化したものでもよい。
【0019】
前記生体吸収性ポリマーは、例えば、前述のポリマーのうち、いずれか1種類でもよいし、2種類以上を含んでもよく、その組み合わせおよび割合は、特に制限されず、適宜設定可能である。
【0020】
前記生体吸収性材料は、前述の造影剤および生体吸収性ポリマー以外に、例えば、他の成分を含んでもよい。前記他の成分は、特に制限されず、例えば、ヒドロキシアパタイト、チタン等があげられる。
【0021】
前記生体吸収性癒着防止材の形状は、特に制限されず、例えば、シート状、管状が好ましく、より好ましくはシート状である。
【0022】
前記生体吸収性癒着防止材は、例えば、単層体でもよいし、積層体でもよく、好ましくは、積層体である。前記積層体は、例えば、前記造影剤を含む層(造影剤含有層)の積層体でもよいし、前記造影剤を含む層と、前記造影剤を含まない層(造影剤非含有層)との積層体でもよい。前記造影剤含有層は、具体的には、造影剤を含有する前記生体吸収性ポリマーの層であり、前記造影剤非含有層は、具体的には、造影剤を含有しない前記生体吸収性ポリマーの層である。前記造影剤含有層および前記造影剤非含有層は、例えば、それぞれ、多孔性でもよいし、非多孔性でもよく、好ましくは非多孔性である。
【0023】
前記生体吸収性癒着防止材が前記積層体の場合、その層数は何ら制限されない。前記層数の下限は、例えば、2層であり、好ましくは、3層であり、より好ましくは、5層であり、上限は、例えば、10層、9層であり、好ましくは、7層である。前記層数の範囲は、例えば、2〜10層であり、好ましくは、3〜7層であり、より好ましくは、5〜7層である。
【0024】
また、前記積層体は、例えば、組成および/または形状等が同じ層の積層体でもよいし、組成および/または形状等が異なる層の積層体でもよい。後者の場合、例えば、各層に含まれる造影剤の種類および濃度、生体吸収性ポリマーの種類および濃度、その他の組成も、特に制限されない。
【0025】
前記積層体が、前記造影剤含有層と前記造影剤非含有層とを含む場合、各層の数および積層順は特に制限されない。前記造影剤含有層における前記造影剤の濃度は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。前記造影剤非含有層は、例えば、実質的に造影剤を含まない層があげられる。実質的に造影剤を含まない層とは、例えば、造影剤を含まない層、または、造影剤が含まれる場合でも、造影剤が検出できない層(造影剤濃度が検出限界以下である層)、造影剤としての機能を奏さない程度の濃度である層等があげられる。
【0026】
前記積層体の構成は、特に制限されない。前記生体吸収性癒着防止材は、例えば、シート状の場合、積層方向の最下層と最上層とが、前記造影剤非含有層であり、前記最下層と前記最上層との間に位置する中層(介在層ともいう)が、前記造影剤含有層を含むことが好ましい。前記最下層と前記最上層との間における中層の層数は、特に制限されず、複数の中層を有する場合、例えば、少なくとも一層が、前記造影剤含有層であればよい。前記最下層は、例えば、適用部位(患部)に接触する側の最外層であり、前記最上層は、例えば、前記最下層とは反対側の最外層である。前記造影剤非含有層は、例えば、前記造影剤含有層より強度に優れる。そこで、このように、例えば、体内の組織と接触する最下層および最上層を前記造影剤非含有層とすれば、前記癒着防止材の物理的強度をさらに向上できる。このため、例えば、前記体内の組織または体液の浸食による、癒着防止材の分解の影響を遅延できる。これによって、前記癒着防止材の形状を、例えば、より長期間、維持可能である。また、前記最下層と前記最上層との間に、前記造影剤含有層を配置すれば、例えば、前記体液の浸食による前記造影剤含有層の分解を抑制できる。これによって、例えば、前記癒着防止材の造影性を、より長期間維持できる。
【0027】
前記積層体は、例えば、前記造影剤含有層を介して、2層の造影剤非含有層が積層された構成があげられる。具体的には、図1(A)に示すように、前記積層体が、3層構造であり、最下層11と最上層13とが、前記造影剤非含有層であり、中層12が、前記造影剤含有層であることが好ましい。
【0028】
また、前記積層体は、例えば、前記造影剤含有層と前記造影剤非含有層とが、1層ずつ交互に積層された構造があげられ、その最下層とその最上層とが、前記造影剤非含有層であることが好ましい。前記積層体の積層数は、特に制限されず、例えば、5層構造または7層構造が好ましい。5層構造の前記積層体の一例を、図1(B)に示す。この積層体は、前記造影剤含有層22、24と前記造影剤非含有層21、23、25とが、1層ずつ交互に積層された構造であり、その最下層21とその最上層25とが、前記造影剤非含有層である。
【0029】
このように、前記造影剤含有層と前記造影剤非含有層とが交互に積層された積層体の場合、各造影剤含有層における造影剤の濃度は、特に制限されず、例えば、全て同じ濃度でもよいし、異なる濃度でもよい。具体例として、前記積層体が、例えば、最下層から最上層の順に、第1層(造影剤非含有層)−第2層(造影剤含有層)−第3層(造影剤非含有層)−第4層(造影剤含有層)−第5層(造影剤非含有層)−第6層(造影剤含有層)−第7層(造影剤非含有層)となる場合、前記第2層、第4層および第6層における造影剤濃度は、例えば、同じでもよいし、異なっていてもよい。前記造影剤濃度が異なる場合、例えば、前記第2層および第6層における各造影剤濃度は、前記第4層における造影剤濃度よりも、低くてもよいし、高くてもよい。前者の場合、前記第4層における造影剤濃度が高いため、例えば、比較的長期間、より高い造影性を維持できる。また、後者の場合、前記第2層および第6層における各造影剤濃度が高いため、例えば、前記第2層および第6層の分解前後で、造影性の差が大きくなる。このため、より容易に、癒着防止材の分解の進行程度を確認できる。
【0030】
前記生体吸収性癒着防止材の生体内における使用方法は、特に制限されない。前記癒着防止材は、例えば、そのままシート状の形態で使用してもよいし、筒状に捲回した形態で使用してもよい。後者は、例えば、腱、神経、卵管等に使用する場合に、好ましい。前記生体は、特に制限されず、例えば、哺乳動物等があげられる。前記哺乳動物は、特に制限されず、例えば、ヒト、サル、イヌ、ネコ、ウマ、ウシ、ヒツジ、ヤギ、ブタ、マウス、ラット、ウサギ、ハムスター等があげられる。
【0031】
本発明の生体吸収性癒着防止材の製造方法は、特に制限されず、造影剤を使用する以外は、公知の方法を採用できる。本発明の生体吸収性癒着防止材の一例として、前記造影剤含有層と前記造影剤非含有層とを含む積層体を製造する方法を、以下に示す。なお、以下の方法は、一例であり、本発明はこれに制限されない。
【0032】
まず、前記生体吸収性ポリマーと溶媒とを混合して、ポリマー液を調製する。前記溶媒は、例えば、前記生体吸収性ポリマーを溶解可能であるものが好ましく、例えば、ジクロロメタン、クロロホルム、1,4−ジオキサン、アセトン、トルエン、ベンゼン、メチルエチルケトン、ジメチルカーボネート、ジメチルホルムアミド、ヘキサフルオロイソプロパノール等の有機溶媒、水等の水系溶媒があげられる。前記溶媒は、例えば、いずれか1種類でもよいし、2種類以上の混合溶媒でもよい。また、前記溶媒は、例えば、前記有機溶媒と前記水系溶媒との混合溶媒でもよい。前記混合溶媒において、組み合わせる溶媒の割合は、特に制限されない。前記ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、例えば、1〜10w/v%であり、好ましくは、3〜7w/v%である。
【0033】
そして、前記ポリマー液に前記造影剤を添加して、造影剤含有ポリマー液を調製する。前記造影剤含有ポリマー液において、前記生体吸収性ポリマー100重量%に対する前記造影剤の割合は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。
【0034】
つぎに、シート状の基材を準備する。前記シート状の基材は、例えば、シリコンシートがあげられる。前記基材の大きさは、特に制限されず、例えば、製造する癒着防止材の大きさに応じて適宜設定できる。
【0035】
さらに、前記基材を、まず、前記造影剤を含まないポリマー液中に浸漬する。前記浸漬時間は、特に制限されず、例えば、1〜10秒間であり、好ましくは、1〜5秒間である。前記浸漬温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬後、前記基材を、前記ポリマー液から引き上げて、乾燥する。これにより、前記基材の表面上に、前記造影剤非含有層が形成される。前記乾燥時間は、特に制限されず、例えば、10〜60分間であり、好ましくは、20〜40分間である。前記乾燥温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬および乾燥の工程は、例えば、1回でもよいし、所望の厚みとなるまで、数回繰り返してもよい。前記造影剤非含有層の厚みは、特に制限されず、例えば、10〜100μmである。
【0036】
続いて、前記造影剤非含有層を形成した基材を、前記造影剤含有ポリマー液中に浸漬する。前記浸漬時間は、特に制限されず、例えば、1〜10秒間であり、好ましくは、1〜5秒間である。前記浸漬温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬後、前記基材を、前記ポリマー液から引き上げて、乾燥する。これにより、前記造影剤非含有層上に、前記造影剤含有層が形成される。前記乾燥時間は、特に制限されず、例えば、10〜60分間であり、好ましくは、20〜40分間である。前記乾燥温度は、特に制限されず、例えば、4〜50℃であり、好ましくは、10〜40℃であり、より好ましくは、20〜30℃である。前記浸漬および乾燥の工程は、例えば、1回でもよいし、所望の厚みとなるまで、数回繰り返してもよい。前記造影剤含有層の厚みは、特に制限されず、例えば、10〜100μmである。
【0037】
そして、再度、前記基材を、前記造影剤を含まないポリマー液に浸漬し、同様にして、前記造影剤非含有層を形成する。これによって、造影剤非含有層−造影剤含有層−造影剤非含有層という3層構造の積層体が形成できる。そして、前記積層体を、前記基材から剥離することにより、本発明の生体吸収性癒着防止材が得られる。前記造影剤非含有層および前記造影剤含有層の形成工程の回数および順序は、何ら制限されず、所望の癒着防止材の構成に応じて適宜決定できる。前記癒着防止材の厚みは、特に制限されず、例えば、50〜400μmである。
【0038】
本発明の生体吸収性癒着防止材の製造方法は、この他に、例えば、熱プレスを利用する方法もあげられる。前記造影剤非含有層は、例えば、前記生体吸収性ポリマーを熱プレスしてシート化し、前記造影剤含有層は、例えば、前記生体吸収性ポリマーと造影剤との混合物を熱プレスしてシート化する。そして、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを積層し、さらに、熱プレスすることで、前記癒着防止材を形成できる。
【0039】
また、本発明の生体吸収性癒着防止材の製造方法は、例えば、キャスト法を利用する方法もあげられる。前記造影剤非含有層は、具体的には、例えば、以下のように作製する。まず、前記生体吸収性ポリマーと溶媒とを混合して、ポリマー液を調製する。前記溶媒は、特に制限されず、前述と同様のものがあげられる。前記ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、例えば、1〜10w/v%であり、好ましくは、3〜7w/v%である。つぎに、前記ポリマー液を、鋳型に流し入れ、前記溶媒を揮発させることで、前記生体吸収性ポリマーをシート化する。また、前記造影剤含有層は、例えば、前記生体吸収性ポリマーと前記造影剤とを混合し、さらに、前記混合物と溶媒とを混合して、造影剤含有ポリマー液を調製する。前記溶媒は、特に制限されず、前述と同様のものがあげられる。前記造影剤含有ポリマー液における前記生体吸収性ポリマーの濃度は、特に制限されず、前記生体吸収性ポリマー液と同様である。また、前記生体吸収性ポリマー100重量%に対する前記造影剤の割合は、特に制限されず、例えば、10〜50重量%、好ましくは、30〜40重量%である。そして、前記造影剤含有ポリマー液を、鋳型に流し入れ、前記溶媒を揮発させることで、前記混合物をシート化する。そして、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを積層し、さらに、熱プレスすることで、前記癒着防止材を形成できる。
【0040】
また、本発明の生体吸収性癒着防止材は、例えば、前記熱プレス法と前記キャスト法とを併用して製造することもできる。例えば、前記造影剤非含有層および前記造影剤含有層の一方を熱プレス法で作製し、他方をキャスト法で作製し、得られたシート状の前記造影剤非含有層と前記造影剤含有層とを熱プレスで積層してもよい。具体例として、例えば、前記造影剤非含有層を前記熱プレスで作製し、前記造影剤含有層をキャスト法で作製する組合せがあげられる。
【0041】
本発明の生体吸収性癒着防止材は、例えば、さらに、補強材を含んでもよい。前記補強材を備えることによって、本発明の生体吸収性癒着防止材は、例えば、その分解性を損なうことなく、前記癒着防止材全体の物理的強度を、さらに向上できる。
【0042】
前記補強材の種類は、特に制限されず、例えば、生体吸収性材料から形成されていることが好ましい。前記生体吸収性材料は、特に制限されず、前述のとおりである。前記補強材の形状は、特に制限されず、例えば、メッシュ状のシートが好ましい。本発明の生体吸収性癒着防止材において、前記補強材の位置は、特に制限されず、例えば、前記造影剤含有層に内包されていることが好ましい。前記造影剤含有層に前記補強材を内包することによって、例えば、前記体液の浸食による前記造影剤含有層の分解を、さらに抑制できる。このため、例えば、本発明の生体吸収性癒着防止材の造影性を、より長期間維持できる。
【0043】
前記補強材の配置方法は、特に制限されない。例えば、予め、前記メッシュ状のシートを補強材として準備し、前記基材上または、前記基材上に形成された造影剤非含有層の上に、前記シートを配置する。そして、前記シートを配置した状態を維持したまま、前記基材を、造影剤含有ポリマー液中に浸漬する。これによって、前記シートのメッシュの間隙に前記造影剤含有ポリマー液が浸透する。浸漬後、前述と同様にして、乾燥処理を施すことによって、前記補強材を内包する前記造影剤含有層を形成できる。
【0044】
前記生体吸収性癒着防止材は、例えば、長い積層体を作製後、所望の長さに切断して製造してもよいし、所望の長さの癒着防止材を直接製造してもよい。なお、本発明の生体吸収性癒着防止材は、前述の浸漬成型法、熱プレス法、キャスト法に限られず、例えば、押出成型、射出成型等の方法を用いて成型してもよい。また、前記生体吸収性癒着防止材の製造方法は、例えば、さらに、滅菌工程等の他の工程を含んでもよい。
【0045】
前記生体吸収性癒着防止材は、例えば、その下面(前記最下層の露出表面)および上面(前記最上層の露出表面)の少なくとも一方に、表面改質処理を施してもよい。前記表面改質処理は、特に制限されず、例えば、親水化処理および疎水化処理等があげられる。前記親水化処理および前記疎水化処理は、特に制限されず、従来公知の方法を採用できる。
【0046】
前記生体吸収性癒着防止材は、例えば、生体内に配置して使用できる。前記配置方法は、特に制限されず、目的の部位に応じて適宜設定できる。前記生体吸収性癒着防止材は、例えば、生体内の組織と共に縫合してもよい。前記縫合により、例えば、前記生体吸収性癒着防止材を、さらに確実に、生体内の組織に固定できる。また、前記生体吸収性癒着防止材は、例えば、複雑で狭小な組織への適用が容易であることから、内視鏡等を用いて、目的部位に配置してもよい。
【0047】
本発明の癒着防止方法は、生体に、前記本発明の生体吸収性癒着防止材を配置する工程と、所望の時点に、前記生体における造影剤を検出することにより、前記生体吸収性癒着防止材を確認することを特徴とする。本発明の方法は、例えば、本発明の生体吸収性癒着防止材の確認方法ともいえる。前記確認工程によれば、前記造影剤の検出により、前記生体吸収性癒着防止材の形状、残存率等を確認できる。
【0048】
本発明の医療用デバイスは、本発明の生体吸収性癒着防止材を含むことを特徴とする。前記医療用デバイスは、本発明の生体吸収性癒着防止材以外に、例えば、内視鏡等を含んでもよい。
【実施例】
【0049】
つぎに、本発明の実施例について説明する。ただし、本発明は、下記実施例により制限されない。
【0050】
(実施例1)
造影剤として硫酸バリウムを含むシート状の生体吸収性癒着防止材を作製した。
【0051】
(1)生体吸収性癒着防止材の作製
生体吸収性ポリマーとして、L−ラクチドとε−カプロラクトンとのコポリマー(以下、「P(LA/CL)」ともいう。)を使用した。前記P(LA/CL)は、分子量が360,000であり、L−ラクチド含有率が69モル%であった。前記P(LA/CL)を、150℃で15分間熱プレスし、非多孔性フィルム状の造影剤非含有層1を作製した。前記造影剤非含有層1の厚みは、120μmとした。
【0052】
他方、前記P(LA/CL)と硫酸バリウムとを重量比100:40となるように混合した。前記混合物を3.5w/v%となるようにジクロロメタンに混合し、造影剤含有ポリマー液を調製した。そして、前記造影剤含有ポリマー液を用いて、キャスト法により、前記混合物をフィルム化した。前記キャスト法は、鋳型に前記造影剤含有ポリマー液を流し入れ、前記ジクロロメタンを揮発させることで行った。これによって、非多孔性フィルム状の造影剤含有層を作製した。前記造影剤含有層2の厚みは、30μmとした。
【0053】
そして、前記造影剤非含有層1、前記造影剤含有層2、前記造影剤非含有層1、前記造影剤含有層2および前記造影剤非含有層1を、この順序で積層し、5層構造の積層フィルムを、130℃で2分間熱プレスした。このようにして、前記造影剤非含有層と前記造影剤含有層とが交互に積層された、シート状の生体吸収性癒着防止材を作製した(以下、「造影剤含有積層フィルム」ともいう。)。前記造影剤含有積層フィルムの厚みは、240μmであった。
【0054】
(2)造影剤含有積層フィルムの評価
前記造影剤含有積層フィルムについて、その断面を顕微鏡で確認した。この結果を、図2に示す。図2は、前記造影剤含有積層フィルムの断面観察(×200)の結果を示す写真である。図2に示すように、前記造影剤含有積層フィルムは、最下層から順に、前記造影剤非含有層と前記造影剤含有層とが交互に積層された、全5層の積層体であることが確認できた。
【0055】
つぎに、前記造影剤含有積層フィルムについて、造影能を確認した。この結果を、図3に示す。図3(a)は、通常条件(自然条件下)で撮影した写真であり、図3(b)は、X線CT撮影した写真である。図3(b)に示すように、前記造影剤含有積層フィルムは、X線CT撮影によりフィルムの形状が明確に写し出されていた。この結果から、前記造影剤含有積層フィルムは、造影能を有することが確認できた。
【0056】
以上、実施形態を参照して本願発明を説明したが、本願発明は、上記実施形態に限定されるものではない。本願発明の構成や詳細には、本願発明のスコープ内で当業者が理解しうる様々な変更をすることができる。
【0057】
この出願は、2011年3月30日に出願された日本出願特願2011−075659を基礎とする優先権を主張し、その開示の全てをここに取り込む。
【産業上の利用可能性】
【0058】
以上のように、本発明の生体吸収性癒着防止材は、造影剤を含むことから、例えば、生体外からの検出が可能である。このため、本発明の生体吸収性癒着防止材によれば、例えば、患者を切開することなく、その配置状態を確認可能である。このように、本発明は、医療分野において極めて有用である。
【符号の説明】
【0059】
11 最下層
12 中層
13 最上層
21 最下層(造影剤非含有層)
22、24 造影剤含有層
23 造影剤非含有層
25 最上層(造影剤非含有層)
【特許請求の範囲】
【請求項1】
生体吸収性材料から形成された生体吸収性癒着防止材であって、
前記生体吸収性材料が、造影剤を含むことを特徴とする生体吸収性癒着防止材。
【請求項2】
前記生体吸収性材料が、生体吸収性ポリマーを含む、請求項1記載の生体吸収性癒着防止材。
【請求項3】
前記生体吸収性ポリマーが、ラクチドとカプロラクトンとのコポリマーを含む、請求項2記載の生体吸収性癒着防止材。
【請求項4】
前記造影剤が、硫酸バリウムおよびヨード造影剤の少なくとも一方である請求項1から3のいずれか一項に記載の生体吸収性癒着防止材。
【請求項5】
前記癒着防止材が、積層体である、請求項1から4のいずれか一項に記載の生体吸収性癒着防止材。
【請求項6】
前記癒着防止材が、シート状である、請求項5記載の生体吸収性癒着防止材。
【請求項7】
前記癒着防止材が、前記造影剤を含む層と、前記造影剤を含まない層との積層体である、請求項1から6のいずれか一項に記載の生体吸収性癒着防止材。
【請求項8】
前記癒着防止材が、3層以上の積層体である、請求項1から7のいずれか一項に記載の生体吸収性癒着防止材。
【請求項9】
前記癒着防止材において、前記造影剤を含む層を介して、2層の造影剤を含まない層が積層されている、請求項8記載の生体吸収性癒着防止材。
【請求項1】
生体吸収性材料から形成された生体吸収性癒着防止材であって、
前記生体吸収性材料が、造影剤を含むことを特徴とする生体吸収性癒着防止材。
【請求項2】
前記生体吸収性材料が、生体吸収性ポリマーを含む、請求項1記載の生体吸収性癒着防止材。
【請求項3】
前記生体吸収性ポリマーが、ラクチドとカプロラクトンとのコポリマーを含む、請求項2記載の生体吸収性癒着防止材。
【請求項4】
前記造影剤が、硫酸バリウムおよびヨード造影剤の少なくとも一方である請求項1から3のいずれか一項に記載の生体吸収性癒着防止材。
【請求項5】
前記癒着防止材が、積層体である、請求項1から4のいずれか一項に記載の生体吸収性癒着防止材。
【請求項6】
前記癒着防止材が、シート状である、請求項5記載の生体吸収性癒着防止材。
【請求項7】
前記癒着防止材が、前記造影剤を含む層と、前記造影剤を含まない層との積層体である、請求項1から6のいずれか一項に記載の生体吸収性癒着防止材。
【請求項8】
前記癒着防止材が、3層以上の積層体である、請求項1から7のいずれか一項に記載の生体吸収性癒着防止材。
【請求項9】
前記癒着防止材において、前記造影剤を含む層を介して、2層の造影剤を含まない層が積層されている、請求項8記載の生体吸収性癒着防止材。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2012−213619(P2012−213619A)
【公開日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願番号】特願2012−69414(P2012−69414)
【出願日】平成24年3月26日(2012.3.26)
【出願人】(000153030)株式会社ジェイ・エム・エス (452)
【Fターム(参考)】
【公開日】平成24年11月8日(2012.11.8)
【国際特許分類】
【出願日】平成24年3月26日(2012.3.26)
【出願人】(000153030)株式会社ジェイ・エム・エス (452)
【Fターム(参考)】
[ Back to top ]

