連続治療台回転/移動および同時コーンビーム撮像を用いた強度変調回転放射線治療
対象物のまわりを移動し治療用放射線のビームを対象物に向けて送る放射線源と、対象物のまわりを移動し撮像放射線のビームを対象物に向けて送る撮像源とを含む放射線治療システム。システムはさらに、対象物が上に配置され、平行移動可動および回転可動である台を含む。システムはまた、1)治療用放射線源で発生された、対象物を透過する放射線を受け取り第1の画像情報を形成する第1の撮像装置と、2)撮像源で発生された、対象物を透過する放射線を受け取り第2の画像情報を形成する第2の撮像装置とを含み、第1の画像情報と第2の画像情報は同時に形成される。
【発明の詳細な説明】
【技術分野】
【0001】
[0001]本出願人らは、米国特許法第119条(e)項の下で、2010年1月5日の出願日、同日出願の米国特許仮出願第61/335,314号の優先権の利益を主張し、同出願の内容全体を参照により本明細書に組み込む。
【0002】
[0002]本発明は、一般に治療用放射線の処置および送達のためのシステムおよび方法に関し、具体的には、治療用放射線の強度変調回転原体放射線治療(VMAT)施行における付加的な治療台の連続円弧回転/移動(C−ARC)、ならびにリアルタイムの治療検証および適合のための同時kVコーンビーム撮像のシステムおよび方法に関する。
【背景技術】
【0003】
[0003]治療用放射線の治療および送達のための知られているシステムおよび方法がいくつかある。これらのうちの1つは、3次元原体放射線治療(3D−CRT)として知られている。3D−CRTでは、3次元撮像、正確な放射線量計算、コンピュータで最適化された治療計画、およびコンピュータで制御された治療施行を伴う。具体的には、3D−CRTではコンピュータと、腫瘍のサイズ、形状および位置、ならびに周囲の臓器を表示するためのCTスキャン、MRスキャンまたはPETスキャンなどの特別な撮像技法とを使用する。その場合、治療用放射線ビームは、マルチリーフコリメータまたは特製の放射線場形成ブロックを用いて腫瘍のサイズおよび形状に正確に適応される。治療用放射線ビームを正確に当てることにより、付近の正常な組織が受ける放射線が少なくなり、したがって正常な組織が放射線治療期間後に速く回復することができる。より多くの正常な組織が治療放射線を受けることから遮蔽されると、腫瘍に実際に送達される放射線量を増加させることができ、したがって腫瘍の治療が成功する確率が高まる。3D−CRTの一例が、Takahashi,S.の公表文献「Conformation radiotherapy: rotation techniques as applied to radiography and radiotherapy of cancer」、Acta Radiol、1965年、補遺242に記載されている。
【0004】
[0004]治療用放射線の治療計画および送達のための別のシステムおよび方法は、強度変調放射線治療またはIMRTとして知られている。IMRTは3D−CRTの特殊な形であり、放射線を変調し、それゆえ腫瘍に適合するようにより正確に成形することができる。具体的には、IMRTでは、治療用放射線ビームを多くの「ビームレット(beamlet)」に分割することを伴う。次に、各ビームレットの強度が個々に調整される。このような強度の調整により、腫瘍の近くの健康な組織が受ける放射線は、3D−CRTと比較してさらに低減させることができる。IMRTの一例が、Brahme,A.らの公表論文「Solution of an integral equation encountered in rotation therapy」、Phys Med Biol Vol.27、No.10、1982年、1221〜1229頁に記載されている。
【0005】
[0005]治療用放射線の処置および送達のための第3のシステムは、強度変調回転放射線治療(IMAT)として、またVMATとして知られるその後の強度変調回転放射線治療として知られている。VMATは、IMRTのいくつかの短所、すなわち多数のビーム方向を必要とすることによる治療時間の増大、および使用するモニタユニット(MU)の増加に対処する。VMATはこれらの短所に、連続ガントリ/コリメータ回転、リーフ動作、および治療計画最適化のための線量率調整を可能にすることによって対処する。ここで線量は、360度までの単一のガントリ円弧の間に送達されるものである。VMAT技法は、最適化のために全360度の範囲のビーム方向が利用可能である点でトモセラピーと類似しているが、全線量が単一の線源回転中に送達される点でIMRTとは根本的に異なる。VMATの一例が、1)Yu,C.X.の「Intensity−modulated arc therapy with dynamic multileaf collimation: an alternative to tomotherapy」、Phys Med Biol Vol.40、1995年、1435〜1449頁、2)Yu,C.X.らの「Clinical implementation of intensity−modulated arc therapy」、Int J Radiat Oncol Biol Phys Vol.53、2002年、453〜463頁、および3)Otto,K.の「Volumetric modulated arc therapy: IMRT in a single gantry arc」、Med Phys Vol.35、2008年、310〜317頁に記載されている。
【0006】
[0006]VMATは一部、マルチリーフコリメータ(MLC)リーフ動作および線量率調整を用いてビーム出力強度を変調することを伴う。加えて、VMATは、治療時間が低減されるように治療用放射線を継続してオンにした状態で、ガントリおよび線形加速器のコリメータを1つまたは複数の完全な円弧または部分円弧を回転させることによって、変調された出力強度のビームを送達する。ガントリの回転中に、i)MLC開口形状,ii)フルエンス出力率(「線量率」)、iii)ガントリ回転速度、およびiv)MLCの向きなど、いくつかのパラメータを動的に変えることができる。パラメータi)〜iv)を変えることが可能なことにより、VMATは、多くの円弧を用いる必要性を低減し、それによって、IMRTに匹敵する線量測定を与えながら、より少ないモニタユニット(MU)に短時間で送達することができる。VMATは、上述の4つの使用可能な可変パラメータを利用できるが、最大ガントリ速度、最大リーフ速度、MLCの向きの制約、およびフルエンス出力率の使用可能な再分割など、線形加速器およびMLCの物理的制約を考慮しながら利用しなければならない。
【0007】
[0007]すべての機械パラメータ、特に機械と患者の向きを治療施行中に動的に制御しなければ、現在のVMAT技術は特定の治療部位に関し制約される。乳ガン治療の場合では、体内乳房結節照射により左側乳ガンを治療するのに適用されるVMATにより、低線量(5Gy)照射を受ける肺、心臓および反対側の乳房の体積が、変形ワイド接線と比較して増大することが示された。本来、その構成により、乳房照射に使用されるVMATは、心臓、肺および反対側の乳房に向けられたビームを含む。
【0008】
[0008]VMATシステムの別の短所は、同時kV撮像と一体化されていないことである。したがって、このようなVMATシステムはリアルタイムの治療検証をすることができない。
【発明の概要】
【0009】
[0009]本発明の一態様は放射線治療システムに関し、このシステムは、対象物のまわりを移動し治療用放射線のビームを対象物に向けて送る放射線源と、対象物のまわりを移動し撮像放射線のビームを対象物に向けて送る撮像源とを含む。システムはさらに、対象物が上に配置され、平行移動可動および回転可動である台を含む。システムはまた、1)治療用放射線源で発生された、対象物を透過する放射線を受け取り第1の画像情報を形成する第1の撮像装置と、2)撮像源で発生された、対象物を透過する放射線を受け取り第2の画像情報を形成する第2の撮像装置とを含み、第1の画像情報と第2の画像情報は同時に形成される。システムはさらに、放射線源、台、第1の撮像装置および第2の撮像装置と通信するコンピュータを備え、このコンピュータは、台の動きと、放射線源の以下のパラメータ、すなわち放射線源の動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、第1の画像情報および第2の画像情報に基づいて同時に制御する。
【0010】
[0010]本発明の第2の態様は、放射線を供給する方法に関し、この方法は、治療用放射線のビームを対象物に向けて送るステップと、撮像放射線のビームを対象物に向けて送るステップとを含む。この方法は、平行移動可動および回転可動である台の上に対象物を配置するステップを含む。この方法はまた、対象物を透過する治療用放射線のビームに基づいて対象物の第1の画像情報を形成するステップと、対象物を透過する撮像放射線のビームに基づいて対象物の第2の画像情報を形成するステップとを含み、第1の画像情報と第2の画像情報は同時に形成される。この方法はさらに、台の動きと、治療用放射線のビームの以下のパラメータ、すなわち治療用放射線のビームの動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、第1の画像情報および第2の画像情報に基づいて同時に制御するステップを含む。
【0011】
[0011]本発明の1つまたは複数の態様は、規定するモニタユニットが少なく、使用する制御点が少ないという利点をもたらす。
[0012]本発明の1つまたは複数の態様は、毒性および二次性悪性腫瘍の危険性を低減する。
【図面の簡単な説明】
【0012】
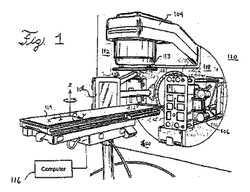
【図1】[0013]本発明によるC−ARC治療を実施できる放射線治療システムの一実施形態を示す図である。
【図2】[0014]本発明による図1の放射線治療システムを動作させる実行可能な一方法の流れ図である。
【図3】[0015]本発明による同時kV/MV撮像のシステムを概略的に示す図である。
【図4A】[0016]定位放射線照射(SRS)治療での90°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4B】定位放射線照射(SRS)治療での135°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4C】定位放射線照射(SRS)治療での180°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4D】定位放射線照射(SRS)治療での270°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図5A】[0017]定位放射線照射治療での90°のガントリ位置におけるkVおよびMVポータル画像である。
【図5B】定位放射線照射治療での135°のガントリ位置におけるkVおよびMVポータル画像である。
【図5C】定位放射線照射治療での180°のガントリ位置におけるkVおよびMVポータル画像である。
【図5D】定位放射線照射治療での270°のガントリ位置におけるkVおよびMVポータル画像である。
【図6】[0018]図6Aは、本発明による乳腺腫瘍治療での実現可能なビーム構成の体外図である。[0019]図6Bは、既知の乳腺腫瘍治療計画でのビーム構成の体外図である。図6Cは、既知の乳腺腫瘍治療計画でのビーム構成の体外図である。
【図7】[0020]図7Aは、図6Aの乳腺腫瘍治療でのビーム構成の体内図である。[0021]図7Bは、図6Bの乳腺腫瘍治療でのビーム構成の体内図である。図7Cは、図6Cの乳腺腫瘍治療でのビーム構成の体内図である。
【図8】[0022]図8Aは、本発明による治療計画と比較した様々な既知の治療計画の、線量に対する同側乳房%体積のグラフである。 [0023]図8Bは、本発明による治療計画と比較した様々な既知の治療計画の、線量に対する同側肺%体積のグラフである。
【図9】[0024]図9Aは、本発明による乳腺腫瘍の治療計画での代表的な軸方向線量分布を示す画像である。[0025]図9Bは、VMAT治療計画での代表的な軸方向線量分布を示す画像である。
【発明を実施するための形態】
【0013】
[0026]図1を見ると、放射線治療システム100が示されており、これは、コーンビームコンピュータ断層撮影システム102などの撮像システムと、医療用線源または加速器104などの治療用放射線源とを含むことができる。コンピュータ断層撮影システム102は、X線源106と、ガントリ110に装着されたフラットパネル撮像装置108とを含む。コンピュータ断層撮影システム102の詳細は、参照によりそれぞれの開示全体が本明細書に組み込まれる米国特許第6,842,502号、および第7,471,765号に記載されている。もちろん、C形アーム支持コーンビームシステムおよびプロトン撮像システムなど、他のタイプの撮像システムも本発明の趣旨から逸脱することなく使用可能である。
【0014】
[0027]システム102は、既存または新規の放射線治療システム112に後付けされ、システム112は医療用線源104など、ヒト患者などの目標体積の治療が可能なレベルで動作する別個の治療用放射線源を含む。医療用線源104は、光子、陽子または電子などの、4MeVから25MeVの範囲のエネルギーを有するX線または粒子のビームを発生する。実際には、医療用線源104は、本発明の趣旨から逸脱することなく、患者の放射線治療に使用される他の放射線源と置き換えることもできる。放射線治療システム112はさらに、ユニットとして可動でリーフを含むマルチリーフコリメータ(MLC)113を含み、このリーフは、治療ビームが患者を透過するように開口を画定するために可動である。放射線治療システム112はまた、医療用線源104と一直線に合わされている撮像装置(図示せず)を含み、これらの間に患者が入る。
【0015】
[0028]患者を支持し、治療用放射線ビームを当てることを支援するために、コンピュータ制御治療台114が設けられる。台114は、図1に概略的に示されたコンピュータ116などのコンピュータによって制御される。台114は、患者をx、yおよびz方向に平行移動させること、ならびにx、yおよびz軸を中心に回転させることを可能にする。さらに、治療台114は、コンピュータ断層撮影画像に著しく障害を与えないように高周波半透過性材料で構成されることが好ましい。台114には、参照によりそれぞれの内容全体が本明細書に組み込まれる米国特許第6,842,502号および第7,471,765号、ならびに米国特許出願公開第US2010−0119032A1号に開示されているものなど、多くの形状がありうる。
【0016】
[0029]図1のシステム100は、本発明によるC−ARC治療用放射線の治療計画を実行するようにコンピュータ116によって制御される。特にC−ARCは、VMATのように、変調ビーム開口および線量率を回転送達と組み合わせることを伴う。VMATと対照的に、C−ARCでは、送達回転の代替モダリティを導入する。特に、台または治療台114は、対象の領域への治療用放射線施行を制御するために、平行移動および/または回転によって移動する。台114の平行移動は、図1に示されたx、yおよびz方向のうちの1つ以上で可能であることに注意されたい。加えて、台114の回転は、x、yおよびz方向のうちの1つ以上を中心にして可能である。台114の回転中、ガントリ110の輪118もまた、脳などの特定の治療部位については同時に回転することができる。
【0017】
[0030]台114が動いている間、開口形状およびMLC113の向きは動的に変えることができる。加えて、フルエンス出力率(「線量率」)およびガントリ回転速度を変えることができ、したがって放射線源104の回転速度を変えることができる。台の動き、ガントリの動き、フルエンス出力率、MLCの向き、およびMLCの形状の制御は、コンピュータ116によって行われる。コンピュータ116を制御するために使用されるソフトウェアは、VMATで使用されるソフトウェアと類似でよく、C−ARC用のソフトウェアは、台114、ガントリ110とその付属品、および患者の間でのいかなる衝突も回避しながら、臨床的に許容可能な線量測定が生じるようなものである。システム100についての上記の説明を念頭において、システム100を動作させる実行可能な方法を図2の流れ図に関して本明細書で説明する。具体的には、方法200が概略的に示されており、この方法は、手順210でまず、腫瘍などの治療の対象物を含むことが分かっている患者の部位のコンピュータ断層撮影または他の3次元計画画像を形成することを伴う。画像の計画は離れたところで、またはその場でコンピュータ断層撮影システム102を使用して行うことができる。次に、健康な組織への放射線量を低減しながら所望の治療線量を腫瘍に当てるために台の動き、ガントリの動き、フルエンス出力率、MLCの向き、MLCの形状を変える手順220で、腫瘍の全体的領域の画像の3次元情報がコンピュータ116または他のコンピュータに供給されて、仮想3次元放射線治療計画が計算される。
【0018】
[0031]仮想計画が計算された後、この計画に従って次には患者を放射線で治療することができる。これに関して、仮想計画では、腫瘍が手順210で撮像されたときと同じ空間位置にあるものと想定することに留意されたい。手順230で患者が台114に配置されると、手順240で腫瘍の空間位置を、その腫瘍が手順210で2つのやり方のうちの1つで撮像されたときと同じになるように微調整することができる。空間位置を微調整する1つのやり方は、患者の皮膚マーカが手順210で撮像されたときにあった位置と同じ位置に見えるようになるまで技術者に患者の位置を変えさせることである。微調整の第2のやり方は、コンピュータ断層撮影システム102を使用して腫瘍の3次元像を撮影し、この微調整画像中に表示される腫瘍の位置が変わって手順210で決定された腫瘍の位置と一致するように患者の位置を調整することである。手順240で患者の位置が変わると、次に手順250で、手順220の仮想計画が腫瘍に適用される。
【0019】
[0032]上述の微調整手順の他に、米国特許第6,842,502号および7,471,765号に記載されているリアルタイムのやり方で、C−ARC計画を使用する治療を実施できることに注意されたい。このリアルタイムのやり方では、腫瘍のリアルタイム撮像が放射線治療中に行われ、この腫瘍のリアルタイム画像は、台の動き、ガントリの動き、フルエンス出力率、MLCの向き、およびMLCの形状を制御するためにコンピュータで使用される。
【0020】
[0033]上述のリアルタイムC−ARC治療の一例が図3に概略的に示されている。具体的には、kVコーンビームが台114上の患者に向けられて通り抜け、3次元リアルタイム画像がフラットパネル画像装置108で生成される。加えて、MVポータル画像もまた同時に使用されて、画像装置120に対向して配置されている線源104(図示せず)から放出された治療放射線に基づいて、患者のリアルタイム2次元画像が生成される。治療用放射線施行中の、kVコーンビーム投影撮像およびMVポータル撮像の両方によるこのような同時リアルタイム撮像は、ビーム患者方向においてVMATおよびC−ARCの回転機能を利用することによって可能になる。MVポータル撮像の投影画像およびkVコーンビーム投影撮像の投影画像をそれぞれ処理して、放射線治療中に患者/生体構造位置の動き/変化をリアルタイムで監視するための2次元検証画像および3次元検証画像を得ることができる。
【0021】
[0034]上述のkVコーンビームおよびMV画像装置によって様々なガントリ回転位置で形成されたkVポータル画像およびMVポータル画像の、脊柱の部位が治療されている例が図5A〜Dに示されている。対応するビーム方向像による参照デジタル再構成放射線透過画像が図4A〜Dに示されている(ビーム方向内および開口内の対象物を表す)。
【0022】
[0035]C−ARC治療計画についての上述の説明と共に、他の既知の治療計画との比較で本発明の利点を示す。加速部分乳房照射(APBI)による乳房内腫瘍の治療の場合では、台114が1つの中間円弧および1つの横方向円弧を回転している間、ガントリ110は接線角で制止したままであり、これらの中間および横方向円弧は、患者の乳房の向きに対して規定される。
【0023】
[0036]問題の乳房が3D−CRT計画によって以前に治療されている場合には、3D−CRTのビーム構成はC−ARC計画を案内するのに使用することができる。というのは、それが台、ガントリおよび患者の間でのいかなる衝突も回避しながら臨床的に許容可能な線量測定を与えていると考えられるからである。3D−CRT計画による台の位置は、台円弧の限界と解釈される。同様に、各円弧に対するガントリ位置は、3D−CRT計画の位置と同じになるように選択される。最適化および線量計算は、円弧に沿って10°間隔で配置された制御点について行われる。このような乳房治療は、3D−CRTで扱われるAPBIの標準接線ビーム構成の利益を維持する。C−ARCは、乳房放射線治療の領域に対するVMATの無理のない拡張であり、標準接線ビーム形状により目標の外側の線量が最少になる。これは図6Aおよび図7Aに示されており、C−ARCを使用する放射ビームはほとんどが乳房に向けられ、心臓および肺などの健康な臓器には放射がほとんど影響を及ぼさない。対照的に、IMRTおよびVMATを用いて適用されるAPBIでは、図6B〜Cおよび図7B〜Cに示されるように、健康な組織にビームが向けられることになりうる。
【0024】
[0037]以下の比較では、以前に3D−CRTによってAPBIで治療された患者に関し、それに続く追加の3つの計画、すなわち1)C−ARC計画、2)IMRT計画、および3)VMAT計画が、患者ごとに生成された。評価に使用されたDVHパラメータは、乳房治療のNSABP−B39/RTOG 0413プロトコルの正常組織制約条件からほとんど選ばれ、次の表1に一覧表示されている。
【0025】
【表1】

【0026】
[0038]上の表1は、C−ARC、IMRTおよびVMAT計画の正常組織線量の平均値を一覧表示しており、そのすべてが当初の3D−CRT計画と比較されている。3つすべての治療計画モダリティで正常同側乳房組織V50%の体積が著しく低下し、この値は平均で7.8%低下している(図8A参照)。図示のように、3つすべての計画で同側肺V30%が著しく低下するが、V5GyについてはC−ARCおよびIMRT計画だけがそのように低下する(図8B参照)。反対側肺V5%では著しい低下がない。4つのVMAT計画は、反対側乳房に不可避の高いDmaxを発生し、このDmaxは3D−CRT計画も、NSABP B−39/RTOG 0413プロトコルに略述されている正常組織線量制約条件(表1)も超える。IMRTおよびC−ARC計画のどれもこのような違反を引き起こさない。C−ARC、IMRTおよびVMAT計画はすべて、3D−CRTと比較してモニタユニットの数を低減し、C−ARC計画がMUの最少平均数を規定する(平均減少 IMRT 136MU、p=0.013、VMAT 281MU、p<0.001、C−ARC 339MU、p<0.001)。
【0027】
[0039]C−ARCとVMATもまた比較されている。これら2つの計画モダリティは、規定線量の50%および100%を受ける同側乳房ならびに規定線量の30%を受ける同側肺の体積の比較に値する低減をもたらす。しかし、VMAT計画では、かなり大きい同側肺体積が5Gyを受けることになり(10.4%対7.8%、p=0.008)、かなり大きい心臓体積が192.5cGyを受けることになる(7.7%対5.5%、p=0.021)。図9A〜Bは、C−ARCおよびVMATそれぞれの代表的な軸方向線量分布を示す。同様に、かなり少ない数のモニタユニットが規定されたC−ARCはVMAT計画(p=0.011)と似ていた。重要でない傾向(p=0.05)が、反対側乳房に低いDmaxを送達するC−ARC計画から現れた。
【0028】
[0040]同側乳房への線量を低減することに加えて、C−ARC計画は、肺および心臓への線量を低減する。C−ARCおよびIMRTは、正面を向いた幾何学的配置がないので、V5Gyで測定された同側肺照射の最大の低減をもたらした。C−ARCおよびIMRT計画はまた、心臓の低線量照射の顕著な低減をもたらした。
【0029】
[0041]ウェッジがないことにより、C−ARC、IMRTおよびVMAT計画ではすべて、規定されたモニタユニットの数が3D−CRT計画と比較して低減し、C−ARC計画が最大の低減をもたらした。C−ARC計画はまた、最小数の制御点を使用し、それによって漏洩放射線が最小限になる。
【0030】
[0042]表1に示されるように、C−ARC計画は、肺、心臓、および反対側乳房への線量を増大させることなく、同側乳房照射の顕著な低減をもたらす。VMAT計画もまた、同側乳房への照射線量を低減することができるが、これは、他のところで線量増大を代償にすることがより多くありうる。
【0031】
[0043]VMAT、C−ARCの無理のない拡張は、快適さの改善、モニタユニットの送達低減、治療時間の短縮が期待される治療を可能にする。C−ARCは、治療計画者および操作員の視点からは、既存の回転放射線治療より著しく複雑なものではない。この革新が行われるためには、治療台回転制御を線量率およびマルチリーフコリメータの動作と連結することが必要になる。VMAT計画ソフトウェアの小修正にはまた、治療台円弧を組み込むことが必要とされる。
【0032】
[0044]APBI C−ARC治療の場合では、ガントリ110は、台114が動いている間静止している。C−ARC治療が、台114とガントリ110が同時に動くことを伴いうる場合がある。この一例は、部分脳放射線治療が用いられる場合である。台114およびガントリ110の動きにより、視交叉、視神経および脳幹を含む健康な部位に当たる治療用放射線の量を加減する。実際には、IMRTと比較してC−ARC治療では、視交叉、視神経および脳幹に対し用いる平均および最大照射線量が低減される。
【0033】
[0045]上記の説明から、当業者は、本発明の本質的特徴を容易に確認することができ、また本発明の趣旨および範囲から逸脱することなく、本発明の様々な変更および/または修正を行って様々な使用法および状況に本発明を適合させることができる。
【技術分野】
【0001】
[0001]本出願人らは、米国特許法第119条(e)項の下で、2010年1月5日の出願日、同日出願の米国特許仮出願第61/335,314号の優先権の利益を主張し、同出願の内容全体を参照により本明細書に組み込む。
【0002】
[0002]本発明は、一般に治療用放射線の処置および送達のためのシステムおよび方法に関し、具体的には、治療用放射線の強度変調回転原体放射線治療(VMAT)施行における付加的な治療台の連続円弧回転/移動(C−ARC)、ならびにリアルタイムの治療検証および適合のための同時kVコーンビーム撮像のシステムおよび方法に関する。
【背景技術】
【0003】
[0003]治療用放射線の治療および送達のための知られているシステムおよび方法がいくつかある。これらのうちの1つは、3次元原体放射線治療(3D−CRT)として知られている。3D−CRTでは、3次元撮像、正確な放射線量計算、コンピュータで最適化された治療計画、およびコンピュータで制御された治療施行を伴う。具体的には、3D−CRTではコンピュータと、腫瘍のサイズ、形状および位置、ならびに周囲の臓器を表示するためのCTスキャン、MRスキャンまたはPETスキャンなどの特別な撮像技法とを使用する。その場合、治療用放射線ビームは、マルチリーフコリメータまたは特製の放射線場形成ブロックを用いて腫瘍のサイズおよび形状に正確に適応される。治療用放射線ビームを正確に当てることにより、付近の正常な組織が受ける放射線が少なくなり、したがって正常な組織が放射線治療期間後に速く回復することができる。より多くの正常な組織が治療放射線を受けることから遮蔽されると、腫瘍に実際に送達される放射線量を増加させることができ、したがって腫瘍の治療が成功する確率が高まる。3D−CRTの一例が、Takahashi,S.の公表文献「Conformation radiotherapy: rotation techniques as applied to radiography and radiotherapy of cancer」、Acta Radiol、1965年、補遺242に記載されている。
【0004】
[0004]治療用放射線の治療計画および送達のための別のシステムおよび方法は、強度変調放射線治療またはIMRTとして知られている。IMRTは3D−CRTの特殊な形であり、放射線を変調し、それゆえ腫瘍に適合するようにより正確に成形することができる。具体的には、IMRTでは、治療用放射線ビームを多くの「ビームレット(beamlet)」に分割することを伴う。次に、各ビームレットの強度が個々に調整される。このような強度の調整により、腫瘍の近くの健康な組織が受ける放射線は、3D−CRTと比較してさらに低減させることができる。IMRTの一例が、Brahme,A.らの公表論文「Solution of an integral equation encountered in rotation therapy」、Phys Med Biol Vol.27、No.10、1982年、1221〜1229頁に記載されている。
【0005】
[0005]治療用放射線の処置および送達のための第3のシステムは、強度変調回転放射線治療(IMAT)として、またVMATとして知られるその後の強度変調回転放射線治療として知られている。VMATは、IMRTのいくつかの短所、すなわち多数のビーム方向を必要とすることによる治療時間の増大、および使用するモニタユニット(MU)の増加に対処する。VMATはこれらの短所に、連続ガントリ/コリメータ回転、リーフ動作、および治療計画最適化のための線量率調整を可能にすることによって対処する。ここで線量は、360度までの単一のガントリ円弧の間に送達されるものである。VMAT技法は、最適化のために全360度の範囲のビーム方向が利用可能である点でトモセラピーと類似しているが、全線量が単一の線源回転中に送達される点でIMRTとは根本的に異なる。VMATの一例が、1)Yu,C.X.の「Intensity−modulated arc therapy with dynamic multileaf collimation: an alternative to tomotherapy」、Phys Med Biol Vol.40、1995年、1435〜1449頁、2)Yu,C.X.らの「Clinical implementation of intensity−modulated arc therapy」、Int J Radiat Oncol Biol Phys Vol.53、2002年、453〜463頁、および3)Otto,K.の「Volumetric modulated arc therapy: IMRT in a single gantry arc」、Med Phys Vol.35、2008年、310〜317頁に記載されている。
【0006】
[0006]VMATは一部、マルチリーフコリメータ(MLC)リーフ動作および線量率調整を用いてビーム出力強度を変調することを伴う。加えて、VMATは、治療時間が低減されるように治療用放射線を継続してオンにした状態で、ガントリおよび線形加速器のコリメータを1つまたは複数の完全な円弧または部分円弧を回転させることによって、変調された出力強度のビームを送達する。ガントリの回転中に、i)MLC開口形状,ii)フルエンス出力率(「線量率」)、iii)ガントリ回転速度、およびiv)MLCの向きなど、いくつかのパラメータを動的に変えることができる。パラメータi)〜iv)を変えることが可能なことにより、VMATは、多くの円弧を用いる必要性を低減し、それによって、IMRTに匹敵する線量測定を与えながら、より少ないモニタユニット(MU)に短時間で送達することができる。VMATは、上述の4つの使用可能な可変パラメータを利用できるが、最大ガントリ速度、最大リーフ速度、MLCの向きの制約、およびフルエンス出力率の使用可能な再分割など、線形加速器およびMLCの物理的制約を考慮しながら利用しなければならない。
【0007】
[0007]すべての機械パラメータ、特に機械と患者の向きを治療施行中に動的に制御しなければ、現在のVMAT技術は特定の治療部位に関し制約される。乳ガン治療の場合では、体内乳房結節照射により左側乳ガンを治療するのに適用されるVMATにより、低線量(5Gy)照射を受ける肺、心臓および反対側の乳房の体積が、変形ワイド接線と比較して増大することが示された。本来、その構成により、乳房照射に使用されるVMATは、心臓、肺および反対側の乳房に向けられたビームを含む。
【0008】
[0008]VMATシステムの別の短所は、同時kV撮像と一体化されていないことである。したがって、このようなVMATシステムはリアルタイムの治療検証をすることができない。
【発明の概要】
【0009】
[0009]本発明の一態様は放射線治療システムに関し、このシステムは、対象物のまわりを移動し治療用放射線のビームを対象物に向けて送る放射線源と、対象物のまわりを移動し撮像放射線のビームを対象物に向けて送る撮像源とを含む。システムはさらに、対象物が上に配置され、平行移動可動および回転可動である台を含む。システムはまた、1)治療用放射線源で発生された、対象物を透過する放射線を受け取り第1の画像情報を形成する第1の撮像装置と、2)撮像源で発生された、対象物を透過する放射線を受け取り第2の画像情報を形成する第2の撮像装置とを含み、第1の画像情報と第2の画像情報は同時に形成される。システムはさらに、放射線源、台、第1の撮像装置および第2の撮像装置と通信するコンピュータを備え、このコンピュータは、台の動きと、放射線源の以下のパラメータ、すなわち放射線源の動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、第1の画像情報および第2の画像情報に基づいて同時に制御する。
【0010】
[0010]本発明の第2の態様は、放射線を供給する方法に関し、この方法は、治療用放射線のビームを対象物に向けて送るステップと、撮像放射線のビームを対象物に向けて送るステップとを含む。この方法は、平行移動可動および回転可動である台の上に対象物を配置するステップを含む。この方法はまた、対象物を透過する治療用放射線のビームに基づいて対象物の第1の画像情報を形成するステップと、対象物を透過する撮像放射線のビームに基づいて対象物の第2の画像情報を形成するステップとを含み、第1の画像情報と第2の画像情報は同時に形成される。この方法はさらに、台の動きと、治療用放射線のビームの以下のパラメータ、すなわち治療用放射線のビームの動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、第1の画像情報および第2の画像情報に基づいて同時に制御するステップを含む。
【0011】
[0011]本発明の1つまたは複数の態様は、規定するモニタユニットが少なく、使用する制御点が少ないという利点をもたらす。
[0012]本発明の1つまたは複数の態様は、毒性および二次性悪性腫瘍の危険性を低減する。
【図面の簡単な説明】
【0012】
【図1】[0013]本発明によるC−ARC治療を実施できる放射線治療システムの一実施形態を示す図である。
【図2】[0014]本発明による図1の放射線治療システムを動作させる実行可能な一方法の流れ図である。
【図3】[0015]本発明による同時kV/MV撮像のシステムを概略的に示す図である。
【図4A】[0016]定位放射線照射(SRS)治療での90°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4B】定位放射線照射(SRS)治療での135°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4C】定位放射線照射(SRS)治療での180°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図4D】定位放射線照射(SRS)治療での270°のガントリ位置におけるビーム方向像(BEV)による参照デジタル再構成放射線透過(DRR)画像である。
【図5A】[0017]定位放射線照射治療での90°のガントリ位置におけるkVおよびMVポータル画像である。
【図5B】定位放射線照射治療での135°のガントリ位置におけるkVおよびMVポータル画像である。
【図5C】定位放射線照射治療での180°のガントリ位置におけるkVおよびMVポータル画像である。
【図5D】定位放射線照射治療での270°のガントリ位置におけるkVおよびMVポータル画像である。
【図6】[0018]図6Aは、本発明による乳腺腫瘍治療での実現可能なビーム構成の体外図である。[0019]図6Bは、既知の乳腺腫瘍治療計画でのビーム構成の体外図である。図6Cは、既知の乳腺腫瘍治療計画でのビーム構成の体外図である。
【図7】[0020]図7Aは、図6Aの乳腺腫瘍治療でのビーム構成の体内図である。[0021]図7Bは、図6Bの乳腺腫瘍治療でのビーム構成の体内図である。図7Cは、図6Cの乳腺腫瘍治療でのビーム構成の体内図である。
【図8】[0022]図8Aは、本発明による治療計画と比較した様々な既知の治療計画の、線量に対する同側乳房%体積のグラフである。 [0023]図8Bは、本発明による治療計画と比較した様々な既知の治療計画の、線量に対する同側肺%体積のグラフである。
【図9】[0024]図9Aは、本発明による乳腺腫瘍の治療計画での代表的な軸方向線量分布を示す画像である。[0025]図9Bは、VMAT治療計画での代表的な軸方向線量分布を示す画像である。
【発明を実施するための形態】
【0013】
[0026]図1を見ると、放射線治療システム100が示されており、これは、コーンビームコンピュータ断層撮影システム102などの撮像システムと、医療用線源または加速器104などの治療用放射線源とを含むことができる。コンピュータ断層撮影システム102は、X線源106と、ガントリ110に装着されたフラットパネル撮像装置108とを含む。コンピュータ断層撮影システム102の詳細は、参照によりそれぞれの開示全体が本明細書に組み込まれる米国特許第6,842,502号、および第7,471,765号に記載されている。もちろん、C形アーム支持コーンビームシステムおよびプロトン撮像システムなど、他のタイプの撮像システムも本発明の趣旨から逸脱することなく使用可能である。
【0014】
[0027]システム102は、既存または新規の放射線治療システム112に後付けされ、システム112は医療用線源104など、ヒト患者などの目標体積の治療が可能なレベルで動作する別個の治療用放射線源を含む。医療用線源104は、光子、陽子または電子などの、4MeVから25MeVの範囲のエネルギーを有するX線または粒子のビームを発生する。実際には、医療用線源104は、本発明の趣旨から逸脱することなく、患者の放射線治療に使用される他の放射線源と置き換えることもできる。放射線治療システム112はさらに、ユニットとして可動でリーフを含むマルチリーフコリメータ(MLC)113を含み、このリーフは、治療ビームが患者を透過するように開口を画定するために可動である。放射線治療システム112はまた、医療用線源104と一直線に合わされている撮像装置(図示せず)を含み、これらの間に患者が入る。
【0015】
[0028]患者を支持し、治療用放射線ビームを当てることを支援するために、コンピュータ制御治療台114が設けられる。台114は、図1に概略的に示されたコンピュータ116などのコンピュータによって制御される。台114は、患者をx、yおよびz方向に平行移動させること、ならびにx、yおよびz軸を中心に回転させることを可能にする。さらに、治療台114は、コンピュータ断層撮影画像に著しく障害を与えないように高周波半透過性材料で構成されることが好ましい。台114には、参照によりそれぞれの内容全体が本明細書に組み込まれる米国特許第6,842,502号および第7,471,765号、ならびに米国特許出願公開第US2010−0119032A1号に開示されているものなど、多くの形状がありうる。
【0016】
[0029]図1のシステム100は、本発明によるC−ARC治療用放射線の治療計画を実行するようにコンピュータ116によって制御される。特にC−ARCは、VMATのように、変調ビーム開口および線量率を回転送達と組み合わせることを伴う。VMATと対照的に、C−ARCでは、送達回転の代替モダリティを導入する。特に、台または治療台114は、対象の領域への治療用放射線施行を制御するために、平行移動および/または回転によって移動する。台114の平行移動は、図1に示されたx、yおよびz方向のうちの1つ以上で可能であることに注意されたい。加えて、台114の回転は、x、yおよびz方向のうちの1つ以上を中心にして可能である。台114の回転中、ガントリ110の輪118もまた、脳などの特定の治療部位については同時に回転することができる。
【0017】
[0030]台114が動いている間、開口形状およびMLC113の向きは動的に変えることができる。加えて、フルエンス出力率(「線量率」)およびガントリ回転速度を変えることができ、したがって放射線源104の回転速度を変えることができる。台の動き、ガントリの動き、フルエンス出力率、MLCの向き、およびMLCの形状の制御は、コンピュータ116によって行われる。コンピュータ116を制御するために使用されるソフトウェアは、VMATで使用されるソフトウェアと類似でよく、C−ARC用のソフトウェアは、台114、ガントリ110とその付属品、および患者の間でのいかなる衝突も回避しながら、臨床的に許容可能な線量測定が生じるようなものである。システム100についての上記の説明を念頭において、システム100を動作させる実行可能な方法を図2の流れ図に関して本明細書で説明する。具体的には、方法200が概略的に示されており、この方法は、手順210でまず、腫瘍などの治療の対象物を含むことが分かっている患者の部位のコンピュータ断層撮影または他の3次元計画画像を形成することを伴う。画像の計画は離れたところで、またはその場でコンピュータ断層撮影システム102を使用して行うことができる。次に、健康な組織への放射線量を低減しながら所望の治療線量を腫瘍に当てるために台の動き、ガントリの動き、フルエンス出力率、MLCの向き、MLCの形状を変える手順220で、腫瘍の全体的領域の画像の3次元情報がコンピュータ116または他のコンピュータに供給されて、仮想3次元放射線治療計画が計算される。
【0018】
[0031]仮想計画が計算された後、この計画に従って次には患者を放射線で治療することができる。これに関して、仮想計画では、腫瘍が手順210で撮像されたときと同じ空間位置にあるものと想定することに留意されたい。手順230で患者が台114に配置されると、手順240で腫瘍の空間位置を、その腫瘍が手順210で2つのやり方のうちの1つで撮像されたときと同じになるように微調整することができる。空間位置を微調整する1つのやり方は、患者の皮膚マーカが手順210で撮像されたときにあった位置と同じ位置に見えるようになるまで技術者に患者の位置を変えさせることである。微調整の第2のやり方は、コンピュータ断層撮影システム102を使用して腫瘍の3次元像を撮影し、この微調整画像中に表示される腫瘍の位置が変わって手順210で決定された腫瘍の位置と一致するように患者の位置を調整することである。手順240で患者の位置が変わると、次に手順250で、手順220の仮想計画が腫瘍に適用される。
【0019】
[0032]上述の微調整手順の他に、米国特許第6,842,502号および7,471,765号に記載されているリアルタイムのやり方で、C−ARC計画を使用する治療を実施できることに注意されたい。このリアルタイムのやり方では、腫瘍のリアルタイム撮像が放射線治療中に行われ、この腫瘍のリアルタイム画像は、台の動き、ガントリの動き、フルエンス出力率、MLCの向き、およびMLCの形状を制御するためにコンピュータで使用される。
【0020】
[0033]上述のリアルタイムC−ARC治療の一例が図3に概略的に示されている。具体的には、kVコーンビームが台114上の患者に向けられて通り抜け、3次元リアルタイム画像がフラットパネル画像装置108で生成される。加えて、MVポータル画像もまた同時に使用されて、画像装置120に対向して配置されている線源104(図示せず)から放出された治療放射線に基づいて、患者のリアルタイム2次元画像が生成される。治療用放射線施行中の、kVコーンビーム投影撮像およびMVポータル撮像の両方によるこのような同時リアルタイム撮像は、ビーム患者方向においてVMATおよびC−ARCの回転機能を利用することによって可能になる。MVポータル撮像の投影画像およびkVコーンビーム投影撮像の投影画像をそれぞれ処理して、放射線治療中に患者/生体構造位置の動き/変化をリアルタイムで監視するための2次元検証画像および3次元検証画像を得ることができる。
【0021】
[0034]上述のkVコーンビームおよびMV画像装置によって様々なガントリ回転位置で形成されたkVポータル画像およびMVポータル画像の、脊柱の部位が治療されている例が図5A〜Dに示されている。対応するビーム方向像による参照デジタル再構成放射線透過画像が図4A〜Dに示されている(ビーム方向内および開口内の対象物を表す)。
【0022】
[0035]C−ARC治療計画についての上述の説明と共に、他の既知の治療計画との比較で本発明の利点を示す。加速部分乳房照射(APBI)による乳房内腫瘍の治療の場合では、台114が1つの中間円弧および1つの横方向円弧を回転している間、ガントリ110は接線角で制止したままであり、これらの中間および横方向円弧は、患者の乳房の向きに対して規定される。
【0023】
[0036]問題の乳房が3D−CRT計画によって以前に治療されている場合には、3D−CRTのビーム構成はC−ARC計画を案内するのに使用することができる。というのは、それが台、ガントリおよび患者の間でのいかなる衝突も回避しながら臨床的に許容可能な線量測定を与えていると考えられるからである。3D−CRT計画による台の位置は、台円弧の限界と解釈される。同様に、各円弧に対するガントリ位置は、3D−CRT計画の位置と同じになるように選択される。最適化および線量計算は、円弧に沿って10°間隔で配置された制御点について行われる。このような乳房治療は、3D−CRTで扱われるAPBIの標準接線ビーム構成の利益を維持する。C−ARCは、乳房放射線治療の領域に対するVMATの無理のない拡張であり、標準接線ビーム形状により目標の外側の線量が最少になる。これは図6Aおよび図7Aに示されており、C−ARCを使用する放射ビームはほとんどが乳房に向けられ、心臓および肺などの健康な臓器には放射がほとんど影響を及ぼさない。対照的に、IMRTおよびVMATを用いて適用されるAPBIでは、図6B〜Cおよび図7B〜Cに示されるように、健康な組織にビームが向けられることになりうる。
【0024】
[0037]以下の比較では、以前に3D−CRTによってAPBIで治療された患者に関し、それに続く追加の3つの計画、すなわち1)C−ARC計画、2)IMRT計画、および3)VMAT計画が、患者ごとに生成された。評価に使用されたDVHパラメータは、乳房治療のNSABP−B39/RTOG 0413プロトコルの正常組織制約条件からほとんど選ばれ、次の表1に一覧表示されている。
【0025】
【表1】

【0026】
[0038]上の表1は、C−ARC、IMRTおよびVMAT計画の正常組織線量の平均値を一覧表示しており、そのすべてが当初の3D−CRT計画と比較されている。3つすべての治療計画モダリティで正常同側乳房組織V50%の体積が著しく低下し、この値は平均で7.8%低下している(図8A参照)。図示のように、3つすべての計画で同側肺V30%が著しく低下するが、V5GyについてはC−ARCおよびIMRT計画だけがそのように低下する(図8B参照)。反対側肺V5%では著しい低下がない。4つのVMAT計画は、反対側乳房に不可避の高いDmaxを発生し、このDmaxは3D−CRT計画も、NSABP B−39/RTOG 0413プロトコルに略述されている正常組織線量制約条件(表1)も超える。IMRTおよびC−ARC計画のどれもこのような違反を引き起こさない。C−ARC、IMRTおよびVMAT計画はすべて、3D−CRTと比較してモニタユニットの数を低減し、C−ARC計画がMUの最少平均数を規定する(平均減少 IMRT 136MU、p=0.013、VMAT 281MU、p<0.001、C−ARC 339MU、p<0.001)。
【0027】
[0039]C−ARCとVMATもまた比較されている。これら2つの計画モダリティは、規定線量の50%および100%を受ける同側乳房ならびに規定線量の30%を受ける同側肺の体積の比較に値する低減をもたらす。しかし、VMAT計画では、かなり大きい同側肺体積が5Gyを受けることになり(10.4%対7.8%、p=0.008)、かなり大きい心臓体積が192.5cGyを受けることになる(7.7%対5.5%、p=0.021)。図9A〜Bは、C−ARCおよびVMATそれぞれの代表的な軸方向線量分布を示す。同様に、かなり少ない数のモニタユニットが規定されたC−ARCはVMAT計画(p=0.011)と似ていた。重要でない傾向(p=0.05)が、反対側乳房に低いDmaxを送達するC−ARC計画から現れた。
【0028】
[0040]同側乳房への線量を低減することに加えて、C−ARC計画は、肺および心臓への線量を低減する。C−ARCおよびIMRTは、正面を向いた幾何学的配置がないので、V5Gyで測定された同側肺照射の最大の低減をもたらした。C−ARCおよびIMRT計画はまた、心臓の低線量照射の顕著な低減をもたらした。
【0029】
[0041]ウェッジがないことにより、C−ARC、IMRTおよびVMAT計画ではすべて、規定されたモニタユニットの数が3D−CRT計画と比較して低減し、C−ARC計画が最大の低減をもたらした。C−ARC計画はまた、最小数の制御点を使用し、それによって漏洩放射線が最小限になる。
【0030】
[0042]表1に示されるように、C−ARC計画は、肺、心臓、および反対側乳房への線量を増大させることなく、同側乳房照射の顕著な低減をもたらす。VMAT計画もまた、同側乳房への照射線量を低減することができるが、これは、他のところで線量増大を代償にすることがより多くありうる。
【0031】
[0043]VMAT、C−ARCの無理のない拡張は、快適さの改善、モニタユニットの送達低減、治療時間の短縮が期待される治療を可能にする。C−ARCは、治療計画者および操作員の視点からは、既存の回転放射線治療より著しく複雑なものではない。この革新が行われるためには、治療台回転制御を線量率およびマルチリーフコリメータの動作と連結することが必要になる。VMAT計画ソフトウェアの小修正にはまた、治療台円弧を組み込むことが必要とされる。
【0032】
[0044]APBI C−ARC治療の場合では、ガントリ110は、台114が動いている間静止している。C−ARC治療が、台114とガントリ110が同時に動くことを伴いうる場合がある。この一例は、部分脳放射線治療が用いられる場合である。台114およびガントリ110の動きにより、視交叉、視神経および脳幹を含む健康な部位に当たる治療用放射線の量を加減する。実際には、IMRTと比較してC−ARC治療では、視交叉、視神経および脳幹に対し用いる平均および最大照射線量が低減される。
【0033】
[0045]上記の説明から、当業者は、本発明の本質的特徴を容易に確認することができ、また本発明の趣旨および範囲から逸脱することなく、本発明の様々な変更および/または修正を行って様々な使用法および状況に本発明を適合させることができる。
【特許請求の範囲】
【請求項1】
対象物のまわりを移動し、前記対象物に治療用放射線のビームを向けて送る放射線源と、
前記対象物のまわりを移動し、前記対象物に撮像放射線のビームを向けて送る撮像源と、
前記対象物が上に配置され、平行移動可動および回転可動である台と、
前記治療用放射線源で発生された、前記対象物を透過する放射線を受け取り第1の画像情報を形成する第1の撮像装置と、
前記撮像源で発生された、前記対象物を透過する放射線を受け取り第2の画像情報を形成する第2の撮像装置であって、前記第1の画像情報と前記第2の画像情報が同時に形成される第2の撮像装置と、
前記放射線源、前記台、前記第1の撮像装置および前記第2の撮像装置と通信するコンピュータとを備える放射線治療システムであって、前記コンピュータが前記台の動きと、前記放射線源の以下のパラメータ、すなわち放射線源の動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて同時に制御する、放射線治療システム。
【請求項2】
前記放射線源から前記対象物に向けられた前記ビームが通る開口を画定する複数の可動リーフを含むマルチリーフコリメータをさらに備え、前記コンピュータが、マルチリーフコリメータの向きおよび前記開口の形状をリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて制御する、請求項1に記載のシステム。
【請求項3】
前記治療用放射線のビームが光子を含み、前記撮像放射線のビームがkV X線を含む、請求項2に記載のシステム。
【請求項4】
前記治療用放射線のビームが粒子を含み、前記撮像放射線のビームがkV X線を含む、請求項2に記載のシステム。
【請求項5】
前記粒子が電子および陽子からなる群から選択される、請求項4に記載のシステム。
【請求項6】
前記対象物が腫瘍である、請求項1に記載のシステム。
【請求項7】
治療用放射線のビームを対象物に向けて送るステップと、
撮像放射線のビームを前記対象物に向けて送るステップと、
平行移動可動および回転可動である台の上に対象物を配置するステップと、
前記対象物を透過する前記治療用放射線のビームに基づいて前記対象物の第1の画像情報を形成するステップと、
前記対象物を透過する前記撮像放射線のビームに基づいて前記対象物の第2の画像情報を形成するステップであって、前記第1の画像情報と前記第2の画像情報が同時に形成されるステップと、
前記台の動きと、前記治療用放射線のビームの以下のパラメータ、すなわち治療用放射線のビームの動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて同時に制御するステップとを含む、放射線を供給する方法。
【請求項8】
前記同時に制御するステップがさらに、前記治療用放射線のビームのパラメータ形状を制御するステップを含む、請求項7に記載の方法。
【請求項9】
前記治療用放射線のビームが光子を含み、前記撮像放射線のビームがkV X線を含む、請求項7に記載の方法。
【請求項10】
前記治療用放射線のビームが粒子を含み、前記撮像放射線のビームがkV X線を含む、請求項7に記載の方法。
【請求項11】
前記粒子が電子および陽子からなる群から選択される、請求項10に記載の方法。
【請求項12】
前記対象物が腫瘍である、請求項7に記載の方法。
【請求項1】
対象物のまわりを移動し、前記対象物に治療用放射線のビームを向けて送る放射線源と、
前記対象物のまわりを移動し、前記対象物に撮像放射線のビームを向けて送る撮像源と、
前記対象物が上に配置され、平行移動可動および回転可動である台と、
前記治療用放射線源で発生された、前記対象物を透過する放射線を受け取り第1の画像情報を形成する第1の撮像装置と、
前記撮像源で発生された、前記対象物を透過する放射線を受け取り第2の画像情報を形成する第2の撮像装置であって、前記第1の画像情報と前記第2の画像情報が同時に形成される第2の撮像装置と、
前記放射線源、前記台、前記第1の撮像装置および前記第2の撮像装置と通信するコンピュータとを備える放射線治療システムであって、前記コンピュータが前記台の動きと、前記放射線源の以下のパラメータ、すなわち放射線源の動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて同時に制御する、放射線治療システム。
【請求項2】
前記放射線源から前記対象物に向けられた前記ビームが通る開口を画定する複数の可動リーフを含むマルチリーフコリメータをさらに備え、前記コンピュータが、マルチリーフコリメータの向きおよび前記開口の形状をリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて制御する、請求項1に記載のシステム。
【請求項3】
前記治療用放射線のビームが光子を含み、前記撮像放射線のビームがkV X線を含む、請求項2に記載のシステム。
【請求項4】
前記治療用放射線のビームが粒子を含み、前記撮像放射線のビームがkV X線を含む、請求項2に記載のシステム。
【請求項5】
前記粒子が電子および陽子からなる群から選択される、請求項4に記載のシステム。
【請求項6】
前記対象物が腫瘍である、請求項1に記載のシステム。
【請求項7】
治療用放射線のビームを対象物に向けて送るステップと、
撮像放射線のビームを前記対象物に向けて送るステップと、
平行移動可動および回転可動である台の上に対象物を配置するステップと、
前記対象物を透過する前記治療用放射線のビームに基づいて前記対象物の第1の画像情報を形成するステップと、
前記対象物を透過する前記撮像放射線のビームに基づいて前記対象物の第2の画像情報を形成するステップであって、前記第1の画像情報と前記第2の画像情報が同時に形成されるステップと、
前記台の動きと、前記治療用放射線のビームの以下のパラメータ、すなわち治療用放射線のビームの動きおよびフルエンス出力率のうちの1つ以上とをリアルタイムで、前記第1の画像情報および前記第2の画像情報に基づいて同時に制御するステップとを含む、放射線を供給する方法。
【請求項8】
前記同時に制御するステップがさらに、前記治療用放射線のビームのパラメータ形状を制御するステップを含む、請求項7に記載の方法。
【請求項9】
前記治療用放射線のビームが光子を含み、前記撮像放射線のビームがkV X線を含む、請求項7に記載の方法。
【請求項10】
前記治療用放射線のビームが粒子を含み、前記撮像放射線のビームがkV X線を含む、請求項7に記載の方法。
【請求項11】
前記粒子が電子および陽子からなる群から選択される、請求項10に記載の方法。
【請求項12】
前記対象物が腫瘍である、請求項7に記載の方法。
【図1】


【図2】


【図3】


【図4A】


【図4B】


【図4C】


【図4D】


【図5A】


【図5B】


【図5C】


【図5D】


【図6A−7C】


【図8】


【図9】




【図2】


【図3】


【図4A】


【図4B】


【図4C】


【図4D】


【図5A】


【図5B】


【図5C】


【図5D】


【図6A−7C】


【図8】


【図9】


【公表番号】特表2013−516278(P2013−516278A)
【公表日】平成25年5月13日(2013.5.13)
【国際特許分類】
【出願番号】特願2012−548050(P2012−548050)
【出願日】平成23年1月4日(2011.1.4)
【国際出願番号】PCT/US2011/000006
【国際公開番号】WO2011/084878
【国際公開日】平成23年7月14日(2011.7.14)
【出願人】(596047609)
【氏名又は名称原語表記】WILLIAM BEAUMONT HOSPITAL
【住所又は居所原語表記】3601 WEST THIRTEEN MILE ROAD, ROYAL OAK, MICHIGAN 48072,UNITED STATES OF AMERICA
【Fターム(参考)】
【公表日】平成25年5月13日(2013.5.13)
【国際特許分類】
【出願日】平成23年1月4日(2011.1.4)
【国際出願番号】PCT/US2011/000006
【国際公開番号】WO2011/084878
【国際公開日】平成23年7月14日(2011.7.14)
【出願人】(596047609)

【氏名又は名称原語表記】WILLIAM BEAUMONT HOSPITAL
【住所又は居所原語表記】3601 WEST THIRTEEN MILE ROAD, ROYAL OAK, MICHIGAN 48072,UNITED STATES OF AMERICA
【Fターム(参考)】
[ Back to top ]

