過塩素酸塩の製造装置および製造方法
【課題】過塩素酸の製造に際して原材料の調達安定性を高めることができる過塩素酸塩の製造装置および製造方法の提供。
【解決手段】陽極4が設けられる陽極側4Aと陰極5が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて塩化ナトリウム水溶液を電解酸化する電解槽1と、陽極側4AにおけるpHを計測するpH計12と、pH計12の計測結果に基づいて、電解槽1の陽極側4Aに水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の陽極側4AにおけるpHを調節するpH調節装置15と、を有する過塩素酸アンモニウム製造装置Aを採用する。
【解決手段】陽極4が設けられる陽極側4Aと陰極5が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて塩化ナトリウム水溶液を電解酸化する電解槽1と、陽極側4AにおけるpHを計測するpH計12と、pH計12の計測結果に基づいて、電解槽1の陽極側4Aに水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の陽極側4AにおけるpHを調節するpH調節装置15と、を有する過塩素酸アンモニウム製造装置Aを採用する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、過塩素酸塩の製造装置および製造方法に関するものである。
【背景技術】
【0002】
過塩素酸塩は、固体燃料ロケットの推進薬の酸化剤(過塩素酸アンモニウム)を始め、リチウムイオン電池の支持電解質(過塩素酸リチウム)やエアバックの着火剤(過塩素酸カリウム)など、様々な用途に利用されている。
ここで、過塩素酸塩の製造方法としては、非特許文献1に詳しく記述されているように、工業的には塩化ナトリウム水溶液の電解酸化により合成した塩素酸ナトリウム水溶液を更に電解酸化して過塩素酸ナトリウムを合成した後、所定の処理を経て製造される。そこで、これまでの従来技術では、例えば特許文献1や特許文献2に記載に記載されているように、過塩素酸ナトリウム(NaClO4)水溶液を効率的に電解合成するための方法に焦点が当てられてきた。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開平3−199387号公報
【特許文献2】特開2007−197740号公報
【非特許文献】
【0004】
【非特許文献1】J. C. Schumacher(ed.), Perchlorates, A.C.S.Monograph No.146, Reinhold, New York, 1960
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかし、過塩素酸ナトリウム以外の過塩素酸塩を製造するにあたり、必ずしも過塩素酸ナトリウムを経由する必要は無い。そこで、本願発明者らは、過塩素酸ナトリウムの製造を経由しないで製造工程を簡略化した過塩素酸塩の製造方法を考案した。この製造方法では、陽極が設けられる陽極側と陰極が設けられる陰極側とを陽イオン交換膜で仕切った電解槽を用い、塩素酸ナトリウム水溶液を陽極側で電解酸化して過塩素酸水溶液を生成し、この電解酸化で生成した過塩素酸水溶液に所定のアルカリ性水溶液を加えて、中和反応により過塩素酸塩を合成する。
しかし、この製造方法においては、塩素酸ナトリウムを原材料としているために、その原材料の調達安定性に課題がある。
【0006】
本発明は、上記課題に鑑みてなされたものであり、過塩素酸の製造に際して原材料の調達安定性を高めることができる過塩素酸塩の製造装置および製造方法の提供を目的とする。
【課題を解決するための手段】
【0007】
上記の課題を解決するために、本発明は、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られ、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する電解槽と、上記電解槽での電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する合成槽と、上記電解槽の陽極側におけるpHを計測するpH計と、 上記pH計の計測結果に基づいて、上記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、上記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、上記電解酸化時の上記陽極側におけるpHを調節するpH調節装置と、を有する過塩素酸塩の製造装置を採用する。
【0008】
また、本発明においては、上記電解槽での電解酸化により上記陽極で発生した酸素ガスの量を計測する酸素ガス量計測装置と、上記電解槽での電解酸化における電流量を計測する電流量計測装置と、上記酸素ガス量計測装置の計測結果と上記電流量計測装置の計測結果とに基づいて、上記電解槽での電解酸化に伴って上記陽極側において生成される次亜塩素酸及び亜塩素酸の生成量を計測する計測装置と、を有するという構成を採用する。
【0009】
そして、本発明においては、上記pH調節装置は、上記次亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを調節するという構成を採用する。
具体的に、本発明における上記pH調節装置は、上記次亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを5.0以上に調節するという構成を採用する。
【0010】
加えて、本発明においては、上記pH調節装置は、上記次亜塩素酸の生成量に基づく調節の後、上記亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを調節するという構成を採用する。
具体的に、本発明における上記pH調節装置は、上記亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを2.3以上に調節するという構成を採用する。
【0011】
さらに、本発明においては、上記pH調節装置は、上記計測装置の計測結果に基づいて、上記次亜塩素酸の生成量に基づく調節と上記亜塩素酸の生成量に基づく調節との切り替えを行うという構成を採用する。
【0012】
また、本発明においては、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用い、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する工程と、上記電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する工程と、上記電解槽の陽極側におけるpHを計測する工程と、上記pHの計測結果に基づいて、上記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、上記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、上記電解酸化時の上記陽極側におけるpHを調節する工程と、を有する過塩素酸塩の製造方法を採用する。
【発明の効果】
【0013】
本発明によれば、塩素酸ナトリウムよりも入手容易な塩化ナトリウムを、原材料として用いることにより、原材料の調達安定性が高まり、しいては過塩素酸塩を安定して供給することができる。
また、本発明は、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用いて、陽極側で塩化ナトリウム水溶液を電解酸化すると、塩化ナトリウム水溶液中のナトリウムイオン(Na+)が陽極側から陽イオン交換膜を通過して陰極側に移動し、一方、塩化ナトリウム水溶液中の塩化物イオン(Cl−)は陽イオン交換膜を通過できずに陽極側に留まり、その陽極側での電解酸化により次亜塩素酸、亜塩素酸を経て、塩素酸が生成される。なお、塩素ガス、若しくは二酸化塩素ガスは、塩素酸が生成する過程において陽極側水溶液が強酸性となることにより生じるが、陽極側のpHを制御することにより、これらのガスの発生を防止することができる。
【0014】
電解槽での電解酸化に伴いナトリウムイオンが陽極側から陰極側へと陽イオン交換膜を介して移動し、陽極側は徐々に強酸性に変化する。その結果、陽極側水溶液のpHの制御を実施しない場合には、生成した次亜塩素酸及び亜塩素酸が塩素ガス、そして二酸化塩素ガスとして系外へと放出される。その結果、塩素酸を生成する過程においてその塩素酸の収率の低下が懸念される。そこで、本発明は、pH計を用いて陽極側のpHを計測し、その計測結果に基づいて、アルカリ性の水酸化ナトリウム水溶液を添加して陽極側のpHを調節することにより、塩素酸の収率の低下を防止する。なお、電解酸化により陰極で生成される水酸化ナトリウムを陽極側水溶液のpH調節に用いると、水酸化ナトリウムを別途準備する必要がないため、なお良い。
【0015】
本発明のpH調節は、先ず、電解槽の陽極側のpHを5.0以上に調節することで、塩素ガスの発生を防止して亜塩素酸の収率を高める。これは、電解槽の陽極側のpHが5.0未満の酸性値になると、次亜塩素酸の存在状態が変化して塩素ガス(Cl2)が発生し、系外に排出されてしまうためである。
次に、本発明のpH調節は、電解槽の陽極側のpHを2.3以上に調節することで、二酸化塩素ガスの発生を防止して塩素酸の収率を高める。これは、電解槽の陽極側のpHが2.3未満の酸性値になると、亜塩素酸が二酸化塩素ガス(ClO2)として系外に排出されてしまうためである。
【0016】
また、本発明では、電解槽での電解酸化に伴って上記陽極側において、次亜塩素酸の酸化により生成される亜塩素酸の生成量に基づいて、電解槽の陽極側のpH調節を5.0以上から2.3以上に切り替える。これは、過塩素酸塩(過塩素酸ナトリウム以外)を製造するにあたり、その純度を高めるためには、電解酸化後の陽極側水溶液中のナトリウムイオンは少ないこと、すなわちpHは小さいことが望ましいことによる。従って、次亜塩素酸が電解酸化され亜塩素酸が生成した場合、陽極側のpHが2.3以上であれば、二酸化塩素ガスが発生することはない。そこで、電解槽での電解酸化に伴い次亜塩素酸が電解酸化され亜塩素酸が生成した後は、陽極側のpHを2.3以上に調節することが、後の工程で有益である。
通常、次亜塩素酸及び亜塩素酸の生成量を計測する方法として、液体イオンクロマトグラフィーが用いられる。しかし、その分析には、時間と手間がかかる。一方、本発明では、電解槽での電解酸化により陽極で発生した酸素ガスの量と、この電解酸化における電流量とに基づいて、次亜塩素酸及び亜塩素酸の生成量をモニタリングすることにより、適切なタイミングで陽極側水溶液のpH調節の切り替えを行うことができる。この結果、連続的に電解工程を実施することが可能となる。
【図面の簡単な説明】
【0017】
【図1】本発明の実施形態における過塩素酸アンモニウムの製造工程を示すフロー図である。
【図2】本発明の実施形態における過塩素酸アンモニウム製造装置の概略構成図である。
【図3】本発明の実施形態における一次電解槽の構成図である。
【図4】次亜塩素酸水溶液の存在状態とpHとの関係を示す図である。
【図5】亜塩素酸水溶液の存在状態とpHとの関係を示す図である。
【図6】本発明の実施形態における二次電解槽の構成図である。
【発明を実施するための形態】
【0018】
以下、本発明の実施形態の過塩素酸塩の製造装置および製造方法について図面を参照して説明する。なお、ここでは、本発明を過塩素酸アンモニウムの製造装置および製造方法に適用した場合の例について説明する。
【0019】
図1は、本発明の実施形態における過塩素酸アンモニウムの製造工程を示すフロー図である。図に示すように、本発明の過塩素酸アンモニウムの製造工程は、大きく分けて、一次電解工程S1、二次電解工程S2、反応工程S3、晶析工程S4の4つの工程からなる。
一次電解工程S1は、塩化ナトリウム水溶液を電解酸化し、塩素酸を主成分とする水溶液を生成する工程である。次の二次電解工程S2は、一次電解工程S1により生成した塩素酸を主成分とする水溶液を電解酸化し、過塩素酸水溶液を生成する工程である。その次の反応工程S3は、二次電解工程S2により生成した過塩素酸水溶液にアンモニア水溶液を添加して中和反応により過塩素酸アンモニウムを合成する工程である。最後の晶析工程S4は、中和反応後の水溶液を真空、高温環境下において蒸発させ、濃縮した水溶液を冷却することにより過塩素酸アンモニウムを晶析させる工程である。
【0020】
続いて、この製造工程を実施する過塩素酸アンモニウム製造装置について説明する。
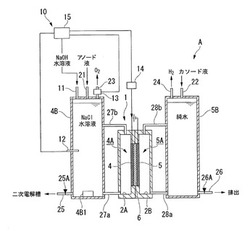
図2は、本発明の実施形態における過塩素酸アンモニウム製造装置(過塩素酸塩の製造装置)Aの概略構成図である。図中のg、l、sの符号は、それぞれ気体、液体、固体の状態であることを示す。実施形態の過塩素酸アンモニウム製造装置Aは、一次電解工程S1を行う一次電解槽(電解槽)1と、二次電解工程S2を行う二次電解槽(電解槽)2と、反応工程S3及び晶析工程S4を行う反応・蒸発槽3とを備えている。
【0021】
図3は、本発明の実施形態における一次電解槽1の構成図である。
一次電解槽1は、陽極4が設けられる陽極側4Aと、陰極5が設けられる陰極側5Aとを仕切るように設けられた陽イオン交換膜6を有する。一次電解槽1は、後述する電解酸化により、陽極側溶液(アノード液)が強酸性に、陰極側溶液(カソード液)が強アルカリ性となる。そこで、一次電解槽1の本体には、耐化学薬品安定性に優れたもの、例えばテフロン(デュポン(株)、登録商標)や塩化ビニル、ガラスを使用することが望ましい。また、配管の継ぎ手についても、耐化学薬品安定性に優れたもの、例えばテフロン(デュポン(株)、登録商標)を用いることが望ましい。
【0022】
陽イオン交換膜6は一次電解槽1内で陽極4と陰極5との間にギャップ無しで挟みこまれたゼロギャップ型の電解セルを構成する。この陽イオン交換膜6は、陽イオンは通過でき、陰イオンは通過できないという特性を有する膜であり、本実施形態では、陽イオン交換膜6にナフィオン424(Nafion、デュポン(株)、登録商標)を用いる。なお、陽イオン交換膜としては、苛性ソーダ製造に広く用いられているAciplex(旭化成(株)、登録商標)やFlemion(旭硝子(株)、登録商標)を用いても良い。
【0023】
陽極4は、陽極側4Aにおける塩素酸イオンの電解合成反応の促進を図るために、触媒を被覆したエキスパンドメタルからなる。本実施形態の陽極4は、基体であるチタンエキスパンドメタルの表面を、酸素ガスの発生を抑制する効果のある、焼成法により酸化イリジウム及び白金からなる触媒層で被覆した電極、あるいは、焼成法により酸化イリジウム及び酸化ルテニウムからなる触媒層で被覆した電極、あるいは、焼成法により酸化イリジウム及び酸化ルテニウム及び白金からなる触媒層で被覆した電極、あるいは、焼成法により酸化タンタル及び白金からなる触媒層で被覆した電極から構成される。
一方、この陽極4と対となる陰極5は、基体であるチタンエキスパンドメタルの表面を電解メッキにより白金の触媒層で被覆した電極、または、ニッケルエキスパンドメタルからなる電極から構成される。
【0024】
陽極側4Aには、アノード液を貯溜するアノード液タンク4Bが設けられている(以下、電解槽1の陽極側4Aを陽極側電解槽2Aと称する)。アノード液タンク4Bにおけるアノード液の液面は、陽極側電解槽2A内の液面よりも高くなっている。アノード液タンク4Bと陽極側電解槽2Aとは、配管27a及び配管27bで接続されている。配管27aは、陽極側電解槽2Aの底部とアノード液タンク4Bの底部とを接続するものであり、配管27bは、陽極側電解槽2Aの天部とアノード液タンク4Bの側部とを接続するものである。なお、アノード液タンク4Bの底部には、アノード液の濃度を均一に保つための超音波振動子4B1を設ける。アノード液の濃度を均一に保つための方法としては、アノード液タンク4B内部に攪拌機を設けても良い。
【0025】
一方、陰極側5Aには、カソード液を貯溜するカソード液タンク5Bが設けられる(以下、電解槽1の陰極側5Aを陰極側電解槽2Bと称する)。カソード液タンク5Bにおけるカソード液の液面は、陰極側電解槽2B内の液面よりも高くなっている。カソード液タンク5Bと陰極側電解槽2Bとは、配管28a及び配管28bで接続されている。配管28aは、陰極側電解槽2Bの底部とカソード液タンク5Bの底部とを接続するものであり、配管28bは、陰極側電解槽2Bの天部とカソード液タンク5Bの側部とを接続するものである。
【0026】
アノード液タンク4Bの天部にはアノード液導入配管21が接続されており、塩化ナトリウム水溶液がアノード液導入配管21を介して導入され、陽極側4A(陽極側電解槽2A、アノード液タンク4Bを含む)を満たす。一方、カソード液タンク5Bの天部にはカソード液導入配管22が接続されており、純水がカソード液導入配管22を介して導入され、陰極側5A(陰極側電解槽2B、カソード液タンク5Bを含む)を満たす。一次電解槽1の内部で各液にそれぞれ浸された陽極4及び陰極5の両極に電圧を印加すると、次の反応が進行する。
【0027】
陽極側4Aにおいては、塩化ナトリウム水溶液が電解酸化され、下記の反応式(1)、反応式(2)に示す反応が生じる。
2Cl− → Cl2+2e− …(1)
2H2O → O2+4H++4e− …(2)
ここで発生した塩素ガスにより、下記の反応式(3)、反応式(4)に示す平衡反応が生じる。この平衡反応は、水溶液のpHによりその形態が変化する。
Cl2+H2O ⇔ H++Cl−+HClO …(3)
HClO ⇔ H++ClO− …(4)
【0028】
この反応で生じた次亜塩素酸を電解酸化すると、下記の反応式(5)、反応式(6)に示す反応により亜塩素酸が生成される。
ClO−+H2O → ClO2−+2H++2e− …(5)
HClO+H2O → HClO2+2H++2e− …(6)
生成された亜塩素酸を更に電解酸化すると、下記の反応式(7)、反応式(8)に示す反応により塩素酸が生成される。
ClO2−+H2O → ClO3−+2H++2e− …(7)
HClO2+H2O → HClO3+2H++2e− …(8)
【0029】
上記反応式(1)〜反応式(8)に示すように、一次電解工程では、塩素酸と副生成物として酸素ガスが生成される。従って、消費電力抑制の観点から、上記の酸化インジウムを触媒として含む被覆チタンエキスパンドメタルを陽極4として用いることにより、酸素ガスの発生を抑制することが望ましい。
ここで、陽極側4Aの液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。一方、次亜塩素酸イオンは陽イオン交換膜6を通過できず、水溶液‐陽極4‐陽イオン交換膜6で構成される三界面での酸化反応により亜塩素酸イオンを経て塩素酸イオンとなる。
【0030】
なお、陽極側電解槽2Aで生じた酸素ガス(気泡)は、配管27bを介してアノード液タンク4Bに導かれる。アノード液タンク4Bの天部には酸素ガス配管23が設けられており、酸素ガス配管23を介して酸素ガスが外部に順次排気される。
また、陽極側電解槽2Aの底部からは、液面の差(水圧差)により配管27aを介してアノード液タンク4Bからアノード液が順次導入されるため、電解酸化されたアノード液は、陽極側電解槽2Aから、配管27bを介してアノード液タンク4B側に押し出される。従って、アノード液はポンプ等の駆動機構によらずに陽極側電解槽2Aとアノード液タンク4Bとの間で循環するため、より多くのアノード液が陽極側電解槽2Aで電解酸化される。
【0031】
陰極側5Aにおいては、下記の反応式(9)、反応式(10)に示す反応が生じ、水素ガスと水酸化ナトリウムとが生成される。
2H++2e− → H2 …(9)
2Na++2H2O+2e− → 2NaOH+H2 …(10)
なお、陰極側電解槽2Bで生じた水素ガス(気泡)は、配管28bを介してカソード液タンク5Bに導かれる。カソード液タンク5Bの天部には水素ガス配管24が設けられており、水素ガス配管24を介して水素ガスが外部に順次排気される。また、陽極側4Aにおいてアノード液が循環することと同様に、陰極側5Aにおいても、カソード液の循環作用が得られる。
【0032】
上記電解酸化により、陽極側4Aの液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。このことは、アノード液が強酸性へと変化する一因となる。そして、電解酸化に伴いアノード液が強酸性となると、塩素ガス、二酸化塩素ガスが発生する。その結果として、塩素酸の収率の低下が生じる。そこで、本実施形態では、塩素ガス、二酸化塩素ガスの発生防止を目的とした、電解酸化時の陽極側4AにおけるpHを調節するpH調節システム10を備える。
【0033】
pH調節システム10は、アノード液タンク4Bの天部に接続されたpH調節剤導入配管11からアノード液にpH調節剤を添加するものであり、アノード液タンク4Bの側部に設けられてアノード液のpHを計測するpH計12と、酸素ガス配管23に設けられ、電解酸化により陽極4で発生した酸素ガスの量を計測する流量計(酸素ガス量計測装置)13と、電解酸化に用いた電流量を計測する電流計(電流量計測装置)14と、それらの計測結果に基づき、pH調節剤導入配管11からpH調節剤として水酸化ナトリウム水溶液をアノード液タンク4B内に添加するpH調節装置15とを有する。
【0034】
pH調節装置15は、pH計12と、流量計13と、電流計14と電気的に接続されており、各々から計測結果のデータが入力され、該データに基づいてpH調節剤の添加量を制御するコンピューターシステム(計測装置)を有する。具体的に、pH調節装置15は、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節プログラムと、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節プログラムと、これらの調節プログラムを陽極側4Aにおいて生成される亜塩素酸の生成量に基づいて切り替えるプログラムとをメモリに記憶しており、これらのプログラムに基づき一次電解槽1の陽極側4AのpH調節を行う構成となっている。
【0035】
先ず、図4を参照して、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節について説明する。
図4は、次亜塩素酸水溶液の存在状態とpHとの関係を示す図である。図4において、横軸はpHを、縦軸は存在比率を示す。
図4に示すように、一次電解槽1での電解酸化に伴い次亜塩素酸を主成分とするアノード液のpHが5未満の酸性値になると、次亜塩素酸が塩素ガス(Cl2)として酸素ガス配管23を介して外部へと排出していくこととなる。その結果、一次電解工程の最終生成物である塩素酸の収率は低下する。
そこで、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節プログラムにおいては、図4に示すデータに基づいて、塩素ガスの生じない、pHが5以上となるように、該アノード液に水酸化ナトリウム水溶液を添加する制御を行う。
【0036】
次に、図5を参照して、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節について説明する。
図5は、亜塩素酸水溶液の存在状態とpHとの関係を示す図(出典:食品安全委員会、添加物評価書、亜塩素酸水、2008年6月)である。図5において、横軸はpHを、縦軸は存在比率を示す。
図5に示すように、一次電解槽1での電解酸化に伴い亜塩素酸を主成分とするアノード液のpHが2.3未満の酸性値になると、亜塩素酸の存在状態が変化して二酸化塩素ガス(ClO2)として存在することとなる。その結果、上記塩素ガスの発生と同様に二酸化塩素ガスは酸素ガス配管23を介して外部へと排出されるため、一次電解工程の最終生成物である塩素酸の収率は低下する。
そこで、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節プログラムにおいては、図5に示すデータに基づいて、二酸化塩素ガスの生じない、pHが2.3以上となるように、該アノード液に水酸化ナトリウム水溶液を添加する制御を行う。
【0037】
過塩素酸アンモニウムを製造するにあたり、その純度を高めるためには、ナトリウムイオンは少ないことが望ましい。ここで、次亜塩素酸の電解酸化により亜塩素酸が生成した場合、陽極側4AのpHが2.3以上であれば、二酸化塩素ガスが発生することはない。従って、一次電解槽1での電解酸化に伴い次亜塩素酸が亜塩素酸に全て転化した後は、陽極側4AのpHの制御値を5.0以上から2.3以上へと切り替えることが、後の工程で有益である。そこで、本実施形態のpH調節装置15は、流量計13及び電流計14の計測結果に基づいて、次亜塩素酸及び亜塩素酸の生成量を推定し、陽極側4AのpHの制御値を5.0以上から2.3以上へと切り替えるプログラムを備える。pH調節装置15は、以下に説明する演算式に基づいて次亜塩素酸及び亜塩素酸の生成量を推定する。
【0038】
先ず、塩化ナトリウム水溶液の電解酸化により次亜塩素酸、亜塩素酸、塩素酸を生成する際に必要となる電子の数について説明する。反応式(1)〜反応式(8)に示したように、塩化ナトリウムを水に1mol溶解した塩化ナトリウム水溶液を電解酸化して、次亜塩素酸を1mol生成するためには、2molの電子が必要となる。更に、次亜塩素酸から亜塩素酸を1mol生成するためには2molの電子が必要となる。従って、出発原料である塩化ナトリウム水溶液から亜塩素酸を1mol生成するためには、4molの電子が必要となる。そして、出発原料である塩化ナトリウム水溶液から塩素酸を1mol生成するためには、6molの電子が必要となる。
なお、現実には、反応式(1)〜反応式(8)に示す反応の他に、陽極4の触媒として白金を用いた場合は、その白金が塩化白金酸イオン(PtCl42−)として水溶液中に溶出する反応が生じる。また、1.0A/cm2以上の高い電流密度で電気分解を実施した際には、オゾン(O3)が生成し得る。しかし、これらの反応により生じる生成物は、反応式(1)〜反応式(8)に示す反応により生じる生成物と比較して十分に少ない。従って、ここでは、これらの反応は無視する。
【0039】
電流量と酸素ガスの発生量から次亜塩素酸、亜塩素酸、塩素酸の生成量を推定するにあたり、電流I(A)でt時間(単位は秒)通電した際の酸素ガスの発生量をPO2(単位はリットル(L))とする。ここで標準状態(0℃、1気圧)を仮定した場合、PO2/22.4(mol)の酸素ガスが発生したこととなり、酸素ガスの発生に伴い、陽極4から陰極5へと移動した電子の数eO2(mol)は、PO2/22.4の4倍となる。一方、陽極4から陰極5へと移動した全電子数etotal(mol)は、ファラデー定数F(=9.6485×104C/mol)を用いて、下記の数式(a)で表すことができる。
【0040】
【数1】

【0041】
従って、次亜塩素酸の生成に伴い、陽極4から陰極5へと移動した電子の数は、下記の数式(b)で表すことができる。
【0042】
【数2】

【0043】
結論として、次亜塩素酸の生成量PHClOは、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(c)で推定できる。ここで、κHClOは、HClOの式量であり、52.46(g/mol)である。
【0044】
【数3】

【0045】
同様にして、亜塩素酸の生成量PHClO2は、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(d)で推定できる。ここで、κHClO2は、HClO2の式量であり、68.46(g/mol)である。
【0046】
【数4】

【0047】
更に、塩素酸の生成量PHClO3は、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(e)で推定できる。ここで、κHClO3は、HClO3の式量であり、84.46(g/mol)である。
【0048】
【数5】

【0049】
従って、pH調節装置15は、一次電解槽1での電解酸化時において、先ず、塩素ガスの発生の防止を目的に、陽極側4Aのアノード液のpHを5以上に調節する。そして、pH調節装置15は、数式(d)に示す演算式に基づき、次亜塩素酸が亜塩素酸へと転換したと推定できる段階で、陽極側4Aのアノード液のpHを2.3以上に調節する。このようにして、pH調節装置15は、塩素ガスの発生、二酸化塩素ガスの発生を防止し、収率を高めると共に、ナトリウムイオンを可能な限り陰極側5Aに移動させる。
【0050】
一次電解槽1での電解酸化により、生成された塩素酸を主成分とするアノード液は、弁25Aを閉状態から開状態にしたアノード液輸送配管25を介してアノード液タンク4Bから二次電解槽2に輸送される。一方、カソード液は、弁26Aを閉状態から開状態にしたカソード液輸送配管26を介してカソード液タンク5Bから外部に輸送される。
【0051】
図6は、本発明の実施形態における二次電解槽2の構成図である。
二次電解槽2は、一次電解槽1で生成した塩素酸を主成分とするアノード液を電解酸化して過塩素酸を生成する。
なお、以下説明する二次電解槽2の構成は、重複説明を避けるため、上述の一次電解槽1と同一又は同等の構成部分については同一の符号を付し、その説明を簡略若しくは省略する。
【0052】
二次電解槽2において、陽イオン交換膜6は陽極4´と陰極5´との間にギャップ無しで挟みこまれたゼロギャップ型の電解セルを構成する。
陽極4´は、陽極側4Aにおける過塩素酸イオンの電解合成反応の促進を図るために、触媒を被覆したエキスパンドメタルからなる。この陽極4´は、基体であるチタンエキスパンドメタルの表面を、電解メッキにより白金の触媒層で被覆した電極から構成される。
一方、この陽極4´と対となる陰極5´は、触媒を被覆したエキスパンドメタルからなる。この陰極5´は、基体であるチタンエキスパンドメタルの表面を、電解メッキにより白金の触媒層で被覆した電極、または、SUS316エキスパンドメタルからなる電極、または、ニッケルエキスパンドメタルからなる電極から構成される。
【0053】
二次電解槽2のアノード液タンク4Bの天部にはアノード液導入配管として、一次電解槽1のアノード液輸送配管25が接続されており、一次電解工程を経たアノード液がアノード液輸送配管25を介して導入され、陽極側4A(陽極側電解槽2A、アノード液タンク4Bを含む)を満たす。一方、カソード液タンク5Bの天部にはカソード液導入配管22が接続されており、純水がカソード液導入配管22を介して導入され、陰極側5A(陰極側電解槽2B、カソード液タンク5Bを含む)を満たす。二次電解槽2の内部で各液にそれぞれ浸された陽極4´及び陰極5´の両極に電圧を印加すると、次の反応が進行する。
【0054】
陽極側4Aにおいては、一次電解工程を経たアノード液が電解酸化され、下記の反応式(11)、反応式(12)に示すように、過塩素酸と副生成物として酸素ガスが生成される。なお、微量ではあるが、下記の反応式(13)に示すように、オゾンガスも副生成物として生成される。
HClO3+H2O → HClO4+2H++2e− …(11)
2H2O → O2+4H++4e− …(12)
3H2O → O3+6H++6e− …(13)
ここで、陽極側4Aの一次電解工程を経た後にアノード液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。一方、塩素酸イオンは陽イオン交換膜6を通過できず、水溶液‐陽極4´‐陽イオン交換膜6で構成される三界面で反応式(11)に示す酸化反応により過塩素酸となる。
【0055】
陰極側5Aにおいては、下記の反応式(14)、反応式(15)に示す反応が生じ、水素ガスと水酸化ナトリウムとが生成される。
2H++2e− → H2 …(14)
2Na++2H2O+2e− → 2NaOH+H2 …(15)
十分な量の過塩素酸が生成されたアノード液は、弁25Aを閉状態から開状態にしたアノード液輸送配管25´を介してアノード液タンク4Bから反応・蒸発槽3に輸送される。一方、カソード液は、弁26Aを閉状態から開状態にしたカソード液輸送配管26を介してカソード液タンク5Bから外部に輸送される。
【0056】
反応・蒸発槽3では、電解酸化後のアノード液中にアンモニア水溶液を添加して過塩素酸アンモニウムを合成する工程と、合成後のアノード液を真空、高温環境下で蒸発させて過塩素酸アンモニウムを晶析させる工程とを行う。なお、ここでアンモニア水溶液の代わりにアンモニアガスをバブリングしてもよい。
反応・蒸発槽3には、アンモニア供給配管31が接続されており、電解酸化後のアノード液中にアンモニア水溶液を供給する構成となっている。電解酸化後のアノード液中にアンモニア水溶液を添加すると、下記の反応式(16)に示す中和反応が生じ、目的物である過塩素酸アンモニウムと副生成物として水が合成される。
HClO4+NH4OH → NH4ClO4+H2O …(16)
【0057】
次に、反応・蒸発槽3において、合成後のアノード液を真空、高温環境下で蒸発させ、濃縮した水溶液を冷却することにより過塩素酸アンモニウムを結晶として取り出す。反応式(16)に示すように、過塩素酸アンモニウムと共に得られる副生成物は水であるため、非特許文献1に記載の方法と比較して、高純度の過塩素酸アンモニウムの結晶が容易に得られる。
【0058】
以上のように、本実施形態によれば、陽極4が設けられる陽極側4Aと陰極5が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて塩化ナトリウム水溶液を電解酸化して、塩素酸を主成分とする水溶液を生成する一次電解槽1と、陽極4´が設けられる陽極側4Aと陰極5´が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて一次電解槽1での電解酸化により生成した塩素酸を主成分とする水溶液を電解酸化して、過塩素酸水溶液を生成する二次電解槽2と、二次電解槽2での電解酸化により生成した過塩素酸水溶液に、アンモニアを添加して、中和反応により過塩素酸アンモニウムを合成する反応・蒸発槽3と、を有する過塩素酸アンモニウム製造装置Aを採用することにより、塩素酸ナトリウムよりも低価で入手容易な塩化ナトリウムを、原材料として用いることで、原材料の調達安定性が高まり、過塩素酸アンモニウムを安定して製造することができる。
【0059】
また、一次電解槽1での電解酸化に伴い陽極側4Aは強酸性に変化する。その結果、次亜塩素酸の存在状態の変化によって生じる塩素ガスや、亜塩素酸の存在状態の変化によって生じる二酸化塩素ガスが一次電解槽1の系外に排出されるため、中間生成物である塩素酸の収率の低下が懸念される。そこで、本実施形態では、pH計12を用いて陽極側4AのpHを計測し、その計測結果に基づいて、アルカリ性の水酸化ナトリウム水溶液を添加して陽極側4AのpHを調節し、塩素酸の収率の低下を防止する。ここで添加する水酸化ナトリウム水溶液は、この電解酸化により陰極側5Aで生成される副生成物を用いると、原材料である水酸化ナトリウムを調達する必要がなくなる。
【0060】
本実施形態のpH調節では、先ず、一次電解工程において、塩素ガスの発生の防止を目的としたpH調節を行う。一次電解槽1の次亜塩素酸を主成分とするアノード液のpHが5未満になると、塩素ガスが発生して系外に排出されるため、pHを5以上に調節することで、塩素ガスの発生を防止して塩素酸の収率を高めることができる。
本実施形態のpH調節は、次に、一次電解工程において、二酸化塩素ガスの発生の防止を目的としたpH調節を行う。一次電解槽1の亜塩素酸を主成分とするアノード液のpHが2.3未満になると、亜塩素酸の存在状態が変化して二酸化塩素ガスとして系外に排出されるため、pHを2.3以上に調節することで、二酸化塩素ガスの発生を防止し、塩素酸の収率を高めることができる。
【0061】
また、本実施形態では、上記塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節と上記二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節とを、次亜塩素酸及び亜塩素酸の生成量に基づいて切り替える。過塩素酸アンモニウムを製造するにあたり、その純度を高めるためには、ナトリウムイオンは少ないことが望ましい。従って、次亜塩素酸の電解酸化により亜塩素酸が生成した場合、陽極側4AのpHが2.3以上であれば、二酸化塩素ガスが発生することはない。そこで、一次電解槽1での電解酸化に伴い亜塩素酸が所定量生成された後は、陽極側4AのpHを2.3以上に調節することが、後の工程で有益である。
通常、次亜塩素酸及び亜塩素酸の生成量を計測するには液体イオンクロマトグラフィーが用いられる。しかし、その分析には、時間と手間がかかるため、本実施形態では、一次電解槽1での電解酸化により陽極4で発生した酸素ガスの量と、この電解酸化における電流量とに基づいて、次亜塩素酸及び亜塩素酸、塩素酸の生成量をモニタリングすることにより、適切なタイミングで陽極側4AのpH調整の切り替えを行うことができる。
【0062】
以上、図面を参照しながら本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。上述した実施形態において示した各構成部材の諸形状や組み合わせ等は一例であって、本発明の主旨から逸脱しない範囲において設計要求等に基づき種々変更可能である。
【0063】
例えば、本発明は、上述した過塩素酸アンモニウムの製造装置への適用に限定されるものではなく、過塩素酸リチウムや過塩素酸カリウム等のアルカリ金属過塩素酸塩の製造装置、過塩素酸カルシウム等のアルカリ土類金属過塩素酸塩の製造装置、また、過塩素酸銀の製造装置等にも適用可能である。
【0064】
また、例えば、本発明は、上述した一次電解槽と二次電解槽の2つの電解槽を用いて過塩素酸水溶液を生成する形態だけでなく、1つの電解槽で過塩素酸水溶液を生成する形態や3つ以上の複数の電解槽で過塩素酸水溶液を生成する形態にも適用可能である。また、電解槽については、ゼロギャップ型のみならず、陽イオン交換膜を陽極と陰極との間にスペースを設けて設置した電解槽を用いても良い。
【符号の説明】
【0065】
A…過塩素酸アンモニウム製造装置(過塩素酸塩の製造装置)、S1…一次電解工程、…、S2…二次電解工程、S3…反応工程(合成工程)、S4…晶析工程、1…一次電解槽(電解槽)、2…二次電解槽(電解槽)、3…反応・蒸発槽、4…陽極、4´…陽極、4A…陽極側、5…陰極、5´…陰極、5A…陰極側、6…陽イオン交換膜、10…pH調節システム、11…pH調節剤導入管、12…pH計、13…流量計(酸素ガス量計測装置)、14…電流計(電流量計測装置)、15…pH調節装置
【技術分野】
【0001】
本発明は、過塩素酸塩の製造装置および製造方法に関するものである。
【背景技術】
【0002】
過塩素酸塩は、固体燃料ロケットの推進薬の酸化剤(過塩素酸アンモニウム)を始め、リチウムイオン電池の支持電解質(過塩素酸リチウム)やエアバックの着火剤(過塩素酸カリウム)など、様々な用途に利用されている。
ここで、過塩素酸塩の製造方法としては、非特許文献1に詳しく記述されているように、工業的には塩化ナトリウム水溶液の電解酸化により合成した塩素酸ナトリウム水溶液を更に電解酸化して過塩素酸ナトリウムを合成した後、所定の処理を経て製造される。そこで、これまでの従来技術では、例えば特許文献1や特許文献2に記載に記載されているように、過塩素酸ナトリウム(NaClO4)水溶液を効率的に電解合成するための方法に焦点が当てられてきた。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開平3−199387号公報
【特許文献2】特開2007−197740号公報
【非特許文献】
【0004】
【非特許文献1】J. C. Schumacher(ed.), Perchlorates, A.C.S.Monograph No.146, Reinhold, New York, 1960
【発明の概要】
【発明が解決しようとする課題】
【0005】
しかし、過塩素酸ナトリウム以外の過塩素酸塩を製造するにあたり、必ずしも過塩素酸ナトリウムを経由する必要は無い。そこで、本願発明者らは、過塩素酸ナトリウムの製造を経由しないで製造工程を簡略化した過塩素酸塩の製造方法を考案した。この製造方法では、陽極が設けられる陽極側と陰極が設けられる陰極側とを陽イオン交換膜で仕切った電解槽を用い、塩素酸ナトリウム水溶液を陽極側で電解酸化して過塩素酸水溶液を生成し、この電解酸化で生成した過塩素酸水溶液に所定のアルカリ性水溶液を加えて、中和反応により過塩素酸塩を合成する。
しかし、この製造方法においては、塩素酸ナトリウムを原材料としているために、その原材料の調達安定性に課題がある。
【0006】
本発明は、上記課題に鑑みてなされたものであり、過塩素酸の製造に際して原材料の調達安定性を高めることができる過塩素酸塩の製造装置および製造方法の提供を目的とする。
【課題を解決するための手段】
【0007】
上記の課題を解決するために、本発明は、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られ、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する電解槽と、上記電解槽での電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する合成槽と、上記電解槽の陽極側におけるpHを計測するpH計と、 上記pH計の計測結果に基づいて、上記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、上記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、上記電解酸化時の上記陽極側におけるpHを調節するpH調節装置と、を有する過塩素酸塩の製造装置を採用する。
【0008】
また、本発明においては、上記電解槽での電解酸化により上記陽極で発生した酸素ガスの量を計測する酸素ガス量計測装置と、上記電解槽での電解酸化における電流量を計測する電流量計測装置と、上記酸素ガス量計測装置の計測結果と上記電流量計測装置の計測結果とに基づいて、上記電解槽での電解酸化に伴って上記陽極側において生成される次亜塩素酸及び亜塩素酸の生成量を計測する計測装置と、を有するという構成を採用する。
【0009】
そして、本発明においては、上記pH調節装置は、上記次亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを調節するという構成を採用する。
具体的に、本発明における上記pH調節装置は、上記次亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを5.0以上に調節するという構成を採用する。
【0010】
加えて、本発明においては、上記pH調節装置は、上記次亜塩素酸の生成量に基づく調節の後、上記亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを調節するという構成を採用する。
具体的に、本発明における上記pH調節装置は、上記亜塩素酸の生成量に基づいて、上記電解酸化時の上記陽極側におけるpHを2.3以上に調節するという構成を採用する。
【0011】
さらに、本発明においては、上記pH調節装置は、上記計測装置の計測結果に基づいて、上記次亜塩素酸の生成量に基づく調節と上記亜塩素酸の生成量に基づく調節との切り替えを行うという構成を採用する。
【0012】
また、本発明においては、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用い、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する工程と、上記電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する工程と、上記電解槽の陽極側におけるpHを計測する工程と、上記pHの計測結果に基づいて、上記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、上記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、上記電解酸化時の上記陽極側におけるpHを調節する工程と、を有する過塩素酸塩の製造方法を採用する。
【発明の効果】
【0013】
本発明によれば、塩素酸ナトリウムよりも入手容易な塩化ナトリウムを、原材料として用いることにより、原材料の調達安定性が高まり、しいては過塩素酸塩を安定して供給することができる。
また、本発明は、陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用いて、陽極側で塩化ナトリウム水溶液を電解酸化すると、塩化ナトリウム水溶液中のナトリウムイオン(Na+)が陽極側から陽イオン交換膜を通過して陰極側に移動し、一方、塩化ナトリウム水溶液中の塩化物イオン(Cl−)は陽イオン交換膜を通過できずに陽極側に留まり、その陽極側での電解酸化により次亜塩素酸、亜塩素酸を経て、塩素酸が生成される。なお、塩素ガス、若しくは二酸化塩素ガスは、塩素酸が生成する過程において陽極側水溶液が強酸性となることにより生じるが、陽極側のpHを制御することにより、これらのガスの発生を防止することができる。
【0014】
電解槽での電解酸化に伴いナトリウムイオンが陽極側から陰極側へと陽イオン交換膜を介して移動し、陽極側は徐々に強酸性に変化する。その結果、陽極側水溶液のpHの制御を実施しない場合には、生成した次亜塩素酸及び亜塩素酸が塩素ガス、そして二酸化塩素ガスとして系外へと放出される。その結果、塩素酸を生成する過程においてその塩素酸の収率の低下が懸念される。そこで、本発明は、pH計を用いて陽極側のpHを計測し、その計測結果に基づいて、アルカリ性の水酸化ナトリウム水溶液を添加して陽極側のpHを調節することにより、塩素酸の収率の低下を防止する。なお、電解酸化により陰極で生成される水酸化ナトリウムを陽極側水溶液のpH調節に用いると、水酸化ナトリウムを別途準備する必要がないため、なお良い。
【0015】
本発明のpH調節は、先ず、電解槽の陽極側のpHを5.0以上に調節することで、塩素ガスの発生を防止して亜塩素酸の収率を高める。これは、電解槽の陽極側のpHが5.0未満の酸性値になると、次亜塩素酸の存在状態が変化して塩素ガス(Cl2)が発生し、系外に排出されてしまうためである。
次に、本発明のpH調節は、電解槽の陽極側のpHを2.3以上に調節することで、二酸化塩素ガスの発生を防止して塩素酸の収率を高める。これは、電解槽の陽極側のpHが2.3未満の酸性値になると、亜塩素酸が二酸化塩素ガス(ClO2)として系外に排出されてしまうためである。
【0016】
また、本発明では、電解槽での電解酸化に伴って上記陽極側において、次亜塩素酸の酸化により生成される亜塩素酸の生成量に基づいて、電解槽の陽極側のpH調節を5.0以上から2.3以上に切り替える。これは、過塩素酸塩(過塩素酸ナトリウム以外)を製造するにあたり、その純度を高めるためには、電解酸化後の陽極側水溶液中のナトリウムイオンは少ないこと、すなわちpHは小さいことが望ましいことによる。従って、次亜塩素酸が電解酸化され亜塩素酸が生成した場合、陽極側のpHが2.3以上であれば、二酸化塩素ガスが発生することはない。そこで、電解槽での電解酸化に伴い次亜塩素酸が電解酸化され亜塩素酸が生成した後は、陽極側のpHを2.3以上に調節することが、後の工程で有益である。
通常、次亜塩素酸及び亜塩素酸の生成量を計測する方法として、液体イオンクロマトグラフィーが用いられる。しかし、その分析には、時間と手間がかかる。一方、本発明では、電解槽での電解酸化により陽極で発生した酸素ガスの量と、この電解酸化における電流量とに基づいて、次亜塩素酸及び亜塩素酸の生成量をモニタリングすることにより、適切なタイミングで陽極側水溶液のpH調節の切り替えを行うことができる。この結果、連続的に電解工程を実施することが可能となる。
【図面の簡単な説明】
【0017】
【図1】本発明の実施形態における過塩素酸アンモニウムの製造工程を示すフロー図である。
【図2】本発明の実施形態における過塩素酸アンモニウム製造装置の概略構成図である。
【図3】本発明の実施形態における一次電解槽の構成図である。
【図4】次亜塩素酸水溶液の存在状態とpHとの関係を示す図である。
【図5】亜塩素酸水溶液の存在状態とpHとの関係を示す図である。
【図6】本発明の実施形態における二次電解槽の構成図である。
【発明を実施するための形態】
【0018】
以下、本発明の実施形態の過塩素酸塩の製造装置および製造方法について図面を参照して説明する。なお、ここでは、本発明を過塩素酸アンモニウムの製造装置および製造方法に適用した場合の例について説明する。
【0019】
図1は、本発明の実施形態における過塩素酸アンモニウムの製造工程を示すフロー図である。図に示すように、本発明の過塩素酸アンモニウムの製造工程は、大きく分けて、一次電解工程S1、二次電解工程S2、反応工程S3、晶析工程S4の4つの工程からなる。
一次電解工程S1は、塩化ナトリウム水溶液を電解酸化し、塩素酸を主成分とする水溶液を生成する工程である。次の二次電解工程S2は、一次電解工程S1により生成した塩素酸を主成分とする水溶液を電解酸化し、過塩素酸水溶液を生成する工程である。その次の反応工程S3は、二次電解工程S2により生成した過塩素酸水溶液にアンモニア水溶液を添加して中和反応により過塩素酸アンモニウムを合成する工程である。最後の晶析工程S4は、中和反応後の水溶液を真空、高温環境下において蒸発させ、濃縮した水溶液を冷却することにより過塩素酸アンモニウムを晶析させる工程である。
【0020】
続いて、この製造工程を実施する過塩素酸アンモニウム製造装置について説明する。
図2は、本発明の実施形態における過塩素酸アンモニウム製造装置(過塩素酸塩の製造装置)Aの概略構成図である。図中のg、l、sの符号は、それぞれ気体、液体、固体の状態であることを示す。実施形態の過塩素酸アンモニウム製造装置Aは、一次電解工程S1を行う一次電解槽(電解槽)1と、二次電解工程S2を行う二次電解槽(電解槽)2と、反応工程S3及び晶析工程S4を行う反応・蒸発槽3とを備えている。
【0021】
図3は、本発明の実施形態における一次電解槽1の構成図である。
一次電解槽1は、陽極4が設けられる陽極側4Aと、陰極5が設けられる陰極側5Aとを仕切るように設けられた陽イオン交換膜6を有する。一次電解槽1は、後述する電解酸化により、陽極側溶液(アノード液)が強酸性に、陰極側溶液(カソード液)が強アルカリ性となる。そこで、一次電解槽1の本体には、耐化学薬品安定性に優れたもの、例えばテフロン(デュポン(株)、登録商標)や塩化ビニル、ガラスを使用することが望ましい。また、配管の継ぎ手についても、耐化学薬品安定性に優れたもの、例えばテフロン(デュポン(株)、登録商標)を用いることが望ましい。
【0022】
陽イオン交換膜6は一次電解槽1内で陽極4と陰極5との間にギャップ無しで挟みこまれたゼロギャップ型の電解セルを構成する。この陽イオン交換膜6は、陽イオンは通過でき、陰イオンは通過できないという特性を有する膜であり、本実施形態では、陽イオン交換膜6にナフィオン424(Nafion、デュポン(株)、登録商標)を用いる。なお、陽イオン交換膜としては、苛性ソーダ製造に広く用いられているAciplex(旭化成(株)、登録商標)やFlemion(旭硝子(株)、登録商標)を用いても良い。
【0023】
陽極4は、陽極側4Aにおける塩素酸イオンの電解合成反応の促進を図るために、触媒を被覆したエキスパンドメタルからなる。本実施形態の陽極4は、基体であるチタンエキスパンドメタルの表面を、酸素ガスの発生を抑制する効果のある、焼成法により酸化イリジウム及び白金からなる触媒層で被覆した電極、あるいは、焼成法により酸化イリジウム及び酸化ルテニウムからなる触媒層で被覆した電極、あるいは、焼成法により酸化イリジウム及び酸化ルテニウム及び白金からなる触媒層で被覆した電極、あるいは、焼成法により酸化タンタル及び白金からなる触媒層で被覆した電極から構成される。
一方、この陽極4と対となる陰極5は、基体であるチタンエキスパンドメタルの表面を電解メッキにより白金の触媒層で被覆した電極、または、ニッケルエキスパンドメタルからなる電極から構成される。
【0024】
陽極側4Aには、アノード液を貯溜するアノード液タンク4Bが設けられている(以下、電解槽1の陽極側4Aを陽極側電解槽2Aと称する)。アノード液タンク4Bにおけるアノード液の液面は、陽極側電解槽2A内の液面よりも高くなっている。アノード液タンク4Bと陽極側電解槽2Aとは、配管27a及び配管27bで接続されている。配管27aは、陽極側電解槽2Aの底部とアノード液タンク4Bの底部とを接続するものであり、配管27bは、陽極側電解槽2Aの天部とアノード液タンク4Bの側部とを接続するものである。なお、アノード液タンク4Bの底部には、アノード液の濃度を均一に保つための超音波振動子4B1を設ける。アノード液の濃度を均一に保つための方法としては、アノード液タンク4B内部に攪拌機を設けても良い。
【0025】
一方、陰極側5Aには、カソード液を貯溜するカソード液タンク5Bが設けられる(以下、電解槽1の陰極側5Aを陰極側電解槽2Bと称する)。カソード液タンク5Bにおけるカソード液の液面は、陰極側電解槽2B内の液面よりも高くなっている。カソード液タンク5Bと陰極側電解槽2Bとは、配管28a及び配管28bで接続されている。配管28aは、陰極側電解槽2Bの底部とカソード液タンク5Bの底部とを接続するものであり、配管28bは、陰極側電解槽2Bの天部とカソード液タンク5Bの側部とを接続するものである。
【0026】
アノード液タンク4Bの天部にはアノード液導入配管21が接続されており、塩化ナトリウム水溶液がアノード液導入配管21を介して導入され、陽極側4A(陽極側電解槽2A、アノード液タンク4Bを含む)を満たす。一方、カソード液タンク5Bの天部にはカソード液導入配管22が接続されており、純水がカソード液導入配管22を介して導入され、陰極側5A(陰極側電解槽2B、カソード液タンク5Bを含む)を満たす。一次電解槽1の内部で各液にそれぞれ浸された陽極4及び陰極5の両極に電圧を印加すると、次の反応が進行する。
【0027】
陽極側4Aにおいては、塩化ナトリウム水溶液が電解酸化され、下記の反応式(1)、反応式(2)に示す反応が生じる。
2Cl− → Cl2+2e− …(1)
2H2O → O2+4H++4e− …(2)
ここで発生した塩素ガスにより、下記の反応式(3)、反応式(4)に示す平衡反応が生じる。この平衡反応は、水溶液のpHによりその形態が変化する。
Cl2+H2O ⇔ H++Cl−+HClO …(3)
HClO ⇔ H++ClO− …(4)
【0028】
この反応で生じた次亜塩素酸を電解酸化すると、下記の反応式(5)、反応式(6)に示す反応により亜塩素酸が生成される。
ClO−+H2O → ClO2−+2H++2e− …(5)
HClO+H2O → HClO2+2H++2e− …(6)
生成された亜塩素酸を更に電解酸化すると、下記の反応式(7)、反応式(8)に示す反応により塩素酸が生成される。
ClO2−+H2O → ClO3−+2H++2e− …(7)
HClO2+H2O → HClO3+2H++2e− …(8)
【0029】
上記反応式(1)〜反応式(8)に示すように、一次電解工程では、塩素酸と副生成物として酸素ガスが生成される。従って、消費電力抑制の観点から、上記の酸化インジウムを触媒として含む被覆チタンエキスパンドメタルを陽極4として用いることにより、酸素ガスの発生を抑制することが望ましい。
ここで、陽極側4Aの液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。一方、次亜塩素酸イオンは陽イオン交換膜6を通過できず、水溶液‐陽極4‐陽イオン交換膜6で構成される三界面での酸化反応により亜塩素酸イオンを経て塩素酸イオンとなる。
【0030】
なお、陽極側電解槽2Aで生じた酸素ガス(気泡)は、配管27bを介してアノード液タンク4Bに導かれる。アノード液タンク4Bの天部には酸素ガス配管23が設けられており、酸素ガス配管23を介して酸素ガスが外部に順次排気される。
また、陽極側電解槽2Aの底部からは、液面の差(水圧差)により配管27aを介してアノード液タンク4Bからアノード液が順次導入されるため、電解酸化されたアノード液は、陽極側電解槽2Aから、配管27bを介してアノード液タンク4B側に押し出される。従って、アノード液はポンプ等の駆動機構によらずに陽極側電解槽2Aとアノード液タンク4Bとの間で循環するため、より多くのアノード液が陽極側電解槽2Aで電解酸化される。
【0031】
陰極側5Aにおいては、下記の反応式(9)、反応式(10)に示す反応が生じ、水素ガスと水酸化ナトリウムとが生成される。
2H++2e− → H2 …(9)
2Na++2H2O+2e− → 2NaOH+H2 …(10)
なお、陰極側電解槽2Bで生じた水素ガス(気泡)は、配管28bを介してカソード液タンク5Bに導かれる。カソード液タンク5Bの天部には水素ガス配管24が設けられており、水素ガス配管24を介して水素ガスが外部に順次排気される。また、陽極側4Aにおいてアノード液が循環することと同様に、陰極側5Aにおいても、カソード液の循環作用が得られる。
【0032】
上記電解酸化により、陽極側4Aの液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。このことは、アノード液が強酸性へと変化する一因となる。そして、電解酸化に伴いアノード液が強酸性となると、塩素ガス、二酸化塩素ガスが発生する。その結果として、塩素酸の収率の低下が生じる。そこで、本実施形態では、塩素ガス、二酸化塩素ガスの発生防止を目的とした、電解酸化時の陽極側4AにおけるpHを調節するpH調節システム10を備える。
【0033】
pH調節システム10は、アノード液タンク4Bの天部に接続されたpH調節剤導入配管11からアノード液にpH調節剤を添加するものであり、アノード液タンク4Bの側部に設けられてアノード液のpHを計測するpH計12と、酸素ガス配管23に設けられ、電解酸化により陽極4で発生した酸素ガスの量を計測する流量計(酸素ガス量計測装置)13と、電解酸化に用いた電流量を計測する電流計(電流量計測装置)14と、それらの計測結果に基づき、pH調節剤導入配管11からpH調節剤として水酸化ナトリウム水溶液をアノード液タンク4B内に添加するpH調節装置15とを有する。
【0034】
pH調節装置15は、pH計12と、流量計13と、電流計14と電気的に接続されており、各々から計測結果のデータが入力され、該データに基づいてpH調節剤の添加量を制御するコンピューターシステム(計測装置)を有する。具体的に、pH調節装置15は、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節プログラムと、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節プログラムと、これらの調節プログラムを陽極側4Aにおいて生成される亜塩素酸の生成量に基づいて切り替えるプログラムとをメモリに記憶しており、これらのプログラムに基づき一次電解槽1の陽極側4AのpH調節を行う構成となっている。
【0035】
先ず、図4を参照して、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節について説明する。
図4は、次亜塩素酸水溶液の存在状態とpHとの関係を示す図である。図4において、横軸はpHを、縦軸は存在比率を示す。
図4に示すように、一次電解槽1での電解酸化に伴い次亜塩素酸を主成分とするアノード液のpHが5未満の酸性値になると、次亜塩素酸が塩素ガス(Cl2)として酸素ガス配管23を介して外部へと排出していくこととなる。その結果、一次電解工程の最終生成物である塩素酸の収率は低下する。
そこで、塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節プログラムにおいては、図4に示すデータに基づいて、塩素ガスの生じない、pHが5以上となるように、該アノード液に水酸化ナトリウム水溶液を添加する制御を行う。
【0036】
次に、図5を参照して、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節について説明する。
図5は、亜塩素酸水溶液の存在状態とpHとの関係を示す図(出典:食品安全委員会、添加物評価書、亜塩素酸水、2008年6月)である。図5において、横軸はpHを、縦軸は存在比率を示す。
図5に示すように、一次電解槽1での電解酸化に伴い亜塩素酸を主成分とするアノード液のpHが2.3未満の酸性値になると、亜塩素酸の存在状態が変化して二酸化塩素ガス(ClO2)として存在することとなる。その結果、上記塩素ガスの発生と同様に二酸化塩素ガスは酸素ガス配管23を介して外部へと排出されるため、一次電解工程の最終生成物である塩素酸の収率は低下する。
そこで、二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節プログラムにおいては、図5に示すデータに基づいて、二酸化塩素ガスの生じない、pHが2.3以上となるように、該アノード液に水酸化ナトリウム水溶液を添加する制御を行う。
【0037】
過塩素酸アンモニウムを製造するにあたり、その純度を高めるためには、ナトリウムイオンは少ないことが望ましい。ここで、次亜塩素酸の電解酸化により亜塩素酸が生成した場合、陽極側4AのpHが2.3以上であれば、二酸化塩素ガスが発生することはない。従って、一次電解槽1での電解酸化に伴い次亜塩素酸が亜塩素酸に全て転化した後は、陽極側4AのpHの制御値を5.0以上から2.3以上へと切り替えることが、後の工程で有益である。そこで、本実施形態のpH調節装置15は、流量計13及び電流計14の計測結果に基づいて、次亜塩素酸及び亜塩素酸の生成量を推定し、陽極側4AのpHの制御値を5.0以上から2.3以上へと切り替えるプログラムを備える。pH調節装置15は、以下に説明する演算式に基づいて次亜塩素酸及び亜塩素酸の生成量を推定する。
【0038】
先ず、塩化ナトリウム水溶液の電解酸化により次亜塩素酸、亜塩素酸、塩素酸を生成する際に必要となる電子の数について説明する。反応式(1)〜反応式(8)に示したように、塩化ナトリウムを水に1mol溶解した塩化ナトリウム水溶液を電解酸化して、次亜塩素酸を1mol生成するためには、2molの電子が必要となる。更に、次亜塩素酸から亜塩素酸を1mol生成するためには2molの電子が必要となる。従って、出発原料である塩化ナトリウム水溶液から亜塩素酸を1mol生成するためには、4molの電子が必要となる。そして、出発原料である塩化ナトリウム水溶液から塩素酸を1mol生成するためには、6molの電子が必要となる。
なお、現実には、反応式(1)〜反応式(8)に示す反応の他に、陽極4の触媒として白金を用いた場合は、その白金が塩化白金酸イオン(PtCl42−)として水溶液中に溶出する反応が生じる。また、1.0A/cm2以上の高い電流密度で電気分解を実施した際には、オゾン(O3)が生成し得る。しかし、これらの反応により生じる生成物は、反応式(1)〜反応式(8)に示す反応により生じる生成物と比較して十分に少ない。従って、ここでは、これらの反応は無視する。
【0039】
電流量と酸素ガスの発生量から次亜塩素酸、亜塩素酸、塩素酸の生成量を推定するにあたり、電流I(A)でt時間(単位は秒)通電した際の酸素ガスの発生量をPO2(単位はリットル(L))とする。ここで標準状態(0℃、1気圧)を仮定した場合、PO2/22.4(mol)の酸素ガスが発生したこととなり、酸素ガスの発生に伴い、陽極4から陰極5へと移動した電子の数eO2(mol)は、PO2/22.4の4倍となる。一方、陽極4から陰極5へと移動した全電子数etotal(mol)は、ファラデー定数F(=9.6485×104C/mol)を用いて、下記の数式(a)で表すことができる。
【0040】
【数1】

【0041】
従って、次亜塩素酸の生成に伴い、陽極4から陰極5へと移動した電子の数は、下記の数式(b)で表すことができる。
【0042】
【数2】

【0043】
結論として、次亜塩素酸の生成量PHClOは、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(c)で推定できる。ここで、κHClOは、HClOの式量であり、52.46(g/mol)である。
【0044】
【数3】

【0045】
同様にして、亜塩素酸の生成量PHClO2は、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(d)で推定できる。ここで、κHClO2は、HClO2の式量であり、68.46(g/mol)である。
【0046】
【数4】

【0047】
更に、塩素酸の生成量PHClO3は、電流量I・t(C)と酸素ガス発生量PO2(L)を用いて、下記の数式(e)で推定できる。ここで、κHClO3は、HClO3の式量であり、84.46(g/mol)である。
【0048】
【数5】

【0049】
従って、pH調節装置15は、一次電解槽1での電解酸化時において、先ず、塩素ガスの発生の防止を目的に、陽極側4Aのアノード液のpHを5以上に調節する。そして、pH調節装置15は、数式(d)に示す演算式に基づき、次亜塩素酸が亜塩素酸へと転換したと推定できる段階で、陽極側4Aのアノード液のpHを2.3以上に調節する。このようにして、pH調節装置15は、塩素ガスの発生、二酸化塩素ガスの発生を防止し、収率を高めると共に、ナトリウムイオンを可能な限り陰極側5Aに移動させる。
【0050】
一次電解槽1での電解酸化により、生成された塩素酸を主成分とするアノード液は、弁25Aを閉状態から開状態にしたアノード液輸送配管25を介してアノード液タンク4Bから二次電解槽2に輸送される。一方、カソード液は、弁26Aを閉状態から開状態にしたカソード液輸送配管26を介してカソード液タンク5Bから外部に輸送される。
【0051】
図6は、本発明の実施形態における二次電解槽2の構成図である。
二次電解槽2は、一次電解槽1で生成した塩素酸を主成分とするアノード液を電解酸化して過塩素酸を生成する。
なお、以下説明する二次電解槽2の構成は、重複説明を避けるため、上述の一次電解槽1と同一又は同等の構成部分については同一の符号を付し、その説明を簡略若しくは省略する。
【0052】
二次電解槽2において、陽イオン交換膜6は陽極4´と陰極5´との間にギャップ無しで挟みこまれたゼロギャップ型の電解セルを構成する。
陽極4´は、陽極側4Aにおける過塩素酸イオンの電解合成反応の促進を図るために、触媒を被覆したエキスパンドメタルからなる。この陽極4´は、基体であるチタンエキスパンドメタルの表面を、電解メッキにより白金の触媒層で被覆した電極から構成される。
一方、この陽極4´と対となる陰極5´は、触媒を被覆したエキスパンドメタルからなる。この陰極5´は、基体であるチタンエキスパンドメタルの表面を、電解メッキにより白金の触媒層で被覆した電極、または、SUS316エキスパンドメタルからなる電極、または、ニッケルエキスパンドメタルからなる電極から構成される。
【0053】
二次電解槽2のアノード液タンク4Bの天部にはアノード液導入配管として、一次電解槽1のアノード液輸送配管25が接続されており、一次電解工程を経たアノード液がアノード液輸送配管25を介して導入され、陽極側4A(陽極側電解槽2A、アノード液タンク4Bを含む)を満たす。一方、カソード液タンク5Bの天部にはカソード液導入配管22が接続されており、純水がカソード液導入配管22を介して導入され、陰極側5A(陰極側電解槽2B、カソード液タンク5Bを含む)を満たす。二次電解槽2の内部で各液にそれぞれ浸された陽極4´及び陰極5´の両極に電圧を印加すると、次の反応が進行する。
【0054】
陽極側4Aにおいては、一次電解工程を経たアノード液が電解酸化され、下記の反応式(11)、反応式(12)に示すように、過塩素酸と副生成物として酸素ガスが生成される。なお、微量ではあるが、下記の反応式(13)に示すように、オゾンガスも副生成物として生成される。
HClO3+H2O → HClO4+2H++2e− …(11)
2H2O → O2+4H++4e− …(12)
3H2O → O3+6H++6e− …(13)
ここで、陽極側4Aの一次電解工程を経た後にアノード液中に含まれるナトリウムイオンは、両極間の電位差によって陽イオン交換膜6を通過して陽極側4Aから陰極側5Aに移動する。一方、塩素酸イオンは陽イオン交換膜6を通過できず、水溶液‐陽極4´‐陽イオン交換膜6で構成される三界面で反応式(11)に示す酸化反応により過塩素酸となる。
【0055】
陰極側5Aにおいては、下記の反応式(14)、反応式(15)に示す反応が生じ、水素ガスと水酸化ナトリウムとが生成される。
2H++2e− → H2 …(14)
2Na++2H2O+2e− → 2NaOH+H2 …(15)
十分な量の過塩素酸が生成されたアノード液は、弁25Aを閉状態から開状態にしたアノード液輸送配管25´を介してアノード液タンク4Bから反応・蒸発槽3に輸送される。一方、カソード液は、弁26Aを閉状態から開状態にしたカソード液輸送配管26を介してカソード液タンク5Bから外部に輸送される。
【0056】
反応・蒸発槽3では、電解酸化後のアノード液中にアンモニア水溶液を添加して過塩素酸アンモニウムを合成する工程と、合成後のアノード液を真空、高温環境下で蒸発させて過塩素酸アンモニウムを晶析させる工程とを行う。なお、ここでアンモニア水溶液の代わりにアンモニアガスをバブリングしてもよい。
反応・蒸発槽3には、アンモニア供給配管31が接続されており、電解酸化後のアノード液中にアンモニア水溶液を供給する構成となっている。電解酸化後のアノード液中にアンモニア水溶液を添加すると、下記の反応式(16)に示す中和反応が生じ、目的物である過塩素酸アンモニウムと副生成物として水が合成される。
HClO4+NH4OH → NH4ClO4+H2O …(16)
【0057】
次に、反応・蒸発槽3において、合成後のアノード液を真空、高温環境下で蒸発させ、濃縮した水溶液を冷却することにより過塩素酸アンモニウムを結晶として取り出す。反応式(16)に示すように、過塩素酸アンモニウムと共に得られる副生成物は水であるため、非特許文献1に記載の方法と比較して、高純度の過塩素酸アンモニウムの結晶が容易に得られる。
【0058】
以上のように、本実施形態によれば、陽極4が設けられる陽極側4Aと陰極5が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて塩化ナトリウム水溶液を電解酸化して、塩素酸を主成分とする水溶液を生成する一次電解槽1と、陽極4´が設けられる陽極側4Aと陰極5´が設けられる陰極側5Aとが陽イオン交換膜6で仕切られ、該陽極側4Aにおいて一次電解槽1での電解酸化により生成した塩素酸を主成分とする水溶液を電解酸化して、過塩素酸水溶液を生成する二次電解槽2と、二次電解槽2での電解酸化により生成した過塩素酸水溶液に、アンモニアを添加して、中和反応により過塩素酸アンモニウムを合成する反応・蒸発槽3と、を有する過塩素酸アンモニウム製造装置Aを採用することにより、塩素酸ナトリウムよりも低価で入手容易な塩化ナトリウムを、原材料として用いることで、原材料の調達安定性が高まり、過塩素酸アンモニウムを安定して製造することができる。
【0059】
また、一次電解槽1での電解酸化に伴い陽極側4Aは強酸性に変化する。その結果、次亜塩素酸の存在状態の変化によって生じる塩素ガスや、亜塩素酸の存在状態の変化によって生じる二酸化塩素ガスが一次電解槽1の系外に排出されるため、中間生成物である塩素酸の収率の低下が懸念される。そこで、本実施形態では、pH計12を用いて陽極側4AのpHを計測し、その計測結果に基づいて、アルカリ性の水酸化ナトリウム水溶液を添加して陽極側4AのpHを調節し、塩素酸の収率の低下を防止する。ここで添加する水酸化ナトリウム水溶液は、この電解酸化により陰極側5Aで生成される副生成物を用いると、原材料である水酸化ナトリウムを調達する必要がなくなる。
【0060】
本実施形態のpH調節では、先ず、一次電解工程において、塩素ガスの発生の防止を目的としたpH調節を行う。一次電解槽1の次亜塩素酸を主成分とするアノード液のpHが5未満になると、塩素ガスが発生して系外に排出されるため、pHを5以上に調節することで、塩素ガスの発生を防止して塩素酸の収率を高めることができる。
本実施形態のpH調節は、次に、一次電解工程において、二酸化塩素ガスの発生の防止を目的としたpH調節を行う。一次電解槽1の亜塩素酸を主成分とするアノード液のpHが2.3未満になると、亜塩素酸の存在状態が変化して二酸化塩素ガスとして系外に排出されるため、pHを2.3以上に調節することで、二酸化塩素ガスの発生を防止し、塩素酸の収率を高めることができる。
【0061】
また、本実施形態では、上記塩素ガスの発生の防止を目的とした次亜塩素酸水溶液のpH調節と上記二酸化塩素ガスの発生の防止を目的とした亜塩素酸水溶液のpH調節とを、次亜塩素酸及び亜塩素酸の生成量に基づいて切り替える。過塩素酸アンモニウムを製造するにあたり、その純度を高めるためには、ナトリウムイオンは少ないことが望ましい。従って、次亜塩素酸の電解酸化により亜塩素酸が生成した場合、陽極側4AのpHが2.3以上であれば、二酸化塩素ガスが発生することはない。そこで、一次電解槽1での電解酸化に伴い亜塩素酸が所定量生成された後は、陽極側4AのpHを2.3以上に調節することが、後の工程で有益である。
通常、次亜塩素酸及び亜塩素酸の生成量を計測するには液体イオンクロマトグラフィーが用いられる。しかし、その分析には、時間と手間がかかるため、本実施形態では、一次電解槽1での電解酸化により陽極4で発生した酸素ガスの量と、この電解酸化における電流量とに基づいて、次亜塩素酸及び亜塩素酸、塩素酸の生成量をモニタリングすることにより、適切なタイミングで陽極側4AのpH調整の切り替えを行うことができる。
【0062】
以上、図面を参照しながら本発明の好適な実施形態について説明したが、本発明は上記実施形態に限定されるものではない。上述した実施形態において示した各構成部材の諸形状や組み合わせ等は一例であって、本発明の主旨から逸脱しない範囲において設計要求等に基づき種々変更可能である。
【0063】
例えば、本発明は、上述した過塩素酸アンモニウムの製造装置への適用に限定されるものではなく、過塩素酸リチウムや過塩素酸カリウム等のアルカリ金属過塩素酸塩の製造装置、過塩素酸カルシウム等のアルカリ土類金属過塩素酸塩の製造装置、また、過塩素酸銀の製造装置等にも適用可能である。
【0064】
また、例えば、本発明は、上述した一次電解槽と二次電解槽の2つの電解槽を用いて過塩素酸水溶液を生成する形態だけでなく、1つの電解槽で過塩素酸水溶液を生成する形態や3つ以上の複数の電解槽で過塩素酸水溶液を生成する形態にも適用可能である。また、電解槽については、ゼロギャップ型のみならず、陽イオン交換膜を陽極と陰極との間にスペースを設けて設置した電解槽を用いても良い。
【符号の説明】
【0065】
A…過塩素酸アンモニウム製造装置(過塩素酸塩の製造装置)、S1…一次電解工程、…、S2…二次電解工程、S3…反応工程(合成工程)、S4…晶析工程、1…一次電解槽(電解槽)、2…二次電解槽(電解槽)、3…反応・蒸発槽、4…陽極、4´…陽極、4A…陽極側、5…陰極、5´…陰極、5A…陰極側、6…陽イオン交換膜、10…pH調節システム、11…pH調節剤導入管、12…pH計、13…流量計(酸素ガス量計測装置)、14…電流計(電流量計測装置)、15…pH調節装置
【特許請求の範囲】
【請求項1】
陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られ、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する電解槽と、
前記電解槽での電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する合成槽と、
前記電解槽の陽極側におけるpHを計測するpH計と、
前記pH計の計測結果に基づいて、前記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の前記陽極側におけるpHを調節するpH調節装置と、
を有することを特徴とする過塩素酸塩の製造装置。
【請求項2】
前記電解槽での電解酸化により前記陽極で発生した酸素ガスの量を計測する酸素ガス量計測装置と、
前記電解槽での電解酸化における電流量を計測する電流量計測装置と、
前記酸素ガス量計測装置の計測結果と前記電流量計測装置の計測結果とに基づいて、前記電解槽での電解酸化に伴って前記陽極側において生成される次亜塩素酸及び亜塩素酸の生成量を計測する計測装置と、
を有することを特徴とする請求項1に記載の過塩素酸塩の製造装置。
【請求項3】
前記pH調節装置は、前記次亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを調節することを特徴とする請求項2に記載の過塩素酸塩の製造装置。
【請求項4】
前記pH調節装置は、前記次亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを5.0以上に調節することを特徴とする請求項3に記載の過塩素酸塩の製造装置。
【請求項5】
前記pH調節装置は、前記次亜塩素酸の生成量に基づく調節の後、前記亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを調節することを特徴とする請求項4に記載の過塩素酸塩の製造装置。
【請求項6】
前記pH調節装置は、前記亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを2.3以上に調節することを特徴とする請求項5に記載の過塩素酸塩の製造装置。
【請求項7】
前記pH調節装置は、前記計測装置の計測結果に基づいて、前記次亜塩素酸の生成量に基づく調節と前記亜塩素酸の生成量に基づく調節との切り替えを行うことを特徴とする請求項2〜6のいずれか一項に記載の過塩素酸塩の製造装置。
【請求項8】
陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用い、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する工程と、
前記電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する工程と、
前記電解槽の陽極側におけるpHを計測する工程と、
前記pHの計測結果に基づいて、前記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の前記陽極側におけるpHを調節する工程と、
を有することを特徴とする過塩素酸塩の製造方法。
【請求項1】
陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られ、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する電解槽と、
前記電解槽での電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する合成槽と、
前記電解槽の陽極側におけるpHを計測するpH計と、
前記pH計の計測結果に基づいて、前記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の前記陽極側におけるpHを調節するpH調節装置と、
を有することを特徴とする過塩素酸塩の製造装置。
【請求項2】
前記電解槽での電解酸化により前記陽極で発生した酸素ガスの量を計測する酸素ガス量計測装置と、
前記電解槽での電解酸化における電流量を計測する電流量計測装置と、
前記酸素ガス量計測装置の計測結果と前記電流量計測装置の計測結果とに基づいて、前記電解槽での電解酸化に伴って前記陽極側において生成される次亜塩素酸及び亜塩素酸の生成量を計測する計測装置と、
を有することを特徴とする請求項1に記載の過塩素酸塩の製造装置。
【請求項3】
前記pH調節装置は、前記次亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを調節することを特徴とする請求項2に記載の過塩素酸塩の製造装置。
【請求項4】
前記pH調節装置は、前記次亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを5.0以上に調節することを特徴とする請求項3に記載の過塩素酸塩の製造装置。
【請求項5】
前記pH調節装置は、前記次亜塩素酸の生成量に基づく調節の後、前記亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを調節することを特徴とする請求項4に記載の過塩素酸塩の製造装置。
【請求項6】
前記pH調節装置は、前記亜塩素酸の生成量に基づいて、前記電解酸化時の前記陽極側におけるpHを2.3以上に調節することを特徴とする請求項5に記載の過塩素酸塩の製造装置。
【請求項7】
前記pH調節装置は、前記計測装置の計測結果に基づいて、前記次亜塩素酸の生成量に基づく調節と前記亜塩素酸の生成量に基づく調節との切り替えを行うことを特徴とする請求項2〜6のいずれか一項に記載の過塩素酸塩の製造装置。
【請求項8】
陽極が設けられる陽極側と陰極が設けられる陰極側とが陽イオン交換膜で仕切られている電解槽を用い、該陽極側において塩化ナトリウム水溶液を電解酸化して、過塩素酸水溶液を生成する工程と、
前記電解酸化により生成した過塩素酸水溶液に、水溶液にした際にアルカリ性を示す物質を添加して、中和反応により過塩素酸塩を合成する工程と、
前記電解槽の陽極側におけるpHを計測する工程と、
前記pHの計測結果に基づいて、前記電解槽の陽極側に水酸化ナトリウム水溶液を添加し、前記塩化ナトリウム水溶液を電解酸化して塩素酸を主成分とする水溶液を生成する過程において、前記電解酸化時の前記陽極側におけるpHを調節する工程と、
を有することを特徴とする過塩素酸塩の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】




【図2】


【図3】


【図4】


【図5】


【図6】


【公開番号】特開2013−91829(P2013−91829A)
【公開日】平成25年5月16日(2013.5.16)
【国際特許分類】
【出願番号】特願2011−234828(P2011−234828)
【出願日】平成23年10月26日(2011.10.26)
【出願人】(000000099)株式会社IHI (5,014)
【Fターム(参考)】
【公開日】平成25年5月16日(2013.5.16)
【国際特許分類】
【出願日】平成23年10月26日(2011.10.26)
【出願人】(000000099)株式会社IHI (5,014)
【Fターム(参考)】
[ Back to top ]

