酵素の直接媒介によりサンプル中の分析物の濃度を測定する方法
血液のグルコース含量を、血液サンプルを、補因子としてのPQQ(またはその誘導体または異性体)に依存性のグルコースデヒドロゲナーゼ、テトラゾリウム塩指示薬を含有するが、メディエータを含有しない試験ストリップと、接触させることにより、決定することができる。
【発明の詳細な説明】
【発明の詳細な説明】
【0001】
発明の属する分野
[0001] 本発明は、一般的には、生物学的液体中の分析物の量を決定するための方法に関する。より具体的には、本発明は、血液またはその他の液体のグルコース含量を測定するための方法を含む。
【0002】
発明の背景
[0002] 全血液などの生物学的液体中での分析物の定量的測定、例えば、血液中のグルコースレベルを頻繁にチェックして、食餌や投薬を制御しなければならない糖尿病個体の血液中のグルコースレベルを測定すること、は、特定の病状の診断および治療において特に重要である。血液のグルコース含量の測定は、いくつかの方法により行うことができる。一つの方法は、電気化学的バイオセンサを使用する方法である。別の方法は、例えば、指示薬の反応による色を呈することにより、グルコース含量の視覚的表示を提供するものである。本発明は、電気化学的方法もまた利用する場合があるが、後者のタイプのものである。
【0003】
[0003] 電気化学的方法は、多数の特許において記載されてきた。それらは、クーロメティク(coulometic)、電流測定、およびサイクリック・ボルタンメトリーを含む、いくつかのカテゴリーに分類される。最近公開されたU.S.特許出願の一つは、2003/0094384A1である。特開2000-171428A2は、グルコース電解センサの調製を記載する。
【0004】
[0004] 一連の反応の最終工程として指示薬が化学的に酸化される場合に発色するかまたはその他の測定可能な反応を起こす指示薬を使用する方法を記載する、多数の特許が存在してきた。一般的に、その様な方法は、分析物オキシダーゼ(例えば、グルコースオキシダーゼ)を利用するものと、分析物デヒドロゲナーゼ(例えば、グルコースデヒドロゲナーゼ)を利用するものとに大きく分類することができる。使用される手順は類似しているが、それらは異なる酵素、メディエータおよび指示薬を使用する。
【0005】
[0005] グルコースオキシダーゼ酵素を使用する方法は、多数のUS特許および特許出願中で教示されている。代表的なものは、U.S. 4,211,845;U.S. 4,808,529;U.S. 5,116,729;U.S. 5,264,348;U.S. 5,620,863;およびU.S. 2003/0077702 A1である。これらの特許/特許出願は、グルコースをグルコン酸に酸化し、過酸化水素の放出を伴う方法を教示する。過酸化水素は、ペルオキシダーゼの存在下で指示薬を酸化し、血液サンプルのグルコース含量を示す測定可能な色を生成すると言われる。いくつかの最近の特許では、グルコースがまずグルコン酸に変換され、そしてその後グルコノラクトンに変換され、過酸化水素が放出されるプロセスが示唆されている。グルコノラクトンがまず形成され、そしてその後、加水分解されてグルコン酸になることも示唆されてきた。どちらのプロセススキームが正しいかに関わらず、グルコースオキシダーゼ酵素は、乾燥ストリップにおいて、そして血液のグルコース含量を測定するためのその他の技術において、幅広く利用されてきた。
【0006】
[0006] ベンジジン-型指示薬や複素環アジンなどの様々な指示薬が、グルコースセンサにおいて使用されてきた。例えば、中でも、3,3',5,5'-テトラメチルベンジジンおよびシリンガルダジン、ルミノール、o-トリジン、o-ジアニシチン(o-dianisitine)である。指示薬の一つのファミリーは、テトラゾリウム色素前駆体のファミリーである。その様な指示薬について記載する特許の例には、U.S. 5,126,275、U.S. 5,322,680、U.S. 5,300,637、U.S. 5,290,536、U.S. 5,360,595およびU.S. 6,586,199が含まれる。テトラゾリウム指示薬は、以下に記載されるように、本発明中で使用される。
【0007】
[0007] 本発明に関して特に興味深いのは、U.S. 6,200,773およびその親特許であるU.S. 5,902,731において記載される方法である。これらの特許において、血液のグルコース含量の試験は、グルコースデヒドロゲナーゼ(GDH)を、補因子としてのNADまたはPQQまたはそれらの誘導体、テトラゾリウム色素前駆体、ジアフォラーゼ酵素またはその類似体、そして亜硝酸塩と共に使用する。'773特許の図5は、テトラゾリウム色素前駆体を還元して生成されたホルマザンからの呈色により、グルコースを検出するプロセスの図である。
【0008】
[0008] グルコースデヒドロゲナーゼ(GDH)酵素に対する補因子としてのPQQ(ピロロ-キノリンキノンまたはその誘導体または異性体)は、U.S. 2002/0076751 A1;EP 1 167 519 A1;U.S. 6,103,509;およびJP 11243949 A2における開示からも明らかな様に、最近興味を持たれている。一般的には、これらの開示は、グルコースセンサにおける性能の改善をもたらすと言われているグルコースデヒドロゲナーゼ酵素の遺伝的修飾を教示する。
【0009】
[0009] 本発明の発明者らは、U.S. 6,200,773中にて開示されたプロセスと類似のプロセスを、ジアフォラーゼ酵素などのメディエータの非存在下で、実行することができることを、予期せず見いだした。以下の本発明の記載において見いだされる様に、この知見により、血液サンプル中のグルコースを検出するより単純な方法が可能になる。
【0010】
発明の概要
[0010] テトラゾリウム指示薬をグルコース溶液と接触させるが、通常は必要とされるメディエータを含まない場合に、特定のグルコースデヒドロゲナーゼ-補因子の組み合わせを使用して、テトラゾリウム指示薬からの比色反応を提供することができることを見いだした。特に、PQQ依存性グルコースデヒドロゲナーゼ(PQQ-GDH)は、メディエータが存在する場合とメディエータが存在しない場合の両方ともで、グルコースに対する同様な反応性を提供することが示された。その他のキノン-依存性デヒドロゲナーゼ酵素は、それらの対応するドナー化合物により、同様な性能を提供することが予想される。
【0011】
[0011] 一側面において、本発明は、血液中のグルコース濃度を測定するための試薬溶液である。補因子としてのピロロ-キノリンキノン(PQQ)(またはその誘導体または異性体)に依存性のグルコースデヒドロゲナーゼ(GDH)は、テトラゾリウム色素前駆体とともに使用されるが、PMS(フェナジンメトスルフェート)またはジアフォラーゼなどのメディエータを含ませることはない。
【0012】
[0012] 別の側面において、本発明は、GDH、補因子としてのPQQ(または誘導体または異性体)、そしてテトラゾリウム色素前駆体を含有するが、通常のメディエータは含まない、乾燥試験ストリップである。このストリップは、グルコース-含有血液と接触させ、そして発色された色を測定し、そしてグルコース含量と相関させる。
【0013】
[0013] 本発明はまた、実質的にメディエータの非存在下で、GDHおよび補因子としてのPQQ(または誘導体または異性体)、およびテトラゾリウム色素前駆体を含有するこの試験ストリップを使用して、全血液のグルコース含量を測定する改良方法である。
【0014】
好ましい態様の説明
血液中のグルコースの測定
[0018] グルコースオキシダーゼを使用する方法において、それらの酵素を、グルコースと反応させ、酸化グルコースと過酸化水素を生成させる。過酸化水素は、指示薬化合物を、ペルオキシダーゼの存在下で酸化する。酸化された指示薬は、血液サンプルのグルコース含量と相関される色を生成する。
【0015】
[0019] 本発明において、グルコースデヒドロゲナーゼを、補因子およびテトラゾリウム色素前駆体とともに使用して、サンプルのグルコース含量に比例した発色反応を生成する。そのような反応は、通常は以下の反応の流れにより記載される:
グルコース+GDH-補因子oxid → グルコノラクトン+GDH-補因子red
GDH-補因子red+メディエータoxid → GDH-補因子oxid+メディエータred
メディエータred+テトラゾリウム指示薬 → メディエータoxid+ホルマザン。
【0016】
[0020] この一連の反応の流れにしたがって、グルコースはグルコノラクトンへと変換され、一方、デヒドロゲナーゼ-補因子は還元され、その後、利用可能なグルコースによるさらなる反応のため、メディエータにより再酸化される。メディエータは、PMS(フェナジンメトスルフェート)、PES(フェナジンエトスルフェート)、DCIP(2,6,-ジクロロフェノリンドフェノール)、およびフェロセンなどの、当業者に一般的であるもののいずれであってもよい。メディエータは、テトラゾリウム指示薬をホルマザンへと還元することにより、有用な反応を得ることが必要であると考えられてきた。しかしながら、本発明において、メディエータは必要とされず、そして有用な反応は、以下の実施例において示される様に、その非存在下で得られる。
【0017】
[0021] 本発明の発明者らは、グルコースデヒドロゲナーゼが、EC 1.1.99.17(現EC 1.1.5.2)(International Union of Biochemistry and Molecular Biology;Nomenclature and Classification of Enzyme-Catalyzed Reactions;NC-IUBMB)として分類される場合に、メディエータが必要とされないことを見いだした。そのような酵素は、特定の補因子に依存し、この場合には、補因子は、ピロロ-キノリンキノン(PQQ)またはその誘導体または異性体である。その他のグルコースデヒドロゲナーゼ酵素は、ニコチンアミドアデニンジヌクレオチド(NAD)、フラビンアデニンジヌクレオチド(FAD)、およびそれらの類似体などの、その他の補酵素または補因子に依存する。実質的にメディエータの非存在下にてPQQ-依存性GDHを使用することに成功した理由は、現時点では理解されていない。理論により束縛される訳ではないが、それは、テトラゾリウム塩が酵素とより直接的に接触する様になる能力および/または補因子に関して拡散の限定が少ないというその能力と関連している可能性がある。
【0018】
[0022] したがって、本発明の方法において、テトラゾリウム指示薬は、以下の反応の流れにしたがって、還元デヒドロゲナーゼ-補因子により還元される様である:
グルコース+GDH-補因子oxid → グルコノラクトン+GDH-補因子red
GDH-補因子red+テトラゾリウム指示薬 → ホルマザン+GDH-補因子oxid。
【0019】
デヒドロゲナーゼ
[0023] グルコースデヒドロゲナーゼ酵素は、Toyobo、Kyowa、Amano、Genzyme、Biozymeなどから商業的に入手可能であり、そして天然の酵素または古典的な発酵および/または組換え方法により生成される組換え酵素のいずれかである。効果的であるために、デヒドロゲナーゼは、NAD、FADおよびPQQ、およびそれらの誘導体または異性体などの補因子を必要とする。デヒドロゲナーゼは、その供給者から補因子と組み合わせて入手されるため、それらは、その供給者により特性決定されており、そしてそれらの性質は、現時点では十分に知られていない。デヒドロゲナーゼ酵素と既知の補因子との組合せが試験され、実施例において示される結果が得られた。そこに見いだされるように、PQQ-依存性GDH酵素は、メディエータの存在を必要としなかった。
【0020】
[0024] 本発明の発明者らは、PQQ(または誘導体または異性体)に依存性のグルコースデヒドロゲナーゼが、テトラゾリウム塩指示薬の存在下にて、グルコースとの反応を測定するため、メディエータを必要としないことを見いだした。本発明の発明者らは、キノンをアクセプター(EC 1.1.5クラス)として伴うその他のデヒドロゲナーゼ酵素が、アルコール類またはその他のCH-OHドナー化合物を酸化する際に、同様に振る舞う可能性があると考えている。
【0021】
メディエータ
[0025] 試験システムには、グルコースとの反応後に還元デヒドロゲナーゼ-補因子を再酸化して、対応するラクトンを形成するためのメディエータが含まれる必要があると考えられてきた。ジアフォラーゼまたはPMS(フェナジンメトスルフェート)は、典型的なメディエータである。メディエータを必要としない点が、本発明の特徴である。以下の実施例においても示される様に、新規試薬システムは、メディエータが含まれていてもいなくても、同様な方法で、振る舞うことがわかる。
【0022】
テトラゾリウム指示薬
[0026] テトラゾリウム指示薬は、既に言及したU.S.特許中に一般的に記載されている。U.S. 6,200,773において、デヒドロゲナーゼ-補因子の組合せとの反応において特に有用なものとして、特定のテトラゾリウム色素前駆体が列挙されている。それらの中で、WST-4と呼ばれるテトラゾリウム化合物が、以下の実施例において使用されている。
【実施例】
【0023】
実施例1:非NAD-依存性グルコースデヒドロゲナーゼおよびWST-4によるグルコースの検出
[0027] 0.8μmポリエーテルスルホンメンブレンのストリップ(細片)を、370 mMリン酸バッファー、pH 7、0.5%ポリマー(例えば、テレオスタチン)、界面活性剤(例えば、0.1%Cremaphor ELおよび0.2%Triton X305)、5.5 mgの非-NAD(P)-依存性グルコースデヒドロゲナーゼ[EC 1.1.99.17(現EC 1.1.5.2)と呼ばれるキノン-依存性GDH](Toyoboから入手)、800 U/mg、および60 mMの指示薬(Dojindoから入手したWST-4)を含有するが、メディエータを含有しない溶液中に浸漬した。
【0024】
[0028] グルコースサンプルを40%ヘマトクリットの全血液サンプルから調製し、そして濃度を、YSIグルコースアナライザ(Yellow Springs Instruments)を使用して以下の様にして測定した:
a)0 mg/dLのヒト血漿、
b)48 mg/dLのヒト血漿、
c)101 mg/dLのヒト血漿、
d)201 mg/dLのヒト血漿、
e)397 mg/dLのヒト血漿、
f)607 mg/dLのヒト血漿。
【0025】
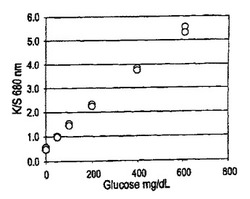
[0029] 試薬ストリップを、グルコース溶液と接触させた際、添加したグルコース濃度に比例した色の変化を発生させた。色の変化は、反射率-測定装置を使用して、50-秒の発色時間の後に測定した。反射率を、Kubelka-Munk式から生成した線形関数であるK/Sに変換した。K/Sは、(1-R2)/2R(ここで、Rは、測定された反射率である)に等しい。2回繰り返しのグルコースサンプルのそれぞれの反応を、図1に示す。
【0026】
実施例1の結果は、デヒドロゲナーゼに基づくグルコースセンサの古典的な技術において記載される様なメディエータ(例えば、PMS)が何も反応混合物中に含まれていなくても、測定可能で実質的に線形の反応が得られたことを示す。
【0027】
実施例2:直接検出によるグルコース測定と、古典的測定(classic Mediation)方法によるグルコース測定の比較
[0030] ポリエチレンテレフタレート(PET, Melenex、Dupontから入手)のストリップを、バッファーの混合物(0.25 Mホスフェート、pH 7.4)、および非活性活性成分(例えば、レオロジー修飾物質、乳白剤、および界面活性剤)を用いてコーティングした。この実施例では、混合物には、0.6 g/Lポリアクリレート、0.6 g/Lポリビニルアルコール、1.5 g/L二酸化チタン、1 g/L炭酸カルシウム、0.001〜0.006%のSilwet L-7600、Gerepon T-77、Surfonyl DF37が含まれ、そして120 mM 指示薬(例えば、WST-4)および6 KU/ mL非-NAD(P)-依存性グルコースデヒドロゲナーゼ(EC 1.1.99.17、現EC 1.1.5.2、Bayerから入手、特許出願中)を含有した。別のストリップを、5 mMのメディエータ(PMS)を添加した同一の混合物によりコーティングした。全血漿グルコースサンプルを上述したコーティングした試薬のサンプルに対して適用し、そして色の変化を実施例1に記載したように測定した。グルコースサンプルを40%ヘマトクリットの全血液サンプルから調製し、そしてそれぞれの濃度をYSIグルコースアナライザ(Yellow Springs Instruments)を使用して以下の様にして測定した:
a)1 mg/dLヒト血漿、
b)56 mg/dLヒト血漿、
c)112 mg/dLヒト血漿、
d)224 mg/dLヒト血漿、
e)448 mg/dLヒト血漿、
f)678 mg/dLヒト血漿
グルコースサンプルのそれぞれについての2回繰り返しの平均反射率は、サンプルをグルコース試薬に対して適用してから7秒後および33秒後の両方で記録した。
【0028】
[0031] 実施例2の結果(図2を参照)は、直接測定(direct mediation)法により測定可能で実質的に線形の反応が得られたこと、そして観察された反応が古典的測定(classic mediation)法の反応と実質的に同一であったこと、を示す。検出速度もまた、7秒および33秒の試験時間で測定された最終点の反射率により示される様に、古典的検出法と実質的に同一であることが示された。
【0029】
実施例3:
[0032] 異なるテトラゾリウム塩指示薬を使用すること以外、実施例2を繰り返した。
[0033] 別のテトラゾリウム塩を使用する直接的測定(direct mediation)が、実施例1のWST-4の代わりに、HTC-45の類似体(チアゾリルテトラゾリウム塩、Bayer Corporation、U.S.特許5,126,275の第21欄を参照)を使用することにより、示された。図3において示される様に、7秒の反応時間の後、グルコースに対する実質的に直線の容量反応性が示された。
【0030】
実施例4:(比較)
[0034] 0.8μmポリエーテルスルホンメンブレン(Osmonics)のストリップを、補因子としてのNADをNAD-依存性GDH(EC 1.1.1.47)およびテトラゾリウム塩指示薬と共に含有するが、メディエータを含有しない溶液中に浸漬した。処理済みのストリップを、既知濃度を有するグルコース溶液と接触させた。図4に示される様に、実質的に何の反応も測定されないことが分かった。
【0031】
[0035] 別の態様A
(a)グルコースデヒドロゲナーゼ(GDH);
(b)GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);および
(c)テトラゾリウム塩指示薬;
を含む、血液中のグルコース濃度を測定するための試薬。
【0032】
[0036] 別の態様B
(a)の前記グルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、態様Aの試薬。
【0033】
[0037] 別の態様C
前記補因子がPQQである、態様Aの試薬。
[0038] 別の態様D
前記補因子がPQQ誘導体または異性体である、態様Aの試薬。
【0034】
[0039] 別の態様E
前記テトラゾリウム塩指示薬がWST-4である、態様Aの試薬。
[0040] 別の態様F
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Aの試薬。
【0035】
[0041] 別の態様G
(a)支持体;
(b)前記支持体上に配置された試薬層(前記試薬システムは:(1)グルコースデヒドロゲナーゼ(GDH);(2)GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);および(3)テトラゾリウム塩指示薬;を含む);
を含む、血液中のグルコースを測定するための試験ストリップ。
【0036】
[0042] 別の態様H
(b)(l)の前記グルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、態様Gの試験ストリップ。
【0037】
[0043] 別の態様I
前記補因子がPQQである、態様Gの試験ストリップ。
[0044] 別の態様J
前記補因子がPQQ誘導体または異性体である、態様Gの試験ストリップ。
【0038】
[0045] 別の態様K
前記テトラゾリウム塩指示薬がWST-4である、態様Gの試験ストリップ。
[0046] 別の態様L
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Gの試験ストリップ。
【0039】
[0047] 別の態様M
(a)支持体;
(b)前記支持体上に配置された試薬システム(前記試薬システムは、グルコースデヒドロゲナーゼ(GDH)、GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ類似体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる)、そしてテトラゾリウム塩指示薬を含む);
(c)前記テトラゾリウム塩指示薬から発色された色を測定すること;そして
(d)工程(b)において発色された色を、前記血液サンプルのグルコース含量と相関させること;
を含む、血液中のグルコースを測定する方法。
【0040】
[0048] 別の態様N
前記グルコースデヒドロゲナーゼが、EC 1.1.99.17と分類される、態様Mの方法。
[0049] 別の態様O
前記補因子がPQQである、態様Mの方法。
【0041】
[0050] 別の態様P
前記補因子がPQQ誘導体または異性体である、態様Mの方法。
[0051] 別の態様Q
前記テトラゾリウム塩指示薬がWST-4である、態様Mの方法。
【0042】
[0052] 別の態様R
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Mの方法。
[0053] 本発明は、様々な修飾および別の形式に影響を受けやすい一方、具体的な態様は図面中の例として示されており、そして本明細書中で詳細に記載されている。しかしながら、本発明が、開示された具体的な形式に限定されることを意図しないことは理解されるべきである。むしろ、本発明は、添付する特許請求の範囲により定義される本発明の精神および範囲に収まるすべての修飾、均等物、そして代替物をカバーするものである。
【図面の簡単な説明】
【0043】
【図1】[0014] 図1は、実施例1の結果のグラフである。
【図2】[0015] 図2は、実施例2の結果のグラフである。
【図3】[0016] 図3は、実施例3の結果のグラフである。
【図4】[0017] 図4は、実施例4の結果のグラフである。
【発明の詳細な説明】
【0001】
発明の属する分野
[0001] 本発明は、一般的には、生物学的液体中の分析物の量を決定するための方法に関する。より具体的には、本発明は、血液またはその他の液体のグルコース含量を測定するための方法を含む。
【0002】
発明の背景
[0002] 全血液などの生物学的液体中での分析物の定量的測定、例えば、血液中のグルコースレベルを頻繁にチェックして、食餌や投薬を制御しなければならない糖尿病個体の血液中のグルコースレベルを測定すること、は、特定の病状の診断および治療において特に重要である。血液のグルコース含量の測定は、いくつかの方法により行うことができる。一つの方法は、電気化学的バイオセンサを使用する方法である。別の方法は、例えば、指示薬の反応による色を呈することにより、グルコース含量の視覚的表示を提供するものである。本発明は、電気化学的方法もまた利用する場合があるが、後者のタイプのものである。
【0003】
[0003] 電気化学的方法は、多数の特許において記載されてきた。それらは、クーロメティク(coulometic)、電流測定、およびサイクリック・ボルタンメトリーを含む、いくつかのカテゴリーに分類される。最近公開されたU.S.特許出願の一つは、2003/0094384A1である。特開2000-171428A2は、グルコース電解センサの調製を記載する。
【0004】
[0004] 一連の反応の最終工程として指示薬が化学的に酸化される場合に発色するかまたはその他の測定可能な反応を起こす指示薬を使用する方法を記載する、多数の特許が存在してきた。一般的に、その様な方法は、分析物オキシダーゼ(例えば、グルコースオキシダーゼ)を利用するものと、分析物デヒドロゲナーゼ(例えば、グルコースデヒドロゲナーゼ)を利用するものとに大きく分類することができる。使用される手順は類似しているが、それらは異なる酵素、メディエータおよび指示薬を使用する。
【0005】
[0005] グルコースオキシダーゼ酵素を使用する方法は、多数のUS特許および特許出願中で教示されている。代表的なものは、U.S. 4,211,845;U.S. 4,808,529;U.S. 5,116,729;U.S. 5,264,348;U.S. 5,620,863;およびU.S. 2003/0077702 A1である。これらの特許/特許出願は、グルコースをグルコン酸に酸化し、過酸化水素の放出を伴う方法を教示する。過酸化水素は、ペルオキシダーゼの存在下で指示薬を酸化し、血液サンプルのグルコース含量を示す測定可能な色を生成すると言われる。いくつかの最近の特許では、グルコースがまずグルコン酸に変換され、そしてその後グルコノラクトンに変換され、過酸化水素が放出されるプロセスが示唆されている。グルコノラクトンがまず形成され、そしてその後、加水分解されてグルコン酸になることも示唆されてきた。どちらのプロセススキームが正しいかに関わらず、グルコースオキシダーゼ酵素は、乾燥ストリップにおいて、そして血液のグルコース含量を測定するためのその他の技術において、幅広く利用されてきた。
【0006】
[0006] ベンジジン-型指示薬や複素環アジンなどの様々な指示薬が、グルコースセンサにおいて使用されてきた。例えば、中でも、3,3',5,5'-テトラメチルベンジジンおよびシリンガルダジン、ルミノール、o-トリジン、o-ジアニシチン(o-dianisitine)である。指示薬の一つのファミリーは、テトラゾリウム色素前駆体のファミリーである。その様な指示薬について記載する特許の例には、U.S. 5,126,275、U.S. 5,322,680、U.S. 5,300,637、U.S. 5,290,536、U.S. 5,360,595およびU.S. 6,586,199が含まれる。テトラゾリウム指示薬は、以下に記載されるように、本発明中で使用される。
【0007】
[0007] 本発明に関して特に興味深いのは、U.S. 6,200,773およびその親特許であるU.S. 5,902,731において記載される方法である。これらの特許において、血液のグルコース含量の試験は、グルコースデヒドロゲナーゼ(GDH)を、補因子としてのNADまたはPQQまたはそれらの誘導体、テトラゾリウム色素前駆体、ジアフォラーゼ酵素またはその類似体、そして亜硝酸塩と共に使用する。'773特許の図5は、テトラゾリウム色素前駆体を還元して生成されたホルマザンからの呈色により、グルコースを検出するプロセスの図である。
【0008】
[0008] グルコースデヒドロゲナーゼ(GDH)酵素に対する補因子としてのPQQ(ピロロ-キノリンキノンまたはその誘導体または異性体)は、U.S. 2002/0076751 A1;EP 1 167 519 A1;U.S. 6,103,509;およびJP 11243949 A2における開示からも明らかな様に、最近興味を持たれている。一般的には、これらの開示は、グルコースセンサにおける性能の改善をもたらすと言われているグルコースデヒドロゲナーゼ酵素の遺伝的修飾を教示する。
【0009】
[0009] 本発明の発明者らは、U.S. 6,200,773中にて開示されたプロセスと類似のプロセスを、ジアフォラーゼ酵素などのメディエータの非存在下で、実行することができることを、予期せず見いだした。以下の本発明の記載において見いだされる様に、この知見により、血液サンプル中のグルコースを検出するより単純な方法が可能になる。
【0010】
発明の概要
[0010] テトラゾリウム指示薬をグルコース溶液と接触させるが、通常は必要とされるメディエータを含まない場合に、特定のグルコースデヒドロゲナーゼ-補因子の組み合わせを使用して、テトラゾリウム指示薬からの比色反応を提供することができることを見いだした。特に、PQQ依存性グルコースデヒドロゲナーゼ(PQQ-GDH)は、メディエータが存在する場合とメディエータが存在しない場合の両方ともで、グルコースに対する同様な反応性を提供することが示された。その他のキノン-依存性デヒドロゲナーゼ酵素は、それらの対応するドナー化合物により、同様な性能を提供することが予想される。
【0011】
[0011] 一側面において、本発明は、血液中のグルコース濃度を測定するための試薬溶液である。補因子としてのピロロ-キノリンキノン(PQQ)(またはその誘導体または異性体)に依存性のグルコースデヒドロゲナーゼ(GDH)は、テトラゾリウム色素前駆体とともに使用されるが、PMS(フェナジンメトスルフェート)またはジアフォラーゼなどのメディエータを含ませることはない。
【0012】
[0012] 別の側面において、本発明は、GDH、補因子としてのPQQ(または誘導体または異性体)、そしてテトラゾリウム色素前駆体を含有するが、通常のメディエータは含まない、乾燥試験ストリップである。このストリップは、グルコース-含有血液と接触させ、そして発色された色を測定し、そしてグルコース含量と相関させる。
【0013】
[0013] 本発明はまた、実質的にメディエータの非存在下で、GDHおよび補因子としてのPQQ(または誘導体または異性体)、およびテトラゾリウム色素前駆体を含有するこの試験ストリップを使用して、全血液のグルコース含量を測定する改良方法である。
【0014】
好ましい態様の説明
血液中のグルコースの測定
[0018] グルコースオキシダーゼを使用する方法において、それらの酵素を、グルコースと反応させ、酸化グルコースと過酸化水素を生成させる。過酸化水素は、指示薬化合物を、ペルオキシダーゼの存在下で酸化する。酸化された指示薬は、血液サンプルのグルコース含量と相関される色を生成する。
【0015】
[0019] 本発明において、グルコースデヒドロゲナーゼを、補因子およびテトラゾリウム色素前駆体とともに使用して、サンプルのグルコース含量に比例した発色反応を生成する。そのような反応は、通常は以下の反応の流れにより記載される:
グルコース+GDH-補因子oxid → グルコノラクトン+GDH-補因子red
GDH-補因子red+メディエータoxid → GDH-補因子oxid+メディエータred
メディエータred+テトラゾリウム指示薬 → メディエータoxid+ホルマザン。
【0016】
[0020] この一連の反応の流れにしたがって、グルコースはグルコノラクトンへと変換され、一方、デヒドロゲナーゼ-補因子は還元され、その後、利用可能なグルコースによるさらなる反応のため、メディエータにより再酸化される。メディエータは、PMS(フェナジンメトスルフェート)、PES(フェナジンエトスルフェート)、DCIP(2,6,-ジクロロフェノリンドフェノール)、およびフェロセンなどの、当業者に一般的であるもののいずれであってもよい。メディエータは、テトラゾリウム指示薬をホルマザンへと還元することにより、有用な反応を得ることが必要であると考えられてきた。しかしながら、本発明において、メディエータは必要とされず、そして有用な反応は、以下の実施例において示される様に、その非存在下で得られる。
【0017】
[0021] 本発明の発明者らは、グルコースデヒドロゲナーゼが、EC 1.1.99.17(現EC 1.1.5.2)(International Union of Biochemistry and Molecular Biology;Nomenclature and Classification of Enzyme-Catalyzed Reactions;NC-IUBMB)として分類される場合に、メディエータが必要とされないことを見いだした。そのような酵素は、特定の補因子に依存し、この場合には、補因子は、ピロロ-キノリンキノン(PQQ)またはその誘導体または異性体である。その他のグルコースデヒドロゲナーゼ酵素は、ニコチンアミドアデニンジヌクレオチド(NAD)、フラビンアデニンジヌクレオチド(FAD)、およびそれらの類似体などの、その他の補酵素または補因子に依存する。実質的にメディエータの非存在下にてPQQ-依存性GDHを使用することに成功した理由は、現時点では理解されていない。理論により束縛される訳ではないが、それは、テトラゾリウム塩が酵素とより直接的に接触する様になる能力および/または補因子に関して拡散の限定が少ないというその能力と関連している可能性がある。
【0018】
[0022] したがって、本発明の方法において、テトラゾリウム指示薬は、以下の反応の流れにしたがって、還元デヒドロゲナーゼ-補因子により還元される様である:
グルコース+GDH-補因子oxid → グルコノラクトン+GDH-補因子red
GDH-補因子red+テトラゾリウム指示薬 → ホルマザン+GDH-補因子oxid。
【0019】
デヒドロゲナーゼ
[0023] グルコースデヒドロゲナーゼ酵素は、Toyobo、Kyowa、Amano、Genzyme、Biozymeなどから商業的に入手可能であり、そして天然の酵素または古典的な発酵および/または組換え方法により生成される組換え酵素のいずれかである。効果的であるために、デヒドロゲナーゼは、NAD、FADおよびPQQ、およびそれらの誘導体または異性体などの補因子を必要とする。デヒドロゲナーゼは、その供給者から補因子と組み合わせて入手されるため、それらは、その供給者により特性決定されており、そしてそれらの性質は、現時点では十分に知られていない。デヒドロゲナーゼ酵素と既知の補因子との組合せが試験され、実施例において示される結果が得られた。そこに見いだされるように、PQQ-依存性GDH酵素は、メディエータの存在を必要としなかった。
【0020】
[0024] 本発明の発明者らは、PQQ(または誘導体または異性体)に依存性のグルコースデヒドロゲナーゼが、テトラゾリウム塩指示薬の存在下にて、グルコースとの反応を測定するため、メディエータを必要としないことを見いだした。本発明の発明者らは、キノンをアクセプター(EC 1.1.5クラス)として伴うその他のデヒドロゲナーゼ酵素が、アルコール類またはその他のCH-OHドナー化合物を酸化する際に、同様に振る舞う可能性があると考えている。
【0021】
メディエータ
[0025] 試験システムには、グルコースとの反応後に還元デヒドロゲナーゼ-補因子を再酸化して、対応するラクトンを形成するためのメディエータが含まれる必要があると考えられてきた。ジアフォラーゼまたはPMS(フェナジンメトスルフェート)は、典型的なメディエータである。メディエータを必要としない点が、本発明の特徴である。以下の実施例においても示される様に、新規試薬システムは、メディエータが含まれていてもいなくても、同様な方法で、振る舞うことがわかる。
【0022】
テトラゾリウム指示薬
[0026] テトラゾリウム指示薬は、既に言及したU.S.特許中に一般的に記載されている。U.S. 6,200,773において、デヒドロゲナーゼ-補因子の組合せとの反応において特に有用なものとして、特定のテトラゾリウム色素前駆体が列挙されている。それらの中で、WST-4と呼ばれるテトラゾリウム化合物が、以下の実施例において使用されている。
【実施例】
【0023】
実施例1:非NAD-依存性グルコースデヒドロゲナーゼおよびWST-4によるグルコースの検出
[0027] 0.8μmポリエーテルスルホンメンブレンのストリップ(細片)を、370 mMリン酸バッファー、pH 7、0.5%ポリマー(例えば、テレオスタチン)、界面活性剤(例えば、0.1%Cremaphor ELおよび0.2%Triton X305)、5.5 mgの非-NAD(P)-依存性グルコースデヒドロゲナーゼ[EC 1.1.99.17(現EC 1.1.5.2)と呼ばれるキノン-依存性GDH](Toyoboから入手)、800 U/mg、および60 mMの指示薬(Dojindoから入手したWST-4)を含有するが、メディエータを含有しない溶液中に浸漬した。
【0024】
[0028] グルコースサンプルを40%ヘマトクリットの全血液サンプルから調製し、そして濃度を、YSIグルコースアナライザ(Yellow Springs Instruments)を使用して以下の様にして測定した:
a)0 mg/dLのヒト血漿、
b)48 mg/dLのヒト血漿、
c)101 mg/dLのヒト血漿、
d)201 mg/dLのヒト血漿、
e)397 mg/dLのヒト血漿、
f)607 mg/dLのヒト血漿。
【0025】
[0029] 試薬ストリップを、グルコース溶液と接触させた際、添加したグルコース濃度に比例した色の変化を発生させた。色の変化は、反射率-測定装置を使用して、50-秒の発色時間の後に測定した。反射率を、Kubelka-Munk式から生成した線形関数であるK/Sに変換した。K/Sは、(1-R2)/2R(ここで、Rは、測定された反射率である)に等しい。2回繰り返しのグルコースサンプルのそれぞれの反応を、図1に示す。
【0026】
実施例1の結果は、デヒドロゲナーゼに基づくグルコースセンサの古典的な技術において記載される様なメディエータ(例えば、PMS)が何も反応混合物中に含まれていなくても、測定可能で実質的に線形の反応が得られたことを示す。
【0027】
実施例2:直接検出によるグルコース測定と、古典的測定(classic Mediation)方法によるグルコース測定の比較
[0030] ポリエチレンテレフタレート(PET, Melenex、Dupontから入手)のストリップを、バッファーの混合物(0.25 Mホスフェート、pH 7.4)、および非活性活性成分(例えば、レオロジー修飾物質、乳白剤、および界面活性剤)を用いてコーティングした。この実施例では、混合物には、0.6 g/Lポリアクリレート、0.6 g/Lポリビニルアルコール、1.5 g/L二酸化チタン、1 g/L炭酸カルシウム、0.001〜0.006%のSilwet L-7600、Gerepon T-77、Surfonyl DF37が含まれ、そして120 mM 指示薬(例えば、WST-4)および6 KU/ mL非-NAD(P)-依存性グルコースデヒドロゲナーゼ(EC 1.1.99.17、現EC 1.1.5.2、Bayerから入手、特許出願中)を含有した。別のストリップを、5 mMのメディエータ(PMS)を添加した同一の混合物によりコーティングした。全血漿グルコースサンプルを上述したコーティングした試薬のサンプルに対して適用し、そして色の変化を実施例1に記載したように測定した。グルコースサンプルを40%ヘマトクリットの全血液サンプルから調製し、そしてそれぞれの濃度をYSIグルコースアナライザ(Yellow Springs Instruments)を使用して以下の様にして測定した:
a)1 mg/dLヒト血漿、
b)56 mg/dLヒト血漿、
c)112 mg/dLヒト血漿、
d)224 mg/dLヒト血漿、
e)448 mg/dLヒト血漿、
f)678 mg/dLヒト血漿
グルコースサンプルのそれぞれについての2回繰り返しの平均反射率は、サンプルをグルコース試薬に対して適用してから7秒後および33秒後の両方で記録した。
【0028】
[0031] 実施例2の結果(図2を参照)は、直接測定(direct mediation)法により測定可能で実質的に線形の反応が得られたこと、そして観察された反応が古典的測定(classic mediation)法の反応と実質的に同一であったこと、を示す。検出速度もまた、7秒および33秒の試験時間で測定された最終点の反射率により示される様に、古典的検出法と実質的に同一であることが示された。
【0029】
実施例3:
[0032] 異なるテトラゾリウム塩指示薬を使用すること以外、実施例2を繰り返した。
[0033] 別のテトラゾリウム塩を使用する直接的測定(direct mediation)が、実施例1のWST-4の代わりに、HTC-45の類似体(チアゾリルテトラゾリウム塩、Bayer Corporation、U.S.特許5,126,275の第21欄を参照)を使用することにより、示された。図3において示される様に、7秒の反応時間の後、グルコースに対する実質的に直線の容量反応性が示された。
【0030】
実施例4:(比較)
[0034] 0.8μmポリエーテルスルホンメンブレン(Osmonics)のストリップを、補因子としてのNADをNAD-依存性GDH(EC 1.1.1.47)およびテトラゾリウム塩指示薬と共に含有するが、メディエータを含有しない溶液中に浸漬した。処理済みのストリップを、既知濃度を有するグルコース溶液と接触させた。図4に示される様に、実質的に何の反応も測定されないことが分かった。
【0031】
[0035] 別の態様A
(a)グルコースデヒドロゲナーゼ(GDH);
(b)GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);および
(c)テトラゾリウム塩指示薬;
を含む、血液中のグルコース濃度を測定するための試薬。
【0032】
[0036] 別の態様B
(a)の前記グルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、態様Aの試薬。
【0033】
[0037] 別の態様C
前記補因子がPQQである、態様Aの試薬。
[0038] 別の態様D
前記補因子がPQQ誘導体または異性体である、態様Aの試薬。
【0034】
[0039] 別の態様E
前記テトラゾリウム塩指示薬がWST-4である、態様Aの試薬。
[0040] 別の態様F
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Aの試薬。
【0035】
[0041] 別の態様G
(a)支持体;
(b)前記支持体上に配置された試薬層(前記試薬システムは:(1)グルコースデヒドロゲナーゼ(GDH);(2)GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);および(3)テトラゾリウム塩指示薬;を含む);
を含む、血液中のグルコースを測定するための試験ストリップ。
【0036】
[0042] 別の態様H
(b)(l)の前記グルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、態様Gの試験ストリップ。
【0037】
[0043] 別の態様I
前記補因子がPQQである、態様Gの試験ストリップ。
[0044] 別の態様J
前記補因子がPQQ誘導体または異性体である、態様Gの試験ストリップ。
【0038】
[0045] 別の態様K
前記テトラゾリウム塩指示薬がWST-4である、態様Gの試験ストリップ。
[0046] 別の態様L
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Gの試験ストリップ。
【0039】
[0047] 別の態様M
(a)支持体;
(b)前記支持体上に配置された試薬システム(前記試薬システムは、グルコースデヒドロゲナーゼ(GDH)、GDHについての補因子として、ピロロ-キノリンキノン(PQQ)またはPQQ類似体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下にて、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる)、そしてテトラゾリウム塩指示薬を含む);
(c)前記テトラゾリウム塩指示薬から発色された色を測定すること;そして
(d)工程(b)において発色された色を、前記血液サンプルのグルコース含量と相関させること;
を含む、血液中のグルコースを測定する方法。
【0040】
[0048] 別の態様N
前記グルコースデヒドロゲナーゼが、EC 1.1.99.17と分類される、態様Mの方法。
[0049] 別の態様O
前記補因子がPQQである、態様Mの方法。
【0041】
[0050] 別の態様P
前記補因子がPQQ誘導体または異性体である、態様Mの方法。
[0051] 別の態様Q
前記テトラゾリウム塩指示薬がWST-4である、態様Mの方法。
【0042】
[0052] 別の態様R
前記テトラゾリウム塩指示薬がHTC-45の類似体である、態様Mの方法。
[0053] 本発明は、様々な修飾および別の形式に影響を受けやすい一方、具体的な態様は図面中の例として示されており、そして本明細書中で詳細に記載されている。しかしながら、本発明が、開示された具体的な形式に限定されることを意図しないことは理解されるべきである。むしろ、本発明は、添付する特許請求の範囲により定義される本発明の精神および範囲に収まるすべての修飾、均等物、そして代替物をカバーするものである。
【図面の簡単な説明】
【0043】
【図1】[0014] 図1は、実施例1の結果のグラフである。
【図2】[0015] 図2は、実施例2の結果のグラフである。
【図3】[0016] 図3は、実施例3の結果のグラフである。
【図4】[0017] 図4は、実施例4の結果のグラフである。
【特許請求の範囲】
【請求項1】
(a)グルコースデヒドロゲナーゼ(GDH);
(b)GDHに対する補因子としての、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);そして
(c)テトラゾリウム塩指示薬;
を含む、血液中のグルコース濃度を測定するための試薬。
【請求項2】
前記(a)のグルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、請求項1に記載の試薬。
【請求項3】
前記補因子がPQQである、請求項1に記載の試薬。
【請求項4】
前記補因子がPQQ誘導体または異性体である、請求項1に記載の試薬。
【請求項5】
前記テトラゾリウム塩指示薬がWST-4である、請求項1に記載の試薬。
【請求項6】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項1に記載の試薬。
【請求項7】
(a)支持体;
(b)前記支持体上に配置された試薬層;
を含み、ここで前記試薬システムが以下のもの:
(1)グルコースデヒドロゲナーゼ(GDH);
(2)GDHに対する補因子としての、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);そして
(3)テトラゾリウム塩指示薬;
を含む、血液中のグルコースを測定するための試験用ストリップ(test strip)。
【請求項8】
前記(b)(l)のグルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、請求項7に記載の試験用ストリップ。
【請求項9】
前記補因子がPQQである、請求項7に記載の試験用ストリップ。
【請求項10】
前記補因子がPQQ誘導体または異性体である、請求項7に記載の試験用ストリップ。
【請求項11】
前記テトラゾリウム塩指示薬がWST-4である、請求項7に記載の試験用ストリップ。
【請求項12】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項7に記載の試験用ストリップ。
【請求項13】
(a)支持体;
(b)前記支持体上に配置されグルコースデヒドロゲナーゼ(GDH)、GDHに対する補因子としてのピロロ-キノリンキノン(PQQ)またはPQQ類似体(ここで前記GDHおよび補因子は、メディエータの非存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる)、およびテトラゾリウム塩指示薬、を含む試薬システム;
(c)前記テトラゾリウム塩指示薬から発色された色を測定する工程;そして
(d)工程(b)において発色された色と前記血液サンプルのグルコース含量とを相関させる工程;
を含む、血液中のグルコースを測定するための方法。
【請求項14】
前記グルコースデヒドロゲナーゼがEC 1.1.99.17として分類される、請求項13に記載の方法。
【請求項15】
前記補因子がPQQである、請求項13に記載の方法。
【請求項16】
前記補因子がPQQ誘導体または異性体である、請求項13に記載の方法。
【請求項17】
前記テトラゾリウム塩指示薬がWST-4である、請求項13に記載の方法。
【請求項18】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項13に記載の方法。
【請求項1】
(a)グルコースデヒドロゲナーゼ(GDH);
(b)GDHに対する補因子としての、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの非存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);そして
(c)テトラゾリウム塩指示薬;
を含む、血液中のグルコース濃度を測定するための試薬。
【請求項2】
前記(a)のグルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、請求項1に記載の試薬。
【請求項3】
前記補因子がPQQである、請求項1に記載の試薬。
【請求項4】
前記補因子がPQQ誘導体または異性体である、請求項1に記載の試薬。
【請求項5】
前記テトラゾリウム塩指示薬がWST-4である、請求項1に記載の試薬。
【請求項6】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項1に記載の試薬。
【請求項7】
(a)支持体;
(b)前記支持体上に配置された試薬層;
を含み、ここで前記試薬システムが以下のもの:
(1)グルコースデヒドロゲナーゼ(GDH);
(2)GDHに対する補因子としての、ピロロ-キノリンキノン(PQQ)またはPQQ誘導体または異性体(ここで前記GDHおよび補因子は、実質的にメディエータの存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる);そして
(3)テトラゾリウム塩指示薬;
を含む、血液中のグルコースを測定するための試験用ストリップ(test strip)。
【請求項8】
前記(b)(l)のグルコースデヒドロゲナーゼが、NC-IUBMBにしたがって、EC 1.1.99.17(現EC 1.1.5.2)として分類される、請求項7に記載の試験用ストリップ。
【請求項9】
前記補因子がPQQである、請求項7に記載の試験用ストリップ。
【請求項10】
前記補因子がPQQ誘導体または異性体である、請求項7に記載の試験用ストリップ。
【請求項11】
前記テトラゾリウム塩指示薬がWST-4である、請求項7に記載の試験用ストリップ。
【請求項12】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項7に記載の試験用ストリップ。
【請求項13】
(a)支持体;
(b)前記支持体上に配置されグルコースデヒドロゲナーゼ(GDH)、GDHに対する補因子としてのピロロ-キノリンキノン(PQQ)またはPQQ類似体(ここで前記GDHおよび補因子は、メディエータの非存在下で、発色したホルマザンテトラゾリウム塩指示薬へと還元することができる)、およびテトラゾリウム塩指示薬、を含む試薬システム;
(c)前記テトラゾリウム塩指示薬から発色された色を測定する工程;そして
(d)工程(b)において発色された色と前記血液サンプルのグルコース含量とを相関させる工程;
を含む、血液中のグルコースを測定するための方法。
【請求項14】
前記グルコースデヒドロゲナーゼがEC 1.1.99.17として分類される、請求項13に記載の方法。
【請求項15】
前記補因子がPQQである、請求項13に記載の方法。
【請求項16】
前記補因子がPQQ誘導体または異性体である、請求項13に記載の方法。
【請求項17】
前記テトラゾリウム塩指示薬がWST-4である、請求項13に記載の方法。
【請求項18】
前記テトラゾリウム塩指示薬がHTC-45類似体である、請求項13に記載の方法。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公表番号】特表2008−510490(P2008−510490A)
【公表日】平成20年4月10日(2008.4.10)
【国際特許分類】
【出願番号】特願2007−530054(P2007−530054)
【出願日】平成17年8月22日(2005.8.22)
【国際出願番号】PCT/US2005/029985
【国際公開番号】WO2006/023927
【国際公開日】平成18年3月2日(2006.3.2)
【出願人】(503106111)バイエル・ヘルスケア・エルエルシー (154)
【Fターム(参考)】
【公表日】平成20年4月10日(2008.4.10)
【国際特許分類】
【出願日】平成17年8月22日(2005.8.22)
【国際出願番号】PCT/US2005/029985
【国際公開番号】WO2006/023927
【国際公開日】平成18年3月2日(2006.3.2)
【出願人】(503106111)バイエル・ヘルスケア・エルエルシー (154)
【Fターム(参考)】
[ Back to top ]

