酵素の計測方法および計測装置
【課題】 誘導期間を待つことなく、その場で結果を知ることができ、サンプルを連続的に採取し測定を行うことができ、サンプル中の酵素濃度の経時変化を追跡することを可能とする酵素の計測方法および計測装置を提供する。
【解決手段】 酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、上記試料液に自己触媒反応に関わる試薬を混合して混合液とし、該混合液を一定の流量で流路に流し、該流路中で自己触媒反応を起こさせ、自己触媒反応に伴って上記流路中で現れる変色の状態から上記試料液に含まれる酵素の量を求めることとした。
【解決手段】 酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、上記試料液に自己触媒反応に関わる試薬を混合して混合液とし、該混合液を一定の流量で流路に流し、該流路中で自己触媒反応を起こさせ、自己触媒反応に伴って上記流路中で現れる変色の状態から上記試料液に含まれる酵素の量を求めることとした。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、酵素の計測方法および計測装置に関する。酵素の計測は、例えば、エンザイムイムノアッセイ(EIA)と呼ばれる分析の中で、目的の生物や化学物質を酵素標識し、それを検出する技術として様々な分野で行なわれている。本発明を用いると、酵素を迅速、簡便、高感度に計測することが可能となる。利用分野としては酵素の計測を行う全ての分野が該当し、臨床をはじめ医薬品、製薬、食品、環境分析など広範である。具体的な用途としては、内分泌撹乱性物質(環境ホルモン)の検出や、ホルモン様作用の測定、アトピー性皮膚炎の原因物質特定、スギ花粉の飛散量測定、ウイルスや細菌のような微生物の計測が挙げられる。
【背景技術】
【0002】
イムノアッセイは生体内での特異的な免疫反応である抗原抗体反応を利用した技術であり、アレルギー反応の原因物質、ウイルス、細菌など多様な対象を高い特異性をもって計測できる優れた分析手法である。計測原理は、抗原に結合させた標識物質の量を測ることにより、間接的に測定対象である抗原を定量するというものである。
【0003】
標識物質としては、放射性物質、蛍光物質、発光物質、酵素などが用いられている。特に、酵素を標識とする分析方法はエンザイムイムノアッセイ(EIA)と呼ばれ、他の方法と比較して安全で操作が簡便である上、感度や選択性が高いという特長があり、広く利用されている。 標識酵素の計測方法としては、発色試薬を用いて吸光度を測定する方法や、化学発光を用いる方法が普及している。
【0004】
しかしながら、これらの方法では、計測システム全体に対して、標識酵素の計測系に関わる分析精度、手間、コストの制約が大きいことが問題になっている。これに対して特許文献1に記載されるような先行技術は、代表的な標識酵素であるペルオキシダーゼ(Peroxydase:以下PODと略す)に着目し、PODが触媒として作用する自己触媒反応を利用して、反応が急激に進行するまでの時間(誘導期間)からPODの量を求めるという方法を提供している。この先行技術では、前記PODが触媒として作用する自己触媒反応は、亜硫酸塩・過酸化水素系の反応またはCo−(5−Br−PAPS)2・ペルオキソー硫酸系の反応としている。
【0005】
また、誘導期間の終点は、pHの急激な変化や、Co(5−Br−PAPS)2の分解進行に伴う呈色状態の急変として目視でもとらえることができ、特別な検出装置を必要とせず簡便である。この技術によって、簡易かつローコストな酵素の計測を実現している。
【特許文献1】特開2001−333797号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1の方法は、反応がバッチ式に進むことから、例えばストップウォッチで時間を測り、誘導期間のあいだ変色を待っていなければならない。また、この先行技術は、一つのサンプルの酵素濃度を測定する方法であり、連続モニタリングができないなど、実用上の制約がある。
【0007】
そこで、本発明では、誘導期間を待つことなく、その場で結果を知ることができ、サンプルを連続的に採取し測定を行うことができ、サンプル中の酵素濃度の経時変化を追跡することを可能とする酵素の計測方法および計測装置を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記目的を達成するために、本発明の請求項1に係る酵素の計測方法は、酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間(誘導期間)にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、試料液に自己触媒反応に関わる試薬を混合し、その混合液を一定の流量で流路に流し、流路中で自己触媒反応を起こさせ、自己触媒反応に伴って流路中で現れる変色の状態から試料液に含まれる酵素の量を求めることを特徴とする。
【0009】
本発明の請求項2に係る酵素の計測方法は、請求項1について酵素の量の計測方法を示したものであり、自己触媒反応に伴って流路中で現れる変色領域の長さ、あるいは、非変色領域の長さのどちらか一方から、試料液に含まれる酵素の量を計測することを特徴とする。
【0010】
本発明の請求項3に係る酵素の計測方法は、請求項1、2の酵素の計測方法を実施するための装置であって、試薬を保持する手段と、試料液を保持する手段と、送液手段と、試薬、試料液およびそれらの混合液を流す流路と、試薬や試料液を混合する手段と、自己触媒反応を検出する手段とを備えることを特徴とする。
【0011】
本発明の請求項4に係る酵素の計測方法は、請求項3について流路の性質を特定したものであり、流路のうち、試薬と試料液の混合液を流す部分が透明であることを特徴とする。
【0012】
本発明の請求項5に係る酵素の計測方法は、請求項4について流路の形状を特定したものであり、流路のうち、試薬と試料液の混合液を流す部分がらせん状構造を有することを特徴とする。
【0013】
本発明の請求項6に係る酵素の計測方法は、複数試料の計測を可能とする発明であり、請求項3〜5に示した装置であって、複数の試料液を保持する手段と、複数の流路とを備えることを特徴とする。
【0014】
本発明の請求項7に係る酵素の計測方法は、校正機能を実現するための発明であり、請求項3〜6に示した装置であって、酵素を含まない校正用溶液(ゼロ校正液)と、既知の濃度の酵素を含む校正用溶液(スパン校正液)とのいずれか一方、ないしは両方を備えることを特徴とする。
【発明の効果】
【0015】
本発明によれば、誘導期間を待つことなく、その場で結果を知ることができ、サンプルを連続的に採取し測定を行うことができ、サンプル中の酵素濃度の経時変化を追跡することを可能とする酵素の計測方法および計測装置が提供される。
【発明を実施するための最良の形態】
【0016】
以下に本発明の実施の形態を述べるが、本発明の適用範囲は、この内容に限定されるものではない。
【0017】
自己触媒反応
自己触媒反応とは、反応進行にともなって、反応物質が増加したり、反応を触媒する物質が増加する化学反応である。
この反応の特徴は、反応進行にともなって、反応速度が指数関数的に増大し、ある時間が経過した時に反応が急激に進むことである。この反応において反応開始剤となる物質(たとえば反応を触媒する酵素)をトリガーと呼ぶ。そして、トリガーの量は反応開始から反応終点までの時間(誘導期間)から求めることができる。自己触媒反応では、混合して反応を開始させても誘導期間は、ほとんど無反応であるかのように進み、このような誘導期間を過ぎて急激に反応が進行すると共に完了する。したがって、誘導期間とは、このように反応物および必要な触媒を混合してから反応が完了するまでの期間であると共に、その期間の経過の直前まで実質的に反応が進行せず、経過時点でほぼ瞬時に反応が完了する期間であることを意味する。
【0018】
自己触媒反応の中でpHの経時変化を利用して反応進行を検出する系として、亜硫酸ナトリウム/過酸化水素反応系がある。この反応系では式(1)の反応が起こり、亜硫酸水素イオン1個が水素イオン1個と反応して、水素イオン2個が生成する。
HSO3- + H2O2 + H+
→ 2H+ + SO42- + H2O ・・・・・(1)
【0019】
生成した水素イオンは式(1)の反応側の要素となることから、反応が進めば進むほど平衡を生成側に押し、反応速度が高まっていく。結果的に、時間が経過するにつれて水素イオンが指数関数的に増加していき、反応溶液のpHは、ある時間(誘導期間)が経過すると急激に低下する。このため、この溶液にpH指示薬、例えばブロモチモールブルー(BTB)を添加しておくと、誘導時間が経過した後、溶液のpH変化に伴って、溶液の色が青色から黄色に瞬時に変化する。この呈色状態の変化は、十分、目視で確認が可能であり、特別な検出装置などを必要としない。
【0020】
自己触媒反応のほかの例としては、Co−(5−Br−PAPS)2 /ペルオキソー硫酸反応系がある。この反応系では式(2)の反応が起こり、Co2+イオンが生成する。
【0021】
【化1】

(2)
Co2+イオンは、式(2)の反応に対して触媒として働くため、結果的に、上記の(1)の反応と同様、反応進行とともに反応速度が高まっていく。Co−(5−Br−PAPS)2 は紫色、その分解生成物は無色であるため、誘導期間が経過した後、紫色だった反応溶液は無色透明になる。
【0022】
上述の2つの自己触媒反応系では、いずれも、酵素ペルオキシダーゼ(POD)の一種であるホースラディッシュペルオキシダーゼ(以下HRPと略)がトリガーとして働く。HRPは、EIAにおいて抗体の標識によく利用される酵素である。自己触媒反応はHRPを微量まで定量可能であり、EIAの信号検知手段として非常に優れている。
【0023】
本発明に係る酵素の計測方法の形態
本発明に係る酵素の計測方法では、自己触媒反応を流路中で行う。自己触媒反応に関わる試薬、および試料液は、ポンプなどを用いて流路に流して混合し、例えば、ガラス棒にポリテトラフロロエチレンチューブをらせん状に巻きつけた流路(コイル)の中に通す。このような形態では、コイルの任意の長さの場所を境に自己触媒反応に伴う変化(例えば溶液の変色)が起こる。
【0024】
例えば、試料液と試薬とを混合した場所をx=0とし、そこから変化が起こる場所までの距離をx、管路の各部における断面積をS(X) 、流量をV(一定)、誘導期間をTとすると、これらの関係は式(3)で表すことができる。
∫S(X) dx = V × T ・・・・・(3)
式(3)において、管路の断面積を一定のSとすると、
S × x = V × T
x = V/S × T
となり、これは、
距離 = 流速 × 時間 ・・・・・(4)
と解釈することもできる。すなわち、流量だけでなく、流速が一定であることを意味する。
式(1)の自己触媒反応にBTBを添加した系を用いた場合、試料液中のHRP濃度が異なると、その濃度の増加とともにガラス棒上の青色バンドの長さが短くなる。それは、HRP濃度の増加に伴って自己触媒反応の速度が向上し、誘導期間が短くなった結果、変化が起こる場所までの距離が短くなるためである。この事実に基づき、自己触媒反応をフロー系で検出する方法を確立したのが本発明である。
【0025】
自己触媒反応はある誘導時間を経た後に反応が急激に進行する。そのため上述のように流路中を所定の流量(管径が一定の領域では一定流速)で流れる反応溶液は、変化が起きる場所までの距離が誘導期間に従属(管径が一定の領域では比例)して変化する。このため、任意の長さの位置で、急激に反応が進行する前の溶液と、進行した後の溶液に分かれる。
管径が一定の場合には、距離と誘導期間とが比例関係にあり、これに基づいて、HRP濃度を特定することができる。
管径が変化しても、流量を一定とすれば、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間とが比例関係にあることからHRP濃度を特定することができる。
本発明者らは、pH変化を利用した自己触媒反応系であるBTB/亜硫酸塩/過酸化水素自己触媒反応を流路に流して行った。その結果、攪拌コイル中の任意の長さを境界として、青色バンドと黄色バンドが現れた。この自己触媒反応系では、ある誘導時間を経て、反応溶液のpHが急激に下降する。そのため、青色バンドの溶液は高pH(反応進行前)の溶液、黄色バンドの溶液は低pH(反応進行後)の溶液に相当する。青色バンドと黄色バンドの境界の位置の変動は6時間の連続運転でおよそ±1mm程度であった。このことから、本発明では、従来の変色時間を目視とストップウォッチで測定するバッチ系自己触媒反応のように、急激に反応が進む瞬間まで溶液を監視する必要はない。
【実施例】
【0026】
次に、本発明に係る酵素の計測方法および計測装置に関し、その実施例と請求項との関係を示し、さらに実施例について説明する。
実施例
1.試薬
BTB、亜硫酸ナトリウム、HRPは和光純薬製を使用した。過酸化水素は関東化学製を使用した。その他の試薬は断りの無い限り市販の特級試薬を蒸留水で希釈して使用した。
【0027】
2.装置
送液手段としては、プランジャーポンプを用いることができる。本実施例では、東京化成製のダブルプランジャー型ポンプTCI−NOX1000ωを2台使用した。プランジャータイプ以外のポンプとしては、流量比保持を重視する場合はペリスタティックポンプが好適であり、微小化を目指すにはピエゾポンプが適している。
【0028】
流路には、ジーエルサイエンス製のポリテトラフロロエチレンチューブ(外径1/16インチ、内径1mm)を使用した。このチューブは半透明であり、流路中の液の色を目視などで検知することができる。また、ポリテトラフロロエチレンチューブをらせん状に巻きつけるために、直径7mm、長さ300mmのガラス管を使用した。チューブをらせん状にすることで、目視観察の際、変色域を認識しやすくなるからである。
【0029】
3.各溶液の調製
亜硫酸塩/BTB水溶液は亜硫酸ナトリウム0.64gとBTB 15mgを蒸留水に溶解し、50mLに希釈し、流路に流す際はこの溶液をさらに5倍に希釈して使用した。過酸化水素水は30%過酸化水素水4mLを蒸留水で100mLに希釈して使用した。
HRP試料溶液は蒸留水で希釈し、HRP濃度100μgL-1に調製したものを母液とし、これをさらに蒸留水で希釈して使用した。
【0030】
4.定量操作
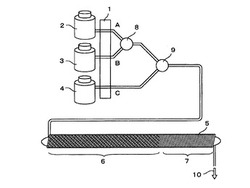
図1に、本発明の実施例であるフローシステム装置の概略を示す。プランジャーポンプ1を用いて、流路AにはBTB/亜硫酸塩水溶液2を、流路Bには過酸化水素水3をそれぞれ流速0.5mL・min-1で流した。同様に、流路CにはHRP試料溶液4を流速1.0mL・min-1で流した。なお、図1の装置は、本発明を実施するための一実施形態であり、本発明を実施するための装置は、図1のものに限定されるものではない。
【0031】
図1の装置では、流路中で混合された溶液は、ガラス棒に巻きつけられた反応コイル5の中を流れる。溶液のpHは、当初、弱アルカリ性であることから、BTBの青色を呈しているが(図中6の領域)、ある長さから先では、自己触媒反応によってpHが急激に低下し、黄色へと変化する(図中7の領域)。このためガラス棒上の反応コイルが変色前の青色領域と変食後の黄色領域とに分かれた様子を目視で判別できる。変色状態の観察は、目視のほか、CCDカメラやCMOSカメラによっても可能であり、ほかには、リニアイメージセンサを利用することもできる。参照番号8、9で示した装置は、試薬と試料液を混合するためのミキサーであり、必要に応じて用いればよい。計測後、廃液10は装置から排出される。
【0032】
本実施例では、図1の装置を用い、反応コイルの左末端から青色と黄色の境界までの長さ、すなわち青色領域6の長さをものさしで測定し、試料液中のHRP濃度の定量を行った。
【0033】
5.HRP濃度と変色域の長さとの関係
本実施例では、試料液中のHRP濃度を0ppm、1ppm、2ppm、1ppm、0ppmと変化させたときに、時間経過に伴ない、青色領域6の長さがどのように変化するかを測定した。結果を図2に示す。HRP濃度が増加すると青色領域6の長さは短くなった。また、濃度が減少して初期の0ppmに戻ると、青色領域の長さは元に戻った。
【0034】
HRPは、過酸化水素が分解されて水素イオンを生成する反応を触媒する。図2の結果から了解されるように、本発明では一つのサンプルの酵素濃度を測定することが可能なだけではなく、そのサンプルの濃度変化をリアルタイムに追跡することも可能である。
【0035】
6.検量線
青色領域6の長さは誘導期間によって変化する。本発明者らは、亜硫酸塩/過酸化水素系自己触媒反応の誘導時間はHRP濃度の負の常用対数値に比例することを認識している。このHRP濃度との相関関係の一致は、流速が一定の場合、距離が時間に比例する式(4)の関係から導くことができる。青色領域6の長さとHRP濃度の対数値の関係は1〜50ppmの間で良好な直線性を示した(図3)。このように、青色領域6の長さはHRP濃度の負の常用対数値に比例した。
なお、図3に係る実施例では、青色領域6の長さとHRP濃度の対数値の関係を示した。このように、管径が一定の場合には、距離(青色領域6の長さ)と誘導期間とが比例関係にあり、これに基づいて、HRP濃度を特定することができる。すなわち、検量線を得ることができる。
しかし、前記したように、管径が変化しても、流量を一定とすれば、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間とが比例関係にあることからHRP濃度を特定することができる。すなわち、流量に基づいて検量線を得ることができる。
例えば、反応時間が遅ければ、反応初期では経路を太くして流速を落とし、反応が現れる頃の到達時間(誘導期間の終了時間)付近では、その反応時間の差を顕著に見るため、半径を細くして、流速を速くするといったように管(チューブ)を構成することもできる。また、管を徐々に細くして、同一流量で引き流速を徐々に速くすることも可能である。このような形態であっても、誘導期間中の全流量を計測することができる。このように、必ずしも流速を一定とせず、流量を一定とし、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間との比例関係からHRP濃度を特定するように実施することも、本発明の技術的範囲に含まれる。
【0036】
7.ブランク反応の抑制
本実施例で用いた、式(1)で表される自己触媒反応は、試薬2、3が混合すると、HRPが存在しなくても、反応が進行する。この、いわゆるブランク反応の影響を軽減するには、試料液4は、試薬と試料液の混合タイミングを近づけることが好ましい。最も好適な方法は、試薬と試料液とを同時に混合することである。
【0037】
次に、図1〜図3について説明した実施例の他、本発明を実施するにあたっての変形例について言及する。
A.複数の試料の計測
複数の試料を計測する場合は、試料液を保持する容器とそれに付随する流路を複数構成し、電磁弁などの流路切りかえ機構を加えて、所望の試料液を送液できるよう、装置を構成すればよい。
【0038】
B.校正機能
本発明の装置の実用化を想定すると、校正機能の実現は重要である。校正機能をもつ装置の構成は、基本的に、上記図1〜図3に係る実施例で用いた装置の構成と同じである。試料液を保持する容器のうち、ひとつに酵素を含まない校正用溶液(ゼロ校正液)を備えれば、それを用いて、ゼロ校正を行うことができる。また、既知の濃度の酵素を含む校正用溶液(スパン校正液)を備えれば、スパン校正を行うことができる。これらのいずれか一方、ないしは両方を備えることで、校正機能を実現できる。
【0039】
C.温度変動の影響排除
自己触媒反応は温度によってその反応速度が影響を受ける。装置を一定温度に調節すれば、周囲温度の影響を避けることが可能である。
また、所定の自己触媒反応について、温度変化が反応速度に与える影響をあらかじめ把握しておけば、装置に温度センサを設けて、その温度によって温度影響を演算で補正することができる。この方式は、装置の温度調節機構を省略できるので、装置の簡略化には好ましい。
【0040】
D.マイクロ化
本発明に係る酵素の計測方法では、測定の間、試薬が消費され続けることになる。試薬消費を抑制するには、計測系のマイクロ化が有効である。マイクロチップフローシステムを実現すれば、環境に与える負荷を軽減した環境調和型の計測方法となることが期待される。
【産業上の利用可能性】
【0041】
特許文献1のバッチ系自己触媒反応を利用したシステムは、誘導期間が終わってから測定結果が分かるというシステムだった。これに対して、本発明に係る酵素の計測方法は、測定中は常に計測結果が現れているため、誘導期間を待つことなく、その場で結果を知ることができる。
【0042】
また、本発明に係る酵素の計測方法では、サンプルを連続的に採取し測定を行うことができる。これにより、サンプル中の酵素濃度の経時変化を追跡することが可能となる。特許文献1の技術では、ただ単に一個のサンプルの濃度を測定していたのに比べて、実用上、大きな効果が期待される。
【0043】
なお、自己触媒反応は反応液の呈色状態の変化として目視でも十分とらえることができ、特別な検出器を必要としない。この特徴は、簡易、ローコストな計測システムを実現する上で、極めて有効である。特許文献1記載の発明で期待できたこの効果は、本発明でも同様に期待することができる。
【0044】
本発明に係る酵素の計測方法および装置は、自己触媒反応系だけでなく、時間計測系を利用したほかの化学計測法、例えば、振動反応系、時計反応系などにも適用が可能である。
【図面の簡単な説明】
【0045】
【図1】本発明に係る酵素の計測方法および装置について、その一実施の形態について概略を示す概念図である。
【図2】HRP濃度を変化させたときの青色領域の長さの変化を示すグラフである。
【図3】HRP濃度と青色領域の長さとの関係を示すグラフである。
【符号の説明】
【0046】
1 プランジャーポンプ
2 BTB/亜硫酸塩水溶液
3 過酸化水素水
4 HRP試料溶液
5 反応コイル
6 青色領域
8、9 ミキサー
10 廃液
【技術分野】
【0001】
本発明は、酵素の計測方法および計測装置に関する。酵素の計測は、例えば、エンザイムイムノアッセイ(EIA)と呼ばれる分析の中で、目的の生物や化学物質を酵素標識し、それを検出する技術として様々な分野で行なわれている。本発明を用いると、酵素を迅速、簡便、高感度に計測することが可能となる。利用分野としては酵素の計測を行う全ての分野が該当し、臨床をはじめ医薬品、製薬、食品、環境分析など広範である。具体的な用途としては、内分泌撹乱性物質(環境ホルモン)の検出や、ホルモン様作用の測定、アトピー性皮膚炎の原因物質特定、スギ花粉の飛散量測定、ウイルスや細菌のような微生物の計測が挙げられる。
【背景技術】
【0002】
イムノアッセイは生体内での特異的な免疫反応である抗原抗体反応を利用した技術であり、アレルギー反応の原因物質、ウイルス、細菌など多様な対象を高い特異性をもって計測できる優れた分析手法である。計測原理は、抗原に結合させた標識物質の量を測ることにより、間接的に測定対象である抗原を定量するというものである。
【0003】
標識物質としては、放射性物質、蛍光物質、発光物質、酵素などが用いられている。特に、酵素を標識とする分析方法はエンザイムイムノアッセイ(EIA)と呼ばれ、他の方法と比較して安全で操作が簡便である上、感度や選択性が高いという特長があり、広く利用されている。 標識酵素の計測方法としては、発色試薬を用いて吸光度を測定する方法や、化学発光を用いる方法が普及している。
【0004】
しかしながら、これらの方法では、計測システム全体に対して、標識酵素の計測系に関わる分析精度、手間、コストの制約が大きいことが問題になっている。これに対して特許文献1に記載されるような先行技術は、代表的な標識酵素であるペルオキシダーゼ(Peroxydase:以下PODと略す)に着目し、PODが触媒として作用する自己触媒反応を利用して、反応が急激に進行するまでの時間(誘導期間)からPODの量を求めるという方法を提供している。この先行技術では、前記PODが触媒として作用する自己触媒反応は、亜硫酸塩・過酸化水素系の反応またはCo−(5−Br−PAPS)2・ペルオキソー硫酸系の反応としている。
【0005】
また、誘導期間の終点は、pHの急激な変化や、Co(5−Br−PAPS)2の分解進行に伴う呈色状態の急変として目視でもとらえることができ、特別な検出装置を必要とせず簡便である。この技術によって、簡易かつローコストな酵素の計測を実現している。
【特許文献1】特開2001−333797号公報
【発明の開示】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1の方法は、反応がバッチ式に進むことから、例えばストップウォッチで時間を測り、誘導期間のあいだ変色を待っていなければならない。また、この先行技術は、一つのサンプルの酵素濃度を測定する方法であり、連続モニタリングができないなど、実用上の制約がある。
【0007】
そこで、本発明では、誘導期間を待つことなく、その場で結果を知ることができ、サンプルを連続的に採取し測定を行うことができ、サンプル中の酵素濃度の経時変化を追跡することを可能とする酵素の計測方法および計測装置を提供することを目的とする。
【課題を解決するための手段】
【0008】
上記目的を達成するために、本発明の請求項1に係る酵素の計測方法は、酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間(誘導期間)にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、試料液に自己触媒反応に関わる試薬を混合し、その混合液を一定の流量で流路に流し、流路中で自己触媒反応を起こさせ、自己触媒反応に伴って流路中で現れる変色の状態から試料液に含まれる酵素の量を求めることを特徴とする。
【0009】
本発明の請求項2に係る酵素の計測方法は、請求項1について酵素の量の計測方法を示したものであり、自己触媒反応に伴って流路中で現れる変色領域の長さ、あるいは、非変色領域の長さのどちらか一方から、試料液に含まれる酵素の量を計測することを特徴とする。
【0010】
本発明の請求項3に係る酵素の計測方法は、請求項1、2の酵素の計測方法を実施するための装置であって、試薬を保持する手段と、試料液を保持する手段と、送液手段と、試薬、試料液およびそれらの混合液を流す流路と、試薬や試料液を混合する手段と、自己触媒反応を検出する手段とを備えることを特徴とする。
【0011】
本発明の請求項4に係る酵素の計測方法は、請求項3について流路の性質を特定したものであり、流路のうち、試薬と試料液の混合液を流す部分が透明であることを特徴とする。
【0012】
本発明の請求項5に係る酵素の計測方法は、請求項4について流路の形状を特定したものであり、流路のうち、試薬と試料液の混合液を流す部分がらせん状構造を有することを特徴とする。
【0013】
本発明の請求項6に係る酵素の計測方法は、複数試料の計測を可能とする発明であり、請求項3〜5に示した装置であって、複数の試料液を保持する手段と、複数の流路とを備えることを特徴とする。
【0014】
本発明の請求項7に係る酵素の計測方法は、校正機能を実現するための発明であり、請求項3〜6に示した装置であって、酵素を含まない校正用溶液(ゼロ校正液)と、既知の濃度の酵素を含む校正用溶液(スパン校正液)とのいずれか一方、ないしは両方を備えることを特徴とする。
【発明の効果】
【0015】
本発明によれば、誘導期間を待つことなく、その場で結果を知ることができ、サンプルを連続的に採取し測定を行うことができ、サンプル中の酵素濃度の経時変化を追跡することを可能とする酵素の計測方法および計測装置が提供される。
【発明を実施するための最良の形態】
【0016】
以下に本発明の実施の形態を述べるが、本発明の適用範囲は、この内容に限定されるものではない。
【0017】
自己触媒反応
自己触媒反応とは、反応進行にともなって、反応物質が増加したり、反応を触媒する物質が増加する化学反応である。
この反応の特徴は、反応進行にともなって、反応速度が指数関数的に増大し、ある時間が経過した時に反応が急激に進むことである。この反応において反応開始剤となる物質(たとえば反応を触媒する酵素)をトリガーと呼ぶ。そして、トリガーの量は反応開始から反応終点までの時間(誘導期間)から求めることができる。自己触媒反応では、混合して反応を開始させても誘導期間は、ほとんど無反応であるかのように進み、このような誘導期間を過ぎて急激に反応が進行すると共に完了する。したがって、誘導期間とは、このように反応物および必要な触媒を混合してから反応が完了するまでの期間であると共に、その期間の経過の直前まで実質的に反応が進行せず、経過時点でほぼ瞬時に反応が完了する期間であることを意味する。
【0018】
自己触媒反応の中でpHの経時変化を利用して反応進行を検出する系として、亜硫酸ナトリウム/過酸化水素反応系がある。この反応系では式(1)の反応が起こり、亜硫酸水素イオン1個が水素イオン1個と反応して、水素イオン2個が生成する。
HSO3- + H2O2 + H+
→ 2H+ + SO42- + H2O ・・・・・(1)
【0019】
生成した水素イオンは式(1)の反応側の要素となることから、反応が進めば進むほど平衡を生成側に押し、反応速度が高まっていく。結果的に、時間が経過するにつれて水素イオンが指数関数的に増加していき、反応溶液のpHは、ある時間(誘導期間)が経過すると急激に低下する。このため、この溶液にpH指示薬、例えばブロモチモールブルー(BTB)を添加しておくと、誘導時間が経過した後、溶液のpH変化に伴って、溶液の色が青色から黄色に瞬時に変化する。この呈色状態の変化は、十分、目視で確認が可能であり、特別な検出装置などを必要としない。
【0020】
自己触媒反応のほかの例としては、Co−(5−Br−PAPS)2 /ペルオキソー硫酸反応系がある。この反応系では式(2)の反応が起こり、Co2+イオンが生成する。
【0021】
【化1】

(2)
Co2+イオンは、式(2)の反応に対して触媒として働くため、結果的に、上記の(1)の反応と同様、反応進行とともに反応速度が高まっていく。Co−(5−Br−PAPS)2 は紫色、その分解生成物は無色であるため、誘導期間が経過した後、紫色だった反応溶液は無色透明になる。
【0022】
上述の2つの自己触媒反応系では、いずれも、酵素ペルオキシダーゼ(POD)の一種であるホースラディッシュペルオキシダーゼ(以下HRPと略)がトリガーとして働く。HRPは、EIAにおいて抗体の標識によく利用される酵素である。自己触媒反応はHRPを微量まで定量可能であり、EIAの信号検知手段として非常に優れている。
【0023】
本発明に係る酵素の計測方法の形態
本発明に係る酵素の計測方法では、自己触媒反応を流路中で行う。自己触媒反応に関わる試薬、および試料液は、ポンプなどを用いて流路に流して混合し、例えば、ガラス棒にポリテトラフロロエチレンチューブをらせん状に巻きつけた流路(コイル)の中に通す。このような形態では、コイルの任意の長さの場所を境に自己触媒反応に伴う変化(例えば溶液の変色)が起こる。
【0024】
例えば、試料液と試薬とを混合した場所をx=0とし、そこから変化が起こる場所までの距離をx、管路の各部における断面積をS(X) 、流量をV(一定)、誘導期間をTとすると、これらの関係は式(3)で表すことができる。
∫S(X) dx = V × T ・・・・・(3)
式(3)において、管路の断面積を一定のSとすると、
S × x = V × T
x = V/S × T
となり、これは、
距離 = 流速 × 時間 ・・・・・(4)
と解釈することもできる。すなわち、流量だけでなく、流速が一定であることを意味する。
式(1)の自己触媒反応にBTBを添加した系を用いた場合、試料液中のHRP濃度が異なると、その濃度の増加とともにガラス棒上の青色バンドの長さが短くなる。それは、HRP濃度の増加に伴って自己触媒反応の速度が向上し、誘導期間が短くなった結果、変化が起こる場所までの距離が短くなるためである。この事実に基づき、自己触媒反応をフロー系で検出する方法を確立したのが本発明である。
【0025】
自己触媒反応はある誘導時間を経た後に反応が急激に進行する。そのため上述のように流路中を所定の流量(管径が一定の領域では一定流速)で流れる反応溶液は、変化が起きる場所までの距離が誘導期間に従属(管径が一定の領域では比例)して変化する。このため、任意の長さの位置で、急激に反応が進行する前の溶液と、進行した後の溶液に分かれる。
管径が一定の場合には、距離と誘導期間とが比例関係にあり、これに基づいて、HRP濃度を特定することができる。
管径が変化しても、流量を一定とすれば、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間とが比例関係にあることからHRP濃度を特定することができる。
本発明者らは、pH変化を利用した自己触媒反応系であるBTB/亜硫酸塩/過酸化水素自己触媒反応を流路に流して行った。その結果、攪拌コイル中の任意の長さを境界として、青色バンドと黄色バンドが現れた。この自己触媒反応系では、ある誘導時間を経て、反応溶液のpHが急激に下降する。そのため、青色バンドの溶液は高pH(反応進行前)の溶液、黄色バンドの溶液は低pH(反応進行後)の溶液に相当する。青色バンドと黄色バンドの境界の位置の変動は6時間の連続運転でおよそ±1mm程度であった。このことから、本発明では、従来の変色時間を目視とストップウォッチで測定するバッチ系自己触媒反応のように、急激に反応が進む瞬間まで溶液を監視する必要はない。
【実施例】
【0026】
次に、本発明に係る酵素の計測方法および計測装置に関し、その実施例と請求項との関係を示し、さらに実施例について説明する。
実施例
1.試薬
BTB、亜硫酸ナトリウム、HRPは和光純薬製を使用した。過酸化水素は関東化学製を使用した。その他の試薬は断りの無い限り市販の特級試薬を蒸留水で希釈して使用した。
【0027】
2.装置
送液手段としては、プランジャーポンプを用いることができる。本実施例では、東京化成製のダブルプランジャー型ポンプTCI−NOX1000ωを2台使用した。プランジャータイプ以外のポンプとしては、流量比保持を重視する場合はペリスタティックポンプが好適であり、微小化を目指すにはピエゾポンプが適している。
【0028】
流路には、ジーエルサイエンス製のポリテトラフロロエチレンチューブ(外径1/16インチ、内径1mm)を使用した。このチューブは半透明であり、流路中の液の色を目視などで検知することができる。また、ポリテトラフロロエチレンチューブをらせん状に巻きつけるために、直径7mm、長さ300mmのガラス管を使用した。チューブをらせん状にすることで、目視観察の際、変色域を認識しやすくなるからである。
【0029】
3.各溶液の調製
亜硫酸塩/BTB水溶液は亜硫酸ナトリウム0.64gとBTB 15mgを蒸留水に溶解し、50mLに希釈し、流路に流す際はこの溶液をさらに5倍に希釈して使用した。過酸化水素水は30%過酸化水素水4mLを蒸留水で100mLに希釈して使用した。
HRP試料溶液は蒸留水で希釈し、HRP濃度100μgL-1に調製したものを母液とし、これをさらに蒸留水で希釈して使用した。
【0030】
4.定量操作
図1に、本発明の実施例であるフローシステム装置の概略を示す。プランジャーポンプ1を用いて、流路AにはBTB/亜硫酸塩水溶液2を、流路Bには過酸化水素水3をそれぞれ流速0.5mL・min-1で流した。同様に、流路CにはHRP試料溶液4を流速1.0mL・min-1で流した。なお、図1の装置は、本発明を実施するための一実施形態であり、本発明を実施するための装置は、図1のものに限定されるものではない。
【0031】
図1の装置では、流路中で混合された溶液は、ガラス棒に巻きつけられた反応コイル5の中を流れる。溶液のpHは、当初、弱アルカリ性であることから、BTBの青色を呈しているが(図中6の領域)、ある長さから先では、自己触媒反応によってpHが急激に低下し、黄色へと変化する(図中7の領域)。このためガラス棒上の反応コイルが変色前の青色領域と変食後の黄色領域とに分かれた様子を目視で判別できる。変色状態の観察は、目視のほか、CCDカメラやCMOSカメラによっても可能であり、ほかには、リニアイメージセンサを利用することもできる。参照番号8、9で示した装置は、試薬と試料液を混合するためのミキサーであり、必要に応じて用いればよい。計測後、廃液10は装置から排出される。
【0032】
本実施例では、図1の装置を用い、反応コイルの左末端から青色と黄色の境界までの長さ、すなわち青色領域6の長さをものさしで測定し、試料液中のHRP濃度の定量を行った。
【0033】
5.HRP濃度と変色域の長さとの関係
本実施例では、試料液中のHRP濃度を0ppm、1ppm、2ppm、1ppm、0ppmと変化させたときに、時間経過に伴ない、青色領域6の長さがどのように変化するかを測定した。結果を図2に示す。HRP濃度が増加すると青色領域6の長さは短くなった。また、濃度が減少して初期の0ppmに戻ると、青色領域の長さは元に戻った。
【0034】
HRPは、過酸化水素が分解されて水素イオンを生成する反応を触媒する。図2の結果から了解されるように、本発明では一つのサンプルの酵素濃度を測定することが可能なだけではなく、そのサンプルの濃度変化をリアルタイムに追跡することも可能である。
【0035】
6.検量線
青色領域6の長さは誘導期間によって変化する。本発明者らは、亜硫酸塩/過酸化水素系自己触媒反応の誘導時間はHRP濃度の負の常用対数値に比例することを認識している。このHRP濃度との相関関係の一致は、流速が一定の場合、距離が時間に比例する式(4)の関係から導くことができる。青色領域6の長さとHRP濃度の対数値の関係は1〜50ppmの間で良好な直線性を示した(図3)。このように、青色領域6の長さはHRP濃度の負の常用対数値に比例した。
なお、図3に係る実施例では、青色領域6の長さとHRP濃度の対数値の関係を示した。このように、管径が一定の場合には、距離(青色領域6の長さ)と誘導期間とが比例関係にあり、これに基づいて、HRP濃度を特定することができる。すなわち、検量線を得ることができる。
しかし、前記したように、管径が変化しても、流量を一定とすれば、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間とが比例関係にあることからHRP濃度を特定することができる。すなわち、流量に基づいて検量線を得ることができる。
例えば、反応時間が遅ければ、反応初期では経路を太くして流速を落とし、反応が現れる頃の到達時間(誘導期間の終了時間)付近では、その反応時間の差を顕著に見るため、半径を細くして、流速を速くするといったように管(チューブ)を構成することもできる。また、管を徐々に細くして、同一流量で引き流速を徐々に速くすることも可能である。このような形態であっても、誘導期間中の全流量を計測することができる。このように、必ずしも流速を一定とせず、流量を一定とし、誘導期間中の全流量を測定し、誘導期間中の全流量と、誘導期間との比例関係からHRP濃度を特定するように実施することも、本発明の技術的範囲に含まれる。
【0036】
7.ブランク反応の抑制
本実施例で用いた、式(1)で表される自己触媒反応は、試薬2、3が混合すると、HRPが存在しなくても、反応が進行する。この、いわゆるブランク反応の影響を軽減するには、試料液4は、試薬と試料液の混合タイミングを近づけることが好ましい。最も好適な方法は、試薬と試料液とを同時に混合することである。
【0037】
次に、図1〜図3について説明した実施例の他、本発明を実施するにあたっての変形例について言及する。
A.複数の試料の計測
複数の試料を計測する場合は、試料液を保持する容器とそれに付随する流路を複数構成し、電磁弁などの流路切りかえ機構を加えて、所望の試料液を送液できるよう、装置を構成すればよい。
【0038】
B.校正機能
本発明の装置の実用化を想定すると、校正機能の実現は重要である。校正機能をもつ装置の構成は、基本的に、上記図1〜図3に係る実施例で用いた装置の構成と同じである。試料液を保持する容器のうち、ひとつに酵素を含まない校正用溶液(ゼロ校正液)を備えれば、それを用いて、ゼロ校正を行うことができる。また、既知の濃度の酵素を含む校正用溶液(スパン校正液)を備えれば、スパン校正を行うことができる。これらのいずれか一方、ないしは両方を備えることで、校正機能を実現できる。
【0039】
C.温度変動の影響排除
自己触媒反応は温度によってその反応速度が影響を受ける。装置を一定温度に調節すれば、周囲温度の影響を避けることが可能である。
また、所定の自己触媒反応について、温度変化が反応速度に与える影響をあらかじめ把握しておけば、装置に温度センサを設けて、その温度によって温度影響を演算で補正することができる。この方式は、装置の温度調節機構を省略できるので、装置の簡略化には好ましい。
【0040】
D.マイクロ化
本発明に係る酵素の計測方法では、測定の間、試薬が消費され続けることになる。試薬消費を抑制するには、計測系のマイクロ化が有効である。マイクロチップフローシステムを実現すれば、環境に与える負荷を軽減した環境調和型の計測方法となることが期待される。
【産業上の利用可能性】
【0041】
特許文献1のバッチ系自己触媒反応を利用したシステムは、誘導期間が終わってから測定結果が分かるというシステムだった。これに対して、本発明に係る酵素の計測方法は、測定中は常に計測結果が現れているため、誘導期間を待つことなく、その場で結果を知ることができる。
【0042】
また、本発明に係る酵素の計測方法では、サンプルを連続的に採取し測定を行うことができる。これにより、サンプル中の酵素濃度の経時変化を追跡することが可能となる。特許文献1の技術では、ただ単に一個のサンプルの濃度を測定していたのに比べて、実用上、大きな効果が期待される。
【0043】
なお、自己触媒反応は反応液の呈色状態の変化として目視でも十分とらえることができ、特別な検出器を必要としない。この特徴は、簡易、ローコストな計測システムを実現する上で、極めて有効である。特許文献1記載の発明で期待できたこの効果は、本発明でも同様に期待することができる。
【0044】
本発明に係る酵素の計測方法および装置は、自己触媒反応系だけでなく、時間計測系を利用したほかの化学計測法、例えば、振動反応系、時計反応系などにも適用が可能である。
【図面の簡単な説明】
【0045】
【図1】本発明に係る酵素の計測方法および装置について、その一実施の形態について概略を示す概念図である。
【図2】HRP濃度を変化させたときの青色領域の長さの変化を示すグラフである。
【図3】HRP濃度と青色領域の長さとの関係を示すグラフである。
【符号の説明】
【0046】
1 プランジャーポンプ
2 BTB/亜硫酸塩水溶液
3 過酸化水素水
4 HRP試料溶液
5 反応コイル
6 青色領域
8、9 ミキサー
10 廃液
【特許請求の範囲】
【請求項1】
酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、
上記試料液に自己触媒反応に関わる試薬を混合して混合液とし、
該混合液を一定の流量で流路に流し、
該流路中で自己触媒反応を起こさせ、
自己触媒反応に伴って上記流路中で現れる変色の状態から上記試料液に含まれる酵素の量を求めることを特徴とする酵素の計測方法。
【請求項2】
自己触媒反応に伴って流路中で現れる変色領域の長さ、または、非変色領域の長さのどちらか一方から、試料液に含まれる酵素の量を計測することを特徴とする請求項1に記載の酵素の計測方法。
【請求項3】
請求項1または2の酵素の計測方法を実施するための装置であって、
上記試薬を保持する手段と、
上記試料液を保持する手段と、
送液手段と、
上記試薬、上記試料液およびそれらの混合液を流す流路と
上記試薬および上記試料液を混合する手段と
自己触媒反応を検出する手段とを備える
ことを特徴とする酵素の計測装置。
【請求項4】
上記流路のうち、上記試薬と上記試料液の上記混合液を流す部分が透明であることを特徴とする請求項3に記載の酵素の計測装置。
【請求項5】
上記混合液を流す部分がらせん状構造を有することを特徴とする請求項4に記載の酵素の計測装置。
【請求項6】
複数の試料液を保持する手段と、
複数の流路と、
該流路の切りかえ機構とを備える
ことを特徴とする請求項3〜5のいずれかに記載の酵素の計測装置。
【請求項7】
酵素を含まない校正用溶液と、
既知の濃度の酵素を含む校正用溶液と
のいずれか一方、または両方を備える
ことを特徴とする請求項3〜6のいずれかに記載の酵素の計測装置。
【請求項1】
酵素が触媒として作用する自己触媒反応を利用し、反応が急激に進行するまでの時間にもとづいて、試料液に含まれる酵素の量を求める酵素の計測方法であって、
上記試料液に自己触媒反応に関わる試薬を混合して混合液とし、
該混合液を一定の流量で流路に流し、
該流路中で自己触媒反応を起こさせ、
自己触媒反応に伴って上記流路中で現れる変色の状態から上記試料液に含まれる酵素の量を求めることを特徴とする酵素の計測方法。
【請求項2】
自己触媒反応に伴って流路中で現れる変色領域の長さ、または、非変色領域の長さのどちらか一方から、試料液に含まれる酵素の量を計測することを特徴とする請求項1に記載の酵素の計測方法。
【請求項3】
請求項1または2の酵素の計測方法を実施するための装置であって、
上記試薬を保持する手段と、
上記試料液を保持する手段と、
送液手段と、
上記試薬、上記試料液およびそれらの混合液を流す流路と
上記試薬および上記試料液を混合する手段と
自己触媒反応を検出する手段とを備える
ことを特徴とする酵素の計測装置。
【請求項4】
上記流路のうち、上記試薬と上記試料液の上記混合液を流す部分が透明であることを特徴とする請求項3に記載の酵素の計測装置。
【請求項5】
上記混合液を流す部分がらせん状構造を有することを特徴とする請求項4に記載の酵素の計測装置。
【請求項6】
複数の試料液を保持する手段と、
複数の流路と、
該流路の切りかえ機構とを備える
ことを特徴とする請求項3〜5のいずれかに記載の酵素の計測装置。
【請求項7】
酵素を含まない校正用溶液と、
既知の濃度の酵素を含む校正用溶液と
のいずれか一方、または両方を備える
ことを特徴とする請求項3〜6のいずれかに記載の酵素の計測装置。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2007−6880(P2007−6880A)
【公開日】平成19年1月18日(2007.1.18)
【国際特許分類】
【出願番号】特願2005−261745(P2005−261745)
【出願日】平成17年9月9日(2005.9.9)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成17年3月11日 社団法人日本化学会発行の「日本化学会第85春季年会 講演予稿集 1」に発表
【出願人】(000005234)富士電機ホールディングス株式会社 (3,146)
【Fターム(参考)】
【公開日】平成19年1月18日(2007.1.18)
【国際特許分類】
【出願日】平成17年9月9日(2005.9.9)
【新規性喪失の例外の表示】特許法第30条第1項適用申請有り 平成17年3月11日 社団法人日本化学会発行の「日本化学会第85春季年会 講演予稿集 1」に発表
【出願人】(000005234)富士電機ホールディングス株式会社 (3,146)
【Fターム(参考)】
[ Back to top ]

