量子触媒およびその製造方法
【課題】効率よく光触媒活性を発現する新規な触媒である量子触媒およびその製造方法を提供する。
【解決手段】本量子触媒は、光触媒活性を発現し得る第1物質と、当該第1物質とは異なる1〜3族および/または5〜7族原子の酸化物である第2物質とが、互いに接合されてなり、第1物質単独の場合に比べ10倍以上に光触媒活性が高められている。
【解決手段】本量子触媒は、光触媒活性を発現し得る第1物質と、当該第1物質とは異なる1〜3族および/または5〜7族原子の酸化物である第2物質とが、互いに接合されてなり、第1物質単独の場合に比べ10倍以上に光触媒活性が高められている。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は新規物質である量子触媒とその製造法に関係する。
【背景技術】
【0002】
量子触媒の第1物質の一例である酸化チタンは、光触媒としてよく知られている。結晶構造がアナターゼ型とブルッカイト型の酸化チタンは、その伝導帯下端と価電子帯上端電位差すなわちバンドギャップ3.2eV以上のエネルギを有する波長が390nmより短い可視光の紫〜波長360nm以下の紫外線(以下、波長390nm以下の可視光の紫〜紫外線を、紫外線等と呼ぶ。)が照射されると、伝導帯に自由電子を価電子帯にホールを生じ、結晶内における自由電子とホールの再結合確率が低く、消滅することなく自由電子とホールを結晶外に放出する。放出されたホールと自由電子が、それぞれ結晶周辺のNOX、SOX、メタンガスなどの温室効果ガスや大気汚染物質、揮発性有機化合物(VOC)、油脂などの脂肪酸、臭気物質およびダイオキシン等を酸化・還元して分解除去することで、大気清浄化、温暖化防止、防汚、消臭、殺菌等、いわゆる光触媒活性を発現する(例えば非特許文献1参照)。
【0003】
周辺の温室効果ガスや大気汚染物質などを酸化・還元など物理的・化学的に作用するとき、物質自身は物理的・化学的に変化せず、外部から与えられるエネルギで半永久的に作用が持続する物質を、触媒と言う。特に、外部エネルギが3.2eV以上の紫外線等を必要とする触媒を光触媒と呼び、本発明に関する触媒を、量子触媒と呼び区別する。また、第2物質が1〜3族原子あるいはその酸化物である量子触媒をn型量子触媒、第2物質が5〜7族の原子あるいはその酸化物である量子触媒をp型量子触媒と呼ぶ。
【0004】
光量子1個が有するエネルギを、アインシュタインは、プランク定数h、波長ν、高速c、振動数λを用いて、E=hν=hc/λなる関係が成立することを明らかにしている。アインシュタインのエネルギ式1から、エネルギE[eV]を有する光量子の波長νは、次に与えられる。
【数1】

【0005】
ここに、
【数2】

【0006】
例えば、エネルギ3.2eVを有する光量子線の波長νは、
【数3】

【0007】
と、略390nmと求まる。略3.4eV以上のエネルギを有する紫外線の最長波長は略360nmであることを考慮すれば、3.2eVエネルギ、波長390nmの光量子線は紫外線に近い紫の可視光であることが知れる。
【0008】
なお、本発明において、ある物質が「光触媒活性を発現し得る」とは、その物質が紫外線、可視光、赤外線、熱線、あるいは量子線などの何らかの光量子エネルギで励起され、励起された結果生じる自由電子とホールが、周辺の物質に物理的、化学的、または生物学的影響を与え得ることを意味する。励起エネルギは酸化・還元作用として現れる場合が多い。従来の光触媒は、励起エネルギを波長390nmの紫色の可視光およびより短波長の紫外線等からエネルギを吸収し光触媒活性を発現するので、「光触媒」と呼ばれている。
一方、後で説明することではあるが、本発明に関する量子触媒は、波長略50μm以下の量子線、可視光、ならびに紫外線等で励起され光触媒活性を発現する物質であるので、「量子触媒」と呼ぶ。
【0009】
光触媒であるアナターゼ型とブルッカイト型の酸化チタンにおいては、水素発生レベルとほぼ等しい−0.2eVに伝導帯の下端が存在し、また、3.0eVに価電子帯の上端が存在し、価電子帯の上端と伝導帯の下端とのエネルギ差(以降、バンドギャップと呼ぶ。)は3.2eVとなる。このバンドギャップ3.2eVを上回るエネルギを有する紫外線等を照射すると、結晶を形成していた一部の電子の束縛が解かれ結晶内を自由に動き回るようになる。
【0010】
結晶を形成するために束縛されていた電子を価電子帯に属すると呼び、結晶内を自由に動き回るようになった電子を伝導帯に属する自由電子と呼ぶ。
価電子帯と伝導帯との間は禁止帯と呼ばれ、電子が存在しない。禁止帯の幅は、バンドギャップと呼ばれる。束縛されていた電子が結晶内を自由に動き回るようになった状態を、励起状態と呼ぶ。
【0011】
結晶を安定に保つためには価電子帯の電子が飛び出した跡に電子を充足する必要があり、近隣原子から電子を奪い取り充足する力が働く。奪い取られた原子は、さらに近隣原子から電子を奪いとる。このように電子の抜け殻であるホールは、再結合するまで結晶内を動き回る。自由電子の移動度(mobility)に比べ、ホールの移動度は若干小さいが略等しく、電子はマイナスの電荷を有し、ホールは電子とは逆のプラスの電荷を有している。
【0012】
再結合して熱となり消滅せず残っている自由電子とホールは、光触媒結晶外に放出されるまで光触媒結晶内を自由に動き回る。自由電子とホールは、光触媒結晶内で再結合され消滅する確率は低い。自由電子は還元リアクションセンターから光触媒結晶外に放出され、光触媒結晶近傍に存在する他の物質を還元する。また、ホールは酸化リアクションセンターから光触媒結晶外へ放出、すなわち光触媒結晶外の電子を取り込み、光触媒結晶近傍に存在する他の物質を酸化する。
【0013】
一方、ルチル型酸化チタンは、水素発生レベルに等しい0eVに伝導帯の下端を、3.0eVに価電子帯エネルギの上端レベルを有し、バンドギャップは3.0eVとアナターゼ型酸化チタンより小さい。ルチル型酸化チタンは、3.0eVの波長410nm以下のエネルギで励起するが、ルチル型酸化チタンの再結合確率はアナターゼ型酸化チタンより大きく自由電子とホールが光触媒結晶内で再結合し熱として消滅する確率が高く、光触媒結晶外へ自由電子とホールを放出する確率が低く、光触媒活性はアナターゼ型酸化チタンに比べ弱い。
【0014】
以下、本発明に関し、光触媒活性を発現し得る光触媒(この光触媒を第1物質として使用する。)として、アナターゼ型酸化チタンについて主に説明するが、ブルッカイト型酸化チタンやルチル型酸化チタンでも、更には、酸化チタン以外の光触媒物質、たとえば、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムからなるグループから選ばれる物質を用いても、光触媒活性を発現するメカニズムや本発明に係る効果は同様であると考えられる。なお、特に断らない限り、以下、アナターゼ型酸化チタンを、単に酸化チタンと略記する場合がある。
【0015】
図1に、酸化チタンが光触媒活性を発現している状態のエネルギダイヤグラムを示す。同図の縦軸はエネルギレベルを意味するポテンシャル電位(eV)を表す。酸化チタンの結晶を構成する束縛されている電子は価電子帯に位置し、自由電子は伝導帯に位置する。価電子帯の下端と伝導帯の上端の間の禁止帯には、電子が存在しない。禁止帯幅、すなわち価電子帯と伝導帯との電位差、バンドギャップが、価電子帯の電子を励起して自由電子とするに必要なエネルギレベルを意味し、図1に示す酸化チタンを励起するには3.2eVのエネルギが必要である。図1に示すように、水の水素発生電位は略0eV、水の酸素発生電位は略1.2eVである。
【0016】
酸化チタンにおいては、自由電子とホールが結晶外部へ放出される確率が高く、結晶外に放出された電子は周辺物質を還元し、結晶外に放出されたホールは周辺物質を酸化する。酸化チタン結晶から外部へ放出される電子の還元作用やホールの酸化作用で、酸化チタン周辺の有機揮発性物質VOC、臭気物質、大気汚染物質NOX,SOX、温室効果ガスや、また環境汚染物質のダイオキシン等、さらに細菌やカビなどが分解除去される。なお、本発明の明細書における「紫外線等」として、390nmの可視光の紫からより波長の短い紫外線、軟X線等を例示することができる。
【0017】
酸化チタンに強い光触媒活性を発現させるには、酸化チタン結晶表面にできるだけ強く紫外線等を照射する必要がある。しかしながら、紫外線等は直進性が強く、かつ物質表面で吸収されやすく、物質内部に到達できない。さらに、影になっている部分に回折して回りこむことは殆ど無い。強い光触媒活性を発現させるためには、酸化チタン結晶を微粒子化して比表面積を大きくしたり、できるだけ多くの粒子が照射されるように酸化チタンの保持方法を工夫したり、吸着剤と組み合わせたりして光触媒活性を効率よく発現させることが考えられるが、十分な解決には至っていない(たとえば特許文献1、非特許文献1、非特許文献2参照)。
【先行技術文献】
【特許文献】
【0018】
【特許文献1】特願2005−281号(特許請求の範囲)
【特許文献2】特願2006−310651号(特許請求の範囲)
【非特許文献】
【0019】
【非特許文献1】「高機能な酸化チタン光触媒〜環境浄化・材料開発から規格・標準化まで〜」、高機能光触媒創製と応用技術研究会編、安保正一監修、NTS出版、初版2004年9月1日、1章1節3〜4、p.10〜15
【非特許文献2】「高機能な酸化チタン光触媒〜環境浄化・材料開発から規格・標準化まで〜」高機能光触媒創製と応用技術研究会編、安保正一監修、NTS出版、初版2004年9月1日、2章5節5、p.110〜114
【発明の概要】
【発明が解決しようとする課題】
【0020】
本発明は、上記問題を解決して、光触媒より効率よく光触媒活性を発現する物質である量子触媒を提供することを目的とする。本発明の更に他の目的および利点は、以下の説明から明らかになるであろう。
【課題を解決するための手段】
【0021】
本発明の一態様によれば、光触媒活性を発現し得る第1物質と、当該第1物質とは異なる4族以外の原子あるいは当該原子の酸化である第2物質とが、互いに接合されてなり、第1物質単独の場合に比べ光触媒活性が高められた量子触媒が提供される。本発明態様により、効率よく励起できる新規な量子触媒を実現できる。
【0022】
光触媒活性が第1物質単独の場合に比べ10倍以上であること、
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にあること、
前記第1物質が、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質であり、前記第2物質が、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウム、5族(5A族)のバナジウム、ニオブ、タンタル、5族(5B族)の窒素、リン、ヒ素、アンチモン、ビスマス、からなる群から選ばれた物質あるいはその酸化物質であること、とりわけ、
前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素であること、および、前記第1物質が酸化チタンであり、前記第2物質が酸化リンであること、
前記第1物質と、前記第2物質とが接合されてなる量子触媒の製造方法であって、
分散剤を加えた溶媒に第1物質の微粒子を分散した第1物質スラリを作製し、
酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を当該第1物質スラリに加え混合スラリを作成、あるいは、
分散剤と酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えた溶媒に第1物質の微粒子を分散した混合スラリを作製して、
必用に応じ当該混合スラリに酸および/または塩基を添加して当該第1物質の微粒子表面に第2物質を析出させた量子触媒を分散した量子触媒スラリを得るに際して、
当該第1物質と分散剤との割合、
当該第1物質の粒径、
当該第1物質スラリおよび/または混合スラリの濃度、
当該第1物質スラリおよび/または混合スラリの温度、
当該第1物質スラリおよび/または混合スラリの撹拌時に照射する超音波の周波数と電力、
当該第1物質スラリのよび/または混合スラリの撹拌時に使用するビーズ径、
当該酸および/または塩基の添加量、
当該酸および/または塩基の濃度、
および
当該量子触媒スラリにおける当該第1物質と当該第2物質の割合からなる群から選ばれた少なくとも一つの条件を選択することにより、
当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、量子触媒の製造方法が提供される。
【0023】
本発明態様により、効率よく励起できる新規な量子触媒の製造方法を実現できる。
【0024】
これらについては、
前記第1物質と分散剤との割合が0.1〜10重量%にすること、
前記第1物質の微粒子の粒径が1nm〜100nmの範囲にすること、
前記第1物質スラリおよび/または混合スラリの濃度を0.1〜35重量%の範囲にすること、
前記第1物質スラリおよび/または混合スラリの温度を1〜35℃の範囲にすること、
前記第1物質スラリおよび/または混合スラリ作成に当たり、周波数19KHz以上の超音波を、第1物質1g当たり0.1Wh〜100Whの強度で照射して攪拌すること、
前記第1物質スラリおよび/または混合スラリ作成に当たり、径0.01〜2mmのビーズを使用して攪拌すること、
前記酸および/または塩基の量を、酸および/または塩基単独で第2物質を析出するに要する量の0〜200%の範囲にすること、
前記混合スラリに添加する酸および/または塩基の溶液量を、第1物質スラリ容積の0.1〜10%の範囲にすること、
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にすること、
特に前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素あるいは酸化リンであることが好ましい。
【発明の効果】
【0025】
本発明により、量子線、熱線や赤外線、ならびに紫外線等の幅広い領域のエネルギを吸収し、強い光触媒活性を発現する新規物質である量子触媒が実現できる。
【図面の簡単な説明】
【0026】
【図1】酸化チタンの光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
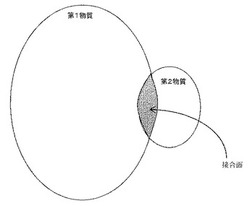
【図2】本発明に係る量子触媒の模式図である。
【図3】酸化チタン結晶のラチスモデル図である。
【図4】チタン原子と酸素原子のモデル図である。
【図5】本発明に係るp型量子触媒結晶のラチスモデル図である。
【図6】ホウ素原子のモデル図である。
【図7】本発明に係るp型量子触媒結晶のラチスモデル図である。
【図8】本発明に係るp型量子触媒の光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
【図9】本発明に係るp型量子触媒の主要製造プロセスを示す図である。
【図10】本発明に係るp型ならびにn型量子触媒の製造方法例における撹拌方法を示す図である。
【図11】本発明に係る酸化チタンスラリ濃度と平均粒径の関係を示す図である。
【図12】本発明に係る分散剤濃度と酸化チタンスラリの平均粒径の関係を示す図である。
【図13】本発明に係る撹拌方法ごとの撹拌時間と酸化チタンスラリ平均粒径の関係を示す図である。
【図14】本発明に係るSTR撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図15】本発明に係るBM撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図16】本発明に係るHG撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図17】本発明に係るNS撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図18】本発明に係る塩酸使用率100%、50%、ならびに0%のp型量子触媒の反応速度比特性を示す図である。
【図19】本発明に係るp型量子触媒の反応速度比とホウ素原子数比との関係を示す特性図である。
【図20】本発明に係るホウ素原子数比100pptのp型量子触媒5Gp−100t/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図21】本発明に係るホウ素原子数比1ppbのp型量子触媒5Gp−1b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図22】本発明に係るホウ素原子数比10ppbのp型量子触媒5Gp−10b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図23】本発明に係るホウ素原子数比100ppbのp型量子触媒5Gp−100b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図24】本発明に係るホウ素原子数比1ppmのp型量子触媒5Gp−1m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図25】本発明に係るホウ素原子数比10ppmのp型量子触媒5Gp−10m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図26】本発明に係るホウ素原子数比100ppmのp型量子触媒5Gp−100m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図27】本発明に係るホウ素原子数比1000ppmのp型量子触媒5Gp−1000m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図28】本発明に係るホウ素原子数比1%のp型量子触媒5Gp−1%/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図29】本発明に係るn型量子触媒結晶のラチスモデル図である。
【図30】リン原子のモデル図である。
【図31】本発明に係るn型量子触媒結晶のラチスモデル図である。
【図32】本発明に係るn型量子触媒の光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
【図33】本発明に係るn型量子触媒の主要製造プロセスを示す図である。
【図34】本発明に係る塩酸使用率100%、50%、ならびに0%のn型量子触媒の反応速度比特性を示す図である。
【図35】本発明に係るn型量子触媒の反応速度比とリン原子数比との関係を示す特性図である。
【図36】本発明に係るリン原子数比100pptのn型量子触媒5Gn−100t/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図37】本発明に係るリン原子数比1ppbのn型量子触媒5Gn−1b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図38】本発明に係るリン原子数比10ppbのn型量子触媒5Gn−10b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図39】本発明に係るリン原子数比100ppbのn型量子触媒5Gn−100b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図40】本発明に係るリン原子数比1ppmのn型量子触媒5Gn−1m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図41】本発明に係るリン原子数比10ppmのn型量子触媒5Gn−10m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図42】本発明に係るリン原子数比100ppmのn型量子触媒5Gn−100m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図43】本発明に係るリン原子数比1000ppmのn型量子触媒5Gn−1000m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図44】本発明に係るリン原子数比1%のn型量子触媒5Gn−1%/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【発明を実施するための形態】
【0027】
以下に、本発明の実施の形態を図、表、式、実施例等を使用して説明する。なお、これらの図、表、式、実施例等および説明は本発明を例示するものであり、本発明の範囲を制限するものではない。本発明の趣旨に合致する限り他の実施の形態も本発明の範疇に属し得ることは言うまでもない。
【0028】
<量子触媒>
本発明に係る量子触媒は、恐らく、図2に示されているように、第1物質と第2物質とが接合して、接合面を実現しているものと思われる。ただし、接合面を実現しているかどうかを証明することは必ずしも本発明の要件ではない。第1物質と第2物質とが互いに接合されていると考えられる結果、第1物質単体の場合に比べ光触媒活性が高められていれば十分である。本発明で開示する量子触媒は、従来の酸化チタンと同じように3.2eV以上の紫外線等から励起エネルギを獲得し光触媒活性を発現することが可能であるが、加えて、1.49〜3.4eV(波長830nm〜360nm)の可視光から励起エネルギを獲得して光触媒活性を発現することも可能である。
【0029】
さらに、例えば第1物質が酸化チタンであり第2物質が3族原子のホウ素の酸化物である場合、第1物質のバンドギャップ中の価電子帯寄りにアクセプタ準位が生じ、アクセプタ準位と価電子帯電位とのエネルギ差の略0.025eV程度の低いエネルギの量子線から励起エネルギを獲得して光触媒活性を発現することが可能となる(かかる量子触媒は、特に、p型量子触媒と呼ぶ。)。あるいは、例えば第1物質が酸化チタンであり第2物質が5族原子のリン酸化物である場合、第1物質のバンドギャップ中の伝導帯電位寄りにドナー準位を設けることができ、ドナー準位と酸化チタンの伝導帯電位とのエネルギ差の略0.025eV程度の低いエネルギの量子線から励起エネルギを獲得して光触媒活性を発現することが可能となる(かかる量子触媒は、特にn型量子触媒と呼ぶ。)。
【0030】
量子触媒は、p型量子触媒とn型量子触媒の2種量子触媒の総称であるが、第2物質を特定する必要がある場合、第2物質が1〜3族原子あるいはその酸化物である量子触媒を「p型量子触媒」と、第2物質が5〜7族原子あるいはその酸化物である量子触媒を「n型量子触媒」と呼び区別する。
【0031】
光触媒である酸化チタンは光触媒活性を発現するためには3.2eV以上の紫外線等の照射を必要としたが、これに対して、本発明で開示する量子触媒は、量子線、熱線や赤外線から紫外線等までの幅広いスペクトラルの光量子線を吸収し光触媒活性を発現できるものであり、可視光や紫外線を遮蔽したいわゆる遮光環境においても光触媒活性を発現する物質である。
【0032】
<p型量子触媒>
本発明に係るp型量子触媒は、光触媒活性を発現し得る第1物質と、1〜3族から選ばれた原子あるいはその酸化物である第2物質とが、互いに接合されてなる物質であり、第1物質単独の場合に比べ光触媒活性が10倍以上高められた物質である。
【0033】
図3に、第1物質として使用する酸化チタン結晶をラチス結晶モデルで示す。図3において、ハッチ付小丸は電子を、白小丸は価電子帯の電子欠乏状態、すなわちホールを示している。ハッチ付小丸と白小丸を通る円は電子の最外殻軌道を示している。同図におけるハッチ付丸は、最外殻軌道等以外の電子軌道や原子核を示し、ハッチ付丸内の文字「Ti」は原子の名称「チタン」、「O」は原子の名称「酸素」を示す。最外殻軌道等として、非遷移原子の最外殻軌道や遷移原子の電子結合に寄与する電子軌道を例示することができる。
【0034】
チタン原子は遷移元素であり、最外殻軌道は電子で満たされており内部軌道が電子で満たされていない原子であるが、ここでは図4aに示すように、4族のチタン原子の最外殻軌道が密では無く4個の電子が存在する最外殻軌道等が存在するものとして説明する。チタン原子の最外殻軌道等が電子で満たされていないとすることで説明の厳密性に欠ける事は否めないが、チタン原子の最外殻軌道等に4個の電子が存在するとして説明しても、本発明の主旨を阻害するものではない。
【0035】
6族の酸素原子は、図4bに示すように最外殻軌道に6個の電子を有している。
図3に戻り酸化チタン結晶を簡単に説明する。原子の最外殻軌道上等に8個の電子が存在(あるいは共有)するか、あるいは全く存在しない場合に、安定した結晶が形成されることは、所謂オクテット理論として周知のところであろう。図3の結晶端を除き、酸素原子の最外殻軌道には8個の電子が存在し、チタン原子の最外殻軌道等に存在する電子は0個であり、安定した結晶を形成する。
【0036】
一方、結晶端では、最外殻軌道が8個の電子で満たされず1個欠如する(1個のホールを有する)酸素原子が6個存在している。さらに、チタン原子の最外殻軌道等に1ないし2個の結晶構成に関与していない、いわゆる自由電子を有するチタン原子が5個存在している。結晶全体では、6個のホールと6個の自由電子が存在し、結晶全体の電荷はホールのプラス電荷と自由電子のマイナス電荷が相殺しゼロとなっている。これらの結晶内の酸素原子の最外殻軌道に存在するホールが酸化リアクションセンターとして、また、結晶内のチタン原子の最外殻軌道等に存在する自由電子が還元リアクションセンターとして機能し、周辺物質を酸化・還元する光触媒活性が発現する。
【0037】
酸化チタンのラチス結晶モデル端ではホールを伴う酸素原子あるいは自由田電子を伴うチタン原子が露出しているので光触媒活性が発現される。しかし、実存する酸化チタン結晶は、ラチス結晶モデルの結晶端の酸素原子のホールが結晶端のチタン原子の自由電子を補足した構造となっており、ホールと自由電子の結合状態に従い、アナターゼ型、ルチル型あるいはブルッカイト型などの立体的な結晶構造を成す。これらの立体構造を成す酸化チタン結晶は、紫外線等を照射されない限り、結晶内に酸化リアクションセンターや還元リアクションセンターが存在せず、光触媒活性を発現しない。3.2eV超エネルギの紫外線等を照射され励起された酸化チタン結晶のチタン原子と酸素原子の電子結合の一部が解離し、酸化リアクションセンターのホールと還元リアクションセンターの自由電子が出現し、強い酸化作用と還元作用を伴う光触媒活性を発現するものと考えられる。
【0038】
かかる観点から、図3に示すラチス結晶モデルは、紫外線等の光エネルギを照射された場合に出現する励起状態にある酸化チタン結晶を模式的に示すものと考えることができる。
【0039】
図5に第1物質である4族原子、3族―5族、あるいは2族-6族の4価化合物(以下、これらを4族原子類と称する)の酸化物(以下、4族原子類酸化物と言う)と第2物質の1例として3族原子の酸化物とが接合面を成す本発明に係るp型量子触媒の模式図をラチス結晶モデルで示す。第1物質の4族原子類酸化物の4族原子の還元リアクションセンターの電子が第2物質の3族原子の酸化物の酸素原子のホールに補足され、第1物質の4族原子類の酸化物の4族原子類に第2物質が結晶成長し、第1物質の結晶構造を保存したまま第2物質を不純物として含む量子触媒が実現される。
【0040】
これら図5はあくまで模式図である。対象となる粒子の1次粒子径が数ナノメートルと小さいため、かつ光触媒活性を発現している場合は動的に結晶構造が変動するものと考えられ、具体的にどのようになっているかは定かでない。
【0041】
本発明に係る量子触媒は、恐らく、第2物質が、第1物質表面に結晶成長した結果、第2物質を不純物として含む第1物質が実現されたものと思われる。第1物質と第2物質が互いに接合されていると考えられる結果、第1物質単独の場合に比べ光触媒活性が10倍以上高められていることが確認できれば十分である。この接合、第1物質と第2物質とが互いに接触した状態にあることを意味し、第2物質が第1物質表面に結晶成長した状態のものや、第1物質が第2物質表面に結晶成長した状態のものや、第2物質と第1物質とのナノレベルの微細結晶が互い接合した状態(以下ナノコンポジット状態と称する)のものを例示することができる。これらは、第1物質の結晶表面に第2物質を析出させるか、第2物質の結晶表面に第1物質を析出させるか、第1物質を析出しうる溶液と第2物質を析出しうる溶液の混合溶液から両物質を析出させ実現できる。第2物質イオンを第1物質にイオンインプラテーションするか、第1物質イオンを第2物質にイオンインプラテーションすることでも実現できるが、結晶構造に歪を与え好ましくないので本発明ではイオンインプランテーションを用いる実現法には言及しない。
【0042】
p型量子触媒における第1物質と第2物質との接合面近傍の結晶模式図を、図5に示す。同5図は、p型量子触媒の動作を説明するためにラチス結晶モデルで単純化した結晶構造を表現したものであり、実際に観測する結晶構造とは異なる場合があるが、将来観測されるようになった場合の観測結果と結晶模式図の相違は本出願の主旨を阻害するものでは無い。
【0043】
図5中、左下がり斜線を施した部分は第1物質を、右下がり斜線を施した部分は第2物質を示し、左下がり斜線部と右下がり斜線部が接する部分が接合面である。同5図は、第2物質の3族原子の酸化物が第1物質の結晶構造を乱す事無く第1物質の不純物となっていることを示している。第2物質として3族原子の酸化物の場合に関してp型量子触媒について説明したが、1〜2族原子の酸化物を第2物質とする場合も同様であり容易に類推できる範疇であるので説明を省略する。
【実施例】
【0044】
次に、第1物質に酸化チタン、第2物質に3族原子の酸化物である酸化ホウ素を用いた量子触媒の製造実施例を説明する。
【0045】
「実施例1」(p型量子触媒の作成)
図6に、第2物質の3族原子として例示するホウ素の原子構造を示す。同図において、図4と同様に、最外殻電子軌道を大きな円で、最外殻軌道上の電子をハッチ付小丸で、ならびに最外殻軌道以外の電子と原子核等をハッチ付丸で模式的に示している。ハッチ付丸の「B」は原子がホウ素であることを示している。
3族のホウ素原子の最外殻軌道には、3個の電子が存在する。
【0046】
図7に第1物質の4族原子類酸化物として例示する酸化チタンを、第2物質として(3族原子の)ホウ素の酸化物である酸化ホウ素を用いる本発明に係るp型量子触媒の模式図をラチスモデルで示す。図7は、第1物質としての酸化チタンのチタン原子のホールに第2物質の酸化ホウ素の酸素原子の電子が捕捉され結晶成長することを示している。同図に示すように本発明で開示するp型量子触媒物質の実施例は、第1物質の酸化チタンと第2物質の酸化ホウ素が接合しており、第2物質のホウ素原子が第1物質の結晶構造を乱す事無く第1物質の不純物となることを示している。
【0047】
酸化ホウ素を酸化チタン表面に結晶成長させると、酸化チタンを種結晶として成長するため、接合面近傍では酸化チタンの結晶構造を継承して第2物質の酸化ホウ素が結晶成長する。酸化ホウ素が結晶成長するとき、酸化チタンの結晶構造が継続されるか、あるいは酸化ホウ素の結晶成長膜厚が単分子層程度と薄膜の場合、p型量子触媒の結晶構造は接合面近傍で連続し、酸化チタンのチタン原子がホウ素原子に置換された結晶構造が実現する。換言すれば、酸化チタン結晶に歪を与えること無く、チタン原子の一部をホウ素原子に置き換えた新しい物質を合成できる。第1物質の酸化チタンのチタン原子がホウ素原子に置き換えられた構造を実現し、第2物質の3族ホウ素を、酸化チタン結晶に歪を与えること無く不純物と為すことができる。
【0048】
3族のホウ素原子の最外殻軌道には電子が3個しか存在していない。量子触媒が完全な結晶構造を成すには、酸素原子の最外殻軌道に8個の電子が配置され、さらにホウ素原子の最外殻軌道に4個の電子が共有された電子配置が必要であるが、図7に示すようにp型量子触媒では、ホウ素原子の外殻軌道で電子が1個欠如し、完全な電子配置にならない。この電子が欠如している場所に周辺原子から電子を補足して完全な電子配置を成す結晶構造となるが、近隣原子から電子を補足することで近隣原子にホールを発生させる。かかる意味から、ホウ素原子の最外殻軌道の電子が欠如している場所に酸化リアクションセンターが生じていると言える。
【0049】
ホウ素原子が近隣原子から電子を補足する作用は、図8に示すように、p型量子触媒の不純物であるホウ素原子が酸化チタンの禁止帯中の価電子帯近くの電位にアクセプタ準位を生じると理解できる。ホウ素原子は、ゲルマニュウム結晶の不純物として、禁止帯中に価電子帯との電位差0.025eVのアクセプタ準位を発生する。ホウ素原子は、酸化チタン結晶の不純物としてゲルマニウム結晶中と同様に、禁止帯中の価電子帯に略0.025eVのアクセプタ準位を生じるものと推察できる。ホウ素原子が酸化チタンの不純物として生じるアクセプタ準位の厳密な値が将来計測され、アクセプタ準位の値が異なっていることが判明しても、本発明の主旨が阻害されるものではなく、ホウ素原子が酸化チタン結晶の不純物としてアクセプタ準位を生じることでp型量子触媒の光触媒活性が第1物質単独の場合に比べ10倍以上に高められていることが示されれば十分である。なお、p型量子触媒の光触媒活性が第1物質単独の場合に比べ10倍以上であることは、反応速度比が1.5以上であることに対応する。
【0050】
「第1物質単独の場合に比べ光触媒活性が高められている」ことは、3族原子の不純物がアクセプタとして機能するため光触媒活性が向上するであろうと推察される。
【0051】
この「光触媒活性が高められている」ことは、第1物質が光触媒活性を発現し得る紫外線等を照射した場合において、基準となる第1物質単独の光触媒活性に対して、p型量子触媒を使用した場合の光触媒活が1倍以上であることと捉えることができる。例えば、光触媒活性が酸化である場合には、その酸化反応で評価し、光触媒活性がある物質の分解である場合には、分解反応で評価することができる。また、反応速度比は、第1物質が光触媒活性を発現し得る紫外線等を照射した場合における、p型量子触媒を使用したときの反応速度(非特許文献2参照。)の、基準となる第1物質単独の反応速度に対する比としてとらえることができる(以下、[量子触媒の反応速度/第1物質単独の反応速度] を反応速度比と呼ぶ。)
【0052】
光触媒活性が酸化である場合には、その酸化反応速度定数の反応速度比で評価し、光触媒活性がある物質の分解である場合には、分解反応の反応速度比で評価することができる。ここで、反応速度比がαである場合、10の2(α-1)乗と一義的に与えられる量βで、光触媒活性はβ倍であると表現できる。例えば、第1物質として光触媒(石原産業製ST−01)はアセトアルデヒドガスを2時間で99%分解するものとし、光触媒の反応速度定比を1とするので、反応速度比1.5に対応する光触媒活性は10の2(1.5−1)乗=10の1乗、すなわち10倍であると一義に与えられる(特許文献2)。
なお、本発明で開示する光触媒の10倍以上の光触媒活性を有する量子触媒は、反応速度定比1.5以上の物質を規定していることになる。
【0053】
第1物質の光触媒活性と本発明に係るp型量子触媒の光触媒活性とを比較する場合、それらの単位重量あたりの光触媒活性を比較する。すなわち、それらの単位重量あたりの反応速度を観る。この比較に使用する光などのエネルギ源については、第1物質が光触媒活性を発現し得る限り特に制限はなく、従来から光触媒の励起に使用し得る紫外線等や可視光の全波長領域について、あるいは赤外線さらには熱源などから発するあらゆる光量子エネルギについて、本発明に係るp型量子触媒の光触媒活性が第1物質単独の場合より大きくなっていることを確認する必要はなく、第1物質単独で光触媒活性を発現する紫外線等の波長範囲を選択した結果、本発明に係るp型量子触媒の光触媒活性が第1物質単独の場合より高くなっていることが確認されれば十分である。
【0054】
紫外線等を照射する場合の反応速度比を比較することは、紫外線等の照射は第1物質である光触媒単独が最大の光触媒活性を発現する場合であることを意味し、光触媒単独の光触媒活性が最大となる場合を選択していることになる。逆に、遮光環境で反応速度を比較する場合は、遮光環境でもp型量子触媒は光触媒活性を発現できるが、第1物質の光触媒単独は光触媒活性を殆ど発現できないため、遮光環境におけるp型量子触媒の反応速度比は無限大となる。可視光の場合は、紫外線照射と遮光環境の中間的な状態と言える。p型量子触媒の反応速度定比が最小となる紫外線等を照射する場合におけるp型量子触媒の光触媒活性を調べれば、p型量子触媒にとっては厳しい評価であり安全サイドの評価となる。かかる観点から、紫外線等を照射した場合におけるp型量子触媒の光触媒活性を評価する。
【0055】
第1物質と第2物質については、第2物質が4族原子酸化物以外という条件を除いて特に制限はない。第2物質は、光触媒活性を有している必要はないが、有していても差し支えない。
【0056】
このような第1物質としては、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウム等からなる群から選ばれた物質を挙げることができる。
【0057】
また、このような第2物質としては、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、プロメトイウム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン、ネプツニウム、プルトニウム、アメリシウム、キュリウム、バークリウム、カリホニウム、アインスタニウム、フェルミウム、メンデレビウム、ノーベリウム、ローレンシウム)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウムからなる群から選ばれた原子あるいはその酸化物質を挙げることができる。
【0058】
この中でも。第1物質が酸化チタンであり、第2物質が酸化ホウ素である組合せが特に好ましい。
【0059】
ホウ素を不純部物とするp型量子触媒の励起に必要最小エネルギ略0.025eVに相当する波長は、アインシュタインのエネルギ式(式1)から49,680nm=49.68μmと与えられる。波長49.68μmは、周波数6.03GHzのサブミリ波の電磁波を意味する。さらに、輻射のピーク波長λが温度Tに反比例することを示すウィーンの変位則を用いて、略0.025eVのエネルギを発する黒体の温度を求める。
【0060】
ウィーンの変位則、
【数4】

【0061】
に、アインシュタインのエネルギ式E=hν、ならびに光量子の速度c=hνの関係式を代入すれば、エネルギと温度の関係は次に求まる。
【数5】

【0062】
続いて、上式に、プランク定数、光速、ならびに電子定数を代入して、禁止帯幅 EeVに対応するエネルギと温度T[K]の関係は定まる。ここに、EJはジュール単位のエネルギを、EeVはeV単位で表現したエネルギ量で、互いに同じエネルギを表す。
【数6】

【0063】
準電位差の略0.025eVを上式に代入すれば、ホウ素原子が励起するに必要な温度は58.3°Kであることが知れる。58.3°Kは−215.9℃であり、ほとんどの自然界全域で、ホウ素原子は励起される。ホウ素原子を不純物とするp型量子触媒は、自然界の略全域において、周辺の熱から十分なエネルギを受け取り励起され、光触媒活性を発現することが明らかになる。
【0064】
遮光環境でも室温程度ならば略0.025eVのエネルギレベルを有する量子線は常に照射されており、p型量子触媒の不純物である酸化ホウ素のホウ素原子のホールは、酸化チタンの価電子帯の電子を補足し、酸化チタンの価電子帯へホールを供給する。一方、不純物のホウ素原子のアクセプタは、酸化チタンの価電子帯から補足した電子を、酸化チタンの伝導帯へ供給する。略0.025eVの低いエネルギを照射されるp型量子触媒は、不純物のホウ素原子のアクセプタ作用で、酸化チタンの伝導帯に自由電子が価電子帯にホールが充足し、p型量子触媒が遮光環境でも強い光触媒活性を発現する。
【0065】
ホウ素原子のアクセプタのこの動作は、略0.025eV以上のエネルギが照射される限り繰り返し遂行される。アクセプタ準位と酸化チタンの価電子順位とのエネルギ差略0.025eVの量子線照射で、酸化チタンが励起され光触媒活性を発現することになる。
【0066】
この様子を更に詳細に説明すると次のようになる。
【0067】
1.第1物質の酸化チタン単体のバンドギャップ3.2eV超のエネルギを有する波長390nm以下の紫外線等を照射する場合
【0068】
紫外線等は、アクセプタ励起エネルギ略0.025eVを超え、第1物質の酸化チタン単独のバンドギャップ値3.2eVも超えるエネルギを有している。したがって、第1物質の酸化チタン単独と、不純物のホウ素原子は、共に励起される。
第1物質において励起された自由電子とホールとは、第1物質の結晶から外部に放出され、第1物質近傍に存在する外部の物質を酸化・還元する光触媒作用を発現する。
第2物質も励起され、アクセプタは第1物質の価電子帯から電子を補足し、補足した電子を第1物質の伝導帯へ注入することで、第1物質単独の光触媒活性を増強する。
【0069】
2.第1物質の酸化チタン単独のバンドギャップ値3.2eV以下で、第2物質のホウ素原子のアクセプタ励起エネルギ略0.025eVを超える(波長49.6μm〜390nmの)量子線、熱線あるいは可視光を照射する場合
【0070】
照射エネルギは酸化チタン単独のバンドギャップ値以下のため、酸化チタン単独では励起されず光触媒活性を発現しない。しかし、照射エネルギは、ホウ素原子のアクセプタ励起エネルギ略0.025eVを超えているので、ホウ素原子は励起され、ホウ素原子のアクセプタは酸化チタンの価電子帯の電子を捕捉し、補足した電子を酸化チタンの伝導帯に注入する。ホウ素原子のアクセプタ経由で自由電子を伝導帯にホールを価電子帯に供給され、酸化チタン単独の励起状態が等価的に実現され、3.2eV超のエネルギが照射された場合と等価な光触媒活性を酸化チタンが発現する。
【0071】
つぎに、本発明に係るp型量子触媒の製造プロセスについて説明する。
【0072】
「実施例2」(p型量子触媒の製造プロセス)
【0073】
光触媒活性を発現し得る第1物質を水などの溶媒に加え第1物質スラリを作製し、当該第1物質スラリに酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えて混合スラリを作成し、必要に応じ当該混合スラリに酸および/または塩基を添加して、当該第1物質の結晶表面に第2物質を析出させる。この操作により、第1物質と第2物質とが接合されてなるp型量子触媒を製造する。
【0074】
第2物質を析出し得る溶液を含む溶媒に第1物質を加え、混合スラリを作成しても構わない。
【0075】
p型量子触媒における当該第1物質と当該第2物質の割合を変えることにより、p型量子触媒の光触媒活性を当該第1物質における光触媒活性より高くすることができることが見出された。典型的には後程説明する図19に示すように、p型量子触媒における第1物質に対する前記第2物質の割合をだんだん多くしていくと、p型量子触媒の光触媒活性(および反応速度比)が上昇後下降して、ピークを示すことが見出された。
【0076】
光触媒活性(反応速度比)が上昇するのは、上述の第2物質の不純物が与えるエネルギ準位によるアクセプタ作用の効果と推定される。一旦上昇しその後下降するのは、恐らく、第1物質と第2物質との接合面積、厚さ、接合していない自由表面の面積等が変化し、これにより第2物質の光触媒活性向上能力が変化するためであろうと考えられる。
【0077】
同様に、分散剤とその濃度、スラリ濃度、スラリ撹拌方法およびスラリ温度などの影響を受け第1物質スラリ中の第1物質の粒子径、添加する酸および/または塩基の量、濃度、および添加速度などが、得られたp型量子触媒の光触媒活性に影響を及ぼし、第2物質が存在しない場合の第1物質単独の光触媒活性より高くする割合が変化することが見出された。なお、上記において「酸および/または塩基」を添加するとしたのは、酸や塩基で第1物質や第2物質を析出させる場合に、その析出速度を調節する等の目的で、酸や塩基単独ではなく、酸と塩基と混合物を使用する場合もあり得るからである。
【0078】
p型量子触媒における第1物質と第2物質の割合は、第1物質1モル部に対して第2物質が1000兆分の1〜1モル部にすることが好ましく、第2物質が1兆分の1〜1モル部の範囲にあることがより好ましい。
【0079】
酸および/または塩基を使用する場合、添加用溶液中の酸および/または塩基の濃度については、100万分の1〜1mol%の範囲にすることが好ましい。更に、第1物質スラリの濃度については、固体物質の濃度が0.1〜35重量%(以下、w%と記述する。)の範囲であることが好ましい。分散剤、スラリの撹拌方法、およびスラリ温度についても光触媒活性に影響を及ぼし得るので、実情に応じて適宜選択することが好ましい。
【0080】
なお、上記とは逆に、光触媒活性を発現し得る第1物質と、3族原子の酸化物である第2物質とが接合されてなるp型量子触媒の製造方法であって、第2物質の粒子を水などの溶液で第2物質スラリを作製し、当該第2物質スラリに酸または塩基による処理により第1物質を析出し得る化合物を含んでなる溶液を加え混合スラリを作成し、当該混合スラリに酸および/または塩基を添加して、当該第2物質の結晶表面に第1物質を析出させ、当該析出に際して、p型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比)、当該酸および/または塩基の濃度、当該酸および/または塩基の添加速度、当該スラリの濃度、当該スラリの撹拌方法、当該スラリの温度ならびに分散剤の種類と量からなる群から選ばれた少なくとも一つの条件を選択することにより、p型量子触媒の光触媒活性を、第1物質単独の光触媒活性より大とする効果が得られることが見出された。
【0081】
次に、本発明に係るp型量子触媒の製造方法について説明する。
【0082】
「実施例3」(p型量子触媒の製造方法)
【0083】
本発明に使用する「第2物質を析出し得る化合物」や「第1物質を析出し得る化合物」については、本発明の主旨に反しない限りどのような化合物を使用してもよい。水酸化物、酸との塩等を好ましく挙げることができる。たとえば第2物質が酸化ホウ素の場合は酸化ホウ素のアルカリ金属塩、メタホウ酸ナトリウム、四ホウ酸ナトリウム、含水鉱物としてのホウ砂等を、第1物質が酸化チタンの場合はチタン酸ナトリウムを例示することができる。四ホウ酸ナトリウムは、化学式B4Na2O7と記述される所謂、ホウ酸ナトリウムであり、ホウ酸ナトリウム1分子は、ホウ素4原子とナトリウム2原子を含む。
【0084】
これらの化合物を溶解するための溶媒は通常水であるが、それ以外のもの、たとえばエタノール等であってもよい。第2物質や第1物質の析出を調整するために複数の溶媒からなる混合溶媒を使用することが有用な場合もあり得る。
【0085】
本発明に係る「第1物質の粒子」や「第2物質の粒子」についてもそのサイズや形状に特に制限があるわけではないが、一般的には、粒子径がナノオーダー、たとえば1次粒径が1〜100nmであることが好ましい。
【0086】
本発明における酸や塩基についても、第1物質や第2物質を析出し得るものであればどのようなものでもよい。酸としては塩酸や硫酸、硝酸を、塩基としては苛性ソーダ等のアルカリ化合物を好ましく例示できる。アルカリ土類金属化合物も使用できる。
【0087】
本発明に係るp型量子触媒の製造方法の概要を、第1物質として酸化チタンを使用し、第2物質として3族原子の酸化物である酸化ホウ素を用いる場合についての1例を、図9に示す。
【0088】
図9工程1の酸化チタンスラリ作成において、粒子径7nm程度の酸化チタンを、界面活性剤を適宜加えた水溶液に加え撹拌して酸化チタンスラリを作製する。次に、同図9工程2の混合スラリ作成において、工程1で作成した酸化チタンスラリに酸化ホウ素のアルカリ金属塩水溶液を加え撹拌して混合スラリを作製する。次に、同9図工程3のイオン交換で、工程2で作製した混合スラリに塩酸を滴下しながら撹拌してイオン交換して酸化ホウ素を酸化チタン粒子の表面に析出させ、酸化チタンと酸化ホウ素とが接合するp型量子触媒スラリを作成する。
【0089】
第2物質の酸化ホウ素のアルカリ金属塩として、酸化ホウ素と水酸化ナトリウムとからなるホウ酸ナトリウムを用いる。酸化ホウ素と水酸化カリウム等のホウ酸アルカリ金属塩等の場合も同様である。また、工程1で作成する酸化チタンスラリは弱酸性を呈し、工程2で加える酸化ホウ素金属塩溶液のアルカリ成分が工程1の酸性成分より多くない場合は、工程2で加える酸化ホウ素アルカリ金属塩溶液を加え撹拌するとき、酸化チタンスラリの酸性成分によりイオン交換され第2物質のホウ酸が第1物質の酸化チタン粒子の表面に析出し、工程3を実施すること無く、p型量子触媒スラリを製造することができる。
【0090】
工程1と工程2を区分する事無く、酸化ホウ素のアルカリ金属塩水溶液を含む溶媒に、界面活性剤を適宜加え、酸化チタン粒子を加え撹拌することで、混合スラリを直接作成しても構わない。
【0091】
次に、本発明に係る撹拌方法について説明する。
【0092】
「実施例4」(撹拌方法)
【0093】
図10に量子触媒の作成に用いる4種の分散方法を模式図で示す。
【0094】
図10(a)は、溶液を回転子で撹拌するSTR撹拌を示す。
【0095】
図10(b)は、溶液に0.5mm径程度のビーズを適量いれ、回転子で撹拌するBM撹拌を示す。量子触媒の合成には、コンタメ成分混入を極力避ける必要があるので、ビーズとして、十分機械的強度が高く、かつ4族のチタンと同じ4族のジルコニウム酸化物のジルコニアビーズを使用することが好ましい。
【0096】
図10(c)は、STR撹拌時に、超音波ホモジナイザを用いて超音波を照射し超臨界場における攪拌を実現するHG撹拌を示す。超音波ホモジナイザとしてBranson社製Sonifierを、超音波周波数として19.9KHzを、超音波照射エネルギとして100Wを、例示することができる。
【0097】
図10(d)は、HG撹拌時に、0.5mm径程度のジルコニアビーズを適量いれ撹拌するNS撹拌を示す。
【0098】
なお、BM攪拌やNS攪拌におけるビーズ量は、効果的に分散できるように適宜調整するものとする。
【0099】
次に、本発明に係る酸化チタンスラリ濃度について説明する。
【0100】
「実施例5」(酸化チタンスラリ濃度)
【0101】
酸化チタンスラリ濃度については、たとえば溶媒が水の場合、濃度は0.1〜35w%程度が好ましい。酸化チタンスラリ濃度は1〜20w%が、より好ましい。酸化チタンは光触媒活性に優れているものを用いることが好ましく、市販品で優れた光触媒活性を発現する石原産業製ST−01、テイカ製TKP−101、アエロジル製P25などを例示することができる。
【0102】
酸化チタンスラリ濃度を、2.5 〜10.0w%の場合について、撹拌時間をパラメータとして、NS拡散の平均粒径を図11に示す。粒径測定には、大塚電子株式会社製濃厚系粒径アナライザーFPRA−1000を使用した。以降、同装置を使用してスラリ粒径を測定する。
【0103】
図11の横軸は、酸化チタンスラリの重量濃度w%を、縦軸は平均粒径nmを表す。酸化チタン1モル部あたり50〜300分(以下、溶質1モルあたりの攪拌時間[分/モル] を、mpmと記述する。)NS攪拌した酸化チタンスラリの平均粒径を、攪拌時間をパラメータとして図11に示す。粒径は50mpm間隔で測定した。図中、NS攪拌時間に対する平均粒径を、50mpmを実曲線、100mpmを破曲線、150mpmを1点鎖曲線、200mpmを2点鎖曲線、250mpmを2重曲線、300mpmを2重破曲線で示す。
【0104】
酸化チタンスラリ濃度が2.5w%の場合、NS撹拌50mpmで163.7nm, 100mpmで144.4nm, 150mpmで138.7nm, 200mpmで166.3nm, 250mpmで131.9nm, 300mpmで125.2nmとなった。NS撹拌200mpmの極大特異点を除き、平均粒径はNS攪拌の経過時間に関して単調に減少した。
【0105】
酸化チタンスラリ濃度が5.0w%の場合、NS撹拌50mpmで175.2nm, 100mpmで147.7nm、150mpmで136.8nm, 200mpmで131.1nm, 250mpmで125.1nm, 300mpmで117.6nmとなった。平均粒径はNS攪の経過時間に関して単調に減少した。
【0106】
酸化チタンスラリ濃度が10.0w%の場合、NS攪拌50mpmで261.3nm, 100mpmで204.5nmと攪拌経過時間に関して平均粒径は減少した。NS攪拌100mpmの平均粒径を極小とし、100mpm以降の平均粒径は攪拌経過時間に関して増大し、150mpmで252.7nm, 200mpmで390.3nm, 250mpmで467.7nm, 300mpmで1334.0nmとなった。
【0107】
次に、本発明に係る分散剤濃度について説明する。
【0108】
「実施例6」(分散剤濃度)
【0109】
酸化チタンスラリの作成において、溶媒が水の場合、分散剤を加えた溶媒に、酸化チタン粉末を加え撹拌することが好ましい。分散剤の使用量は、酸化チタンに対して0.1〜10.0w%を加えることが好ましく、0.2〜4.0w%が、より好ましい。分散剤として酸化チタンの水媒体中の分散特性に優れる界面活性剤を用いることが好ましい。市販の界面活性剤として、花王株式会社製ポリカルボン酸型高分子界面活性剤DEMOL EP、サンノプコ株式会社製ポリカルボン酸アンモニウム塩SNディスパーサント5468等を例示することができる。
【0110】
図12に、酸化チタンに対する分散剤DEMOL EPの濃度を0.2〜4.0w%に関するNS攪拌した酸化チタンスラリの平均粒径を示す。酸化チタンスラリ濃度は5.0w%とした。同図において、横軸は分散剤濃度w%を示し、縦軸は平均粒径nmを示す。
図12において、NS攪拌50mpmの平均粒径を実曲線、100mpmを破曲線、150mpmを1点鎖曲線、200mpmを2点鎖曲線、250mpmを2重曲線、300mpmを2重破曲線で示す。
【0111】
分散剤濃度が0.2w%の場合、NS攪拌50mpmで平均粒径184.7nm、100mpmで178.6nm、150mpmで170.2nmと攪拌経過時間に関して平均粒径は減少し、150mpmで極小平均粒径となった。さらに攪拌を継続すると、攪拌経過時間に関して平均粒径は増大し、200mpmで200.8nm, 250mpmで235.7nm, 300mpmで301.4nmとなった。
【0112】
分散剤濃度が0.4w%の場合、NS攪拌50mpmで平均粒径175.2nm、100mpmで147.7nm、150mpmで136.8nm、200mpmで131.1nm、 250mpmで125.1nm, 300mpmで117.6nmと、攪拌経過時間に関して平均粒径は単調に減少し、300mpmの117.6nmが最小値となった。
【0113】
分散剤濃度が1.2 w%の場合、NS攪拌50mpmで平均粒径165.6nm、100mpmで147.5nm、150mpmで141.9nmと、攪拌経過時間に関して平均粒径は単調に減少した。NS撹拌200mpmで193.1nmと極大値を呈した。さらに、NS撹拌を継続すると、250mpmで141.4nm, 300mpmで145.6nmと、撹拌継続時間に関して緩やかに増大した。
【0114】
分散剤濃度が4.0 w%の場合、NS攪拌50mpmで平均粒径218.0nm、100mpmで192.3nm、150mpmで186.5nm、200mpmで173.9nmと、攪拌継続時間に関して単調に減少し、200mpmで極小値を呈した。さらにNS撹拌を継続すると、250mpmで184.6nm, 300mpmで191.9nmと撹拌時間に関して増大した。
【0115】
次に、本発明に係る酸化チタンスラリの分散特性について説明する。
【0116】
「実施例7」(酸化チタンスラリの分散)
【0117】
図13に、粒径7nmの光触媒酸化チタンST−01と、酸化チタンの0.4w%の分散剤DEMOL EPを、溶媒の逆浸透膜処理水(RO水)に加え、図10に示した4種の攪拌方法で作成した酸化チタンスラリの撹拌継続時間に関する平均粒径特性を示す。酸化チタンスラリ濃度は5.0w%とした。図13の横軸は酸化チタンスラリの撹拌時間mpmを線形スケールで、縦軸は平均粒径nmを対数スケールで表す。
【0118】
図13の曲線は、それぞれ4種の攪拌方法の平均粒径特性を示しており、STR撹拌を実曲線、BM撹拌を破曲線、HG撹拌を1点鎖曲線、NS撹拌を2点鎖曲線で、それぞれ示す。4種の撹拌における酸化チタンスラリの温度を10℃に保ち、50mpm間隔で処理時間600mpmまでの平均粒径を測定した。
【0119】
(STR攪拌)
【0120】
図13の実曲線で示すSTR攪拌の平均粒径は、STR撹拌時間に対して、50mpmで578.5nm、100mpmで653.8nm、150mpmで626.1nm、200mpmで623.0nm、250mpmで523.5nm、300mpmで601.0nm、350mpmで735.9nm、400mpmで584.6nm、450mpmで579.2nm、500分で876.2nm、550mpmで923.6nm、600mpmで809.9nmであった。
【0121】
STR撹拌の平均粒径が、撹拌継続時間に関して単調に減少せず振動しながら変動していることは、STR撹拌の分散力が弱く、酸化チタン粒子間の凝集力に対抗しうる破砕力が実現できず、再凝集していることを示している。
【0122】
STR撹拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図14(a)に、STR撹拌600mpmの散乱強度分布と散乱強度累積を図14(b)に示す。図の棒グラフは散乱強度分布を、曲線は累積を示す。図の横軸は粒径値nmを、左縦軸は散乱強度分布%を、右縦軸は累積%を表す。
【0123】
STR攪拌300mpmの散乱強度分布は、ピーク713.6nmの単峰性を有し、平均粒径は601.0nmであった。STR攪拌600mpmの散乱強度分布は、粒径630.4nmに第1ピーク、2299.7nmに第2ピークを有し、平均粒径は809.9nmであった。
【0124】
(BM攪拌)
【0125】
図13の破曲線は、STR撹拌特性に機械的破砕力を加えたBM撹拌の平均粒径特性を示す。BM撹拌時間に対して、50mpmで390.9nm、100mpmで443.1nm、150mpmで342.9nm、200mpmで340.1nm、250mpmで312.5nm、300mpmで305.1nm、350mpmで301.6nm、400mpmで322.1、450mpmで310.3nm、500mpmで(極小値の)297.7nm、550mpmで299.9nm、600mpmで292.1nmであった。BM攪拌の平均粒径特性のPeak to Peak値は、145.4nmであった。
【0126】
図13に示したように、BM撹拌300mpmの平均粒径305.1nmは、STR撹拌300mpmの601.0nmの略1/2のデメンションとなった。また、300mpmを超えBM攪拌を継続すると、平均粒径290nmをフロワとする略平坦な特性を呈した。略290nmのフロワに沿って平坦な平均粒径特性となることは、STR攪拌との大きな差異であり、ビーズによる機械的破砕力で高次粒子を破砕し、高次粒子の再凝集を防止していると考えられる。
【0127】
BM攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図15(a)に、BM攪拌600mpmの散乱強度分布と累積を図15(b)に示す。BM攪拌300mpmの散乱強度分布は、粒径411.4nmにピークを、平均粒径は305.1nmであった。BM攪拌600mpmの散乱強度分布は、粒径407.2nmにピークを、平均粒径は292.1nmであった。BM撹拌300mpmのピーク粒径が、平均粒径の34.8%大なること、BM撹拌600mpmのピーク粒径が、平均粒径の39.4%大になること、ならびにBM撹拌が長時間になれば解離率が増大することから、ビーズ破砕力が不十分であり、再凝集を十分に防ぎ切れていないことが知れる。
【0128】
(HG攪拌)
【0129】
図13の1点鎖曲線は、HG撹拌の酸化チタンスラリの平均粒径特性を示す。攪拌時間に対して、50mpmで178.6nm、100mpmで144.9nm、150mpmで137.0nm、200mpmで123.1nm、250mpmで129.8nm、300mpmで113.7nm、350mpmで103.1nm、400mpmで103.0nm、450mpmで154.8nm、500mpmで153.9nm、550mpmで143.9nm、600mpmで120.5nmであった。
【0130】
HG撹拌の平均粒径は、若干の変動を除きHG撹拌400mpmまで攪拌継続時間に単調に減少し、400mpmで103.0nmの最小値を呈した。さらに攪拌を継続すると、450mpmで粒径が急激に反転増大し、平均粒径が50.3%増大し、再凝集が強く現れた。
【0131】
HG攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図16(a)に、HG攪拌600mpmの散乱強度分布と累積を図16(b)に示す。HG攪拌300mpmの散乱強度分布は、212.1nmにピークを、平均粒径は113.7nmであった。HG撹拌600mpmの散乱強度分布は、第1ピークが52.3nmに、第2ピークが263.4nmの双峰性を呈し、平均粒径は120.5nmであった。HG撹拌300mpmのピーク粒径の平均粒径に対する解離率が86.5%と大きく、高次粒子の潜在的存在が示されている。HG撹拌600mpmでは、複数のピークが検出され高次粒子の存在が直接確認でき、HG撹拌では、機械的破砕力が弱区、発生する強い再凝集力を抑圧できない。
【0132】
(NS攪拌)
【0133】
図13の2点鎖曲線は、HG撹拌にビーズによる機械的破砕力を加えたNS攪拌の酸化チタンスラリの平均粒径を示す。NS撹拌の平均粒径は、攪拌時間に対して、50mpmで175.25nm、100mpmで147.7nm、150mpmで136.8nm、200mpmで131.1nm、250mpmで125.1nm、300mpmで117.6nm、350mpmで114.0nm、400mpmで110.6nm、450mpmで105.3nm、500mpmで99.4nm、550mpmで99.4nm、600mpmで98.9nmと、攪拌時間に対して単調に減少した。
【0134】
NS攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図17(a)に、NSG攪拌600mpmの散乱強度分布と累積を図17(b)に示す。NS撹拌300mpmの散乱強度分布は、ピークが193.3nm、平均粒径が117.6nmであった。NS撹拌600mpmの散乱強度分布は、ピーク170.1nm、平均粒径98.9nmであった。
【0135】
NS撹拌300mpmと600mpmの散乱強度分布は、共に、単峰性特性であった。NS撹拌300mpmのピーク粒径の平均粒径に対する解離率が64.4%、HG撹拌600mpmの解離率は72.0%と、NS撹拌が長時間程、解離率が増大し、再凝集が発生し、高次粒子が潜在していることが知れ、NS撹拌のビーズ破砕力が、不十分であったことが判明した。
【0136】
図10に示した4種の何れの攪拌方法で作成した酸化チタンスラリを、1次粒子まで分散できなかった。
【0137】
NS攪拌が酸化チタンスラリ平均粒径の最小値98.9nmを提示した。図10に示すビーズ破砕力を増強すれば、酸化チタンスラリの再凝集粒子は分散され、引いては、比表面積の大きな量子触媒を合成することが可能になる。再凝集を阻止する分散手段を採用することで、さらなる比表面積の大なる量子触媒の合成が可能になり、量子触媒の光触媒活性をさらに改善することが可能となるが、本特許で開示する合成方法の主旨を阻害するものではない。再凝集している酸化チタンスラリから量子触媒を合成した場合でも、光触媒活性が第1物質の光触媒単独に比べ10倍以上改善できているならば、本発明の主旨を証明するに十分である。また、1次粒子まで分散した酸化チタンスラリを用いて合成する量子触媒の光触媒活性は、さらに光触媒活性を改善することは容易に推察できる。
【0138】
次に、本発明に係るp型量子触媒の第2物質析出に用いる塩酸量について説明する。
【0139】
「実施例8」(p型量子触媒の第2物質析出)
【0140】
p型量子触媒の主要製造プロセスにおいて、図9に示した工程1で溶媒の水に分散剤と酸化チタン結晶を加え撹拌して酸化チタンスラリを作成し、工程2で当該酸化チタンスラリに酸化ホウ素アルカリ塩溶液を加え撹拌し混合スラリを作成し、工程3のイオン交換工程で当該混合スラリに酸/アルカリを加え第2物質を酸化チタン表面に析出させp型量子触媒スラリを作成する。混合スラリの作成にあたり、溶媒に分散剤、酸化チタン結晶、ならびに酸化ホウ素アルカリ塩溶液を加え撹拌し、酸化チタンスラリを作成すること無く、混合スラリを作成しても構わない。
【0141】
ナノメートルオーダと小さな粒径の酸化チタン結晶は水等の溶媒中で強い凝集力を生じるので、超音波を照射し超臨界場を発生させ、超臨界場中においてジルコニアビーズで撹拌することが好ましい。超音波周波数は、19kH以上が好ましい。超音波照射強度は、溶質1gあたり0.1W〜100Wが好ましい。0.01〜2mm径ジルコニアビーズでビーズ撹拌することが好ましい。酸化チタンスラリ中の酸化チタン濃度は0.1〜35w%が、好ましい。酸化チタンスラリを1〜35℃の範囲に保ちながらNS撹拌することが好ましい。
【0142】
混合スラリ中の酸化ホウ素濃度が、酸化チタン1モル部に対して4000兆分の1〜0.25モル部が好ましい。酸化ホウ素の量は、酸化チタン1モル部に対して酸化ホウ素4兆分の1〜0.025モル部が、より好ましい。酸化ホウ素アルカリ塩溶液の濃度を調整し、混合スラリへの添加容量を混合スラリの1〜10%の範囲にすることが好ましい。
【0143】
酸化ホウ素アルカリ塩としてホウ酸ナトリウムを例示できる。ホウ酸ナトリウム(Na2B4O7)1分子には、ナトリウム(Na)が2原子、ホウ素(B)が4原子含まれているので、混合スラリ中におけるチタン1原子に対するホウ素原子数比 が、1000兆分の1〜1の割合が好ましく、ホウ素原子数比1兆分の1〜1がよりに好ましい。以降、比( ホウ素原子の数/チタン原子の数) を、ホウ素原子数比と呼ぶ。
【0144】
チタン金属の酸化物である酸化チタンの水を溶媒とする酸化チタンスラリは弱酸性を呈し、ホウ酸ナトリウムは弱アルカリ性を呈するので、混合スラリの作成にあたり、ホウ酸ナトリウム溶液をゆっくり滴下することが好ましい。混合スラリ作成にあたり、酸化チタンスラリを10℃前後に保ちNS撹拌しながらホウ酸ナトリウム溶液をゆっくり滴下することが、より好ましい。
【0145】
ホウ酸ナトリウム溶液のアルカリ成分が、酸化チタンスラリの酸性成分に比べ少ない場合は、図9工程3のイオン交換のために塩酸を添加することは必ずしも必要無い。
【0146】
ホウ素原子数比100万分の1の混合スラリを作成し、工程3のイオン交換の塩酸滴下量がp型量子触媒の光触媒活性に及ぼす影響を調べた。
【0147】
図18は、イオン交換に使用した塩酸使用率(100%、50%、0%)をパラメータとして、観測ポイントの反応速度比を示す。ホウ酸ナトリウム1モル部に、ナトリウムが2モル部含まれているので、ナトリウム全量を塩酸で中和するには2モル部の塩酸を要する。この2モル部の塩酸を使用する場合を塩酸使用率100%、その半分の1モル部の塩酸を用いる場合を塩酸使用率50%、塩酸を全く使用しない場合を塩酸使用率0%とした。滴下する塩酸溶液の容積を、酸化チタンスラリ容積の0.1〜10%の範囲にすることが好ましい。
以降、塩酸使用率は、混合スラリに含まれるアルカリ成分を中和するために使用する塩酸の使用率を示すものとする。
【0148】
塩酸使用率100%、50%、0%として作成したp型量子触媒の光触媒活性を測定した。
【0149】
作成したp型量子触媒スラリをシャーレに採り室温乾燥させたサンプルを作成し、略24時間間隔でガスパックA法に準拠してアセトアルデヒドガスの残留濃度比を20回測定した。p型量子触媒ならびに第1物質単独の残留濃度比から反応速度を求め、p型量子触媒の反応速度と第1物質単独の反応速度との比(反応速度定比)を求めた。以降、値(p型量子触媒の反応速度/第1物質単独の反応速度) を反応速度比と呼び、量子触媒がn型の場合は、値(n型量子触媒の反応速度/第1物質単独の反応速度) を反応速度比と呼ぶ。以降、反応速度定比を量子触媒の光触媒活性の評価に使用する。
反応速度定比は、量子触媒の光触媒活性を表現する重要な値である。量子触媒がp型であるかn型であるかは区別しない。さらに、量子触媒の活性が酸化あるいは還元性であるかを区別せず、統一的に光触媒活性を表現する。反応速度は、残留濃度比の対数の定数倍で与えられる。しかし、測定系の特性と対象物質の質量で定まる値であるので、第1物質と量子触媒の残留濃度を同一条件で測定する場合の定数は互いに等しくなり、反応速度定比から測定系と質量で定まる定数は相殺され、量子触媒と第1物質単独の光触媒活性との比を表す量となる。
【0150】
残留濃度比の平均値から求まる反応速度定比を平均反応速度比とした。
p型量子触媒の反応速度比と平均反応速度比を、塩酸使用率をパラメータとして、図18に示す。
【0151】
図18の横軸は、観測ポイントを表し、縦軸は反応速度比を表す。観測ポイント間隔は、略24時間とした。
【0152】
図18の実曲線は、p型量子触媒5Gp-1m/1の反応速度定比特性を示す。名称「5Gp-1m/1」における、「5Gp−1m」は、ホウ素原子数比が1ppm、すなわち100万分の1のp型量子触媒であることを、名称末尾の「/1」は塩酸使用率が100%であることを示す。実曲線上のドットは5Gp-1m/1の反応速度比を、データラベルはその値を示す。
【0153】
5Gp-1m/1の反応速度比は、観測ポイントに対して順に、3.56、2.41、2.32、1.79、2.41、2.91、2.41、2.33、2.71、2.27、2.65、2.33、2.65、2.71、2.94、2.65、3.24、3.00、3.00、3.24であった。第1観測ポイントで最大値3.56を、第4観測ポイントで最小値1.79を呈した。
【0154】
図18の実線は、p型量子触媒5Gp−1m/1の平均反応速度比5Gp-1m/1 Aveを示し、その値は2.64であった。
【0155】
図18の破曲線は、p型量子触媒5Gp-1m/0.5の反応速度比特性を示す。名称「5Gp-1m/0.5」における、「5Gp-1m」はホウ素原子数比が1ppmのp型量子触媒であることを、「/0.5」は塩酸使用率が50%であることを示す。破曲線上のドットは反応速度比を、データラベルはその値である。
【0156】
5Gp-1m/0.5の反応速度比は、第1観測ポイントの2.36、第16観測ポイントならびに第20観測ポイントの2.33を下限とし、第6観測ポイントの最大値3.53との間で変動した。
【0157】
図18の破線は、p型量子触媒5Gp−1m/0.5の平均反応速度定比5Gp-1m/0.5 Aveを示し、その値は2.76であった。
【0158】
図18の1点鎖曲線は、p型量子触媒「5Gp-1m/0」の反応速度比特性を示す。名称「5Gp―1m/1」における、「5Gp-1m」はホウ素原子数比が1ppmのp型量子触媒であることを、「/0」は塩酸使用率が0%であることを示す。1点鎖曲線上のドットは反応速度比の観測値、データラベルはそのデータ値である。
【0159】
5Gp-1m/0の反応速度比は、第1観測ポイントの2.36、第13観測ポイントならびに第14観測ポイントの2.59を下限とし、第9観測ポイントの最大値3.44との間を変動した。
【0160】
図18の1点鎖線は、量子触媒5Gp−1m/0の20観測ポイントの平均反応速度比5Gp-1m/0 Aveを示し、その値は2.92であった。
【0161】
p型量子触媒5Gp-1m/1 Ave、5Gp-1m/0.5 Ave、ならびに5Gp-1m/1 Aveの平均反応速度比が2.61、2.76、5、ならびに2.92であり、塩酸を使用しない5Gp-1m/0 Aveの平均反応速度比が最大となることが判明した。
【0162】
p型量子触媒5Gp-1m/0の最小反応速度比、平均反応速度比、最大反応速度比は、それぞれ2.36、2.92、3.44であり、光触媒活性が第1物質の酸化チタン単独の場合に比べ525倍、6918倍、7万5858倍であった。
【0163】
p型量子触媒5Gp-1m/0の光触媒活性は、最悪の場合でも、第1物質の酸化チタン単独の525倍あり、量子触媒の制約条件である10倍以上を保証している。
【0164】
p型量子触媒5Gp-1m/0が3種の塩酸使用率で最も大きな反応速度比を与えるように、ホウ素原子数比が1ppm、すなわち100万分の1と十分小さい場合、塩酸によるイオン交換は必ずしも必要では無く、金属酸化物である酸化チタンの水スラリが呈する酸成分で、十分に第2物質の酸化ホウ素アルカリ金属塩のナトリウムを中和し、イオン交換できることが判明した。かかる塩酸使用率が小さい場合、図9の工程3のイオン交換のための塩酸添加を実行する必要が無く、工程2の混合スラリ作成時にp型量子触媒が合成され、塩酸などの酸化チタンと酸化ホウ素以外の物質の混入を防止できる高純度なp型量子触媒スラリを合成できる利点に加え、大きな平均反応速度比値を獲得できる優れたp型量子触媒合成手段を提供できる利点が生じる。
【0165】
次に、本発明に係るp型量子触媒のホウ素原子数比に対する反応速度定比特性について説明する。
【0166】
「実施例9」(p型量子触媒のホウ素原子数比特性)
【0167】
p型量子触媒または酸化チタンST−01の各10mgを、5Lのテドラーバッグに入れ、80〜100重量ppm濃度に調整した標準ガス(窒素キャリアガス、アセトアルデヒド標準ガス)を3L注入し、照射強度1.0mW/平方cmの紫外線を照射し、20分経過後の残留濃度をガス検知管(ガステック社製 No.92M)で測定した。酸化チタンST−01を基準光触媒として求めた反応速度比を、図19に示す。
【0168】
紫外線光源として、東芝ライテック社製ブラックライトFL40SBLを用い、コニカ・ミノルタ社製UV RadioMeterUM−10、受光部同社製UM−360にて量子触媒表面の紫外線強度を測定した。
【0169】
同一重量を用いて同一環境で残留濃度を測定する場合、測定対象のp型量子触媒に含まれる第1物質である酸化チタン量は、第1物質以外の物質の重量分だけ少なくなる。また、第1物質以外の物質である酸化ホウ素は、光触媒活性をほとんど発揮しないことが知られている。このような条件で、p型量子触媒の光触媒活性が第1物質の光触媒活性を上回ること、すなわちp型量子触媒の反応速度比が1を上回ることは、これまで知られていなかった。これは、既述のごとく、第2物質が不純物としてアクセプタ準位を第1物質のバンドギャップに付与し、第1物質へ自由電子とホールとが効果的に注入され、これによって第1物質の表面から放出される自由電子とホールとの量が増大し、酸化チタンの有する光触媒活性を上回る光触媒活性を獲得することを明確に示すことになる。
【0170】
ホウ素原子数比が、100ppt(=100億分の1)、1ppb(=10億分の1)、10ppb(=1億分の1)、100ppb(=1000万分の1)、1ppm(=100万分の1)、10ppm(=10万分の1)、100ppm(=1万分の1)、1000ppm(=0.001)、ならびに1%(=0.01)の場合について、第4の形態のp型量子触媒の製造方法に示した手順に従い、p型量子触媒5Gp―100t/1、5Gp―1b/1、5Gp―10b/1、5Gp―100b/1、5Gp―1m/1、5Gp―100m/1、5Gp―1000m/1、および5Gp―1%/1を作成した。
【0171】
これらp型量子触媒の名称は、上記と同様であり、例えば名称「5Gp―100t/1」における、「5Gp―100t」は、ホウ素原子数比が100億分の1、すなわち100pptのp型量子触媒であることを、「/1」は塩酸使用率が100%であることを示す。
【0172】
図9工程1における酸化チタンスラリ濃度は、工程1の水と分散剤と工程2で印加するホウ酸ナトリウム溶液と第3工程で滴下する塩酸溶液に含まれる水を勘案し10w%となるように調整、NS撹拌を150mpm、分散剤Demol EP量は酸化チタン重量の0.4%とした。
【0173】
図9工程2における(四)ホウ酸ナトリウム溶液は、液量が酸化チタンスラリ容量の略3%となるように濃度を調整、NS撹拌を50mpmとした。
【0174】
第3工程の希塩酸量を酸化チタンスラリ容量の略0.5%になるように濃度を調整、NS撹拌を25mpmとした。
【0175】
図19に、作成したp型量子触媒5Gp―100t/1、5Gp―1b/1、5Gp―10b/1、5Gp―100b/1、5Gp―1m/1、5Gp―10m/1、5Gp―100m/1、5Gp―1000m/1、および5Gp―1%/1のホウ素原子数比に対する反応速度比特性を示す。図19の横軸はホウ素原子数比を示し、単位pptは1兆分の1、ppbは10億分の1、ppmは100万分の1、%は0.01を表す。
【0176】
作成した濃度10w%のp型量子触媒スラリ100mgをシャーレに採り室温乾燥させたp型量子触媒10mgを用いて、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を、略24時間の間隔を置き30回測定した。30回計測した残留濃度比の算術平均に対する反応速度比を平均反応速度比5Gp/1-Aveとした。平均反応速度比を、図19の実曲線で示す。実曲線5Gp/1-Ave上のドットの横位置はホウ素原子数比を、その縦位置は平均反応速度比を、データラベルは反応速度比の値を示す。
【0177】
同19図の1点鎖曲線5Gp/1−worstは、最小反応速度比を示す。30回計測した残留濃度比の最大値に対する反応速度比を最小反応速度比とした。1点鎖曲線5Gp/1−worst上のドットの横位置はホウ素原子数比を、縦位置は最小反応速度比を、データラベルは最小反応速度比の値を示す。
【0178】
同図19の破曲線5Gp/1−bestは、最大反応速度比を示す。30回計測した残留濃度比の最小値に対する反応速度比を最大反応速度比とした。破曲線5Gp/1−best上のドットの横位置はホウ素原子数比を、縦位置は最大反応速度比を、データラベルは最大反応速度比の値を示す。
【0179】
繰り返し30回計測して、計測上の擾乱要因を除去し、ホウ素原子数比100ppt〜1%に関するp型量子触媒5Gp−100t/1〜5Gp−1%/1の反応速度比値の信頼度を高めた。計測間隔は、略24時間であった。
【0180】
図19の平均反応速度比5Gp/1−ave、最大反応速度比5Gp/1−best、ならびに最小反応速度比5Gp/1−worstが示すように、ホウ素原子数比が変化すると、反応速度比すなわち光触媒活性が敏感に変化することが見出された。
【0181】
具体的には、図19の5Gp/1−aveが示すように、p型量子触媒のホウ素原子数比に対する平均反応速度比は、ホウ素原子数比が100pptの場合2.29、1ppbの場合2.60、10ppbの場合2.72、100ppbの場合3.35、1ppmの場合3.21、10ppmの場合2.73、100ppmの場合2.63、1000ppmの場合2.55、1%の場合2.63であった。p型量子触媒のホウ素原子数比が100ppb〜1ppm前後における平均反応速度比は3.35〜3.21の最大な値を示した。平均反応速度定比の3.35は、光触媒活性が第1物質の酸化チタン単独の5万119倍であることを示すものである。
【0182】
また、図19に示すようにホウ素原子数比1ppt〜1%の領域におけるp型量子触媒の平均反応速度定比は1以上であり、第1物質の酸化チタン単独の光触媒活性を上回っていた。
【0183】
図19の最大反応速度比5Gp/1−bestが示すように、p型量子触媒のホウ素原子数比に対する最大反応速度比は、100pptの場合3.03、1ppbの場合3.27、10ppbの場合4.58、100ppbの場合4.67、1ppmの場合5.08、10ppmの場合3.71、100ppmの場合3.34、1000ppmの場合3.71、1%の場合3.27であった。ホウ素原子数比が1ppmの最大反応速度比5.08が最大であった。最大反応速度定比5.08は、光触媒活性が1億4454万3977倍であることを示す。
【0184】
図19の最小反応速度比5Gp/1−worstに示すように、p型量子触媒のホウ素原子数比に対する最小反応速度比は、100pptの場合1.65、1ppbの場合1.70、10ppbでの場合2.21、100ppbの場合2.68、1ppmの場合2.59、10ppmの場合2.13、100ppmの場合2.24、1000ppmの場合1.91、1%の場合1.91であった。p型量子触媒のホウ素原子数比が100pptの最小反応速度比1.65が最小であった。最小反応速度比1.65は第1物質の酸化チタン単独の光触媒活性の20倍であることを示す。ホウ素原子数比100ppt〜1%の領域におけるp型量子触媒の光触媒活性は、光触媒の20倍以上あり、本発明で開示するp型量子触媒は第1物質の酸化チタンの10倍以上の光触媒活性を最悪の場合でも保障することが知れた。
【0185】
ホウ素原子数比が1pptのp型量子触媒の反応速度定比は、最大値5.08、最小2.59、平均3.21であり、光触媒活性は第1物質の酸化チタンの光触媒活性の最大1億4千万倍強、最小1500倍強、平均2万6千倍強であることが判明した。
【0186】
作成したp型量子触媒スラリ5Gp―100t/1〜5Gp―1%/1粒径の散乱強度分布と累積の測定結果を、図20〜28に示す。
【0187】
図20にp型量子触媒スラリ5Gp−100t/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100t/1は、813.6nmに散乱強度ピークを有し、平均粒径は395.9nmであった。
【0188】
図21にp型量子触媒スラリ5Gp−1b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1b/1は、53.8nmに第1、390.4nmに第2、2625.8nmに第3の散乱強度ピークを有し、平均粒径は409.7nmであった。
【0189】
図22にp型量子触媒スラリ5Gp−10b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−10b/1は、86.8nmに第1、1164.7nmに第2の散乱強度ピークを有し、平均粒径は572.9nmであった。
【0190】
図23にp型量子触媒スラリ5Gp−100b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100b/1は、528.2nmに第1、4295.0nmに第2の散乱強度ピークを有し、平均粒径は801.7nmであった。
【0191】
図24にp型量子触媒スラリ5Gp−1m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1m/1は、927.9nmに散乱強度ピークを有し、平均粒径は801.7nmであった。
【0192】
図25にp型量子触媒スラリ5Gp−10m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−10m/1は、300.5nmに散乱強度ピークを有し、平均粒径は159.1nmであった。
【0193】
図26にp型量子触媒スラリ5Gp−100m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100m/1は、1860.7nmに散乱強度ピークを有し、平均粒径は778.8nmであった。
【0194】
図27にp型量子触媒スラリ5Gp−1000m/1の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1000m/1は、202.5nmに散乱強度ピークを有し、平均粒径は125.6nmであった。
【0195】
図28にp型量子触媒スラリ5Gp−1%/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1%/1は、49.9nmに第1、378.4nmに第2、2560.6nmに第3、4万7162.1nmに第4の散乱強度ピークを有し、平均粒径は2112.1nmであった。
【0196】
p型量子触媒における当該第1物質と当該第2物質の割合については特に制限はないが、p型量子触媒における第1物質に対する第2物質の比率をだんだん多くしていくと、p型量子触媒の反応速度比(言い換えれば光触媒活性)が上昇後下降するか、あるいは反応速度比が1以上で上昇下降を繰り返して、1個以上のピークが存在することが見出されており、ある範囲内にあることが好ましいと言えよう。一般的に言えば、p型量子触媒におけるホウ素原子数比が1000兆分の1〜1の範囲にあることが好ましく、ホウ素原子数比が1兆分の1(1ppt)〜1の範囲にあることがより好ましい。
【0197】
以下、光触媒活性が、第1物質単独の場合に比べ高くなるメカニズムについて説明する。ただし、以下の説明は本発明の理解を助けるためのものであり、本発明の範囲を制限するものではない。
【0198】
図7に示したように、接合面では酸化チタンのチタン原子と酸化ホウ素の酸素原子が電子を共有し、チタン原子とホウ素原子が酸素原子を挟み互いに接合されている。換言すれば、接合面において、ホウ素原子が酸化チタン結晶に直接接した結晶構造が構築され、第2物質のホウ素原子は、酸化ホウ素分子の励起エネルギより低い励起エネルギでアクセプタとして励起する。以降、第2物質の酸化ホウ素の励起エネルギを略0.025eVと記述するのは、前述の考察に基づくものであるが、この考察結果は本発明の本質とは関係が無く、p型量子触媒が量子線で励起するという物理現象を解析した一例として記述したものである
【0199】
次に、本発明に係るn型量子触媒について説明する。
【0200】
<n型量子触媒>
【0201】
本発明に係るn型量子触媒は、光触媒活性を発現し得る「いわゆる光触媒」である第1物質と、5族〜7族から選ばれた原子あるいはその酸化物である第2物質から成る物質であり、光触媒活性が第1物質単独の10倍以上の物質である。
【0202】
図29に第1物質である4族原子類酸化物と第2物質の5族原子の酸化物とが接合して成る本発明に係るn型量子触媒の模式図をラチス結晶モデルで示す。
【0203】
第1物質の4族原子類酸化物の酸素原子の最外殻軌道のホールに第2物質の5族原子酸化物の5族原子の電子が捕捉され、第1物質の4族原子類酸化物の酸素原子に第2物質が結晶成長し、第1物質の結晶構造を保存したまま、第1物質と第2物質が接合するn型量子触媒が実現される。
【0204】
図29はあくまで模式図である。対象となる粒子の1次粒子径が数ナノメートルと小さいため、かつ光触媒活性を発現している場合は動的に結晶構造が変動するものと考えられ、具体的にどのようになっているかは定かでない。
【0205】
本発明に係るn型量子触媒は、恐らく、図29に示すように、第2物質が、第1物質表面に結晶成長した結果、第2物質が接合面を成しているものと思われる。第1物質が第2物質と接合面を成していると考えられる結果、第1物質単独の場合に比べ光触媒活性が高められていることが確かめられれば十分である。この接合は、第1物質と第2物質とが互いに接触した状態にあることを意味し、第2物質が第1物質表面に結晶成長した状態のものや、第1物質が第2物質表面に結晶成長した状態のものや、第2物質と第1物質とのナノコンポジット状態のものを例示することができる。これらは、第1物質の結晶表面上に第2物質を析出させるか、第2物質の結晶表面上に第1物質を析出させるか、第1物質を析出しうる溶液と第2物質を析出しうる溶液の混合溶液から両物質を析出させる。また、結晶構造に歪を与えるので好ましくないが、イオン打ち込み技術で第2物質イオンを第1物質にイオンインプラテーションするか、イオン打ち込み技術で第1物質イオンを第2物質にイオンインプラテーションすることでも実現できる。
【0206】
n型量子触媒における第1物質と5族原子酸化物を不純物として含む接合面近傍の結晶構造を示す模式図29は、n型量子触媒の動作を説明するためにラチス結晶モデルで単純化した結晶構造を表現したものであり、実際に観測する結晶構造とは異なる場合があるが、将来観測されるようになった場合の観測結果と結晶模式図の相違は本特許の主旨を阻害するものでは無い。
【0207】
図29の左下がり斜線を施した部分は第1物質を、右下がり斜線を施した部分は第2物質を示し、左下がり斜線部と右下がり斜線部が接する部分が接合面であり、第2物質の5族原子が第1物質の結晶構造を乱す事無く第1物質の不純物として接合している。
【0208】
次に、本発明に係るn型量子触媒の作成について説明する。
【0209】
「実施例10」(n型量子触媒の作成)
【0210】
図30に、第2物質の5族原子酸化物として例示する酸化リンのリン原子構造を示す。同図において、図4と同様に、最外殻電子軌道を大きな円で、最外殻軌道上の電子をハッチ付小丸で、ならびに最外殻軌道以外の電子と原子核等をハッチ付丸で模式的に示している。ハッチ付丸の「P」は、原子名「リン」を示す。
【0211】
図31に第1物質の4族原子類酸化物として例示する酸化チタンを、第2物質の5族原子酸化物として例示する酸化リンから成る本発明に係るn型量子触媒の模式図をラチスモデルで示す。同図は、第1物質の酸化チタンの酸素原子の酸化リアクションセンターに第2物質のリン原子の電子が捕捉され結晶成長した量子触媒の一種であるn型量子触媒を、ラチス結晶モデルを示した図である。同図は本発明の一例として開示するn型量子触媒であり、第1物質の酸化チタンと第2物質の酸化リンが接合面を成し、接合面近傍において、第2物質のリン原子が第1物質の結晶構造を乱す事無く第1物質の不純物となっていることを示す。
【0212】
第2物質の酸化リンが第1物質の酸化チタンに結晶成長した場合、接合面近傍では第1物質の酸化チタンの結晶構造を第2物質が継承する。本発明が開示するように、第1物質の結晶サイズが数ナノメートルと小さく、かつ第2物質である酸化リンのリン原子数に対する第1物質の酸化チタンのチタン原子数に対する比が1000兆分の1〜0.1の範囲と小さい場合、第1物質を種結晶として第2物質を結晶成長させると第1物質の結晶構造が継承される。以降、(リン原子の数/チタン原子の数)を、リン原子数比と呼ぶ。
【0213】
第1物質の結晶構造が継続されるか、あるいは第2物質の膜厚が単分子層程度と薄膜の場合などでは、n型量子物質の結晶構造は接合面近傍で連続的となり、第1物質のチタン原子が第2物質のリン原子に置換された構造になるものと理解できる。換言すれば、酸化チタン結晶に歪を与えること無く、チタン原子の一部をリン原子に置き換えた物質が実現されることになる。この物質をマクロに捉えると、第1物質の酸化チタン結晶バルク中のチタン原子がリン原子に置き換えられた構造を成し、第2物質のリン原子が酸化チタンの不純物となっていると解釈できる。
【0214】
図30に示したように、5族のリン原子の最外殻軌道には電子が5個存在しているため、図31に示すn型量子触媒の結晶において、リン原子の外殻軌道に結晶構築に関与していない過剰な電子が1個存在することになる。この過剰な電子が酸化チタンの禁止帯中の伝導帯近くにドナー準位を生じる。
【0215】
リン原子は、ゲルマニュウム結晶の不純物として機能するとき、禁止帯中に伝導帯との電位差0.025eVのドナー準位を発生する。酸化チタン結晶の不純物として機能するリン原子は、ゲルマニウム結晶中と同様に、禁止帯中の伝導帯と略0.025eV差のドナー準位を生じるものと想定できる。リン原子の酸化チタンの不純物として機能するドナー準位の厳密な計測は別途に委ねるものとするが、ドナー準位の厳密な値を測定しないことが本発明の主旨を阻害するものでは無く、リン原子が酸化チタンの不純物としてドナー準位を生じ、ドナー準位が生じた結果、n型量子触媒物質の光触媒活性が第1物質の酸化チタン単独の場合に比して改善されることが示されれば十分である。特に、光触媒活性が第1物質単独の場合に比して10倍以上改善される場合、n型量子触媒と呼ぶことにする。
【0216】
第1物質の光触媒活性と本発明に係るn型量子触媒の光触媒活性とを比較する場合、それらの単位重量あたりの光触媒活性を比較する。すなわち、それらの単位重量あたりの反応速度を観る。この比較に使用する光などのエネルギ源については、第1物質が光触媒活性を発現し得る限り特に制限はなく、従来から光触媒の励起に使用し得る紫外線等や可視光の全波長領域について、あるいは赤外線さらには熱源などから発するあらゆる光量子エネルギについて、本発明に係るn型量子触媒の光触媒活性が第1物質単独の場合より大きくなっていることを確認する必要はなく、第1物質単独で光触媒活性を発現する紫外線等の波長範囲を選択した結果、本発明に係るn型量子触媒の光触媒活性が第1物質単独の場合より高くなっていることが確認されれば十分である。紫外線等を照射する場合の反応速度比を比較することは、紫外線照射は第1物質である光触媒単独が最大の光触媒活性を発現する場合であることを意味し、光触媒単独の光触媒活性が最大となる場合を選択していることになる。逆に、遮光環境で反応速度を比較する場合は、遮光環境ではn型量子触媒は光触媒活性を発現できるが、第1物質の光触媒単独は光触媒活性を殆ど発現できないため、遮光環境におけるn型量子触媒の反応速度比は無限大となる。可視光の場合は、紫外線照射と遮光環境の中間的な状態と言える。n型量子触媒の反応速度定比が最小となる紫外線等を照射する場合におけるn型量子触媒の光触媒活性を調べれば、n型量子触媒にとっては厳しい評価であり安全サイドの評価となる。かかる観点から、紫外線等を照射した場合におけるn型量子触媒の光触媒活性を評価することにする。
【0217】
第1物質と第2物質については、第2物質が4族原子酸化物以外という条件を除いて特に制限はない。第2物質は、光触媒活性を有している必要はないが、有していても差し支えない。
【0218】
このような第1物質としては、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質を挙げることができる。
【0219】
また、このような第2物質としては、当該第1物質とは異なる5A族のバナジウム、ニオブ、タンタル、5B族の窒素、リン、ヒ素、アンチモン、ビスマスからなる群から選ばれた物質あるいはその酸化物質を挙げることができる。この中でも。第1物質が酸化チタンであり、第2物質が酸化リンである組合せが、より好ましい。
【0220】
n型量子触媒の励起に必要最低エネルギの略0.025eVに相当する波長は、アインシュタインのエネルギ式(式1)から49,680nm=49.68μmと与えられるように、ほぼ6.03GHzのサブミリ波の電磁波に相当する。さらに、輻射のピーク波長λが温度Tに反比例することを示すウィーンの変位則を用いて、略0.025eVのエネルギを発する黒体の温度を求める。
【0221】
ウィーンの変位則、
【数7】

【0222】
に、アインシュタインのエネルギ式E=hν、ならびに光量子の速度c=hνの関係式を代入すれば、エネルギと温度の関係が次のように求まる。
【数8】

【0223】
続いて、上式に、プランク定数、光速、ならびに電子定数を代入すれば、禁止帯幅 EeVに対応するエネルギは温度T[K]の関係で与えられる。ここに、EJはジュール単位のエネルギを、EeVはeV単位で表現したエネルギ量で、互いに同じエネルギを表す。
【数9】

【0224】
電位差の略0.025eVを上式に代入すれば、第2物質が励起するに必要な温度は58.3°Kとなる。58.3°Kは−215.9℃であり、ほとんど自然界全域で第2物質のリン原子のドナーは励起されていることが知れる。第2物質のリン原子を不純物として含むn型量子触媒は、自然界の略全域において、周辺の熱から十分なエネルギを受け取り励起され、光触媒活性を発現することが示され、自然界の略全域でn型量子触媒が光触媒機能を発現することが明らかになる。
【0225】
室温程度の常温環境ならば略0.025eVのエネルギレベルを有する量子線は常に照射されており、n型量子触媒の不純物であるリン原子は励起されドナーとして機能し、酸化チタンの伝導帯へ電子を供給し、酸化チタンの価電子帯から電子を補足、酸化チタンの価電子帯から電子を補足することで酸化チタンの価電子帯へホールを供給する。
【0226】
略0.025eVのエネルギが照射されるn型量子触媒は、不純物のリン原子のドナー機能で、酸化チタンの伝導帯に自由電子が価電子帯にホールが充足し、n型量子触媒が強い光触媒活性を発現するようになる。
【0227】
図32に示すように、略0.025eV超のエネルギを有する波長49.6μm以下の量子線や赤外線、波長830〜390nmの可視光が照射されると、リン原子はドナーとして機能し、酸化チタンの伝導帯へ自由電子が供給され、さらにドナーは酸化チタンの価電子帯から電子を補足する。酸化チタンの価電子帯から電子を捕捉することは、酸化チタンの価電子帯にホールを供給することを意味する。
【0228】
このリン原子のドナー機能は、略0.025eV以上のエネルギが照射される間継続する。換言すれば、ドナー準位と酸化チタンの伝導帯とのエネルギ差略0.025eVの量子線が照射されると、酸化チタンが等価的に励起され光触媒活性を発現する。
【0229】
この様子を更に詳細に説明すると次のようになる。
【0230】
1.第1物質のバンドギャップ3.2eV超のエネルギを有する波長390nm以下の紫外線等を照射する場合
【0231】
照射光は、第1物質の酸化チタンのバンドギャップ値3.2eV超のエネルギを有し、ドナー励起エネルギ略0.025eVも超えている。したがって、第1物質の酸化チタン自身も、不純物のリン原子のドナーも、共に励起される。
第1物質で励起された自由電子とホールとは、第1物質の結晶から外部に放出され、第1物質近傍に存在する外部の物質を酸化・還元する光触媒作用を発揮する。
第2物質のドナーが励起され、第1物質の伝導帯へ自由電子が注入し、かつ価電子帯へホールが注入することで、第1物質の光触媒活性が増強される。換言すれば、第1物質単独の場合よりn型量子触媒の光触媒活性が増強されることは、リン原子のドナー機能に由来すると理解できる。
【0232】
2.第1物質のバンドギャップ値3.2eV以下で、第2物質のリン素原子のドナー励起エネルギ略0.025eV超の波長49.6μm〜390nmの熱線あるいは可視光などの量子線を照射する場合
【0233】
照射量子線のエネルギは第1物質のバンドギャップ値3.2eVを超えていないため、第1物質の酸化チタンは励起されず、酸化チタン単独では光触媒活性を発現できない。しかし、照射エネルギが第2物質のリン原子のドナー励起エネルギ略0.025eVを超えているため、第2物質のドナーが励起され、電子を第1物質の酸化チタンの伝導帯に注入し、さらに、第1物質の酸化チタンの価電子帯の電子を捕捉することで価電子帯にホールを注入する。
第1物質の酸化チタン単独では略0.025eVの低いエネルギでは励起されないが、第2物質のドナー準位を中継し、電子が酸化チタンの価電子帯から伝導帯へ移動することで、等価的に3.2eV超のエネルギが照射された酸化チタンの励起状態が実現されることになる。
第2物質の酸化リン単独では、第1物質のような強い光触媒活性を有さないが、第2物質のリン原子がドナーとして機能して、第1物質の酸化チタンへ光触媒活性の原動力のホールと自由電子を供給し、光触媒活性を発現する。たとえば、第1物質が酸化チタン、第2物質が酸化リンの場合、酸化リンは酸化チタンのような強い光触媒活性を有していないが、酸化リンのリン原子が量子触媒物質中で励起されドナーとして機能することで、接合面で接触する第1物質の酸化チタンの伝導帯へ自由電子を、価電子帯へホールを注入する。
【0234】
このようにして、第1物質の酸化チタン単独では量子線のような略0.025eVという低いエネルギによって直接的には励起されないが、第2物質のリン原子のドナー機能を介して自由電子とホールとが供給され、供給された自由電子とホールを第1物質の結晶表面から外部に放出することで、第1物質の酸化チタンが光触媒として作用するようになる。この結果、第1物質の酸化チタンのバンドギャップ以下エネルギの量子線しか照射されない遮光環境においても、n型量子触媒は光触媒作用を発現する。
【0235】
次に、本発明に係るn型量子触媒の製造プロセスについて説明する。
【0236】
「実施例11」(n型量子触媒の製造プロセス)
【0237】
本発明に係るn型量子触媒の製造方法において、光触媒活性を発現し得る第1物質と、当該第1物質にドナーを付与する5族原子の酸化物である第2物質とが接合されてなるn型量子触媒を以下に示すプロセスに従い製造する。
【0238】
第1物質の粉末を溶媒に加えて第1物質スラリを作製し、当該第1物質スラリに酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えて混合スラリを作成し、必要に応じ当該スラリに酸および/または塩基を添加して、当該第1物質の表面に第2物質を析出させる。この操作により、第1物質と第2物質とが接合されてなるn型量子触媒スラリが作成される。
【0239】
本発明に係るn型量子触媒の製造方法における第2物質を析出させる際、n型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比あるいは原子数比)を変えることにより、n型量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より高くすることができることが見出された。典型的には後程説明する図35に示すように、n型量子触媒における第1物質に対する前記第2物質をだんだん多くしていくと、n型量子触媒の光触媒活性(光触媒活性を一義的に与える反応速度比)が上昇後下降して、ピークを示すことが見出された。
【0240】
反応速度比が上昇して第2物質が存在しない場合の第1物質の反応速度より高くなるのは、上述の第2物質の不純物のエネルギ準位によるドナー効果と推定される。一旦上昇しその後下降するのは、恐らく、第1物質と第2物質との接合面積、厚さ、接合していない自由表面の面積等が変化し、これにより第2物質の光触媒活性の増強能力が変化するためであろうと考えられる。
【0241】
同様に、分散剤とその濃度、スラリ濃度、スラリ撹拌方法およびスラリ温度などの条件で変化するスラリ中の第1物質粒子径、添加する酸および/または塩基の量、濃度、および添加速度などが、得られたn型量子触媒の光触媒活性に影響を及ぼし、第2物質が存在しない場合の第1物質における光触媒活性をより強くすることができることが見出された。なお、上記において「酸および/または塩基」を添加するとしたのは、酸や塩基で第1物質や第2物質を析出させる場合に、その析出速度を調節する等の目的で、酸や塩基単独ではなく、酸と塩基と混合物を使用する場合もあり得るからである。
【0242】
n型量子触媒における当該第1物質と当該第2物質のモル比としては、n型量子触媒における前記第1物質1モル部に対して、第2物質が1000兆分の1〜0.1モル部にすることが好ましく、第2物質が1兆分の1〜0.01モル部の範囲にあることがより好ましい。
【0243】
酸および/または塩基を使用する場合、添加用溶液中の酸および/または塩基の濃度については、100万分の1〜1mol%の範囲にすることが好ましい。更に、スラリ濃度については、固体物質の濃度が1〜25w%の範囲であることが好ましい。スラリの撹拌方法、およびスラリ温度についても光触媒活性に影響を及ぼし得るので、実情に応じて適宜選択することが好ましい。
【0244】
なお、上記とは逆に、光触媒作用を発現し得る第1物質と、5族原子の酸化物である第2物質とが接合されてなるn型量子触媒の製造方法であって、第2物質の粉末を水などの溶媒でスラリを作製し、当該スラリに酸または塩基による処理により第1物質を析出し得る化合物を含んでなる溶液を加え混合スラリを作成し、当該混合スラリに酸および/または塩基を添加して、当該第2物質の表面に第1物質を析出させn型量子触媒を溶質とするn型量子触媒スラリを作成する。当該析出に際して、n型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比あるいは原子数比)、当該酸および/または塩基の濃度、当該酸および/または塩基の添加速度、当該スラリの濃度、当該スラリの撹拌方法、当該スラリの温度ならびに分散剤の種類と量からなる群から選ばれた少なくとも一つの条件を選択することにより、n型量子触媒の光触媒活性を、第2物質が存在しない場合の当該第1物質における光触媒活性を高らしめる、n型量子触媒の製造方法でも、同様の効果を得ることができる。
【0245】
本方法に係る発明に使用する第1物質および第2物質については、上記のn型量子触媒に係る発明で説明したと同様に考えることができる。
【0246】
次に、本発明に係るn型量子触媒の製造方法について説明する。
【0247】
「実施例12」(n型量子触媒の製造方法)
【0248】
本発明に使用する「第2物質を析出し得る化合物」や「第1物質を析出し得る化合物」については、本発明の主旨に反しない限りどのような化合物を使用してもよい。水酸化物、酸との塩等を好ましく挙げることができる。たとえば第2物質が酸化リンの場合は酸化リンのアルカリ金属塩であるリン酸ナトリウム(第1リン酸ナトリウム:NaH2PO4、第2リン酸ナトリウム:Na2HPO4、第3リン酸ナトリウム:Na3PO4)、リン酸カルシウム等を例示することができ、第1物質が酸化チタンの場合はチタン酸ナトリウム等を例示することができる。
【0249】
これらの化合物を溶解するための溶媒は通常水であるが、それ以外のもの、たとえばエタノール等であってもよい。第2物質や第1物質の析出を調整するために複数の溶媒からなる混合溶媒を使用することが有用な場合もあり得る。
【0250】
本発明に係る「第1物質の粒子」や「第2物質の粒子」についてもそのサイズや形状に特に制限があるわけではないが、一般的には、1次粒子径がナノオーダー(たとえば1〜100nm)の粒子であることが好ましい。
【0251】
本発明における酸や塩基についても、第1物質や第2物質を析出し得るものであればどのようなものでもよい。酸としては塩酸や硫酸、硝酸を、塩基としては苛性ソーダ等のアルカリ化合物を好ましく例示できる。アルカリ土類金属化合物も使用できる。
【0252】
本発明に係るn型量子触媒の製造に関して、第1物質として酸化チタンを使用し、第2物質として5族リンの酸化物である酸化リンを使用する場合の製造方法を、図33に示す。
【0253】
酸化チタンスラリ作成の工程1において、1次粒子径7nm程度の酸化チタン粒子を、分散剤を適宜加えた水溶媒に加え撹拌して酸化チタンスラリを作製する。次いで混合スラリ作成の工程2において、工程1で作成した酸化チタンスラリに酸化リンのアルカリ金属塩水溶液を加え撹拌して混合スラリを作製する。さらに次いで、イオン交換の工程3において、工程2で作製した混合スラリに塩酸を滴下しながら撹拌してイオン交換して酸化リンを酸化チタン微粒子の表面に析出させ、酸化チタンと酸化リンとが接合したn型量子触媒を溶質とするn型量子触媒スラリを作成する。
【0254】
第2物質の酸化リンのアルカリ金属塩として、酸化リンと水酸化ナトリウムとからなる第2リン酸ナトリウムNa2HPO4を用いた。酸化リンと水酸化カリウム等のリン酸アルカリ金属塩等の場合も同様である。また、工程1で作成する酸化チタンスラリは弱酸性を呈し、工程2で加える酸化リン金属塩溶液のアルカリ成分が工程1の酸性成分より多くない場合には、工程2で加える酸化リンアルカリ金属塩溶液を加え撹拌するとき、酸化チタンスラリの酸性成分によりイオン交換され第2物質の酸化リンが第1物質の酸化チタン粒子表面に析出するので、工程3を実行することは必ずしも無く、n型量子触媒スラリを製造することができる。
【0255】
次に、本発明に係るn型量子触媒の第2物質析出に用いる塩酸量について説明する。
【0256】
「実施例13」(n型量子触媒の第2物質析出)
【0257】
n型量子触媒の主要製造プロセスの工程1において酸化チタンスラリを作成、同工程2において酸化チタンスラリに酸化リンアルカリ塩溶液を加え撹拌し混合スラリを作成、同工程3において混合スラリに酸/アルカリを加え第2物質を酸化チタン表面に析出させたn型量子触媒スラリを作成する。
【0258】
酸化チタン粒子は水等の溶媒中では強い凝集力を生じるので、超音波を照射し超臨界場を発生させ、超臨界場でジルコニアビーズ撹拌することが好ましい。超音波は、19kH以上が好ましい。超音波照射量は、溶質1gあたり0.01W〜100Wが好ましい。0.01〜2mm径ジルコニアビーズでビーズ撹拌することが好ましい。酸化チタンスラリ中の酸化チタン濃度は0.1〜35w%が好ましい。酸化チタンスラリを1〜35℃に保ちNS撹拌することが好ましい。
【0259】
酸化リンのアルカリ塩として第2リン酸ナトリウム(Na2HPO4)を例示できる。
【0260】
たとえば水を溶媒とする場合、酸化チタン1モル部に対する酸化リン1000兆分の1〜0.1モル部が好ましく、酸化チタン1モル部に対する酸化リン1兆分の1〜0.01モル部がより好ましい。第2リン酸ナトリウム(Na2HPO4)1分子には、ナトリウム(Na)が2分子、水素が1原子、酸化リン(PO3)が1分子すなわちリン原子(P)が1原子含まれているので、n型量子触媒の酸化チタン1モル部に対する酸化リンのモル部の比の値は、リン原子数と酸化チタンのチタン原子数との比に一致する。以降、比 (リン原子の数/チタン原子の数)を、リン原子数比と呼ぶ。
すなわち、混合スラリ中のリン原子数比が1000兆分の1〜0.1が好ましく、リン原子数比が1兆分の1〜0.01がより好ましい。
【0261】
チタン金属の酸化物である酸化チタンの水スラリは弱酸性を呈し、第2リン酸ナトリウム(Na2HPO4)は弱アルカリ性を呈するので、混合スラリの作成にあたり、第2リン酸ナトリウム(Na2HPO4)溶液をゆっくり滴下することが好ましい。混合スラリ作成にあたり、酸化チタンスラリを10℃に保ちNS撹拌しながら第2リン酸ナトリウム(Na2HPO4)溶液をゆっくり滴下することが、より好ましい。
【0262】
第2リン酸ナトリウム(Na2HPO4)溶液のアルカリ成分が、酸化チタンスラリの酸性成分に比べ、少ない場合は、図33工程3の塩酸を滴下してイオン交換する必要は必ずしも無い。
【0263】
リン原子数比100万分の1(1ppm)のn型量子触媒スラリの具体例を示す。
【0264】
混合スラリを工程3においてイオン交換するに当たり、滴下塩酸量のn型量子触媒の反応速度比に及ぼす影響を調べた。図34は、イオン交換に使用した塩酸使用率(100%、50%、0%)をパラメータとして、反応速度比の時間経過特性を示す。
【0265】
例えば、第2リン酸ナトリウム(Na2HPO4)1モル部を含む混合スラリには、ナトリウムが2モル部含まれることになる。当該混合スラリのナトリウム全量を塩酸でイオン交換する場合には、2モル部の塩酸が必要になる。ナトリウムに対する塩酸のモル割合を塩酸使用率と定義しているので、2モル部の塩酸を使用してイオン交換する場合は塩酸使用率100%、半量の1モル部の塩酸を用いる場合は塩酸使用率50%、塩酸を全く使用しない場合は塩酸使用率0%となる。
【0266】
リン原子数比1ppmの混合スラリを塩酸使用率100%、50%および0%としてイオン交換して、3種のn型量子触媒5Gn−1m/1,5Gn−1m/0.5,5Gn−1m/0を作成した。
【0267】
作成したn型量子触媒スラリをシャーレに採り室温乾燥させたサンプルを作成し、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を20回測定し、残留濃度から反応速度比を、また残留ガス濃度の平均から平均反応速度比を求めた。求めたn型量子触媒の反応速度比と平均反応速度比を、塩酸使用率をパラメータに採り、図34に示す。図34の横軸は、観測ポイントを表し、縦軸は反応速度比を表す。観測ポイント間隔は、略24時間であった。
【0268】
図34の実曲線は、n型量子触媒5Gn-1m/1の特性を示す。名称「5Gn-1m/1」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/1」は塩酸使用率が100%であることを示す。
【0269】
図34の実曲線上のドットはn型量子触媒5Gn-1m/1の反応速度比を、データラベルは反応速度比の値を示す。
【0270】
5Gn-1m/1の反応速度比は、第1〜20観測ポイントで、順に2.74、2.97、2.97、2.74、2.74、3.27、3.47、2.68、2.97、2.74、2.62、2.43、2.68、3.03、3.03、3.10、3.34、3.10、3.34、2.81であり、最大2.97と最小2.43の間で変動していた。
【0271】
20観測ポイントの残留濃度比の平均値に対する反応速度定比を平均反応速度比とした。同34図の実線はn型量子触媒5Gn-1m/1の平均反応速度比5Gn-1m/1 Aveを示し、その値は2.90であった。
【0272】
図34の破曲線は、n型量子触媒5Gn-1m/0.5の特性を示す。名称「5Gn−1p/05」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/0.5」は塩酸使用率が50%であることを示す。破曲線上のドットはn型量子触媒5Gn-1m/0.5の反応速度比、データラベルは反応速度定比の値を示す。
【0273】
5Gn-1m/0.5の反応速度比は、第1〜第20観測ポイントで、順に3.03、2.74、3.03、3.64、3.03、3.03、3.47、3.27、3.03、2.43、2.37、2.30、2.74、2.68、2.74、3.34、2.74、2.74、2.43、3.03であり、最大3.64と最小2.30の間で変動していた。同34図の破線は、n型量子触媒5Gn-1m/0.5の平均反応速度比5Gn-1m/0.5 Aveを示し、その値は2.84であった。
【0274】
図34の1点鎖曲線は、n型量子触媒5Gn-1m/0の特性を示す。名称「5Gn−1p/05」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/0」は塩酸使用率が0%であることを示す。同34図1点鎖曲線上のドットはn型量子触媒5Gn-1m/0の反応速度比、データラベルは反応速度定比の値を示す。
【0275】
5Gn-1m/0の反応速度比は、第1〜20観測ポイントで、順に3.47、2.74、2.74、3.03、3.80、3.03、2.74、2.68、2.74、2.37、2.43、2.43、2.74、2.74、2.74、2.74、2.81、2.74、3.47、3.47であり、最大3.80と最小2.37の間で変動していた。同34図の1点鎖線は、n型量子触媒5Gn-1m/0の平均反応速度比5Gn-1m/0 Aveを示し、その値は2.82であった。
【0276】
塩酸使用率を100%、50%、0%のn型量子触媒5Gn-1m/1、5Gn-1m/0.5、5Gn-1m/0の平均反応速度比は、それぞれ、2.90、2.83、2.82であり、塩酸使用率50%と0%では大きな差異は認められなかったが、塩酸使用率100%が最大の平均反応速度定比を与えることが知れた。
【0277】
n型量子触媒5Gn-1m/1の反応速度比の最大、平均、最小値はそれぞれ3.47、2.90、2.43であり、光触媒活性が第1物質の酸化チタン単独の場合の最大8万7千倍強、平均6千3百倍強、最小724倍であることが知れた。n型量子触媒5Gn-1m/1の光触媒活性は、第1物質の酸化チタン単独の10倍以上であることを保障することが判明した。
【0278】
次に、本発明に係るn型量子触媒のリン原子数比に対する反応速度定比特性について説明する。
【0279】
「実施例14」(n型量子触媒のリン原子数比特性)
【0280】
n型量子触媒または第1物質単独(酸化チタンST−01)の各10mgを、5Lのテドラーバッグに入れ、80〜100重量ppm濃度に調整した標準ガス(窒素キャリアガス、アセトアルデヒド標準ガス)を3L注入し、照射強度1.0mW/平方cmの紫外線を照射し、20分経過後の残留濃度をガス検知管(ガステック社製 No.92M)で測定し、残留濃度と初発濃度との比(残留濃度比)を求め、n型量子触媒の反応速度と酸化チタンの反応速度の比[p型量子触媒の反応速度/酸化チタンの反応速度]を、反応速度定比とした。
【0281】
n型量子触媒の反応速度比を図35に示す。
【0282】
n型量子触媒としての量は一定10mgであった。紫外線光源として、東芝ライテック社製ブラックライトFL40SBL2本点灯し、コニカ・ミノルタ社製UV RadioMeterUM−10、受光部同社製UM−360を用いて照射面にて紫外線強度を測定した。
【0283】
同一重量を用いて同一環境で残留濃度を測定する場合、測定対象のn型量子触媒に含まれる第1物質である酸化チタン量は、第1物質以外の物質の重量分だけ少なくなる。また、第1物質以外の物質である酸化リンは、光触媒活性をほとんど発現しないことが知られている。このような条件で、n型量子触媒の光触媒活性が第1物質の光触媒活性を上回ること、すなわち、n型量子触媒の反応速度比が1を上回ることは、これまで知られていなかった。これは、前述のごとく、第2物質の酸化リンのリン原子が酸化チタンの不純物として酸化チタンのバンドギャップにドナー準位を生じ、略0.025eV以上のエネルギを吸収したリン原子のドナーが酸化チタンへ自由電子とホールを注入するようになり、酸化チタンの表面から自由電子とホールが放出さるようになる結果、酸化チタン単体の光触媒活性を上回る光触媒活性を実現したものと考えられる。
【0284】
リン原子数比が、100ppt(=100億分の1)、1ppb(=10億分の1)、10ppb(=1億分の1)、100ppb(=1000万分の1)、1ppm(=100万分の1)、10ppm(=10万分の1)、100ppm=(1万分の1)、1000ppm(=0.001)、ならびに1%(=0.01)の場合について、第13の形態のn型量子触媒の製造プロセスに示した手順に従い、n型量子触媒5Gn―100t/1、5Gn―1b/1、5Gn―10b/1、5Gn―100b/1、5Gn―1m/1、5Gn―10m/1、5Gn―100m/1、5Gn―1000m/1、および5Gn―1%/1を作成した。
【0285】
これらn型量子触媒の名称は、上記と同様であり、例えば名称「5Gn―100t/1」の「5Gn―100t」は、リン原子数比が100pptすなわち100億分の1であるn型量子触媒であることを、「/1」は塩酸使用率が100%であることを示す。
【0286】
図33工程1における酸化チタンスラリ濃度を、工程1の水成分と分散剤と工程2で印加するリン酸ナトリウム溶液と第3工程で滴下する塩酸溶液に含まれる水成分を勘案し、重量濃度が10w%となるように調整、NS撹拌を150mpm、分散剤Demol EP量を酸化チタン重量の0.4%とした。
【0287】
図33工程2における酸化ホウ素アルカリ金属溶液量が酸化チタンスラリ容量の3%となるように濃度を調整、NS撹拌を50mpm実施した。
【0288】
第3工程の希塩酸量を酸化チタンスラリ容量の0.5%になるように濃度を調整、NS撹拌を25mpm実施した。
【0289】
図35に、作成したn型量子触媒5Gn―100t/1、5Gn―1b/1、5Gn―10b/1、5Gn―100b/1、5Gn―1m/1、5Gn―10m/1、5Gn―100m/1、5Gn―1000m/1、および5Gn―1%/1のリン原子数比に対する反応速度比特性を示す。図34の横軸はリン原子数比を示し、単位pptは1兆分の1、ppbは10億分の1、ppmは100万分の1、%は0.01を表す。
【0290】
作成した濃度10w%のn型量子触媒スラリ100mgをシャーレに採り室温乾燥させたn型量子触媒10mgを用いて、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を、24時間の間隔を置き30回測定した。30回計測した残留濃度の算術平均から求めた反応速度定比を平均反応速度比5Gn/1-Aveとした。平均反応速度定比を、図35の実曲線で示す。実曲線5Gn/1-Aveにおける、ドットの横位置はリン原子数比を、ドットの縦位置は平均反応速度比を、ドットのデータラベルは平均反応速度比の値を表す。
【0291】
同図35の1点鎖曲線5Gn/1−worstは、最小反応速度比を示す。30回計測した残留濃度比の最大値に対する反応速度比を最小反応速度比とした。1点鎖曲線5Gn/1−worst上のドットの横位置はリン原子数比を、縦位置は最小反応速度比を示し、データラベルは最小反応速度比の値を表す。
【0292】
同図35の破曲線5Gn/1−bestは、最大反応速度比を示す。30回計測した残留濃度比の最小値に対する反応速度比を最大反応速度比とした。破曲線5Gn/1−best上のドットの横位置はリン原子数比を、縦位置は最小反応速度比を示し、データラベルは最小反応速度比の値を表す。
【0293】
繰り返し30回計測して計測上の擾乱要因を除去するように努め、リン原子数比100ppt〜1%に関するn型量子触媒5Gn−100t/1〜5Gn−1%/1の反応速度比の信頼度を高めた。
【0294】
図35の平均反応速度比5Gn/1−ave、最大反応速度比5Gn/1−best、ならびに最小反応速度比5Gn/1−worstが示すように、リン原子数比が変化すると、反応速度比すなわち光触媒活性が敏感に変化することを示すことが見出された。
【0295】
具体的には、図35の平均反応速度比5Gn/1−aveに示すように、リン原子数比に対するn型量子触媒の平均反応速度比は、100pptの場合2.53、1ppbの場合2.58、10ppbの場合2.68、100ppbの場合3.29、1ppmの場合3.34、10ppmの場合3.18、100ppmの場合2.96、1000ppmの場合2.91、1%の場合1.20であった。n型量子触媒のリン原子数比が100ppb〜10ppm前後で平均反応速度比の値は3.18〜3.34と最大になった。最大の平均反応速度定比3.34のn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の光触媒活性の4万7千8百倍であることが判明した。
【0296】
また、図35に示すようにリン原子数比が1兆分の1〜1%の領域における平均反応速度定比の値は1以上であり、全域においてn型量子触媒の光触媒活性が第1物質の酸化チタン単独の場合の光触媒活性を上回ることが明らかになった。
【0297】
図35の最大反応速度比5Gn/1−bestに示すように、n型量子触媒のリン原子数比に対する最大反応速度比は、100pptの場合3.55、1ppbの場合3.56、10ppbの場合3.88、100ppbの場合5.38、1ppmの時場合4.72、10ppmの場合4.27、100ppmの場合3.88、1000ppmの場合3.71、1%の場合1.35であった。
【0298】
リン原子数比が100ppbの最大反応速度比は5.38であった。最大反応速度定比5.38のn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の5億7千5百万倍強であった。
【0299】
図35の最小反応速度比5Gn/1−worstに示すように、n型量子触媒のリン原子数比に対する最小反応速度比は、100pptの場合1.81、1ppbの時場合1.94、10ppbの場合2.09、100ppbの場合2.32、1ppmの場合2.71、10ppmの場合2.68、100ppmの場合2.37、1000ppmの場合2.24、1%の場合1.00であった。
【0300】
n型量子触媒中のリン原子数比が100pptの場合、最小反応速度比が最小の1.81となった。最小反応速度定比1.81は光触媒活性42倍を意味し、リン原子数比100ppt〜1000ppmの領域におけるn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の42倍以上あり、本発明で開示するn型量子触媒は10倍以上の光触媒活性を最悪の場合でも保障することが明らかになった。
【0301】
また、リン原子数比が1ppmのn型量子触媒は、最大値反応速度定比が4.72、平均反応速度定比が3.34、最小反応速度定比が2.71であり、第1物質の酸化チタン単独の光触媒活性を最大2754万倍強、平均4万7千8百倍強、最小2千6百倍強で、平均反応速度定比が最大値となることが知れた。
【0302】
図36〜図44に、リン原子数比が100ppt〜1%の作成したn型量子触媒スラリ粒径の散乱強度分布と累積を示す。
【0303】
図36にn型量子触媒5Gn−100t/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100t/1スラリは、594.5nmに散乱強度ピークを有し、平均粒径は297.1nmであった。
【0304】
図37にn型量子触媒5Gn−1b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1b/1スラリは、458.0nmに散乱強度ピークを有し、平均粒径は244.7nmであった。
【0305】
図38にn型量子触媒5Gn−10b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−10b/1スラリは、888.3nmに第1、3万8924.4nmに第2散乱強度ピークを有し、平均粒径は3273.5nmであった。
【0306】
図39にn型量子触媒5Gn−100b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100b/1スラリは、593.1nmに散乱強度ピークを有し、平均粒径は298.7nmであった。
【0307】
図40にn型量子触媒5Gn−1m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1m/1スラリは、569.4nmに散乱強度ピークを有し、平均粒径は301.1nmであった。
【0308】
図41にn型量子触媒5Gn−10m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−10m/1スラリは、714.9nmに第1、7657.6nmに第2散乱強度ピークを有し、平均粒径は1430.1nmであった。
【0309】
図42にn型量子触媒5Gn−100m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100m/1スラリは、431.9nmに散乱強度ピークを有し、平均粒径は233.6nmであった。
【0310】
図43にn型量子触媒5Gn−1000m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1000m/1スラリは、299.2nmに散乱強度ピークを有し、平均粒径は165.7nmであった。
【0311】
図44にn型量子触媒5Gn−1%/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1%/1スラリは、1083.7nmに散乱強度ピークを有し、平均粒径は1463.8nmであった。
【0312】
n型量子触媒に含まれる第1物質と第2物質の割合については特に制限はないが、n型量子触媒におけるリン原子数比をだんだん大きくしていくと、n型量子触媒の光触媒活性、言い換えれば反応速度比が上昇後下降し次第に反応速度比が1を下回るか、あるいは反応速度比が1以上で上昇下降を繰り返したのち反応速度比が1を下回り、ピークを示すことが見出されており、ある範囲内にあることが好ましいと言えよう。一般的に言えば、n型量子触媒におけるリン原子数比が1000兆分の1〜1の範囲にすることが好ましく、1兆分の1〜0.01の範囲にすることがより好ましい。以下、光触媒活性が、第1物質単独の場合に比べ高くなるメカニズムについて説明する。ただし、以下の説明は本発明の理解を助けるためのものであり、本発明の範囲を制限するものではない。
【0313】
図31に示したように、接合面近傍では酸化チタンの酸素原子と酸化リンのリン原子が電子を共有しており、チタン原子とリン原子が酸素原子を挟み互いに接合されているものと想定される。換言すれば、接合面の酸化チタンにリン原子が直接接合されている構造が実現され、第2物質の酸化リンの励起に必要なエネルギは、酸化リン分子の励起に必要なエネルギより低く、リン原子の励起エネルギに等しくなる。
【0314】
チタン原子とリン原子が酸素原子を挟み互いに接合され、接合面の酸化チタンにリン原子が直接接合されていると見做すことができ、第2物質の酸化リンのリン原子が、酸化チタンの結晶構造を乱すことなく、不純物となっていることになる。リン原子が酸化チタンの不純物となった結果、酸化チタンの禁止帯にドナー準位が生じる。
【0315】
第2物質の酸化リンのリン原子の励起エネルギを略0.025eVと単純に記述するのは、上記机上実験結果に基づくものであるが、この机上実験結果が将来詳細に測定され得られるドナー準位の値と異なっていても、本特許の主旨を阻害するものでは無く、リン不純物によりドナー準位が生じた結果、n型量子触媒の光触媒活性が第1物質単独の光触媒活性を上回っていることが示されば十分である。
【0316】
次に、本発明に係る量子触媒の紛体化について説明する。
【0317】
「実施例15」(量子触媒の紛体化)
【0318】
p型及び/あるいはn型量子触媒の紛体は、図9及び/あるいは図33の工程4〜6に従い乾燥粉砕して製造する。図9及び/あるいは図33の工程4で、p型及び/あるいはn型量子触媒スラリを適切な方法、例えば加熱してp型及び/あるいはn型量子触媒スラリの凝集を加速し、図9及び/あるいは図33の工程5で凝集したp型及び/あるいはn型量子触媒スラリを冷却した後フィルタープレス等で脱水しプレスケーキを作成し、図9及び/あるいは図33の工程6で当該プレスケーキを乾燥粉砕しp型及び/あるいはn型量子触媒を紛体化する。
【産業上の利用可能性】
【0319】
このようにして、本発明は、第1物質の結晶構造を乱すこと無く第4と第8族を除く第1〜3族または第5〜7族原子あるいはその酸化物からなる第2物質を不純物として含む新しい物質である量子触媒を作成する方法、さらに、第2物質の不純物が第1物質の禁止帯に準電位を生じしめる結果、第1物質単独の場合に比して光触媒活性を10倍以上に改善することを明らかにした。
【0320】
本発で開示した量子触媒は、第1物質の光触媒単独では光触媒活性を発現できない環境でも光触媒活性を発現することを示した。量子触媒は、紫外線のみならず、量子線、赤外線、可視光などの低エネルギレベルの量子線の照射時においても光触媒活性を発現する。
【0321】
本発明に係る量子触媒からどのような光触媒作用を発揮させるかについては特に制限はない。使用された第1物質の場合と同様の光触媒活性が適切である場合が多い。一般的には、有害物質や臭い発生物質の分解作用や色素増感型太陽電池における光電変換作用を好ましく挙げることができる。また、製造の簡便さと安定性ならびに経済性を満たす新しい太陽電池および癌治療を特に好ましく挙げることができる。この新しい太陽電池は、p型量子触媒を正極材、n型量子触媒を負極剤として使用する。さらに、酸化チタンと酸化リン及び/あるいは酸化ホウ素とからなる量子触媒は、人体内部の癌細胞や癌病巣を分解除去する新しい治療を可能とする。
【0322】
本発明に係る量子触媒に照射する光や量子線などのエネルギについても特に制限はない。使用された第1物質が光触媒活性を発現する場合と同様の紫外線等を使用することが適切である場合が多いが、それより長波長側でもよいことは上述の通りである。授受されるエネルギが第2物質の原子が不純物として励起するに足るならば、赤外線、可視光、あるいは紫外線等の照射は必ずしも必要ない。電子が動けない絶対零度のような環境を除けば、室温程度で十分な熱エネルギの照射を受けているので、夜間や遮光環境においても、第2物質の不純物は励起し、第1物質の伝導帯へ自由電子を、第1物質の価電子帯へホールを供給する。不純物から供給される自由電子とホールが充分な量に達すれば、光触媒作用が発現するのは前記の通りである。エネルギにより電子が励起される確率は、ドナー準位と伝導帯電位あるいはアクセプタ準位と価電子帯電位との電位差で定まる励起エネルギレベルが小さい程、指数関数的に大きくなり、本発明が開示する量子触媒が室温程度の温度で効果的に光触媒作用を発揮するようになり、夜間においても発電可能な上記の新しい太陽電池の実現できる。さらに、可視光や紫外線の照射を不要とする量子触媒の特徴は、人体内部の略遮光環境における光触媒活性を利用した安全な治療法を提供できる。
【技術分野】
【0001】
本発明は新規物質である量子触媒とその製造法に関係する。
【背景技術】
【0002】
量子触媒の第1物質の一例である酸化チタンは、光触媒としてよく知られている。結晶構造がアナターゼ型とブルッカイト型の酸化チタンは、その伝導帯下端と価電子帯上端電位差すなわちバンドギャップ3.2eV以上のエネルギを有する波長が390nmより短い可視光の紫〜波長360nm以下の紫外線(以下、波長390nm以下の可視光の紫〜紫外線を、紫外線等と呼ぶ。)が照射されると、伝導帯に自由電子を価電子帯にホールを生じ、結晶内における自由電子とホールの再結合確率が低く、消滅することなく自由電子とホールを結晶外に放出する。放出されたホールと自由電子が、それぞれ結晶周辺のNOX、SOX、メタンガスなどの温室効果ガスや大気汚染物質、揮発性有機化合物(VOC)、油脂などの脂肪酸、臭気物質およびダイオキシン等を酸化・還元して分解除去することで、大気清浄化、温暖化防止、防汚、消臭、殺菌等、いわゆる光触媒活性を発現する(例えば非特許文献1参照)。
【0003】
周辺の温室効果ガスや大気汚染物質などを酸化・還元など物理的・化学的に作用するとき、物質自身は物理的・化学的に変化せず、外部から与えられるエネルギで半永久的に作用が持続する物質を、触媒と言う。特に、外部エネルギが3.2eV以上の紫外線等を必要とする触媒を光触媒と呼び、本発明に関する触媒を、量子触媒と呼び区別する。また、第2物質が1〜3族原子あるいはその酸化物である量子触媒をn型量子触媒、第2物質が5〜7族の原子あるいはその酸化物である量子触媒をp型量子触媒と呼ぶ。
【0004】
光量子1個が有するエネルギを、アインシュタインは、プランク定数h、波長ν、高速c、振動数λを用いて、E=hν=hc/λなる関係が成立することを明らかにしている。アインシュタインのエネルギ式1から、エネルギE[eV]を有する光量子の波長νは、次に与えられる。
【数1】

【0005】
ここに、
【数2】

【0006】
例えば、エネルギ3.2eVを有する光量子線の波長νは、
【数3】

【0007】
と、略390nmと求まる。略3.4eV以上のエネルギを有する紫外線の最長波長は略360nmであることを考慮すれば、3.2eVエネルギ、波長390nmの光量子線は紫外線に近い紫の可視光であることが知れる。
【0008】
なお、本発明において、ある物質が「光触媒活性を発現し得る」とは、その物質が紫外線、可視光、赤外線、熱線、あるいは量子線などの何らかの光量子エネルギで励起され、励起された結果生じる自由電子とホールが、周辺の物質に物理的、化学的、または生物学的影響を与え得ることを意味する。励起エネルギは酸化・還元作用として現れる場合が多い。従来の光触媒は、励起エネルギを波長390nmの紫色の可視光およびより短波長の紫外線等からエネルギを吸収し光触媒活性を発現するので、「光触媒」と呼ばれている。
一方、後で説明することではあるが、本発明に関する量子触媒は、波長略50μm以下の量子線、可視光、ならびに紫外線等で励起され光触媒活性を発現する物質であるので、「量子触媒」と呼ぶ。
【0009】
光触媒であるアナターゼ型とブルッカイト型の酸化チタンにおいては、水素発生レベルとほぼ等しい−0.2eVに伝導帯の下端が存在し、また、3.0eVに価電子帯の上端が存在し、価電子帯の上端と伝導帯の下端とのエネルギ差(以降、バンドギャップと呼ぶ。)は3.2eVとなる。このバンドギャップ3.2eVを上回るエネルギを有する紫外線等を照射すると、結晶を形成していた一部の電子の束縛が解かれ結晶内を自由に動き回るようになる。
【0010】
結晶を形成するために束縛されていた電子を価電子帯に属すると呼び、結晶内を自由に動き回るようになった電子を伝導帯に属する自由電子と呼ぶ。
価電子帯と伝導帯との間は禁止帯と呼ばれ、電子が存在しない。禁止帯の幅は、バンドギャップと呼ばれる。束縛されていた電子が結晶内を自由に動き回るようになった状態を、励起状態と呼ぶ。
【0011】
結晶を安定に保つためには価電子帯の電子が飛び出した跡に電子を充足する必要があり、近隣原子から電子を奪い取り充足する力が働く。奪い取られた原子は、さらに近隣原子から電子を奪いとる。このように電子の抜け殻であるホールは、再結合するまで結晶内を動き回る。自由電子の移動度(mobility)に比べ、ホールの移動度は若干小さいが略等しく、電子はマイナスの電荷を有し、ホールは電子とは逆のプラスの電荷を有している。
【0012】
再結合して熱となり消滅せず残っている自由電子とホールは、光触媒結晶外に放出されるまで光触媒結晶内を自由に動き回る。自由電子とホールは、光触媒結晶内で再結合され消滅する確率は低い。自由電子は還元リアクションセンターから光触媒結晶外に放出され、光触媒結晶近傍に存在する他の物質を還元する。また、ホールは酸化リアクションセンターから光触媒結晶外へ放出、すなわち光触媒結晶外の電子を取り込み、光触媒結晶近傍に存在する他の物質を酸化する。
【0013】
一方、ルチル型酸化チタンは、水素発生レベルに等しい0eVに伝導帯の下端を、3.0eVに価電子帯エネルギの上端レベルを有し、バンドギャップは3.0eVとアナターゼ型酸化チタンより小さい。ルチル型酸化チタンは、3.0eVの波長410nm以下のエネルギで励起するが、ルチル型酸化チタンの再結合確率はアナターゼ型酸化チタンより大きく自由電子とホールが光触媒結晶内で再結合し熱として消滅する確率が高く、光触媒結晶外へ自由電子とホールを放出する確率が低く、光触媒活性はアナターゼ型酸化チタンに比べ弱い。
【0014】
以下、本発明に関し、光触媒活性を発現し得る光触媒(この光触媒を第1物質として使用する。)として、アナターゼ型酸化チタンについて主に説明するが、ブルッカイト型酸化チタンやルチル型酸化チタンでも、更には、酸化チタン以外の光触媒物質、たとえば、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムからなるグループから選ばれる物質を用いても、光触媒活性を発現するメカニズムや本発明に係る効果は同様であると考えられる。なお、特に断らない限り、以下、アナターゼ型酸化チタンを、単に酸化チタンと略記する場合がある。
【0015】
図1に、酸化チタンが光触媒活性を発現している状態のエネルギダイヤグラムを示す。同図の縦軸はエネルギレベルを意味するポテンシャル電位(eV)を表す。酸化チタンの結晶を構成する束縛されている電子は価電子帯に位置し、自由電子は伝導帯に位置する。価電子帯の下端と伝導帯の上端の間の禁止帯には、電子が存在しない。禁止帯幅、すなわち価電子帯と伝導帯との電位差、バンドギャップが、価電子帯の電子を励起して自由電子とするに必要なエネルギレベルを意味し、図1に示す酸化チタンを励起するには3.2eVのエネルギが必要である。図1に示すように、水の水素発生電位は略0eV、水の酸素発生電位は略1.2eVである。
【0016】
酸化チタンにおいては、自由電子とホールが結晶外部へ放出される確率が高く、結晶外に放出された電子は周辺物質を還元し、結晶外に放出されたホールは周辺物質を酸化する。酸化チタン結晶から外部へ放出される電子の還元作用やホールの酸化作用で、酸化チタン周辺の有機揮発性物質VOC、臭気物質、大気汚染物質NOX,SOX、温室効果ガスや、また環境汚染物質のダイオキシン等、さらに細菌やカビなどが分解除去される。なお、本発明の明細書における「紫外線等」として、390nmの可視光の紫からより波長の短い紫外線、軟X線等を例示することができる。
【0017】
酸化チタンに強い光触媒活性を発現させるには、酸化チタン結晶表面にできるだけ強く紫外線等を照射する必要がある。しかしながら、紫外線等は直進性が強く、かつ物質表面で吸収されやすく、物質内部に到達できない。さらに、影になっている部分に回折して回りこむことは殆ど無い。強い光触媒活性を発現させるためには、酸化チタン結晶を微粒子化して比表面積を大きくしたり、できるだけ多くの粒子が照射されるように酸化チタンの保持方法を工夫したり、吸着剤と組み合わせたりして光触媒活性を効率よく発現させることが考えられるが、十分な解決には至っていない(たとえば特許文献1、非特許文献1、非特許文献2参照)。
【先行技術文献】
【特許文献】
【0018】
【特許文献1】特願2005−281号(特許請求の範囲)
【特許文献2】特願2006−310651号(特許請求の範囲)
【非特許文献】
【0019】
【非特許文献1】「高機能な酸化チタン光触媒〜環境浄化・材料開発から規格・標準化まで〜」、高機能光触媒創製と応用技術研究会編、安保正一監修、NTS出版、初版2004年9月1日、1章1節3〜4、p.10〜15
【非特許文献2】「高機能な酸化チタン光触媒〜環境浄化・材料開発から規格・標準化まで〜」高機能光触媒創製と応用技術研究会編、安保正一監修、NTS出版、初版2004年9月1日、2章5節5、p.110〜114
【発明の概要】
【発明が解決しようとする課題】
【0020】
本発明は、上記問題を解決して、光触媒より効率よく光触媒活性を発現する物質である量子触媒を提供することを目的とする。本発明の更に他の目的および利点は、以下の説明から明らかになるであろう。
【課題を解決するための手段】
【0021】
本発明の一態様によれば、光触媒活性を発現し得る第1物質と、当該第1物質とは異なる4族以外の原子あるいは当該原子の酸化である第2物質とが、互いに接合されてなり、第1物質単独の場合に比べ光触媒活性が高められた量子触媒が提供される。本発明態様により、効率よく励起できる新規な量子触媒を実現できる。
【0022】
光触媒活性が第1物質単独の場合に比べ10倍以上であること、
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にあること、
前記第1物質が、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質であり、前記第2物質が、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウム、5族(5A族)のバナジウム、ニオブ、タンタル、5族(5B族)の窒素、リン、ヒ素、アンチモン、ビスマス、からなる群から選ばれた物質あるいはその酸化物質であること、とりわけ、
前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素であること、および、前記第1物質が酸化チタンであり、前記第2物質が酸化リンであること、
前記第1物質と、前記第2物質とが接合されてなる量子触媒の製造方法であって、
分散剤を加えた溶媒に第1物質の微粒子を分散した第1物質スラリを作製し、
酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を当該第1物質スラリに加え混合スラリを作成、あるいは、
分散剤と酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えた溶媒に第1物質の微粒子を分散した混合スラリを作製して、
必用に応じ当該混合スラリに酸および/または塩基を添加して当該第1物質の微粒子表面に第2物質を析出させた量子触媒を分散した量子触媒スラリを得るに際して、
当該第1物質と分散剤との割合、
当該第1物質の粒径、
当該第1物質スラリおよび/または混合スラリの濃度、
当該第1物質スラリおよび/または混合スラリの温度、
当該第1物質スラリおよび/または混合スラリの撹拌時に照射する超音波の周波数と電力、
当該第1物質スラリのよび/または混合スラリの撹拌時に使用するビーズ径、
当該酸および/または塩基の添加量、
当該酸および/または塩基の濃度、
および
当該量子触媒スラリにおける当該第1物質と当該第2物質の割合からなる群から選ばれた少なくとも一つの条件を選択することにより、
当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、量子触媒の製造方法が提供される。
【0023】
本発明態様により、効率よく励起できる新規な量子触媒の製造方法を実現できる。
【0024】
これらについては、
前記第1物質と分散剤との割合が0.1〜10重量%にすること、
前記第1物質の微粒子の粒径が1nm〜100nmの範囲にすること、
前記第1物質スラリおよび/または混合スラリの濃度を0.1〜35重量%の範囲にすること、
前記第1物質スラリおよび/または混合スラリの温度を1〜35℃の範囲にすること、
前記第1物質スラリおよび/または混合スラリ作成に当たり、周波数19KHz以上の超音波を、第1物質1g当たり0.1Wh〜100Whの強度で照射して攪拌すること、
前記第1物質スラリおよび/または混合スラリ作成に当たり、径0.01〜2mmのビーズを使用して攪拌すること、
前記酸および/または塩基の量を、酸および/または塩基単独で第2物質を析出するに要する量の0〜200%の範囲にすること、
前記混合スラリに添加する酸および/または塩基の溶液量を、第1物質スラリ容積の0.1〜10%の範囲にすること、
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にすること、
特に前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素あるいは酸化リンであることが好ましい。
【発明の効果】
【0025】
本発明により、量子線、熱線や赤外線、ならびに紫外線等の幅広い領域のエネルギを吸収し、強い光触媒活性を発現する新規物質である量子触媒が実現できる。
【図面の簡単な説明】
【0026】
【図1】酸化チタンの光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
【図2】本発明に係る量子触媒の模式図である。
【図3】酸化チタン結晶のラチスモデル図である。
【図4】チタン原子と酸素原子のモデル図である。
【図5】本発明に係るp型量子触媒結晶のラチスモデル図である。
【図6】ホウ素原子のモデル図である。
【図7】本発明に係るp型量子触媒結晶のラチスモデル図である。
【図8】本発明に係るp型量子触媒の光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
【図9】本発明に係るp型量子触媒の主要製造プロセスを示す図である。
【図10】本発明に係るp型ならびにn型量子触媒の製造方法例における撹拌方法を示す図である。
【図11】本発明に係る酸化チタンスラリ濃度と平均粒径の関係を示す図である。
【図12】本発明に係る分散剤濃度と酸化チタンスラリの平均粒径の関係を示す図である。
【図13】本発明に係る撹拌方法ごとの撹拌時間と酸化チタンスラリ平均粒径の関係を示す図である。
【図14】本発明に係るSTR撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図15】本発明に係るBM撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図16】本発明に係るHG撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図17】本発明に係るNS撹拌の酸化チタンスラリ粒径に関する散乱強度と累積特性を示す図である。
【図18】本発明に係る塩酸使用率100%、50%、ならびに0%のp型量子触媒の反応速度比特性を示す図である。
【図19】本発明に係るp型量子触媒の反応速度比とホウ素原子数比との関係を示す特性図である。
【図20】本発明に係るホウ素原子数比100pptのp型量子触媒5Gp−100t/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図21】本発明に係るホウ素原子数比1ppbのp型量子触媒5Gp−1b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図22】本発明に係るホウ素原子数比10ppbのp型量子触媒5Gp−10b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図23】本発明に係るホウ素原子数比100ppbのp型量子触媒5Gp−100b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図24】本発明に係るホウ素原子数比1ppmのp型量子触媒5Gp−1m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図25】本発明に係るホウ素原子数比10ppmのp型量子触媒5Gp−10m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図26】本発明に係るホウ素原子数比100ppmのp型量子触媒5Gp−100m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図27】本発明に係るホウ素原子数比1000ppmのp型量子触媒5Gp−1000m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図28】本発明に係るホウ素原子数比1%のp型量子触媒5Gp−1%/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図29】本発明に係るn型量子触媒結晶のラチスモデル図である。
【図30】リン原子のモデル図である。
【図31】本発明に係るn型量子触媒結晶のラチスモデル図である。
【図32】本発明に係るn型量子触媒の光触媒活性発現メカニズムを示すエネルギダイヤグラムである。
【図33】本発明に係るn型量子触媒の主要製造プロセスを示す図である。
【図34】本発明に係る塩酸使用率100%、50%、ならびに0%のn型量子触媒の反応速度比特性を示す図である。
【図35】本発明に係るn型量子触媒の反応速度比とリン原子数比との関係を示す特性図である。
【図36】本発明に係るリン原子数比100pptのn型量子触媒5Gn−100t/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図37】本発明に係るリン原子数比1ppbのn型量子触媒5Gn−1b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図38】本発明に係るリン原子数比10ppbのn型量子触媒5Gn−10b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図39】本発明に係るリン原子数比100ppbのn型量子触媒5Gn−100b/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図40】本発明に係るリン原子数比1ppmのn型量子触媒5Gn−1m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図41】本発明に係るリン原子数比10ppmのn型量子触媒5Gn−10m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図42】本発明に係るリン原子数比100ppmのn型量子触媒5Gn−100m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図43】本発明に係るリン原子数比1000ppmのn型量子触媒5Gn−1000m/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【図44】本発明に係るリン原子数比1%のn型量子触媒5Gn−1%/1スラリ粒径の散乱強度分布と累積を示す特性図である。
【発明を実施するための形態】
【0027】
以下に、本発明の実施の形態を図、表、式、実施例等を使用して説明する。なお、これらの図、表、式、実施例等および説明は本発明を例示するものであり、本発明の範囲を制限するものではない。本発明の趣旨に合致する限り他の実施の形態も本発明の範疇に属し得ることは言うまでもない。
【0028】
<量子触媒>
本発明に係る量子触媒は、恐らく、図2に示されているように、第1物質と第2物質とが接合して、接合面を実現しているものと思われる。ただし、接合面を実現しているかどうかを証明することは必ずしも本発明の要件ではない。第1物質と第2物質とが互いに接合されていると考えられる結果、第1物質単体の場合に比べ光触媒活性が高められていれば十分である。本発明で開示する量子触媒は、従来の酸化チタンと同じように3.2eV以上の紫外線等から励起エネルギを獲得し光触媒活性を発現することが可能であるが、加えて、1.49〜3.4eV(波長830nm〜360nm)の可視光から励起エネルギを獲得して光触媒活性を発現することも可能である。
【0029】
さらに、例えば第1物質が酸化チタンであり第2物質が3族原子のホウ素の酸化物である場合、第1物質のバンドギャップ中の価電子帯寄りにアクセプタ準位が生じ、アクセプタ準位と価電子帯電位とのエネルギ差の略0.025eV程度の低いエネルギの量子線から励起エネルギを獲得して光触媒活性を発現することが可能となる(かかる量子触媒は、特に、p型量子触媒と呼ぶ。)。あるいは、例えば第1物質が酸化チタンであり第2物質が5族原子のリン酸化物である場合、第1物質のバンドギャップ中の伝導帯電位寄りにドナー準位を設けることができ、ドナー準位と酸化チタンの伝導帯電位とのエネルギ差の略0.025eV程度の低いエネルギの量子線から励起エネルギを獲得して光触媒活性を発現することが可能となる(かかる量子触媒は、特にn型量子触媒と呼ぶ。)。
【0030】
量子触媒は、p型量子触媒とn型量子触媒の2種量子触媒の総称であるが、第2物質を特定する必要がある場合、第2物質が1〜3族原子あるいはその酸化物である量子触媒を「p型量子触媒」と、第2物質が5〜7族原子あるいはその酸化物である量子触媒を「n型量子触媒」と呼び区別する。
【0031】
光触媒である酸化チタンは光触媒活性を発現するためには3.2eV以上の紫外線等の照射を必要としたが、これに対して、本発明で開示する量子触媒は、量子線、熱線や赤外線から紫外線等までの幅広いスペクトラルの光量子線を吸収し光触媒活性を発現できるものであり、可視光や紫外線を遮蔽したいわゆる遮光環境においても光触媒活性を発現する物質である。
【0032】
<p型量子触媒>
本発明に係るp型量子触媒は、光触媒活性を発現し得る第1物質と、1〜3族から選ばれた原子あるいはその酸化物である第2物質とが、互いに接合されてなる物質であり、第1物質単独の場合に比べ光触媒活性が10倍以上高められた物質である。
【0033】
図3に、第1物質として使用する酸化チタン結晶をラチス結晶モデルで示す。図3において、ハッチ付小丸は電子を、白小丸は価電子帯の電子欠乏状態、すなわちホールを示している。ハッチ付小丸と白小丸を通る円は電子の最外殻軌道を示している。同図におけるハッチ付丸は、最外殻軌道等以外の電子軌道や原子核を示し、ハッチ付丸内の文字「Ti」は原子の名称「チタン」、「O」は原子の名称「酸素」を示す。最外殻軌道等として、非遷移原子の最外殻軌道や遷移原子の電子結合に寄与する電子軌道を例示することができる。
【0034】
チタン原子は遷移元素であり、最外殻軌道は電子で満たされており内部軌道が電子で満たされていない原子であるが、ここでは図4aに示すように、4族のチタン原子の最外殻軌道が密では無く4個の電子が存在する最外殻軌道等が存在するものとして説明する。チタン原子の最外殻軌道等が電子で満たされていないとすることで説明の厳密性に欠ける事は否めないが、チタン原子の最外殻軌道等に4個の電子が存在するとして説明しても、本発明の主旨を阻害するものではない。
【0035】
6族の酸素原子は、図4bに示すように最外殻軌道に6個の電子を有している。
図3に戻り酸化チタン結晶を簡単に説明する。原子の最外殻軌道上等に8個の電子が存在(あるいは共有)するか、あるいは全く存在しない場合に、安定した結晶が形成されることは、所謂オクテット理論として周知のところであろう。図3の結晶端を除き、酸素原子の最外殻軌道には8個の電子が存在し、チタン原子の最外殻軌道等に存在する電子は0個であり、安定した結晶を形成する。
【0036】
一方、結晶端では、最外殻軌道が8個の電子で満たされず1個欠如する(1個のホールを有する)酸素原子が6個存在している。さらに、チタン原子の最外殻軌道等に1ないし2個の結晶構成に関与していない、いわゆる自由電子を有するチタン原子が5個存在している。結晶全体では、6個のホールと6個の自由電子が存在し、結晶全体の電荷はホールのプラス電荷と自由電子のマイナス電荷が相殺しゼロとなっている。これらの結晶内の酸素原子の最外殻軌道に存在するホールが酸化リアクションセンターとして、また、結晶内のチタン原子の最外殻軌道等に存在する自由電子が還元リアクションセンターとして機能し、周辺物質を酸化・還元する光触媒活性が発現する。
【0037】
酸化チタンのラチス結晶モデル端ではホールを伴う酸素原子あるいは自由田電子を伴うチタン原子が露出しているので光触媒活性が発現される。しかし、実存する酸化チタン結晶は、ラチス結晶モデルの結晶端の酸素原子のホールが結晶端のチタン原子の自由電子を補足した構造となっており、ホールと自由電子の結合状態に従い、アナターゼ型、ルチル型あるいはブルッカイト型などの立体的な結晶構造を成す。これらの立体構造を成す酸化チタン結晶は、紫外線等を照射されない限り、結晶内に酸化リアクションセンターや還元リアクションセンターが存在せず、光触媒活性を発現しない。3.2eV超エネルギの紫外線等を照射され励起された酸化チタン結晶のチタン原子と酸素原子の電子結合の一部が解離し、酸化リアクションセンターのホールと還元リアクションセンターの自由電子が出現し、強い酸化作用と還元作用を伴う光触媒活性を発現するものと考えられる。
【0038】
かかる観点から、図3に示すラチス結晶モデルは、紫外線等の光エネルギを照射された場合に出現する励起状態にある酸化チタン結晶を模式的に示すものと考えることができる。
【0039】
図5に第1物質である4族原子、3族―5族、あるいは2族-6族の4価化合物(以下、これらを4族原子類と称する)の酸化物(以下、4族原子類酸化物と言う)と第2物質の1例として3族原子の酸化物とが接合面を成す本発明に係るp型量子触媒の模式図をラチス結晶モデルで示す。第1物質の4族原子類酸化物の4族原子の還元リアクションセンターの電子が第2物質の3族原子の酸化物の酸素原子のホールに補足され、第1物質の4族原子類の酸化物の4族原子類に第2物質が結晶成長し、第1物質の結晶構造を保存したまま第2物質を不純物として含む量子触媒が実現される。
【0040】
これら図5はあくまで模式図である。対象となる粒子の1次粒子径が数ナノメートルと小さいため、かつ光触媒活性を発現している場合は動的に結晶構造が変動するものと考えられ、具体的にどのようになっているかは定かでない。
【0041】
本発明に係る量子触媒は、恐らく、第2物質が、第1物質表面に結晶成長した結果、第2物質を不純物として含む第1物質が実現されたものと思われる。第1物質と第2物質が互いに接合されていると考えられる結果、第1物質単独の場合に比べ光触媒活性が10倍以上高められていることが確認できれば十分である。この接合、第1物質と第2物質とが互いに接触した状態にあることを意味し、第2物質が第1物質表面に結晶成長した状態のものや、第1物質が第2物質表面に結晶成長した状態のものや、第2物質と第1物質とのナノレベルの微細結晶が互い接合した状態(以下ナノコンポジット状態と称する)のものを例示することができる。これらは、第1物質の結晶表面に第2物質を析出させるか、第2物質の結晶表面に第1物質を析出させるか、第1物質を析出しうる溶液と第2物質を析出しうる溶液の混合溶液から両物質を析出させ実現できる。第2物質イオンを第1物質にイオンインプラテーションするか、第1物質イオンを第2物質にイオンインプラテーションすることでも実現できるが、結晶構造に歪を与え好ましくないので本発明ではイオンインプランテーションを用いる実現法には言及しない。
【0042】
p型量子触媒における第1物質と第2物質との接合面近傍の結晶模式図を、図5に示す。同5図は、p型量子触媒の動作を説明するためにラチス結晶モデルで単純化した結晶構造を表現したものであり、実際に観測する結晶構造とは異なる場合があるが、将来観測されるようになった場合の観測結果と結晶模式図の相違は本出願の主旨を阻害するものでは無い。
【0043】
図5中、左下がり斜線を施した部分は第1物質を、右下がり斜線を施した部分は第2物質を示し、左下がり斜線部と右下がり斜線部が接する部分が接合面である。同5図は、第2物質の3族原子の酸化物が第1物質の結晶構造を乱す事無く第1物質の不純物となっていることを示している。第2物質として3族原子の酸化物の場合に関してp型量子触媒について説明したが、1〜2族原子の酸化物を第2物質とする場合も同様であり容易に類推できる範疇であるので説明を省略する。
【実施例】
【0044】
次に、第1物質に酸化チタン、第2物質に3族原子の酸化物である酸化ホウ素を用いた量子触媒の製造実施例を説明する。
【0045】
「実施例1」(p型量子触媒の作成)
図6に、第2物質の3族原子として例示するホウ素の原子構造を示す。同図において、図4と同様に、最外殻電子軌道を大きな円で、最外殻軌道上の電子をハッチ付小丸で、ならびに最外殻軌道以外の電子と原子核等をハッチ付丸で模式的に示している。ハッチ付丸の「B」は原子がホウ素であることを示している。
3族のホウ素原子の最外殻軌道には、3個の電子が存在する。
【0046】
図7に第1物質の4族原子類酸化物として例示する酸化チタンを、第2物質として(3族原子の)ホウ素の酸化物である酸化ホウ素を用いる本発明に係るp型量子触媒の模式図をラチスモデルで示す。図7は、第1物質としての酸化チタンのチタン原子のホールに第2物質の酸化ホウ素の酸素原子の電子が捕捉され結晶成長することを示している。同図に示すように本発明で開示するp型量子触媒物質の実施例は、第1物質の酸化チタンと第2物質の酸化ホウ素が接合しており、第2物質のホウ素原子が第1物質の結晶構造を乱す事無く第1物質の不純物となることを示している。
【0047】
酸化ホウ素を酸化チタン表面に結晶成長させると、酸化チタンを種結晶として成長するため、接合面近傍では酸化チタンの結晶構造を継承して第2物質の酸化ホウ素が結晶成長する。酸化ホウ素が結晶成長するとき、酸化チタンの結晶構造が継続されるか、あるいは酸化ホウ素の結晶成長膜厚が単分子層程度と薄膜の場合、p型量子触媒の結晶構造は接合面近傍で連続し、酸化チタンのチタン原子がホウ素原子に置換された結晶構造が実現する。換言すれば、酸化チタン結晶に歪を与えること無く、チタン原子の一部をホウ素原子に置き換えた新しい物質を合成できる。第1物質の酸化チタンのチタン原子がホウ素原子に置き換えられた構造を実現し、第2物質の3族ホウ素を、酸化チタン結晶に歪を与えること無く不純物と為すことができる。
【0048】
3族のホウ素原子の最外殻軌道には電子が3個しか存在していない。量子触媒が完全な結晶構造を成すには、酸素原子の最外殻軌道に8個の電子が配置され、さらにホウ素原子の最外殻軌道に4個の電子が共有された電子配置が必要であるが、図7に示すようにp型量子触媒では、ホウ素原子の外殻軌道で電子が1個欠如し、完全な電子配置にならない。この電子が欠如している場所に周辺原子から電子を補足して完全な電子配置を成す結晶構造となるが、近隣原子から電子を補足することで近隣原子にホールを発生させる。かかる意味から、ホウ素原子の最外殻軌道の電子が欠如している場所に酸化リアクションセンターが生じていると言える。
【0049】
ホウ素原子が近隣原子から電子を補足する作用は、図8に示すように、p型量子触媒の不純物であるホウ素原子が酸化チタンの禁止帯中の価電子帯近くの電位にアクセプタ準位を生じると理解できる。ホウ素原子は、ゲルマニュウム結晶の不純物として、禁止帯中に価電子帯との電位差0.025eVのアクセプタ準位を発生する。ホウ素原子は、酸化チタン結晶の不純物としてゲルマニウム結晶中と同様に、禁止帯中の価電子帯に略0.025eVのアクセプタ準位を生じるものと推察できる。ホウ素原子が酸化チタンの不純物として生じるアクセプタ準位の厳密な値が将来計測され、アクセプタ準位の値が異なっていることが判明しても、本発明の主旨が阻害されるものではなく、ホウ素原子が酸化チタン結晶の不純物としてアクセプタ準位を生じることでp型量子触媒の光触媒活性が第1物質単独の場合に比べ10倍以上に高められていることが示されれば十分である。なお、p型量子触媒の光触媒活性が第1物質単独の場合に比べ10倍以上であることは、反応速度比が1.5以上であることに対応する。
【0050】
「第1物質単独の場合に比べ光触媒活性が高められている」ことは、3族原子の不純物がアクセプタとして機能するため光触媒活性が向上するであろうと推察される。
【0051】
この「光触媒活性が高められている」ことは、第1物質が光触媒活性を発現し得る紫外線等を照射した場合において、基準となる第1物質単独の光触媒活性に対して、p型量子触媒を使用した場合の光触媒活が1倍以上であることと捉えることができる。例えば、光触媒活性が酸化である場合には、その酸化反応で評価し、光触媒活性がある物質の分解である場合には、分解反応で評価することができる。また、反応速度比は、第1物質が光触媒活性を発現し得る紫外線等を照射した場合における、p型量子触媒を使用したときの反応速度(非特許文献2参照。)の、基準となる第1物質単独の反応速度に対する比としてとらえることができる(以下、[量子触媒の反応速度/第1物質単独の反応速度] を反応速度比と呼ぶ。)
【0052】
光触媒活性が酸化である場合には、その酸化反応速度定数の反応速度比で評価し、光触媒活性がある物質の分解である場合には、分解反応の反応速度比で評価することができる。ここで、反応速度比がαである場合、10の2(α-1)乗と一義的に与えられる量βで、光触媒活性はβ倍であると表現できる。例えば、第1物質として光触媒(石原産業製ST−01)はアセトアルデヒドガスを2時間で99%分解するものとし、光触媒の反応速度定比を1とするので、反応速度比1.5に対応する光触媒活性は10の2(1.5−1)乗=10の1乗、すなわち10倍であると一義に与えられる(特許文献2)。
なお、本発明で開示する光触媒の10倍以上の光触媒活性を有する量子触媒は、反応速度定比1.5以上の物質を規定していることになる。
【0053】
第1物質の光触媒活性と本発明に係るp型量子触媒の光触媒活性とを比較する場合、それらの単位重量あたりの光触媒活性を比較する。すなわち、それらの単位重量あたりの反応速度を観る。この比較に使用する光などのエネルギ源については、第1物質が光触媒活性を発現し得る限り特に制限はなく、従来から光触媒の励起に使用し得る紫外線等や可視光の全波長領域について、あるいは赤外線さらには熱源などから発するあらゆる光量子エネルギについて、本発明に係るp型量子触媒の光触媒活性が第1物質単独の場合より大きくなっていることを確認する必要はなく、第1物質単独で光触媒活性を発現する紫外線等の波長範囲を選択した結果、本発明に係るp型量子触媒の光触媒活性が第1物質単独の場合より高くなっていることが確認されれば十分である。
【0054】
紫外線等を照射する場合の反応速度比を比較することは、紫外線等の照射は第1物質である光触媒単独が最大の光触媒活性を発現する場合であることを意味し、光触媒単独の光触媒活性が最大となる場合を選択していることになる。逆に、遮光環境で反応速度を比較する場合は、遮光環境でもp型量子触媒は光触媒活性を発現できるが、第1物質の光触媒単独は光触媒活性を殆ど発現できないため、遮光環境におけるp型量子触媒の反応速度比は無限大となる。可視光の場合は、紫外線照射と遮光環境の中間的な状態と言える。p型量子触媒の反応速度定比が最小となる紫外線等を照射する場合におけるp型量子触媒の光触媒活性を調べれば、p型量子触媒にとっては厳しい評価であり安全サイドの評価となる。かかる観点から、紫外線等を照射した場合におけるp型量子触媒の光触媒活性を評価する。
【0055】
第1物質と第2物質については、第2物質が4族原子酸化物以外という条件を除いて特に制限はない。第2物質は、光触媒活性を有している必要はないが、有していても差し支えない。
【0056】
このような第1物質としては、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウム等からなる群から選ばれた物質を挙げることができる。
【0057】
また、このような第2物質としては、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、プロメトイウム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン、ネプツニウム、プルトニウム、アメリシウム、キュリウム、バークリウム、カリホニウム、アインスタニウム、フェルミウム、メンデレビウム、ノーベリウム、ローレンシウム)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウムからなる群から選ばれた原子あるいはその酸化物質を挙げることができる。
【0058】
この中でも。第1物質が酸化チタンであり、第2物質が酸化ホウ素である組合せが特に好ましい。
【0059】
ホウ素を不純部物とするp型量子触媒の励起に必要最小エネルギ略0.025eVに相当する波長は、アインシュタインのエネルギ式(式1)から49,680nm=49.68μmと与えられる。波長49.68μmは、周波数6.03GHzのサブミリ波の電磁波を意味する。さらに、輻射のピーク波長λが温度Tに反比例することを示すウィーンの変位則を用いて、略0.025eVのエネルギを発する黒体の温度を求める。
【0060】
ウィーンの変位則、
【数4】

【0061】
に、アインシュタインのエネルギ式E=hν、ならびに光量子の速度c=hνの関係式を代入すれば、エネルギと温度の関係は次に求まる。
【数5】

【0062】
続いて、上式に、プランク定数、光速、ならびに電子定数を代入して、禁止帯幅 EeVに対応するエネルギと温度T[K]の関係は定まる。ここに、EJはジュール単位のエネルギを、EeVはeV単位で表現したエネルギ量で、互いに同じエネルギを表す。
【数6】

【0063】
準電位差の略0.025eVを上式に代入すれば、ホウ素原子が励起するに必要な温度は58.3°Kであることが知れる。58.3°Kは−215.9℃であり、ほとんどの自然界全域で、ホウ素原子は励起される。ホウ素原子を不純物とするp型量子触媒は、自然界の略全域において、周辺の熱から十分なエネルギを受け取り励起され、光触媒活性を発現することが明らかになる。
【0064】
遮光環境でも室温程度ならば略0.025eVのエネルギレベルを有する量子線は常に照射されており、p型量子触媒の不純物である酸化ホウ素のホウ素原子のホールは、酸化チタンの価電子帯の電子を補足し、酸化チタンの価電子帯へホールを供給する。一方、不純物のホウ素原子のアクセプタは、酸化チタンの価電子帯から補足した電子を、酸化チタンの伝導帯へ供給する。略0.025eVの低いエネルギを照射されるp型量子触媒は、不純物のホウ素原子のアクセプタ作用で、酸化チタンの伝導帯に自由電子が価電子帯にホールが充足し、p型量子触媒が遮光環境でも強い光触媒活性を発現する。
【0065】
ホウ素原子のアクセプタのこの動作は、略0.025eV以上のエネルギが照射される限り繰り返し遂行される。アクセプタ準位と酸化チタンの価電子順位とのエネルギ差略0.025eVの量子線照射で、酸化チタンが励起され光触媒活性を発現することになる。
【0066】
この様子を更に詳細に説明すると次のようになる。
【0067】
1.第1物質の酸化チタン単体のバンドギャップ3.2eV超のエネルギを有する波長390nm以下の紫外線等を照射する場合
【0068】
紫外線等は、アクセプタ励起エネルギ略0.025eVを超え、第1物質の酸化チタン単独のバンドギャップ値3.2eVも超えるエネルギを有している。したがって、第1物質の酸化チタン単独と、不純物のホウ素原子は、共に励起される。
第1物質において励起された自由電子とホールとは、第1物質の結晶から外部に放出され、第1物質近傍に存在する外部の物質を酸化・還元する光触媒作用を発現する。
第2物質も励起され、アクセプタは第1物質の価電子帯から電子を補足し、補足した電子を第1物質の伝導帯へ注入することで、第1物質単独の光触媒活性を増強する。
【0069】
2.第1物質の酸化チタン単独のバンドギャップ値3.2eV以下で、第2物質のホウ素原子のアクセプタ励起エネルギ略0.025eVを超える(波長49.6μm〜390nmの)量子線、熱線あるいは可視光を照射する場合
【0070】
照射エネルギは酸化チタン単独のバンドギャップ値以下のため、酸化チタン単独では励起されず光触媒活性を発現しない。しかし、照射エネルギは、ホウ素原子のアクセプタ励起エネルギ略0.025eVを超えているので、ホウ素原子は励起され、ホウ素原子のアクセプタは酸化チタンの価電子帯の電子を捕捉し、補足した電子を酸化チタンの伝導帯に注入する。ホウ素原子のアクセプタ経由で自由電子を伝導帯にホールを価電子帯に供給され、酸化チタン単独の励起状態が等価的に実現され、3.2eV超のエネルギが照射された場合と等価な光触媒活性を酸化チタンが発現する。
【0071】
つぎに、本発明に係るp型量子触媒の製造プロセスについて説明する。
【0072】
「実施例2」(p型量子触媒の製造プロセス)
【0073】
光触媒活性を発現し得る第1物質を水などの溶媒に加え第1物質スラリを作製し、当該第1物質スラリに酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えて混合スラリを作成し、必要に応じ当該混合スラリに酸および/または塩基を添加して、当該第1物質の結晶表面に第2物質を析出させる。この操作により、第1物質と第2物質とが接合されてなるp型量子触媒を製造する。
【0074】
第2物質を析出し得る溶液を含む溶媒に第1物質を加え、混合スラリを作成しても構わない。
【0075】
p型量子触媒における当該第1物質と当該第2物質の割合を変えることにより、p型量子触媒の光触媒活性を当該第1物質における光触媒活性より高くすることができることが見出された。典型的には後程説明する図19に示すように、p型量子触媒における第1物質に対する前記第2物質の割合をだんだん多くしていくと、p型量子触媒の光触媒活性(および反応速度比)が上昇後下降して、ピークを示すことが見出された。
【0076】
光触媒活性(反応速度比)が上昇するのは、上述の第2物質の不純物が与えるエネルギ準位によるアクセプタ作用の効果と推定される。一旦上昇しその後下降するのは、恐らく、第1物質と第2物質との接合面積、厚さ、接合していない自由表面の面積等が変化し、これにより第2物質の光触媒活性向上能力が変化するためであろうと考えられる。
【0077】
同様に、分散剤とその濃度、スラリ濃度、スラリ撹拌方法およびスラリ温度などの影響を受け第1物質スラリ中の第1物質の粒子径、添加する酸および/または塩基の量、濃度、および添加速度などが、得られたp型量子触媒の光触媒活性に影響を及ぼし、第2物質が存在しない場合の第1物質単独の光触媒活性より高くする割合が変化することが見出された。なお、上記において「酸および/または塩基」を添加するとしたのは、酸や塩基で第1物質や第2物質を析出させる場合に、その析出速度を調節する等の目的で、酸や塩基単独ではなく、酸と塩基と混合物を使用する場合もあり得るからである。
【0078】
p型量子触媒における第1物質と第2物質の割合は、第1物質1モル部に対して第2物質が1000兆分の1〜1モル部にすることが好ましく、第2物質が1兆分の1〜1モル部の範囲にあることがより好ましい。
【0079】
酸および/または塩基を使用する場合、添加用溶液中の酸および/または塩基の濃度については、100万分の1〜1mol%の範囲にすることが好ましい。更に、第1物質スラリの濃度については、固体物質の濃度が0.1〜35重量%(以下、w%と記述する。)の範囲であることが好ましい。分散剤、スラリの撹拌方法、およびスラリ温度についても光触媒活性に影響を及ぼし得るので、実情に応じて適宜選択することが好ましい。
【0080】
なお、上記とは逆に、光触媒活性を発現し得る第1物質と、3族原子の酸化物である第2物質とが接合されてなるp型量子触媒の製造方法であって、第2物質の粒子を水などの溶液で第2物質スラリを作製し、当該第2物質スラリに酸または塩基による処理により第1物質を析出し得る化合物を含んでなる溶液を加え混合スラリを作成し、当該混合スラリに酸および/または塩基を添加して、当該第2物質の結晶表面に第1物質を析出させ、当該析出に際して、p型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比)、当該酸および/または塩基の濃度、当該酸および/または塩基の添加速度、当該スラリの濃度、当該スラリの撹拌方法、当該スラリの温度ならびに分散剤の種類と量からなる群から選ばれた少なくとも一つの条件を選択することにより、p型量子触媒の光触媒活性を、第1物質単独の光触媒活性より大とする効果が得られることが見出された。
【0081】
次に、本発明に係るp型量子触媒の製造方法について説明する。
【0082】
「実施例3」(p型量子触媒の製造方法)
【0083】
本発明に使用する「第2物質を析出し得る化合物」や「第1物質を析出し得る化合物」については、本発明の主旨に反しない限りどのような化合物を使用してもよい。水酸化物、酸との塩等を好ましく挙げることができる。たとえば第2物質が酸化ホウ素の場合は酸化ホウ素のアルカリ金属塩、メタホウ酸ナトリウム、四ホウ酸ナトリウム、含水鉱物としてのホウ砂等を、第1物質が酸化チタンの場合はチタン酸ナトリウムを例示することができる。四ホウ酸ナトリウムは、化学式B4Na2O7と記述される所謂、ホウ酸ナトリウムであり、ホウ酸ナトリウム1分子は、ホウ素4原子とナトリウム2原子を含む。
【0084】
これらの化合物を溶解するための溶媒は通常水であるが、それ以外のもの、たとえばエタノール等であってもよい。第2物質や第1物質の析出を調整するために複数の溶媒からなる混合溶媒を使用することが有用な場合もあり得る。
【0085】
本発明に係る「第1物質の粒子」や「第2物質の粒子」についてもそのサイズや形状に特に制限があるわけではないが、一般的には、粒子径がナノオーダー、たとえば1次粒径が1〜100nmであることが好ましい。
【0086】
本発明における酸や塩基についても、第1物質や第2物質を析出し得るものであればどのようなものでもよい。酸としては塩酸や硫酸、硝酸を、塩基としては苛性ソーダ等のアルカリ化合物を好ましく例示できる。アルカリ土類金属化合物も使用できる。
【0087】
本発明に係るp型量子触媒の製造方法の概要を、第1物質として酸化チタンを使用し、第2物質として3族原子の酸化物である酸化ホウ素を用いる場合についての1例を、図9に示す。
【0088】
図9工程1の酸化チタンスラリ作成において、粒子径7nm程度の酸化チタンを、界面活性剤を適宜加えた水溶液に加え撹拌して酸化チタンスラリを作製する。次に、同図9工程2の混合スラリ作成において、工程1で作成した酸化チタンスラリに酸化ホウ素のアルカリ金属塩水溶液を加え撹拌して混合スラリを作製する。次に、同9図工程3のイオン交換で、工程2で作製した混合スラリに塩酸を滴下しながら撹拌してイオン交換して酸化ホウ素を酸化チタン粒子の表面に析出させ、酸化チタンと酸化ホウ素とが接合するp型量子触媒スラリを作成する。
【0089】
第2物質の酸化ホウ素のアルカリ金属塩として、酸化ホウ素と水酸化ナトリウムとからなるホウ酸ナトリウムを用いる。酸化ホウ素と水酸化カリウム等のホウ酸アルカリ金属塩等の場合も同様である。また、工程1で作成する酸化チタンスラリは弱酸性を呈し、工程2で加える酸化ホウ素金属塩溶液のアルカリ成分が工程1の酸性成分より多くない場合は、工程2で加える酸化ホウ素アルカリ金属塩溶液を加え撹拌するとき、酸化チタンスラリの酸性成分によりイオン交換され第2物質のホウ酸が第1物質の酸化チタン粒子の表面に析出し、工程3を実施すること無く、p型量子触媒スラリを製造することができる。
【0090】
工程1と工程2を区分する事無く、酸化ホウ素のアルカリ金属塩水溶液を含む溶媒に、界面活性剤を適宜加え、酸化チタン粒子を加え撹拌することで、混合スラリを直接作成しても構わない。
【0091】
次に、本発明に係る撹拌方法について説明する。
【0092】
「実施例4」(撹拌方法)
【0093】
図10に量子触媒の作成に用いる4種の分散方法を模式図で示す。
【0094】
図10(a)は、溶液を回転子で撹拌するSTR撹拌を示す。
【0095】
図10(b)は、溶液に0.5mm径程度のビーズを適量いれ、回転子で撹拌するBM撹拌を示す。量子触媒の合成には、コンタメ成分混入を極力避ける必要があるので、ビーズとして、十分機械的強度が高く、かつ4族のチタンと同じ4族のジルコニウム酸化物のジルコニアビーズを使用することが好ましい。
【0096】
図10(c)は、STR撹拌時に、超音波ホモジナイザを用いて超音波を照射し超臨界場における攪拌を実現するHG撹拌を示す。超音波ホモジナイザとしてBranson社製Sonifierを、超音波周波数として19.9KHzを、超音波照射エネルギとして100Wを、例示することができる。
【0097】
図10(d)は、HG撹拌時に、0.5mm径程度のジルコニアビーズを適量いれ撹拌するNS撹拌を示す。
【0098】
なお、BM攪拌やNS攪拌におけるビーズ量は、効果的に分散できるように適宜調整するものとする。
【0099】
次に、本発明に係る酸化チタンスラリ濃度について説明する。
【0100】
「実施例5」(酸化チタンスラリ濃度)
【0101】
酸化チタンスラリ濃度については、たとえば溶媒が水の場合、濃度は0.1〜35w%程度が好ましい。酸化チタンスラリ濃度は1〜20w%が、より好ましい。酸化チタンは光触媒活性に優れているものを用いることが好ましく、市販品で優れた光触媒活性を発現する石原産業製ST−01、テイカ製TKP−101、アエロジル製P25などを例示することができる。
【0102】
酸化チタンスラリ濃度を、2.5 〜10.0w%の場合について、撹拌時間をパラメータとして、NS拡散の平均粒径を図11に示す。粒径測定には、大塚電子株式会社製濃厚系粒径アナライザーFPRA−1000を使用した。以降、同装置を使用してスラリ粒径を測定する。
【0103】
図11の横軸は、酸化チタンスラリの重量濃度w%を、縦軸は平均粒径nmを表す。酸化チタン1モル部あたり50〜300分(以下、溶質1モルあたりの攪拌時間[分/モル] を、mpmと記述する。)NS攪拌した酸化チタンスラリの平均粒径を、攪拌時間をパラメータとして図11に示す。粒径は50mpm間隔で測定した。図中、NS攪拌時間に対する平均粒径を、50mpmを実曲線、100mpmを破曲線、150mpmを1点鎖曲線、200mpmを2点鎖曲線、250mpmを2重曲線、300mpmを2重破曲線で示す。
【0104】
酸化チタンスラリ濃度が2.5w%の場合、NS撹拌50mpmで163.7nm, 100mpmで144.4nm, 150mpmで138.7nm, 200mpmで166.3nm, 250mpmで131.9nm, 300mpmで125.2nmとなった。NS撹拌200mpmの極大特異点を除き、平均粒径はNS攪拌の経過時間に関して単調に減少した。
【0105】
酸化チタンスラリ濃度が5.0w%の場合、NS撹拌50mpmで175.2nm, 100mpmで147.7nm、150mpmで136.8nm, 200mpmで131.1nm, 250mpmで125.1nm, 300mpmで117.6nmとなった。平均粒径はNS攪の経過時間に関して単調に減少した。
【0106】
酸化チタンスラリ濃度が10.0w%の場合、NS攪拌50mpmで261.3nm, 100mpmで204.5nmと攪拌経過時間に関して平均粒径は減少した。NS攪拌100mpmの平均粒径を極小とし、100mpm以降の平均粒径は攪拌経過時間に関して増大し、150mpmで252.7nm, 200mpmで390.3nm, 250mpmで467.7nm, 300mpmで1334.0nmとなった。
【0107】
次に、本発明に係る分散剤濃度について説明する。
【0108】
「実施例6」(分散剤濃度)
【0109】
酸化チタンスラリの作成において、溶媒が水の場合、分散剤を加えた溶媒に、酸化チタン粉末を加え撹拌することが好ましい。分散剤の使用量は、酸化チタンに対して0.1〜10.0w%を加えることが好ましく、0.2〜4.0w%が、より好ましい。分散剤として酸化チタンの水媒体中の分散特性に優れる界面活性剤を用いることが好ましい。市販の界面活性剤として、花王株式会社製ポリカルボン酸型高分子界面活性剤DEMOL EP、サンノプコ株式会社製ポリカルボン酸アンモニウム塩SNディスパーサント5468等を例示することができる。
【0110】
図12に、酸化チタンに対する分散剤DEMOL EPの濃度を0.2〜4.0w%に関するNS攪拌した酸化チタンスラリの平均粒径を示す。酸化チタンスラリ濃度は5.0w%とした。同図において、横軸は分散剤濃度w%を示し、縦軸は平均粒径nmを示す。
図12において、NS攪拌50mpmの平均粒径を実曲線、100mpmを破曲線、150mpmを1点鎖曲線、200mpmを2点鎖曲線、250mpmを2重曲線、300mpmを2重破曲線で示す。
【0111】
分散剤濃度が0.2w%の場合、NS攪拌50mpmで平均粒径184.7nm、100mpmで178.6nm、150mpmで170.2nmと攪拌経過時間に関して平均粒径は減少し、150mpmで極小平均粒径となった。さらに攪拌を継続すると、攪拌経過時間に関して平均粒径は増大し、200mpmで200.8nm, 250mpmで235.7nm, 300mpmで301.4nmとなった。
【0112】
分散剤濃度が0.4w%の場合、NS攪拌50mpmで平均粒径175.2nm、100mpmで147.7nm、150mpmで136.8nm、200mpmで131.1nm、 250mpmで125.1nm, 300mpmで117.6nmと、攪拌経過時間に関して平均粒径は単調に減少し、300mpmの117.6nmが最小値となった。
【0113】
分散剤濃度が1.2 w%の場合、NS攪拌50mpmで平均粒径165.6nm、100mpmで147.5nm、150mpmで141.9nmと、攪拌経過時間に関して平均粒径は単調に減少した。NS撹拌200mpmで193.1nmと極大値を呈した。さらに、NS撹拌を継続すると、250mpmで141.4nm, 300mpmで145.6nmと、撹拌継続時間に関して緩やかに増大した。
【0114】
分散剤濃度が4.0 w%の場合、NS攪拌50mpmで平均粒径218.0nm、100mpmで192.3nm、150mpmで186.5nm、200mpmで173.9nmと、攪拌継続時間に関して単調に減少し、200mpmで極小値を呈した。さらにNS撹拌を継続すると、250mpmで184.6nm, 300mpmで191.9nmと撹拌時間に関して増大した。
【0115】
次に、本発明に係る酸化チタンスラリの分散特性について説明する。
【0116】
「実施例7」(酸化チタンスラリの分散)
【0117】
図13に、粒径7nmの光触媒酸化チタンST−01と、酸化チタンの0.4w%の分散剤DEMOL EPを、溶媒の逆浸透膜処理水(RO水)に加え、図10に示した4種の攪拌方法で作成した酸化チタンスラリの撹拌継続時間に関する平均粒径特性を示す。酸化チタンスラリ濃度は5.0w%とした。図13の横軸は酸化チタンスラリの撹拌時間mpmを線形スケールで、縦軸は平均粒径nmを対数スケールで表す。
【0118】
図13の曲線は、それぞれ4種の攪拌方法の平均粒径特性を示しており、STR撹拌を実曲線、BM撹拌を破曲線、HG撹拌を1点鎖曲線、NS撹拌を2点鎖曲線で、それぞれ示す。4種の撹拌における酸化チタンスラリの温度を10℃に保ち、50mpm間隔で処理時間600mpmまでの平均粒径を測定した。
【0119】
(STR攪拌)
【0120】
図13の実曲線で示すSTR攪拌の平均粒径は、STR撹拌時間に対して、50mpmで578.5nm、100mpmで653.8nm、150mpmで626.1nm、200mpmで623.0nm、250mpmで523.5nm、300mpmで601.0nm、350mpmで735.9nm、400mpmで584.6nm、450mpmで579.2nm、500分で876.2nm、550mpmで923.6nm、600mpmで809.9nmであった。
【0121】
STR撹拌の平均粒径が、撹拌継続時間に関して単調に減少せず振動しながら変動していることは、STR撹拌の分散力が弱く、酸化チタン粒子間の凝集力に対抗しうる破砕力が実現できず、再凝集していることを示している。
【0122】
STR撹拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図14(a)に、STR撹拌600mpmの散乱強度分布と散乱強度累積を図14(b)に示す。図の棒グラフは散乱強度分布を、曲線は累積を示す。図の横軸は粒径値nmを、左縦軸は散乱強度分布%を、右縦軸は累積%を表す。
【0123】
STR攪拌300mpmの散乱強度分布は、ピーク713.6nmの単峰性を有し、平均粒径は601.0nmであった。STR攪拌600mpmの散乱強度分布は、粒径630.4nmに第1ピーク、2299.7nmに第2ピークを有し、平均粒径は809.9nmであった。
【0124】
(BM攪拌)
【0125】
図13の破曲線は、STR撹拌特性に機械的破砕力を加えたBM撹拌の平均粒径特性を示す。BM撹拌時間に対して、50mpmで390.9nm、100mpmで443.1nm、150mpmで342.9nm、200mpmで340.1nm、250mpmで312.5nm、300mpmで305.1nm、350mpmで301.6nm、400mpmで322.1、450mpmで310.3nm、500mpmで(極小値の)297.7nm、550mpmで299.9nm、600mpmで292.1nmであった。BM攪拌の平均粒径特性のPeak to Peak値は、145.4nmであった。
【0126】
図13に示したように、BM撹拌300mpmの平均粒径305.1nmは、STR撹拌300mpmの601.0nmの略1/2のデメンションとなった。また、300mpmを超えBM攪拌を継続すると、平均粒径290nmをフロワとする略平坦な特性を呈した。略290nmのフロワに沿って平坦な平均粒径特性となることは、STR攪拌との大きな差異であり、ビーズによる機械的破砕力で高次粒子を破砕し、高次粒子の再凝集を防止していると考えられる。
【0127】
BM攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図15(a)に、BM攪拌600mpmの散乱強度分布と累積を図15(b)に示す。BM攪拌300mpmの散乱強度分布は、粒径411.4nmにピークを、平均粒径は305.1nmであった。BM攪拌600mpmの散乱強度分布は、粒径407.2nmにピークを、平均粒径は292.1nmであった。BM撹拌300mpmのピーク粒径が、平均粒径の34.8%大なること、BM撹拌600mpmのピーク粒径が、平均粒径の39.4%大になること、ならびにBM撹拌が長時間になれば解離率が増大することから、ビーズ破砕力が不十分であり、再凝集を十分に防ぎ切れていないことが知れる。
【0128】
(HG攪拌)
【0129】
図13の1点鎖曲線は、HG撹拌の酸化チタンスラリの平均粒径特性を示す。攪拌時間に対して、50mpmで178.6nm、100mpmで144.9nm、150mpmで137.0nm、200mpmで123.1nm、250mpmで129.8nm、300mpmで113.7nm、350mpmで103.1nm、400mpmで103.0nm、450mpmで154.8nm、500mpmで153.9nm、550mpmで143.9nm、600mpmで120.5nmであった。
【0130】
HG撹拌の平均粒径は、若干の変動を除きHG撹拌400mpmまで攪拌継続時間に単調に減少し、400mpmで103.0nmの最小値を呈した。さらに攪拌を継続すると、450mpmで粒径が急激に反転増大し、平均粒径が50.3%増大し、再凝集が強く現れた。
【0131】
HG攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図16(a)に、HG攪拌600mpmの散乱強度分布と累積を図16(b)に示す。HG攪拌300mpmの散乱強度分布は、212.1nmにピークを、平均粒径は113.7nmであった。HG撹拌600mpmの散乱強度分布は、第1ピークが52.3nmに、第2ピークが263.4nmの双峰性を呈し、平均粒径は120.5nmであった。HG撹拌300mpmのピーク粒径の平均粒径に対する解離率が86.5%と大きく、高次粒子の潜在的存在が示されている。HG撹拌600mpmでは、複数のピークが検出され高次粒子の存在が直接確認でき、HG撹拌では、機械的破砕力が弱区、発生する強い再凝集力を抑圧できない。
【0132】
(NS攪拌)
【0133】
図13の2点鎖曲線は、HG撹拌にビーズによる機械的破砕力を加えたNS攪拌の酸化チタンスラリの平均粒径を示す。NS撹拌の平均粒径は、攪拌時間に対して、50mpmで175.25nm、100mpmで147.7nm、150mpmで136.8nm、200mpmで131.1nm、250mpmで125.1nm、300mpmで117.6nm、350mpmで114.0nm、400mpmで110.6nm、450mpmで105.3nm、500mpmで99.4nm、550mpmで99.4nm、600mpmで98.9nmと、攪拌時間に対して単調に減少した。
【0134】
NS攪拌300mpmの酸化チタンスラリ粒径の散乱強度分布と累積を図17(a)に、NSG攪拌600mpmの散乱強度分布と累積を図17(b)に示す。NS撹拌300mpmの散乱強度分布は、ピークが193.3nm、平均粒径が117.6nmであった。NS撹拌600mpmの散乱強度分布は、ピーク170.1nm、平均粒径98.9nmであった。
【0135】
NS撹拌300mpmと600mpmの散乱強度分布は、共に、単峰性特性であった。NS撹拌300mpmのピーク粒径の平均粒径に対する解離率が64.4%、HG撹拌600mpmの解離率は72.0%と、NS撹拌が長時間程、解離率が増大し、再凝集が発生し、高次粒子が潜在していることが知れ、NS撹拌のビーズ破砕力が、不十分であったことが判明した。
【0136】
図10に示した4種の何れの攪拌方法で作成した酸化チタンスラリを、1次粒子まで分散できなかった。
【0137】
NS攪拌が酸化チタンスラリ平均粒径の最小値98.9nmを提示した。図10に示すビーズ破砕力を増強すれば、酸化チタンスラリの再凝集粒子は分散され、引いては、比表面積の大きな量子触媒を合成することが可能になる。再凝集を阻止する分散手段を採用することで、さらなる比表面積の大なる量子触媒の合成が可能になり、量子触媒の光触媒活性をさらに改善することが可能となるが、本特許で開示する合成方法の主旨を阻害するものではない。再凝集している酸化チタンスラリから量子触媒を合成した場合でも、光触媒活性が第1物質の光触媒単独に比べ10倍以上改善できているならば、本発明の主旨を証明するに十分である。また、1次粒子まで分散した酸化チタンスラリを用いて合成する量子触媒の光触媒活性は、さらに光触媒活性を改善することは容易に推察できる。
【0138】
次に、本発明に係るp型量子触媒の第2物質析出に用いる塩酸量について説明する。
【0139】
「実施例8」(p型量子触媒の第2物質析出)
【0140】
p型量子触媒の主要製造プロセスにおいて、図9に示した工程1で溶媒の水に分散剤と酸化チタン結晶を加え撹拌して酸化チタンスラリを作成し、工程2で当該酸化チタンスラリに酸化ホウ素アルカリ塩溶液を加え撹拌し混合スラリを作成し、工程3のイオン交換工程で当該混合スラリに酸/アルカリを加え第2物質を酸化チタン表面に析出させp型量子触媒スラリを作成する。混合スラリの作成にあたり、溶媒に分散剤、酸化チタン結晶、ならびに酸化ホウ素アルカリ塩溶液を加え撹拌し、酸化チタンスラリを作成すること無く、混合スラリを作成しても構わない。
【0141】
ナノメートルオーダと小さな粒径の酸化チタン結晶は水等の溶媒中で強い凝集力を生じるので、超音波を照射し超臨界場を発生させ、超臨界場中においてジルコニアビーズで撹拌することが好ましい。超音波周波数は、19kH以上が好ましい。超音波照射強度は、溶質1gあたり0.1W〜100Wが好ましい。0.01〜2mm径ジルコニアビーズでビーズ撹拌することが好ましい。酸化チタンスラリ中の酸化チタン濃度は0.1〜35w%が、好ましい。酸化チタンスラリを1〜35℃の範囲に保ちながらNS撹拌することが好ましい。
【0142】
混合スラリ中の酸化ホウ素濃度が、酸化チタン1モル部に対して4000兆分の1〜0.25モル部が好ましい。酸化ホウ素の量は、酸化チタン1モル部に対して酸化ホウ素4兆分の1〜0.025モル部が、より好ましい。酸化ホウ素アルカリ塩溶液の濃度を調整し、混合スラリへの添加容量を混合スラリの1〜10%の範囲にすることが好ましい。
【0143】
酸化ホウ素アルカリ塩としてホウ酸ナトリウムを例示できる。ホウ酸ナトリウム(Na2B4O7)1分子には、ナトリウム(Na)が2原子、ホウ素(B)が4原子含まれているので、混合スラリ中におけるチタン1原子に対するホウ素原子数比 が、1000兆分の1〜1の割合が好ましく、ホウ素原子数比1兆分の1〜1がよりに好ましい。以降、比( ホウ素原子の数/チタン原子の数) を、ホウ素原子数比と呼ぶ。
【0144】
チタン金属の酸化物である酸化チタンの水を溶媒とする酸化チタンスラリは弱酸性を呈し、ホウ酸ナトリウムは弱アルカリ性を呈するので、混合スラリの作成にあたり、ホウ酸ナトリウム溶液をゆっくり滴下することが好ましい。混合スラリ作成にあたり、酸化チタンスラリを10℃前後に保ちNS撹拌しながらホウ酸ナトリウム溶液をゆっくり滴下することが、より好ましい。
【0145】
ホウ酸ナトリウム溶液のアルカリ成分が、酸化チタンスラリの酸性成分に比べ少ない場合は、図9工程3のイオン交換のために塩酸を添加することは必ずしも必要無い。
【0146】
ホウ素原子数比100万分の1の混合スラリを作成し、工程3のイオン交換の塩酸滴下量がp型量子触媒の光触媒活性に及ぼす影響を調べた。
【0147】
図18は、イオン交換に使用した塩酸使用率(100%、50%、0%)をパラメータとして、観測ポイントの反応速度比を示す。ホウ酸ナトリウム1モル部に、ナトリウムが2モル部含まれているので、ナトリウム全量を塩酸で中和するには2モル部の塩酸を要する。この2モル部の塩酸を使用する場合を塩酸使用率100%、その半分の1モル部の塩酸を用いる場合を塩酸使用率50%、塩酸を全く使用しない場合を塩酸使用率0%とした。滴下する塩酸溶液の容積を、酸化チタンスラリ容積の0.1〜10%の範囲にすることが好ましい。
以降、塩酸使用率は、混合スラリに含まれるアルカリ成分を中和するために使用する塩酸の使用率を示すものとする。
【0148】
塩酸使用率100%、50%、0%として作成したp型量子触媒の光触媒活性を測定した。
【0149】
作成したp型量子触媒スラリをシャーレに採り室温乾燥させたサンプルを作成し、略24時間間隔でガスパックA法に準拠してアセトアルデヒドガスの残留濃度比を20回測定した。p型量子触媒ならびに第1物質単独の残留濃度比から反応速度を求め、p型量子触媒の反応速度と第1物質単独の反応速度との比(反応速度定比)を求めた。以降、値(p型量子触媒の反応速度/第1物質単独の反応速度) を反応速度比と呼び、量子触媒がn型の場合は、値(n型量子触媒の反応速度/第1物質単独の反応速度) を反応速度比と呼ぶ。以降、反応速度定比を量子触媒の光触媒活性の評価に使用する。
反応速度定比は、量子触媒の光触媒活性を表現する重要な値である。量子触媒がp型であるかn型であるかは区別しない。さらに、量子触媒の活性が酸化あるいは還元性であるかを区別せず、統一的に光触媒活性を表現する。反応速度は、残留濃度比の対数の定数倍で与えられる。しかし、測定系の特性と対象物質の質量で定まる値であるので、第1物質と量子触媒の残留濃度を同一条件で測定する場合の定数は互いに等しくなり、反応速度定比から測定系と質量で定まる定数は相殺され、量子触媒と第1物質単独の光触媒活性との比を表す量となる。
【0150】
残留濃度比の平均値から求まる反応速度定比を平均反応速度比とした。
p型量子触媒の反応速度比と平均反応速度比を、塩酸使用率をパラメータとして、図18に示す。
【0151】
図18の横軸は、観測ポイントを表し、縦軸は反応速度比を表す。観測ポイント間隔は、略24時間とした。
【0152】
図18の実曲線は、p型量子触媒5Gp-1m/1の反応速度定比特性を示す。名称「5Gp-1m/1」における、「5Gp−1m」は、ホウ素原子数比が1ppm、すなわち100万分の1のp型量子触媒であることを、名称末尾の「/1」は塩酸使用率が100%であることを示す。実曲線上のドットは5Gp-1m/1の反応速度比を、データラベルはその値を示す。
【0153】
5Gp-1m/1の反応速度比は、観測ポイントに対して順に、3.56、2.41、2.32、1.79、2.41、2.91、2.41、2.33、2.71、2.27、2.65、2.33、2.65、2.71、2.94、2.65、3.24、3.00、3.00、3.24であった。第1観測ポイントで最大値3.56を、第4観測ポイントで最小値1.79を呈した。
【0154】
図18の実線は、p型量子触媒5Gp−1m/1の平均反応速度比5Gp-1m/1 Aveを示し、その値は2.64であった。
【0155】
図18の破曲線は、p型量子触媒5Gp-1m/0.5の反応速度比特性を示す。名称「5Gp-1m/0.5」における、「5Gp-1m」はホウ素原子数比が1ppmのp型量子触媒であることを、「/0.5」は塩酸使用率が50%であることを示す。破曲線上のドットは反応速度比を、データラベルはその値である。
【0156】
5Gp-1m/0.5の反応速度比は、第1観測ポイントの2.36、第16観測ポイントならびに第20観測ポイントの2.33を下限とし、第6観測ポイントの最大値3.53との間で変動した。
【0157】
図18の破線は、p型量子触媒5Gp−1m/0.5の平均反応速度定比5Gp-1m/0.5 Aveを示し、その値は2.76であった。
【0158】
図18の1点鎖曲線は、p型量子触媒「5Gp-1m/0」の反応速度比特性を示す。名称「5Gp―1m/1」における、「5Gp-1m」はホウ素原子数比が1ppmのp型量子触媒であることを、「/0」は塩酸使用率が0%であることを示す。1点鎖曲線上のドットは反応速度比の観測値、データラベルはそのデータ値である。
【0159】
5Gp-1m/0の反応速度比は、第1観測ポイントの2.36、第13観測ポイントならびに第14観測ポイントの2.59を下限とし、第9観測ポイントの最大値3.44との間を変動した。
【0160】
図18の1点鎖線は、量子触媒5Gp−1m/0の20観測ポイントの平均反応速度比5Gp-1m/0 Aveを示し、その値は2.92であった。
【0161】
p型量子触媒5Gp-1m/1 Ave、5Gp-1m/0.5 Ave、ならびに5Gp-1m/1 Aveの平均反応速度比が2.61、2.76、5、ならびに2.92であり、塩酸を使用しない5Gp-1m/0 Aveの平均反応速度比が最大となることが判明した。
【0162】
p型量子触媒5Gp-1m/0の最小反応速度比、平均反応速度比、最大反応速度比は、それぞれ2.36、2.92、3.44であり、光触媒活性が第1物質の酸化チタン単独の場合に比べ525倍、6918倍、7万5858倍であった。
【0163】
p型量子触媒5Gp-1m/0の光触媒活性は、最悪の場合でも、第1物質の酸化チタン単独の525倍あり、量子触媒の制約条件である10倍以上を保証している。
【0164】
p型量子触媒5Gp-1m/0が3種の塩酸使用率で最も大きな反応速度比を与えるように、ホウ素原子数比が1ppm、すなわち100万分の1と十分小さい場合、塩酸によるイオン交換は必ずしも必要では無く、金属酸化物である酸化チタンの水スラリが呈する酸成分で、十分に第2物質の酸化ホウ素アルカリ金属塩のナトリウムを中和し、イオン交換できることが判明した。かかる塩酸使用率が小さい場合、図9の工程3のイオン交換のための塩酸添加を実行する必要が無く、工程2の混合スラリ作成時にp型量子触媒が合成され、塩酸などの酸化チタンと酸化ホウ素以外の物質の混入を防止できる高純度なp型量子触媒スラリを合成できる利点に加え、大きな平均反応速度比値を獲得できる優れたp型量子触媒合成手段を提供できる利点が生じる。
【0165】
次に、本発明に係るp型量子触媒のホウ素原子数比に対する反応速度定比特性について説明する。
【0166】
「実施例9」(p型量子触媒のホウ素原子数比特性)
【0167】
p型量子触媒または酸化チタンST−01の各10mgを、5Lのテドラーバッグに入れ、80〜100重量ppm濃度に調整した標準ガス(窒素キャリアガス、アセトアルデヒド標準ガス)を3L注入し、照射強度1.0mW/平方cmの紫外線を照射し、20分経過後の残留濃度をガス検知管(ガステック社製 No.92M)で測定した。酸化チタンST−01を基準光触媒として求めた反応速度比を、図19に示す。
【0168】
紫外線光源として、東芝ライテック社製ブラックライトFL40SBLを用い、コニカ・ミノルタ社製UV RadioMeterUM−10、受光部同社製UM−360にて量子触媒表面の紫外線強度を測定した。
【0169】
同一重量を用いて同一環境で残留濃度を測定する場合、測定対象のp型量子触媒に含まれる第1物質である酸化チタン量は、第1物質以外の物質の重量分だけ少なくなる。また、第1物質以外の物質である酸化ホウ素は、光触媒活性をほとんど発揮しないことが知られている。このような条件で、p型量子触媒の光触媒活性が第1物質の光触媒活性を上回ること、すなわちp型量子触媒の反応速度比が1を上回ることは、これまで知られていなかった。これは、既述のごとく、第2物質が不純物としてアクセプタ準位を第1物質のバンドギャップに付与し、第1物質へ自由電子とホールとが効果的に注入され、これによって第1物質の表面から放出される自由電子とホールとの量が増大し、酸化チタンの有する光触媒活性を上回る光触媒活性を獲得することを明確に示すことになる。
【0170】
ホウ素原子数比が、100ppt(=100億分の1)、1ppb(=10億分の1)、10ppb(=1億分の1)、100ppb(=1000万分の1)、1ppm(=100万分の1)、10ppm(=10万分の1)、100ppm(=1万分の1)、1000ppm(=0.001)、ならびに1%(=0.01)の場合について、第4の形態のp型量子触媒の製造方法に示した手順に従い、p型量子触媒5Gp―100t/1、5Gp―1b/1、5Gp―10b/1、5Gp―100b/1、5Gp―1m/1、5Gp―100m/1、5Gp―1000m/1、および5Gp―1%/1を作成した。
【0171】
これらp型量子触媒の名称は、上記と同様であり、例えば名称「5Gp―100t/1」における、「5Gp―100t」は、ホウ素原子数比が100億分の1、すなわち100pptのp型量子触媒であることを、「/1」は塩酸使用率が100%であることを示す。
【0172】
図9工程1における酸化チタンスラリ濃度は、工程1の水と分散剤と工程2で印加するホウ酸ナトリウム溶液と第3工程で滴下する塩酸溶液に含まれる水を勘案し10w%となるように調整、NS撹拌を150mpm、分散剤Demol EP量は酸化チタン重量の0.4%とした。
【0173】
図9工程2における(四)ホウ酸ナトリウム溶液は、液量が酸化チタンスラリ容量の略3%となるように濃度を調整、NS撹拌を50mpmとした。
【0174】
第3工程の希塩酸量を酸化チタンスラリ容量の略0.5%になるように濃度を調整、NS撹拌を25mpmとした。
【0175】
図19に、作成したp型量子触媒5Gp―100t/1、5Gp―1b/1、5Gp―10b/1、5Gp―100b/1、5Gp―1m/1、5Gp―10m/1、5Gp―100m/1、5Gp―1000m/1、および5Gp―1%/1のホウ素原子数比に対する反応速度比特性を示す。図19の横軸はホウ素原子数比を示し、単位pptは1兆分の1、ppbは10億分の1、ppmは100万分の1、%は0.01を表す。
【0176】
作成した濃度10w%のp型量子触媒スラリ100mgをシャーレに採り室温乾燥させたp型量子触媒10mgを用いて、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を、略24時間の間隔を置き30回測定した。30回計測した残留濃度比の算術平均に対する反応速度比を平均反応速度比5Gp/1-Aveとした。平均反応速度比を、図19の実曲線で示す。実曲線5Gp/1-Ave上のドットの横位置はホウ素原子数比を、その縦位置は平均反応速度比を、データラベルは反応速度比の値を示す。
【0177】
同19図の1点鎖曲線5Gp/1−worstは、最小反応速度比を示す。30回計測した残留濃度比の最大値に対する反応速度比を最小反応速度比とした。1点鎖曲線5Gp/1−worst上のドットの横位置はホウ素原子数比を、縦位置は最小反応速度比を、データラベルは最小反応速度比の値を示す。
【0178】
同図19の破曲線5Gp/1−bestは、最大反応速度比を示す。30回計測した残留濃度比の最小値に対する反応速度比を最大反応速度比とした。破曲線5Gp/1−best上のドットの横位置はホウ素原子数比を、縦位置は最大反応速度比を、データラベルは最大反応速度比の値を示す。
【0179】
繰り返し30回計測して、計測上の擾乱要因を除去し、ホウ素原子数比100ppt〜1%に関するp型量子触媒5Gp−100t/1〜5Gp−1%/1の反応速度比値の信頼度を高めた。計測間隔は、略24時間であった。
【0180】
図19の平均反応速度比5Gp/1−ave、最大反応速度比5Gp/1−best、ならびに最小反応速度比5Gp/1−worstが示すように、ホウ素原子数比が変化すると、反応速度比すなわち光触媒活性が敏感に変化することが見出された。
【0181】
具体的には、図19の5Gp/1−aveが示すように、p型量子触媒のホウ素原子数比に対する平均反応速度比は、ホウ素原子数比が100pptの場合2.29、1ppbの場合2.60、10ppbの場合2.72、100ppbの場合3.35、1ppmの場合3.21、10ppmの場合2.73、100ppmの場合2.63、1000ppmの場合2.55、1%の場合2.63であった。p型量子触媒のホウ素原子数比が100ppb〜1ppm前後における平均反応速度比は3.35〜3.21の最大な値を示した。平均反応速度定比の3.35は、光触媒活性が第1物質の酸化チタン単独の5万119倍であることを示すものである。
【0182】
また、図19に示すようにホウ素原子数比1ppt〜1%の領域におけるp型量子触媒の平均反応速度定比は1以上であり、第1物質の酸化チタン単独の光触媒活性を上回っていた。
【0183】
図19の最大反応速度比5Gp/1−bestが示すように、p型量子触媒のホウ素原子数比に対する最大反応速度比は、100pptの場合3.03、1ppbの場合3.27、10ppbの場合4.58、100ppbの場合4.67、1ppmの場合5.08、10ppmの場合3.71、100ppmの場合3.34、1000ppmの場合3.71、1%の場合3.27であった。ホウ素原子数比が1ppmの最大反応速度比5.08が最大であった。最大反応速度定比5.08は、光触媒活性が1億4454万3977倍であることを示す。
【0184】
図19の最小反応速度比5Gp/1−worstに示すように、p型量子触媒のホウ素原子数比に対する最小反応速度比は、100pptの場合1.65、1ppbの場合1.70、10ppbでの場合2.21、100ppbの場合2.68、1ppmの場合2.59、10ppmの場合2.13、100ppmの場合2.24、1000ppmの場合1.91、1%の場合1.91であった。p型量子触媒のホウ素原子数比が100pptの最小反応速度比1.65が最小であった。最小反応速度比1.65は第1物質の酸化チタン単独の光触媒活性の20倍であることを示す。ホウ素原子数比100ppt〜1%の領域におけるp型量子触媒の光触媒活性は、光触媒の20倍以上あり、本発明で開示するp型量子触媒は第1物質の酸化チタンの10倍以上の光触媒活性を最悪の場合でも保障することが知れた。
【0185】
ホウ素原子数比が1pptのp型量子触媒の反応速度定比は、最大値5.08、最小2.59、平均3.21であり、光触媒活性は第1物質の酸化チタンの光触媒活性の最大1億4千万倍強、最小1500倍強、平均2万6千倍強であることが判明した。
【0186】
作成したp型量子触媒スラリ5Gp―100t/1〜5Gp―1%/1粒径の散乱強度分布と累積の測定結果を、図20〜28に示す。
【0187】
図20にp型量子触媒スラリ5Gp−100t/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100t/1は、813.6nmに散乱強度ピークを有し、平均粒径は395.9nmであった。
【0188】
図21にp型量子触媒スラリ5Gp−1b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1b/1は、53.8nmに第1、390.4nmに第2、2625.8nmに第3の散乱強度ピークを有し、平均粒径は409.7nmであった。
【0189】
図22にp型量子触媒スラリ5Gp−10b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−10b/1は、86.8nmに第1、1164.7nmに第2の散乱強度ピークを有し、平均粒径は572.9nmであった。
【0190】
図23にp型量子触媒スラリ5Gp−100b/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100b/1は、528.2nmに第1、4295.0nmに第2の散乱強度ピークを有し、平均粒径は801.7nmであった。
【0191】
図24にp型量子触媒スラリ5Gp−1m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1m/1は、927.9nmに散乱強度ピークを有し、平均粒径は801.7nmであった。
【0192】
図25にp型量子触媒スラリ5Gp−10m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−10m/1は、300.5nmに散乱強度ピークを有し、平均粒径は159.1nmであった。
【0193】
図26にp型量子触媒スラリ5Gp−100m/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−100m/1は、1860.7nmに散乱強度ピークを有し、平均粒径は778.8nmであった。
【0194】
図27にp型量子触媒スラリ5Gp−1000m/1の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1000m/1は、202.5nmに散乱強度ピークを有し、平均粒径は125.6nmであった。
【0195】
図28にp型量子触媒スラリ5Gp−1%/1粒径の散乱強度分布と累積を示す。p型量子触媒スラリ5Gp−1%/1は、49.9nmに第1、378.4nmに第2、2560.6nmに第3、4万7162.1nmに第4の散乱強度ピークを有し、平均粒径は2112.1nmであった。
【0196】
p型量子触媒における当該第1物質と当該第2物質の割合については特に制限はないが、p型量子触媒における第1物質に対する第2物質の比率をだんだん多くしていくと、p型量子触媒の反応速度比(言い換えれば光触媒活性)が上昇後下降するか、あるいは反応速度比が1以上で上昇下降を繰り返して、1個以上のピークが存在することが見出されており、ある範囲内にあることが好ましいと言えよう。一般的に言えば、p型量子触媒におけるホウ素原子数比が1000兆分の1〜1の範囲にあることが好ましく、ホウ素原子数比が1兆分の1(1ppt)〜1の範囲にあることがより好ましい。
【0197】
以下、光触媒活性が、第1物質単独の場合に比べ高くなるメカニズムについて説明する。ただし、以下の説明は本発明の理解を助けるためのものであり、本発明の範囲を制限するものではない。
【0198】
図7に示したように、接合面では酸化チタンのチタン原子と酸化ホウ素の酸素原子が電子を共有し、チタン原子とホウ素原子が酸素原子を挟み互いに接合されている。換言すれば、接合面において、ホウ素原子が酸化チタン結晶に直接接した結晶構造が構築され、第2物質のホウ素原子は、酸化ホウ素分子の励起エネルギより低い励起エネルギでアクセプタとして励起する。以降、第2物質の酸化ホウ素の励起エネルギを略0.025eVと記述するのは、前述の考察に基づくものであるが、この考察結果は本発明の本質とは関係が無く、p型量子触媒が量子線で励起するという物理現象を解析した一例として記述したものである
【0199】
次に、本発明に係るn型量子触媒について説明する。
【0200】
<n型量子触媒>
【0201】
本発明に係るn型量子触媒は、光触媒活性を発現し得る「いわゆる光触媒」である第1物質と、5族〜7族から選ばれた原子あるいはその酸化物である第2物質から成る物質であり、光触媒活性が第1物質単独の10倍以上の物質である。
【0202】
図29に第1物質である4族原子類酸化物と第2物質の5族原子の酸化物とが接合して成る本発明に係るn型量子触媒の模式図をラチス結晶モデルで示す。
【0203】
第1物質の4族原子類酸化物の酸素原子の最外殻軌道のホールに第2物質の5族原子酸化物の5族原子の電子が捕捉され、第1物質の4族原子類酸化物の酸素原子に第2物質が結晶成長し、第1物質の結晶構造を保存したまま、第1物質と第2物質が接合するn型量子触媒が実現される。
【0204】
図29はあくまで模式図である。対象となる粒子の1次粒子径が数ナノメートルと小さいため、かつ光触媒活性を発現している場合は動的に結晶構造が変動するものと考えられ、具体的にどのようになっているかは定かでない。
【0205】
本発明に係るn型量子触媒は、恐らく、図29に示すように、第2物質が、第1物質表面に結晶成長した結果、第2物質が接合面を成しているものと思われる。第1物質が第2物質と接合面を成していると考えられる結果、第1物質単独の場合に比べ光触媒活性が高められていることが確かめられれば十分である。この接合は、第1物質と第2物質とが互いに接触した状態にあることを意味し、第2物質が第1物質表面に結晶成長した状態のものや、第1物質が第2物質表面に結晶成長した状態のものや、第2物質と第1物質とのナノコンポジット状態のものを例示することができる。これらは、第1物質の結晶表面上に第2物質を析出させるか、第2物質の結晶表面上に第1物質を析出させるか、第1物質を析出しうる溶液と第2物質を析出しうる溶液の混合溶液から両物質を析出させる。また、結晶構造に歪を与えるので好ましくないが、イオン打ち込み技術で第2物質イオンを第1物質にイオンインプラテーションするか、イオン打ち込み技術で第1物質イオンを第2物質にイオンインプラテーションすることでも実現できる。
【0206】
n型量子触媒における第1物質と5族原子酸化物を不純物として含む接合面近傍の結晶構造を示す模式図29は、n型量子触媒の動作を説明するためにラチス結晶モデルで単純化した結晶構造を表現したものであり、実際に観測する結晶構造とは異なる場合があるが、将来観測されるようになった場合の観測結果と結晶模式図の相違は本特許の主旨を阻害するものでは無い。
【0207】
図29の左下がり斜線を施した部分は第1物質を、右下がり斜線を施した部分は第2物質を示し、左下がり斜線部と右下がり斜線部が接する部分が接合面であり、第2物質の5族原子が第1物質の結晶構造を乱す事無く第1物質の不純物として接合している。
【0208】
次に、本発明に係るn型量子触媒の作成について説明する。
【0209】
「実施例10」(n型量子触媒の作成)
【0210】
図30に、第2物質の5族原子酸化物として例示する酸化リンのリン原子構造を示す。同図において、図4と同様に、最外殻電子軌道を大きな円で、最外殻軌道上の電子をハッチ付小丸で、ならびに最外殻軌道以外の電子と原子核等をハッチ付丸で模式的に示している。ハッチ付丸の「P」は、原子名「リン」を示す。
【0211】
図31に第1物質の4族原子類酸化物として例示する酸化チタンを、第2物質の5族原子酸化物として例示する酸化リンから成る本発明に係るn型量子触媒の模式図をラチスモデルで示す。同図は、第1物質の酸化チタンの酸素原子の酸化リアクションセンターに第2物質のリン原子の電子が捕捉され結晶成長した量子触媒の一種であるn型量子触媒を、ラチス結晶モデルを示した図である。同図は本発明の一例として開示するn型量子触媒であり、第1物質の酸化チタンと第2物質の酸化リンが接合面を成し、接合面近傍において、第2物質のリン原子が第1物質の結晶構造を乱す事無く第1物質の不純物となっていることを示す。
【0212】
第2物質の酸化リンが第1物質の酸化チタンに結晶成長した場合、接合面近傍では第1物質の酸化チタンの結晶構造を第2物質が継承する。本発明が開示するように、第1物質の結晶サイズが数ナノメートルと小さく、かつ第2物質である酸化リンのリン原子数に対する第1物質の酸化チタンのチタン原子数に対する比が1000兆分の1〜0.1の範囲と小さい場合、第1物質を種結晶として第2物質を結晶成長させると第1物質の結晶構造が継承される。以降、(リン原子の数/チタン原子の数)を、リン原子数比と呼ぶ。
【0213】
第1物質の結晶構造が継続されるか、あるいは第2物質の膜厚が単分子層程度と薄膜の場合などでは、n型量子物質の結晶構造は接合面近傍で連続的となり、第1物質のチタン原子が第2物質のリン原子に置換された構造になるものと理解できる。換言すれば、酸化チタン結晶に歪を与えること無く、チタン原子の一部をリン原子に置き換えた物質が実現されることになる。この物質をマクロに捉えると、第1物質の酸化チタン結晶バルク中のチタン原子がリン原子に置き換えられた構造を成し、第2物質のリン原子が酸化チタンの不純物となっていると解釈できる。
【0214】
図30に示したように、5族のリン原子の最外殻軌道には電子が5個存在しているため、図31に示すn型量子触媒の結晶において、リン原子の外殻軌道に結晶構築に関与していない過剰な電子が1個存在することになる。この過剰な電子が酸化チタンの禁止帯中の伝導帯近くにドナー準位を生じる。
【0215】
リン原子は、ゲルマニュウム結晶の不純物として機能するとき、禁止帯中に伝導帯との電位差0.025eVのドナー準位を発生する。酸化チタン結晶の不純物として機能するリン原子は、ゲルマニウム結晶中と同様に、禁止帯中の伝導帯と略0.025eV差のドナー準位を生じるものと想定できる。リン原子の酸化チタンの不純物として機能するドナー準位の厳密な計測は別途に委ねるものとするが、ドナー準位の厳密な値を測定しないことが本発明の主旨を阻害するものでは無く、リン原子が酸化チタンの不純物としてドナー準位を生じ、ドナー準位が生じた結果、n型量子触媒物質の光触媒活性が第1物質の酸化チタン単独の場合に比して改善されることが示されれば十分である。特に、光触媒活性が第1物質単独の場合に比して10倍以上改善される場合、n型量子触媒と呼ぶことにする。
【0216】
第1物質の光触媒活性と本発明に係るn型量子触媒の光触媒活性とを比較する場合、それらの単位重量あたりの光触媒活性を比較する。すなわち、それらの単位重量あたりの反応速度を観る。この比較に使用する光などのエネルギ源については、第1物質が光触媒活性を発現し得る限り特に制限はなく、従来から光触媒の励起に使用し得る紫外線等や可視光の全波長領域について、あるいは赤外線さらには熱源などから発するあらゆる光量子エネルギについて、本発明に係るn型量子触媒の光触媒活性が第1物質単独の場合より大きくなっていることを確認する必要はなく、第1物質単独で光触媒活性を発現する紫外線等の波長範囲を選択した結果、本発明に係るn型量子触媒の光触媒活性が第1物質単独の場合より高くなっていることが確認されれば十分である。紫外線等を照射する場合の反応速度比を比較することは、紫外線照射は第1物質である光触媒単独が最大の光触媒活性を発現する場合であることを意味し、光触媒単独の光触媒活性が最大となる場合を選択していることになる。逆に、遮光環境で反応速度を比較する場合は、遮光環境ではn型量子触媒は光触媒活性を発現できるが、第1物質の光触媒単独は光触媒活性を殆ど発現できないため、遮光環境におけるn型量子触媒の反応速度比は無限大となる。可視光の場合は、紫外線照射と遮光環境の中間的な状態と言える。n型量子触媒の反応速度定比が最小となる紫外線等を照射する場合におけるn型量子触媒の光触媒活性を調べれば、n型量子触媒にとっては厳しい評価であり安全サイドの評価となる。かかる観点から、紫外線等を照射した場合におけるn型量子触媒の光触媒活性を評価することにする。
【0217】
第1物質と第2物質については、第2物質が4族原子酸化物以外という条件を除いて特に制限はない。第2物質は、光触媒活性を有している必要はないが、有していても差し支えない。
【0218】
このような第1物質としては、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質を挙げることができる。
【0219】
また、このような第2物質としては、当該第1物質とは異なる5A族のバナジウム、ニオブ、タンタル、5B族の窒素、リン、ヒ素、アンチモン、ビスマスからなる群から選ばれた物質あるいはその酸化物質を挙げることができる。この中でも。第1物質が酸化チタンであり、第2物質が酸化リンである組合せが、より好ましい。
【0220】
n型量子触媒の励起に必要最低エネルギの略0.025eVに相当する波長は、アインシュタインのエネルギ式(式1)から49,680nm=49.68μmと与えられるように、ほぼ6.03GHzのサブミリ波の電磁波に相当する。さらに、輻射のピーク波長λが温度Tに反比例することを示すウィーンの変位則を用いて、略0.025eVのエネルギを発する黒体の温度を求める。
【0221】
ウィーンの変位則、
【数7】

【0222】
に、アインシュタインのエネルギ式E=hν、ならびに光量子の速度c=hνの関係式を代入すれば、エネルギと温度の関係が次のように求まる。
【数8】

【0223】
続いて、上式に、プランク定数、光速、ならびに電子定数を代入すれば、禁止帯幅 EeVに対応するエネルギは温度T[K]の関係で与えられる。ここに、EJはジュール単位のエネルギを、EeVはeV単位で表現したエネルギ量で、互いに同じエネルギを表す。
【数9】

【0224】
電位差の略0.025eVを上式に代入すれば、第2物質が励起するに必要な温度は58.3°Kとなる。58.3°Kは−215.9℃であり、ほとんど自然界全域で第2物質のリン原子のドナーは励起されていることが知れる。第2物質のリン原子を不純物として含むn型量子触媒は、自然界の略全域において、周辺の熱から十分なエネルギを受け取り励起され、光触媒活性を発現することが示され、自然界の略全域でn型量子触媒が光触媒機能を発現することが明らかになる。
【0225】
室温程度の常温環境ならば略0.025eVのエネルギレベルを有する量子線は常に照射されており、n型量子触媒の不純物であるリン原子は励起されドナーとして機能し、酸化チタンの伝導帯へ電子を供給し、酸化チタンの価電子帯から電子を補足、酸化チタンの価電子帯から電子を補足することで酸化チタンの価電子帯へホールを供給する。
【0226】
略0.025eVのエネルギが照射されるn型量子触媒は、不純物のリン原子のドナー機能で、酸化チタンの伝導帯に自由電子が価電子帯にホールが充足し、n型量子触媒が強い光触媒活性を発現するようになる。
【0227】
図32に示すように、略0.025eV超のエネルギを有する波長49.6μm以下の量子線や赤外線、波長830〜390nmの可視光が照射されると、リン原子はドナーとして機能し、酸化チタンの伝導帯へ自由電子が供給され、さらにドナーは酸化チタンの価電子帯から電子を補足する。酸化チタンの価電子帯から電子を捕捉することは、酸化チタンの価電子帯にホールを供給することを意味する。
【0228】
このリン原子のドナー機能は、略0.025eV以上のエネルギが照射される間継続する。換言すれば、ドナー準位と酸化チタンの伝導帯とのエネルギ差略0.025eVの量子線が照射されると、酸化チタンが等価的に励起され光触媒活性を発現する。
【0229】
この様子を更に詳細に説明すると次のようになる。
【0230】
1.第1物質のバンドギャップ3.2eV超のエネルギを有する波長390nm以下の紫外線等を照射する場合
【0231】
照射光は、第1物質の酸化チタンのバンドギャップ値3.2eV超のエネルギを有し、ドナー励起エネルギ略0.025eVも超えている。したがって、第1物質の酸化チタン自身も、不純物のリン原子のドナーも、共に励起される。
第1物質で励起された自由電子とホールとは、第1物質の結晶から外部に放出され、第1物質近傍に存在する外部の物質を酸化・還元する光触媒作用を発揮する。
第2物質のドナーが励起され、第1物質の伝導帯へ自由電子が注入し、かつ価電子帯へホールが注入することで、第1物質の光触媒活性が増強される。換言すれば、第1物質単独の場合よりn型量子触媒の光触媒活性が増強されることは、リン原子のドナー機能に由来すると理解できる。
【0232】
2.第1物質のバンドギャップ値3.2eV以下で、第2物質のリン素原子のドナー励起エネルギ略0.025eV超の波長49.6μm〜390nmの熱線あるいは可視光などの量子線を照射する場合
【0233】
照射量子線のエネルギは第1物質のバンドギャップ値3.2eVを超えていないため、第1物質の酸化チタンは励起されず、酸化チタン単独では光触媒活性を発現できない。しかし、照射エネルギが第2物質のリン原子のドナー励起エネルギ略0.025eVを超えているため、第2物質のドナーが励起され、電子を第1物質の酸化チタンの伝導帯に注入し、さらに、第1物質の酸化チタンの価電子帯の電子を捕捉することで価電子帯にホールを注入する。
第1物質の酸化チタン単独では略0.025eVの低いエネルギでは励起されないが、第2物質のドナー準位を中継し、電子が酸化チタンの価電子帯から伝導帯へ移動することで、等価的に3.2eV超のエネルギが照射された酸化チタンの励起状態が実現されることになる。
第2物質の酸化リン単独では、第1物質のような強い光触媒活性を有さないが、第2物質のリン原子がドナーとして機能して、第1物質の酸化チタンへ光触媒活性の原動力のホールと自由電子を供給し、光触媒活性を発現する。たとえば、第1物質が酸化チタン、第2物質が酸化リンの場合、酸化リンは酸化チタンのような強い光触媒活性を有していないが、酸化リンのリン原子が量子触媒物質中で励起されドナーとして機能することで、接合面で接触する第1物質の酸化チタンの伝導帯へ自由電子を、価電子帯へホールを注入する。
【0234】
このようにして、第1物質の酸化チタン単独では量子線のような略0.025eVという低いエネルギによって直接的には励起されないが、第2物質のリン原子のドナー機能を介して自由電子とホールとが供給され、供給された自由電子とホールを第1物質の結晶表面から外部に放出することで、第1物質の酸化チタンが光触媒として作用するようになる。この結果、第1物質の酸化チタンのバンドギャップ以下エネルギの量子線しか照射されない遮光環境においても、n型量子触媒は光触媒作用を発現する。
【0235】
次に、本発明に係るn型量子触媒の製造プロセスについて説明する。
【0236】
「実施例11」(n型量子触媒の製造プロセス)
【0237】
本発明に係るn型量子触媒の製造方法において、光触媒活性を発現し得る第1物質と、当該第1物質にドナーを付与する5族原子の酸化物である第2物質とが接合されてなるn型量子触媒を以下に示すプロセスに従い製造する。
【0238】
第1物質の粉末を溶媒に加えて第1物質スラリを作製し、当該第1物質スラリに酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えて混合スラリを作成し、必要に応じ当該スラリに酸および/または塩基を添加して、当該第1物質の表面に第2物質を析出させる。この操作により、第1物質と第2物質とが接合されてなるn型量子触媒スラリが作成される。
【0239】
本発明に係るn型量子触媒の製造方法における第2物質を析出させる際、n型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比あるいは原子数比)を変えることにより、n型量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より高くすることができることが見出された。典型的には後程説明する図35に示すように、n型量子触媒における第1物質に対する前記第2物質をだんだん多くしていくと、n型量子触媒の光触媒活性(光触媒活性を一義的に与える反応速度比)が上昇後下降して、ピークを示すことが見出された。
【0240】
反応速度比が上昇して第2物質が存在しない場合の第1物質の反応速度より高くなるのは、上述の第2物質の不純物のエネルギ準位によるドナー効果と推定される。一旦上昇しその後下降するのは、恐らく、第1物質と第2物質との接合面積、厚さ、接合していない自由表面の面積等が変化し、これにより第2物質の光触媒活性の増強能力が変化するためであろうと考えられる。
【0241】
同様に、分散剤とその濃度、スラリ濃度、スラリ撹拌方法およびスラリ温度などの条件で変化するスラリ中の第1物質粒子径、添加する酸および/または塩基の量、濃度、および添加速度などが、得られたn型量子触媒の光触媒活性に影響を及ぼし、第2物質が存在しない場合の第1物質における光触媒活性をより強くすることができることが見出された。なお、上記において「酸および/または塩基」を添加するとしたのは、酸や塩基で第1物質や第2物質を析出させる場合に、その析出速度を調節する等の目的で、酸や塩基単独ではなく、酸と塩基と混合物を使用する場合もあり得るからである。
【0242】
n型量子触媒における当該第1物質と当該第2物質のモル比としては、n型量子触媒における前記第1物質1モル部に対して、第2物質が1000兆分の1〜0.1モル部にすることが好ましく、第2物質が1兆分の1〜0.01モル部の範囲にあることがより好ましい。
【0243】
酸および/または塩基を使用する場合、添加用溶液中の酸および/または塩基の濃度については、100万分の1〜1mol%の範囲にすることが好ましい。更に、スラリ濃度については、固体物質の濃度が1〜25w%の範囲であることが好ましい。スラリの撹拌方法、およびスラリ温度についても光触媒活性に影響を及ぼし得るので、実情に応じて適宜選択することが好ましい。
【0244】
なお、上記とは逆に、光触媒作用を発現し得る第1物質と、5族原子の酸化物である第2物質とが接合されてなるn型量子触媒の製造方法であって、第2物質の粉末を水などの溶媒でスラリを作製し、当該スラリに酸または塩基による処理により第1物質を析出し得る化合物を含んでなる溶液を加え混合スラリを作成し、当該混合スラリに酸および/または塩基を添加して、当該第2物質の表面に第1物質を析出させn型量子触媒を溶質とするn型量子触媒スラリを作成する。当該析出に際して、n型量子触媒における当該第1物質と当該第2物質の割合(たとえばモル比あるいは原子数比)、当該酸および/または塩基の濃度、当該酸および/または塩基の添加速度、当該スラリの濃度、当該スラリの撹拌方法、当該スラリの温度ならびに分散剤の種類と量からなる群から選ばれた少なくとも一つの条件を選択することにより、n型量子触媒の光触媒活性を、第2物質が存在しない場合の当該第1物質における光触媒活性を高らしめる、n型量子触媒の製造方法でも、同様の効果を得ることができる。
【0245】
本方法に係る発明に使用する第1物質および第2物質については、上記のn型量子触媒に係る発明で説明したと同様に考えることができる。
【0246】
次に、本発明に係るn型量子触媒の製造方法について説明する。
【0247】
「実施例12」(n型量子触媒の製造方法)
【0248】
本発明に使用する「第2物質を析出し得る化合物」や「第1物質を析出し得る化合物」については、本発明の主旨に反しない限りどのような化合物を使用してもよい。水酸化物、酸との塩等を好ましく挙げることができる。たとえば第2物質が酸化リンの場合は酸化リンのアルカリ金属塩であるリン酸ナトリウム(第1リン酸ナトリウム:NaH2PO4、第2リン酸ナトリウム:Na2HPO4、第3リン酸ナトリウム:Na3PO4)、リン酸カルシウム等を例示することができ、第1物質が酸化チタンの場合はチタン酸ナトリウム等を例示することができる。
【0249】
これらの化合物を溶解するための溶媒は通常水であるが、それ以外のもの、たとえばエタノール等であってもよい。第2物質や第1物質の析出を調整するために複数の溶媒からなる混合溶媒を使用することが有用な場合もあり得る。
【0250】
本発明に係る「第1物質の粒子」や「第2物質の粒子」についてもそのサイズや形状に特に制限があるわけではないが、一般的には、1次粒子径がナノオーダー(たとえば1〜100nm)の粒子であることが好ましい。
【0251】
本発明における酸や塩基についても、第1物質や第2物質を析出し得るものであればどのようなものでもよい。酸としては塩酸や硫酸、硝酸を、塩基としては苛性ソーダ等のアルカリ化合物を好ましく例示できる。アルカリ土類金属化合物も使用できる。
【0252】
本発明に係るn型量子触媒の製造に関して、第1物質として酸化チタンを使用し、第2物質として5族リンの酸化物である酸化リンを使用する場合の製造方法を、図33に示す。
【0253】
酸化チタンスラリ作成の工程1において、1次粒子径7nm程度の酸化チタン粒子を、分散剤を適宜加えた水溶媒に加え撹拌して酸化チタンスラリを作製する。次いで混合スラリ作成の工程2において、工程1で作成した酸化チタンスラリに酸化リンのアルカリ金属塩水溶液を加え撹拌して混合スラリを作製する。さらに次いで、イオン交換の工程3において、工程2で作製した混合スラリに塩酸を滴下しながら撹拌してイオン交換して酸化リンを酸化チタン微粒子の表面に析出させ、酸化チタンと酸化リンとが接合したn型量子触媒を溶質とするn型量子触媒スラリを作成する。
【0254】
第2物質の酸化リンのアルカリ金属塩として、酸化リンと水酸化ナトリウムとからなる第2リン酸ナトリウムNa2HPO4を用いた。酸化リンと水酸化カリウム等のリン酸アルカリ金属塩等の場合も同様である。また、工程1で作成する酸化チタンスラリは弱酸性を呈し、工程2で加える酸化リン金属塩溶液のアルカリ成分が工程1の酸性成分より多くない場合には、工程2で加える酸化リンアルカリ金属塩溶液を加え撹拌するとき、酸化チタンスラリの酸性成分によりイオン交換され第2物質の酸化リンが第1物質の酸化チタン粒子表面に析出するので、工程3を実行することは必ずしも無く、n型量子触媒スラリを製造することができる。
【0255】
次に、本発明に係るn型量子触媒の第2物質析出に用いる塩酸量について説明する。
【0256】
「実施例13」(n型量子触媒の第2物質析出)
【0257】
n型量子触媒の主要製造プロセスの工程1において酸化チタンスラリを作成、同工程2において酸化チタンスラリに酸化リンアルカリ塩溶液を加え撹拌し混合スラリを作成、同工程3において混合スラリに酸/アルカリを加え第2物質を酸化チタン表面に析出させたn型量子触媒スラリを作成する。
【0258】
酸化チタン粒子は水等の溶媒中では強い凝集力を生じるので、超音波を照射し超臨界場を発生させ、超臨界場でジルコニアビーズ撹拌することが好ましい。超音波は、19kH以上が好ましい。超音波照射量は、溶質1gあたり0.01W〜100Wが好ましい。0.01〜2mm径ジルコニアビーズでビーズ撹拌することが好ましい。酸化チタンスラリ中の酸化チタン濃度は0.1〜35w%が好ましい。酸化チタンスラリを1〜35℃に保ちNS撹拌することが好ましい。
【0259】
酸化リンのアルカリ塩として第2リン酸ナトリウム(Na2HPO4)を例示できる。
【0260】
たとえば水を溶媒とする場合、酸化チタン1モル部に対する酸化リン1000兆分の1〜0.1モル部が好ましく、酸化チタン1モル部に対する酸化リン1兆分の1〜0.01モル部がより好ましい。第2リン酸ナトリウム(Na2HPO4)1分子には、ナトリウム(Na)が2分子、水素が1原子、酸化リン(PO3)が1分子すなわちリン原子(P)が1原子含まれているので、n型量子触媒の酸化チタン1モル部に対する酸化リンのモル部の比の値は、リン原子数と酸化チタンのチタン原子数との比に一致する。以降、比 (リン原子の数/チタン原子の数)を、リン原子数比と呼ぶ。
すなわち、混合スラリ中のリン原子数比が1000兆分の1〜0.1が好ましく、リン原子数比が1兆分の1〜0.01がより好ましい。
【0261】
チタン金属の酸化物である酸化チタンの水スラリは弱酸性を呈し、第2リン酸ナトリウム(Na2HPO4)は弱アルカリ性を呈するので、混合スラリの作成にあたり、第2リン酸ナトリウム(Na2HPO4)溶液をゆっくり滴下することが好ましい。混合スラリ作成にあたり、酸化チタンスラリを10℃に保ちNS撹拌しながら第2リン酸ナトリウム(Na2HPO4)溶液をゆっくり滴下することが、より好ましい。
【0262】
第2リン酸ナトリウム(Na2HPO4)溶液のアルカリ成分が、酸化チタンスラリの酸性成分に比べ、少ない場合は、図33工程3の塩酸を滴下してイオン交換する必要は必ずしも無い。
【0263】
リン原子数比100万分の1(1ppm)のn型量子触媒スラリの具体例を示す。
【0264】
混合スラリを工程3においてイオン交換するに当たり、滴下塩酸量のn型量子触媒の反応速度比に及ぼす影響を調べた。図34は、イオン交換に使用した塩酸使用率(100%、50%、0%)をパラメータとして、反応速度比の時間経過特性を示す。
【0265】
例えば、第2リン酸ナトリウム(Na2HPO4)1モル部を含む混合スラリには、ナトリウムが2モル部含まれることになる。当該混合スラリのナトリウム全量を塩酸でイオン交換する場合には、2モル部の塩酸が必要になる。ナトリウムに対する塩酸のモル割合を塩酸使用率と定義しているので、2モル部の塩酸を使用してイオン交換する場合は塩酸使用率100%、半量の1モル部の塩酸を用いる場合は塩酸使用率50%、塩酸を全く使用しない場合は塩酸使用率0%となる。
【0266】
リン原子数比1ppmの混合スラリを塩酸使用率100%、50%および0%としてイオン交換して、3種のn型量子触媒5Gn−1m/1,5Gn−1m/0.5,5Gn−1m/0を作成した。
【0267】
作成したn型量子触媒スラリをシャーレに採り室温乾燥させたサンプルを作成し、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を20回測定し、残留濃度から反応速度比を、また残留ガス濃度の平均から平均反応速度比を求めた。求めたn型量子触媒の反応速度比と平均反応速度比を、塩酸使用率をパラメータに採り、図34に示す。図34の横軸は、観測ポイントを表し、縦軸は反応速度比を表す。観測ポイント間隔は、略24時間であった。
【0268】
図34の実曲線は、n型量子触媒5Gn-1m/1の特性を示す。名称「5Gn-1m/1」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/1」は塩酸使用率が100%であることを示す。
【0269】
図34の実曲線上のドットはn型量子触媒5Gn-1m/1の反応速度比を、データラベルは反応速度比の値を示す。
【0270】
5Gn-1m/1の反応速度比は、第1〜20観測ポイントで、順に2.74、2.97、2.97、2.74、2.74、3.27、3.47、2.68、2.97、2.74、2.62、2.43、2.68、3.03、3.03、3.10、3.34、3.10、3.34、2.81であり、最大2.97と最小2.43の間で変動していた。
【0271】
20観測ポイントの残留濃度比の平均値に対する反応速度定比を平均反応速度比とした。同34図の実線はn型量子触媒5Gn-1m/1の平均反応速度比5Gn-1m/1 Aveを示し、その値は2.90であった。
【0272】
図34の破曲線は、n型量子触媒5Gn-1m/0.5の特性を示す。名称「5Gn−1p/05」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/0.5」は塩酸使用率が50%であることを示す。破曲線上のドットはn型量子触媒5Gn-1m/0.5の反応速度比、データラベルは反応速度定比の値を示す。
【0273】
5Gn-1m/0.5の反応速度比は、第1〜第20観測ポイントで、順に3.03、2.74、3.03、3.64、3.03、3.03、3.47、3.27、3.03、2.43、2.37、2.30、2.74、2.68、2.74、3.34、2.74、2.74、2.43、3.03であり、最大3.64と最小2.30の間で変動していた。同34図の破線は、n型量子触媒5Gn-1m/0.5の平均反応速度比5Gn-1m/0.5 Aveを示し、その値は2.84であった。
【0274】
図34の1点鎖曲線は、n型量子触媒5Gn-1m/0の特性を示す。名称「5Gn−1p/05」は、リン原子数比が1ppm、すなわち100万分の1のn型量子触媒であることを、名称末尾の「/0」は塩酸使用率が0%であることを示す。同34図1点鎖曲線上のドットはn型量子触媒5Gn-1m/0の反応速度比、データラベルは反応速度定比の値を示す。
【0275】
5Gn-1m/0の反応速度比は、第1〜20観測ポイントで、順に3.47、2.74、2.74、3.03、3.80、3.03、2.74、2.68、2.74、2.37、2.43、2.43、2.74、2.74、2.74、2.74、2.81、2.74、3.47、3.47であり、最大3.80と最小2.37の間で変動していた。同34図の1点鎖線は、n型量子触媒5Gn-1m/0の平均反応速度比5Gn-1m/0 Aveを示し、その値は2.82であった。
【0276】
塩酸使用率を100%、50%、0%のn型量子触媒5Gn-1m/1、5Gn-1m/0.5、5Gn-1m/0の平均反応速度比は、それぞれ、2.90、2.83、2.82であり、塩酸使用率50%と0%では大きな差異は認められなかったが、塩酸使用率100%が最大の平均反応速度定比を与えることが知れた。
【0277】
n型量子触媒5Gn-1m/1の反応速度比の最大、平均、最小値はそれぞれ3.47、2.90、2.43であり、光触媒活性が第1物質の酸化チタン単独の場合の最大8万7千倍強、平均6千3百倍強、最小724倍であることが知れた。n型量子触媒5Gn-1m/1の光触媒活性は、第1物質の酸化チタン単独の10倍以上であることを保障することが判明した。
【0278】
次に、本発明に係るn型量子触媒のリン原子数比に対する反応速度定比特性について説明する。
【0279】
「実施例14」(n型量子触媒のリン原子数比特性)
【0280】
n型量子触媒または第1物質単独(酸化チタンST−01)の各10mgを、5Lのテドラーバッグに入れ、80〜100重量ppm濃度に調整した標準ガス(窒素キャリアガス、アセトアルデヒド標準ガス)を3L注入し、照射強度1.0mW/平方cmの紫外線を照射し、20分経過後の残留濃度をガス検知管(ガステック社製 No.92M)で測定し、残留濃度と初発濃度との比(残留濃度比)を求め、n型量子触媒の反応速度と酸化チタンの反応速度の比[p型量子触媒の反応速度/酸化チタンの反応速度]を、反応速度定比とした。
【0281】
n型量子触媒の反応速度比を図35に示す。
【0282】
n型量子触媒としての量は一定10mgであった。紫外線光源として、東芝ライテック社製ブラックライトFL40SBL2本点灯し、コニカ・ミノルタ社製UV RadioMeterUM−10、受光部同社製UM−360を用いて照射面にて紫外線強度を測定した。
【0283】
同一重量を用いて同一環境で残留濃度を測定する場合、測定対象のn型量子触媒に含まれる第1物質である酸化チタン量は、第1物質以外の物質の重量分だけ少なくなる。また、第1物質以外の物質である酸化リンは、光触媒活性をほとんど発現しないことが知られている。このような条件で、n型量子触媒の光触媒活性が第1物質の光触媒活性を上回ること、すなわち、n型量子触媒の反応速度比が1を上回ることは、これまで知られていなかった。これは、前述のごとく、第2物質の酸化リンのリン原子が酸化チタンの不純物として酸化チタンのバンドギャップにドナー準位を生じ、略0.025eV以上のエネルギを吸収したリン原子のドナーが酸化チタンへ自由電子とホールを注入するようになり、酸化チタンの表面から自由電子とホールが放出さるようになる結果、酸化チタン単体の光触媒活性を上回る光触媒活性を実現したものと考えられる。
【0284】
リン原子数比が、100ppt(=100億分の1)、1ppb(=10億分の1)、10ppb(=1億分の1)、100ppb(=1000万分の1)、1ppm(=100万分の1)、10ppm(=10万分の1)、100ppm=(1万分の1)、1000ppm(=0.001)、ならびに1%(=0.01)の場合について、第13の形態のn型量子触媒の製造プロセスに示した手順に従い、n型量子触媒5Gn―100t/1、5Gn―1b/1、5Gn―10b/1、5Gn―100b/1、5Gn―1m/1、5Gn―10m/1、5Gn―100m/1、5Gn―1000m/1、および5Gn―1%/1を作成した。
【0285】
これらn型量子触媒の名称は、上記と同様であり、例えば名称「5Gn―100t/1」の「5Gn―100t」は、リン原子数比が100pptすなわち100億分の1であるn型量子触媒であることを、「/1」は塩酸使用率が100%であることを示す。
【0286】
図33工程1における酸化チタンスラリ濃度を、工程1の水成分と分散剤と工程2で印加するリン酸ナトリウム溶液と第3工程で滴下する塩酸溶液に含まれる水成分を勘案し、重量濃度が10w%となるように調整、NS撹拌を150mpm、分散剤Demol EP量を酸化チタン重量の0.4%とした。
【0287】
図33工程2における酸化ホウ素アルカリ金属溶液量が酸化チタンスラリ容量の3%となるように濃度を調整、NS撹拌を50mpm実施した。
【0288】
第3工程の希塩酸量を酸化チタンスラリ容量の0.5%になるように濃度を調整、NS撹拌を25mpm実施した。
【0289】
図35に、作成したn型量子触媒5Gn―100t/1、5Gn―1b/1、5Gn―10b/1、5Gn―100b/1、5Gn―1m/1、5Gn―10m/1、5Gn―100m/1、5Gn―1000m/1、および5Gn―1%/1のリン原子数比に対する反応速度比特性を示す。図34の横軸はリン原子数比を示し、単位pptは1兆分の1、ppbは10億分の1、ppmは100万分の1、%は0.01を表す。
【0290】
作成した濃度10w%のn型量子触媒スラリ100mgをシャーレに採り室温乾燥させたn型量子触媒10mgを用いて、ガスパックA法に準拠してアセトアルデヒドガスの残留濃度を、24時間の間隔を置き30回測定した。30回計測した残留濃度の算術平均から求めた反応速度定比を平均反応速度比5Gn/1-Aveとした。平均反応速度定比を、図35の実曲線で示す。実曲線5Gn/1-Aveにおける、ドットの横位置はリン原子数比を、ドットの縦位置は平均反応速度比を、ドットのデータラベルは平均反応速度比の値を表す。
【0291】
同図35の1点鎖曲線5Gn/1−worstは、最小反応速度比を示す。30回計測した残留濃度比の最大値に対する反応速度比を最小反応速度比とした。1点鎖曲線5Gn/1−worst上のドットの横位置はリン原子数比を、縦位置は最小反応速度比を示し、データラベルは最小反応速度比の値を表す。
【0292】
同図35の破曲線5Gn/1−bestは、最大反応速度比を示す。30回計測した残留濃度比の最小値に対する反応速度比を最大反応速度比とした。破曲線5Gn/1−best上のドットの横位置はリン原子数比を、縦位置は最小反応速度比を示し、データラベルは最小反応速度比の値を表す。
【0293】
繰り返し30回計測して計測上の擾乱要因を除去するように努め、リン原子数比100ppt〜1%に関するn型量子触媒5Gn−100t/1〜5Gn−1%/1の反応速度比の信頼度を高めた。
【0294】
図35の平均反応速度比5Gn/1−ave、最大反応速度比5Gn/1−best、ならびに最小反応速度比5Gn/1−worstが示すように、リン原子数比が変化すると、反応速度比すなわち光触媒活性が敏感に変化することを示すことが見出された。
【0295】
具体的には、図35の平均反応速度比5Gn/1−aveに示すように、リン原子数比に対するn型量子触媒の平均反応速度比は、100pptの場合2.53、1ppbの場合2.58、10ppbの場合2.68、100ppbの場合3.29、1ppmの場合3.34、10ppmの場合3.18、100ppmの場合2.96、1000ppmの場合2.91、1%の場合1.20であった。n型量子触媒のリン原子数比が100ppb〜10ppm前後で平均反応速度比の値は3.18〜3.34と最大になった。最大の平均反応速度定比3.34のn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の光触媒活性の4万7千8百倍であることが判明した。
【0296】
また、図35に示すようにリン原子数比が1兆分の1〜1%の領域における平均反応速度定比の値は1以上であり、全域においてn型量子触媒の光触媒活性が第1物質の酸化チタン単独の場合の光触媒活性を上回ることが明らかになった。
【0297】
図35の最大反応速度比5Gn/1−bestに示すように、n型量子触媒のリン原子数比に対する最大反応速度比は、100pptの場合3.55、1ppbの場合3.56、10ppbの場合3.88、100ppbの場合5.38、1ppmの時場合4.72、10ppmの場合4.27、100ppmの場合3.88、1000ppmの場合3.71、1%の場合1.35であった。
【0298】
リン原子数比が100ppbの最大反応速度比は5.38であった。最大反応速度定比5.38のn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の5億7千5百万倍強であった。
【0299】
図35の最小反応速度比5Gn/1−worstに示すように、n型量子触媒のリン原子数比に対する最小反応速度比は、100pptの場合1.81、1ppbの時場合1.94、10ppbの場合2.09、100ppbの場合2.32、1ppmの場合2.71、10ppmの場合2.68、100ppmの場合2.37、1000ppmの場合2.24、1%の場合1.00であった。
【0300】
n型量子触媒中のリン原子数比が100pptの場合、最小反応速度比が最小の1.81となった。最小反応速度定比1.81は光触媒活性42倍を意味し、リン原子数比100ppt〜1000ppmの領域におけるn型量子触媒の光触媒活性は、第1物質の酸化チタン単独の42倍以上あり、本発明で開示するn型量子触媒は10倍以上の光触媒活性を最悪の場合でも保障することが明らかになった。
【0301】
また、リン原子数比が1ppmのn型量子触媒は、最大値反応速度定比が4.72、平均反応速度定比が3.34、最小反応速度定比が2.71であり、第1物質の酸化チタン単独の光触媒活性を最大2754万倍強、平均4万7千8百倍強、最小2千6百倍強で、平均反応速度定比が最大値となることが知れた。
【0302】
図36〜図44に、リン原子数比が100ppt〜1%の作成したn型量子触媒スラリ粒径の散乱強度分布と累積を示す。
【0303】
図36にn型量子触媒5Gn−100t/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100t/1スラリは、594.5nmに散乱強度ピークを有し、平均粒径は297.1nmであった。
【0304】
図37にn型量子触媒5Gn−1b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1b/1スラリは、458.0nmに散乱強度ピークを有し、平均粒径は244.7nmであった。
【0305】
図38にn型量子触媒5Gn−10b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−10b/1スラリは、888.3nmに第1、3万8924.4nmに第2散乱強度ピークを有し、平均粒径は3273.5nmであった。
【0306】
図39にn型量子触媒5Gn−100b/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100b/1スラリは、593.1nmに散乱強度ピークを有し、平均粒径は298.7nmであった。
【0307】
図40にn型量子触媒5Gn−1m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1m/1スラリは、569.4nmに散乱強度ピークを有し、平均粒径は301.1nmであった。
【0308】
図41にn型量子触媒5Gn−10m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−10m/1スラリは、714.9nmに第1、7657.6nmに第2散乱強度ピークを有し、平均粒径は1430.1nmであった。
【0309】
図42にn型量子触媒5Gn−100m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−100m/1スラリは、431.9nmに散乱強度ピークを有し、平均粒径は233.6nmであった。
【0310】
図43にn型量子触媒5Gn−1000m/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1000m/1スラリは、299.2nmに散乱強度ピークを有し、平均粒径は165.7nmであった。
【0311】
図44にn型量子触媒5Gn−1%/1スラリ粒径の散乱強度分布と累積を示す。n型量子触媒5Gn−1%/1スラリは、1083.7nmに散乱強度ピークを有し、平均粒径は1463.8nmであった。
【0312】
n型量子触媒に含まれる第1物質と第2物質の割合については特に制限はないが、n型量子触媒におけるリン原子数比をだんだん大きくしていくと、n型量子触媒の光触媒活性、言い換えれば反応速度比が上昇後下降し次第に反応速度比が1を下回るか、あるいは反応速度比が1以上で上昇下降を繰り返したのち反応速度比が1を下回り、ピークを示すことが見出されており、ある範囲内にあることが好ましいと言えよう。一般的に言えば、n型量子触媒におけるリン原子数比が1000兆分の1〜1の範囲にすることが好ましく、1兆分の1〜0.01の範囲にすることがより好ましい。以下、光触媒活性が、第1物質単独の場合に比べ高くなるメカニズムについて説明する。ただし、以下の説明は本発明の理解を助けるためのものであり、本発明の範囲を制限するものではない。
【0313】
図31に示したように、接合面近傍では酸化チタンの酸素原子と酸化リンのリン原子が電子を共有しており、チタン原子とリン原子が酸素原子を挟み互いに接合されているものと想定される。換言すれば、接合面の酸化チタンにリン原子が直接接合されている構造が実現され、第2物質の酸化リンの励起に必要なエネルギは、酸化リン分子の励起に必要なエネルギより低く、リン原子の励起エネルギに等しくなる。
【0314】
チタン原子とリン原子が酸素原子を挟み互いに接合され、接合面の酸化チタンにリン原子が直接接合されていると見做すことができ、第2物質の酸化リンのリン原子が、酸化チタンの結晶構造を乱すことなく、不純物となっていることになる。リン原子が酸化チタンの不純物となった結果、酸化チタンの禁止帯にドナー準位が生じる。
【0315】
第2物質の酸化リンのリン原子の励起エネルギを略0.025eVと単純に記述するのは、上記机上実験結果に基づくものであるが、この机上実験結果が将来詳細に測定され得られるドナー準位の値と異なっていても、本特許の主旨を阻害するものでは無く、リン不純物によりドナー準位が生じた結果、n型量子触媒の光触媒活性が第1物質単独の光触媒活性を上回っていることが示されば十分である。
【0316】
次に、本発明に係る量子触媒の紛体化について説明する。
【0317】
「実施例15」(量子触媒の紛体化)
【0318】
p型及び/あるいはn型量子触媒の紛体は、図9及び/あるいは図33の工程4〜6に従い乾燥粉砕して製造する。図9及び/あるいは図33の工程4で、p型及び/あるいはn型量子触媒スラリを適切な方法、例えば加熱してp型及び/あるいはn型量子触媒スラリの凝集を加速し、図9及び/あるいは図33の工程5で凝集したp型及び/あるいはn型量子触媒スラリを冷却した後フィルタープレス等で脱水しプレスケーキを作成し、図9及び/あるいは図33の工程6で当該プレスケーキを乾燥粉砕しp型及び/あるいはn型量子触媒を紛体化する。
【産業上の利用可能性】
【0319】
このようにして、本発明は、第1物質の結晶構造を乱すこと無く第4と第8族を除く第1〜3族または第5〜7族原子あるいはその酸化物からなる第2物質を不純物として含む新しい物質である量子触媒を作成する方法、さらに、第2物質の不純物が第1物質の禁止帯に準電位を生じしめる結果、第1物質単独の場合に比して光触媒活性を10倍以上に改善することを明らかにした。
【0320】
本発で開示した量子触媒は、第1物質の光触媒単独では光触媒活性を発現できない環境でも光触媒活性を発現することを示した。量子触媒は、紫外線のみならず、量子線、赤外線、可視光などの低エネルギレベルの量子線の照射時においても光触媒活性を発現する。
【0321】
本発明に係る量子触媒からどのような光触媒作用を発揮させるかについては特に制限はない。使用された第1物質の場合と同様の光触媒活性が適切である場合が多い。一般的には、有害物質や臭い発生物質の分解作用や色素増感型太陽電池における光電変換作用を好ましく挙げることができる。また、製造の簡便さと安定性ならびに経済性を満たす新しい太陽電池および癌治療を特に好ましく挙げることができる。この新しい太陽電池は、p型量子触媒を正極材、n型量子触媒を負極剤として使用する。さらに、酸化チタンと酸化リン及び/あるいは酸化ホウ素とからなる量子触媒は、人体内部の癌細胞や癌病巣を分解除去する新しい治療を可能とする。
【0322】
本発明に係る量子触媒に照射する光や量子線などのエネルギについても特に制限はない。使用された第1物質が光触媒活性を発現する場合と同様の紫外線等を使用することが適切である場合が多いが、それより長波長側でもよいことは上述の通りである。授受されるエネルギが第2物質の原子が不純物として励起するに足るならば、赤外線、可視光、あるいは紫外線等の照射は必ずしも必要ない。電子が動けない絶対零度のような環境を除けば、室温程度で十分な熱エネルギの照射を受けているので、夜間や遮光環境においても、第2物質の不純物は励起し、第1物質の伝導帯へ自由電子を、第1物質の価電子帯へホールを供給する。不純物から供給される自由電子とホールが充分な量に達すれば、光触媒作用が発現するのは前記の通りである。エネルギにより電子が励起される確率は、ドナー準位と伝導帯電位あるいはアクセプタ準位と価電子帯電位との電位差で定まる励起エネルギレベルが小さい程、指数関数的に大きくなり、本発明が開示する量子触媒が室温程度の温度で効果的に光触媒作用を発揮するようになり、夜間においても発電可能な上記の新しい太陽電池の実現できる。さらに、可視光や紫外線の照射を不要とする量子触媒の特徴は、人体内部の略遮光環境における光触媒活性を利用した安全な治療法を提供できる。
【特許請求の範囲】
【請求項1】
光触媒活性を発現し得る第1物質と、当該第1物質とは異なる4族以外の原子あるいは当該原子の酸化である第2物質とが互いに接合されてなり、前記第1物質1モル部に対し前記第2物質が1000兆分の1〜1モル部の範囲にある、第1物質単独である場合に比べ光触媒活性が10倍以上に高められた量子触媒。
【請求項2】
前記第1物質が、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質であり、前記第2物質が、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウム、5族(5A族)のバナジウム、ニオブ、タンタル、5族(5B族)の窒素、リン、ヒ素、アンチモン、ビスマスからなる群から選ばれた物質あるいはその酸化物質である、請求項1に記載の量子触媒。
【請求項3】
前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素である、請求項1に記載の量子触媒。
【請求項4】
前記第1物質が酸化チタンであり、前記第2物質が酸化リンである、請求項1に記載の量子触媒。
【請求項5】
前記第1物質と、前記第2物質とが接合されてなる量子触媒の製造方法であって、
分散剤を加えた溶媒に第1物質の微粒子を分散した第1物質スラリを作製し、
酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を当該第1物質スラリに加え混合スラリを作成、あるいは、分散剤と酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えた溶媒に第1物質の微粒子を分散した混合スラリを作製して、必用に応じ当該混合スラリに酸および/または塩基を添加して当該第1物質の微粒子表面に第2物質を析出させた量子触媒スラリを得るに際して、
当該第1物質と分散剤との割合、当該第1物質の粒径、
当該第1物質スラリおよび/または混合スラリの濃度、
当該第1物質スラリおよび/または混合スラリの温度、
当該第1物質スラリおよび/または混合スラリの撹拌時に照射する超音波の周波数と照射強度、
当該第1物質スラリのよび/または混合スラリの撹拌時に使用するビーズ径、当該酸および/または塩基の添加量、
当該酸および/または塩基の濃度、
および当該量子触媒スラリにおける当該第1物質と当該第2物質の割合からなる群から選ばれた少なくとも一つの条件を選択することにより、
当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、量子触媒の製造方法。
【請求項6】
前記第1物質と分散剤との割合が0.1〜10重量%にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項7】
前記第1物質の微粒子の粒径が1nm〜100nmの範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の製造方法。
【請求項8】
前記第1物質スラリおよび/または混合スラリの濃度を0.1〜35重量%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項9】
前記第1物質スラリおよび/または混合スラリの温度を1〜35℃の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項10】
前記第1物質スラリおよび/または混合スラリ作成に当たり、周波数19KHz以上の超音波を、第1物質1g当たり0.1Wh〜100Whの強度で照射して攪拌することにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項11】
前記第1物質スラリおよび/または混合スラリ作成に当たり、径0.01〜2mmのビーズを使用して攪拌することにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項12】
前記酸および/または塩基の量を、酸および/または塩基単独で第2物質を析出するに要する量の0〜200%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項13】
前記混合スラリに添加する酸および/または塩基の溶液量を、第1物質スラリ容積の0.1〜10%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項14】
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項1】
光触媒活性を発現し得る第1物質と、当該第1物質とは異なる4族以外の原子あるいは当該原子の酸化である第2物質とが互いに接合されてなり、前記第1物質1モル部に対し前記第2物質が1000兆分の1〜1モル部の範囲にある、第1物質単独である場合に比べ光触媒活性が10倍以上に高められた量子触媒。
【請求項2】
前記第1物質が、炭化珪素、ガリウム燐、ガリウム砒素、酸化ジルコニウム、酸化タンタル、硫化カドニウム、カドミウムセレン、酸化チタン、酸化亜鉛、酸化ニオブ、酸化タングステン、リン酸銀、酸化ケイ素、酸化ゲルマニウム、酸化ストロンチウム、硫化モリブデン、酸化インジウム、酸化ビスマス、酸化スズ、酸化バリウム、酸化ルテニウム、および酸化ハフニウムなどからなる群から選ばれた物質であり、前記第2物質が、当該第1物質とは異なる3族(3A族)のスカンジウム、イットリウム、ランタノイド(ランタン、セリウム、プラセオジム、ネオジム、サマリウム、ユウロビウム、ガドリウム、テルビウム、ジスプロウム、モルミウム、エルビウム、ツリウム、イッテリビウム、ルテチウム)、アクチノイド(アクチニウム、トリウム、プロトアクチニウム、ウラン)、3族(3B族)のホウ素、アルミニウム、ガリウム、インジウム、タリウム、5族(5A族)のバナジウム、ニオブ、タンタル、5族(5B族)の窒素、リン、ヒ素、アンチモン、ビスマスからなる群から選ばれた物質あるいはその酸化物質である、請求項1に記載の量子触媒。
【請求項3】
前記第1物質が酸化チタンであり、前記第2物質が酸化ホウ素である、請求項1に記載の量子触媒。
【請求項4】
前記第1物質が酸化チタンであり、前記第2物質が酸化リンである、請求項1に記載の量子触媒。
【請求項5】
前記第1物質と、前記第2物質とが接合されてなる量子触媒の製造方法であって、
分散剤を加えた溶媒に第1物質の微粒子を分散した第1物質スラリを作製し、
酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を当該第1物質スラリに加え混合スラリを作成、あるいは、分散剤と酸または塩基による処理により第2物質を析出し得る化合物を含んでなる溶液を加えた溶媒に第1物質の微粒子を分散した混合スラリを作製して、必用に応じ当該混合スラリに酸および/または塩基を添加して当該第1物質の微粒子表面に第2物質を析出させた量子触媒スラリを得るに際して、
当該第1物質と分散剤との割合、当該第1物質の粒径、
当該第1物質スラリおよび/または混合スラリの濃度、
当該第1物質スラリおよび/または混合スラリの温度、
当該第1物質スラリおよび/または混合スラリの撹拌時に照射する超音波の周波数と照射強度、
当該第1物質スラリのよび/または混合スラリの撹拌時に使用するビーズ径、当該酸および/または塩基の添加量、
当該酸および/または塩基の濃度、
および当該量子触媒スラリにおける当該第1物質と当該第2物質の割合からなる群から選ばれた少なくとも一つの条件を選択することにより、
当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、量子触媒の製造方法。
【請求項6】
前記第1物質と分散剤との割合が0.1〜10重量%にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項7】
前記第1物質の微粒子の粒径が1nm〜100nmの範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の製造方法。
【請求項8】
前記第1物質スラリおよび/または混合スラリの濃度を0.1〜35重量%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項9】
前記第1物質スラリおよび/または混合スラリの温度を1〜35℃の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項10】
前記第1物質スラリおよび/または混合スラリ作成に当たり、周波数19KHz以上の超音波を、第1物質1g当たり0.1Wh〜100Whの強度で照射して攪拌することにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項11】
前記第1物質スラリおよび/または混合スラリ作成に当たり、径0.01〜2mmのビーズを使用して攪拌することにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項12】
前記酸および/または塩基の量を、酸および/または塩基単独で第2物質を析出するに要する量の0〜200%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項13】
前記混合スラリに添加する酸および/または塩基の溶液量を、第1物質スラリ容積の0.1〜10%の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【請求項14】
前記第1物質1モル部に対し、前記第2物質が1000兆分の1〜1モル部の範囲にすることにより、当該量子触媒の光触媒活性を、当該第1物質単独における光触媒活性より10倍以上高くする、請求項5に記載の量子触媒の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【図30】


【図31】


【図32】


【図33】


【図34】


【図35】


【図36】


【図37】


【図38】


【図39】


【図40】


【図41】


【図42】


【図43】


【図44】


【公開番号】特開2013−39522(P2013−39522A)
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願番号】特願2011−177434(P2011−177434)
【出願日】平成23年8月15日(2011.8.15)
【出願人】(593210189)
【Fターム(参考)】
【公開日】平成25年2月28日(2013.2.28)
【国際特許分類】
【出願日】平成23年8月15日(2011.8.15)
【出願人】(593210189)

【Fターム(参考)】
[ Back to top ]

