金属イオン捕捉剤、金属イオンの捕捉方法
【課題】 金属イオンを速やかに捕捉できる金属イオン捕捉剤、及び金属イオンを速やかに捕捉可能な金属イオン捕捉方法を提供すること、特に、多くの金属イオンを速やかに捕捉でき、且つ各種形状に成形可能である金属イオン捕捉剤を提供すること。
【解決手段】 直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤、及び金属イオンを含有する溶液と、金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることを特徴とする金属イオンの捕捉方法。
【解決手段】 直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤、及び金属イオンを含有する溶液と、金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることを特徴とする金属イオンの捕捉方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、金属イオンを捕捉する捕捉剤、及び該捕捉剤を用いた金属イオンの捕捉方法に関する。
【背景技術】
【0002】
金属イオンの分離、除去、回収は環境浄化、環境保護の視点から、産業問題の枠を越えた全社会的な課題として、ますます重視されている。従って、効率的な金属イオン捕捉剤または捕捉方法についての技術開発においては、従来の有機系ポリマー、例えばイオン交換樹脂系より、多くの優位性、例えば、速いイオン交換速度、高いイオン選択性、高いイオン交換率、簡易なイオン回収性、耐熱性、環境適切性などを有する新しい材料系に転換されて行く傾向がある。
【0003】
こうした金属イオンの捕捉剤として近年注目されているのがシリカ(珪素)系の捕捉剤である。珪素は地殻上で酸素に次ぐ第二番目を誇る豊富な存在であり、自然界の石英、水晶、オパール、雲母、石綿などはよく知られている珪素の酸化物である。規則的な空間構造やパターン構造を有するシリカ系材料は様々な機能系材料、例えば、分離、精製、または触媒担持体用の材料として極めて有望であり、この機能または効能が従来のポリマー樹脂系より優れていることから、これに関する技術開発がこの数年大きく進歩している。
【0004】
シリカ系金属イオン捕捉剤としては、主にメソポーラスシリカが使用されている。シリカ中にメソポーラス空洞構造を発現させるための方法としては、分子組織体、例えば、低分子または高分子系の会合体をテンプレートとして用い、その会合体周辺でシリカソースであるアルコキシシランのゾルゲル反応を行うことで、シリカゲルが与えられる。このシリカゲルを高温で焼結し、内部の有機テンプレートを除去することにより、シリカ中空洞が残る。テンプレートとしては、界面活性剤(非特許文献1参照)、ブロックポリマー(非特許文献2参照)、ウイルス、バクテリア(非特許文献3参照)などが使用されている。テンプレートの種類により、得られるシリカ中の空洞が2〜20nm程度の範囲で変化し、かつその空洞は平行したチャンネルとして規則的に配列される。このようなことから、メソポーラスシリカ材料は、触媒、電子材料、ナノフィルター、クロマトグラフィー、分離、バイオ工学などの分野で多くの関心を集めている。
【0005】
しかし、メソポーラスシリカを金属イオン捕捉剤として用いるには、そのシリカ空洞表面に、アミン、チオールなどの金属イオンに配位能力を有する官能基を導入しなければならない(非特許文献4〜6参照)。メソポーラスシリカは球状の形に作製することができるが、多くの場合、これらのシリカは形状が制御されてない粉末または塊である。従って、金属イオン捕捉のプロセスからいえば、メソポーラスシリカ中の空洞中に金属イオンが入り込み、さらに該金属イオンが空洞内部のアミン、チオールなどの官能基に安定して配位されるには、金属イオンの拡散、配位など全プロセスにおける長い時間を要するものであった。また、メソポーラスシリカ中に固定化できる官能基の数にも制限があり、多量の金属イオンを捕捉する場合にはシリカ量を多くする必要があった。
【0006】
【非特許文献1】C.T.Kresge et al.,Nature,(1992),359,p.710
【非特許文献2】A.Monnier et al.,Science,(1993),261,p1299
【非特許文献3】S.A.Davis et al.,Nature,(1997),385,p420
【非特許文献4】T. Kang et al., J. Mater. Chem. (2004) 14, p1043
【非特許文献5】B. Lee et al., Langmuir, (2003) 19, p4246
【非特許文献6】K. Zakir et al., Adv. Mater. (2002) 14, p1053)
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明が解決しようとする課題は、金属イオンを速やかに捕捉できる金属イオン捕捉剤、及び金属イオンを速やかに捕捉可能な金属イオン捕捉方法を提供すること、特に、多くの金属イオンを速やかに捕捉でき、且つ各種形状に成形可能である金属イオン捕捉剤を提供することにある。
【課題を解決するための手段】
【0008】
本発明においては、金属イオンに高い配位能力を有する直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さがナノメートルオーダーの繊維状複合体を会合させ、全体のネットワークを形成させた捕捉剤が、スポンジのようにその内部に微少な空間と、大きな表面積を確保できるため、多くの金属イオンを速やかに捕捉することができる。さらに、太さがナノメートルオーダーの繊維状複合体の会合体からなるものであるため任意の形状への成形が可能である。
【0009】
すなわち、本発明は直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤を提供することにある。
【0010】
さらに本発明は、金属イオンを含有する溶液と、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記遷移金属捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることからなる金属の捕捉方法、及び金属イオン捕捉剤に捕捉された金属イオンを酸性処理により金属捕捉剤から分離する方法を提供することにある。
【発明の効果】
【0011】
本発明の金属イオン捕捉剤は、ナノメートルオーダーの繊維状複合体が会合した三次元網目構造、即ち、シリカスポンジ構造を有する。従って、そのスポンジ内部は繊維状複合体と空隙で構成され、かつ内部の繊維状複合体の表面積が非常に大きい。このため、本発明の金属イオン捕捉剤は金属イオン水溶液と接触させた際、金属イオンがシリカの全表面と接触することができ、多くの金属イオンを速やかに捕捉することが可能となる。更に、本発明の金属イオン捕捉剤は、成形が容易であることから、カラム状や板状への加工により、ナノフィルター形式の金属イオン捕捉剤として用いることができる。
【0012】
また、本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマーは、溶液のpHの変化より、プロトン化されたカチオン状態、または脱プロトンのアミン状態に変化できる。このため、本発明の金属イオン捕捉剤は、金属イオンを選択的に捕捉することが可能である。
【0013】
さらに、本発明の金属イオン捕捉剤においては、シリカの有する耐酸性、耐酸化性、耐有機溶剤性に優れ、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーは該繊維状複合体から溶出されることがない。従って、金属と配位する活性部が繊維状複合体中に安定に固定化された状態を保持できる。
【0014】
また、本発明のポリマー結晶とシリカからなる捕捉剤の形成において、その結晶フィラメント中に機能性物質、例えば、蛍光物質など機能性化合物を含有させることが可能であり、含有させた機能性物質に由来する機能を発現させることもできる。
【0015】
また、本発明の金属イオン捕捉剤を使用した捕捉方法によると、多くの金属イオンを速やかに捕捉でき、さらに、シリカ繊維中に捕捉された金属イオンを酸性水溶液で洗浄することにより、その金属を容易に回収できる。
【発明を実施するための最良の形態】
【0016】
本発明の捕捉剤は、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さがナノメートルオーダーの範囲にある繊維状複合体同士が会合してなるものである。
【0017】
[直鎖状ポリエチレンイミン骨格を有するポリマー]
本発明でいう直鎖状ポリエチレンイミン骨格とは、二級アミンのエチレンイミン単位を主たる構造単位とするポリマー骨格をいう。該骨格中においては、エチレンイミン単位以外の構造単位が存在していてもよいが、ポリマー結晶を形成させるためには、ポリマー鎖の一定鎖長が連続的なエチレンイミン単位であることが好ましい。該直鎖状ポリエチレンイミン骨格の長さは、該骨格を有するポリマーが結晶を形成できる範囲であれば特に制限されないが、好適にポリマー結晶を形成するためには、該骨格部分のエチレンイミン単位の繰り返し単位数が10以上であることが好ましく、20〜10000の範囲であることが特に好ましい。
【0018】
本発明において使用するポリマーは、その構造中に直鎖状ポリエチレンイミン骨格を有するものであればよく、その形状が線状、星状または櫛状であっても、水中または水と水溶性有機溶媒混合の水性媒体中で結晶体を与えることができる。
【0019】
また、これら線状、星状または櫛状のポリマーは、直鎖状ポリエチレンイミン骨格のみからなるものであっても、直鎖状ポリエチレンイミン骨格からなるブロック(以下、ポリエチレンイミンブロックと略記する。)と他のポリマーブロックとのブロックコポリマーからなるものであってもよい。他のポリマーブロックとしては、例えば、ポリエチレングリコール、ポリプロピオニルエチレンイミン、ポリアクリルアミドなどの水溶性のポリマーブロック、あるいは、ポリスチレン、ポリオキサゾリン類のポリフェニルオキサゾリン、ポリオクチルオキサゾリン、ポリドデシルオキサゾリン、ポリアクリレート類のポリメチルメタクリレート、ポリブチルメタクリレートなどの疎水性のポリマーブロックを使用できる。これら他のポリマーブロックとのブロックコポリマーとすることで、ポリマー結晶の形状や特性を調整することができる。
【0020】
直鎖状ポリエチレンイミン骨格を有するポリマーが、ブロックコポリマーである場合の該ポリマー中における直鎖状ポリエチレンイミン骨格の割合は、ポリマー結晶を形成できる範囲であれば特に制限されないが、好適にポリマー結晶を形成するためには、ポリマー中の直鎖状ポリエチレンイミン骨格の割合が40モル%以上であることが好ましく、50モル%以上であることがさらに好ましい。
【0021】
上記直鎖状ポリエチレンイミン骨格を有するポリマーは、その前駆体となるポリオキサゾリン類からなる直鎖状の骨格を有するポリマー(以下、前駆体ポリマーと略記する。)を、酸性条件下またはアルカリ条件下で加水分解することで容易に得ることができる。従って、直鎖状ポリエチレンイミン骨格を有するポリマーの線状、星状、または櫛状などの形状は、この前駆体ポリマーの形状を制御することで容易に設計することができる。また、重合度や末端構造も、前駆体ポリマーの重合度や末端機能団を制御することで容易に調整できる。さらに、直鎖状ポリエチレンイミン骨格を有するブロックコポリマーを形成する場合には、前駆体ポリマーをブロックコポリマーとし、該前駆体中のポリオキサゾリン類からなる直鎖状の骨格を選択的に加水分解することで得ることができる。
【0022】
前駆体ポリマーは、オキサゾリン類のモノマーを使用して、カチオン型の重合法、あるいは、マクロモノマー法などの合成方法により合成が可能であり、合成方法や開始剤を適宜選択することにより、線状、星状、あるいは櫛状などの各種形状の前駆体ポリマーを合成できる。
【0023】
ポリオキサゾリン類からなる直鎖状の骨格を形成するモノマーとしては、メチルオキサゾリン、エチルオキサゾリン、メチルビニルオキサゾリン、フェニルオキサゾリンなどのオキサゾリンモノマーを使用できる。
【0024】
重合開始剤としては、分子中に塩化アルキル基、臭化アルキル基、ヨウ化アルキル基、トルエンスルホニルオキシ基、あるいはトリフルオロメチルスルホニルオキシ基などの官能基を有する化合物を使用できる。これら重合開始剤は、多くのアルコール類化合物の水酸基を他の官能基に変換させることで得られる。なかでも、官能基変換として、臭素化、ヨウ素化、トルエンスルホン酸化、およびトリフルオロメチルスルホン酸化されたものは重合開始効率が高いため好ましく、特に臭化アルキル、トルエンスルホン酸アルキルが好ましい。
【0025】
また、ポリ(エチレングリコール)の末端水酸基を臭素あるいはヨウ素に変換したもの、またはトルエンスルホニル基に変換したものを重合開始剤として使用することもできる。その場合、ポリ(エチレングリコール)の重合度は5〜100の範囲であることが好ましく、10〜50の範囲であれば特に好ましい。
【0026】
また、カチオン開環リビング重合開始能を有する官能基を有し、かつ光による発光機能、エネルギー移動機能、電子移動機能を有するポルフィリン骨格、フタロシアニン骨格、またはピレン骨格のいずれかの骨格を有する色素類は、得られるポリマーに特殊な機能を付与することができる。
【0027】
線状の前駆体ポリマーは、上記オキサゾリンモノマーを1価または2価の官能基を有する重合開始剤により重合することで得られる。このような重合開始剤としては、例えば、塩化メチルベンゼン、臭化メチルベンゼン、ヨウ化メチルベンゼン、トルエンスルホン酸メチルベンゼン、トリフルオロメチルスルホン酸メチルベンゼン、臭化メタン、ヨウ化メタン、トルエンスルホン酸メタンまたはトルエンスルホン酸無水物、トリフルオロメチルスルホン酸無水物、5−(4−ブロモメチルフェニル)−10,15,20−トリ(フェニル)ポルフィリン、またはブロモメチルピレンなどの1価のもの、ジブロモメチルベンゼン、ジヨウ化メチルベンゼン、ジブロモメチルビフェニレン、またはジブロモメチルアゾベンゼンなどの2価のものが挙げられる。また、ポリ(メチルオキサゾリン)、ポリ(エチルオキサゾリン)、または、ポリ(メチルビニルオキサゾリン)などの工業的に使用されている線状のポリオキサゾリンを、そのまま前駆体ポリマーとして使用することもできる。
【0028】
星状の前駆体ポリマーは、上記したようなオキサゾリンモノマーを3価以上の官能基を有する重合開始剤により重合することで得られる。3価以上の重合開始剤としては、例えば、トリブロモメチルベンゼン、などの3価のもの、テトラブロモメチルベンゼン、テトラ(4−クロロメチルフェニル)ポルフィリン、テトラブロモエトキシフタロシアニンなどの4価のもの、ヘキサブロモメチルベンゼン、テトラ(3,5−ジトシリルエチルオキシフェニル)ポルフィリンなどの5価以上のものが挙げられる。
【0029】
櫛状の前駆体ポリマーを得るためには、多価の重合開始基を有する線状のポリマーを用いて、該重合開始基からオキサゾリンモノマーを重合させることができるが、例えば、通常のエポキシ樹脂やポリビニルアルコールなどの側鎖に水酸基を有するポリマーの水酸基を、臭素やヨウ素等でハロゲン化するか、あるいはトルエンスルホニル基に変換させた後、該変換部分を重合開始基として用いることでも得ることができる。
【0030】
また、櫛状の前駆体ポリマーを得る方法として、ポリアミン型重合停止剤を用いることもできる。例えば、一価の重合開始剤を用い、オキサゾリンを重合させ、そのポリオキサゾリンの末端をポリエチレンイミン、ポリビニルアミン、ポリプロピルアミンなどのポリアミンのアミノ基に結合させることで、櫛状のポリオキサゾリンを得ることができる。
【0031】
上記により得られる前駆体ポリマーのポリオキサゾリン類からなる直鎖状の骨格の加水分解は、酸性条件下またはアルカリ条件下のいずれの条件下でもよい。酸性条件下での加水分解は、例えば、塩酸水溶液中でポリオキサゾリンを加熱下で攪拌することにより、ポリエチレンイミンの塩酸塩を得ることができる。得られた塩酸塩を過剰のアンモニウム水で処理することで、塩基性のポリエチレンイミンの結晶粉末を得ることができる。用いる塩酸水溶液は、濃塩酸でも、1mol/L程度の水溶液でもよいが、加水分解を効率的に行うには、5mol/Lの塩酸水溶液を用いることが望ましい。また、反応温度は80℃前後が望ましい。
【0032】
アルカリ条件下での加水分解は、例えば、水酸化ナトリウム水溶液を用いることで、ポリオキサゾリンをポリエチレンイミンに変換させることができる。アルカリ条件下で反応させた後、反応液を透析膜にて洗浄することで、過剰な水酸化ナトリウムを除去し、ポリエチレンイミンの結晶粉末を得ることができる。用いる水酸化ナトリウムの濃度は1〜10mol/Lの範囲であればよく、より効率的な反応を行うには3〜5mol/Lの範囲であることが好ましい。また、反応温度は80℃前後が好ましい。
【0033】
酸性条件下またはアルカリ条件下での加水分解における、酸またはアルカリの使用量は、ポリマー中のオキサゾリン単位に対し、1〜10当量でよく、反応効率の向上と後処理の簡便化のためには、3当量程度とすることが好ましい。
【0034】
上記加水分解により、前駆体ポリマー中のポリオキサゾリン類からなる直鎖状の骨格が、直鎖状ポリエチレンイミン骨格となり、該ポリエチレンイミン骨格を有するポリマーが得られる。
【0035】
また、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーを形成する場合には、前駆体ポリマーをポリオキサゾリン類からなる直鎖状のポリマーブロックと、他のポリマーブロックとからなるブロックコポリマーとし、該前駆体ポリマー中のポリオキサゾリン類からなる直鎖状のブロックを選択的に加水分解することで得ることができる。
【0036】
他のポリマーブロックが、ポリ(N−プロピオニルエチレンイミン)などの水溶性ポリマーブロックである場合には、ポリ(N−プロピオニルエチレンイミン)が、ポリ(N−ホルミルエチレンイミン)やポリ(N−アセチルエチレンイミン)に比べて、有機溶媒への溶解性が高いことを利用してブロックコポリマーを形成することができる。即ち、2−オキサゾリンまたは2−メチル−2−オキサゾリンを、前記した重合開始化合物の存在下でカチオン開環リビング重合した後、得られたリビングポリマーに、さらに2−エチル−2−オキサゾリンを重合させることによって、ポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとからなる前駆体ポリマーを得る。該前駆体ポリマーを水に溶解させ、該水溶液にポリ(N−プロピオニルエチレンイミン)ブロックを溶解する水とは非相溶の有機溶媒を混合して攪拌することによりエマルジョンを形成する。該エマルジョンの水相に、酸またはアルカリを添加することによりポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックを優先的に加水分解させることにより、直鎖状ポリエチレンイミンブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとを有するブロックコポリマーを形成できる。
【0037】
ここで使用する重合開始化合物の価数が1および2の場合には、直鎖状のブロックコポリマーとなり、それ以上の価数であれば星型のブロックコポリマーが得られる。また、前駆体ポリマーを多段のブロックコポリマーとすることで、得られるポリマーも多段のブロック構造とすることも可能である。
【0038】
[ポリマー結晶]
上記ポリエチレンイミン骨格を有するポリマーは、一次構造中の直鎖状ポリエチレンイミン骨格が、水又は水と親水性溶媒の混合溶液中で結晶性を発現してポリマー結晶を形成する。該ポリマー結晶は、水の存在下でのポリマー結晶同士の物理的な結合により三次元網目構造を有するヒドロゲルを形成することもでき、さらにポリマー結晶同士を架橋剤で架橋することにより化学的な架橋結合を有する架橋ヒドロゲルを形成することもできる。
【0039】
従来広く使用されてきたポリエチレンイミンは、環状エチレンイミンの開環重合により得られる分岐状ポリマーであり、その一次構造には一級アミン、二級アミン、三級アミンが存在する。従って、分岐状ポリエチレンイミンは水溶性であるが、結晶性は持たないため、分岐状ポリエチレンイミンを用いてヒドロゲルを作るためには、架橋剤による共有結合により網目構造を与えなくてはならない。しかしながら本発明に使用するポリマーが骨格として有する直鎖状ポリエチレンイミンは、二級アミンだけで構成されており、該二級アミン型の直鎖状ポリエチレンイミンは水溶性でありながら、優れた結晶性を有する。
【0040】
このような、直鎖状ポリエチレンイミンの結晶は、そのポリマーのエチレンイミン単位に含まれる結晶水数により、ポリマー結晶構造が大きく異なることが知られている(Y.Chatani et al.、Macromolecules、1981年、第14巻、p.315−321)。無水のポリエチレンイミンは二重螺旋構造を特徴とする結晶構造を優先するが、モノマー単位に2分子の水が含まれると、ポリマーはzigzag構造を特徴とする結晶体に成長することが知られている。実際、水中から得られる直鎖状ポリエチレンイミンの結晶は一つのモノマー単位に2分子水を含む結晶であり、その結晶は室温状態では水中不溶である。
【0041】
本発明における直鎖状ポリエチレンイミン骨格を有するポリマーの結晶は、上記の場合と同様に直鎖状ポリエチレンイミン骨格の結晶発現により形成されるものであり、ポリマー形状が線状、星状、または櫛状などの形状であっても、一次構造に直鎖状ポリエチレンイミン骨格を有するポリマーであれば、ポリマーの結晶が得られる。
【0042】
本発明におけるポリマー結晶の存在はX線散乱により確認でき、広角X線回折計(WAXS)における2θ角度値で20°,27°,28°近傍の結晶性ヒドロゲル中の直鎖状ポリエチレンイミン骨格に由来するピーク値により確認される。
【0043】
また、本発明におけるポリマー結晶の示差走査熱量計(DSC)における融点は、ポリエチレンイミン骨格のポリマーの一次構造にも依存するが、概ねその融点が45〜90℃で現れる。
【0044】
本発明におけるポリマー結晶は、その結晶を構成するポリマー構造の幾何学的な形状や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー結晶の形成条件などの影響により各種形状を取り得ることができ、例えば繊維状、ブラシ状、星状などの形状を有する。
【0045】
上記ポリマー結晶は、5〜30nm程度のナノメートルオーダーの繊維状ポリマー結晶(以下、該結晶を繊維状ナノ結晶と略記する。)を基礎とするものであり、該繊維状ナノ結晶表面に存在するフリーなエチレンイミン鎖により、繊維状ナノ結晶同士が水素結合による物理的な結合で繋がれて空間に配置され、上記したような三次元形状に成長する。これらポリマー結晶間が、さらに物理的に結合し、該ポリマー結晶の三次元網目構造を作り上げる。これらは水の存在下で生じるため、結果的には該三次元網目構造中に水を包含したヒドロゲルが与えられる。
【0046】
ここでいう三次元網目構造とは、通常の高分子ヒドロゲルと異なり、マイクロ、またはナノスケールの結晶同士が、その結晶表面に存在するフリーなエチレンイミン鎖の水素結合により、物理的に架橋化された網目構造を言う。従って、その結晶の融点以上の温度では、結晶が水中溶解されてしまい、三次元網目構造も解体される。ところが、それが室温に戻ると、ポリマー結晶が成長し、その結晶間では水素結合による物理的な架橋が形成するため、再び、三次元網目構造が現れる。
【0047】
本発明のポリマー結晶は、直鎖状ポリエチレンイミン骨格を有するポリマーが室温の水に不溶である性質を利用し、該直鎖状ポリエチレンイミン骨格を有するポリマーの水中での溶解−結晶変換により得ることができる。
【0048】
また、ヒドロゲルは、まず直鎖状ポリエチレンイミン骨格を有するポリマーを一定量水中に分散し、該分散液を加熱することにより、ポリエチレンイミン骨格を有するポリマーの透明な水溶液を得る。次いで、加熱状態のポリマーの水溶液を室温に冷やすことにより得られる。該ヒドロゲルは、剪断力等の外力により変形を生じるが、概ねの形状を保持できるアイスクリームのような状態を有し、多様な形状に変形させることが可能である。
【0049】
上記ポリマー分散液の加熱温度は100℃以下が好ましく、90〜95℃の範囲であることがより好ましい。また、ポリマー分散液中のポリマー含有量は、ヒドロゲルが得られる範囲であれば特に限定されないが、0.01〜20質量%の範囲であることが好ましく、安定形状の結晶体からなるヒドロゲルを得るためには0.1〜10質量%の範囲がさらに好ましい。このように、本発明においては、直鎖状ポリエチレンイミン骨格を有するポリマーを使用すると、ごく少量のポリマー濃度でもヒドロゲルを形成することができる。
【0050】
上記ポリマー水溶液の温度を室温まで低下させる過程により、得られるヒドロゲル中の結晶形状を調整することができる。例えば、ポリマー水溶液を80℃に1時間保持した後、1時間かけて60℃にし、該温度でさらに1時間保持する。その後1時間かけて40℃まで低下させた後、自然に室温まで下げることで、水溶液の水が流動性をなくした状態のヒドロゲル結晶体を得ることができる。また、上記ポリマー水溶液を一気に氷点の氷り水、または氷点下のメタノール/ドライアイス、あるいはアセトン/ドライアイスの冷媒液にて冷却させた後、その状態のものを室温のワータバスにて保持させることでヒドロゲル結晶体を得ることができる。さらには、上記のポリマー水溶液を室温のワータバスまたは室温空気環境にて、室温まで温度を低下させることで、ヒドロゲル結晶体を得ることができる。
【0051】
上記ポリマー水溶液の温度を低下させる工程は、得られるヒドロゲル中のポリマー結晶の形状に強く影響を与えるため、上記異なる工程により得られるヒドロゲル中のポリマーの結晶形態は同一ではない。
【0052】
上記のポリマー水溶液の温度を、濃度を一定として多段階的に低下させた場合、ヒドロゲル中におけるポリマーの結晶形態を、ファイバー状のポリマー結晶形態とすることができる。これを急冷した後、室温に戻した場合には、花弁状のポリマー結晶形態とすることができ。また、これをドライアイス上のアセトンで再度急冷して、室温に戻した場合、波状のポリマー結晶形態とすることができる。このように、本発明のヒドロゲル中におけるポリマーの結晶形態を、各種形状に設定することができる。
【0053】
上記により得られるヒドロゲルは、不透明なゲルであり、ゲル中にはポリエチレンイミン骨格を有するポリマーの結晶が形成し、その結晶体同士の水素結合により物理的に架橋化され、三次元の物理的な網目構造を形成している。一旦形成したヒドロゲル中のポリマー結晶は室温中では不溶状態を保つが、加熱するとポリマー結晶が解離し、ヒドロゲルはゾル状態に変化してしまう。従って、本発明の物理的なヒドロゲルは、熱処理を行うことでゾルからゲル、またゲルからゾルへと可逆的な変化が可能である。
【0054】
本発明でいうヒドロゲルは三次元網目構造中に少なくとも水を含有するが、該ヒドロゲルの調製時に、水溶性有機溶剤を加えることで、有機溶剤を含有したヒドロゲルが得られる。該親水性有機溶剤としては、例えば、メタノール、エタノール、テトラヒドロフラン、アセトン、ジメチルアセトアミド、ジメチルスルフォンオキシド、ジオキシラン、ピロリドンなどの水溶性有機溶剤を取りあげることができる。
【0055】
有機溶剤の含有量は、水の体積に対し、0.1〜5倍の範囲であることが好ましく、1〜3倍の範囲であればより好ましい。
【0056】
上記親水性有機溶媒を含有させることにより、ポリマー結晶の形態を変えることができ、単純な水系と異なる形態の結晶を与えることができる。例えば、水中では繊維状の広がりを有する分岐結晶形態であっても、その調製に一定量のエタノールが含まれた場合、繊維が収縮したような球状結晶形態を得ることができる。
【0057】
本発明でいうヒドロゲル調製時に、他の水溶性ポリマーを加えることで、水溶性ポリマーを含有するヒドロゲルが得られる。該水溶性ポリマーとしては、例えば、ポリエチレングリコール、ポリビニルアルコール、ポリビニルピロリドン、ポリアクリルアミド、ポリ(N−イソプロピルアクリルアミド)、ポリヒドロキシエチルアクリレート、ポリメチルオキサゾリン、ポリエチルオキサゾリンなどを取りあげることができる。
【0058】
水溶性ポリマーの含有量は、直鎖状ポリエチレンイミン骨格を有するポリマーの質量に対し、0.1〜5倍の範囲であることが好ましく、0.5〜2倍の範囲であればより好ましい。
【0059】
上記水溶性ポリマーを含有させることによっても、ポリマー結晶の形態を変えることができ、単純な水系と異なる形態の結晶を与えることができる。また、ヒドロゲルの粘性を増大させ、ヒドロゲルの安定性を向上させることに有効である。
【0060】
上記方法で得られたヒドロゲルを、ポリエチレンイミンのアミノ基と反応する2官能基以上を含む化合物で処理することで、ヒドロゲル中のポリマー結晶表面同士を化学結合でリンクさせた架橋ヒドロゲルを得ることができる。
【0061】
前記アミノ基と室温状態で反応できる2官能基以上を含む化合物としては、アルデヒド類架橋剤、エポキシ類架橋剤、酸クロリド類、酸無水物、エステル類架橋剤を用いることができる。アルデヒド類架橋剤としては、例えば、マロニルアルデヒド、スクシニルアルデヒド、グルタリルアルデヒド、アジホイルアルデヒド、フタロイルアルデヒド、イソフタロイルアルデヒド、テレフタロイルアルデヒドなどがあげられる。また、エポキシ類架橋剤としては、例えば、ポリエチレングリコールジグリシジルエーテル、ビスフェノールAジグリシジルエーテル、グリシジルクロライド、グリシジルブロマイドなどがあげられる。酸クロリド類としては、例えば、マロニル酸クロリド、スクシニル酸クロリド、グルタリル酸クロリド、アジホイル酸クロリド、フタロイル酸クロリド、イソフタロイル酸クロリド、テレフタロイル酸クロリドなどがあげられる。また、酸無水物としては、例えば、フタル酸無水物、スクシニル酸無水物、グルタリル酸無水物などがあげられる。また、エステル類架橋剤としては、マロニル酸メチルエステル、スクシニル酸メチルエステル、グルタリル酸メチルエステル、フタロイル酸メチルエステル、ポリエチレングリコールカルボン酸メチルエステルなどがあげられる。
【0062】
架橋反応は、得られたヒドロゲルを架橋剤の溶液に浸す方法にでも、架橋剤溶液をヒドロゲル中に加える方法でも可能である。この際、架橋剤は系内での浸透圧変化と共に、ヒドロゲル内部へ浸透し、そこで結晶体同士を水素結合で繋いでエチレンイミンの窒素原子との化学反応を引き起こす。
【0063】
架橋反応は、ポリエチレンイミン結晶体表面のフリーなエチレンイミンとの反応により進行するが、その反応を結晶内部では起こらないようにするためには、ヒドロゲルを形成する結晶体の融点以下の温度で反応を行うことが望ましく、さらには架橋反応を室温で行うことが最も望ましい。
【0064】
架橋反応を室温で進行させる場合には、ヒドロゲルを架橋剤溶液と混合した状態で放置しておくことで、架橋ヒドロゲルを得ることができる。架橋反応させる時間は、数分から数日でよく、概ね一晩放置することで好適に架橋が進行する。
【0065】
架橋剤量はヒドロゲル形成に用いるポリエチレンイミン骨格を有するポリマー中のエチレンイミンユニットのモル数に対し、0.05〜20%であればよく、それが1〜10%であればもっと好適である。
【0066】
上記ヒドロゲルは、ゲル化剤が結晶性のポリマーであるため多様なモルフォロジーのゲル構造を発現できる。また少量のポリマー結晶であっても水中で好適に三次元網目構造を形成するため高い水保持性を有する。さらに、使用する直鎖状ポリエチレンイミン骨格を有するポリマーは構造設計や合成が容易であり、かつヒドロゲルの調整が簡便である。また、該ヒドロゲル中のポリマー結晶間を架橋剤により架橋することにより、ヒドロゲルの形状を固定化できる。
【0067】
[繊維状複合体、繊維状複合体の会合]
本発明の金属イオン捕捉剤は、上記のポリマー結晶の水中分散液またはポリマー結晶のヒドロゲル中に、通常のゾルゲル反応において使用できる溶媒にシリカソースを溶解した溶液を加えて、室温下でゾルゲル反応させることにより容易に得ることができる。
【0068】
ポリマー結晶表面には不可避的に結晶に関わりがないフリーなポリエチレンイミンの鎖が多数存在し、これらフリーな鎖は結晶表面でブラシのように存在する。これらのブラシのような鎖はシリカソースを引き寄せる足場であり、同時にシリカソースを重合させる触媒の働きをする。これにより、直鎖状ポリエチレンイミン骨格を有するポリマーの繊維状ナノ結晶表面でゾルゲル反応が進行し、該繊維状ナノ結晶表面がシリカで被覆され、結果的には、結繊維状ナノ結晶がシリカ被覆された繊維状複合体が相互に会合した状態の金属イオン捕捉剤が得られる。
【0069】
シリカソースとして用いる化合物としては、テトラアルコキシシラン類、アルキルトリアルコキシシラン類などが挙げられる。
【0070】
テトラアルコキシシラン類としては、例えば、テトラメトキシシラン、テトラエトキシシラン、テトラプロポキシシラン、テトラブトキシシラン、テトラ−t−ブトキシシランなどを挙げられる。
【0071】
アルキルトリアルコキシシラン類としては、メチルトリメトキシラン、メチルトリエトキシラン、エチルトリメトキシラン、エチルトリエトキシシラン、n−プロピルトリメトキシラン、n−プロピルトリエトキシラン、iso−プロピルトリメトキシシラン、iso−プロピルトリエトキシシラン、3−クロロプロピルトリメトキシシラン、3−クロロプロピルトリエトキシシラン、ビニルトリメトキシシラン、ビニルトリエトキシシラン、3−グリシトキシプロピルトリメトキシシラン、3−グリシトキシプロピルトリエトキシシラン、3−アミノプロピルトリメトキシシラン、3−アミノプロピルトリエトキシラン、3−メルカプトプロピルトメトキシシラン、3−メルカプトトリエトキシシラン、3,3,3−トリフロロプロピルトリメトシシラン、3,3,3−トリフロロプロピルトリエトシシラン、3−メタクリルオキシプロピルトリメトキシシラン、3−メタクリルオキシプロピルトリエトキシシラン、フェニルトリメトキシシラン、フェニルトリエトキシラン、p−クロロメチルフェニルトリメトキシラン、p−クロロメチルフェニルトリエトキシシラン、ジメチルジメトキシシラン、ジメチルジエトキシシラン、ジエチルジメトキシシラン、ジエチルジエトキシシアンなどを挙げられる。
【0072】
本発明の金属イオン捕捉剤を与える上記ゾルゲル反応は、水、あるいは水と親水性有機溶媒の混合溶液などの水性液体中、ポリマー結晶の存在下で進行するが、その反応は水性液体相では起こらず、結晶体の表面で進行する。従って、複合化反応条件ではポリマー結晶が溶解することがなければ、反応条件は任意である。
【0073】
ポリマー結晶を不溶とするためには、ゾルゲル反応の際、親水性有機溶媒を含む水性液体中、水の存在が20%以上とすることが好ましく、それが40%以上であればさらに好ましい。
【0074】
ゾルゲル反応においては、ポリエチレンイミンのモノマー単位であるエチレンイミンに対し、シリカソースであるアルコキシシランの量を過剰とすれば好適に捕捉剤を形成できる。過剰の度合いとしては、エチレンイミンに対し4〜1000倍等量の範囲であることが好ましい。
【0075】
また、ポリマー結晶を形成する際の水、水性液体中のポリマー濃度はそのポリマー中に含まれるポリエチレンイミンの量を基準に、0.1〜30%にすることが好ましい。
【0076】
ゾルゲル反応の時間は1分から数日まで様々であるが、アルコキシシランの反応活性が高いメトキシシラン類の場合は、反応時間は1分〜24時間でよく、反応効率を上げることから、反応時間を30分〜5時間に設定すればさらに好適である。また、反応活性が低い、エトキシシラン類、ブトキシシラン類の場合は、ゾルゲル反応時間が24時間以上が好ましく、その時間を一週間程度とすることも望ましい。
【0077】
本発明の金属イオン捕捉剤は、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの繊維状複合体(以下、単に繊維状複合体と略記する。)の会合と空間配置から形成された三次元網目形状を有する。該金属イオン捕捉剤の三次元網目構造は、太さがナノメートルオーダーの繊維状複合体を基本ユニットとし、該基本ユニットが相互に会合して三次元網目構造を形成したものである。該金属イオン捕捉剤の内部では、基本ユニットとなる繊維状複合体が、繊維状ナノ結晶が形成したマイクロメートルオーダーの二次的な形状を転写して、微細な会合形状を有している場合が多く、該微細な会合形状の会合体がさらに会合して全体として三次元網目構造を有する金属イオン捕捉剤が形成される。
【0078】
繊維状複合体が形成するマイクロメートルオーダーの二次的な形状は、上記したようにポリマー構造の幾何学的な形状や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー結晶の形成条件等により調整でき、レタス状、ファイバー状、スポンジ状、アスター状、サボテン状、タンポポ状など様々な形状に調整できる。これら形状は、使用するポリマーの分子構造、重合度、組成、及びポリマー結晶調製時の温度低下の方法によく依存する。
【0079】
また、本発明の金属イオン捕捉剤は、形状を任意に制御できるヒドロゲルの形状をシリカにより固定化できるため、任意の形状に成形することが可能である。この場合には、ポリマー結晶間が化学結合で架橋された架橋ヒドロゲルを用いると、成形が容易となるため好ましい。該金属イオン捕捉剤の形状や大きさは、ヒドロゲル調製時に用いた容器の大きさ及び形状と同一なものにすることができ、例えば、円盤状、円柱状、プレート状、球状などの任意の形状に調製できる。さらに、架橋させたヒドロゲルを切断したり、削ったりすることにより、目的の形に成形することもできる。このように成形したヒドロゲルをシリカソースの溶液と浸漬等により接触させることにより、ポリマー結晶とシリカからなる成形体が簡単に得られる。シリカソースの溶液に浸漬する時間としては、使用するシランソースの種類により1時間〜1週間と様々であるため適宜調製する必要があるが、メトキシシラン類の溶液中では1〜48時間程度であればよく、エトキシシラン類の溶液中では、1〜7日間程度が好適である。
【0080】
通常、本発明の捕捉剤はポリマー結晶とシリカとから構成され、捕捉剤中のシリカの含有量は、反応条件などにより一定の幅で変化するが、捕捉剤全体の30〜90質量%の範囲のものを得ることができる。なかでもシリカ含有量が捕捉剤全体の40〜80質量%のものが好ましく使用できる。
【0081】
シリカの含有量はゾルゲル反応の際用いたポリエチレンイミンポリマーの量、すなわちヒドロゲル中のポリマー濃度が増えることにつれて増える。また、ゾルゲル反応時間を長くする事により増大する。
【0082】
本発明の金属イオン捕捉剤は、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーに蛍光性物質を組み込むことができる。例えば、酸性基を有するポルフィリンとポリエチレンイミンを混合した後、ゾルゲル反応をすることで、ポルフィリンの残基が金属イオン捕捉剤中に取り込まれる。また、例えば、直鎖状ポリエチレンイミン骨格を有するポリマーの側鎖に少量のピレン類、例えば、ピレンアルデヒド(好ましくは、イミンに対し10モル%以下)を反応させたポリマー結晶を用いることで、ピレン残基を金属イオン捕捉剤に取り込むことができる。さらに、直鎖状ポリエチレンイミン骨格を有するポリマーの塩基に酸性基、例えば、カルボン酸基、スルホン酸基を有するポルフィリン類、フタロシアニン類、ピレン類など蛍光性染料を(好ましくは、イミンのモル数に対し0.1モル%以下)少量混合させ、その結晶体をテンプレートとした金属イオン捕捉剤中には、これらの蛍光性物質を取り込むことができる。
【0083】
本発明の金属イオン捕捉剤の窒素原子の含有量は、金属イオン捕捉剤を調製するとき、ヒドロゲル中の直鎖状ポリエチレンイミン骨格を有するポリマー濃度を変えることで変えることができる。濃度が高くなると、得られたシリカ捕捉剤中の窒素原子の含有量は増大する。通常、窒素原子の含有量は1〜15質量%の範囲にすることができる。本発明の金属イオン捕捉剤中の窒素原子は、金属イオンに高い配位能力を有する部分であり、該窒素原子の含有量に応じて本発明の金属イオン捕捉剤が捕捉できる金属イオンの量を調製でき、該窒素原子の含有量が多い程、捕捉できる金属イオンの量が多くなる。本発明の金属捕捉剤が捕捉できる金属イオンの捕捉量としては、最大、金属イオン捕捉剤中の窒素原子4モルに対し、金属イオン1モルの捕捉が可能である。
【0084】
本発明の金属イオン捕捉剤は、ナノメートルオーダーの繊維状複合体が会合した三次元網目構造を有することから、その内部には空隙が多く、かつ繊維状複合体の表面積が非常に大きい。このため、本発明の金属イオン捕捉剤は金属イオン水溶液と接触させた際、金属イオンがシリカの全表面と接触することができ、多くの金属イオンを速やかに捕捉することが可能となる。更に、本発明の金属イオン捕捉剤は、成形が容易であることから、カラム状や板状への加工により、ナノフィルター形式の金属イオン捕捉剤として用いることができる。
【0085】
また、本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマーは、溶液のpHの変化より、プロトン化されたカチオン状態、または脱プロトンのアミン状態に変化できる。このため、本発明の金属イオン捕捉剤は、金属イオンを選択的に捕捉することが可能である。
【0086】
さらに、本発明の金属イオン捕捉剤においては、シリカの有する耐酸性、耐酸化性、耐有機溶剤性に優れ、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーは該繊維状複合体から溶出されることができない。従って、金属と配位する活性部が繊維状複合体中に安定に固定化された状態を保持できる。
【0087】
本発明の金属イオン捕捉剤は、有機ポリマーに配位子を結合した従来のイオン交換樹脂の使用条件と同様なプロセスで使用できる。また、有機ポリマー系イオン交換樹脂は耐酸化性、耐酸性が弱く、そのような条件下では使用できない場合があるが、本発明の金属イオン捕捉剤はシリカの耐酸化性、耐酸性が高いので、そのような環境でも使用することができる。即ち、pH<1の環境でも十分安定に使用できる。
【0088】
本発明での捕捉剤はシリカが支持体として機能するため、水中使用は勿論、有機溶剤が含まれた水中、または有機溶剤中でも使用することができる。
【0089】
[金属イオン分離方法]
本発明の金属イオン捕捉剤において、金属イオンを取り込むのは繊維状複合体中に含まれたポリエチレンイミン骨格を有するポリマーの金属イオンに対する強い配位能力によるものである。この際、シリカはその配位子を支える支持体として機能する。
【0090】
本発明の金属イオン捕捉剤が捕捉可能な金属イオンとしては、アルカリ金属イオン、アルカリ土類金属イオン、遷移金属イオン、ランタン金属イオン、ポリオキソメタレートイオンなどが挙げられる。
【0091】
本発明での捕捉剤が金属イオンを捕捉する機構は、シリカ中のポリエチレンイミンが金属イオンに配位することにより、金属イオンを水液相から、シリカ中に取り込まれ、そのままシリカ中に固定化される。これは、イオン結合等の過程と異なり、金属がカチオンでも、またはアニオンでも、ポリエチレンイミンの配位により、捕捉されることになる。従って、本発明の金属イオン捕捉剤は、遷移金属イオンの捕捉に特に好適に用いることができる。遷移金属イオンとして、それが金属カチオン(Mn+)であっても、または遷移金属が酸素との結合からなる酸根アニオン(MOxn−)、またはハロゲン類結合からなるアニオン(MLxn−)であっても、本捕捉剤はそれらの捕捉、固定、除去、回収に好適に用いることができる。
【0092】
遷移金属イオンとしては、下記の遷移金属のカチオン(Mn+)、例えば、Cu,Zn,Co,Ni,Cr,Mn,Mo,Fe,Ru,W,Rh,Cd,Os,Hg,Cd,Ir,Ag,Pt,Sn,Pb,Gaの一価、二価、三価または四価のカチオンなどが挙げられる。これら金属カチオンの捕捉においては、その金属カチオンの対アニオンは、Cl,NO3,SO4、またはポリオキソメタレート類アニオン、あるいはカルボン酸類の有機アニオンのいずれであってもよい。
【0093】
また、下記の遷移金属アニオン(MOxn−)、例えば、MnO4,MoO4,ReO4,WO3,RuO4,CoO4,CrO4,VO3,NiO4のアニオンが挙げられる。
【0094】
本発明での捕捉剤は、ポリオキソメタレート類の金属化合物にも好適に用いることができるが、具体的には、遷移金属カチオンと組み合わせられたモリブデン酸塩、タングステン酸塩、バナジン酸塩類である。
【0095】
さらに、下記の金属が含まれたアニオン(MLxn−)、例えば、AuCl4,PtCl6,RhCl4,RoF6,NiF6,CuF6,RuCl6,In2Cl6の如く、金属がハロゲンに配位されてからなるアニオンの捕捉、濃縮、回収または除去などにも好適に用いることができる。
【0096】
アルカリ金属としては、例えば、リチウム、ナトリウム、カリウム、セシウムなどが挙げられる。この場合、媒体の使用条件としては、pHが5〜14の範囲であることが好ましく、pHが7〜9の範囲であれば更に好ましい。また、アルカリ金属イオンの捕捉においては、アルカリ金属イオンがカチオンである場合に、そのアルカリ金属カチオンの対アニオンが、Cl,NO3,SO4,PO4,ClO4,PF6,BF4などである系にも好ましく用いることができる。
【0097】
アルカリ土類金属イオンとしては、例えば、バリウム、マグネシウム、カルシウムなどが挙げられる。
【0098】
ランタン金属イオンとしては、例えば、La,Eu,Gd,Yb,Euなど3価のカチオンが挙げられる。
【0099】
本発明の金属イオン捕捉剤は、粉末、粒子、多面体、シリンダーなど様々な形状で使用することができる。このため、本発明の金属イオン捕捉剤を使用して金属イオンを捕捉する場合には、これらのシリカ捕捉剤をバッチ法またはフロー法で用いることができる。
【0100】
バッチ法で捕捉する際は、シリカ粉末または粒子を金属のイオンの水液に加える方法や、金属イオンの水液をシリカ粉末に加える方法などにより、好適に金属イオンを捕捉できる。
【0101】
バッチ法で金属イオンを捕捉する際は、混合系を10分から24時間までシェイキングすることで行う。シェイキング時間は、金属種類により大きく異なるが、カチオン類金属イオンでは、数時間であれば好適に捕捉することができる。
【0102】
また、フロー法の場合は、シリカ粉末、粒子などを湿式でガラスカラムに充填し、そのカラムに金属イオン水液を流すことで、好適に金属イオンを捕捉できる。特に、カチオン性金属イオンには、フロー法が好適である。
【0103】
本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマー由来の窒素の含有量は、金属イオンに配位する活性点であるため、窒素原子が配位に全部使われたら、金属イオン捕捉剤は飽和状態となる。この際には、金属イオン捕捉剤を取り出し、これを塩酸水溶液または硝酸水溶液で洗浄し、金属イオンを容易に脱配位させることができる。即ち、捕捉剤はこれで再生される。この再生に用いる塩酸または硝酸水溶液の濃度は、1〜7Mであればよく、好ましくは3〜5Mである。
【0104】
酸で捕捉された金属イオンを金属イオン捕捉剤から脱離させた後、金属イオン捕捉剤を蒸留水、0.001Mのアルカリ水溶液や蒸留水で洗浄した後、再び、金属イオンの捕捉に用いることができる。
【実施例】
【0105】
以下、実施例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0106】
[X線回折法による捕捉剤の分析]
単離乾燥した試料を測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−Ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲10〜40°の条件で測定を行った。
【0107】
[走査電子顕微鏡による捕捉剤の形状分析]
単離乾燥した試料をガラススライドに乗せ、それをキーエンス製表面観察装置VE−7800にて観察した。
【0108】
[透過電子顕微鏡による捕捉剤の観察]
単離乾燥した試料を炭素蒸着された銅グリッドに乗せ、それを日本電子製JEM-200CX透過型電子顕微鏡にて観察した。
【0109】
(作製例1)
<線状のポリエチレンイミン(L−PEI)の合成>
ポリエチルオキサゾリン(数平均分子量500000,平均重合度5000,Aldrich社製)5gを、5Mの塩酸水溶液20mLに溶解させた。その溶液をオイルバスにて90℃に加熱し、その温度で10時間攪拌した。反応液にアセトン50mLを加え、ポリマーを完全に沈殿させ、それを濾過し、メタノールで3回洗浄し、白色のポリエチレンイミンの粉末を得た。得られた粉末を1H−NMR(重水)にて同定したところ、ポリエチルオキサゾリンの側鎖エチル基に由来したピーク1.2ppm(CH3)と2.3ppm(CH2)が完全に消失していることが確認された。即ち、ポリエチルオキサゾリンが完全に加水分解され、ポリエチレンイミンに変換されたことが示された。
【0110】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿したポリマー結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温乾燥し、線状のポリエチレンイミン(L−PEI)を得た。収量は4.2g(結晶水含有)であった。ポリオキサゾリンの加水分解により得られるポリエチレンイミンは、側鎖だけが反応し、主鎖には変化がない。従って、L−PEIの重合度は加水分解前の5000と同様である。
【0111】
<線状ポリエチレンイミン系からの捕捉剤の作製>
合成例1で得られたL−PEI粉末を蒸留水中に分散させ、その分散液をオイルバスにて、90℃に加熱し、濃度が2%となる完全透明な水溶液を得た。その水溶液を室温に放置し、自然に室温までに冷やし、不透明なL−PEIヒドロゲルを得た。得られたヒドロゲルは、剪断力を加えると変形を生じるが、概ねの形状を保持できるアイスクリーム状態のヒドロゲルであった。
【0112】
得られたヒドロゲルにつき、X線回折測定を行った結果、20.7°、27.6°、28.4°に散乱強度のピークが表れることが確認された。また、熱量分析装置による吸熱状態変化の測定結果により、64.5℃で吸熱のピークが確認された。これら測定結果より、ヒドロゲル中におけるL−PEIの結晶の存在が確認された。
【0113】
これで得られたヒドロゲル20mL中に、テトラメトキシシラン(TMSO)とエタノールの1/1(体積比)の混合液を20mL加え、アイスクリーム状態のものを軽く一分間かき混ぜた後、そのまま40分放置した。その後、過剰なアセトンで洗浄し、それを円心分離器にて3回洗浄を行った。固形物を回収し、室温で乾燥し、白色の金属イオン捕捉剤を得た。捕捉剤のX線回折測定から、L−PEIの結晶由来のピークが20.5°、27.2°、28.2°に表れた。
【0114】
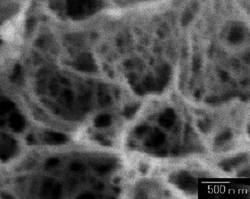
得られた金属イオン捕捉剤を走査型顕微鏡により観察したところ、図1に示したように繊維状複合体の三次元網目構造を有するものであった。
【0115】
捕捉剤の元素分析から、窒素の含有量は8.5%であることが確認された。このことから、1グラムの該捕捉剤中、配位子である窒素のミリモル数は、6.07と換算された。これは、メソポーラス系シリカ中の配位子導入が通常2ミリモル以下であることに比べると、極めて大きいものであった。
【0116】
(実施例1)
<銅イオンの捕捉>
上記により得られた金属イオン捕捉剤50mgを秤取り、それに10mLの1mM硝酸銅水溶液を加えた。混合物中の白色の金属イオン捕捉剤は、一瞬で青色に変わった。その代わり、液部はほぼ無色に近い状態であった。これにより銅イオンが金属イオン捕捉剤に迅速に取り込まれることが確認された。このまま、2時間静置させた後、液部を取り出し、吸収スペクトル測定を行ったが、残存銅イオンは認められる濃度ではないことが判断された。即ち、銅イオンはほぼ完全に金属イオン捕捉剤に捕捉された。
濾過により、青く染まった金属イオン捕捉剤を回収し、それを2Mの硝酸水溶液で洗浄したところ、水液は青色になることが確認された。これより、金属イオン捕捉剤に捕捉された銅イオンは簡単に回収されることが示された。
【0117】
(実施例2)
<パラジウムイオンの捕捉と還元>
上記金属イオン捕捉剤20mgを秤取り、それを4mLの0.5Mパラジウム硝酸水溶液に加え、そのまま、2時間静置させた。混合物を濾過し、金属イオン捕捉剤を蒸留水で洗浄した後、それを3mLのNaBH4水溶液(重量濃度2%)中に加え、30分間シェイクした。混合物を濾過し、それを蒸留水、アセトン順で洗浄した。白色の金属イオン捕捉剤は黒色に変化した。これにより、金属イオン捕捉剤に捕捉されたパラジウムイオンが還元剤より、パラジウム金属に還元されたことが示された。
該金属イオン捕捉剤をXRDで観測した結果、金属パラジウム結晶に由来のピークが36,43,66°に顕著に現れた。また、TEM観察から(図2)、シリカ繊維中にパラジウムの多量のナノ粒子が固定されていることが確認された。これより、捕捉剤に捕捉された金属イオンを金属状態で固定化できることが示された。
【図面の簡単な説明】
【0118】
【図1】本発明の作製例1における金属イオン捕捉剤の走査型電子顕微鏡写真である。
【図2】本発明の実施例3におけるパラジウム金属結晶が固定化された金属イオン捕捉剤の透過型電子顕微鏡写真である。
【技術分野】
【0001】
本発明は、金属イオンを捕捉する捕捉剤、及び該捕捉剤を用いた金属イオンの捕捉方法に関する。
【背景技術】
【0002】
金属イオンの分離、除去、回収は環境浄化、環境保護の視点から、産業問題の枠を越えた全社会的な課題として、ますます重視されている。従って、効率的な金属イオン捕捉剤または捕捉方法についての技術開発においては、従来の有機系ポリマー、例えばイオン交換樹脂系より、多くの優位性、例えば、速いイオン交換速度、高いイオン選択性、高いイオン交換率、簡易なイオン回収性、耐熱性、環境適切性などを有する新しい材料系に転換されて行く傾向がある。
【0003】
こうした金属イオンの捕捉剤として近年注目されているのがシリカ(珪素)系の捕捉剤である。珪素は地殻上で酸素に次ぐ第二番目を誇る豊富な存在であり、自然界の石英、水晶、オパール、雲母、石綿などはよく知られている珪素の酸化物である。規則的な空間構造やパターン構造を有するシリカ系材料は様々な機能系材料、例えば、分離、精製、または触媒担持体用の材料として極めて有望であり、この機能または効能が従来のポリマー樹脂系より優れていることから、これに関する技術開発がこの数年大きく進歩している。
【0004】
シリカ系金属イオン捕捉剤としては、主にメソポーラスシリカが使用されている。シリカ中にメソポーラス空洞構造を発現させるための方法としては、分子組織体、例えば、低分子または高分子系の会合体をテンプレートとして用い、その会合体周辺でシリカソースであるアルコキシシランのゾルゲル反応を行うことで、シリカゲルが与えられる。このシリカゲルを高温で焼結し、内部の有機テンプレートを除去することにより、シリカ中空洞が残る。テンプレートとしては、界面活性剤(非特許文献1参照)、ブロックポリマー(非特許文献2参照)、ウイルス、バクテリア(非特許文献3参照)などが使用されている。テンプレートの種類により、得られるシリカ中の空洞が2〜20nm程度の範囲で変化し、かつその空洞は平行したチャンネルとして規則的に配列される。このようなことから、メソポーラスシリカ材料は、触媒、電子材料、ナノフィルター、クロマトグラフィー、分離、バイオ工学などの分野で多くの関心を集めている。
【0005】
しかし、メソポーラスシリカを金属イオン捕捉剤として用いるには、そのシリカ空洞表面に、アミン、チオールなどの金属イオンに配位能力を有する官能基を導入しなければならない(非特許文献4〜6参照)。メソポーラスシリカは球状の形に作製することができるが、多くの場合、これらのシリカは形状が制御されてない粉末または塊である。従って、金属イオン捕捉のプロセスからいえば、メソポーラスシリカ中の空洞中に金属イオンが入り込み、さらに該金属イオンが空洞内部のアミン、チオールなどの官能基に安定して配位されるには、金属イオンの拡散、配位など全プロセスにおける長い時間を要するものであった。また、メソポーラスシリカ中に固定化できる官能基の数にも制限があり、多量の金属イオンを捕捉する場合にはシリカ量を多くする必要があった。
【0006】
【非特許文献1】C.T.Kresge et al.,Nature,(1992),359,p.710
【非特許文献2】A.Monnier et al.,Science,(1993),261,p1299
【非特許文献3】S.A.Davis et al.,Nature,(1997),385,p420
【非特許文献4】T. Kang et al., J. Mater. Chem. (2004) 14, p1043
【非特許文献5】B. Lee et al., Langmuir, (2003) 19, p4246
【非特許文献6】K. Zakir et al., Adv. Mater. (2002) 14, p1053)
【発明の開示】
【発明が解決しようとする課題】
【0007】
本発明が解決しようとする課題は、金属イオンを速やかに捕捉できる金属イオン捕捉剤、及び金属イオンを速やかに捕捉可能な金属イオン捕捉方法を提供すること、特に、多くの金属イオンを速やかに捕捉でき、且つ各種形状に成形可能である金属イオン捕捉剤を提供することにある。
【課題を解決するための手段】
【0008】
本発明においては、金属イオンに高い配位能力を有する直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さがナノメートルオーダーの繊維状複合体を会合させ、全体のネットワークを形成させた捕捉剤が、スポンジのようにその内部に微少な空間と、大きな表面積を確保できるため、多くの金属イオンを速やかに捕捉することができる。さらに、太さがナノメートルオーダーの繊維状複合体の会合体からなるものであるため任意の形状への成形が可能である。
【0009】
すなわち、本発明は直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤を提供することにある。
【0010】
さらに本発明は、金属イオンを含有する溶液と、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記遷移金属捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることからなる金属の捕捉方法、及び金属イオン捕捉剤に捕捉された金属イオンを酸性処理により金属捕捉剤から分離する方法を提供することにある。
【発明の効果】
【0011】
本発明の金属イオン捕捉剤は、ナノメートルオーダーの繊維状複合体が会合した三次元網目構造、即ち、シリカスポンジ構造を有する。従って、そのスポンジ内部は繊維状複合体と空隙で構成され、かつ内部の繊維状複合体の表面積が非常に大きい。このため、本発明の金属イオン捕捉剤は金属イオン水溶液と接触させた際、金属イオンがシリカの全表面と接触することができ、多くの金属イオンを速やかに捕捉することが可能となる。更に、本発明の金属イオン捕捉剤は、成形が容易であることから、カラム状や板状への加工により、ナノフィルター形式の金属イオン捕捉剤として用いることができる。
【0012】
また、本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマーは、溶液のpHの変化より、プロトン化されたカチオン状態、または脱プロトンのアミン状態に変化できる。このため、本発明の金属イオン捕捉剤は、金属イオンを選択的に捕捉することが可能である。
【0013】
さらに、本発明の金属イオン捕捉剤においては、シリカの有する耐酸性、耐酸化性、耐有機溶剤性に優れ、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーは該繊維状複合体から溶出されることがない。従って、金属と配位する活性部が繊維状複合体中に安定に固定化された状態を保持できる。
【0014】
また、本発明のポリマー結晶とシリカからなる捕捉剤の形成において、その結晶フィラメント中に機能性物質、例えば、蛍光物質など機能性化合物を含有させることが可能であり、含有させた機能性物質に由来する機能を発現させることもできる。
【0015】
また、本発明の金属イオン捕捉剤を使用した捕捉方法によると、多くの金属イオンを速やかに捕捉でき、さらに、シリカ繊維中に捕捉された金属イオンを酸性水溶液で洗浄することにより、その金属を容易に回収できる。
【発明を実施するための最良の形態】
【0016】
本発明の捕捉剤は、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さがナノメートルオーダーの範囲にある繊維状複合体同士が会合してなるものである。
【0017】
[直鎖状ポリエチレンイミン骨格を有するポリマー]
本発明でいう直鎖状ポリエチレンイミン骨格とは、二級アミンのエチレンイミン単位を主たる構造単位とするポリマー骨格をいう。該骨格中においては、エチレンイミン単位以外の構造単位が存在していてもよいが、ポリマー結晶を形成させるためには、ポリマー鎖の一定鎖長が連続的なエチレンイミン単位であることが好ましい。該直鎖状ポリエチレンイミン骨格の長さは、該骨格を有するポリマーが結晶を形成できる範囲であれば特に制限されないが、好適にポリマー結晶を形成するためには、該骨格部分のエチレンイミン単位の繰り返し単位数が10以上であることが好ましく、20〜10000の範囲であることが特に好ましい。
【0018】
本発明において使用するポリマーは、その構造中に直鎖状ポリエチレンイミン骨格を有するものであればよく、その形状が線状、星状または櫛状であっても、水中または水と水溶性有機溶媒混合の水性媒体中で結晶体を与えることができる。
【0019】
また、これら線状、星状または櫛状のポリマーは、直鎖状ポリエチレンイミン骨格のみからなるものであっても、直鎖状ポリエチレンイミン骨格からなるブロック(以下、ポリエチレンイミンブロックと略記する。)と他のポリマーブロックとのブロックコポリマーからなるものであってもよい。他のポリマーブロックとしては、例えば、ポリエチレングリコール、ポリプロピオニルエチレンイミン、ポリアクリルアミドなどの水溶性のポリマーブロック、あるいは、ポリスチレン、ポリオキサゾリン類のポリフェニルオキサゾリン、ポリオクチルオキサゾリン、ポリドデシルオキサゾリン、ポリアクリレート類のポリメチルメタクリレート、ポリブチルメタクリレートなどの疎水性のポリマーブロックを使用できる。これら他のポリマーブロックとのブロックコポリマーとすることで、ポリマー結晶の形状や特性を調整することができる。
【0020】
直鎖状ポリエチレンイミン骨格を有するポリマーが、ブロックコポリマーである場合の該ポリマー中における直鎖状ポリエチレンイミン骨格の割合は、ポリマー結晶を形成できる範囲であれば特に制限されないが、好適にポリマー結晶を形成するためには、ポリマー中の直鎖状ポリエチレンイミン骨格の割合が40モル%以上であることが好ましく、50モル%以上であることがさらに好ましい。
【0021】
上記直鎖状ポリエチレンイミン骨格を有するポリマーは、その前駆体となるポリオキサゾリン類からなる直鎖状の骨格を有するポリマー(以下、前駆体ポリマーと略記する。)を、酸性条件下またはアルカリ条件下で加水分解することで容易に得ることができる。従って、直鎖状ポリエチレンイミン骨格を有するポリマーの線状、星状、または櫛状などの形状は、この前駆体ポリマーの形状を制御することで容易に設計することができる。また、重合度や末端構造も、前駆体ポリマーの重合度や末端機能団を制御することで容易に調整できる。さらに、直鎖状ポリエチレンイミン骨格を有するブロックコポリマーを形成する場合には、前駆体ポリマーをブロックコポリマーとし、該前駆体中のポリオキサゾリン類からなる直鎖状の骨格を選択的に加水分解することで得ることができる。
【0022】
前駆体ポリマーは、オキサゾリン類のモノマーを使用して、カチオン型の重合法、あるいは、マクロモノマー法などの合成方法により合成が可能であり、合成方法や開始剤を適宜選択することにより、線状、星状、あるいは櫛状などの各種形状の前駆体ポリマーを合成できる。
【0023】
ポリオキサゾリン類からなる直鎖状の骨格を形成するモノマーとしては、メチルオキサゾリン、エチルオキサゾリン、メチルビニルオキサゾリン、フェニルオキサゾリンなどのオキサゾリンモノマーを使用できる。
【0024】
重合開始剤としては、分子中に塩化アルキル基、臭化アルキル基、ヨウ化アルキル基、トルエンスルホニルオキシ基、あるいはトリフルオロメチルスルホニルオキシ基などの官能基を有する化合物を使用できる。これら重合開始剤は、多くのアルコール類化合物の水酸基を他の官能基に変換させることで得られる。なかでも、官能基変換として、臭素化、ヨウ素化、トルエンスルホン酸化、およびトリフルオロメチルスルホン酸化されたものは重合開始効率が高いため好ましく、特に臭化アルキル、トルエンスルホン酸アルキルが好ましい。
【0025】
また、ポリ(エチレングリコール)の末端水酸基を臭素あるいはヨウ素に変換したもの、またはトルエンスルホニル基に変換したものを重合開始剤として使用することもできる。その場合、ポリ(エチレングリコール)の重合度は5〜100の範囲であることが好ましく、10〜50の範囲であれば特に好ましい。
【0026】
また、カチオン開環リビング重合開始能を有する官能基を有し、かつ光による発光機能、エネルギー移動機能、電子移動機能を有するポルフィリン骨格、フタロシアニン骨格、またはピレン骨格のいずれかの骨格を有する色素類は、得られるポリマーに特殊な機能を付与することができる。
【0027】
線状の前駆体ポリマーは、上記オキサゾリンモノマーを1価または2価の官能基を有する重合開始剤により重合することで得られる。このような重合開始剤としては、例えば、塩化メチルベンゼン、臭化メチルベンゼン、ヨウ化メチルベンゼン、トルエンスルホン酸メチルベンゼン、トリフルオロメチルスルホン酸メチルベンゼン、臭化メタン、ヨウ化メタン、トルエンスルホン酸メタンまたはトルエンスルホン酸無水物、トリフルオロメチルスルホン酸無水物、5−(4−ブロモメチルフェニル)−10,15,20−トリ(フェニル)ポルフィリン、またはブロモメチルピレンなどの1価のもの、ジブロモメチルベンゼン、ジヨウ化メチルベンゼン、ジブロモメチルビフェニレン、またはジブロモメチルアゾベンゼンなどの2価のものが挙げられる。また、ポリ(メチルオキサゾリン)、ポリ(エチルオキサゾリン)、または、ポリ(メチルビニルオキサゾリン)などの工業的に使用されている線状のポリオキサゾリンを、そのまま前駆体ポリマーとして使用することもできる。
【0028】
星状の前駆体ポリマーは、上記したようなオキサゾリンモノマーを3価以上の官能基を有する重合開始剤により重合することで得られる。3価以上の重合開始剤としては、例えば、トリブロモメチルベンゼン、などの3価のもの、テトラブロモメチルベンゼン、テトラ(4−クロロメチルフェニル)ポルフィリン、テトラブロモエトキシフタロシアニンなどの4価のもの、ヘキサブロモメチルベンゼン、テトラ(3,5−ジトシリルエチルオキシフェニル)ポルフィリンなどの5価以上のものが挙げられる。
【0029】
櫛状の前駆体ポリマーを得るためには、多価の重合開始基を有する線状のポリマーを用いて、該重合開始基からオキサゾリンモノマーを重合させることができるが、例えば、通常のエポキシ樹脂やポリビニルアルコールなどの側鎖に水酸基を有するポリマーの水酸基を、臭素やヨウ素等でハロゲン化するか、あるいはトルエンスルホニル基に変換させた後、該変換部分を重合開始基として用いることでも得ることができる。
【0030】
また、櫛状の前駆体ポリマーを得る方法として、ポリアミン型重合停止剤を用いることもできる。例えば、一価の重合開始剤を用い、オキサゾリンを重合させ、そのポリオキサゾリンの末端をポリエチレンイミン、ポリビニルアミン、ポリプロピルアミンなどのポリアミンのアミノ基に結合させることで、櫛状のポリオキサゾリンを得ることができる。
【0031】
上記により得られる前駆体ポリマーのポリオキサゾリン類からなる直鎖状の骨格の加水分解は、酸性条件下またはアルカリ条件下のいずれの条件下でもよい。酸性条件下での加水分解は、例えば、塩酸水溶液中でポリオキサゾリンを加熱下で攪拌することにより、ポリエチレンイミンの塩酸塩を得ることができる。得られた塩酸塩を過剰のアンモニウム水で処理することで、塩基性のポリエチレンイミンの結晶粉末を得ることができる。用いる塩酸水溶液は、濃塩酸でも、1mol/L程度の水溶液でもよいが、加水分解を効率的に行うには、5mol/Lの塩酸水溶液を用いることが望ましい。また、反応温度は80℃前後が望ましい。
【0032】
アルカリ条件下での加水分解は、例えば、水酸化ナトリウム水溶液を用いることで、ポリオキサゾリンをポリエチレンイミンに変換させることができる。アルカリ条件下で反応させた後、反応液を透析膜にて洗浄することで、過剰な水酸化ナトリウムを除去し、ポリエチレンイミンの結晶粉末を得ることができる。用いる水酸化ナトリウムの濃度は1〜10mol/Lの範囲であればよく、より効率的な反応を行うには3〜5mol/Lの範囲であることが好ましい。また、反応温度は80℃前後が好ましい。
【0033】
酸性条件下またはアルカリ条件下での加水分解における、酸またはアルカリの使用量は、ポリマー中のオキサゾリン単位に対し、1〜10当量でよく、反応効率の向上と後処理の簡便化のためには、3当量程度とすることが好ましい。
【0034】
上記加水分解により、前駆体ポリマー中のポリオキサゾリン類からなる直鎖状の骨格が、直鎖状ポリエチレンイミン骨格となり、該ポリエチレンイミン骨格を有するポリマーが得られる。
【0035】
また、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーを形成する場合には、前駆体ポリマーをポリオキサゾリン類からなる直鎖状のポリマーブロックと、他のポリマーブロックとからなるブロックコポリマーとし、該前駆体ポリマー中のポリオキサゾリン類からなる直鎖状のブロックを選択的に加水分解することで得ることができる。
【0036】
他のポリマーブロックが、ポリ(N−プロピオニルエチレンイミン)などの水溶性ポリマーブロックである場合には、ポリ(N−プロピオニルエチレンイミン)が、ポリ(N−ホルミルエチレンイミン)やポリ(N−アセチルエチレンイミン)に比べて、有機溶媒への溶解性が高いことを利用してブロックコポリマーを形成することができる。即ち、2−オキサゾリンまたは2−メチル−2−オキサゾリンを、前記した重合開始化合物の存在下でカチオン開環リビング重合した後、得られたリビングポリマーに、さらに2−エチル−2−オキサゾリンを重合させることによって、ポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとからなる前駆体ポリマーを得る。該前駆体ポリマーを水に溶解させ、該水溶液にポリ(N−プロピオニルエチレンイミン)ブロックを溶解する水とは非相溶の有機溶媒を混合して攪拌することによりエマルジョンを形成する。該エマルジョンの水相に、酸またはアルカリを添加することによりポリ(N−ホルミルエチレンイミン)ブロックまたはポリ(N−アセチルエチレンイミン)ブロックを優先的に加水分解させることにより、直鎖状ポリエチレンイミンブロックと、ポリ(N−プロピオニルエチレンイミン)ブロックとを有するブロックコポリマーを形成できる。
【0037】
ここで使用する重合開始化合物の価数が1および2の場合には、直鎖状のブロックコポリマーとなり、それ以上の価数であれば星型のブロックコポリマーが得られる。また、前駆体ポリマーを多段のブロックコポリマーとすることで、得られるポリマーも多段のブロック構造とすることも可能である。
【0038】
[ポリマー結晶]
上記ポリエチレンイミン骨格を有するポリマーは、一次構造中の直鎖状ポリエチレンイミン骨格が、水又は水と親水性溶媒の混合溶液中で結晶性を発現してポリマー結晶を形成する。該ポリマー結晶は、水の存在下でのポリマー結晶同士の物理的な結合により三次元網目構造を有するヒドロゲルを形成することもでき、さらにポリマー結晶同士を架橋剤で架橋することにより化学的な架橋結合を有する架橋ヒドロゲルを形成することもできる。
【0039】
従来広く使用されてきたポリエチレンイミンは、環状エチレンイミンの開環重合により得られる分岐状ポリマーであり、その一次構造には一級アミン、二級アミン、三級アミンが存在する。従って、分岐状ポリエチレンイミンは水溶性であるが、結晶性は持たないため、分岐状ポリエチレンイミンを用いてヒドロゲルを作るためには、架橋剤による共有結合により網目構造を与えなくてはならない。しかしながら本発明に使用するポリマーが骨格として有する直鎖状ポリエチレンイミンは、二級アミンだけで構成されており、該二級アミン型の直鎖状ポリエチレンイミンは水溶性でありながら、優れた結晶性を有する。
【0040】
このような、直鎖状ポリエチレンイミンの結晶は、そのポリマーのエチレンイミン単位に含まれる結晶水数により、ポリマー結晶構造が大きく異なることが知られている(Y.Chatani et al.、Macromolecules、1981年、第14巻、p.315−321)。無水のポリエチレンイミンは二重螺旋構造を特徴とする結晶構造を優先するが、モノマー単位に2分子の水が含まれると、ポリマーはzigzag構造を特徴とする結晶体に成長することが知られている。実際、水中から得られる直鎖状ポリエチレンイミンの結晶は一つのモノマー単位に2分子水を含む結晶であり、その結晶は室温状態では水中不溶である。
【0041】
本発明における直鎖状ポリエチレンイミン骨格を有するポリマーの結晶は、上記の場合と同様に直鎖状ポリエチレンイミン骨格の結晶発現により形成されるものであり、ポリマー形状が線状、星状、または櫛状などの形状であっても、一次構造に直鎖状ポリエチレンイミン骨格を有するポリマーであれば、ポリマーの結晶が得られる。
【0042】
本発明におけるポリマー結晶の存在はX線散乱により確認でき、広角X線回折計(WAXS)における2θ角度値で20°,27°,28°近傍の結晶性ヒドロゲル中の直鎖状ポリエチレンイミン骨格に由来するピーク値により確認される。
【0043】
また、本発明におけるポリマー結晶の示差走査熱量計(DSC)における融点は、ポリエチレンイミン骨格のポリマーの一次構造にも依存するが、概ねその融点が45〜90℃で現れる。
【0044】
本発明におけるポリマー結晶は、その結晶を構成するポリマー構造の幾何学的な形状や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー結晶の形成条件などの影響により各種形状を取り得ることができ、例えば繊維状、ブラシ状、星状などの形状を有する。
【0045】
上記ポリマー結晶は、5〜30nm程度のナノメートルオーダーの繊維状ポリマー結晶(以下、該結晶を繊維状ナノ結晶と略記する。)を基礎とするものであり、該繊維状ナノ結晶表面に存在するフリーなエチレンイミン鎖により、繊維状ナノ結晶同士が水素結合による物理的な結合で繋がれて空間に配置され、上記したような三次元形状に成長する。これらポリマー結晶間が、さらに物理的に結合し、該ポリマー結晶の三次元網目構造を作り上げる。これらは水の存在下で生じるため、結果的には該三次元網目構造中に水を包含したヒドロゲルが与えられる。
【0046】
ここでいう三次元網目構造とは、通常の高分子ヒドロゲルと異なり、マイクロ、またはナノスケールの結晶同士が、その結晶表面に存在するフリーなエチレンイミン鎖の水素結合により、物理的に架橋化された網目構造を言う。従って、その結晶の融点以上の温度では、結晶が水中溶解されてしまい、三次元網目構造も解体される。ところが、それが室温に戻ると、ポリマー結晶が成長し、その結晶間では水素結合による物理的な架橋が形成するため、再び、三次元網目構造が現れる。
【0047】
本発明のポリマー結晶は、直鎖状ポリエチレンイミン骨格を有するポリマーが室温の水に不溶である性質を利用し、該直鎖状ポリエチレンイミン骨格を有するポリマーの水中での溶解−結晶変換により得ることができる。
【0048】
また、ヒドロゲルは、まず直鎖状ポリエチレンイミン骨格を有するポリマーを一定量水中に分散し、該分散液を加熱することにより、ポリエチレンイミン骨格を有するポリマーの透明な水溶液を得る。次いで、加熱状態のポリマーの水溶液を室温に冷やすことにより得られる。該ヒドロゲルは、剪断力等の外力により変形を生じるが、概ねの形状を保持できるアイスクリームのような状態を有し、多様な形状に変形させることが可能である。
【0049】
上記ポリマー分散液の加熱温度は100℃以下が好ましく、90〜95℃の範囲であることがより好ましい。また、ポリマー分散液中のポリマー含有量は、ヒドロゲルが得られる範囲であれば特に限定されないが、0.01〜20質量%の範囲であることが好ましく、安定形状の結晶体からなるヒドロゲルを得るためには0.1〜10質量%の範囲がさらに好ましい。このように、本発明においては、直鎖状ポリエチレンイミン骨格を有するポリマーを使用すると、ごく少量のポリマー濃度でもヒドロゲルを形成することができる。
【0050】
上記ポリマー水溶液の温度を室温まで低下させる過程により、得られるヒドロゲル中の結晶形状を調整することができる。例えば、ポリマー水溶液を80℃に1時間保持した後、1時間かけて60℃にし、該温度でさらに1時間保持する。その後1時間かけて40℃まで低下させた後、自然に室温まで下げることで、水溶液の水が流動性をなくした状態のヒドロゲル結晶体を得ることができる。また、上記ポリマー水溶液を一気に氷点の氷り水、または氷点下のメタノール/ドライアイス、あるいはアセトン/ドライアイスの冷媒液にて冷却させた後、その状態のものを室温のワータバスにて保持させることでヒドロゲル結晶体を得ることができる。さらには、上記のポリマー水溶液を室温のワータバスまたは室温空気環境にて、室温まで温度を低下させることで、ヒドロゲル結晶体を得ることができる。
【0051】
上記ポリマー水溶液の温度を低下させる工程は、得られるヒドロゲル中のポリマー結晶の形状に強く影響を与えるため、上記異なる工程により得られるヒドロゲル中のポリマーの結晶形態は同一ではない。
【0052】
上記のポリマー水溶液の温度を、濃度を一定として多段階的に低下させた場合、ヒドロゲル中におけるポリマーの結晶形態を、ファイバー状のポリマー結晶形態とすることができる。これを急冷した後、室温に戻した場合には、花弁状のポリマー結晶形態とすることができ。また、これをドライアイス上のアセトンで再度急冷して、室温に戻した場合、波状のポリマー結晶形態とすることができる。このように、本発明のヒドロゲル中におけるポリマーの結晶形態を、各種形状に設定することができる。
【0053】
上記により得られるヒドロゲルは、不透明なゲルであり、ゲル中にはポリエチレンイミン骨格を有するポリマーの結晶が形成し、その結晶体同士の水素結合により物理的に架橋化され、三次元の物理的な網目構造を形成している。一旦形成したヒドロゲル中のポリマー結晶は室温中では不溶状態を保つが、加熱するとポリマー結晶が解離し、ヒドロゲルはゾル状態に変化してしまう。従って、本発明の物理的なヒドロゲルは、熱処理を行うことでゾルからゲル、またゲルからゾルへと可逆的な変化が可能である。
【0054】
本発明でいうヒドロゲルは三次元網目構造中に少なくとも水を含有するが、該ヒドロゲルの調製時に、水溶性有機溶剤を加えることで、有機溶剤を含有したヒドロゲルが得られる。該親水性有機溶剤としては、例えば、メタノール、エタノール、テトラヒドロフラン、アセトン、ジメチルアセトアミド、ジメチルスルフォンオキシド、ジオキシラン、ピロリドンなどの水溶性有機溶剤を取りあげることができる。
【0055】
有機溶剤の含有量は、水の体積に対し、0.1〜5倍の範囲であることが好ましく、1〜3倍の範囲であればより好ましい。
【0056】
上記親水性有機溶媒を含有させることにより、ポリマー結晶の形態を変えることができ、単純な水系と異なる形態の結晶を与えることができる。例えば、水中では繊維状の広がりを有する分岐結晶形態であっても、その調製に一定量のエタノールが含まれた場合、繊維が収縮したような球状結晶形態を得ることができる。
【0057】
本発明でいうヒドロゲル調製時に、他の水溶性ポリマーを加えることで、水溶性ポリマーを含有するヒドロゲルが得られる。該水溶性ポリマーとしては、例えば、ポリエチレングリコール、ポリビニルアルコール、ポリビニルピロリドン、ポリアクリルアミド、ポリ(N−イソプロピルアクリルアミド)、ポリヒドロキシエチルアクリレート、ポリメチルオキサゾリン、ポリエチルオキサゾリンなどを取りあげることができる。
【0058】
水溶性ポリマーの含有量は、直鎖状ポリエチレンイミン骨格を有するポリマーの質量に対し、0.1〜5倍の範囲であることが好ましく、0.5〜2倍の範囲であればより好ましい。
【0059】
上記水溶性ポリマーを含有させることによっても、ポリマー結晶の形態を変えることができ、単純な水系と異なる形態の結晶を与えることができる。また、ヒドロゲルの粘性を増大させ、ヒドロゲルの安定性を向上させることに有効である。
【0060】
上記方法で得られたヒドロゲルを、ポリエチレンイミンのアミノ基と反応する2官能基以上を含む化合物で処理することで、ヒドロゲル中のポリマー結晶表面同士を化学結合でリンクさせた架橋ヒドロゲルを得ることができる。
【0061】
前記アミノ基と室温状態で反応できる2官能基以上を含む化合物としては、アルデヒド類架橋剤、エポキシ類架橋剤、酸クロリド類、酸無水物、エステル類架橋剤を用いることができる。アルデヒド類架橋剤としては、例えば、マロニルアルデヒド、スクシニルアルデヒド、グルタリルアルデヒド、アジホイルアルデヒド、フタロイルアルデヒド、イソフタロイルアルデヒド、テレフタロイルアルデヒドなどがあげられる。また、エポキシ類架橋剤としては、例えば、ポリエチレングリコールジグリシジルエーテル、ビスフェノールAジグリシジルエーテル、グリシジルクロライド、グリシジルブロマイドなどがあげられる。酸クロリド類としては、例えば、マロニル酸クロリド、スクシニル酸クロリド、グルタリル酸クロリド、アジホイル酸クロリド、フタロイル酸クロリド、イソフタロイル酸クロリド、テレフタロイル酸クロリドなどがあげられる。また、酸無水物としては、例えば、フタル酸無水物、スクシニル酸無水物、グルタリル酸無水物などがあげられる。また、エステル類架橋剤としては、マロニル酸メチルエステル、スクシニル酸メチルエステル、グルタリル酸メチルエステル、フタロイル酸メチルエステル、ポリエチレングリコールカルボン酸メチルエステルなどがあげられる。
【0062】
架橋反応は、得られたヒドロゲルを架橋剤の溶液に浸す方法にでも、架橋剤溶液をヒドロゲル中に加える方法でも可能である。この際、架橋剤は系内での浸透圧変化と共に、ヒドロゲル内部へ浸透し、そこで結晶体同士を水素結合で繋いでエチレンイミンの窒素原子との化学反応を引き起こす。
【0063】
架橋反応は、ポリエチレンイミン結晶体表面のフリーなエチレンイミンとの反応により進行するが、その反応を結晶内部では起こらないようにするためには、ヒドロゲルを形成する結晶体の融点以下の温度で反応を行うことが望ましく、さらには架橋反応を室温で行うことが最も望ましい。
【0064】
架橋反応を室温で進行させる場合には、ヒドロゲルを架橋剤溶液と混合した状態で放置しておくことで、架橋ヒドロゲルを得ることができる。架橋反応させる時間は、数分から数日でよく、概ね一晩放置することで好適に架橋が進行する。
【0065】
架橋剤量はヒドロゲル形成に用いるポリエチレンイミン骨格を有するポリマー中のエチレンイミンユニットのモル数に対し、0.05〜20%であればよく、それが1〜10%であればもっと好適である。
【0066】
上記ヒドロゲルは、ゲル化剤が結晶性のポリマーであるため多様なモルフォロジーのゲル構造を発現できる。また少量のポリマー結晶であっても水中で好適に三次元網目構造を形成するため高い水保持性を有する。さらに、使用する直鎖状ポリエチレンイミン骨格を有するポリマーは構造設計や合成が容易であり、かつヒドロゲルの調整が簡便である。また、該ヒドロゲル中のポリマー結晶間を架橋剤により架橋することにより、ヒドロゲルの形状を固定化できる。
【0067】
[繊維状複合体、繊維状複合体の会合]
本発明の金属イオン捕捉剤は、上記のポリマー結晶の水中分散液またはポリマー結晶のヒドロゲル中に、通常のゾルゲル反応において使用できる溶媒にシリカソースを溶解した溶液を加えて、室温下でゾルゲル反応させることにより容易に得ることができる。
【0068】
ポリマー結晶表面には不可避的に結晶に関わりがないフリーなポリエチレンイミンの鎖が多数存在し、これらフリーな鎖は結晶表面でブラシのように存在する。これらのブラシのような鎖はシリカソースを引き寄せる足場であり、同時にシリカソースを重合させる触媒の働きをする。これにより、直鎖状ポリエチレンイミン骨格を有するポリマーの繊維状ナノ結晶表面でゾルゲル反応が進行し、該繊維状ナノ結晶表面がシリカで被覆され、結果的には、結繊維状ナノ結晶がシリカ被覆された繊維状複合体が相互に会合した状態の金属イオン捕捉剤が得られる。
【0069】
シリカソースとして用いる化合物としては、テトラアルコキシシラン類、アルキルトリアルコキシシラン類などが挙げられる。
【0070】
テトラアルコキシシラン類としては、例えば、テトラメトキシシラン、テトラエトキシシラン、テトラプロポキシシラン、テトラブトキシシラン、テトラ−t−ブトキシシランなどを挙げられる。
【0071】
アルキルトリアルコキシシラン類としては、メチルトリメトキシラン、メチルトリエトキシラン、エチルトリメトキシラン、エチルトリエトキシシラン、n−プロピルトリメトキシラン、n−プロピルトリエトキシラン、iso−プロピルトリメトキシシラン、iso−プロピルトリエトキシシラン、3−クロロプロピルトリメトキシシラン、3−クロロプロピルトリエトキシシラン、ビニルトリメトキシシラン、ビニルトリエトキシシラン、3−グリシトキシプロピルトリメトキシシラン、3−グリシトキシプロピルトリエトキシシラン、3−アミノプロピルトリメトキシシラン、3−アミノプロピルトリエトキシラン、3−メルカプトプロピルトメトキシシラン、3−メルカプトトリエトキシシラン、3,3,3−トリフロロプロピルトリメトシシラン、3,3,3−トリフロロプロピルトリエトシシラン、3−メタクリルオキシプロピルトリメトキシシラン、3−メタクリルオキシプロピルトリエトキシシラン、フェニルトリメトキシシラン、フェニルトリエトキシラン、p−クロロメチルフェニルトリメトキシラン、p−クロロメチルフェニルトリエトキシシラン、ジメチルジメトキシシラン、ジメチルジエトキシシラン、ジエチルジメトキシシラン、ジエチルジエトキシシアンなどを挙げられる。
【0072】
本発明の金属イオン捕捉剤を与える上記ゾルゲル反応は、水、あるいは水と親水性有機溶媒の混合溶液などの水性液体中、ポリマー結晶の存在下で進行するが、その反応は水性液体相では起こらず、結晶体の表面で進行する。従って、複合化反応条件ではポリマー結晶が溶解することがなければ、反応条件は任意である。
【0073】
ポリマー結晶を不溶とするためには、ゾルゲル反応の際、親水性有機溶媒を含む水性液体中、水の存在が20%以上とすることが好ましく、それが40%以上であればさらに好ましい。
【0074】
ゾルゲル反応においては、ポリエチレンイミンのモノマー単位であるエチレンイミンに対し、シリカソースであるアルコキシシランの量を過剰とすれば好適に捕捉剤を形成できる。過剰の度合いとしては、エチレンイミンに対し4〜1000倍等量の範囲であることが好ましい。
【0075】
また、ポリマー結晶を形成する際の水、水性液体中のポリマー濃度はそのポリマー中に含まれるポリエチレンイミンの量を基準に、0.1〜30%にすることが好ましい。
【0076】
ゾルゲル反応の時間は1分から数日まで様々であるが、アルコキシシランの反応活性が高いメトキシシラン類の場合は、反応時間は1分〜24時間でよく、反応効率を上げることから、反応時間を30分〜5時間に設定すればさらに好適である。また、反応活性が低い、エトキシシラン類、ブトキシシラン類の場合は、ゾルゲル反応時間が24時間以上が好ましく、その時間を一週間程度とすることも望ましい。
【0077】
本発明の金属イオン捕捉剤は、直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの繊維状複合体(以下、単に繊維状複合体と略記する。)の会合と空間配置から形成された三次元網目形状を有する。該金属イオン捕捉剤の三次元網目構造は、太さがナノメートルオーダーの繊維状複合体を基本ユニットとし、該基本ユニットが相互に会合して三次元網目構造を形成したものである。該金属イオン捕捉剤の内部では、基本ユニットとなる繊維状複合体が、繊維状ナノ結晶が形成したマイクロメートルオーダーの二次的な形状を転写して、微細な会合形状を有している場合が多く、該微細な会合形状の会合体がさらに会合して全体として三次元網目構造を有する金属イオン捕捉剤が形成される。
【0078】
繊維状複合体が形成するマイクロメートルオーダーの二次的な形状は、上記したようにポリマー構造の幾何学的な形状や、分子量、一次構造中に導入できる非エチレンイミン部分、さらにはポリマー結晶の形成条件等により調整でき、レタス状、ファイバー状、スポンジ状、アスター状、サボテン状、タンポポ状など様々な形状に調整できる。これら形状は、使用するポリマーの分子構造、重合度、組成、及びポリマー結晶調製時の温度低下の方法によく依存する。
【0079】
また、本発明の金属イオン捕捉剤は、形状を任意に制御できるヒドロゲルの形状をシリカにより固定化できるため、任意の形状に成形することが可能である。この場合には、ポリマー結晶間が化学結合で架橋された架橋ヒドロゲルを用いると、成形が容易となるため好ましい。該金属イオン捕捉剤の形状や大きさは、ヒドロゲル調製時に用いた容器の大きさ及び形状と同一なものにすることができ、例えば、円盤状、円柱状、プレート状、球状などの任意の形状に調製できる。さらに、架橋させたヒドロゲルを切断したり、削ったりすることにより、目的の形に成形することもできる。このように成形したヒドロゲルをシリカソースの溶液と浸漬等により接触させることにより、ポリマー結晶とシリカからなる成形体が簡単に得られる。シリカソースの溶液に浸漬する時間としては、使用するシランソースの種類により1時間〜1週間と様々であるため適宜調製する必要があるが、メトキシシラン類の溶液中では1〜48時間程度であればよく、エトキシシラン類の溶液中では、1〜7日間程度が好適である。
【0080】
通常、本発明の捕捉剤はポリマー結晶とシリカとから構成され、捕捉剤中のシリカの含有量は、反応条件などにより一定の幅で変化するが、捕捉剤全体の30〜90質量%の範囲のものを得ることができる。なかでもシリカ含有量が捕捉剤全体の40〜80質量%のものが好ましく使用できる。
【0081】
シリカの含有量はゾルゲル反応の際用いたポリエチレンイミンポリマーの量、すなわちヒドロゲル中のポリマー濃度が増えることにつれて増える。また、ゾルゲル反応時間を長くする事により増大する。
【0082】
本発明の金属イオン捕捉剤は、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーに蛍光性物質を組み込むことができる。例えば、酸性基を有するポルフィリンとポリエチレンイミンを混合した後、ゾルゲル反応をすることで、ポルフィリンの残基が金属イオン捕捉剤中に取り込まれる。また、例えば、直鎖状ポリエチレンイミン骨格を有するポリマーの側鎖に少量のピレン類、例えば、ピレンアルデヒド(好ましくは、イミンに対し10モル%以下)を反応させたポリマー結晶を用いることで、ピレン残基を金属イオン捕捉剤に取り込むことができる。さらに、直鎖状ポリエチレンイミン骨格を有するポリマーの塩基に酸性基、例えば、カルボン酸基、スルホン酸基を有するポルフィリン類、フタロシアニン類、ピレン類など蛍光性染料を(好ましくは、イミンのモル数に対し0.1モル%以下)少量混合させ、その結晶体をテンプレートとした金属イオン捕捉剤中には、これらの蛍光性物質を取り込むことができる。
【0083】
本発明の金属イオン捕捉剤の窒素原子の含有量は、金属イオン捕捉剤を調製するとき、ヒドロゲル中の直鎖状ポリエチレンイミン骨格を有するポリマー濃度を変えることで変えることができる。濃度が高くなると、得られたシリカ捕捉剤中の窒素原子の含有量は増大する。通常、窒素原子の含有量は1〜15質量%の範囲にすることができる。本発明の金属イオン捕捉剤中の窒素原子は、金属イオンに高い配位能力を有する部分であり、該窒素原子の含有量に応じて本発明の金属イオン捕捉剤が捕捉できる金属イオンの量を調製でき、該窒素原子の含有量が多い程、捕捉できる金属イオンの量が多くなる。本発明の金属捕捉剤が捕捉できる金属イオンの捕捉量としては、最大、金属イオン捕捉剤中の窒素原子4モルに対し、金属イオン1モルの捕捉が可能である。
【0084】
本発明の金属イオン捕捉剤は、ナノメートルオーダーの繊維状複合体が会合した三次元網目構造を有することから、その内部には空隙が多く、かつ繊維状複合体の表面積が非常に大きい。このため、本発明の金属イオン捕捉剤は金属イオン水溶液と接触させた際、金属イオンがシリカの全表面と接触することができ、多くの金属イオンを速やかに捕捉することが可能となる。更に、本発明の金属イオン捕捉剤は、成形が容易であることから、カラム状や板状への加工により、ナノフィルター形式の金属イオン捕捉剤として用いることができる。
【0085】
また、本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマーは、溶液のpHの変化より、プロトン化されたカチオン状態、または脱プロトンのアミン状態に変化できる。このため、本発明の金属イオン捕捉剤は、金属イオンを選択的に捕捉することが可能である。
【0086】
さらに、本発明の金属イオン捕捉剤においては、シリカの有する耐酸性、耐酸化性、耐有機溶剤性に優れ、繊維状複合体中の直鎖状ポリエチレンイミン骨格を有するポリマーは該繊維状複合体から溶出されることができない。従って、金属と配位する活性部が繊維状複合体中に安定に固定化された状態を保持できる。
【0087】
本発明の金属イオン捕捉剤は、有機ポリマーに配位子を結合した従来のイオン交換樹脂の使用条件と同様なプロセスで使用できる。また、有機ポリマー系イオン交換樹脂は耐酸化性、耐酸性が弱く、そのような条件下では使用できない場合があるが、本発明の金属イオン捕捉剤はシリカの耐酸化性、耐酸性が高いので、そのような環境でも使用することができる。即ち、pH<1の環境でも十分安定に使用できる。
【0088】
本発明での捕捉剤はシリカが支持体として機能するため、水中使用は勿論、有機溶剤が含まれた水中、または有機溶剤中でも使用することができる。
【0089】
[金属イオン分離方法]
本発明の金属イオン捕捉剤において、金属イオンを取り込むのは繊維状複合体中に含まれたポリエチレンイミン骨格を有するポリマーの金属イオンに対する強い配位能力によるものである。この際、シリカはその配位子を支える支持体として機能する。
【0090】
本発明の金属イオン捕捉剤が捕捉可能な金属イオンとしては、アルカリ金属イオン、アルカリ土類金属イオン、遷移金属イオン、ランタン金属イオン、ポリオキソメタレートイオンなどが挙げられる。
【0091】
本発明での捕捉剤が金属イオンを捕捉する機構は、シリカ中のポリエチレンイミンが金属イオンに配位することにより、金属イオンを水液相から、シリカ中に取り込まれ、そのままシリカ中に固定化される。これは、イオン結合等の過程と異なり、金属がカチオンでも、またはアニオンでも、ポリエチレンイミンの配位により、捕捉されることになる。従って、本発明の金属イオン捕捉剤は、遷移金属イオンの捕捉に特に好適に用いることができる。遷移金属イオンとして、それが金属カチオン(Mn+)であっても、または遷移金属が酸素との結合からなる酸根アニオン(MOxn−)、またはハロゲン類結合からなるアニオン(MLxn−)であっても、本捕捉剤はそれらの捕捉、固定、除去、回収に好適に用いることができる。
【0092】
遷移金属イオンとしては、下記の遷移金属のカチオン(Mn+)、例えば、Cu,Zn,Co,Ni,Cr,Mn,Mo,Fe,Ru,W,Rh,Cd,Os,Hg,Cd,Ir,Ag,Pt,Sn,Pb,Gaの一価、二価、三価または四価のカチオンなどが挙げられる。これら金属カチオンの捕捉においては、その金属カチオンの対アニオンは、Cl,NO3,SO4、またはポリオキソメタレート類アニオン、あるいはカルボン酸類の有機アニオンのいずれであってもよい。
【0093】
また、下記の遷移金属アニオン(MOxn−)、例えば、MnO4,MoO4,ReO4,WO3,RuO4,CoO4,CrO4,VO3,NiO4のアニオンが挙げられる。
【0094】
本発明での捕捉剤は、ポリオキソメタレート類の金属化合物にも好適に用いることができるが、具体的には、遷移金属カチオンと組み合わせられたモリブデン酸塩、タングステン酸塩、バナジン酸塩類である。
【0095】
さらに、下記の金属が含まれたアニオン(MLxn−)、例えば、AuCl4,PtCl6,RhCl4,RoF6,NiF6,CuF6,RuCl6,In2Cl6の如く、金属がハロゲンに配位されてからなるアニオンの捕捉、濃縮、回収または除去などにも好適に用いることができる。
【0096】
アルカリ金属としては、例えば、リチウム、ナトリウム、カリウム、セシウムなどが挙げられる。この場合、媒体の使用条件としては、pHが5〜14の範囲であることが好ましく、pHが7〜9の範囲であれば更に好ましい。また、アルカリ金属イオンの捕捉においては、アルカリ金属イオンがカチオンである場合に、そのアルカリ金属カチオンの対アニオンが、Cl,NO3,SO4,PO4,ClO4,PF6,BF4などである系にも好ましく用いることができる。
【0097】
アルカリ土類金属イオンとしては、例えば、バリウム、マグネシウム、カルシウムなどが挙げられる。
【0098】
ランタン金属イオンとしては、例えば、La,Eu,Gd,Yb,Euなど3価のカチオンが挙げられる。
【0099】
本発明の金属イオン捕捉剤は、粉末、粒子、多面体、シリンダーなど様々な形状で使用することができる。このため、本発明の金属イオン捕捉剤を使用して金属イオンを捕捉する場合には、これらのシリカ捕捉剤をバッチ法またはフロー法で用いることができる。
【0100】
バッチ法で捕捉する際は、シリカ粉末または粒子を金属のイオンの水液に加える方法や、金属イオンの水液をシリカ粉末に加える方法などにより、好適に金属イオンを捕捉できる。
【0101】
バッチ法で金属イオンを捕捉する際は、混合系を10分から24時間までシェイキングすることで行う。シェイキング時間は、金属種類により大きく異なるが、カチオン類金属イオンでは、数時間であれば好適に捕捉することができる。
【0102】
また、フロー法の場合は、シリカ粉末、粒子などを湿式でガラスカラムに充填し、そのカラムに金属イオン水液を流すことで、好適に金属イオンを捕捉できる。特に、カチオン性金属イオンには、フロー法が好適である。
【0103】
本発明の金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格を有するポリマー由来の窒素の含有量は、金属イオンに配位する活性点であるため、窒素原子が配位に全部使われたら、金属イオン捕捉剤は飽和状態となる。この際には、金属イオン捕捉剤を取り出し、これを塩酸水溶液または硝酸水溶液で洗浄し、金属イオンを容易に脱配位させることができる。即ち、捕捉剤はこれで再生される。この再生に用いる塩酸または硝酸水溶液の濃度は、1〜7Mであればよく、好ましくは3〜5Mである。
【0104】
酸で捕捉された金属イオンを金属イオン捕捉剤から脱離させた後、金属イオン捕捉剤を蒸留水、0.001Mのアルカリ水溶液や蒸留水で洗浄した後、再び、金属イオンの捕捉に用いることができる。
【実施例】
【0105】
以下、実施例によって本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。特に断らない限り、「%」は「質量%」を表す。
【0106】
[X線回折法による捕捉剤の分析]
単離乾燥した試料を測定試料用ホルダーにのせ、それを株式会社リガク製広角X線回折装置「Rint−Ultma」にセットし、Cu/Kα線、40kV/30mA、スキャンスピード1.0°/分、走査範囲10〜40°の条件で測定を行った。
【0107】
[走査電子顕微鏡による捕捉剤の形状分析]
単離乾燥した試料をガラススライドに乗せ、それをキーエンス製表面観察装置VE−7800にて観察した。
【0108】
[透過電子顕微鏡による捕捉剤の観察]
単離乾燥した試料を炭素蒸着された銅グリッドに乗せ、それを日本電子製JEM-200CX透過型電子顕微鏡にて観察した。
【0109】
(作製例1)
<線状のポリエチレンイミン(L−PEI)の合成>
ポリエチルオキサゾリン(数平均分子量500000,平均重合度5000,Aldrich社製)5gを、5Mの塩酸水溶液20mLに溶解させた。その溶液をオイルバスにて90℃に加熱し、その温度で10時間攪拌した。反応液にアセトン50mLを加え、ポリマーを完全に沈殿させ、それを濾過し、メタノールで3回洗浄し、白色のポリエチレンイミンの粉末を得た。得られた粉末を1H−NMR(重水)にて同定したところ、ポリエチルオキサゾリンの側鎖エチル基に由来したピーク1.2ppm(CH3)と2.3ppm(CH2)が完全に消失していることが確認された。即ち、ポリエチルオキサゾリンが完全に加水分解され、ポリエチレンイミンに変換されたことが示された。
【0110】
その粉末を5mLの蒸留水に溶解し、攪拌しながら、その溶液に15%のアンモニア水50mLを滴下した。その混合液を一晩放置した後、沈殿したポリマー結晶粉末を濾過し、その結晶粉末を冷水で3回洗浄した。洗浄後の結晶粉末をデシケータ中で室温乾燥し、線状のポリエチレンイミン(L−PEI)を得た。収量は4.2g(結晶水含有)であった。ポリオキサゾリンの加水分解により得られるポリエチレンイミンは、側鎖だけが反応し、主鎖には変化がない。従って、L−PEIの重合度は加水分解前の5000と同様である。
【0111】
<線状ポリエチレンイミン系からの捕捉剤の作製>
合成例1で得られたL−PEI粉末を蒸留水中に分散させ、その分散液をオイルバスにて、90℃に加熱し、濃度が2%となる完全透明な水溶液を得た。その水溶液を室温に放置し、自然に室温までに冷やし、不透明なL−PEIヒドロゲルを得た。得られたヒドロゲルは、剪断力を加えると変形を生じるが、概ねの形状を保持できるアイスクリーム状態のヒドロゲルであった。
【0112】
得られたヒドロゲルにつき、X線回折測定を行った結果、20.7°、27.6°、28.4°に散乱強度のピークが表れることが確認された。また、熱量分析装置による吸熱状態変化の測定結果により、64.5℃で吸熱のピークが確認された。これら測定結果より、ヒドロゲル中におけるL−PEIの結晶の存在が確認された。
【0113】
これで得られたヒドロゲル20mL中に、テトラメトキシシラン(TMSO)とエタノールの1/1(体積比)の混合液を20mL加え、アイスクリーム状態のものを軽く一分間かき混ぜた後、そのまま40分放置した。その後、過剰なアセトンで洗浄し、それを円心分離器にて3回洗浄を行った。固形物を回収し、室温で乾燥し、白色の金属イオン捕捉剤を得た。捕捉剤のX線回折測定から、L−PEIの結晶由来のピークが20.5°、27.2°、28.2°に表れた。
【0114】
得られた金属イオン捕捉剤を走査型顕微鏡により観察したところ、図1に示したように繊維状複合体の三次元網目構造を有するものであった。
【0115】
捕捉剤の元素分析から、窒素の含有量は8.5%であることが確認された。このことから、1グラムの該捕捉剤中、配位子である窒素のミリモル数は、6.07と換算された。これは、メソポーラス系シリカ中の配位子導入が通常2ミリモル以下であることに比べると、極めて大きいものであった。
【0116】
(実施例1)
<銅イオンの捕捉>
上記により得られた金属イオン捕捉剤50mgを秤取り、それに10mLの1mM硝酸銅水溶液を加えた。混合物中の白色の金属イオン捕捉剤は、一瞬で青色に変わった。その代わり、液部はほぼ無色に近い状態であった。これにより銅イオンが金属イオン捕捉剤に迅速に取り込まれることが確認された。このまま、2時間静置させた後、液部を取り出し、吸収スペクトル測定を行ったが、残存銅イオンは認められる濃度ではないことが判断された。即ち、銅イオンはほぼ完全に金属イオン捕捉剤に捕捉された。
濾過により、青く染まった金属イオン捕捉剤を回収し、それを2Mの硝酸水溶液で洗浄したところ、水液は青色になることが確認された。これより、金属イオン捕捉剤に捕捉された銅イオンは簡単に回収されることが示された。
【0117】
(実施例2)
<パラジウムイオンの捕捉と還元>
上記金属イオン捕捉剤20mgを秤取り、それを4mLの0.5Mパラジウム硝酸水溶液に加え、そのまま、2時間静置させた。混合物を濾過し、金属イオン捕捉剤を蒸留水で洗浄した後、それを3mLのNaBH4水溶液(重量濃度2%)中に加え、30分間シェイクした。混合物を濾過し、それを蒸留水、アセトン順で洗浄した。白色の金属イオン捕捉剤は黒色に変化した。これにより、金属イオン捕捉剤に捕捉されたパラジウムイオンが還元剤より、パラジウム金属に還元されたことが示された。
該金属イオン捕捉剤をXRDで観測した結果、金属パラジウム結晶に由来のピークが36,43,66°に顕著に現れた。また、TEM観察から(図2)、シリカ繊維中にパラジウムの多量のナノ粒子が固定されていることが確認された。これより、捕捉剤に捕捉された金属イオンを金属状態で固定化できることが示された。
【図面の簡単な説明】
【0118】
【図1】本発明の作製例1における金属イオン捕捉剤の走査型電子顕微鏡写真である。
【図2】本発明の実施例3におけるパラジウム金属結晶が固定化された金属イオン捕捉剤の透過型電子顕微鏡写真である。
【特許請求の範囲】
【請求項1】
直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤。
【請求項2】
前記繊維状複合体同士の会合が三次元網目状の会合である請求項1に記載の金属イオン捕捉剤。
【請求項3】
前記直鎖状ポリエチレンイミン骨格を有するポリマーが、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーからなるものである請求項1〜3のいずれかに記載の金属イオン捕捉剤。
【請求項4】
前記直鎖状ポリエチレンイミン骨格を有するポリマー中のポリエチレンイミン骨格の割合が、40モル%以上である請求項1〜4のいずれかに記載の金属イオン捕捉剤。
【請求項5】
シリカの含有量が40〜80質量%の範囲にある請求項1〜5のいずれかに記載の金属イオン捕捉剤。
【請求項6】
金属イオンを含有する溶液と、請求項1〜6のいずれかに記載の金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることを特徴とする金属イオンの捕捉方法。
【請求項7】
前記金属イオンが、アルカリ金属系イオン、アルカリ土類金属イオン、遷移金属系イオン、ポリオキソメタレート類、ランタン系金属イオンから選ばれる少なくとも一種の金属イオンである請求項7に記載の金属イオンの捕捉方法。
【請求項8】
請求項7に記載の方法により金属イオン捕捉剤に捕捉された金属イオンを酸性処理により金属捕捉剤から分離する金属イオン分離方法。
【請求項1】
直鎖状ポリエチレンイミン骨格を有するポリマーの結晶をシリカが被覆した、太さが15〜100nmの範囲にある繊維状複合体同士が会合してなる金属イオン捕捉剤。
【請求項2】
前記繊維状複合体同士の会合が三次元網目状の会合である請求項1に記載の金属イオン捕捉剤。
【請求項3】
前記直鎖状ポリエチレンイミン骨格を有するポリマーが、直鎖状ポリエチレンイミンブロックと他のポリマーブロックとのブロックコポリマーからなるものである請求項1〜3のいずれかに記載の金属イオン捕捉剤。
【請求項4】
前記直鎖状ポリエチレンイミン骨格を有するポリマー中のポリエチレンイミン骨格の割合が、40モル%以上である請求項1〜4のいずれかに記載の金属イオン捕捉剤。
【請求項5】
シリカの含有量が40〜80質量%の範囲にある請求項1〜5のいずれかに記載の金属イオン捕捉剤。
【請求項6】
金属イオンを含有する溶液と、請求項1〜6のいずれかに記載の金属イオン捕捉剤とを接触させて、前記溶液中に含まれる金属イオンを、前記金属イオン捕捉剤中の直鎖状ポリエチレンイミン骨格に配位させることを特徴とする金属イオンの捕捉方法。
【請求項7】
前記金属イオンが、アルカリ金属系イオン、アルカリ土類金属イオン、遷移金属系イオン、ポリオキソメタレート類、ランタン系金属イオンから選ばれる少なくとも一種の金属イオンである請求項7に記載の金属イオンの捕捉方法。
【請求項8】
請求項7に記載の方法により金属イオン捕捉剤に捕捉された金属イオンを酸性処理により金属捕捉剤から分離する金属イオン分離方法。
【図1】


【図2】




【図2】


【公開番号】特開2006−8732(P2006−8732A)
【公開日】平成18年1月12日(2006.1.12)
【国際特許分類】
【出願番号】特願2004−183578(P2004−183578)
【出願日】平成16年6月22日(2004.6.22)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
【公開日】平成18年1月12日(2006.1.12)
【国際特許分類】
【出願日】平成16年6月22日(2004.6.22)
【出願人】(000173751)財団法人川村理化学研究所 (206)
【Fターム(参考)】
[ Back to top ]

