金属含有ブロック共重合体及びその製造方法
【課題】ブロック共重合体に多量の金属をナノレベルでかつ規則的に含有した金属含有ブロック共重合体を製造する。
【解決手段】金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、当該金属の化合物である金属化合物と、をブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒に溶解した混合溶液を調製し、それから溶媒を除去する。当該金属がポリマーブロックA相に直接配位結合して凝集するのを、当該金属と溶媒との溶媒和によって確実に防止できる。
【解決手段】金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、当該金属の化合物である金属化合物と、をブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒に溶解した混合溶液を調製し、それから溶媒を除去する。当該金属がポリマーブロックA相に直接配位結合して凝集するのを、当該金属と溶媒との溶媒和によって確実に防止できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、金属がナノメータ単位のサイズで規則的に含有された金属含有ブロック共重合体と、その製造方法に関するものである。
【背景技術】
【0002】
近年、ポリマーやガラスなどのマトリックス中に金属をナノレベルで含む複合材料が開発され、その特異な光学特性や電気的、磁気的特性を利用した機能材料への応用、あるいは触媒や医薬への応用が期待されている。例えば、光の波長ほどのサイズの金属微粒子をマトリックス中に規則的に含ませることで表面プラズモン共鳴(SPR)が生じるが、これを利用したセンサー、導波路、光デバイスなどが研究されている。
【0003】
Phys.Rev.Lett.95(2005)237401には、銀又は金を直径数100nmのナノリングに加工し、これにギャップ間隔10nm程度のスリットを設けたものを無数に集積化することで、可視光全体をカバーする広い周波数領域でSPRによって電流が流れ、人工的な磁性を発現できることが記載されている。したがって、このような微細金属集積体をマトリックス中につくり込んだメタマテリアルを用いれば、光を自在に曲げることが可能となり、負の屈折率も実現できる。
【0004】
ポリマーやガラスなどのマトリックス中に金属をナノレベルで含む複合材料を製造する一つの例として、PVDあるいはCVDなどにより製造された金属ナノ粒子を高分子溶液あるいは溶融高分子と混合する方法が知られている。しかしこの方法では、金属ナノ粒子がマトリックス内に分散される時に非可逆的な凝集物を形成し易く、得られたものは光散乱が生じるなど光学機能材料としては満足し難いものであった。
【0005】
そこで特開2002−179931号公報には、AgBF4塩などの金属前駆体を高分子溶液中に溶解して分子レベルで分散させ、その後に光を照射して金属前駆体を還元することで、金属銀をナノレベルで高分子中に固定する方法が提案されている。この製造方法によれば、高分子マトリックス中に金属前駆体を凝集することなくナノレベルで分散させることができるため、還元後の金属も高分子マトリックス中にナノレベルで分散させることができる。
【0006】
しかしながらこの製造方法では、高分子マトリックス中に金属粒子が均一に分散した複合材料が得られるのみであり、高分子マトリックス中に金属粒子を規則的に配列させることはできない。したがって、メタマテリアルやフォトニッククリスタルなどの金属含有ナノ構造体としての利用分野が規制されるという不具合があった。
【0007】
一方、Macromolecules,2008,41(7),2577-2583には、ポリスチレンブロックとポリビニルピリジンブロックとからなるブロック共重合体中に、CdCl2をナノレベルで規則的に配置した金属含有ブロック共重合体が記載されている。その製造方法は、アニオン重合によって得られたブロック共重合体をテトラヒドロフラン/エタノール(8:2)の混合溶媒に溶解した溶液にCdCl2を混合し、それをフィルム状にキャストした後にアニールするものである。
【0008】
この金属含有ブロック共重合体によれば、CdCl2がポリビニルピリジンブロックのピリジン単位に配位結合することでナノレベルで固定化されている。したがってCdCl2はブロック共重合体の内部にラメラ構造など規則的に配置されることとなり、光学機能材料としての利用分野が格段に拡がる。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2002−179931号公報
【非特許文献】
【0010】
【非特許文献1】Phys.Rev.Lett.95(2005)237401
【非特許文献2】Macromolecules,2008,41(7),2577-2583
【発明の概要】
【発明が解決しようとする課題】
【0011】
ところが非特許文献2には、ポリビニルピリジンブロックのピリジン単位1モルに対して0.2モルを超えるCdCl2を混合した場合には、ブロック共重合体とは均一に配位結合せずに沈殿するCdCl2が存在したことが記載されている。すなわち、ピリジン単位1モルに対して0.2モル(4.4体積%)を超えるCdCl2をナノレベルで構造制御しながら複合化することは困難であった。したがって得られる金属含有ブロック共重合体は、金属含有量が低いがために光学特性その他物理特性などの向上には限界があり、利用分野の拡大にも限度があった。
【0012】
本発明はこのような事情に鑑みてなされたものであり、ブロック共重合体に多量の金属をナノレベルでかつ規則的に含有させることを解決すべき課題とする。
【課題を解決するための手段】
【0013】
上記課題を解決する本発明の金属含有ブロック共重合体の製造方法の特徴は、金属が配位結合可能なポリマーブロックA相と金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、当該金属の化合物である金属化合物と、をブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒に溶解した混合溶液を調製する溶解工程と、混合溶液から溶媒を除去する除去工程と、からなることにある。
【0014】
混合溶液には、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で含まれていることが望ましい。又は金属化合物が4.4体積%を超え33体積%以下の量で含まれていることが望ましい。
【0015】
溶解工程は、ブロック共重合体を溶媒に溶解した溶液と、金属化合物を溶媒に溶解した溶液とを混合して行うことが望ましい。また除去工程は、混合溶液から溶媒を10ml/秒以下の速度で除去することが望ましい。さらに、除去工程前に膜厚を調整する塗布工程、または、除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程の少なくともいずれかを行うことが望ましい。
【0016】
そして本発明の金属含有ブロック共重合体の特徴は、本発明の製造方法により製造された金属含有ブロック共重合体であって、金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、ブロック共重合体のポリマーブロックA相に選択的に配位結合してなる当該金属の化合物である金属化合物と、からなり、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で、又は金属化合物として4.4体積%を超え33体積%以下の量で配位結合していることにある。
【発明の効果】
【0017】
本発明の製造方法によれば、ブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒を用いている。したがって金属化合物は先ず溶媒分子と配位結合し溶媒和の状態となるため、溶解工程後の混合溶液中ではポリマーブロックA相と配位結合するのが規制されている。そのため金属化合物の量が多くても均一な混合溶液となり凝集や沈殿が生じない。
【0018】
その後除去工程を行うと、先ず混合溶液中の溶媒分子が離脱し、その後に金属化合物に配位結合している溶媒分子が離脱すると考えられる。この時、金属化合物から配位結合している溶媒分子の1個が離脱すると、その金属化合物はポリマーブロックA相と配位結合して固定化される。したがってポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モル以下の場合には、金属化合物中の金属原子はそれぞれポリマーブロックA相の配位結合可能な単位と配位結合し、金属がナノメータ単位のサイズで含有されることとなる。
【0019】
またポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モルを超える場合には、過剰の金属化合物は静電相互作用によって既に配位結合している金属化合物に近接して保持されると考えられ、凝集や沈殿が生じることが無い。
【0020】
したがって金属化合物はポリマーブロックA相にのみ含まれ、ブロック共重合体はポリマーブロックA相とポリマーブロックB相とが規則的に配列したナノ相分離構造をなしているので、金属が規則的に配列したナノ相分離構造をなす金属含有ブロック共重合体が得られる。
【0021】
すなわち本発明の製造方法によれば、ブロック共重合体に多量の金属をナノレベルでかつ規則的に含有させることができる。したがって得られた本発明の金属含有ブロック共重合体は、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で配位結合し、しかも金属化合物はポリマーブロックA相のみに含まれているので、金属がナノレベルでかつ規則的に含まれている。したがってメタマテリアルとしての利用分野が格段に拡がる。
【図面の簡単な説明】
【0022】
【図1】本発明の一実施例において、金属塩が溶媒和した状態を示す化学式である。
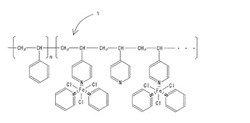
【図2】本発明の一実施例における混合溶液の組成を示す化学式である。
【図3】本発明の一実施例における除去工程の途中の段階を示す化学式である。
【図4】本発明の一実施例で製造された金属含有ブロック共重合体を示す化学式である。
【図5】本発明の一実施例においてブランクとして製造されたFeCl3を含有しないブロック共重合体の構造を示すTEM写真である。
【図6】本発明の一実施例で製造されたFeCl3を0.5モル(11.2体積%)含有する金属含有ブロック共重合体の構造を示すTEM写真である。
【図7】本発明の実施例2で製造されFeCl3を2.0モル(33体積%)含有する金属含有ブロック共重合体の構造を示すTEM写真である。
【図8】ブランクであるブロック共重合体と本発明の一実施例で製造された金属含有ブロック共重合体のDSCチャートである。
【図9】ブランクであるブロック共重合体と本発明の一実施例で製造された金属含有ブロック共重合体のFT−IRチャートである。
【図10】本発明の製造方法における反応機構を模式的に示す説明図である。
【図11】実施例1及び比較例における除去工程後の金属含有ブロック共重合体の状態を示す説明図である。
【発明を実施するための形態】
【0023】
本発明の製造方法に用いられるブロック共重合体は、金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含む。ポリマーブロックA相,B相以外の他のポリマーブロックを含んでもよい。このブロック共重合体は、段階的重合法、カップリング法、リビングアニオン重合、リビングカチオン重合、リビングラジカル重合(RAFT重合など)など、公知の重合法によって製造することができる。
【0024】
ここでRAFT重合とは、可逆的付加開裂連鎖移動(Reversible Addition-Fragmentation Chain Transfer)重合であり、可逆的付加開裂連鎖移動剤(Reversible Addition-Fragmentation Chain Transfer剤、以下、「RAFT剤」と略す。)を用いることを特徴とする重合方法である。RAFT剤としては、ジチオ安息香酸クミル、S-1-ドデシル-S'(a,a"-ジメチル-a"-酢酸)トリチオカーボネイト、ジチオ安息香酸2-シアノプロピ2-イルなどが挙げられる。
【0025】
ポリマーブロックA相は金属が配位結合可能なポリマーであり、配位能を有する酸素原子や窒素原子を含むモノマーが重合したものが望ましい。例えばポリビニルピリジン、ポリビニルピロリドン、ポリビニルエーテル、ポリエチレングリコール、ポリプロピレンオキシド、ポリアクリル酸、ポリアクリル酸エステル、ポリメタクリル酸、ポリメタクリル酸エステル、ポリ酢酸ビニル、ポリビニルフェノール、ポリエチレンテレフタレート、ポリアミド、ポリビニルアルコール、ポリカーボネート、ポリオキシメチレンなどが例示される。
【0026】
ポリマーブロックB相は当該金属が配位結合しないポリマーであり、ポリマーブロックA相とブロック化できるものであれば特に制限されない。例えばポリスチレン、ポリイソプレン、ポリブタジエン、ポリフッ化ビニリデン、ポリ塩化ビニリデン、ポリジメチルシロキサン、ポリイソブチレン、ポリエチレン、ポリプロピレン、ポリアルケンなどが例示される。金属が配位結合することで金属含有ブロック共重合体の硬度が増大する場合には、ポリマーブロックB相には軟質のポリマーを用いることも好ましい。
【0027】
ポリマーブロックA相とポリマーブロックB相との構成比率、それぞれの分子量又はブロック共重合体の分子量は特に制限されないが、可視光を利用する光学機能材料として用いる場合には、ブロック共重合体の構造周期が100nm〜250nm(可視光波長の1/4〜1/3倍)程度とするのが好ましい。
【0028】
本発明に用いられる金属は、少なくともポリマーブロックA相を構成する配位結合可能な単位に配位結合可能なものである。一般的に金属は電子が失われた酸化状態で存在しやすく、それは配位結合可能なものであるので、ほとんどの金属や合金あるいは金属間化合物を用いることができる。光学機能材料として用いる場合には、例えばCu、Ag、Auなどを含むことが好ましい。
【0029】
金属化合物としては、当該金属のアセチルアセトン塩、臭化物、塩化物、ヨウ化物、酸化物、硝酸塩、硫酸塩、炭酸塩、酢酸塩、リン酸塩、水素化物など、後述の溶媒に可溶のものが用いられる。金属化合物の混合量は、例えばFeCl3の場合には、ポリマーブロックA相の配位結合可能な単位1モルに対してFeとして 0.2モルを超え 2.0モル以下の範囲、体積分率としては4.8体積%〜33体積%であることが望ましい。なお臭化亜鉛(ZnBr2)の場合には、0.2〜2.0モルは4.5体積%〜32体積%に相当し、臭化銅(CuBr)の場合には、0.2〜2.0モルは2.6体積%〜21体積%に相当する。
【0030】
本発明に用いる溶媒は、ブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能なものであって、除去工程で除去できるものであればよく、特には水、アルコール、ピリジン、ピロリドン、アミン類、アンモニア水などが例示される。これらの溶媒単品でもよいし、複数種の溶媒が混合された混合溶媒を用いてもよい。溶媒の混合量は、ブロック共重合体及び金属化合物が完全に溶解する量以上とする。
【0031】
溶解工程では、ブロック共重合体及び金属化合物が溶媒に溶解した混合溶液を調製する。このとき、金属化合物の金属が溶媒と配位結合するより先にポリマーブロックA相と配位結合すると、その金属が他のポリマーブロックA相とも配位結合して架橋状態となり、凝集が生じる場合がある。そこで、ブロック共重合体を溶媒に予め溶解した溶液と、金属化合物を溶媒に予め溶解した溶液とを混合することが望ましい。このようにすることで、金属化合物と溶媒とを確実に配位結合させることができ、凝集が生じるのを確実に防止することができる。
【0032】
なお、金属がポリマーブロックA相に配位する速度と、金属が溶媒に配位する速度とが異なる場合には、溶媒に配位する速度がポリマーブロックA相に配位する速度より大きくなるように、溶媒又はポリマーブロックA相の種類を選択するのが望ましい。
【0033】
除去工程では、先ず混合溶液中の溶媒分子が離脱し、その後に金属化合物に配位結合している溶媒分子が離脱すると考えられる。この時、金属化合物から配位結合している溶媒分子の1個が離脱すると、その金属化合物はポリマーブロックA相と配位結合して固定化される。したがってポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モル以下の場合には、金属化合物の金属原子はそれぞれポリマーブロックA相の配位結合可能な単位と配位結合し、金属がナノメータ単位のサイズで含有されることとなる。
【0034】
この除去工程は、混合溶液を加熱して溶媒を蒸発させる一般的な乾燥方法で行うことができる。また減圧雰囲気下で乾燥させることも好ましい。しかし除去工程を急激に行うと、溶媒和した金属化合物から溶媒が離脱する速度と混合溶液中の溶媒が蒸発する速度とが近くなり、ポリマーブロックA相が金属化合物によって架橋されて凝集する場合がある。したがって溶媒の除去速度はできるだけ小さくすることが望ましく、10ml/秒以下の速度で除去することが好ましい。
【0035】
得られた金属含有ブロック共重合体は、そのままでも構わないが、除去工程前に膜厚を調整する塗布工程、または、除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程との少なくともいずれかを行うことが望ましい。バーコーター、スピンコーターなどを用いて、適宜、混合溶液の濃度を調整して塗布工程を行うことにより膜厚を調整することができる。またアニール工程を行うことで、金属含有ブロック共重合体のナノ相分離構造をより均一化することができる。加熱温度は、金属を含まないポリマーブロックB相のガラス転移温度以上とすることが好ましい。また還元工程を行うことで、金属化合物を金属へ還元することができ利用分野の自由度がさらに高まる。
【0036】
以下、実施例により本発明を具体的に説明する。
【実施例1】
【0037】
<ブロック共重合体の調製>
スチレンモノマー中に[化1]に示すRAFT剤{S-1-ドデシル-S'(a,a"-ジメチル-a"-酢酸)トリチオカーボネイト}を溶解し、130℃で6時間かけて重合してポリスチレンブロックを合成した。次いで4-ビニルピリジンモノマ−を加えて70℃で1時間重合し、[化2]に示すブロック共重合体を合成した。
【0038】
【化1】

【0039】
【化2】

このブロック共重合体は、ポリビニルピリジンブロック(以下、ポリマーブロックA相という)と、ポリスチレンブロック(以下、ポリマーブロックB相という)と、から構成されている。数平均分子量は48,000であり、分子量分布は1.30であり、ポリマーブロックA相の体積分率は0.60である。
【0040】
<溶解工程>
得られたブロック共重合体溶液にピリジンを追加し、ブロック共重合体の濃度が4質量%のポリマー溶液を調製した。また市販のFeCl3をピリジンに溶解し、FeCl3の濃度が2質量%の金属塩溶液を調製した。そしてポリマー溶液と金属塩溶液を体積比で1対1に混合し、混合溶液を調製した。混合溶液は、凝集や沈殿が生じることなく均一な溶液状態であった。
【0041】
この混合溶液は、質量比でブロック共重合体:FeCl3=3:1であり、ポリマーブロックA相のピリジン単位1モルに対して0.5モルのFeCl3が含まれている。FeCl3の体積分率は11.2%である。
【0042】
<除去工程>
混合溶液をテフロン(商標)製容器へ移し、50 ℃で36時間保持してピリジンを蒸発させた。蒸発速度は5μl/分である。この除去工程後のブロック共重合体フィルムは、図11に示すように凝集や分離の無い均一な茶色透明体であった。この除去工程では、以下のような反応が生じたと推察される。
【0043】
FeCl3のピリジン溶液では、FeCl3はFe原子が3分子のピリジンと配位結合して図1に示す溶媒和状態となっている。これをポリマー溶液と混合しても、その状態は変化せず、図2に示すようにブロック共重合体1とFeCl3の溶媒和物2とがピリジン3中に溶解した状態である。
【0044】
FeCl3と配位結合しているピリジンは、溶媒のピリジンより蒸発しにくい。したがってこの溶液から徐々にピリジンを蒸発させると、先ず溶媒のピリジンが蒸発する。溶媒のピリジンが少なくなるとFeCl3の溶媒和物2に配位結合していたピリジンも蒸発する。しかし3個のピリジンのうち1個が離脱すると、図3に示すように、ピリジンが離脱したFe原子はブロック共重合体1におけるポリマーブロックA相のピリジン単位と配位結合する。その後、Feに配位結合していた残りのピリジンが離脱することで、図4に示すように凝集や分離の無い均一な金属含有ブロック共重合体が生成する。
【0045】
<アニール工程>
次いで160℃で60時間保持し、均一なフィルム状の金属含有ブロック共重合体を得た。
[ブランク]
実施例1で製造されたブロック共重合体にピリジンを追加し、ブロック共重合体の濃度が4質量%のポリマー溶液を調製した。このポリマー溶液のみをテフロン(商標)製容器へ移し、実施例1と同様にしてピリジンを蒸発させるとともにアニールし、ブランクとしてFeCl3を含まないブロック共重合体のフィルムを得た。
【0046】
<TEM観察>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、加速電圧:100kVの条件にてTEM観察した。その結果を図5、図6に示す。なおブランクのブロック共重合体のフィルムは、沃素にて染色している。また図7に、後述の実施例2に係るFeCl3が2.0モル(33体積%)含まれた金属含有ブロック共重合体のフィルムのTEM写真を示す。
【0047】
図5には、薄い灰色の海中に濃い灰色の部分が島状に存在し、濃い灰色の部分がシリンダ構造のナノ相分離構造をなしていることが示されている。一方、図6には、薄い灰色の部分と濃い灰色の部分が層状に形成されたラメラ構造のナノ相分離構造であることが示されている。また図7には、薄い灰色の部分がシリンダ構造のナノ相分離構造であることが示されている。
【0048】
すなわちFeCl3を含有することによって、さらにFeCl3の含有量が多くなるにつれて、図5、図6、図7へと変化するモルフォロジー転移が生じたことが観察された。なお図6及び図7に係る金属含有ブロック共重合体は、染色しなくともラメラ構造を明瞭に観察することができた。
【0049】
<DSC測定>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、昇温速度:10℃/分、温度範囲:20〜250℃の条件にてDSC測定を行った。結果を図8に示す。図8において108〜109℃近傍の吸熱ピークはポリマーブロックB相に起因し、152℃近傍の吸熱ピークはポリマーブロックA相に起因している。金属含有ブロック共重合体からはポリマーブロックA相に起因する吸熱ピークが消失し、これはFe原子がポリマーブロックA相にのみ選択的に分散したことを示している。
【0050】
<FT−IR測定>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、それぞれピリジンに溶解しKBr板にそれぞれ塗布して、120℃で真空乾燥した。これらを大気圧下、検出器:TGS、分解能:2cm-1の条件にてFT−IR測定を行った。結果を図9に示す。なお実施例1の金属含有ブロック共重合体のフィルムは、ピリジンに完全に溶解した。これはフィルム中に不可逆的な凝集物などが存在しないことを意味している。
【0051】
図9に示すように、金属含有ブロック共重合体には1613cm-1に吸収ピークが現れ、これはポリマーブロックA相のピリジン単位の不対電子にFeが配位結合していることを示している。
【0052】
<考察>
したがってFeCl3を含有することで、TEMにおいてモルフォロジー転移が生じたのが観察されたのは、図10に模式的に示すように、FeCl3のFe原子がポリマーブロックA相にのみ配位結合したことで、ポリマーブロックA相の体積が増加したことに起因すると考えられる。すなわちブランクのブロック共重合体1では、図5にも示したように、ポリマーブロックB相10の海の中にポリマーブロックA相11がシリンダ構造で存在している。そこへFeCl3が添加されると、Fe原子がポリマーブロックA相11に選択的に配位結合する。するとポリマーブロックA相11の体積が増加して、隣接するポリマーブロックA相11どうしが連結されることでラメラ構造となったと考えられる。
【0053】
なお小角X線散乱(SAXS)による構造観察でもラメラ構造が確認されたので、実施例1の金属含有ブロック共重合体はTEMの視野以外の部分も図6と同様のナノ相分離構造となっていることが明らかである。
【0054】
すなわち実施例1で得られた金属含有ブロック共重合体は、ブロック共重合体のポリマーブロックA相のピリジン単位にFeCl3が選択的に配位結合してなり、ラメラ構造のナノ相分離構造をなしている。しかもポリマーブロックA相のピリジン単位1モルに対して、0.5モルという多量でFeCl3が含まれているにも関わらず、凝集や分離などの不具合なく均一な組成の金属含有ブロック共重合体であった。
【実施例2】
【0055】
溶解工程において、ポリマー溶液と金属塩溶液との混合比を種々変化させたこと以外は実施例1と同様にして、ポリマーブロックA相のピリジン単位1モルに対してFeCl3を0.2〜2.0モル(4.8体積%〜33体積%)含有する金属含有ブロック共重合体をそれぞれ調製した。
【0056】
得られた金属含有ブロック共重合体を実施例1と同様にしてそれぞれTEM観察したところ、表1に示すナノ相分離構造が観察された。なお各実施例における混合溶液とフィルムは、実施例1と同様に凝集や分離の無い均一な組成であった。
【0057】
【表1】

ポリマーブロックA相のシリンダ構造とは、図5及び図10にも示したように、ポリマーブロックB相の海の中にポリマーブロックA相が細長い円柱状で規則的に並んだ状態をいい、ポリマーブロックB相のシリンダ構造とは、図7にも示したように、ポリマーブロックA相の海の中にポリマーブロックB相が細長い円柱状で規則的に並んだ状態をいう。FeCl3のモル比が増大するにつれて、ポリマーブロックA相の体積が増大したため、シリンダ構造からラメラ構造へ転移し、さらにポリマーブロックB相のシリンダ構造へ転移していることがわかる。
【0058】
すなわち本発明の製造方法によれば、ポリマーブロックA相のピリジン単位1モルに対してFeCl3を 0.2モル(4.8体積%)を超える量で配位結合させることができ、FeCl3を2.0モル(33体積%)まで含有しても安定なナノ相分離構造を形成できることが明らかである。
【実施例3】
【0059】
FeCl3に代えて、アセチルアセトンニッケル(II){Ni(acac)2}、臭化亜鉛{ZnBr2}、硝酸銀(I){AgNO3}、酸化鉄(III){Fe2O3}、臭化銅(I){CuBr}をそれぞれ用いたこと以外は、実施例1と同様(金属含有量0.5モル)にして、金属含有ブロック共重合体をそれぞれ製造した。
【0060】
いずれの金属化合物でも均一なフィルムが得られ、それらをTEM観察したところ、図6と同様のラメラ構造が確認された。
[比較例]
ピリジンに代えてクロロホルムを用いたこと以外は実施例1と同様にして、ポリマー溶液と金属塩溶液とを調製した。そしてポリマー溶液と金属塩溶液とを混合したところ、凝集による沈殿及び分離が生じた。さらに実施例1と同様にしてクロロホルムを除去する除去工程を行ったが、図10に示すように不均一な塊状体となったため、その後の実験は取りやめた。
【0061】
すなわちFe原子はクロロホルムと配位結合しないため、ポリマー溶液と金属塩溶液とを混合した瞬間にFe原子がポリマーブロックA相に配位結合し、FeCl3が他のポリマーブロックA相との間を架橋したため凝集が生じたと考えられる。
【産業上の利用可能性】
【0062】
本発明の金属含有ブロック共重合体は、表面増強ラマン散乱、表面増強赤外吸収、バイオセンサー、走査型近接場光学顕微鏡、導波路、表面プラズモン励起デバイス、エネルギー増強デバイス、光定法処理デバイス、光記録・再生デバイス、フォトニック結晶デバイスなどに利用できる他、そのままで、もしくは金属を還元させて、あるいは有機物を焼失させるなどして、各種テンプレートとしての利用も期待される。
【符号の説明】
【0063】
1:ブロック共重合体
10:ポリスチレンブロック相(ポリマーブロックB相)
11:ポリビニルピリジンブロック相(ポリマーブロックA相)
【技術分野】
【0001】
本発明は、金属がナノメータ単位のサイズで規則的に含有された金属含有ブロック共重合体と、その製造方法に関するものである。
【背景技術】
【0002】
近年、ポリマーやガラスなどのマトリックス中に金属をナノレベルで含む複合材料が開発され、その特異な光学特性や電気的、磁気的特性を利用した機能材料への応用、あるいは触媒や医薬への応用が期待されている。例えば、光の波長ほどのサイズの金属微粒子をマトリックス中に規則的に含ませることで表面プラズモン共鳴(SPR)が生じるが、これを利用したセンサー、導波路、光デバイスなどが研究されている。
【0003】
Phys.Rev.Lett.95(2005)237401には、銀又は金を直径数100nmのナノリングに加工し、これにギャップ間隔10nm程度のスリットを設けたものを無数に集積化することで、可視光全体をカバーする広い周波数領域でSPRによって電流が流れ、人工的な磁性を発現できることが記載されている。したがって、このような微細金属集積体をマトリックス中につくり込んだメタマテリアルを用いれば、光を自在に曲げることが可能となり、負の屈折率も実現できる。
【0004】
ポリマーやガラスなどのマトリックス中に金属をナノレベルで含む複合材料を製造する一つの例として、PVDあるいはCVDなどにより製造された金属ナノ粒子を高分子溶液あるいは溶融高分子と混合する方法が知られている。しかしこの方法では、金属ナノ粒子がマトリックス内に分散される時に非可逆的な凝集物を形成し易く、得られたものは光散乱が生じるなど光学機能材料としては満足し難いものであった。
【0005】
そこで特開2002−179931号公報には、AgBF4塩などの金属前駆体を高分子溶液中に溶解して分子レベルで分散させ、その後に光を照射して金属前駆体を還元することで、金属銀をナノレベルで高分子中に固定する方法が提案されている。この製造方法によれば、高分子マトリックス中に金属前駆体を凝集することなくナノレベルで分散させることができるため、還元後の金属も高分子マトリックス中にナノレベルで分散させることができる。
【0006】
しかしながらこの製造方法では、高分子マトリックス中に金属粒子が均一に分散した複合材料が得られるのみであり、高分子マトリックス中に金属粒子を規則的に配列させることはできない。したがって、メタマテリアルやフォトニッククリスタルなどの金属含有ナノ構造体としての利用分野が規制されるという不具合があった。
【0007】
一方、Macromolecules,2008,41(7),2577-2583には、ポリスチレンブロックとポリビニルピリジンブロックとからなるブロック共重合体中に、CdCl2をナノレベルで規則的に配置した金属含有ブロック共重合体が記載されている。その製造方法は、アニオン重合によって得られたブロック共重合体をテトラヒドロフラン/エタノール(8:2)の混合溶媒に溶解した溶液にCdCl2を混合し、それをフィルム状にキャストした後にアニールするものである。
【0008】
この金属含有ブロック共重合体によれば、CdCl2がポリビニルピリジンブロックのピリジン単位に配位結合することでナノレベルで固定化されている。したがってCdCl2はブロック共重合体の内部にラメラ構造など規則的に配置されることとなり、光学機能材料としての利用分野が格段に拡がる。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2002−179931号公報
【非特許文献】
【0010】
【非特許文献1】Phys.Rev.Lett.95(2005)237401
【非特許文献2】Macromolecules,2008,41(7),2577-2583
【発明の概要】
【発明が解決しようとする課題】
【0011】
ところが非特許文献2には、ポリビニルピリジンブロックのピリジン単位1モルに対して0.2モルを超えるCdCl2を混合した場合には、ブロック共重合体とは均一に配位結合せずに沈殿するCdCl2が存在したことが記載されている。すなわち、ピリジン単位1モルに対して0.2モル(4.4体積%)を超えるCdCl2をナノレベルで構造制御しながら複合化することは困難であった。したがって得られる金属含有ブロック共重合体は、金属含有量が低いがために光学特性その他物理特性などの向上には限界があり、利用分野の拡大にも限度があった。
【0012】
本発明はこのような事情に鑑みてなされたものであり、ブロック共重合体に多量の金属をナノレベルでかつ規則的に含有させることを解決すべき課題とする。
【課題を解決するための手段】
【0013】
上記課題を解決する本発明の金属含有ブロック共重合体の製造方法の特徴は、金属が配位結合可能なポリマーブロックA相と金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、当該金属の化合物である金属化合物と、をブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒に溶解した混合溶液を調製する溶解工程と、混合溶液から溶媒を除去する除去工程と、からなることにある。
【0014】
混合溶液には、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で含まれていることが望ましい。又は金属化合物が4.4体積%を超え33体積%以下の量で含まれていることが望ましい。
【0015】
溶解工程は、ブロック共重合体を溶媒に溶解した溶液と、金属化合物を溶媒に溶解した溶液とを混合して行うことが望ましい。また除去工程は、混合溶液から溶媒を10ml/秒以下の速度で除去することが望ましい。さらに、除去工程前に膜厚を調整する塗布工程、または、除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程の少なくともいずれかを行うことが望ましい。
【0016】
そして本発明の金属含有ブロック共重合体の特徴は、本発明の製造方法により製造された金属含有ブロック共重合体であって、金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、ブロック共重合体のポリマーブロックA相に選択的に配位結合してなる当該金属の化合物である金属化合物と、からなり、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で、又は金属化合物として4.4体積%を超え33体積%以下の量で配位結合していることにある。
【発明の効果】
【0017】
本発明の製造方法によれば、ブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能な溶媒を用いている。したがって金属化合物は先ず溶媒分子と配位結合し溶媒和の状態となるため、溶解工程後の混合溶液中ではポリマーブロックA相と配位結合するのが規制されている。そのため金属化合物の量が多くても均一な混合溶液となり凝集や沈殿が生じない。
【0018】
その後除去工程を行うと、先ず混合溶液中の溶媒分子が離脱し、その後に金属化合物に配位結合している溶媒分子が離脱すると考えられる。この時、金属化合物から配位結合している溶媒分子の1個が離脱すると、その金属化合物はポリマーブロックA相と配位結合して固定化される。したがってポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モル以下の場合には、金属化合物中の金属原子はそれぞれポリマーブロックA相の配位結合可能な単位と配位結合し、金属がナノメータ単位のサイズで含有されることとなる。
【0019】
またポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モルを超える場合には、過剰の金属化合物は静電相互作用によって既に配位結合している金属化合物に近接して保持されると考えられ、凝集や沈殿が生じることが無い。
【0020】
したがって金属化合物はポリマーブロックA相にのみ含まれ、ブロック共重合体はポリマーブロックA相とポリマーブロックB相とが規則的に配列したナノ相分離構造をなしているので、金属が規則的に配列したナノ相分離構造をなす金属含有ブロック共重合体が得られる。
【0021】
すなわち本発明の製造方法によれば、ブロック共重合体に多量の金属をナノレベルでかつ規則的に含有させることができる。したがって得られた本発明の金属含有ブロック共重合体は、ポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として 0.2モルを超え 2.0モル以下の量で配位結合し、しかも金属化合物はポリマーブロックA相のみに含まれているので、金属がナノレベルでかつ規則的に含まれている。したがってメタマテリアルとしての利用分野が格段に拡がる。
【図面の簡単な説明】
【0022】
【図1】本発明の一実施例において、金属塩が溶媒和した状態を示す化学式である。
【図2】本発明の一実施例における混合溶液の組成を示す化学式である。
【図3】本発明の一実施例における除去工程の途中の段階を示す化学式である。
【図4】本発明の一実施例で製造された金属含有ブロック共重合体を示す化学式である。
【図5】本発明の一実施例においてブランクとして製造されたFeCl3を含有しないブロック共重合体の構造を示すTEM写真である。
【図6】本発明の一実施例で製造されたFeCl3を0.5モル(11.2体積%)含有する金属含有ブロック共重合体の構造を示すTEM写真である。
【図7】本発明の実施例2で製造されFeCl3を2.0モル(33体積%)含有する金属含有ブロック共重合体の構造を示すTEM写真である。
【図8】ブランクであるブロック共重合体と本発明の一実施例で製造された金属含有ブロック共重合体のDSCチャートである。
【図9】ブランクであるブロック共重合体と本発明の一実施例で製造された金属含有ブロック共重合体のFT−IRチャートである。
【図10】本発明の製造方法における反応機構を模式的に示す説明図である。
【図11】実施例1及び比較例における除去工程後の金属含有ブロック共重合体の状態を示す説明図である。
【発明を実施するための形態】
【0023】
本発明の製造方法に用いられるブロック共重合体は、金属が配位結合可能なポリマーブロックA相と当該金属が配位結合しないポリマーブロックB相とを含む。ポリマーブロックA相,B相以外の他のポリマーブロックを含んでもよい。このブロック共重合体は、段階的重合法、カップリング法、リビングアニオン重合、リビングカチオン重合、リビングラジカル重合(RAFT重合など)など、公知の重合法によって製造することができる。
【0024】
ここでRAFT重合とは、可逆的付加開裂連鎖移動(Reversible Addition-Fragmentation Chain Transfer)重合であり、可逆的付加開裂連鎖移動剤(Reversible Addition-Fragmentation Chain Transfer剤、以下、「RAFT剤」と略す。)を用いることを特徴とする重合方法である。RAFT剤としては、ジチオ安息香酸クミル、S-1-ドデシル-S'(a,a"-ジメチル-a"-酢酸)トリチオカーボネイト、ジチオ安息香酸2-シアノプロピ2-イルなどが挙げられる。
【0025】
ポリマーブロックA相は金属が配位結合可能なポリマーであり、配位能を有する酸素原子や窒素原子を含むモノマーが重合したものが望ましい。例えばポリビニルピリジン、ポリビニルピロリドン、ポリビニルエーテル、ポリエチレングリコール、ポリプロピレンオキシド、ポリアクリル酸、ポリアクリル酸エステル、ポリメタクリル酸、ポリメタクリル酸エステル、ポリ酢酸ビニル、ポリビニルフェノール、ポリエチレンテレフタレート、ポリアミド、ポリビニルアルコール、ポリカーボネート、ポリオキシメチレンなどが例示される。
【0026】
ポリマーブロックB相は当該金属が配位結合しないポリマーであり、ポリマーブロックA相とブロック化できるものであれば特に制限されない。例えばポリスチレン、ポリイソプレン、ポリブタジエン、ポリフッ化ビニリデン、ポリ塩化ビニリデン、ポリジメチルシロキサン、ポリイソブチレン、ポリエチレン、ポリプロピレン、ポリアルケンなどが例示される。金属が配位結合することで金属含有ブロック共重合体の硬度が増大する場合には、ポリマーブロックB相には軟質のポリマーを用いることも好ましい。
【0027】
ポリマーブロックA相とポリマーブロックB相との構成比率、それぞれの分子量又はブロック共重合体の分子量は特に制限されないが、可視光を利用する光学機能材料として用いる場合には、ブロック共重合体の構造周期が100nm〜250nm(可視光波長の1/4〜1/3倍)程度とするのが好ましい。
【0028】
本発明に用いられる金属は、少なくともポリマーブロックA相を構成する配位結合可能な単位に配位結合可能なものである。一般的に金属は電子が失われた酸化状態で存在しやすく、それは配位結合可能なものであるので、ほとんどの金属や合金あるいは金属間化合物を用いることができる。光学機能材料として用いる場合には、例えばCu、Ag、Auなどを含むことが好ましい。
【0029】
金属化合物としては、当該金属のアセチルアセトン塩、臭化物、塩化物、ヨウ化物、酸化物、硝酸塩、硫酸塩、炭酸塩、酢酸塩、リン酸塩、水素化物など、後述の溶媒に可溶のものが用いられる。金属化合物の混合量は、例えばFeCl3の場合には、ポリマーブロックA相の配位結合可能な単位1モルに対してFeとして 0.2モルを超え 2.0モル以下の範囲、体積分率としては4.8体積%〜33体積%であることが望ましい。なお臭化亜鉛(ZnBr2)の場合には、0.2〜2.0モルは4.5体積%〜32体積%に相当し、臭化銅(CuBr)の場合には、0.2〜2.0モルは2.6体積%〜21体積%に相当する。
【0030】
本発明に用いる溶媒は、ブロック共重合体及び金属化合物が溶解可能でありかつ当該金属が配位結合可能なものであって、除去工程で除去できるものであればよく、特には水、アルコール、ピリジン、ピロリドン、アミン類、アンモニア水などが例示される。これらの溶媒単品でもよいし、複数種の溶媒が混合された混合溶媒を用いてもよい。溶媒の混合量は、ブロック共重合体及び金属化合物が完全に溶解する量以上とする。
【0031】
溶解工程では、ブロック共重合体及び金属化合物が溶媒に溶解した混合溶液を調製する。このとき、金属化合物の金属が溶媒と配位結合するより先にポリマーブロックA相と配位結合すると、その金属が他のポリマーブロックA相とも配位結合して架橋状態となり、凝集が生じる場合がある。そこで、ブロック共重合体を溶媒に予め溶解した溶液と、金属化合物を溶媒に予め溶解した溶液とを混合することが望ましい。このようにすることで、金属化合物と溶媒とを確実に配位結合させることができ、凝集が生じるのを確実に防止することができる。
【0032】
なお、金属がポリマーブロックA相に配位する速度と、金属が溶媒に配位する速度とが異なる場合には、溶媒に配位する速度がポリマーブロックA相に配位する速度より大きくなるように、溶媒又はポリマーブロックA相の種類を選択するのが望ましい。
【0033】
除去工程では、先ず混合溶液中の溶媒分子が離脱し、その後に金属化合物に配位結合している溶媒分子が離脱すると考えられる。この時、金属化合物から配位結合している溶媒分子の1個が離脱すると、その金属化合物はポリマーブロックA相と配位結合して固定化される。したがってポリマーブロックA相の配位結合可能な単位1モルに対して金属化合物が金属として1モル以下の場合には、金属化合物の金属原子はそれぞれポリマーブロックA相の配位結合可能な単位と配位結合し、金属がナノメータ単位のサイズで含有されることとなる。
【0034】
この除去工程は、混合溶液を加熱して溶媒を蒸発させる一般的な乾燥方法で行うことができる。また減圧雰囲気下で乾燥させることも好ましい。しかし除去工程を急激に行うと、溶媒和した金属化合物から溶媒が離脱する速度と混合溶液中の溶媒が蒸発する速度とが近くなり、ポリマーブロックA相が金属化合物によって架橋されて凝集する場合がある。したがって溶媒の除去速度はできるだけ小さくすることが望ましく、10ml/秒以下の速度で除去することが好ましい。
【0035】
得られた金属含有ブロック共重合体は、そのままでも構わないが、除去工程前に膜厚を調整する塗布工程、または、除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程との少なくともいずれかを行うことが望ましい。バーコーター、スピンコーターなどを用いて、適宜、混合溶液の濃度を調整して塗布工程を行うことにより膜厚を調整することができる。またアニール工程を行うことで、金属含有ブロック共重合体のナノ相分離構造をより均一化することができる。加熱温度は、金属を含まないポリマーブロックB相のガラス転移温度以上とすることが好ましい。また還元工程を行うことで、金属化合物を金属へ還元することができ利用分野の自由度がさらに高まる。
【0036】
以下、実施例により本発明を具体的に説明する。
【実施例1】
【0037】
<ブロック共重合体の調製>
スチレンモノマー中に[化1]に示すRAFT剤{S-1-ドデシル-S'(a,a"-ジメチル-a"-酢酸)トリチオカーボネイト}を溶解し、130℃で6時間かけて重合してポリスチレンブロックを合成した。次いで4-ビニルピリジンモノマ−を加えて70℃で1時間重合し、[化2]に示すブロック共重合体を合成した。
【0038】
【化1】

【0039】
【化2】

このブロック共重合体は、ポリビニルピリジンブロック(以下、ポリマーブロックA相という)と、ポリスチレンブロック(以下、ポリマーブロックB相という)と、から構成されている。数平均分子量は48,000であり、分子量分布は1.30であり、ポリマーブロックA相の体積分率は0.60である。
【0040】
<溶解工程>
得られたブロック共重合体溶液にピリジンを追加し、ブロック共重合体の濃度が4質量%のポリマー溶液を調製した。また市販のFeCl3をピリジンに溶解し、FeCl3の濃度が2質量%の金属塩溶液を調製した。そしてポリマー溶液と金属塩溶液を体積比で1対1に混合し、混合溶液を調製した。混合溶液は、凝集や沈殿が生じることなく均一な溶液状態であった。
【0041】
この混合溶液は、質量比でブロック共重合体:FeCl3=3:1であり、ポリマーブロックA相のピリジン単位1モルに対して0.5モルのFeCl3が含まれている。FeCl3の体積分率は11.2%である。
【0042】
<除去工程>
混合溶液をテフロン(商標)製容器へ移し、50 ℃で36時間保持してピリジンを蒸発させた。蒸発速度は5μl/分である。この除去工程後のブロック共重合体フィルムは、図11に示すように凝集や分離の無い均一な茶色透明体であった。この除去工程では、以下のような反応が生じたと推察される。
【0043】
FeCl3のピリジン溶液では、FeCl3はFe原子が3分子のピリジンと配位結合して図1に示す溶媒和状態となっている。これをポリマー溶液と混合しても、その状態は変化せず、図2に示すようにブロック共重合体1とFeCl3の溶媒和物2とがピリジン3中に溶解した状態である。
【0044】
FeCl3と配位結合しているピリジンは、溶媒のピリジンより蒸発しにくい。したがってこの溶液から徐々にピリジンを蒸発させると、先ず溶媒のピリジンが蒸発する。溶媒のピリジンが少なくなるとFeCl3の溶媒和物2に配位結合していたピリジンも蒸発する。しかし3個のピリジンのうち1個が離脱すると、図3に示すように、ピリジンが離脱したFe原子はブロック共重合体1におけるポリマーブロックA相のピリジン単位と配位結合する。その後、Feに配位結合していた残りのピリジンが離脱することで、図4に示すように凝集や分離の無い均一な金属含有ブロック共重合体が生成する。
【0045】
<アニール工程>
次いで160℃で60時間保持し、均一なフィルム状の金属含有ブロック共重合体を得た。
[ブランク]
実施例1で製造されたブロック共重合体にピリジンを追加し、ブロック共重合体の濃度が4質量%のポリマー溶液を調製した。このポリマー溶液のみをテフロン(商標)製容器へ移し、実施例1と同様にしてピリジンを蒸発させるとともにアニールし、ブランクとしてFeCl3を含まないブロック共重合体のフィルムを得た。
【0046】
<TEM観察>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、加速電圧:100kVの条件にてTEM観察した。その結果を図5、図6に示す。なおブランクのブロック共重合体のフィルムは、沃素にて染色している。また図7に、後述の実施例2に係るFeCl3が2.0モル(33体積%)含まれた金属含有ブロック共重合体のフィルムのTEM写真を示す。
【0047】
図5には、薄い灰色の海中に濃い灰色の部分が島状に存在し、濃い灰色の部分がシリンダ構造のナノ相分離構造をなしていることが示されている。一方、図6には、薄い灰色の部分と濃い灰色の部分が層状に形成されたラメラ構造のナノ相分離構造であることが示されている。また図7には、薄い灰色の部分がシリンダ構造のナノ相分離構造であることが示されている。
【0048】
すなわちFeCl3を含有することによって、さらにFeCl3の含有量が多くなるにつれて、図5、図6、図7へと変化するモルフォロジー転移が生じたことが観察された。なお図6及び図7に係る金属含有ブロック共重合体は、染色しなくともラメラ構造を明瞭に観察することができた。
【0049】
<DSC測定>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、昇温速度:10℃/分、温度範囲:20〜250℃の条件にてDSC測定を行った。結果を図8に示す。図8において108〜109℃近傍の吸熱ピークはポリマーブロックB相に起因し、152℃近傍の吸熱ピークはポリマーブロックA相に起因している。金属含有ブロック共重合体からはポリマーブロックA相に起因する吸熱ピークが消失し、これはFe原子がポリマーブロックA相にのみ選択的に分散したことを示している。
【0050】
<FT−IR測定>
ブランクであるブロック共重合体のフィルムと、実施例1の金属含有ブロック共重合体のフィルムとを、それぞれピリジンに溶解しKBr板にそれぞれ塗布して、120℃で真空乾燥した。これらを大気圧下、検出器:TGS、分解能:2cm-1の条件にてFT−IR測定を行った。結果を図9に示す。なお実施例1の金属含有ブロック共重合体のフィルムは、ピリジンに完全に溶解した。これはフィルム中に不可逆的な凝集物などが存在しないことを意味している。
【0051】
図9に示すように、金属含有ブロック共重合体には1613cm-1に吸収ピークが現れ、これはポリマーブロックA相のピリジン単位の不対電子にFeが配位結合していることを示している。
【0052】
<考察>
したがってFeCl3を含有することで、TEMにおいてモルフォロジー転移が生じたのが観察されたのは、図10に模式的に示すように、FeCl3のFe原子がポリマーブロックA相にのみ配位結合したことで、ポリマーブロックA相の体積が増加したことに起因すると考えられる。すなわちブランクのブロック共重合体1では、図5にも示したように、ポリマーブロックB相10の海の中にポリマーブロックA相11がシリンダ構造で存在している。そこへFeCl3が添加されると、Fe原子がポリマーブロックA相11に選択的に配位結合する。するとポリマーブロックA相11の体積が増加して、隣接するポリマーブロックA相11どうしが連結されることでラメラ構造となったと考えられる。
【0053】
なお小角X線散乱(SAXS)による構造観察でもラメラ構造が確認されたので、実施例1の金属含有ブロック共重合体はTEMの視野以外の部分も図6と同様のナノ相分離構造となっていることが明らかである。
【0054】
すなわち実施例1で得られた金属含有ブロック共重合体は、ブロック共重合体のポリマーブロックA相のピリジン単位にFeCl3が選択的に配位結合してなり、ラメラ構造のナノ相分離構造をなしている。しかもポリマーブロックA相のピリジン単位1モルに対して、0.5モルという多量でFeCl3が含まれているにも関わらず、凝集や分離などの不具合なく均一な組成の金属含有ブロック共重合体であった。
【実施例2】
【0055】
溶解工程において、ポリマー溶液と金属塩溶液との混合比を種々変化させたこと以外は実施例1と同様にして、ポリマーブロックA相のピリジン単位1モルに対してFeCl3を0.2〜2.0モル(4.8体積%〜33体積%)含有する金属含有ブロック共重合体をそれぞれ調製した。
【0056】
得られた金属含有ブロック共重合体を実施例1と同様にしてそれぞれTEM観察したところ、表1に示すナノ相分離構造が観察された。なお各実施例における混合溶液とフィルムは、実施例1と同様に凝集や分離の無い均一な組成であった。
【0057】
【表1】

ポリマーブロックA相のシリンダ構造とは、図5及び図10にも示したように、ポリマーブロックB相の海の中にポリマーブロックA相が細長い円柱状で規則的に並んだ状態をいい、ポリマーブロックB相のシリンダ構造とは、図7にも示したように、ポリマーブロックA相の海の中にポリマーブロックB相が細長い円柱状で規則的に並んだ状態をいう。FeCl3のモル比が増大するにつれて、ポリマーブロックA相の体積が増大したため、シリンダ構造からラメラ構造へ転移し、さらにポリマーブロックB相のシリンダ構造へ転移していることがわかる。
【0058】
すなわち本発明の製造方法によれば、ポリマーブロックA相のピリジン単位1モルに対してFeCl3を 0.2モル(4.8体積%)を超える量で配位結合させることができ、FeCl3を2.0モル(33体積%)まで含有しても安定なナノ相分離構造を形成できることが明らかである。
【実施例3】
【0059】
FeCl3に代えて、アセチルアセトンニッケル(II){Ni(acac)2}、臭化亜鉛{ZnBr2}、硝酸銀(I){AgNO3}、酸化鉄(III){Fe2O3}、臭化銅(I){CuBr}をそれぞれ用いたこと以外は、実施例1と同様(金属含有量0.5モル)にして、金属含有ブロック共重合体をそれぞれ製造した。
【0060】
いずれの金属化合物でも均一なフィルムが得られ、それらをTEM観察したところ、図6と同様のラメラ構造が確認された。
[比較例]
ピリジンに代えてクロロホルムを用いたこと以外は実施例1と同様にして、ポリマー溶液と金属塩溶液とを調製した。そしてポリマー溶液と金属塩溶液とを混合したところ、凝集による沈殿及び分離が生じた。さらに実施例1と同様にしてクロロホルムを除去する除去工程を行ったが、図10に示すように不均一な塊状体となったため、その後の実験は取りやめた。
【0061】
すなわちFe原子はクロロホルムと配位結合しないため、ポリマー溶液と金属塩溶液とを混合した瞬間にFe原子がポリマーブロックA相に配位結合し、FeCl3が他のポリマーブロックA相との間を架橋したため凝集が生じたと考えられる。
【産業上の利用可能性】
【0062】
本発明の金属含有ブロック共重合体は、表面増強ラマン散乱、表面増強赤外吸収、バイオセンサー、走査型近接場光学顕微鏡、導波路、表面プラズモン励起デバイス、エネルギー増強デバイス、光定法処理デバイス、光記録・再生デバイス、フォトニック結晶デバイスなどに利用できる他、そのままで、もしくは金属を還元させて、あるいは有機物を焼失させるなどして、各種テンプレートとしての利用も期待される。
【符号の説明】
【0063】
1:ブロック共重合体
10:ポリスチレンブロック相(ポリマーブロックB相)
11:ポリビニルピリジンブロック相(ポリマーブロックA相)
【特許請求の範囲】
【請求項1】
金属が配位結合可能なポリマーブロックA相と該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、該金属の化合物である金属化合物と、を該ブロック共重合体及び該金属化合物が溶解可能でありかつ該金属が配位結合可能な溶媒に溶解した混合溶液を調製する溶解工程と、
該混合溶液から該溶媒を除去する除去工程と、からなることを特徴とする金属含有ブロック共重合体の製造方法。
【請求項2】
前記混合溶液には、前記ポリマーブロックA相の配位結合可能な単位1モルに対して前記金属化合物が金属として 0.2モルを超え 2.0モル以下の量で含まれている請求項1に記載の金属含有ブロック共重合体の製造方法。
【請求項3】
前記溶解工程は、前記ブロック共重合体を前記溶媒に溶解した溶液と、前記金属化合物を前記溶媒に溶解した溶液とを混合して行う請求項1又は請求項2に記載の金属含有ブロック共重合体の製造方法。
【請求項4】
前記除去工程は前記混合溶液から前記溶媒を10ml/秒以下の速度で除去する請求項1〜3のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項5】
前記除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程との少なくとも一方をさらに行う請求項1〜4のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項6】
前記ポリマーブロックA相はピリジン環を含み、前記溶媒はピリジンを含む請求項1〜5のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項7】
請求項1〜6のいずれかに記載の製造方法により製造された金属含有ブロック共重合体であって、
金属が配位結合可能なポリマーブロックA相と該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、該ブロック共重合体の該ポリマーブロックA相に選択的に配位結合してなる該金属の化合物である金属化合物と、からなり、
該ポリマーブロックA相の配位結合可能な単位1モルに対して該金属化合物が金属として 0.2モルを超え 2.0モル以下の量で配位結合していることを特徴とする金属含有ブロック共重合体。
【請求項1】
金属が配位結合可能なポリマーブロックA相と該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、該金属の化合物である金属化合物と、を該ブロック共重合体及び該金属化合物が溶解可能でありかつ該金属が配位結合可能な溶媒に溶解した混合溶液を調製する溶解工程と、
該混合溶液から該溶媒を除去する除去工程と、からなることを特徴とする金属含有ブロック共重合体の製造方法。
【請求項2】
前記混合溶液には、前記ポリマーブロックA相の配位結合可能な単位1モルに対して前記金属化合物が金属として 0.2モルを超え 2.0モル以下の量で含まれている請求項1に記載の金属含有ブロック共重合体の製造方法。
【請求項3】
前記溶解工程は、前記ブロック共重合体を前記溶媒に溶解した溶液と、前記金属化合物を前記溶媒に溶解した溶液とを混合して行う請求項1又は請求項2に記載の金属含有ブロック共重合体の製造方法。
【請求項4】
前記除去工程は前記混合溶液から前記溶媒を10ml/秒以下の速度で除去する請求項1〜3のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項5】
前記除去工程後に金属含有ブロック共重合体を加熱保持するアニール工程と金属含有ブロック共重合体を還元する還元工程との少なくとも一方をさらに行う請求項1〜4のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項6】
前記ポリマーブロックA相はピリジン環を含み、前記溶媒はピリジンを含む請求項1〜5のいずれかに記載の金属含有ブロック共重合体の製造方法。
【請求項7】
請求項1〜6のいずれかに記載の製造方法により製造された金属含有ブロック共重合体であって、
金属が配位結合可能なポリマーブロックA相と該金属が配位結合しないポリマーブロックB相とを含むブロック共重合体と、該ブロック共重合体の該ポリマーブロックA相に選択的に配位結合してなる該金属の化合物である金属化合物と、からなり、
該ポリマーブロックA相の配位結合可能な単位1モルに対して該金属化合物が金属として 0.2モルを超え 2.0モル以下の量で配位結合していることを特徴とする金属含有ブロック共重合体。
【図1】


【図2】


【図3】


【図4】


【図8】


【図9】


【図10】


【図5】


【図6】


【図7】


【図11】




【図2】


【図3】


【図4】


【図8】


【図9】


【図10】


【図5】


【図6】


【図7】


【図11】


【公開番号】特開2010−260994(P2010−260994A)
【公開日】平成22年11月18日(2010.11.18)
【国際特許分類】
【出願番号】特願2009−114660(P2009−114660)
【出願日】平成21年5月11日(2009.5.11)
【出願人】(504139662)国立大学法人名古屋大学 (996)
【Fターム(参考)】
【公開日】平成22年11月18日(2010.11.18)
【国際特許分類】
【出願日】平成21年5月11日(2009.5.11)
【出願人】(504139662)国立大学法人名古屋大学 (996)
【Fターム(参考)】
[ Back to top ]

