金属酸化物ナノ粒子とカーボンの複合体、その製造方法、この複合体を用いた電極及び電気化学素子
【課題】100nm以下の金属酸化物ナノ粒子がカーボンに高分散担持された複合体を提供する。
【解決手段】金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物の結晶化を進行させ、金属酸化物ナノ粒子をカーボンに高分散担持させる。金属酸化物ナノ粒子の前駆体とこれを担持したカーボンナノ粒子は、旋回する反応器内で反応物にずり応力と遠心力を与えるメカノケミカル反応によって作製する。前記窒素雰囲気内の急速加熱処理は、400℃〜1000℃に加熱することが望ましい。加熱した複合体を更に粉砕することで、その凝集を解消し、金属酸化物ナノ粒子の分散度をより均一化する。金属酸化物としては、酸化マンガン、リン酸鉄リチウム、チタン酸リチウムなどが使用できる。カーボンとしては、カーボンナノファイバーやケッチェンブラックが使用できる。
【解決手段】金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物の結晶化を進行させ、金属酸化物ナノ粒子をカーボンに高分散担持させる。金属酸化物ナノ粒子の前駆体とこれを担持したカーボンナノ粒子は、旋回する反応器内で反応物にずり応力と遠心力を与えるメカノケミカル反応によって作製する。前記窒素雰囲気内の急速加熱処理は、400℃〜1000℃に加熱することが望ましい。加熱した複合体を更に粉砕することで、その凝集を解消し、金属酸化物ナノ粒子の分散度をより均一化する。金属酸化物としては、酸化マンガン、リン酸鉄リチウム、チタン酸リチウムなどが使用できる。カーボンとしては、カーボンナノファイバーやケッチェンブラックが使用できる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、金属酸化物ナノ粒子とカーボンの複合体、その製造方法、この複合体を用いた電極及び電気化学素子に関する。
【背景技術】
【0002】
現在、リチウム電池の電極としてリチウムを貯蔵、放出するカーボン材料等が用いられているが、マイナス電位が水素の還元分解電位より小さいので電解液の分解という危険性がある。そこで、特許文献1や特許文献2に記載のように、マイナス電位が水素の還元分解電位より大きいチタン酸リチウムの使用が検討されているが、チタン酸リチウムは出力特性が低いという問題点がある。そこで、チタン酸リチウムをナノ粒子化し、炭素に担持させた電極によって、出力特性を向上する試みがある。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2007−160151号公報
【特許文献2】特開2008−270795号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
これらの特許文献に記載の発明は、旋回する反応器内で反応物にずり応力と遠心力を加えて、化学反応を促進させる方法(一般に、メカノケミカル反応と呼ばれる)によって、カーボンに分散担持されたチタン酸リチウムを得るものである。この場合、反応物としては、例えば、チタン酸リチウムの出発原料であるチタンアルコキシドと酢酸リチウム、及びカーボンナノチューブやケッチェンブラック等のカーボン、酢酸等を使用する。
【0005】
これらの特許文献に記載のチタン酸リチウムナノ粒子を担持したカーボンを使用した電極は、優れた出力特性を発揮するものの、最近では、この種の電極において、さらに出力特性を向上させ、電気伝導度を向上させる要求がある。
【0006】
また、チタン酸リチウムナノ粒子に限らず、他の金属酸化ナノ粒子についても、これをカーボンに担持させた複合体を製造し、それによって、より優れた出力特性を有する電極や電気化学素子を得ようとする要求もある。特に、酸化マンガンのようなリチウムに比べて安価な金属酸化物の使用が望まれている。
【0007】
本発明は、上述したような従来技術の問題点を解決するために提案されたものであって、その目的は、出力特性及び電気伝導度の向上を可能とした電極や電気化学素子を得ることのできる金属酸化物ナノ粒子とカーボンの複合体、及びその製造方法を提供することにある。また、本発明の他の目的は、前記複合体を用いた電極及び電気化学素子を提供することにある。
【課題を解決するための手段】
【0008】
前記の目的を達成するため、本発明の金属酸化物ナノ粒子とカーボンの複合体の製造方法は、金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物ナノ粒子の結晶化を進行させ、金属酸化物ナノ粒子をカーボンに高分散担持させることを特徴とする。この場合、前記急速加熱処理が、前記複合体を窒素雰囲気中で、400〜1000℃に加熱するものであること、前記金属酸化物ナノ粒子が2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上の結晶構造体(超薄膜構造体)であることも、本発明の一態様である。更に、前記のような方法で製造した複合体、この複合体を用いた電極や電気化学素子も本発明に包含される。
【発明の効果】
【0009】
本発明によれば、金属酸化物ナノ粒子の前駆体を担持したカーボンの焼成工程において、急速加熱処理することによって、金属酸化物ナノ粒子の良好な結晶化を進行することができ、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上の結晶構造体が形成される。
【図面の簡単な説明】
【0010】
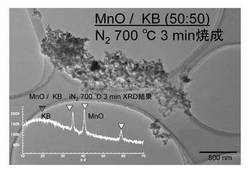
【図1】実施例1の複合体のXRD分析結果とTEM像を示す図面代用写真。
【図2】実施例1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図3】実施例1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図4】実施例2−1の複合体のXRD分析結果とTEM像を示す図面代用写真。
【図5】実施例2−1の複合体の他の部分のTEM像を示す図面代用写真。
【図6】実施例2−1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図7】実施例2−1の高解像度TEM像を示す図面代用写真。
【図8】実施例2−1の複合体を使用した電気化学素子の充放電特性を示すグラフ。
【図9】実施例2−1の複合体を使用した電気化学素子と、従来の電気化学素子の充放電特性を比較したグラフ。
【図10】実施例2−1の複合体を使用した電気化学素子の出力特性を示すグラフ。
【図11】実施例2−1の複合体を使用した電気化学素子のサイクル特性を示すグラフ。
【図12】実施例2−2の複合体の高解像度TEM像を示す図面代用写真。
【図13】実施例2−3の複合体の高解像度TEM像を示す図面代用写真。
【図14】実施例2−5の複合体の高解像度TEM像を示す図面代用写真。
【図15】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体のTEM像を示す図面代用写真。
【図16】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の拡大したTEM像を示す図面代用写真。
【図17】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の放電挙動特性を示すグラフ。
【図18】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の出力特性を示すグラフ。
【図19】実施例4の高出力エネルギー貯蔵デバイスの特性を示すグラフ。
【図20】本発明の製造方法に使用する反応器の一例を示す斜視図。
【図21】実施例2−1のリン酸鉄リチウムナノ粒子とカーボンの複合体の細孔分布を示す図面代用写真及びグラフ。
【図22】実施例5の充放電特性を示すグラフ。
【図23】実施例5のXRD分析を行った結果を示すグラフ。
【図24】実施例2−1の拡大写真とその模式図。
【図25】実施例2−3の複合体粉末の高解像度TEM像とその模式図。
【発明を実施するための形態】
【0011】
本発明を実施するための形態について、以下、説明する。
【0012】
(メカノケミカル反応)
本発明で用いる反応方法は、本出願人等が先に特許出願した特許文献1及び特許文献2に示した方法と同様のメカノケミカル反応であって、化学反応の過程で、旋回する反応器内で反応物にずり応力と遠心力を加えて化学反応を促進させるものである。
【0013】
この反応方法は、例えば、図20に示すような反応器を用いて行うことができる。図20に示すように、反応器は、開口部にせき板1−2を有する外筒1と、貫通孔2−1を有し旋回する内筒2からなる。この反応器の内筒内部に反応物を投入し、内筒を旋回することによってその遠心力で内筒内部の反応物が内筒の貫通孔を通って外筒の内壁1−3に移動する。この時反応物は内筒の遠心力によって外筒の内壁に衝突し、薄膜状となって内壁の上部へずり上がる。この状態では反応物には内壁との間のずり応力と内筒からの遠心力の双方が同時に加わり、薄膜状の反応物に大きな機械的エネルギーが加わることになる。この機械的なエネルギーが反応に必要な化学エネルギー、いわゆる活性化エネルギーに転化するものと思われるが、短時間で反応が進行する。
【0014】
この反応において、薄膜状であると反応物に加えられる機械的エネルギーは大きなものとなるため、薄膜の厚みは5mm以下、好ましくは2.5mm以下、さらに好ましくは1.0mm以下である。なお、薄膜の厚みはせき板の幅、反応液の量によって設定することができる。
【0015】
この反応方法は、反応物に加えられるずり応力と遠心力の機械的エネルギーによって実現できるものと考えられるが、このずり応力と遠心力は内筒内の反応物に加えられる遠心力によって生じる。したがって、本発明に必要な内筒内の反応物に加えられる遠心力は1500N(kgms-2)以上、好ましくは60000N(kgms-2)以上、さらに好ましくは270000N(kgms-2)以上である。
【0016】
この反応方法においては、反応物にずり応力と遠心力の双方の機械的エネルギーが同時に加えられることによって、このエネルギーが化学エネルギーに転化することによるものと思われるが、従来にない速度で化学反応を促進させることができる。
【0017】
(金属酸化物)
本発明に係る金属酸化物ナノ粒子を生成するための金属酸化物としては、例えば、酸化マンガンMnO、リン酸鉄リチウムLiFePO4、チタン酸リチウムLi4Ti5O12が使用できる。また、その他の酸化物として、MxOz、AxMyOz、Mx(DO4)y、AxMy(DO4)z(ただし、M:金属元素 A:アルカリ金属又はランタノイド元素)で表される金属酸化物の使用も可能である。
【0018】
酸化マンガンMnOの場合は、例えば、過マンガン酸ナトリウム、酢酸マンガン、硝酸マンガン、硫酸マンガンなどのマンガン源及びカーボンを出発原料として、前記メカノケミカル反応により、酸化マンガンナノ粒子の前駆体とこれを分散担持したカーボンの複合体を生成する。この複合体を窒素雰囲気中で急速加熱することにより、本発明の金属酸化物である酸化マンガンとカーボンの複合体が生成される。
【0019】
リン酸鉄リチウムLiFePO4の場合は、例えば、過マンガン酸ナトリウム、酢酸マンガン、硝酸マンガン、硫酸マンガンなどのマンガン源及びカーボンを出発原料として、前記メカノケミカル反応により、リン酸鉄リチウムナノ粒子の前駆体とこれを分散担持したカーボンの複合体を生成する。この複合体を窒素雰囲気中で急速加熱することにより、本発明の金属酸化物であるリン酸鉄リチウムとカーボンの複合体が生成される。
【0020】
チタン酸リチウムLi4Ti5O12の場合は、例えば、チタンアルコキシドなどのチタン源、酢酸リチウム、硝酸リチウム、炭酸リチウム、水酸化リチウムなどのリチウム源を出発原料として使用し、前記メカノケミカル反応により、チタン酸リチウムナノ粒子の前駆体を生成する。このチタン酸リチウムナノ粒子の前駆体を窒素雰囲気中で加熱することにより、酸素欠陥のサイトに窒素がドープされた本発明のチタン酸リチウムナノ粒子が生成される。
【0021】
(カーボン)
反応過程で所定のカーボンを加えることによって、5〜100nmのチタン酸リチウムを高分散担持させたカーボンを得ることができる。すなわち、反応器の内筒の内部に金属塩と所定の反応抑制剤とカーボンを投入して、内筒を旋回して金属塩と反応抑制剤とカーボンを混合、分散する。さらに内筒を旋回させながら水酸化ナトリウムなどの触媒を投入して加水分解、縮合反応を進行させ、金属酸化物を生成すると共に、この金属酸化物とカーボンを分散状態で、混合する。反応終了後にこれを急速加熱することで、金属酸化物ナノ粒子を高分散担持させたカーボンを形成することができる。
【0022】
ここで用いるカーボンとしては、ケッチェンブラック、アセチレンブラック等のカーボンブラック、カーボンナノチューブ、カーボンナノホーン、無定形炭素、炭素繊維、天然黒鉛、人造黒鉛、活性炭、メソポーラス炭素、気相炭素繊維等を挙げることができ、これらの複合材を用いることもできる。
【0023】
(溶媒)
溶媒としては、アルコール類、水、これらの混合溶媒を用いることができる。例えば、酢酸と酢酸リチウムをイソプロパノールと水の混合物に溶解した混合溶媒を使用することができる。
【0024】
(反応抑制剤)
出発原料として金属アルコキシドを使用した場合には、特許文献2に記載のように、前記メカノケミカル反応を適用する所定の金属アルコキシドに、反応抑制剤として該金属アルコキシドと錯体を形成する所定の化合物を添加することができる。これにより、化学反応が促進しすぎるのを抑制することができる。
【0025】
すなわち、金属アルコキシドに、これと錯体を形成する酢酸等の所定の化合物を該金属アルコキシド1モルに対して、1〜3モル添加して錯体を形成することにより、反応を抑制、制御することができることが分かった。なお、この反応によって生成されるのは、金属と酸化物の複合体のナノ粒子、例えば、チタン酸リチウムの前駆体である、リチウムと酸化チタンの複合体のナノ粒子であり、これを焼成することにより、チタン酸リチウムの結晶が得られる。
【0026】
このように、反応抑制剤として酢酸等の所定の化合物を添加することにより、化学反応が促進しすぎるのを抑制することができるのは、酢酸等の所定の化合物が金属アルコキシドと安定な錯体を形成するためであると考えられる。
【0027】
金属アルコキシドと錯体を形成することができる物質としては、酢酸の他、クエン酸、蓚酸、ギ酸、乳酸、酒石酸、フマル酸、コハク酸、プロピオン酸、レプリン酸等のカルボン酸、EDTA等のアミノポリカルボン酸、トリエタノールアミン等のアミノアルコールに代表される錯化剤が挙げられる。
【0028】
(加熱)
本発明は、メカノケミカル反応によりカーボンナノ粒子の構造体の内部に金属酸化物ナノ粒子の前駆体を担持させた複合体を得ると共に、この金属酸化物とカーボンの複合体を窒素雰囲気中で加熱することによって、金属酸化物の結晶化を促進させ、この複合体を使用した電極や電気化学素子の容量、出力特性を向上させるものである。
【0029】
すなわち、得られた金属酸化物ナノ粒子の前駆体とカーボンナノ粒子の複合体の焼成工程において、室温から400〜1000℃まで急熱することによって、金属酸化物ナノ粒子の凝集を防止することができ、粒径の小さなナノ粒子が形成されることが分かった。急速加熱とは、酸素濃度が1000ppm程度の低酸素濃度の雰囲気下で、カーボンが酸化されないような程度に急速に加熱する。たとえば焼成温度に設定した焼成炉に少量の金属酸化物ナノ粒子の前駆体とカーボンナノ粒子の複合体を投入することなどの手法によって急速加熱することができる。前記加熱温度は、金属酸化物の種類によって好適な温度範囲が異なる。すなわち、前記の温度範囲において、金属酸化物の結晶化が良好に進行するものであり、この温度未満では良好な結晶化の進行が得られず、この温度を越えると相転移によって、エネルギー貯蔵特性の良好な金属酸化物が得られない。
【0030】
(電極)
本発明により得られた金属酸化物ナノ粒子とカーボンの複合体は、バインダーと混錬、成型し、電気化学素子の電極、すなわち電気エネルギー貯蔵用電極とすることができ、その電極は高出力特性、高容量特性を示す。
【0031】
(電気化学素子)
この電極を用いることができる電気化学素子は、リチウムやマグネシウムなどの金属イオンを含有する電解液を用いる電気化学キャパシタ、電池である。すなわち、本発明の電極は、金属イオンの吸蔵、脱着を行うことができ、負極や正極として作動する。したがって、金属イオンを含有する電解液を用い、対極として活性炭、金属イオンが吸蔵、脱着するカーボンや金属酸化物等を用いることによって、電気化学キャパシタ、電池を構成することができる。
【実施例】
【0032】
以下、実施例により本発明をさらに具体的に説明する。
【0033】
(実施例1)
酢酸マンガン1モル、エタノール、水の混合溶液を作製した。この混合溶液とケッチェンブラック(KB)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、酸化マンガンの前駆体を高分散担持したKBを得た。
【0034】
得られた酸化マンガンの前駆体を高分散担持させたKBを、真空中において80℃で17時間乾燥することにより、酸化マンガンの前駆体がKBに高分散担持された複合体粉末を得た。
【0035】
得られた酸化マンガンの前駆体がKBに高分散担持された複合体粉末を、窒素雰囲気中で700℃まで急熱することによって酸化マンガンの結晶化を進行させ、酸化マンガンのナノ粒子がKBに高分散担持された複合体粉末を得た。
【0036】
この実施例1の複合体粉末のXRD分析結果とTEM像を図1〜図3に示す。図1に示すXRD分析からは、酸化マンガンが担持したKBが得られていることが分かる。
【0037】
図1〜図3のTEM像から分かるように、カーボンナノ粒子(ケッチェンブラックナノ粒子)がグラファイトフラグメントのビルディング構造を示し、特に、図2からは、カーボンナノ粒子に小径(数nm)の酸化マンガンナノ粒子が内包されていることが分かる。また、図3によれば、ケッチェンブラックのグラファイトが剥がれて薄い膜状になったグラフェン(KB−Graphene)が形成され、グラフェンの間に酸化マンガンナノ粒子が入り込んで、サンドイッチ状になっていることが観察できる。
【0038】
ついで、前記のように構成した実施例1の複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(MnO/KB/PVDF 40:40:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレンEC:炭酸ジメチルDEC(1:1 w/w)を浸透させて、セルとした。この状態で、作用電圧0−2Vとして、その充放電特性からエネルギー密度を算出した。結果は酸化マンガンあたり、691mAh/g(1C)、418mAh/g(3C)と高いエネルギー密度を示した。
【0039】
(実施例2−1)
酢酸鉄1モルに対して、リン酸1.0モル、酢酸リチウム1モルの水溶液を作製した。ここで反応抑制剤としてクエン酸を用いた。この溶液とカーボンナノファイバー(CNF)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、オリビン型リン酸鉄リチウムの前駆体を高分散担持したCNFを得た。この場合、混合溶媒に溶解する酢酸鉄、リン酸、酢酸リチウムとCNFの量は、得られる複合体の組成が、リン酸鉄リチウム/CNFが、50/50の質量比(w/w)となるように設定した。
【0040】
得られたリン酸鉄リチウムの前駆体を高分散担持させたCNFを、真空中において80℃で17時間乾燥することにより、リン酸鉄リチウムの前駆体がCNFに高分散担持された複合体粉末を得た。
【0041】
得られたリン酸鉄リチウムの前駆体がCNFに高分散担持された複合体粉末を、窒素雰囲気中で700℃まで急熱することによってリン酸鉄リチウムの結晶化を進行させ、リン酸鉄リチウムのナノ粒子がCNFに高分散担持された複合体粉末を得た。
【0042】
この実施例2−1の複合体粉末のXRD分析結果とTEM像を図4〜図6に、充放電挙動とこの結果から算出した容量を図8及び図9に示す。図4に示すXRD分析からリン酸鉄リチウムが担持したCNFが得られていることが分かる。
【0043】
図4〜図6のTEM像から分かるように、CNFナノ粒子がネット状に絡み合った構造を示していることが観察できる。また、高解像度TEM像を図7に示す。図24は、図7のさらに拡大写真とその模式図であって、この図24から分かるように、サヤエンドウのようなCNF内にリン酸鉄リチウムナノ粒子が入っている。図から分かるように、結晶構造体が透けて見え、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体(超薄膜構造体)に担持していることが分かる。
【0044】
図8は、実施例2−1の複合体を使用した電気化学素子の充放電特性を示すグラフである。すなわち、前記のように構成した実施例1の複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(LiFePO4/CNF/PVDF 40:40:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレン(EC):炭酸ジメチル(DEC)(1:1 w/w)を浸透させて、セルとした。この状態で、作用電圧2.0−4.2Vとして、その充放電特性を調べた。
【0045】
この図8から分かるように、複合体粉末あたりの容量が81mAh/gと優れた容量特性が確認された。また、図9に示す通り、従来の製品に比較して、より優れた出力特性を示した。すなわち、図9は、このリン酸鉄リチウムを使用した電気化学素子の60Cでのリン酸鉄リチウムあたりの容量を、従来発表されている各技術のおおよその容量と比較したグラフである。S.BLee(2008年)、D.Kim(2006年)、Y.Wang(2008年)、B.Kang(2009年)に比較して、本実施例の複合体を使用した素子の放電容量が増加している。さらに、図10に出力特性、図11にサイクル特性を示すが、出力特性、サイクル特性とも良好である。図10の放電出力特性は、前記図8と同様な条件下で、充電レート1Cに対して、放電レートを1/120/180/240/300/360Cに変化させて、その放電容量を計測したものである。この図10から分かるように、360Cにおける放電容量がリン酸鉄リチウム活物質当り70mAh/g、コンポジット当り35mAh/gと高い値を示している。図11のサイクル特性は、3000サイクル(10C)においても89%の放電容量を維持することができた。
【0046】
本実施例の複合体粉末について、BJH法(Barrett−Joyner−Halenda法)により、その細孔分布を測定したところ、図21に示すようにCNFの細孔分布は10〜50nmであるが、本願の複合体の細孔分布は20nmとなっており、50nmのCNFの空隙にリン酸鉄リチウムナノ粒子が担持され、20nmの細孔分布を有する複合体が形成されたことが分かる。すなわち、本実施例の複合体とCNFの細孔分布を算出し、これらのメソ孔について観察した。図21のグラフ中、四角が複合体、丸がCNFのプロットである。まずCNFはdV/d(logr)の値より、10〜50nmのメソ孔を多く有していることが分かる。また、このCNFにリン酸鉄を複合化すると細孔分布に大きな変化がみられる。10〜50nmの細孔径が大幅に減少し20nm周辺の細孔分布が維持される。また、これはdV/drにも顕著にその傾向が見られる。この結果より、リン酸鉄のCNFへの担時はCNFの10〜50nmの細孔径の間隙で起こり、さらに20nm付近の細孔径を有するメソ孔のネットワークを構築することが分かる。したがって、この複合体電極は良好なイオンパスを構築できていると推測される。
【0047】
(実施例2−2)
リン酸鉄リチウム/CNFが、60/40の質量比(w/w)となるように設定する以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は71mAh/gであった。また、図12にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体がCNFに担持していることが分かる。
【0048】
(実施例2−3)
カーボンとしてケッチェンブラックを用いた以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は108mAh/gであった。また、図13にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜20nmの平板上のリン酸鉄リチウム結晶構造体がケッチェンブラックに内包されていることが分かる。図25は、この実施例2−3の複合体粉末の高解像度TEM像とその模式図を示すものである。この実施例2−3では、ホオヅキのように中空で球状のカーボンの中にリン酸鉄リチウムナノ粒子が1粒ずつ入っているような構造になっている。
【0049】
(実施例2−4)
リン酸鉄リチウム/ケッチェンブラックが、60/40の質量比(w/w)となるように設定する以外は、実施例2−3と同様にしてセルを作製した。このセルの容量は102mAh/gであった。
【0050】
(実施例2−5)
カーボンとしてキャボット社製、BP2000を用いた以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は88mAh/gであった。また、図14にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体がBP2000に担持していることが分かる。
【0051】
(実施例2−6)
リン酸鉄リチウム/BP2000が、60/40の質量比(w/w)となるように設定する以外は、実施例2−3と同様にしてセルを作製した。このセルの容量は96mAh/gであった。
【0052】
(実施例3)
チタンアルコキシド1モルに対して、酢酸1.8モル、酢酸リチウム1モルとなる量の酢酸と酢酸リチウムをイソプロパノールと水の混合物に溶解して混合溶媒を作製した。この混合溶媒とチタンアルコキシド、カーボンナノファイバー(CNF)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、チタン酸リチウムの前駆体を高分散担持したCNFを得た。この場合、混合溶媒に溶解するチタンアルコキシドとCNFの量は、得られる複合体の組成が、チタン酸リチウム/CNFが、70/30の質量比(w/w)となるように設定した。
【0053】
得られたチタン酸リチウムの前駆体を高分散担持させたCNFを、真空中において80℃で17時間乾燥することにより、チタン酸リチウムの前駆体がCNFに高分散担持された複合体粉末を得た。
【0054】
得られたチタン酸リチウムの前駆体がCNFに高分散担持された複合体粉末を、窒素雰囲気中において800℃まで急速加熱することによってリチウムを含有するチタン酸化物の結晶化を進行させ、チタン酸リチウムのナノ粒子がCNFに高分散担持された複合体粉末を得た。
【0055】
このようにして得られた実施例3のチタン酸リチウムナノ粒子を担持したカーボンのTEM像を図15に示した。図15においては5nm〜20nmのチタン酸リチウムのナノ粒子がCNFに高分散担持していることが分かる。
【0056】
特に、図15のTEM像にみられるように、本発明の「チタン酸リチウムナノ粒子とカーボンの複合体」は、CNFがつながった「グラファイトフラグメントのビルディング構造」をとっており、この構造体にチタン酸リチウムナノ粒子が高分散担持されている。
【0057】
図16に、実施例3のチタン酸リチウムの前駆体を高分散担持したCNFを高解像度TEMで観察した図を示す。図16から分かるように、チタン酸リチウムナノ粒子は、結晶構造体が透けて見え、2〜5原子層レベルで1nm以下の厚みを有し、一辺が5〜10nmの平板上のチタン酸リチウム結晶構造体となっている。このような超薄膜構造体は厚みが極度に薄く、体積あたりの表面積が極度に大きい。したがって、高い出力特性を示すことができる。
【0058】
すなわち、体積あたりの表面積について、厚みが無限にゼロに近いシートの表面積が最も大きいが、実施例3のシートは、厚みがゼロに近い数原子層レベルの厚みを持つ構造を有している。以上の超薄膜構造体は旋回する反応器内で金属酸化物の出発原料とカーボン粉末とを含む溶液にずり応力と遠心力を加えて反応させるとともに、その後の急速加熱処理によって形成されるものと思われるが、リン酸鉄リチウムでも観察されたように、チタン酸リチウム以外の金属酸化物ナノ粒子も超薄膜構造体となっている。
【0059】
前記のように構成した実施例3で得られた複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(Li4Ti5O12/CNF/PVDF 56:24:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 四フッ化ホウ酸リチウム(LiBF4)/炭酸エチレン(EC):炭酸ジメチル(DEC)(1:1 w/w)を浸透させて、セルとした。
【0060】
前記のようにして得られた実施例3と、同じ条件で真空中において加熱した比較例1の複合体粉末を用いた電極を有するセルについて、その充放電挙動とそれに基づいて算出した容量を図17に、出力特性を図18に示す。図17及び図18において、左側のグラフが実施例3、右側のグラフが比較例1を示している。この場合、作用電圧は1.0−3.0Vであり、スキャンレートは10Cである。
【0061】
図17から分かるように、窒素雰囲気中で加熱した実施例3の複合体粉末を使用したセルは、真空中で加熱した比較例1の複合体粉末を使用したセルに比較して、容量が増加していることが分かる。特に、比較例1の真空中で800℃まで加熱した複合体粉末を使用したセルが、従来技術では最も容量が大きかったが、実施例3のセルはいずれも、比較例1の容量を大きく上回っている。
【0062】
図18は、横軸にC-rateを、縦軸に放電容量維持率(%)を取った各セルの出力特性を示すグラフである。この図18から分かるように、C-rateが200Cの時点における放電容量維持率は、実施例3のセルが比較例1のセルを大きく上回っている。
【0063】
(実施例4)
実施例2−1で作製した作用電極を正極とし、実施例3で作製した作用電極を負極とし、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレン(EC):炭酸ジメチル(DMC)(1:1 w/w)を用いて、電気化学素子を作製した。この電気化学素子について、エネルギー密度とパワー密度を測定した結果を図19に示す。
【0064】
この図19は、実施例4の電気化学素子と、正極に活性炭電極を使用し負極に実施例3で作成した作用電極を使用した電気化学素子と、正極及び負極に活性炭を使用した電気二重層キャパシタ(EDLC)のそれぞれについて、エネルギー密度と出力特性を測定したラゴンプロットである。この図19から分かるように、実施例4の電気化学素子は、高いエネルギー密度と高い出力特性を有する、高出力エネルギー貯蔵デバイスを実現している。
【0065】
(実施例5)
Li4Ti5O12/CNF複合体の合成には、チタン源にTi(OC4H9)4を、リチウム源にCH3COOLiを用いた。これらの原料を、Li4Ti5O12/CNF全体に対して10〜40wt%のCNFや有機溶媒などと共に超遠心力処理(UC処理)を行い、前駆体を得た。その後、高温短時間焼成を行うことにより高結晶性ナノ粒子Li4Ti5O12/CNF複合体を得た。本複合体を、PVDFを用いて電極化し、対極にLi金属、電解液に1M LiBF4/EC+DMC 1:1(in volume)を用いたハーフセルにより、電気化学特性を評価した。充放電試験の結果、出力特性はLi4Ti5O12の重量比に依存することがわかった。また、図22から分かるように、高出力特性の要求される600Cにおいても10C容量の81%(87mAh/g)を、さらに1200Cにおいても68%(72mAh/g)の容量を維持した。
【0066】
この実施例5の複合体について、XRD分析を行った結果、図23に示すように、CNF含有比率が20%の(111)面の結晶サイズは30〜50%に比べて大きく、チタン酸リチウムナノ粒子の結晶は、(111)面が大きい、超薄膜構造体になっていることが確認された。
【技術分野】
【0001】
本発明は、金属酸化物ナノ粒子とカーボンの複合体、その製造方法、この複合体を用いた電極及び電気化学素子に関する。
【背景技術】
【0002】
現在、リチウム電池の電極としてリチウムを貯蔵、放出するカーボン材料等が用いられているが、マイナス電位が水素の還元分解電位より小さいので電解液の分解という危険性がある。そこで、特許文献1や特許文献2に記載のように、マイナス電位が水素の還元分解電位より大きいチタン酸リチウムの使用が検討されているが、チタン酸リチウムは出力特性が低いという問題点がある。そこで、チタン酸リチウムをナノ粒子化し、炭素に担持させた電極によって、出力特性を向上する試みがある。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2007−160151号公報
【特許文献2】特開2008−270795号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
これらの特許文献に記載の発明は、旋回する反応器内で反応物にずり応力と遠心力を加えて、化学反応を促進させる方法(一般に、メカノケミカル反応と呼ばれる)によって、カーボンに分散担持されたチタン酸リチウムを得るものである。この場合、反応物としては、例えば、チタン酸リチウムの出発原料であるチタンアルコキシドと酢酸リチウム、及びカーボンナノチューブやケッチェンブラック等のカーボン、酢酸等を使用する。
【0005】
これらの特許文献に記載のチタン酸リチウムナノ粒子を担持したカーボンを使用した電極は、優れた出力特性を発揮するものの、最近では、この種の電極において、さらに出力特性を向上させ、電気伝導度を向上させる要求がある。
【0006】
また、チタン酸リチウムナノ粒子に限らず、他の金属酸化ナノ粒子についても、これをカーボンに担持させた複合体を製造し、それによって、より優れた出力特性を有する電極や電気化学素子を得ようとする要求もある。特に、酸化マンガンのようなリチウムに比べて安価な金属酸化物の使用が望まれている。
【0007】
本発明は、上述したような従来技術の問題点を解決するために提案されたものであって、その目的は、出力特性及び電気伝導度の向上を可能とした電極や電気化学素子を得ることのできる金属酸化物ナノ粒子とカーボンの複合体、及びその製造方法を提供することにある。また、本発明の他の目的は、前記複合体を用いた電極及び電気化学素子を提供することにある。
【課題を解決するための手段】
【0008】
前記の目的を達成するため、本発明の金属酸化物ナノ粒子とカーボンの複合体の製造方法は、金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物ナノ粒子の結晶化を進行させ、金属酸化物ナノ粒子をカーボンに高分散担持させることを特徴とする。この場合、前記急速加熱処理が、前記複合体を窒素雰囲気中で、400〜1000℃に加熱するものであること、前記金属酸化物ナノ粒子が2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上の結晶構造体(超薄膜構造体)であることも、本発明の一態様である。更に、前記のような方法で製造した複合体、この複合体を用いた電極や電気化学素子も本発明に包含される。
【発明の効果】
【0009】
本発明によれば、金属酸化物ナノ粒子の前駆体を担持したカーボンの焼成工程において、急速加熱処理することによって、金属酸化物ナノ粒子の良好な結晶化を進行することができ、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上の結晶構造体が形成される。
【図面の簡単な説明】
【0010】
【図1】実施例1の複合体のXRD分析結果とTEM像を示す図面代用写真。
【図2】実施例1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図3】実施例1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図4】実施例2−1の複合体のXRD分析結果とTEM像を示す図面代用写真。
【図5】実施例2−1の複合体の他の部分のTEM像を示す図面代用写真。
【図6】実施例2−1の複合体の他の部分の拡大TEM像を示す図面代用写真。
【図7】実施例2−1の高解像度TEM像を示す図面代用写真。
【図8】実施例2−1の複合体を使用した電気化学素子の充放電特性を示すグラフ。
【図9】実施例2−1の複合体を使用した電気化学素子と、従来の電気化学素子の充放電特性を比較したグラフ。
【図10】実施例2−1の複合体を使用した電気化学素子の出力特性を示すグラフ。
【図11】実施例2−1の複合体を使用した電気化学素子のサイクル特性を示すグラフ。
【図12】実施例2−2の複合体の高解像度TEM像を示す図面代用写真。
【図13】実施例2−3の複合体の高解像度TEM像を示す図面代用写真。
【図14】実施例2−5の複合体の高解像度TEM像を示す図面代用写真。
【図15】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体のTEM像を示す図面代用写真。
【図16】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の拡大したTEM像を示す図面代用写真。
【図17】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の放電挙動特性を示すグラフ。
【図18】実施例3のチタン酸リチウムナノ粒子とカーボンの複合体の出力特性を示すグラフ。
【図19】実施例4の高出力エネルギー貯蔵デバイスの特性を示すグラフ。
【図20】本発明の製造方法に使用する反応器の一例を示す斜視図。
【図21】実施例2−1のリン酸鉄リチウムナノ粒子とカーボンの複合体の細孔分布を示す図面代用写真及びグラフ。
【図22】実施例5の充放電特性を示すグラフ。
【図23】実施例5のXRD分析を行った結果を示すグラフ。
【図24】実施例2−1の拡大写真とその模式図。
【図25】実施例2−3の複合体粉末の高解像度TEM像とその模式図。
【発明を実施するための形態】
【0011】
本発明を実施するための形態について、以下、説明する。
【0012】
(メカノケミカル反応)
本発明で用いる反応方法は、本出願人等が先に特許出願した特許文献1及び特許文献2に示した方法と同様のメカノケミカル反応であって、化学反応の過程で、旋回する反応器内で反応物にずり応力と遠心力を加えて化学反応を促進させるものである。
【0013】
この反応方法は、例えば、図20に示すような反応器を用いて行うことができる。図20に示すように、反応器は、開口部にせき板1−2を有する外筒1と、貫通孔2−1を有し旋回する内筒2からなる。この反応器の内筒内部に反応物を投入し、内筒を旋回することによってその遠心力で内筒内部の反応物が内筒の貫通孔を通って外筒の内壁1−3に移動する。この時反応物は内筒の遠心力によって外筒の内壁に衝突し、薄膜状となって内壁の上部へずり上がる。この状態では反応物には内壁との間のずり応力と内筒からの遠心力の双方が同時に加わり、薄膜状の反応物に大きな機械的エネルギーが加わることになる。この機械的なエネルギーが反応に必要な化学エネルギー、いわゆる活性化エネルギーに転化するものと思われるが、短時間で反応が進行する。
【0014】
この反応において、薄膜状であると反応物に加えられる機械的エネルギーは大きなものとなるため、薄膜の厚みは5mm以下、好ましくは2.5mm以下、さらに好ましくは1.0mm以下である。なお、薄膜の厚みはせき板の幅、反応液の量によって設定することができる。
【0015】
この反応方法は、反応物に加えられるずり応力と遠心力の機械的エネルギーによって実現できるものと考えられるが、このずり応力と遠心力は内筒内の反応物に加えられる遠心力によって生じる。したがって、本発明に必要な内筒内の反応物に加えられる遠心力は1500N(kgms-2)以上、好ましくは60000N(kgms-2)以上、さらに好ましくは270000N(kgms-2)以上である。
【0016】
この反応方法においては、反応物にずり応力と遠心力の双方の機械的エネルギーが同時に加えられることによって、このエネルギーが化学エネルギーに転化することによるものと思われるが、従来にない速度で化学反応を促進させることができる。
【0017】
(金属酸化物)
本発明に係る金属酸化物ナノ粒子を生成するための金属酸化物としては、例えば、酸化マンガンMnO、リン酸鉄リチウムLiFePO4、チタン酸リチウムLi4Ti5O12が使用できる。また、その他の酸化物として、MxOz、AxMyOz、Mx(DO4)y、AxMy(DO4)z(ただし、M:金属元素 A:アルカリ金属又はランタノイド元素)で表される金属酸化物の使用も可能である。
【0018】
酸化マンガンMnOの場合は、例えば、過マンガン酸ナトリウム、酢酸マンガン、硝酸マンガン、硫酸マンガンなどのマンガン源及びカーボンを出発原料として、前記メカノケミカル反応により、酸化マンガンナノ粒子の前駆体とこれを分散担持したカーボンの複合体を生成する。この複合体を窒素雰囲気中で急速加熱することにより、本発明の金属酸化物である酸化マンガンとカーボンの複合体が生成される。
【0019】
リン酸鉄リチウムLiFePO4の場合は、例えば、過マンガン酸ナトリウム、酢酸マンガン、硝酸マンガン、硫酸マンガンなどのマンガン源及びカーボンを出発原料として、前記メカノケミカル反応により、リン酸鉄リチウムナノ粒子の前駆体とこれを分散担持したカーボンの複合体を生成する。この複合体を窒素雰囲気中で急速加熱することにより、本発明の金属酸化物であるリン酸鉄リチウムとカーボンの複合体が生成される。
【0020】
チタン酸リチウムLi4Ti5O12の場合は、例えば、チタンアルコキシドなどのチタン源、酢酸リチウム、硝酸リチウム、炭酸リチウム、水酸化リチウムなどのリチウム源を出発原料として使用し、前記メカノケミカル反応により、チタン酸リチウムナノ粒子の前駆体を生成する。このチタン酸リチウムナノ粒子の前駆体を窒素雰囲気中で加熱することにより、酸素欠陥のサイトに窒素がドープされた本発明のチタン酸リチウムナノ粒子が生成される。
【0021】
(カーボン)
反応過程で所定のカーボンを加えることによって、5〜100nmのチタン酸リチウムを高分散担持させたカーボンを得ることができる。すなわち、反応器の内筒の内部に金属塩と所定の反応抑制剤とカーボンを投入して、内筒を旋回して金属塩と反応抑制剤とカーボンを混合、分散する。さらに内筒を旋回させながら水酸化ナトリウムなどの触媒を投入して加水分解、縮合反応を進行させ、金属酸化物を生成すると共に、この金属酸化物とカーボンを分散状態で、混合する。反応終了後にこれを急速加熱することで、金属酸化物ナノ粒子を高分散担持させたカーボンを形成することができる。
【0022】
ここで用いるカーボンとしては、ケッチェンブラック、アセチレンブラック等のカーボンブラック、カーボンナノチューブ、カーボンナノホーン、無定形炭素、炭素繊維、天然黒鉛、人造黒鉛、活性炭、メソポーラス炭素、気相炭素繊維等を挙げることができ、これらの複合材を用いることもできる。
【0023】
(溶媒)
溶媒としては、アルコール類、水、これらの混合溶媒を用いることができる。例えば、酢酸と酢酸リチウムをイソプロパノールと水の混合物に溶解した混合溶媒を使用することができる。
【0024】
(反応抑制剤)
出発原料として金属アルコキシドを使用した場合には、特許文献2に記載のように、前記メカノケミカル反応を適用する所定の金属アルコキシドに、反応抑制剤として該金属アルコキシドと錯体を形成する所定の化合物を添加することができる。これにより、化学反応が促進しすぎるのを抑制することができる。
【0025】
すなわち、金属アルコキシドに、これと錯体を形成する酢酸等の所定の化合物を該金属アルコキシド1モルに対して、1〜3モル添加して錯体を形成することにより、反応を抑制、制御することができることが分かった。なお、この反応によって生成されるのは、金属と酸化物の複合体のナノ粒子、例えば、チタン酸リチウムの前駆体である、リチウムと酸化チタンの複合体のナノ粒子であり、これを焼成することにより、チタン酸リチウムの結晶が得られる。
【0026】
このように、反応抑制剤として酢酸等の所定の化合物を添加することにより、化学反応が促進しすぎるのを抑制することができるのは、酢酸等の所定の化合物が金属アルコキシドと安定な錯体を形成するためであると考えられる。
【0027】
金属アルコキシドと錯体を形成することができる物質としては、酢酸の他、クエン酸、蓚酸、ギ酸、乳酸、酒石酸、フマル酸、コハク酸、プロピオン酸、レプリン酸等のカルボン酸、EDTA等のアミノポリカルボン酸、トリエタノールアミン等のアミノアルコールに代表される錯化剤が挙げられる。
【0028】
(加熱)
本発明は、メカノケミカル反応によりカーボンナノ粒子の構造体の内部に金属酸化物ナノ粒子の前駆体を担持させた複合体を得ると共に、この金属酸化物とカーボンの複合体を窒素雰囲気中で加熱することによって、金属酸化物の結晶化を促進させ、この複合体を使用した電極や電気化学素子の容量、出力特性を向上させるものである。
【0029】
すなわち、得られた金属酸化物ナノ粒子の前駆体とカーボンナノ粒子の複合体の焼成工程において、室温から400〜1000℃まで急熱することによって、金属酸化物ナノ粒子の凝集を防止することができ、粒径の小さなナノ粒子が形成されることが分かった。急速加熱とは、酸素濃度が1000ppm程度の低酸素濃度の雰囲気下で、カーボンが酸化されないような程度に急速に加熱する。たとえば焼成温度に設定した焼成炉に少量の金属酸化物ナノ粒子の前駆体とカーボンナノ粒子の複合体を投入することなどの手法によって急速加熱することができる。前記加熱温度は、金属酸化物の種類によって好適な温度範囲が異なる。すなわち、前記の温度範囲において、金属酸化物の結晶化が良好に進行するものであり、この温度未満では良好な結晶化の進行が得られず、この温度を越えると相転移によって、エネルギー貯蔵特性の良好な金属酸化物が得られない。
【0030】
(電極)
本発明により得られた金属酸化物ナノ粒子とカーボンの複合体は、バインダーと混錬、成型し、電気化学素子の電極、すなわち電気エネルギー貯蔵用電極とすることができ、その電極は高出力特性、高容量特性を示す。
【0031】
(電気化学素子)
この電極を用いることができる電気化学素子は、リチウムやマグネシウムなどの金属イオンを含有する電解液を用いる電気化学キャパシタ、電池である。すなわち、本発明の電極は、金属イオンの吸蔵、脱着を行うことができ、負極や正極として作動する。したがって、金属イオンを含有する電解液を用い、対極として活性炭、金属イオンが吸蔵、脱着するカーボンや金属酸化物等を用いることによって、電気化学キャパシタ、電池を構成することができる。
【実施例】
【0032】
以下、実施例により本発明をさらに具体的に説明する。
【0033】
(実施例1)
酢酸マンガン1モル、エタノール、水の混合溶液を作製した。この混合溶液とケッチェンブラック(KB)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、酸化マンガンの前駆体を高分散担持したKBを得た。
【0034】
得られた酸化マンガンの前駆体を高分散担持させたKBを、真空中において80℃で17時間乾燥することにより、酸化マンガンの前駆体がKBに高分散担持された複合体粉末を得た。
【0035】
得られた酸化マンガンの前駆体がKBに高分散担持された複合体粉末を、窒素雰囲気中で700℃まで急熱することによって酸化マンガンの結晶化を進行させ、酸化マンガンのナノ粒子がKBに高分散担持された複合体粉末を得た。
【0036】
この実施例1の複合体粉末のXRD分析結果とTEM像を図1〜図3に示す。図1に示すXRD分析からは、酸化マンガンが担持したKBが得られていることが分かる。
【0037】
図1〜図3のTEM像から分かるように、カーボンナノ粒子(ケッチェンブラックナノ粒子)がグラファイトフラグメントのビルディング構造を示し、特に、図2からは、カーボンナノ粒子に小径(数nm)の酸化マンガンナノ粒子が内包されていることが分かる。また、図3によれば、ケッチェンブラックのグラファイトが剥がれて薄い膜状になったグラフェン(KB−Graphene)が形成され、グラフェンの間に酸化マンガンナノ粒子が入り込んで、サンドイッチ状になっていることが観察できる。
【0038】
ついで、前記のように構成した実施例1の複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(MnO/KB/PVDF 40:40:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレンEC:炭酸ジメチルDEC(1:1 w/w)を浸透させて、セルとした。この状態で、作用電圧0−2Vとして、その充放電特性からエネルギー密度を算出した。結果は酸化マンガンあたり、691mAh/g(1C)、418mAh/g(3C)と高いエネルギー密度を示した。
【0039】
(実施例2−1)
酢酸鉄1モルに対して、リン酸1.0モル、酢酸リチウム1モルの水溶液を作製した。ここで反応抑制剤としてクエン酸を用いた。この溶液とカーボンナノファイバー(CNF)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、オリビン型リン酸鉄リチウムの前駆体を高分散担持したCNFを得た。この場合、混合溶媒に溶解する酢酸鉄、リン酸、酢酸リチウムとCNFの量は、得られる複合体の組成が、リン酸鉄リチウム/CNFが、50/50の質量比(w/w)となるように設定した。
【0040】
得られたリン酸鉄リチウムの前駆体を高分散担持させたCNFを、真空中において80℃で17時間乾燥することにより、リン酸鉄リチウムの前駆体がCNFに高分散担持された複合体粉末を得た。
【0041】
得られたリン酸鉄リチウムの前駆体がCNFに高分散担持された複合体粉末を、窒素雰囲気中で700℃まで急熱することによってリン酸鉄リチウムの結晶化を進行させ、リン酸鉄リチウムのナノ粒子がCNFに高分散担持された複合体粉末を得た。
【0042】
この実施例2−1の複合体粉末のXRD分析結果とTEM像を図4〜図6に、充放電挙動とこの結果から算出した容量を図8及び図9に示す。図4に示すXRD分析からリン酸鉄リチウムが担持したCNFが得られていることが分かる。
【0043】
図4〜図6のTEM像から分かるように、CNFナノ粒子がネット状に絡み合った構造を示していることが観察できる。また、高解像度TEM像を図7に示す。図24は、図7のさらに拡大写真とその模式図であって、この図24から分かるように、サヤエンドウのようなCNF内にリン酸鉄リチウムナノ粒子が入っている。図から分かるように、結晶構造体が透けて見え、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体(超薄膜構造体)に担持していることが分かる。
【0044】
図8は、実施例2−1の複合体を使用した電気化学素子の充放電特性を示すグラフである。すなわち、前記のように構成した実施例1の複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(LiFePO4/CNF/PVDF 40:40:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレン(EC):炭酸ジメチル(DEC)(1:1 w/w)を浸透させて、セルとした。この状態で、作用電圧2.0−4.2Vとして、その充放電特性を調べた。
【0045】
この図8から分かるように、複合体粉末あたりの容量が81mAh/gと優れた容量特性が確認された。また、図9に示す通り、従来の製品に比較して、より優れた出力特性を示した。すなわち、図9は、このリン酸鉄リチウムを使用した電気化学素子の60Cでのリン酸鉄リチウムあたりの容量を、従来発表されている各技術のおおよその容量と比較したグラフである。S.BLee(2008年)、D.Kim(2006年)、Y.Wang(2008年)、B.Kang(2009年)に比較して、本実施例の複合体を使用した素子の放電容量が増加している。さらに、図10に出力特性、図11にサイクル特性を示すが、出力特性、サイクル特性とも良好である。図10の放電出力特性は、前記図8と同様な条件下で、充電レート1Cに対して、放電レートを1/120/180/240/300/360Cに変化させて、その放電容量を計測したものである。この図10から分かるように、360Cにおける放電容量がリン酸鉄リチウム活物質当り70mAh/g、コンポジット当り35mAh/gと高い値を示している。図11のサイクル特性は、3000サイクル(10C)においても89%の放電容量を維持することができた。
【0046】
本実施例の複合体粉末について、BJH法(Barrett−Joyner−Halenda法)により、その細孔分布を測定したところ、図21に示すようにCNFの細孔分布は10〜50nmであるが、本願の複合体の細孔分布は20nmとなっており、50nmのCNFの空隙にリン酸鉄リチウムナノ粒子が担持され、20nmの細孔分布を有する複合体が形成されたことが分かる。すなわち、本実施例の複合体とCNFの細孔分布を算出し、これらのメソ孔について観察した。図21のグラフ中、四角が複合体、丸がCNFのプロットである。まずCNFはdV/d(logr)の値より、10〜50nmのメソ孔を多く有していることが分かる。また、このCNFにリン酸鉄を複合化すると細孔分布に大きな変化がみられる。10〜50nmの細孔径が大幅に減少し20nm周辺の細孔分布が維持される。また、これはdV/drにも顕著にその傾向が見られる。この結果より、リン酸鉄のCNFへの担時はCNFの10〜50nmの細孔径の間隙で起こり、さらに20nm付近の細孔径を有するメソ孔のネットワークを構築することが分かる。したがって、この複合体電極は良好なイオンパスを構築できていると推測される。
【0047】
(実施例2−2)
リン酸鉄リチウム/CNFが、60/40の質量比(w/w)となるように設定する以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は71mAh/gであった。また、図12にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体がCNFに担持していることが分かる。
【0048】
(実施例2−3)
カーボンとしてケッチェンブラックを用いた以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は108mAh/gであった。また、図13にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜20nmの平板上のリン酸鉄リチウム結晶構造体がケッチェンブラックに内包されていることが分かる。図25は、この実施例2−3の複合体粉末の高解像度TEM像とその模式図を示すものである。この実施例2−3では、ホオヅキのように中空で球状のカーボンの中にリン酸鉄リチウムナノ粒子が1粒ずつ入っているような構造になっている。
【0049】
(実施例2−4)
リン酸鉄リチウム/ケッチェンブラックが、60/40の質量比(w/w)となるように設定する以外は、実施例2−3と同様にしてセルを作製した。このセルの容量は102mAh/gであった。
【0050】
(実施例2−5)
カーボンとしてキャボット社製、BP2000を用いた以外は、実施例2−1と同様にしてセルを作製した。このセルの容量は88mAh/gであった。また、図14にこの複合体粉末の高解像度TEM像を示す。この図から分かるように、2〜5原子層レベルで1nm以下の厚みを有し、径が5〜100nmの平板上のリン酸鉄リチウム結晶構造体がBP2000に担持していることが分かる。
【0051】
(実施例2−6)
リン酸鉄リチウム/BP2000が、60/40の質量比(w/w)となるように設定する以外は、実施例2−3と同様にしてセルを作製した。このセルの容量は96mAh/gであった。
【0052】
(実施例3)
チタンアルコキシド1モルに対して、酢酸1.8モル、酢酸リチウム1モルとなる量の酢酸と酢酸リチウムをイソプロパノールと水の混合物に溶解して混合溶媒を作製した。この混合溶媒とチタンアルコキシド、カーボンナノファイバー(CNF)を旋回反応器内に投入し、66,000N(kgms-2)の遠心力で5分間、内筒を旋回して外筒の内壁に反応物の薄膜を形成すると共に、反応物にずり応力と遠心力を加えて化学反応を促進させ、チタン酸リチウムの前駆体を高分散担持したCNFを得た。この場合、混合溶媒に溶解するチタンアルコキシドとCNFの量は、得られる複合体の組成が、チタン酸リチウム/CNFが、70/30の質量比(w/w)となるように設定した。
【0053】
得られたチタン酸リチウムの前駆体を高分散担持させたCNFを、真空中において80℃で17時間乾燥することにより、チタン酸リチウムの前駆体がCNFに高分散担持された複合体粉末を得た。
【0054】
得られたチタン酸リチウムの前駆体がCNFに高分散担持された複合体粉末を、窒素雰囲気中において800℃まで急速加熱することによってリチウムを含有するチタン酸化物の結晶化を進行させ、チタン酸リチウムのナノ粒子がCNFに高分散担持された複合体粉末を得た。
【0055】
このようにして得られた実施例3のチタン酸リチウムナノ粒子を担持したカーボンのTEM像を図15に示した。図15においては5nm〜20nmのチタン酸リチウムのナノ粒子がCNFに高分散担持していることが分かる。
【0056】
特に、図15のTEM像にみられるように、本発明の「チタン酸リチウムナノ粒子とカーボンの複合体」は、CNFがつながった「グラファイトフラグメントのビルディング構造」をとっており、この構造体にチタン酸リチウムナノ粒子が高分散担持されている。
【0057】
図16に、実施例3のチタン酸リチウムの前駆体を高分散担持したCNFを高解像度TEMで観察した図を示す。図16から分かるように、チタン酸リチウムナノ粒子は、結晶構造体が透けて見え、2〜5原子層レベルで1nm以下の厚みを有し、一辺が5〜10nmの平板上のチタン酸リチウム結晶構造体となっている。このような超薄膜構造体は厚みが極度に薄く、体積あたりの表面積が極度に大きい。したがって、高い出力特性を示すことができる。
【0058】
すなわち、体積あたりの表面積について、厚みが無限にゼロに近いシートの表面積が最も大きいが、実施例3のシートは、厚みがゼロに近い数原子層レベルの厚みを持つ構造を有している。以上の超薄膜構造体は旋回する反応器内で金属酸化物の出発原料とカーボン粉末とを含む溶液にずり応力と遠心力を加えて反応させるとともに、その後の急速加熱処理によって形成されるものと思われるが、リン酸鉄リチウムでも観察されたように、チタン酸リチウム以外の金属酸化物ナノ粒子も超薄膜構造体となっている。
【0059】
前記のように構成した実施例3で得られた複合体粉末をバインダーとしてのポリフッ化ビニリデンPVDFと共に(Li4Ti5O12/CNF/PVDF 56:24:20)、SUS板上に溶接されたSUSメッシュ中に投入し、作用電極W.E.とした。前記電極上にセパレータと対極C.E.及び参照極としてLiフォイルを乗せ、電解液として、1.0M 四フッ化ホウ酸リチウム(LiBF4)/炭酸エチレン(EC):炭酸ジメチル(DEC)(1:1 w/w)を浸透させて、セルとした。
【0060】
前記のようにして得られた実施例3と、同じ条件で真空中において加熱した比較例1の複合体粉末を用いた電極を有するセルについて、その充放電挙動とそれに基づいて算出した容量を図17に、出力特性を図18に示す。図17及び図18において、左側のグラフが実施例3、右側のグラフが比較例1を示している。この場合、作用電圧は1.0−3.0Vであり、スキャンレートは10Cである。
【0061】
図17から分かるように、窒素雰囲気中で加熱した実施例3の複合体粉末を使用したセルは、真空中で加熱した比較例1の複合体粉末を使用したセルに比較して、容量が増加していることが分かる。特に、比較例1の真空中で800℃まで加熱した複合体粉末を使用したセルが、従来技術では最も容量が大きかったが、実施例3のセルはいずれも、比較例1の容量を大きく上回っている。
【0062】
図18は、横軸にC-rateを、縦軸に放電容量維持率(%)を取った各セルの出力特性を示すグラフである。この図18から分かるように、C-rateが200Cの時点における放電容量維持率は、実施例3のセルが比較例1のセルを大きく上回っている。
【0063】
(実施例4)
実施例2−1で作製した作用電極を正極とし、実施例3で作製した作用電極を負極とし、電解液として、1.0M 六フッ化リン酸リチウム(LiPF6)/炭酸エチレン(EC):炭酸ジメチル(DMC)(1:1 w/w)を用いて、電気化学素子を作製した。この電気化学素子について、エネルギー密度とパワー密度を測定した結果を図19に示す。
【0064】
この図19は、実施例4の電気化学素子と、正極に活性炭電極を使用し負極に実施例3で作成した作用電極を使用した電気化学素子と、正極及び負極に活性炭を使用した電気二重層キャパシタ(EDLC)のそれぞれについて、エネルギー密度と出力特性を測定したラゴンプロットである。この図19から分かるように、実施例4の電気化学素子は、高いエネルギー密度と高い出力特性を有する、高出力エネルギー貯蔵デバイスを実現している。
【0065】
(実施例5)
Li4Ti5O12/CNF複合体の合成には、チタン源にTi(OC4H9)4を、リチウム源にCH3COOLiを用いた。これらの原料を、Li4Ti5O12/CNF全体に対して10〜40wt%のCNFや有機溶媒などと共に超遠心力処理(UC処理)を行い、前駆体を得た。その後、高温短時間焼成を行うことにより高結晶性ナノ粒子Li4Ti5O12/CNF複合体を得た。本複合体を、PVDFを用いて電極化し、対極にLi金属、電解液に1M LiBF4/EC+DMC 1:1(in volume)を用いたハーフセルにより、電気化学特性を評価した。充放電試験の結果、出力特性はLi4Ti5O12の重量比に依存することがわかった。また、図22から分かるように、高出力特性の要求される600Cにおいても10C容量の81%(87mAh/g)を、さらに1200Cにおいても68%(72mAh/g)の容量を維持した。
【0066】
この実施例5の複合体について、XRD分析を行った結果、図23に示すように、CNF含有比率が20%の(111)面の結晶サイズは30〜50%に比べて大きく、チタン酸リチウムナノ粒子の結晶は、(111)面が大きい、超薄膜構造体になっていることが確認された。
【特許請求の範囲】
【請求項1】
旋回する反応器内で金属酸化物の出発原料とカーボン粉末とを含む溶液にずり応力と遠心力を加えて反応させ、金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物の結晶化を進行させ、超薄膜構造体を有する、金属酸化物ナノ粒子をカーボンに高分散担持させることを特徴とする金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項2】
前記急速加熱処理が、前記複合体を窒素雰囲気中で、400〜1000℃に加熱するものであることを特徴とする請求項1に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項3】
前記反応器内において、反応物と共に反応抑制剤を含む溶液にずり応力と遠心力を加えて反応させることを特徴とする請求項2に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項4】
前記金属酸化物が、MxOz、AxMyOz、Mx(DO4)y、AxMy(DO4)z(ただし、M:金属元素 A:アルカリ金属又はランタノイド元素)で表されるものである請求項1から請求項3のいずれか1項に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項5】
前記金属酸化物が、酸化マンガンMnO、リン酸鉄リチウムLiFePO4、チタン酸リチウムLi4Ti5O12のいずれかである請求項4に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項6】
請求項1から請求項5のいずれか1項に記載の方法で製造した金属酸化物ナノ粒子とカーボンの複合体。
【請求項7】
前記請求項6に記載の複合体をバインダーと混合した後、成形して得られる電極。
【請求項8】
請求項7に記載の電極を用いた電気化学素子。
【請求項9】
正極にリン酸鉄リチウムLiFePO4、負極にチタン酸リチウムLi4Ti5O12を用いた請求項8の電気化学素子。
【請求項1】
旋回する反応器内で金属酸化物の出発原料とカーボン粉末とを含む溶液にずり応力と遠心力を加えて反応させ、金属酸化物ナノ粒子の前駆体がカーボンに高分散担持された複合体粉末を、窒素雰囲気中で急速加熱処理することによって、金属酸化物の結晶化を進行させ、超薄膜構造体を有する、金属酸化物ナノ粒子をカーボンに高分散担持させることを特徴とする金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項2】
前記急速加熱処理が、前記複合体を窒素雰囲気中で、400〜1000℃に加熱するものであることを特徴とする請求項1に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項3】
前記反応器内において、反応物と共に反応抑制剤を含む溶液にずり応力と遠心力を加えて反応させることを特徴とする請求項2に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項4】
前記金属酸化物が、MxOz、AxMyOz、Mx(DO4)y、AxMy(DO4)z(ただし、M:金属元素 A:アルカリ金属又はランタノイド元素)で表されるものである請求項1から請求項3のいずれか1項に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項5】
前記金属酸化物が、酸化マンガンMnO、リン酸鉄リチウムLiFePO4、チタン酸リチウムLi4Ti5O12のいずれかである請求項4に記載の金属酸化物ナノ粒子とカーボンの複合体の製造方法。
【請求項6】
請求項1から請求項5のいずれか1項に記載の方法で製造した金属酸化物ナノ粒子とカーボンの複合体。
【請求項7】
前記請求項6に記載の複合体をバインダーと混合した後、成形して得られる電極。
【請求項8】
請求項7に記載の電極を用いた電気化学素子。
【請求項9】
正極にリン酸鉄リチウムLiFePO4、負極にチタン酸リチウムLi4Ti5O12を用いた請求項8の電気化学素子。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【公開番号】特開2011−251889(P2011−251889A)
【公開日】平成23年12月15日(2011.12.15)
【国際特許分類】
【出願番号】特願2010−250185(P2010−250185)
【出願日】平成22年11月8日(2010.11.8)
【出願人】(000228578)日本ケミコン株式会社 (514)
【出願人】(504358517)有限会社ケー・アンド・ダブル (19)
【出願人】(504132881)国立大学法人東京農工大学 (595)
【Fターム(参考)】
【公開日】平成23年12月15日(2011.12.15)
【国際特許分類】
【出願日】平成22年11月8日(2010.11.8)
【出願人】(000228578)日本ケミコン株式会社 (514)
【出願人】(504358517)有限会社ケー・アンド・ダブル (19)
【出願人】(504132881)国立大学法人東京農工大学 (595)
【Fターム(参考)】
[ Back to top ]

