鉛簡易測定法及びこれに用いる試薬
【課題】 極めて低濃度のPb量を測定する際に、高価な分析法を用いずに、安価で簡易な比色分析方法を用いて測定できる測定条件を提示することにより測定可能にした新規の鉛簡易測定法及びこれに用いる試薬を提供する。
【解決手段】 検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする。
【解決手段】 検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、水道水中に溶出した鉛成分を測定する鉛簡易測定法及びこれに用いる試薬に関するものである。
【背景技術】
【0002】
一般に、黄銅合金や青銅合金は、耐食性や生産性および経済性に優れていることから、給水装置や水道配管経路の主要材料として長年使用されている。これらの銅合金には快削性、鋳造性、耐圧性を改善するため数%の鉛が存在している。その鉛が表面に露呈した場合、その一部が水道水中へ溶出するため、健康に対する影響が懸念されている。このため厚生省水道環境部長通知による行政指導が行われ、2003年には鉛の基準値が0.01ppm(=10ppb)へ強化されることになった。
【0003】
今日、銅合金メーカーは鉛を含有しない、あるいは基準値を満足する材料の研究や開発を精力的に行っている。鋳造企業は中小企業が多いため、新合金の鉛フリー材料と従来からある鉛含有材料を完全に分離することは現状ではできない。
【0004】
このため、当面は、新合金と旧合金を共に用いて生産を続けざるを得ない。また鋳造品には地金に含有していた鉛ばかりではなく、製造過程で鋳物砂やショット材等その他の設備からの混入もあり、しかも再生循環利用をしているため、鉛を全く含まない銅合金(鉛完全フリー銅合金)に完全に置き換わるまでは鉛を若干含有した製品が市場に出回ることになる。この過渡期の銅合金は鉛フリー銅合金と呼称され、市場で使用されている。
【0005】
この過渡期の鉛フリー銅合金も当然厚生労働省の基準値0.01ppmをクリアーしなければならず、製品ごとの安全性の確認が必要となってくる。
【0006】
そこで、たとえば次に述べるICP質量分析法 や鉛簡易測定法(共立理化学研究所製)で、最終実装段階での溶出試験を実施することが多い。
【0007】
各銅合金メーカーは、自社の鋳物部品が鉛の溶出基準を満足しているかどうか最終製品段階まで判断できない。また公的機関などへ製品毎に溶出試験依頼ではコストと時間がかかっていた。
【0008】
しかしながら、上記ICP質量分析法は、一番確実な方法であるが、高価(2000万くらい)であり、JIS規定に従うため測定に時間(24時間)がかかる問題があった。他方、鉛簡易測定法(共立理化学研究所製)は、市販品で、これもJIS規定に従うため測定に時間(24時間)がかかる上、そもそも水道水中で実施するため溶出Pb量が少なく、感度はあまり思わしくない等の問題あった。
【0009】
いずれにしても現状は、時間と費用がかかりすぎるため安全性の確認に手間取っているので、正確で迅速な鉛簡易測定法への強い要望がある。
【0010】
そこで、本発明者は、鉛簡易測定法を提案するための一環として
(1)合金中の鉛の選択溶出条件の選定
(2)簡易鉛測定値のICP質量分析(誘導結合プラズマ質量分析)による調査を行い、鉛の選択溶解挙動と溶出条件を実験的に調べた。具体的には鉛含有量に差がある複数個のCu-5%Sn-6%Zn-2%Bi系青銅鋳物の電気化学的挙動を調べた。その結果に着目し、本発明を案出した。
【発明の開示】
【発明が解決しようとする課題】
【0011】
すなわち、本発明は、極低濃度のPb量を測定する上で、高価な分析法(ICP-MS法)を用いずに、安価で簡易な比色分析方法(例えばWA-Pb法)を用いて測定できる測定条件を提示することにより測定可能にした新規の鉛簡易測定法及びこれに用いる試薬を提供することを課題とする。
【課題を解決するための手段】
【0012】
上記課題を達成するために、本発明に係る鉛簡易測定法は、検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、Pbの分析測定の妨害元素となるZnを錯体化若しくは化合物化して測定されない状態にする化学種を添加した試薬の中で定電位電解を行ったのちにPbを定量することを特徴とする。
【0013】
したがって、上記化学種を添加した水道水の中に銅合金鋳物をいれて定電位電解を行ったのちに鉛成分を定量するWA-Pb法を行うことにより測定が可能になるから、銅合金鋳物のPb溶出量を迅速に測定できる。結果として厚生省基準の10ppb以下であるか否かを素早く判定できる。このような測定・判定が迅速にできる装置そのものは、簡単なものであるため、現場でも難なく使うことができる。
【0014】
請求項2に係る鉛簡易測定法は、試薬として、100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液を用いることを特徴とする。
【0015】
この請求項2に係る鉛簡易測定法は、Pbの溶解時(定電位電解時)に測定を妨害する元素であるZnが不可避的に溶出されても、これを上記試薬の中の1-10フェナントロリンが錯体化若しくは化合物化して測定されない状態にするので、結果として誤差のない正しい測定ができると同時に選択的にPbを早く溶出しうるようになるから測定時間の迅速化ができる。
【0016】
請求項3に係る鉛簡易測定法は、検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする。
【0017】
請求項3に係る鉛簡易測定法によれば、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液からなる試薬(溶液種)を用いてPbの選択的溶解及びその溶解の速度を加速しながら定電位(-0.2V)電解を2時間以上行うようにしたので、より精度のよい測定ができると同時に選択的にPbをより早く溶出でき、かつ測定時間をより迅速化できる。
【0018】
請求項4に係る鉛簡易測定法に用いる試薬は、100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液からなることを特徴とするので、これを用いることにより本発明に係る鉛簡易測定法の実施を可能にできる。
【発明の効果】
【0019】
本発明によれば、高価な分析法(ICP-MS法)を用いずに安価で簡易な比色分析方法(例えばWA-Pb法)を用いて、極低濃度のPb量を測定しうるようにした新規の鉛簡易測定法及びこれに用いる試薬を提供できる。しかも、誤差のない正しい測定及びその測定時間の迅速化ができる。
【発明を実施するための最良の形態】
【0020】
本発明者は、鉛簡易測定法及びこれに用いる試薬を提供するための一環として、青銅鋳物を例に次のことを行った。
【0021】
≪1.はじめに≫
(1)合金中の鉛の選択溶出条件の選定
(2)簡易鉛測定値のICP質量分析による調査
を行い、鉛の選択溶解挙動と溶出条件を実験的に調べた。具体的には鉛含有量を変化させたCu-5%Sn-6%Zn-2%Bi系青銅鋳物の電気化学的挙動を調べた。以下、その詳細を次に述べる。
【0022】
≪2.供試材≫
実験に用いる合金試験片を製作した。Cu-5%Sn-6%Zn-2%Bi系青銅鋳物を母合金とし、Pb量を4種類(Pb=0.1、0.2、0.5、1.0%)に変化させた試料(以下、Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0Pbと略記する)を製作した。成分調整後、各青銅鋳物試験片は1746〜1776Kで溶解した。鋳造温度1403KでJIS規格A号シェル型鋳型(φ36×110mm)に鋳造し、水冷した。各供試材の化学分析値を図1の表に示す。
【0023】
青銅鋳物の各種構成金属(試料番号Pb、Cu、Bi、Sn、Zn)は、市販のものを用いた。各試験片はエポキシ樹脂に埋め込み、湿式研磨(1200番エメリー研磨)後、アセトン洗浄して実験に供した。電気化学測定における作用電極表面積は3.14cm2とした。表面SEM(電子顕微鏡)観察やEPMA(電子プローブエックス線マイクロアナライザ)分析の各試料はエポキシ樹脂に埋め込み、湿式研磨(1500番エメリー研磨)後ダイヤモンド(3ミクロン)で研磨し、アセトン洗浄して供した。
【0024】
≪3.試験液≫
試薬は、特級の酢酸および1、10-フェナントロリン(以下1-10phenanと略記する場合もある)を用いた。試験液はイオン交換水を用い、300ppm酢酸水溶液(約pH3.4)とした。容量はすべて1dm3とし、試験液はマグネティックスターラーを用いて撹拌状態下にしておいた。脱気状態には99.999ppmの高純度窒素ガスを通気しておいた。液温は室温(約298K)とした。
【0025】
≪4.測定方法≫
分極曲線の測定には通常の動電位法を採用し、電位掃引速度は0.2mV/sとした。照合電極には飽和塩化カリウム水溶液中のAg/AgCl電極を用いた。なお、本発明では、特に断らない限り、銀塩化銀照合電極基準のV vs. Ag/AgClあるいはV vs. SSEを「V」と略記する。
対極には白金電極を用いた。定電位試験ではポテンシオスタットを用い、定電位(-0.2V)時に流れる電流密度を526ks間測定した。その時溶液中へ溶出する元素を誘導結合プラズマ質量分析法(以下、ICP-MS法と略記する)および簡易鉛測定セット((株)共立理化学研究所、WA-Pb:以下WA-Pbと略記する)で測定した。表面観察には電子顕微鏡(SEM)(日本電子(株)JSM-5310LV)を用い、EPMA分析にはWD/EDコンバインマイクロアナライザ(日本電子(株)JXA-8900R)を用いた。
【0026】
≪5.試料表面観察≫
試料表面の析出物とPbの分布状態を調べるためEPMA分析を行った。その結果を、Bronze-1.0Pbを代表にとって図2に示す。
この図2によると、試料表面には十数ミクロンの白い析出物が存在し、Pb分布は析出物分布に対応し、特に析出物中あるいはその周囲にPbは存在していることがわかる。白い析出物がPbの量に関係することが判ったので、白い析出物の分布状態を更に詳細に調べた。各試料表面のSEM観察結果を図3に示す。
【0027】
数回の観察結果から、鉛含有量が増えるにつれ析出物の存在割合は大きくなり、またBronze-0.1PbやBronze-0.2Pbでは析出物が脱落した痕と見られる孔が観察された。
【0028】
SEMで観察されている析出物の表面積と青銅中の鉛の関係を画像処理を用いて調べた。ランダムに試料端から中心までの間を12等間隔に区切り、そのときの表面を倍率500倍で撮影し、得られた撮影画面を画像処理ソフト(Adobe Photoshop)で二値化し析出物に対応する面積を画像処理ソフト(LIA for Win32)を用い計測した。これらの操作を十数回繰り返した。得られた結果を図4に示す。この図4中には、EPMAによるPb面分析による結果も併記しておいた。
【0029】
本実施で用いた青銅試験片中のPbの値は、0.5%以下では合金表面のPb露呈面積に反映されるが、0.5%以上では一定値を取るケースが多くなることが分った。
【0030】
また、青銅鋳物試料片中のPbの金属組織については、銅二元系合金状態図によれば、合金添加元素の内Zn、Sn、Sbは、銅中に固溶するがPb、Biは固溶しないことがわかっている。この固溶しないPbとBiは析出物あるいは異相として結晶粒界に出現する可能性が高い。従って析出物あるいは異相中にPbは含有されているものと考えられる。計量形態学より、青銅鋳物中のPb添加量が増加するにつれて、表面に露呈するPbの面積も大きくなる。従って青銅試験片Bronze-0.1PbからBronze-1.0Pbになるにつれて、表面の析出物の面積は大きくなるものと考えられる。本実施で用いた青銅試験片中のPbは、極端な偏析や偏在は起こっていず、試験片として適切に製作されていたものと考えられる。
【0031】
≪6.JIS規格による鉛の定量分析(ICP-MS法による)≫
Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0PbからのPb溶出量をJIS規格による試験法(JIS S3200-7)で調べた。浸出液には水道水を用い、コンディショニング作業は省略した。試験は6回行いICP-MS法(誘導結合プラズマ質量分析法)によりPb溶出量を分析した。その全結果を図5の表に示す。
なお、表中の<5ppbは、Pb溶出量がICP-MS法の測定限界値以下の5ppb以内に収まったことを示す。分布データの平均値のプロットを図6に示す。
【0032】
これにより、ICP-MS法によるPbイオン溶出量は、試験片中のPb含有量0.5%以下では合金試片中の含有Pb量に関係するが、0.5%以上では影響を及ぼさずほぼ一定値を示すことがわかった。
【0033】
≪7.JIS規格による鉛の簡易測定(WA-Pb法による)≫
Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0PbからのPb溶出量を簡易測定方法(WA-Pb法)を用いて測定した。試験は6回行い、その結果を図7の表に示す。この表をプロットしたものを図8に示す。
【0034】
Bronze-0.1PbとBronze-0.2PbのPb溶出量は、ほぼ10ppb以内に収まっている。合金中の鉛含有量に応じてPb溶出量は増加する。しかしBronze-0.5PbとBronze-1.0Pbのデータのバラツキは大きいことがわかる。
【0035】
≪8.酢酸水溶液中における構成合金元素の分極曲線≫
0.03ppm酢酸水溶液中で試料番号Pb、Bi、Cu、Sn、Zn の各分極曲線を測定した。その結果をまとめて図9に示す。
【0036】
各試片の腐食電位EcorrはそれぞれEcorr(Zn)=-997mV、Ecorr(Sn)=-502mV、

3回の測定結果からEcorrの序列関係から-0.2V(定電位)ではBiとCuの溶出の可能性はないことを確認した。
【0037】
各試片のアノード分極抵抗値の大小関係からZn、Sn、Pbの3元素のうち、一番溶けやすいのはPbであり、溶けにくいのはSnであることがわかった。
【0038】
青銅鋳物中のPbの選択溶解の電気化学的条件としては、青銅鋳物の構成元素のうちZn、Pb、Sn、Bi、Cuの電位-pH(E-pH)図を重ね合わせたものを図10に示す。
【0039】
300ppm酢酸水溶液中で定電位-0.2V保持した時の安定な化学種を見積る。溶液pHは約3.4であるので安定化学種はZn2+、Pb2+、Sn(OH)4、Bi(金属)、Cu(金属)となる。従ってイオンとして溶出する化学種はZn2+とPb2+となる。
【0040】
青銅鋳物中のPb2+の選択溶解において、Pb2+の測定上不要な元素であるZn2+の溶出を止めるには、電位とpHの制御だけでは不可能であり、別の手法を探すことになる。
【0041】
本法においてZn2+の存在はWA-Pb分析時の妨害元素となるだけであり、Zn2+を他の物質として変えればよい。ここでは妨害元素のマスキングとして分析化学でしばしば用いられている手法の1つを採用した。
【0042】
すなわち1-10phenanを添加し、Zn2+を錯体としてマスキングする手法を採用し、Zn2+の影響を減らした。
【0043】
1-10phenan過剰添加によるPb2+イオンへの誤差が懸念される。しかし分析時に千数百度の高温に元素を励起するICP-MS法では有機物である1-10phenanは安定に存在できず分解するものと思われる。ICP-MS法とWA-Pb法には強い相関関係があり、1-10phenan添加によるPb2+測定結果による影響はほとんどないものと考えられる。
【0044】
≪9.酢酸水溶液中における青銅鋳物試験片の分極曲線≫
300ppm酢酸水溶液中で試料番号Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0Pbの各分極曲線を測定した。その結果をまとめて図11に示す。
【0045】
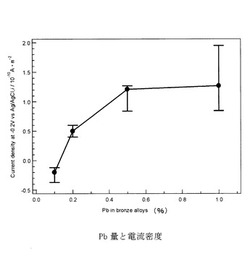
分極曲線は、各試料ともほぼ同じような分極挙動を示す。-0.2Vにおける電流密度と合金試料中のPb添加量の関係を調べた。その結果を図12に示す。
【0046】
合金中のPb量が増えるにつれて電流密度は増加し、概形としては飽和傾向を示している。
【0047】
≪10.定電位-0.2V下における溶液中のPb量の時間変化≫
300ppm酢酸水溶液中に各青銅鋳物試片を浸漬し、定電位-0.2Vで保持し、溶液中に溶出するPb量の時間変化を測定した。測定方法としてはICP-MS法とWA-Pb法の2種類を用いて調べた。なお、Pb簡易測定(WA-Pb法)に妨害元素として作用するZnを固定するため、溶液中に1-10phenanを100ppm添加しておいた。図13にICP-MS法による結果の代表的な例を示す。
【0048】
Pb<0.5%では溶出Pb量は、試片中のPb量と序列関係を示すが0.5以上になると対応関係が無くなることがわかる。
【0049】
ICP-MS法とWA-Pb法の相関関係を求めるため、2つの測定データをまとめてプロットした。その結果を図14に示す。
【0050】
測定時間t=7200sにおける2つの分析法の相関係数rは0.87であり、14400sではr=0.92、28800sではr=0.85、57600sではr=0.93となる。全データの相関係数はr=0.88となり、危険率1%で相関関係があると判定される。
【0051】
Pb<0.5%に限定した場合の2分析法の相関関係を調べた。すなわち試片をBronze-0.1PbとBronze-0.2Pbに限定した場合の相関関係を求めた。その結果を図15に示す。
【0052】
相関係数r=0.83であり、危険率1%でWA-Pb法とICP-MS法の間にはすべての時間で相関関係が成立していると判定される。
≪11.青銅鋳物中のPbの簡易測定とその測定条件≫
本発明の目的は、極低濃度のPb量を測定する上で、高価な分析法(ICP-MS法)を用いずに安価で簡易な比色分析方法(例えばWA-Pb法)で代替可能かどうか、可能ならばその測定条件を提示することにある。
【0053】
JIS規格による測定結果では、本文で用いた青銅鋳物試験片のBronze-0.1PbとBronze-0.2Pbが厚生省基準のPb<10ppbを満足する。しかしBronze-0.5PbとBronze-1.0Pbは10ppb前後を大きく逸脱し、基準を満足しない場合が多い結果を得た。データのバラツキや測定法の誤差等総合的に考え、しかもPb許容値等の安全面から考えると実際問題として青銅鋳物中のPb添加量がおおよそ0.2%以下で厚生省基準を満足することを見出すことができた。
【0054】
要するに、JIS規格の代替測定法としてWA-Pb法を用いるに当たっては、Pbの選択溶解とその溶解速度を加速するため、(1)100ppm1-10フェナントロリン添加の300ppm酢酸水溶液中で(2)定電位(-0.2V)電解を(3)2時間以上行うという3条件下で、青銅鋳物中のPb溶出量をWA-Pb法で測定し、得られた値が100ppb以下ならば厚生省基準の10ppb以下を満足すると言える。本実験の場合、青銅鋳物中のPb含有量が0.2%以下ならば厚生省基準を満足することがわかった。
【0055】
なお、本発明の1-10フェナントロリンは、100〜300ppmの範囲で使用することが望ましく、また酢酸水溶液は、100〜500ppmの範囲で使用することが望ましい。この場合、市販の簡易測定法(水道水を用いる方法)を用いる限り、添加する酢酸と 1-10フェナントロリンは薄いほど感度はよくなるが、100ppmより薄い場合にはPbの選択溶解が難しくなり、また1-10フェナントロリンを300ppmより濃く、酢酸水溶液を500ppmより濃くした場合には測定誤差になるから好ましくない。
【0056】
また、上記したように定電位電解の電位を-0.2Vとし、その電解時間を2時間以上とした場合において良い結果を得ることができたが、本発明はこれら電位、時間に拘らずに他の電位、時間であっても実施が可能である。要するに、本発明は、特許請求の範囲に記載された発明の精神を逸脱しない範囲において、種々の態様で実施することが可能であり、そしてこれ等実施されたものにも及ぶものである。さらに、本発明の1-10フェナントロリンは、Znを測定されない状態にすることが可能であれば、他の化学種で代用することができる。
【図面の簡単な説明】
【0057】
【図1】本発明の実施の形態に係る供試材の化学分析値を示す表である。
【図2】試料表面の析出物とPbの分布状態を示す顕微鏡写真である。
【図3】試料表面のSEM観察結果を示す観察図である。
【図4】銅合金中のPbと表面のPbの割合を示す図である。
【図5】ICP-MS法によるPb溶出量を示す表である。
【図6】分布データの平均値のプロットを示す図である。
【図7】WA-Pb法によるPb溶出量を示す表である。
【図8】分布データの平均値のプロットを示す図である。
【図9】試料の構成合金元素の分極曲線の測定結果を示す図である。
【図10】青銅鋳物の構成元素の電位-pH図を重ねて示した図である。
【図11】青銅鋳物の構成元素の分極曲線の測定結果を示す図である。
【図12】Pb量と電流密度の関係を示す図である。
【図13】ICP-MS法によるPb溶出量の時間変化を示す図である。
【図14】全試料のICP-MS法とWA-Pb法の相関関係を示す図である。
【図15】限定試料のICP-MS法とWA-Pb法の相関関係を示す図である。
【技術分野】
【0001】
本発明は、水道水中に溶出した鉛成分を測定する鉛簡易測定法及びこれに用いる試薬に関するものである。
【背景技術】
【0002】
一般に、黄銅合金や青銅合金は、耐食性や生産性および経済性に優れていることから、給水装置や水道配管経路の主要材料として長年使用されている。これらの銅合金には快削性、鋳造性、耐圧性を改善するため数%の鉛が存在している。その鉛が表面に露呈した場合、その一部が水道水中へ溶出するため、健康に対する影響が懸念されている。このため厚生省水道環境部長通知による行政指導が行われ、2003年には鉛の基準値が0.01ppm(=10ppb)へ強化されることになった。
【0003】
今日、銅合金メーカーは鉛を含有しない、あるいは基準値を満足する材料の研究や開発を精力的に行っている。鋳造企業は中小企業が多いため、新合金の鉛フリー材料と従来からある鉛含有材料を完全に分離することは現状ではできない。
【0004】
このため、当面は、新合金と旧合金を共に用いて生産を続けざるを得ない。また鋳造品には地金に含有していた鉛ばかりではなく、製造過程で鋳物砂やショット材等その他の設備からの混入もあり、しかも再生循環利用をしているため、鉛を全く含まない銅合金(鉛完全フリー銅合金)に完全に置き換わるまでは鉛を若干含有した製品が市場に出回ることになる。この過渡期の銅合金は鉛フリー銅合金と呼称され、市場で使用されている。
【0005】
この過渡期の鉛フリー銅合金も当然厚生労働省の基準値0.01ppmをクリアーしなければならず、製品ごとの安全性の確認が必要となってくる。
【0006】
そこで、たとえば次に述べるICP質量分析法 や鉛簡易測定法(共立理化学研究所製)で、最終実装段階での溶出試験を実施することが多い。
【0007】
各銅合金メーカーは、自社の鋳物部品が鉛の溶出基準を満足しているかどうか最終製品段階まで判断できない。また公的機関などへ製品毎に溶出試験依頼ではコストと時間がかかっていた。
【0008】
しかしながら、上記ICP質量分析法は、一番確実な方法であるが、高価(2000万くらい)であり、JIS規定に従うため測定に時間(24時間)がかかる問題があった。他方、鉛簡易測定法(共立理化学研究所製)は、市販品で、これもJIS規定に従うため測定に時間(24時間)がかかる上、そもそも水道水中で実施するため溶出Pb量が少なく、感度はあまり思わしくない等の問題あった。
【0009】
いずれにしても現状は、時間と費用がかかりすぎるため安全性の確認に手間取っているので、正確で迅速な鉛簡易測定法への強い要望がある。
【0010】
そこで、本発明者は、鉛簡易測定法を提案するための一環として
(1)合金中の鉛の選択溶出条件の選定
(2)簡易鉛測定値のICP質量分析(誘導結合プラズマ質量分析)による調査を行い、鉛の選択溶解挙動と溶出条件を実験的に調べた。具体的には鉛含有量に差がある複数個のCu-5%Sn-6%Zn-2%Bi系青銅鋳物の電気化学的挙動を調べた。その結果に着目し、本発明を案出した。
【発明の開示】
【発明が解決しようとする課題】
【0011】
すなわち、本発明は、極低濃度のPb量を測定する上で、高価な分析法(ICP-MS法)を用いずに、安価で簡易な比色分析方法(例えばWA-Pb法)を用いて測定できる測定条件を提示することにより測定可能にした新規の鉛簡易測定法及びこれに用いる試薬を提供することを課題とする。
【課題を解決するための手段】
【0012】
上記課題を達成するために、本発明に係る鉛簡易測定法は、検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、Pbの分析測定の妨害元素となるZnを錯体化若しくは化合物化して測定されない状態にする化学種を添加した試薬の中で定電位電解を行ったのちにPbを定量することを特徴とする。
【0013】
したがって、上記化学種を添加した水道水の中に銅合金鋳物をいれて定電位電解を行ったのちに鉛成分を定量するWA-Pb法を行うことにより測定が可能になるから、銅合金鋳物のPb溶出量を迅速に測定できる。結果として厚生省基準の10ppb以下であるか否かを素早く判定できる。このような測定・判定が迅速にできる装置そのものは、簡単なものであるため、現場でも難なく使うことができる。
【0014】
請求項2に係る鉛簡易測定法は、試薬として、100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液を用いることを特徴とする。
【0015】
この請求項2に係る鉛簡易測定法は、Pbの溶解時(定電位電解時)に測定を妨害する元素であるZnが不可避的に溶出されても、これを上記試薬の中の1-10フェナントロリンが錯体化若しくは化合物化して測定されない状態にするので、結果として誤差のない正しい測定ができると同時に選択的にPbを早く溶出しうるようになるから測定時間の迅速化ができる。
【0016】
請求項3に係る鉛簡易測定法は、検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする。
【0017】
請求項3に係る鉛簡易測定法によれば、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液からなる試薬(溶液種)を用いてPbの選択的溶解及びその溶解の速度を加速しながら定電位(-0.2V)電解を2時間以上行うようにしたので、より精度のよい測定ができると同時に選択的にPbをより早く溶出でき、かつ測定時間をより迅速化できる。
【0018】
請求項4に係る鉛簡易測定法に用いる試薬は、100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液からなることを特徴とするので、これを用いることにより本発明に係る鉛簡易測定法の実施を可能にできる。
【発明の効果】
【0019】
本発明によれば、高価な分析法(ICP-MS法)を用いずに安価で簡易な比色分析方法(例えばWA-Pb法)を用いて、極低濃度のPb量を測定しうるようにした新規の鉛簡易測定法及びこれに用いる試薬を提供できる。しかも、誤差のない正しい測定及びその測定時間の迅速化ができる。
【発明を実施するための最良の形態】
【0020】
本発明者は、鉛簡易測定法及びこれに用いる試薬を提供するための一環として、青銅鋳物を例に次のことを行った。
【0021】
≪1.はじめに≫
(1)合金中の鉛の選択溶出条件の選定
(2)簡易鉛測定値のICP質量分析による調査
を行い、鉛の選択溶解挙動と溶出条件を実験的に調べた。具体的には鉛含有量を変化させたCu-5%Sn-6%Zn-2%Bi系青銅鋳物の電気化学的挙動を調べた。以下、その詳細を次に述べる。
【0022】
≪2.供試材≫
実験に用いる合金試験片を製作した。Cu-5%Sn-6%Zn-2%Bi系青銅鋳物を母合金とし、Pb量を4種類(Pb=0.1、0.2、0.5、1.0%)に変化させた試料(以下、Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0Pbと略記する)を製作した。成分調整後、各青銅鋳物試験片は1746〜1776Kで溶解した。鋳造温度1403KでJIS規格A号シェル型鋳型(φ36×110mm)に鋳造し、水冷した。各供試材の化学分析値を図1の表に示す。
【0023】
青銅鋳物の各種構成金属(試料番号Pb、Cu、Bi、Sn、Zn)は、市販のものを用いた。各試験片はエポキシ樹脂に埋め込み、湿式研磨(1200番エメリー研磨)後、アセトン洗浄して実験に供した。電気化学測定における作用電極表面積は3.14cm2とした。表面SEM(電子顕微鏡)観察やEPMA(電子プローブエックス線マイクロアナライザ)分析の各試料はエポキシ樹脂に埋め込み、湿式研磨(1500番エメリー研磨)後ダイヤモンド(3ミクロン)で研磨し、アセトン洗浄して供した。
【0024】
≪3.試験液≫
試薬は、特級の酢酸および1、10-フェナントロリン(以下1-10phenanと略記する場合もある)を用いた。試験液はイオン交換水を用い、300ppm酢酸水溶液(約pH3.4)とした。容量はすべて1dm3とし、試験液はマグネティックスターラーを用いて撹拌状態下にしておいた。脱気状態には99.999ppmの高純度窒素ガスを通気しておいた。液温は室温(約298K)とした。
【0025】
≪4.測定方法≫
分極曲線の測定には通常の動電位法を採用し、電位掃引速度は0.2mV/sとした。照合電極には飽和塩化カリウム水溶液中のAg/AgCl電極を用いた。なお、本発明では、特に断らない限り、銀塩化銀照合電極基準のV vs. Ag/AgClあるいはV vs. SSEを「V」と略記する。
対極には白金電極を用いた。定電位試験ではポテンシオスタットを用い、定電位(-0.2V)時に流れる電流密度を526ks間測定した。その時溶液中へ溶出する元素を誘導結合プラズマ質量分析法(以下、ICP-MS法と略記する)および簡易鉛測定セット((株)共立理化学研究所、WA-Pb:以下WA-Pbと略記する)で測定した。表面観察には電子顕微鏡(SEM)(日本電子(株)JSM-5310LV)を用い、EPMA分析にはWD/EDコンバインマイクロアナライザ(日本電子(株)JXA-8900R)を用いた。
【0026】
≪5.試料表面観察≫
試料表面の析出物とPbの分布状態を調べるためEPMA分析を行った。その結果を、Bronze-1.0Pbを代表にとって図2に示す。
この図2によると、試料表面には十数ミクロンの白い析出物が存在し、Pb分布は析出物分布に対応し、特に析出物中あるいはその周囲にPbは存在していることがわかる。白い析出物がPbの量に関係することが判ったので、白い析出物の分布状態を更に詳細に調べた。各試料表面のSEM観察結果を図3に示す。
【0027】
数回の観察結果から、鉛含有量が増えるにつれ析出物の存在割合は大きくなり、またBronze-0.1PbやBronze-0.2Pbでは析出物が脱落した痕と見られる孔が観察された。
【0028】
SEMで観察されている析出物の表面積と青銅中の鉛の関係を画像処理を用いて調べた。ランダムに試料端から中心までの間を12等間隔に区切り、そのときの表面を倍率500倍で撮影し、得られた撮影画面を画像処理ソフト(Adobe Photoshop)で二値化し析出物に対応する面積を画像処理ソフト(LIA for Win32)を用い計測した。これらの操作を十数回繰り返した。得られた結果を図4に示す。この図4中には、EPMAによるPb面分析による結果も併記しておいた。
【0029】
本実施で用いた青銅試験片中のPbの値は、0.5%以下では合金表面のPb露呈面積に反映されるが、0.5%以上では一定値を取るケースが多くなることが分った。
【0030】
また、青銅鋳物試料片中のPbの金属組織については、銅二元系合金状態図によれば、合金添加元素の内Zn、Sn、Sbは、銅中に固溶するがPb、Biは固溶しないことがわかっている。この固溶しないPbとBiは析出物あるいは異相として結晶粒界に出現する可能性が高い。従って析出物あるいは異相中にPbは含有されているものと考えられる。計量形態学より、青銅鋳物中のPb添加量が増加するにつれて、表面に露呈するPbの面積も大きくなる。従って青銅試験片Bronze-0.1PbからBronze-1.0Pbになるにつれて、表面の析出物の面積は大きくなるものと考えられる。本実施で用いた青銅試験片中のPbは、極端な偏析や偏在は起こっていず、試験片として適切に製作されていたものと考えられる。
【0031】
≪6.JIS規格による鉛の定量分析(ICP-MS法による)≫
Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0PbからのPb溶出量をJIS規格による試験法(JIS S3200-7)で調べた。浸出液には水道水を用い、コンディショニング作業は省略した。試験は6回行いICP-MS法(誘導結合プラズマ質量分析法)によりPb溶出量を分析した。その全結果を図5の表に示す。
なお、表中の<5ppbは、Pb溶出量がICP-MS法の測定限界値以下の5ppb以内に収まったことを示す。分布データの平均値のプロットを図6に示す。
【0032】
これにより、ICP-MS法によるPbイオン溶出量は、試験片中のPb含有量0.5%以下では合金試片中の含有Pb量に関係するが、0.5%以上では影響を及ぼさずほぼ一定値を示すことがわかった。
【0033】
≪7.JIS規格による鉛の簡易測定(WA-Pb法による)≫
Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0PbからのPb溶出量を簡易測定方法(WA-Pb法)を用いて測定した。試験は6回行い、その結果を図7の表に示す。この表をプロットしたものを図8に示す。
【0034】
Bronze-0.1PbとBronze-0.2PbのPb溶出量は、ほぼ10ppb以内に収まっている。合金中の鉛含有量に応じてPb溶出量は増加する。しかしBronze-0.5PbとBronze-1.0Pbのデータのバラツキは大きいことがわかる。
【0035】
≪8.酢酸水溶液中における構成合金元素の分極曲線≫
0.03ppm酢酸水溶液中で試料番号Pb、Bi、Cu、Sn、Zn の各分極曲線を測定した。その結果をまとめて図9に示す。
【0036】
各試片の腐食電位EcorrはそれぞれEcorr(Zn)=-997mV、Ecorr(Sn)=-502mV、

3回の測定結果からEcorrの序列関係から-0.2V(定電位)ではBiとCuの溶出の可能性はないことを確認した。
【0037】
各試片のアノード分極抵抗値の大小関係からZn、Sn、Pbの3元素のうち、一番溶けやすいのはPbであり、溶けにくいのはSnであることがわかった。
【0038】
青銅鋳物中のPbの選択溶解の電気化学的条件としては、青銅鋳物の構成元素のうちZn、Pb、Sn、Bi、Cuの電位-pH(E-pH)図を重ね合わせたものを図10に示す。
【0039】
300ppm酢酸水溶液中で定電位-0.2V保持した時の安定な化学種を見積る。溶液pHは約3.4であるので安定化学種はZn2+、Pb2+、Sn(OH)4、Bi(金属)、Cu(金属)となる。従ってイオンとして溶出する化学種はZn2+とPb2+となる。
【0040】
青銅鋳物中のPb2+の選択溶解において、Pb2+の測定上不要な元素であるZn2+の溶出を止めるには、電位とpHの制御だけでは不可能であり、別の手法を探すことになる。
【0041】
本法においてZn2+の存在はWA-Pb分析時の妨害元素となるだけであり、Zn2+を他の物質として変えればよい。ここでは妨害元素のマスキングとして分析化学でしばしば用いられている手法の1つを採用した。
【0042】
すなわち1-10phenanを添加し、Zn2+を錯体としてマスキングする手法を採用し、Zn2+の影響を減らした。
【0043】
1-10phenan過剰添加によるPb2+イオンへの誤差が懸念される。しかし分析時に千数百度の高温に元素を励起するICP-MS法では有機物である1-10phenanは安定に存在できず分解するものと思われる。ICP-MS法とWA-Pb法には強い相関関係があり、1-10phenan添加によるPb2+測定結果による影響はほとんどないものと考えられる。
【0044】
≪9.酢酸水溶液中における青銅鋳物試験片の分極曲線≫
300ppm酢酸水溶液中で試料番号Bronze-0.1Pb、Bronze-0.2Pb、Bronze-0.5Pb、Bronze-1.0Pbの各分極曲線を測定した。その結果をまとめて図11に示す。
【0045】
分極曲線は、各試料ともほぼ同じような分極挙動を示す。-0.2Vにおける電流密度と合金試料中のPb添加量の関係を調べた。その結果を図12に示す。
【0046】
合金中のPb量が増えるにつれて電流密度は増加し、概形としては飽和傾向を示している。
【0047】
≪10.定電位-0.2V下における溶液中のPb量の時間変化≫
300ppm酢酸水溶液中に各青銅鋳物試片を浸漬し、定電位-0.2Vで保持し、溶液中に溶出するPb量の時間変化を測定した。測定方法としてはICP-MS法とWA-Pb法の2種類を用いて調べた。なお、Pb簡易測定(WA-Pb法)に妨害元素として作用するZnを固定するため、溶液中に1-10phenanを100ppm添加しておいた。図13にICP-MS法による結果の代表的な例を示す。
【0048】
Pb<0.5%では溶出Pb量は、試片中のPb量と序列関係を示すが0.5以上になると対応関係が無くなることがわかる。
【0049】
ICP-MS法とWA-Pb法の相関関係を求めるため、2つの測定データをまとめてプロットした。その結果を図14に示す。
【0050】
測定時間t=7200sにおける2つの分析法の相関係数rは0.87であり、14400sではr=0.92、28800sではr=0.85、57600sではr=0.93となる。全データの相関係数はr=0.88となり、危険率1%で相関関係があると判定される。
【0051】
Pb<0.5%に限定した場合の2分析法の相関関係を調べた。すなわち試片をBronze-0.1PbとBronze-0.2Pbに限定した場合の相関関係を求めた。その結果を図15に示す。
【0052】
相関係数r=0.83であり、危険率1%でWA-Pb法とICP-MS法の間にはすべての時間で相関関係が成立していると判定される。
≪11.青銅鋳物中のPbの簡易測定とその測定条件≫
本発明の目的は、極低濃度のPb量を測定する上で、高価な分析法(ICP-MS法)を用いずに安価で簡易な比色分析方法(例えばWA-Pb法)で代替可能かどうか、可能ならばその測定条件を提示することにある。
【0053】
JIS規格による測定結果では、本文で用いた青銅鋳物試験片のBronze-0.1PbとBronze-0.2Pbが厚生省基準のPb<10ppbを満足する。しかしBronze-0.5PbとBronze-1.0Pbは10ppb前後を大きく逸脱し、基準を満足しない場合が多い結果を得た。データのバラツキや測定法の誤差等総合的に考え、しかもPb許容値等の安全面から考えると実際問題として青銅鋳物中のPb添加量がおおよそ0.2%以下で厚生省基準を満足することを見出すことができた。
【0054】
要するに、JIS規格の代替測定法としてWA-Pb法を用いるに当たっては、Pbの選択溶解とその溶解速度を加速するため、(1)100ppm1-10フェナントロリン添加の300ppm酢酸水溶液中で(2)定電位(-0.2V)電解を(3)2時間以上行うという3条件下で、青銅鋳物中のPb溶出量をWA-Pb法で測定し、得られた値が100ppb以下ならば厚生省基準の10ppb以下を満足すると言える。本実験の場合、青銅鋳物中のPb含有量が0.2%以下ならば厚生省基準を満足することがわかった。
【0055】
なお、本発明の1-10フェナントロリンは、100〜300ppmの範囲で使用することが望ましく、また酢酸水溶液は、100〜500ppmの範囲で使用することが望ましい。この場合、市販の簡易測定法(水道水を用いる方法)を用いる限り、添加する酢酸と 1-10フェナントロリンは薄いほど感度はよくなるが、100ppmより薄い場合にはPbの選択溶解が難しくなり、また1-10フェナントロリンを300ppmより濃く、酢酸水溶液を500ppmより濃くした場合には測定誤差になるから好ましくない。
【0056】
また、上記したように定電位電解の電位を-0.2Vとし、その電解時間を2時間以上とした場合において良い結果を得ることができたが、本発明はこれら電位、時間に拘らずに他の電位、時間であっても実施が可能である。要するに、本発明は、特許請求の範囲に記載された発明の精神を逸脱しない範囲において、種々の態様で実施することが可能であり、そしてこれ等実施されたものにも及ぶものである。さらに、本発明の1-10フェナントロリンは、Znを測定されない状態にすることが可能であれば、他の化学種で代用することができる。
【図面の簡単な説明】
【0057】
【図1】本発明の実施の形態に係る供試材の化学分析値を示す表である。
【図2】試料表面の析出物とPbの分布状態を示す顕微鏡写真である。
【図3】試料表面のSEM観察結果を示す観察図である。
【図4】銅合金中のPbと表面のPbの割合を示す図である。
【図5】ICP-MS法によるPb溶出量を示す表である。
【図6】分布データの平均値のプロットを示す図である。
【図7】WA-Pb法によるPb溶出量を示す表である。
【図8】分布データの平均値のプロットを示す図である。
【図9】試料の構成合金元素の分極曲線の測定結果を示す図である。
【図10】青銅鋳物の構成元素の電位-pH図を重ねて示した図である。
【図11】青銅鋳物の構成元素の分極曲線の測定結果を示す図である。
【図12】Pb量と電流密度の関係を示す図である。
【図13】ICP-MS法によるPb溶出量の時間変化を示す図である。
【図14】全試料のICP-MS法とWA-Pb法の相関関係を示す図である。
【図15】限定試料のICP-MS法とWA-Pb法の相関関係を示す図である。
【特許請求の範囲】
【請求項1】
検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、Pbの分析測定の妨害元素となるZnを錯体化若しくは化合物化して測定されない状態とする化学種を添加した試薬の中で定電位電解を行ったのちにPbを定量することを特徴とする鉛簡易測定法。
【請求項2】
試薬として、100〜300ppm1-10フェナントロリンを添加した100〜500ppm酢酸水溶液を用いることを特徴とする請求項1記載の鉛簡易測定法。
【請求項3】
検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする鉛簡易測定法。
【請求項4】
100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液からなることを特徴とする鉛簡易測定法に用いる試薬。
【請求項1】
検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、Pbの分析測定の妨害元素となるZnを錯体化若しくは化合物化して測定されない状態とする化学種を添加した試薬の中で定電位電解を行ったのちにPbを定量することを特徴とする鉛簡易測定法。
【請求項2】
試薬として、100〜300ppm1-10フェナントロリンを添加した100〜500ppm酢酸水溶液を用いることを特徴とする請求項1記載の鉛簡易測定法。
【請求項3】
検液にPbと反応する試薬を添加し、該試薬との反応で生ずるPbの錯体の色の濃さからPbを定量する簡易比色法による鉛簡易測定法に関し、100ppm1-10フェナントロリン添加の300ppm酢酸水溶液の中で-0.2V定電位電解を2時間以上行ったのちにPbを定量することを特徴とする鉛簡易測定法。
【請求項4】
100〜300ppm1-10フェナントロリン添加の100〜500ppm酢酸水溶液からなることを特徴とする鉛簡易測定法に用いる試薬。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【公開番号】特開2008−32585(P2008−32585A)
【公開日】平成20年2月14日(2008.2.14)
【国際特許分類】
【出願番号】特願2006−207485(P2006−207485)
【出願日】平成18年7月31日(2006.7.31)
【出願人】(506262128)社団法人日本非鉄金属鋳物協会 (2)
【Fターム(参考)】
【公開日】平成20年2月14日(2008.2.14)
【国際特許分類】
【出願日】平成18年7月31日(2006.7.31)
【出願人】(506262128)社団法人日本非鉄金属鋳物協会 (2)
【Fターム(参考)】
[ Back to top ]

