電子顕微鏡観察用染色剤および該染色剤を用いた染色方法
【課題】適用範囲が広く高い染色性を示し、取り扱いが容易で安全性の高い電子顕微鏡観察用染色剤を提供する。
【解決手段】一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]
(式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)
で表されるリンタングステン酸を含む電子顕微鏡観察用染色剤。
【解決手段】一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]
(式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)
で表されるリンタングステン酸を含む電子顕微鏡観察用染色剤。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、電子顕微鏡観察用試料のネガティブ染色剤および該染色剤を用いた電子顕微鏡観察用試料のネガティブ染色方法に関する。
【背景技術】
【0002】
ナノレベルからマイクロレベルの微細構造を高精度に観察することへの要求は、有機物、無機物を問わず近年ますます高まっている。さらにこのところ、新型インフルエンザ、ノロウイルスおよび口蹄疫などのウイルスが原因となる流行性の感染症の発生および拡大が問題となっている。これら感染症の蔓延を防止するためには、原因となるウイルスの分類を同定するための微細構造解析を行うことが不可欠である。
【0003】
ウイルスは10〜200ナノメートルと小さいため、微細構造解析には走査型および/または透過型電子顕微鏡(TEM)を用いる必要がある。この中でも、特にTEMを用いることが有効である。しかしながら、有機物であるウイルス上では電子線の散乱が起こりにくいため、重元素などを用いた染色が必須となる。重元素などを用いた染色を行うことで、染色剤部分は電子線が散乱するため暗い像となり、観察対象部分は電子線が透過するため明るい像となる。染色剤が観察対象や観察対象を固定する支持膜と上手く相互作用していれば、観察対象の微細構造を反映した像が得られる。このような染色方法はネガティブ染色方法と呼ばれる。
【0004】
これまでに、ネガティブ染色方法に用いられるネガティブ染色剤は数多く提案されている。ネガティブ染色剤としては、例えば、酢酸ウラニル(特許文献1、非特許文献1および非特許文献3〜5)、クエン酸鉛(特許文献1および非特許文献1)、酢酸鉛および硝酸鉛(非特許文献1)、リンタングステン酸(特許文献2、3および非特許文献1、2)、モリブデン酸アンモニウム・4水和物(非特許文献1、2)、タングステン酸アンモニウム・5水和物(非特許文献3)、塩化ハフニウム(非特許文献4)、塩化ジルコニウム(非特許文献4)および白金ブルー(非特許文献5)などが提案されている。さらに、粘度や浸透性能の制御を目的として、染色剤溶液への添加剤の添加についても提案されている(非特許文献1)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2007−309872号公報
【特許文献2】特開平5−306979号公報
【特許文献3】特開平2−118431号公報
【非特許文献】
【0006】
【非特許文献1】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p93−98、2007年
【非特許文献2】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p1−6、2007年
【非特許文献3】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第24巻(第2号)、p59−60、2010年
【非特許文献4】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第20巻(第1号)、p69−70、2006年
【非特許文献5】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p90−92、2007年
【発明の概要】
【発明が解決しようとする課題】
【0007】
しかしながら、最も汎用されている酢酸ウラニル(酢酸ウラン)は、良好な染色性を示すものの、放射性物質であるウラン(劣化ウラン)が使用されており、兵器への転用が可能であることから使用制限や管理などが強化されつつあるため、安全性が高く簡便に使用可能な代替染色剤の開発が望まれている。また、鉛塩類、モリブデン酸アンモニウム、タングステン酸アンモニウム、塩化ハフニウム、塩化ジルコニウムおよび白金ブルーは、安全性の面では優れているが酢酸ウラニルに比べてコントラストが弱く染色能力が劣り、観察対象の性質や調製条件などの点でも適正に使用できる範囲が狭い。
【0008】
一方、特許文献2、3および非特許文献1、2に開示されているリンタングステン酸は、酢酸ウラニルに次いで汎用なネガティブ染色剤であり、ケギン(Keggin)型と呼ばれるリン酸とタングステン酸との縮合により合成されるヘテロポリ酸(ポリオキソメタレート)である。現在、市販試薬として容易に入手できるリンタングステン酸は、Keggin型リンタングステン酸のみであり、ネガティブ染色剤において単にリンタングステン酸あるいはPTA(Phosphotungstic Acid)と表記される場合には、Keggin型リンタングステン酸を意味する。さらに、本願発明者は、ネガティブ染色剤として市販されているリンタングステン酸(Phosphotungustate acid EM、TAAB Laboratories製)をFT−IRおよび31P−NMRを用いて分析したところ、Keggin型リンタングステン酸に特有なスペクトルを示すことを確認している。
【0009】
図1にKeggin型リンタングステン酸アニオンの一次構造を示す。H3PW12O40で表されるKeggin型リンタングステン酸は、水溶液中での安定性が非常に低く、pH<1の領域でしか構造を保てない課題がある。例えば、ウイルス、菌および細胞などの試料の観察はほぼ中性領域で行われるため、Keggin型リンタングステン酸の安定pH領域以外では、Keggin型構造の分解が懸念される。また、前記分解が生じた場合、ウイルスの表面蛋白質や支持膜との相互作用も大きく変化する可能性がある。
【0010】
したがって、Keggin型リンタングステン酸を染色剤に用いる場合には、種々の分解生成物に由来する観察試料の均質性の低下が生じ、染色性が低下する。また、これを改善するためにKeggin型リンタングステン酸溶液に酢酸などを添加する場合にも、染色剤溶液の調製が煩雑になり、好適条件の決定が難しい。このような背景から、染色が簡便で、染色性が十分に高く、使用可能範囲が広い代替染色剤の開発が望まれている。
【0011】
本発明の目的は、適用範囲が広く高い染色性を示し、取り扱いが容易で安全性の高い電子顕微鏡観察用染色剤を提供することにある。
【課題を解決するための手段】
【0012】
本発明に係る電子顕微鏡観察用染色剤は、一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110](式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)で表されるリンタングステン酸を含む。
【0013】
本発明に係る電子顕微鏡観察用試料の染色方法は、本発明に係る電子顕微鏡観察用染色剤を用いる。
【発明の効果】
【0014】
本発明によれば、適用範囲が広く高い染色性を示し、取り扱いが容易で安全性の高い電子顕微鏡観察用染色剤を提供することができる。
【図面の簡単な説明】
【0015】
【図1】Keggin型リンタングステン酸アニオンの一次構造を示す模式図である。
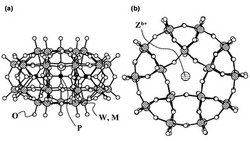
【図2】Preyssler型リンタングステン酸アニオンの一次構造を示す(a)側面図、(b)上面図である。
【図3】本発明に係る染色方法の一例を示す模式図である。
【図4】(a)マイクロピペットを用いてグリッドに染色剤溶液を滴下する操作の概略図、(b)ろ紙で余分な溶液を吸い取る際の、グリッドとろ紙との位置関係を示す概略図である。
【図5】(a)実施例1、(b)比較例1、(c)比較例4の各種染色剤により染色したT4ファージのTEM像である。
【図6】(a)実施例2、(b)比較例2、(c)比較例5の各種染色剤により染色したT7ファージのTEM像である。
【図7】(a)実施例3、(b)比較例3、(c)比較例6の各種染色剤により染色したλファージのTEM像である。
【図8】(a)実施例4、(b)実施例5の各種濃度の染色剤溶液を用いて染色したT4ファージのTEM像である。
【図9】実施例6の染色剤により染色したT4ファージのTEM像である。
【図10】実施例7の染色剤により染色したT4ファージのTEM像である。
【図11】実施例8の染色剤により染色したT4ファージのTEM像である。
【図12】実施例9の染色剤により染色したT4ファージのTEM像である。
【図13】実施例10の染色剤により染色したT4ファージのTEM像である。
【図14】実施例11の染色剤により染色したT7ファージのTEM像である。
【図15】実施例12の染色剤により染色したλファージのTEM像である。
【図16】実施例13の染色剤により染色したT4ファージのTEM像である。
【図17】実施例14の染色剤により染色したT4ファージのTEM像である。
【発明を実施するための形態】
【0016】
[電子顕微鏡観察用染色剤]
本発明に係る電子顕微鏡観察用染色剤に含まれる、一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]で表されるリンタングステン酸は、Preyssler型と呼ばれるリンタングステン酸である。Preyssler型リンタングステン酸は、Keggin型とは異なる形でリン酸とタングステン酸とが縮合したヘテロポリ酸の一種である。Preyssler型リンタングステン酸アニオンの一次構造を図2に示す。
【0017】
Keggin型リンタングステン酸は、1933年にその一次構造が決定され、染色剤の他、触媒、導電材料およびナノ材料などとして広く研究されてきた。一方、Preyssler型リンタングステン酸は1970年に初めて合成され、その一次構造が決定されたのは1985年である。Preyssler型リンタングステン酸は、Keggin型のそれよりも研究の歴史が浅く、合成も難しいとされていた。本願発明者はPreyssler型リンタングステン酸の調製方法、物性および特徴を鋭意研究しており、Keggin型リンタングステン酸よりも、重元素であるタングステンを一次構造中に多く有するPreyssler型リンタングステン酸の方が、電子顕微鏡観察用染色剤としてより良好な性能を示すと考えた。また、電子顕微鏡観察用染色剤としてPreyssler型リンタングステン酸は、pH<12の広いpH範囲で安定に存在するため、ネガティブ染色剤としてKeggin型リンタングステン酸と比較して良好な染色性能を示すことができる。さらに、Preyssler型リンタングステン酸は、アニオンおよびカチオンの構成元素(Aa+、Zb+およびM(d))を種々変えることができるため、分子設計・物性制御の幅が広く、適用可能な検体の範囲も広い。
【0018】
前記一般式において、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。なお、前記一般式で表されるリンタングステン酸には、前記一般式の水和物も含まれる。リンタングステン酸が水和物の場合、水和物の水和水量(nH2O)は特に限定されず、0≦nであることができる。水和物の水和水量は、その乾燥状態や保管状態などにより変化する。仮に水和物の水和水量が異なったとしても、電子顕微鏡観察用染色剤としての性能は同じである。そのため、前記一般式では、水和水の記載は省略している。
【0019】
前記一般式において、Aa+としては0<aであれば特に制限されない。aは、0<a≦3とすることもでき、0<a≦2とすることもできる。Aa+としては、第1族元素のカチオン、第2族元素のカチオン、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであることが好ましい。Aa+としては、H+、Li+、Na+、K+、Rb+、Cs+、Be2+、Mg2+、Ca2+、Sr2+、Ba2+、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであることがより好ましい。
【0020】
前記ピリジニウムカチオンはC5H5N+Rで表され、前記第4級アンモニウムカチオンはR4N+で表される。ピリジニウムカチオンおよび4級アンモニウムカチオンは、C1からC21までの種々の炭化水素基(R)で窒素原子がアルキル化されたピリジンおよびアルキルアンモニウムのカチオンである。Rとしては特に限定されないが、メチル基、エチル基、n−プロピル基、n−ブチル基、ドデシル基、セチル基などが挙げられる。第4級アンモニウムカチオンにおいては、複数のRは同じでも異なっていてもよい。また、Rは官能基を有していても差し支えない。なお、Aa+が複数の種類のカチオンを含む場合、aの値は各カチオンの価数に各モル比を乗じた値の和とする。例えば、Aa+がK+と、Ca2+とをモル比0.5:0.5で含む場合、aの値は1×0.5+2×0.5=1.5となる。
【0021】
前記一般式において、Zb+としては0<bであれば特に制限されない。bは、0<b≦6とすることもでき、0<b≦4とすることもできる。Zb+としては、第1族元素のカチオン、第2族元素のカチオン、第3族元素のカチオン、第15族元素のカチオン、ランタノイド元素のカチオンおよびアクチノイド元素のカチオンからなる群より選ばれる少なくとも一つのカチオンであることが好ましい。Zb+としては、Na+、Ca2+、Sr2+、Bi3+、Y3+、La3+、Ce3+、Eu3+、Gd3+、Lu3+、Am3+、Th4+およびU4+からなる群より選ばれる少なくとも一つのカチオンであることがより好ましい。なお、ネガティブ染色の原理からは、Aa+およびZb+により重い元素を導入すれば、より鮮明な像が得られる。
【0022】
前記一般式において、M(d)としては0<d≦6であれば特に制限されない。dは2≦d≦6とすることもでき、3≦d≦6とすることもできる。M(d)としては、d価の第5族元素およびd価の第6族元素の少なくとも一方であることが好ましい。M(d)としては、W(VI)、Mo(VI)およびV(IV)からなる群より選ばれる少なくとも一つの元素であることがより好ましい。cは0≦c<30であるが、0≦c≦5とすることができ、合成の困難さや構造安定性の観点から、cは0、1または2が好ましい。
【0023】
なお、c=0の場合、前記一般式にはM(d)は含まれないが、この場合前記一般式は、Aa+(15-b)/a[Zb+P5W30O110](式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオンを示す。0<a、0<bである。)で表される。
【0024】
前記一般式で表されるリンタングステン酸は、例えばM.T.Popeら,Inorganic Chemistry,1993,32,1573−1578、またはY.Jeanninら,Journal of American Chemical Society,1985,107,2662−2669に開示されている方法により製造することができる。
【0025】
例えば、K12.5Na1.5[NaP5W30O110]・nH2Oの製造方法としては、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O)を水に溶解し、85質量%リン酸(H3PO4)を加え、圧力容器中、120℃において一晩水熱合成を行う。室温まで冷却後、水および塩化カリウム(KCl)を添加し、析出した固体をろ過し、酢酸カリウムおよびメタノールで洗浄する。得られた固体を熱水に溶解して室温まで放冷し、再結晶を行うことで得ることができる。再結晶を繰り返すと収率は低下するものの、純度を向上させることができる。
【0026】
[NaP5W30O110]14-アニオン中の、Na+のZb+への交換は、[NaP5W30O110]14-アニオン水溶液に交換するZb+を含有する溶液を添加して、圧力容器中、140〜180℃において一晩水熱合成を行う。その後、KClを添加し、ろ別し、洗浄および乾燥を行うことで、Na+のZb+への交換を行うことができる。
【0027】
[NaP5W30O110]14-アニオン中の、W(VI)のM(d)への置換は、pHを調整した[NaP5W30O110]14-アニオン水溶液にM(d)を含有する溶液を添加する。その後、KClを添加し、ろ別し、洗浄および乾燥を行うことで、W(VI)のM(d)への置換を行うことができる。
【0028】
カチオンAa+を交換する方法としては、陽イオン交換樹脂を用いる方法が有用である。各種カチオン型交換樹脂に、[NaP5W30O110]14-アニオン水溶液を処理することで、カチオンAa+を交換することが可能である。また、プロトン型交換樹脂で処理してプロトン型H14[NaP5W30O110]とした後、各種カチオンでプロトンを部分中和することも可能である。
【0029】
Aa+、Zb+およびM(d)の交換および置換に用いる原料は特に制限されず、交換および置換したいカチオンまたは元素の硝酸塩、硫酸塩、酢酸塩、炭酸塩および塩化物などを用いることができる。これらは一種のみを用いてもよく、二種以上を併用してもよい。
【0030】
合成した前記一般式で表されるリンタングステン酸は、FT−IR、ICP発光分析や原子吸光などの元素分析、X線回折、31P−NMR、183W−NMR等により構造と組成を確認することができる。
【0031】
[電子顕微鏡観察用試料の染色方法]
本発明に係る電子顕微鏡観察用染色剤は、電子顕微鏡観察用試料の染色に用いることができる。本発明に係る方法によれば、電子顕微鏡観察用試料をより簡便に染色することができる。
【0032】
本発明に係る電子顕微鏡観察用染色剤を用いて染色し、電子顕微鏡観察を行う観察対象としては、特に制限されず、例えば細胞、ウイルス、ファージ(細菌に感染するウイルスの総称)、たんぱく質、低分子酵素、核、ミトコンドリア、リポソーム、グリコーゲン、脂肪滴、膜系、菌体、細菌鞭毛およびグラム陰性菌などが挙げられる。
【0033】
観察対象を定着させる支持膜としては、特に制限されず、コロジオン膜、フォルムバール膜およびカーボン膜などが挙げられ、必要に応じて蒸着処理や親水化処理を施したものであってもよい。
【0034】
本発明に係る染色剤に含まれるリンタングステン酸はPreyssler型リンタングステン酸であるため、染色剤溶液の調製においては、Keggin型リンタングステン酸やモリブデン酸アンモニウム等を用いる場合とは異なり、アルカリを用いたpH調整や酢酸などの添加は不要である。このため、本発明に係る染色剤を用いた染色剤溶液の調製は、非常に簡便に行うことができる。
【0035】
染色剤溶液に含まれる溶媒としては、水、アルコールなどが挙げられる。
【0036】
染色剤溶液中の前記一般式で表されるリンタングステン酸の濃度は、0.1質量%以上が好ましく、0.2質量%以上がより好ましく、0.3質量%以上がさらに好ましい。また、前記濃度は1.9質量%以下が好ましく、1.5質量%以下がより好ましく、1.0質量%以下がさらに好ましい。前記濃度を前記範囲とすることで、分散性、浸透圧、表面張力、支持膜や試料表面との相互作用などをバランスよく制御でき、高コントラストで微細構造の電子顕微鏡観察が可能となる。
【0037】
本発明に係る染色方法の一例を図3に示す。支持膜である透過型電子顕微鏡(TEM)用コロジオン膜に親水化処理を施し、観察対象であるウイルスを接触させ、定着させる。定着させたウイルスに、本発明に係る染色剤を溶解させた染色剤溶液を滴下して接触させる。その後、余分な溶液をろ紙で吸い取ることで取り除き、定置乾燥を行う。観察対象の支持膜への接触時間、染色剤溶液の観察対象への接触時間および定置乾燥の乾燥時間は特に限定されず、電子顕微鏡観察の結果を考慮しながら、観察対象に応じて適宜決定することができる。
【0038】
その後、得られた観察用試料について電子顕微鏡観察を行う。この時、重金属元素を含む染色剤部分については、電子線は透過せずに散乱する。このため、観察される像は、ウイルス部分は明るい像となり、染色剤部分は暗い像となる。使用する電子顕微鏡には制限はなく、透過型電子顕微鏡であれば差し支えない。観察される像の綺麗さは、観測対象像の鮮明性(高コントラスト、高解像度)、染色剤のひび割れの有無、バックグラウンドの均一性などの基準により判断することができる。
【実施例】
【0039】
以下、本発明において、実施例および比較例を挙げてさらに具体的に説明するが、本発明は実施例に限定されるものではない。
【0040】
[実施例1] Preyssler/T4
(Preyssler型リンタングステン酸の合成)
Preyssler型リンタングステン酸として、既報(Y.Jeanninら,Journal of American Chemical Society,1985,107,2662−2669)に従い、カリウムとナトリウムの混合塩であるK12.5Na1.5[NaP5W30O110]を合成し、単離した。
【0041】
具体的な合成方法としては、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O、和光純薬製)33gを純水30mlに溶解し、85質量%リン酸(85質量%H3PO4、和光純薬製)26.5mlを添加した。この溶液を、テフロン(登録商標)内筒型密閉容器(TAF−SR型、内容積100ml、耐圧硝子工業製)に入れて密閉後、120℃の水熱条件下で一晩静置した。容器を室温まで放冷して容器を開放し、純水15mlをゆっくりと添加、引き続いて塩化カリウム(和光純薬製)10gを添加した。生じた沈澱は、吸引ろ過によりろ別し、2mol/lの酢酸カリウム(和光純薬製)水溶液およびメタノール(和光純薬製)で洗浄した。吸引条件下で乾燥後、得られた黄白色固体を熱水30mlに溶解し、静置して室温まで放冷し、再結晶した。吸引ろ過して得られた白色固体について、同様な方法で再結晶を2回繰返し、白色結晶を得た。
【0042】
また、合成した化合物がK12.5Na1.5[NaP5W30O110]・37H2Oであることは、FT−IR(PARAGON 1000、Perkin−Elmer製)、元素分析(ICP発光分析:IRIS−AP、Jarrell Ash Japan製、原子吸光:AAnalyst 800、Perkin−Elmer製)、31P−NMR(Varian System 500、Varian製)および183W−NMR(Varian System 500、Varian製)により確認した。FT−IRスペクトルにおいては、789、912、937、1018、1083および1164cm-1に[NaP5W30O110]14-アニオンに特徴的な振動が観測された。元素分析においては、質量%での実測値(計算値)として、K:6.03(5.65)、Na:0.48(0.67)、P:1.51(1.79)、W:63.7(63.8)であった。31P−NMR(共鳴周波数:202.333MHz、溶媒:重水)においては、85質量%H3PO4を外部標準とし、H3PO4のP由来のシグナルを0ppmとした場合の化学シフト値として、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。183W−NMR(共鳴周波数:20.825MHz、溶媒:重水)においては、飽和Na2WO4重水溶液を外部標準とし、Na2WO4のW由来のシグナルを0ppmとした場合の化学シフト値として、−207.9、−209.9、−275.0および−287.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが、積分比2:2:1:1で確認された。なお、183W−NMRの前処理として、K12.5Na1.5[NaP5W30O110]を重水中でLi+型陽イオン交換樹脂とともに攪拌してカチオン交換を施した。この操作により、サンプルの重水への溶解度が向上し、より良好なスペクトルを得ることができる。このとき、カチオンの相違は、183W−NMRでのケミカルシフト値に影響を与えないことを確認している。
【0043】
(観察対象)
細菌に感染するウイルスであるT4ファージ(NBRC;NITE Biological Resource Centerより購入、T4(NBRC20004))を二重寒天培養法により37℃で24時間培養し、精製したものを用いた。
【0044】
(染色剤溶液)
Preyssler型リンタングステン酸を蒸留水に溶かし、濃度を0.5質量%とした溶液を用いた。
【0045】
(染色方法)
染色は以下の手順で行った。前記ファージの濃度を約1011PFU/ml(PFU:Plaque forming unit)に調整したファージ溶液(PBS:phosphate buffered saline)5μlを、カーボン蒸着および親水化処理を施したコロジオン膜張りCuグリッド(日新EM社製、製品番号:6511、200メッシュ)上にマイクロピペット3を用いて図4(a)に示すように滴下し、グリッドと3分間接触させた後、余分な溶液を5Cのろ紙で吸い取った。その後、試料に前記染色剤溶液5μlを、マイクロピペットを用いて図4(a)に示すように滴下し、3分間接触させた後、余分な溶液を5Cのろ紙により吸い取った。なお、ろ紙で余分な溶液を吸い取る際には、図4(b)に示すようにグリッド2とろ紙4との角度を30度に保った。その後、室温にて1時間定置乾燥させて観察用試料を得た。
【0046】
(電子顕微鏡観察)
前記観察用試料について電子顕微鏡観察を行った。電子顕微鏡観察は、広島大学自然科学研究支援開発センター遺伝子実験部門所有の透過型電子顕微鏡(JEM−1200EX、日本電子製、加速電圧80kV)を用いて行った。結果を図5(a)に示す。
【0047】
[実施例2] Preyssler/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(a)に示す。
【0048】
[実施例3] Preyssler/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(a)に示す。
【0049】
[比較例1] 酢酸ウラニル/T4
染色剤溶液として、酢酸ウラニルを蒸留水に溶かし、濃度を3質量%とした溶液を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図5(b)に示す。
【0050】
[比較例2] 酢酸ウラニル/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、比較例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(b)に示す。
【0051】
[比較例3] 酢酸ウラニル/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、比較例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(b)に示す。
【0052】
[比較例4] Keggin/T4
染色剤溶液として、Keggin型リンタングステン酸(TAAB社製)を蒸留水に溶かして濃度を0.5質量%とした後、KOH水溶液によりpHを6に調整した溶液を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図5(c)に示す。
【0053】
[比較例5] Keggin/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、比較例4と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(c)に示す。
【0054】
[比較例6] Keggin/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、比較例4と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(c)に示す。
【0055】
[実施例4] Preyssler濃度0.3質量%/T4
染色剤溶液中のPreyssler型リンタングステン酸の濃度を0.3質量%としたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図8(a)に示す。
【0056】
[実施例5] Preyssler濃度2.0質量%/T4
染色剤溶液中のPreyssler型リンタングステン酸の濃度を2.0質量%としたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図8(b)に示す。
【0057】
[実施例6] Ca−Preyssler/T4
(Ca2+交換Preyssler型リンタングステン酸の合成)
実施例1と同様な方法で調製したK12.5Na1.5[NaP5W30O110]・15H2Oを純水に溶解し、1.2当量の塩化カルシウム(CaCl2、和光純薬製)を加え、既報(M.T.Popeら,Inorganic Chemistry,1993,32,1573−1578)に従って160℃で2日間反応させることにより、K13[CaP5W30O110]を合成し、単離した。元素分析(Mikroanalytisches Labor Pascher社により分析、所在地:An der Pulvermuhle 1,D−53424,Remagen−Bndorf,Germany)により、質量%での実測値(計算値)として、K:5.78(5.94)、Ca:0.48(0.46)、P:1.84(1.84)、W:65.4(65.4)、H:0.59(0.60)が得られ、本化合物がK13[CaP5W30O110]・25H2Oであることを確認した。また、実施例1と同様な方法で31P−NMRを測定し、−9.0および−11.1ppmに[CaP5W30O110]13-アニオン由来のシグナルが確認された。
【0058】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK13[CaP5W30O110]を用いたこと以外は、実施例1と同様な方法で行った。結果を図9に示す。
【0059】
[実施例7] Y−Preyssler/T4
(Y3+交換Preyssler型リンタングステン酸の合成)
塩化カルシウムの代わりに1.2当量の硝酸イットリウム・6水和物(Y(NO3)3・6H2O、アルドリッチ製)を用いたこと以外は、実施例6と同様にして、K12[YP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.78(5.74)、Y:1.05(1.04)、P:1.84(1.84)、W:65.4(65.4)、H:0.59(0.55)が得られ、本化合物がK12[YP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−10.1ppmに[YP5W30O110]12-アニオン由来のシグナルが確認された。
【0060】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[YP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図10に示す。
【0061】
[実施例8] Ce−Preyssler/T4
(Ce3+交換Preyssler型リンタングステン酸の合成)
溶媒として0.1mol/lの硝酸(HNO3)水溶液を用いたこと、塩化カルシウムの代わりに3当量の硝酸アンモニウムセリウム(IV)((NH4)2[Ce(NO3)6]、和光純薬製)を用いたことおよび反応温度を180℃としたこと以外は、実施例6と同様にして、K12[CeP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.74(5.78)、Ce:1.65(1.63)、P:1.83(1.81)、W:65.0(64.7)、H:0.59(0.60)が得られ、得られた化合物がK12[CeP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−15.9ppmに[CeP5W30O110]12-アニオン由来のシグナルが確認された。
【0062】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[CeP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図11に示す。
【0063】
[実施例9] Eu−Preyssler/T4
(Eu3+交換Preyssler型リンタングステン酸の合成)
塩化カルシウムの代わりに1.2当量の硝酸ユウロピウム(III)・6水和物(Eu(NO3)3・6H2O、和光純薬製)を用いたこと以外は、実施例6と同様にして、K12[EuP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.74(5.80)、Eu:1.79(1.81)、P:1.82(1.82)、W:64.9(64.8)、H:0.59(0.53)が得られ、本化合物がK12[EuP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、0.6ppmに[EuP5W30O110]12-アニオン由来のシグナルが確認された。
【0064】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[EuP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図12に示す。
【0065】
[実施例10] Bi−Preyssler/T4
(Bi3+交換Preyssler型リンタングステン酸の合成)
溶媒として0.1mol/lのHCl水溶液を用いたこと、塩化カルシウムの代わりに2当量の塩化ビスマス(III)(BiCl3、和光純薬製)を用いたこと以外は、実施例6と同様にして、K12[BiP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.70(5.73)、Bi:2.44(2.41)、P:1.81(1.80)、W:64.5(64.6)、H:0.58(0.54)が得られ、本化合物がK12[BiP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−8.2ppmに[BiP5W30O110]12-アニオン由来のシグナルが確認された。
【0066】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[BiP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図13に示す。
【0067】
[実施例11] Eu−Preyssler/T7
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
実施例9の染色剤を用いたこと以外は、実施例2と同様な方法で行った。結果を図14に示す。
【0068】
[実施例12] Eu−Preyssler/λ
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
実施例3の観察対象を用いたこと以外は、実施例11と同様な方法で行った。結果を図15に示す。
【0069】
[実施例13] Preyssler−NH4塩/T4
(Preyssler型リンタングステン酸NH4塩の合成)
実施例1記載の既報に従って合成したK12.5Na1.5[NaP5W30O110]を原料とし、H14[NaP5W30O110]を経由して(NH4)14[NaP5W30O110]を合成した。具体的には、20gのK12.5Na1.5[NaP5W30O110]・15H2Oを300mlの純水に溶解し、50gのDowex50W×8(プロトン型陽イオン交換樹脂、和光純薬製)をつめたカラム(カラム内径:約15mm)にこの溶液を流通させることでH14[NaP5W30O110]へ変換した。得られた溶液をロータリーエバポレーター(32mbar、45℃)を用いて濃縮、乾燥し、固体を得た。実施例6と同様な方法で元素分析と31P−NMRを測定し、実施例1と同様な方法で183W−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:<0.0002(0.00)、Na:0.26(0.28)、P:1.72(1.88)、W:67.02(66.77)、H:1.10(1.24)が得られ、本化合物がH14[NaP5W30O110]・44H2Oであることを確認した。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。183W−NMRにより、−207.8、−209.7、−275.9および−288.3ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0070】
0.772gのH14[NaP5W30O110]・44H2Oと10mlの純水を、冷却管を取り付けた200ml二口フラスコに入れ、95℃に加熱したオイルバス中に30分間保持した。その溶液に0.12gの炭酸水素アンモニウム(NH4HCO3、和光純薬製)を55mlの純水に溶解した溶液を、滴下ロートを用いて30分かけて滴下した。滴下終了後、室温まで冷却し、ロータリーエバポレーター(32mbar、45℃)を用いて、3時間濃縮乾燥した。実施例1と同様な方法でFT−IRと31P−NMRを測定した。FT−IRスペクトルにおいては、784、912、935、984、1018、1079および1164cm-1に[NaP5W30O110]14-アニオンに特徴的な振動が、1401cm-1にNH4+カチオンに特徴的な振動が観測された。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0071】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
(NH4)14[NaP5W30O110]を染色剤として用いたこと以外は、実施例1と同様な方法で行った。結果を図16に示す。
【0072】
[実施例14] Preyssler−K塩/T4
(Preyssler型リンタングステン酸K塩の合成)
実施例1記載の既報に従い、K14[NaP5W30O110]を合成した。具体的には、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O、和光純薬製)99gを純水90mlに溶解し、85質量%リン酸(85質量%H3PO4、和光純薬製)79.5mlを添加した。この溶液を、テフロン(登録商標)内筒型密閉容器(TAF−SR型、内容積300ml、耐圧硝子工業製)に入れて密閉後、120℃の水熱条件下で一晩静置した。容器を室温まで放冷して容器を開放し、純水45mlをゆっくりと添加、引き続いて塩化カリウム(和光純薬製)30gを添加した。生じた沈澱は、吸引ろ過によりろ別し、2mol/lの酢酸カリウム(和光純薬製)水溶液(150ml)およびメタノール(和光純薬製)(150ml)で洗浄した。吸引条件下で乾燥すると薄い黄白色固体が得られた(約60g)。得られた黄白色固体(約60g)を100度の熱水70mlに溶解し、静置してゆっくり室温まで放冷し、再結晶した。吸引ろ過して白色固体を得た(約25g)。この得られた白色固体(約25g)を100度の熱水20mlに溶解し、静置して室温までゆっくり放冷し、再結晶した。析出した固体を吸引ろ過して、白色固体を得た(約20g)。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:6.31(6.50)、Na:0.28(0.27)、P:1.83(1.84)、W:65.5(65.5)、H:0.54(0.55)が得られ、本化合物がK14[NaP5W30O110]・23H2Oであることを確認した。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0073】
なお、前述したように、リンタングステン酸の水和水量(nH2O)は、乾燥状態や保管状態などにより変化するが、本発明においては、その変化は染色剤としての性能に影響を及ぼさない。また、本願発明者の検討により、K14-xNax[NaP5W30O110]・nH2OにおけるNaの含有率xは、同様な調製条件で合成された場合にも、元素分析結果におけるxが0〜1.5の間で変化する場合があることが分かった(例えば、実施例1と実施例6ではx=1.5、実施例14ではx=0)。この変化も、原料としての性質および染色剤としての性能に影響は与えないため、xおよびnの異なるK14-xNax[NaP5W30O110]・nH2Oは本発明において問題なく使用できる。
【0074】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
K14[NaP5W30O110]を染色剤として用いたこと以外は、実施例1と同様な方法で行った。結果を図17に示す。
【符号の説明】
【0075】
1 ピンセット
2 グリッド
3 マイクロピペット
4 ろ紙
【技術分野】
【0001】
本発明は、電子顕微鏡観察用試料のネガティブ染色剤および該染色剤を用いた電子顕微鏡観察用試料のネガティブ染色方法に関する。
【背景技術】
【0002】
ナノレベルからマイクロレベルの微細構造を高精度に観察することへの要求は、有機物、無機物を問わず近年ますます高まっている。さらにこのところ、新型インフルエンザ、ノロウイルスおよび口蹄疫などのウイルスが原因となる流行性の感染症の発生および拡大が問題となっている。これら感染症の蔓延を防止するためには、原因となるウイルスの分類を同定するための微細構造解析を行うことが不可欠である。
【0003】
ウイルスは10〜200ナノメートルと小さいため、微細構造解析には走査型および/または透過型電子顕微鏡(TEM)を用いる必要がある。この中でも、特にTEMを用いることが有効である。しかしながら、有機物であるウイルス上では電子線の散乱が起こりにくいため、重元素などを用いた染色が必須となる。重元素などを用いた染色を行うことで、染色剤部分は電子線が散乱するため暗い像となり、観察対象部分は電子線が透過するため明るい像となる。染色剤が観察対象や観察対象を固定する支持膜と上手く相互作用していれば、観察対象の微細構造を反映した像が得られる。このような染色方法はネガティブ染色方法と呼ばれる。
【0004】
これまでに、ネガティブ染色方法に用いられるネガティブ染色剤は数多く提案されている。ネガティブ染色剤としては、例えば、酢酸ウラニル(特許文献1、非特許文献1および非特許文献3〜5)、クエン酸鉛(特許文献1および非特許文献1)、酢酸鉛および硝酸鉛(非特許文献1)、リンタングステン酸(特許文献2、3および非特許文献1、2)、モリブデン酸アンモニウム・4水和物(非特許文献1、2)、タングステン酸アンモニウム・5水和物(非特許文献3)、塩化ハフニウム(非特許文献4)、塩化ジルコニウム(非特許文献4)および白金ブルー(非特許文献5)などが提案されている。さらに、粘度や浸透性能の制御を目的として、染色剤溶液への添加剤の添加についても提案されている(非特許文献1)。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2007−309872号公報
【特許文献2】特開平5−306979号公報
【特許文献3】特開平2−118431号公報
【非特許文献】
【0006】
【非特許文献1】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p93−98、2007年
【非特許文献2】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p1−6、2007年
【非特許文献3】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第24巻(第2号)、p59−60、2010年
【非特許文献4】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第20巻(第1号)、p69−70、2006年
【非特許文献5】医生電顕技術誌(J.Electr.Microsc.Technol.Med.Biol.)、第21巻(第1号)、p90−92、2007年
【発明の概要】
【発明が解決しようとする課題】
【0007】
しかしながら、最も汎用されている酢酸ウラニル(酢酸ウラン)は、良好な染色性を示すものの、放射性物質であるウラン(劣化ウラン)が使用されており、兵器への転用が可能であることから使用制限や管理などが強化されつつあるため、安全性が高く簡便に使用可能な代替染色剤の開発が望まれている。また、鉛塩類、モリブデン酸アンモニウム、タングステン酸アンモニウム、塩化ハフニウム、塩化ジルコニウムおよび白金ブルーは、安全性の面では優れているが酢酸ウラニルに比べてコントラストが弱く染色能力が劣り、観察対象の性質や調製条件などの点でも適正に使用できる範囲が狭い。
【0008】
一方、特許文献2、3および非特許文献1、2に開示されているリンタングステン酸は、酢酸ウラニルに次いで汎用なネガティブ染色剤であり、ケギン(Keggin)型と呼ばれるリン酸とタングステン酸との縮合により合成されるヘテロポリ酸(ポリオキソメタレート)である。現在、市販試薬として容易に入手できるリンタングステン酸は、Keggin型リンタングステン酸のみであり、ネガティブ染色剤において単にリンタングステン酸あるいはPTA(Phosphotungstic Acid)と表記される場合には、Keggin型リンタングステン酸を意味する。さらに、本願発明者は、ネガティブ染色剤として市販されているリンタングステン酸(Phosphotungustate acid EM、TAAB Laboratories製)をFT−IRおよび31P−NMRを用いて分析したところ、Keggin型リンタングステン酸に特有なスペクトルを示すことを確認している。
【0009】
図1にKeggin型リンタングステン酸アニオンの一次構造を示す。H3PW12O40で表されるKeggin型リンタングステン酸は、水溶液中での安定性が非常に低く、pH<1の領域でしか構造を保てない課題がある。例えば、ウイルス、菌および細胞などの試料の観察はほぼ中性領域で行われるため、Keggin型リンタングステン酸の安定pH領域以外では、Keggin型構造の分解が懸念される。また、前記分解が生じた場合、ウイルスの表面蛋白質や支持膜との相互作用も大きく変化する可能性がある。
【0010】
したがって、Keggin型リンタングステン酸を染色剤に用いる場合には、種々の分解生成物に由来する観察試料の均質性の低下が生じ、染色性が低下する。また、これを改善するためにKeggin型リンタングステン酸溶液に酢酸などを添加する場合にも、染色剤溶液の調製が煩雑になり、好適条件の決定が難しい。このような背景から、染色が簡便で、染色性が十分に高く、使用可能範囲が広い代替染色剤の開発が望まれている。
【0011】
本発明の目的は、適用範囲が広く高い染色性を示し、取り扱いが容易で安全性の高い電子顕微鏡観察用染色剤を提供することにある。
【課題を解決するための手段】
【0012】
本発明に係る電子顕微鏡観察用染色剤は、一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110](式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)で表されるリンタングステン酸を含む。
【0013】
本発明に係る電子顕微鏡観察用試料の染色方法は、本発明に係る電子顕微鏡観察用染色剤を用いる。
【発明の効果】
【0014】
本発明によれば、適用範囲が広く高い染色性を示し、取り扱いが容易で安全性の高い電子顕微鏡観察用染色剤を提供することができる。
【図面の簡単な説明】
【0015】
【図1】Keggin型リンタングステン酸アニオンの一次構造を示す模式図である。
【図2】Preyssler型リンタングステン酸アニオンの一次構造を示す(a)側面図、(b)上面図である。
【図3】本発明に係る染色方法の一例を示す模式図である。
【図4】(a)マイクロピペットを用いてグリッドに染色剤溶液を滴下する操作の概略図、(b)ろ紙で余分な溶液を吸い取る際の、グリッドとろ紙との位置関係を示す概略図である。
【図5】(a)実施例1、(b)比較例1、(c)比較例4の各種染色剤により染色したT4ファージのTEM像である。
【図6】(a)実施例2、(b)比較例2、(c)比較例5の各種染色剤により染色したT7ファージのTEM像である。
【図7】(a)実施例3、(b)比較例3、(c)比較例6の各種染色剤により染色したλファージのTEM像である。
【図8】(a)実施例4、(b)実施例5の各種濃度の染色剤溶液を用いて染色したT4ファージのTEM像である。
【図9】実施例6の染色剤により染色したT4ファージのTEM像である。
【図10】実施例7の染色剤により染色したT4ファージのTEM像である。
【図11】実施例8の染色剤により染色したT4ファージのTEM像である。
【図12】実施例9の染色剤により染色したT4ファージのTEM像である。
【図13】実施例10の染色剤により染色したT4ファージのTEM像である。
【図14】実施例11の染色剤により染色したT7ファージのTEM像である。
【図15】実施例12の染色剤により染色したλファージのTEM像である。
【図16】実施例13の染色剤により染色したT4ファージのTEM像である。
【図17】実施例14の染色剤により染色したT4ファージのTEM像である。
【発明を実施するための形態】
【0016】
[電子顕微鏡観察用染色剤]
本発明に係る電子顕微鏡観察用染色剤に含まれる、一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]で表されるリンタングステン酸は、Preyssler型と呼ばれるリンタングステン酸である。Preyssler型リンタングステン酸は、Keggin型とは異なる形でリン酸とタングステン酸とが縮合したヘテロポリ酸の一種である。Preyssler型リンタングステン酸アニオンの一次構造を図2に示す。
【0017】
Keggin型リンタングステン酸は、1933年にその一次構造が決定され、染色剤の他、触媒、導電材料およびナノ材料などとして広く研究されてきた。一方、Preyssler型リンタングステン酸は1970年に初めて合成され、その一次構造が決定されたのは1985年である。Preyssler型リンタングステン酸は、Keggin型のそれよりも研究の歴史が浅く、合成も難しいとされていた。本願発明者はPreyssler型リンタングステン酸の調製方法、物性および特徴を鋭意研究しており、Keggin型リンタングステン酸よりも、重元素であるタングステンを一次構造中に多く有するPreyssler型リンタングステン酸の方が、電子顕微鏡観察用染色剤としてより良好な性能を示すと考えた。また、電子顕微鏡観察用染色剤としてPreyssler型リンタングステン酸は、pH<12の広いpH範囲で安定に存在するため、ネガティブ染色剤としてKeggin型リンタングステン酸と比較して良好な染色性能を示すことができる。さらに、Preyssler型リンタングステン酸は、アニオンおよびカチオンの構成元素(Aa+、Zb+およびM(d))を種々変えることができるため、分子設計・物性制御の幅が広く、適用可能な検体の範囲も広い。
【0018】
前記一般式において、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。なお、前記一般式で表されるリンタングステン酸には、前記一般式の水和物も含まれる。リンタングステン酸が水和物の場合、水和物の水和水量(nH2O)は特に限定されず、0≦nであることができる。水和物の水和水量は、その乾燥状態や保管状態などにより変化する。仮に水和物の水和水量が異なったとしても、電子顕微鏡観察用染色剤としての性能は同じである。そのため、前記一般式では、水和水の記載は省略している。
【0019】
前記一般式において、Aa+としては0<aであれば特に制限されない。aは、0<a≦3とすることもでき、0<a≦2とすることもできる。Aa+としては、第1族元素のカチオン、第2族元素のカチオン、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであることが好ましい。Aa+としては、H+、Li+、Na+、K+、Rb+、Cs+、Be2+、Mg2+、Ca2+、Sr2+、Ba2+、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであることがより好ましい。
【0020】
前記ピリジニウムカチオンはC5H5N+Rで表され、前記第4級アンモニウムカチオンはR4N+で表される。ピリジニウムカチオンおよび4級アンモニウムカチオンは、C1からC21までの種々の炭化水素基(R)で窒素原子がアルキル化されたピリジンおよびアルキルアンモニウムのカチオンである。Rとしては特に限定されないが、メチル基、エチル基、n−プロピル基、n−ブチル基、ドデシル基、セチル基などが挙げられる。第4級アンモニウムカチオンにおいては、複数のRは同じでも異なっていてもよい。また、Rは官能基を有していても差し支えない。なお、Aa+が複数の種類のカチオンを含む場合、aの値は各カチオンの価数に各モル比を乗じた値の和とする。例えば、Aa+がK+と、Ca2+とをモル比0.5:0.5で含む場合、aの値は1×0.5+2×0.5=1.5となる。
【0021】
前記一般式において、Zb+としては0<bであれば特に制限されない。bは、0<b≦6とすることもでき、0<b≦4とすることもできる。Zb+としては、第1族元素のカチオン、第2族元素のカチオン、第3族元素のカチオン、第15族元素のカチオン、ランタノイド元素のカチオンおよびアクチノイド元素のカチオンからなる群より選ばれる少なくとも一つのカチオンであることが好ましい。Zb+としては、Na+、Ca2+、Sr2+、Bi3+、Y3+、La3+、Ce3+、Eu3+、Gd3+、Lu3+、Am3+、Th4+およびU4+からなる群より選ばれる少なくとも一つのカチオンであることがより好ましい。なお、ネガティブ染色の原理からは、Aa+およびZb+により重い元素を導入すれば、より鮮明な像が得られる。
【0022】
前記一般式において、M(d)としては0<d≦6であれば特に制限されない。dは2≦d≦6とすることもでき、3≦d≦6とすることもできる。M(d)としては、d価の第5族元素およびd価の第6族元素の少なくとも一方であることが好ましい。M(d)としては、W(VI)、Mo(VI)およびV(IV)からなる群より選ばれる少なくとも一つの元素であることがより好ましい。cは0≦c<30であるが、0≦c≦5とすることができ、合成の困難さや構造安定性の観点から、cは0、1または2が好ましい。
【0023】
なお、c=0の場合、前記一般式にはM(d)は含まれないが、この場合前記一般式は、Aa+(15-b)/a[Zb+P5W30O110](式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオンを示す。0<a、0<bである。)で表される。
【0024】
前記一般式で表されるリンタングステン酸は、例えばM.T.Popeら,Inorganic Chemistry,1993,32,1573−1578、またはY.Jeanninら,Journal of American Chemical Society,1985,107,2662−2669に開示されている方法により製造することができる。
【0025】
例えば、K12.5Na1.5[NaP5W30O110]・nH2Oの製造方法としては、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O)を水に溶解し、85質量%リン酸(H3PO4)を加え、圧力容器中、120℃において一晩水熱合成を行う。室温まで冷却後、水および塩化カリウム(KCl)を添加し、析出した固体をろ過し、酢酸カリウムおよびメタノールで洗浄する。得られた固体を熱水に溶解して室温まで放冷し、再結晶を行うことで得ることができる。再結晶を繰り返すと収率は低下するものの、純度を向上させることができる。
【0026】
[NaP5W30O110]14-アニオン中の、Na+のZb+への交換は、[NaP5W30O110]14-アニオン水溶液に交換するZb+を含有する溶液を添加して、圧力容器中、140〜180℃において一晩水熱合成を行う。その後、KClを添加し、ろ別し、洗浄および乾燥を行うことで、Na+のZb+への交換を行うことができる。
【0027】
[NaP5W30O110]14-アニオン中の、W(VI)のM(d)への置換は、pHを調整した[NaP5W30O110]14-アニオン水溶液にM(d)を含有する溶液を添加する。その後、KClを添加し、ろ別し、洗浄および乾燥を行うことで、W(VI)のM(d)への置換を行うことができる。
【0028】
カチオンAa+を交換する方法としては、陽イオン交換樹脂を用いる方法が有用である。各種カチオン型交換樹脂に、[NaP5W30O110]14-アニオン水溶液を処理することで、カチオンAa+を交換することが可能である。また、プロトン型交換樹脂で処理してプロトン型H14[NaP5W30O110]とした後、各種カチオンでプロトンを部分中和することも可能である。
【0029】
Aa+、Zb+およびM(d)の交換および置換に用いる原料は特に制限されず、交換および置換したいカチオンまたは元素の硝酸塩、硫酸塩、酢酸塩、炭酸塩および塩化物などを用いることができる。これらは一種のみを用いてもよく、二種以上を併用してもよい。
【0030】
合成した前記一般式で表されるリンタングステン酸は、FT−IR、ICP発光分析や原子吸光などの元素分析、X線回折、31P−NMR、183W−NMR等により構造と組成を確認することができる。
【0031】
[電子顕微鏡観察用試料の染色方法]
本発明に係る電子顕微鏡観察用染色剤は、電子顕微鏡観察用試料の染色に用いることができる。本発明に係る方法によれば、電子顕微鏡観察用試料をより簡便に染色することができる。
【0032】
本発明に係る電子顕微鏡観察用染色剤を用いて染色し、電子顕微鏡観察を行う観察対象としては、特に制限されず、例えば細胞、ウイルス、ファージ(細菌に感染するウイルスの総称)、たんぱく質、低分子酵素、核、ミトコンドリア、リポソーム、グリコーゲン、脂肪滴、膜系、菌体、細菌鞭毛およびグラム陰性菌などが挙げられる。
【0033】
観察対象を定着させる支持膜としては、特に制限されず、コロジオン膜、フォルムバール膜およびカーボン膜などが挙げられ、必要に応じて蒸着処理や親水化処理を施したものであってもよい。
【0034】
本発明に係る染色剤に含まれるリンタングステン酸はPreyssler型リンタングステン酸であるため、染色剤溶液の調製においては、Keggin型リンタングステン酸やモリブデン酸アンモニウム等を用いる場合とは異なり、アルカリを用いたpH調整や酢酸などの添加は不要である。このため、本発明に係る染色剤を用いた染色剤溶液の調製は、非常に簡便に行うことができる。
【0035】
染色剤溶液に含まれる溶媒としては、水、アルコールなどが挙げられる。
【0036】
染色剤溶液中の前記一般式で表されるリンタングステン酸の濃度は、0.1質量%以上が好ましく、0.2質量%以上がより好ましく、0.3質量%以上がさらに好ましい。また、前記濃度は1.9質量%以下が好ましく、1.5質量%以下がより好ましく、1.0質量%以下がさらに好ましい。前記濃度を前記範囲とすることで、分散性、浸透圧、表面張力、支持膜や試料表面との相互作用などをバランスよく制御でき、高コントラストで微細構造の電子顕微鏡観察が可能となる。
【0037】
本発明に係る染色方法の一例を図3に示す。支持膜である透過型電子顕微鏡(TEM)用コロジオン膜に親水化処理を施し、観察対象であるウイルスを接触させ、定着させる。定着させたウイルスに、本発明に係る染色剤を溶解させた染色剤溶液を滴下して接触させる。その後、余分な溶液をろ紙で吸い取ることで取り除き、定置乾燥を行う。観察対象の支持膜への接触時間、染色剤溶液の観察対象への接触時間および定置乾燥の乾燥時間は特に限定されず、電子顕微鏡観察の結果を考慮しながら、観察対象に応じて適宜決定することができる。
【0038】
その後、得られた観察用試料について電子顕微鏡観察を行う。この時、重金属元素を含む染色剤部分については、電子線は透過せずに散乱する。このため、観察される像は、ウイルス部分は明るい像となり、染色剤部分は暗い像となる。使用する電子顕微鏡には制限はなく、透過型電子顕微鏡であれば差し支えない。観察される像の綺麗さは、観測対象像の鮮明性(高コントラスト、高解像度)、染色剤のひび割れの有無、バックグラウンドの均一性などの基準により判断することができる。
【実施例】
【0039】
以下、本発明において、実施例および比較例を挙げてさらに具体的に説明するが、本発明は実施例に限定されるものではない。
【0040】
[実施例1] Preyssler/T4
(Preyssler型リンタングステン酸の合成)
Preyssler型リンタングステン酸として、既報(Y.Jeanninら,Journal of American Chemical Society,1985,107,2662−2669)に従い、カリウムとナトリウムの混合塩であるK12.5Na1.5[NaP5W30O110]を合成し、単離した。
【0041】
具体的な合成方法としては、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O、和光純薬製)33gを純水30mlに溶解し、85質量%リン酸(85質量%H3PO4、和光純薬製)26.5mlを添加した。この溶液を、テフロン(登録商標)内筒型密閉容器(TAF−SR型、内容積100ml、耐圧硝子工業製)に入れて密閉後、120℃の水熱条件下で一晩静置した。容器を室温まで放冷して容器を開放し、純水15mlをゆっくりと添加、引き続いて塩化カリウム(和光純薬製)10gを添加した。生じた沈澱は、吸引ろ過によりろ別し、2mol/lの酢酸カリウム(和光純薬製)水溶液およびメタノール(和光純薬製)で洗浄した。吸引条件下で乾燥後、得られた黄白色固体を熱水30mlに溶解し、静置して室温まで放冷し、再結晶した。吸引ろ過して得られた白色固体について、同様な方法で再結晶を2回繰返し、白色結晶を得た。
【0042】
また、合成した化合物がK12.5Na1.5[NaP5W30O110]・37H2Oであることは、FT−IR(PARAGON 1000、Perkin−Elmer製)、元素分析(ICP発光分析:IRIS−AP、Jarrell Ash Japan製、原子吸光:AAnalyst 800、Perkin−Elmer製)、31P−NMR(Varian System 500、Varian製)および183W−NMR(Varian System 500、Varian製)により確認した。FT−IRスペクトルにおいては、789、912、937、1018、1083および1164cm-1に[NaP5W30O110]14-アニオンに特徴的な振動が観測された。元素分析においては、質量%での実測値(計算値)として、K:6.03(5.65)、Na:0.48(0.67)、P:1.51(1.79)、W:63.7(63.8)であった。31P−NMR(共鳴周波数:202.333MHz、溶媒:重水)においては、85質量%H3PO4を外部標準とし、H3PO4のP由来のシグナルを0ppmとした場合の化学シフト値として、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。183W−NMR(共鳴周波数:20.825MHz、溶媒:重水)においては、飽和Na2WO4重水溶液を外部標準とし、Na2WO4のW由来のシグナルを0ppmとした場合の化学シフト値として、−207.9、−209.9、−275.0および−287.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが、積分比2:2:1:1で確認された。なお、183W−NMRの前処理として、K12.5Na1.5[NaP5W30O110]を重水中でLi+型陽イオン交換樹脂とともに攪拌してカチオン交換を施した。この操作により、サンプルの重水への溶解度が向上し、より良好なスペクトルを得ることができる。このとき、カチオンの相違は、183W−NMRでのケミカルシフト値に影響を与えないことを確認している。
【0043】
(観察対象)
細菌に感染するウイルスであるT4ファージ(NBRC;NITE Biological Resource Centerより購入、T4(NBRC20004))を二重寒天培養法により37℃で24時間培養し、精製したものを用いた。
【0044】
(染色剤溶液)
Preyssler型リンタングステン酸を蒸留水に溶かし、濃度を0.5質量%とした溶液を用いた。
【0045】
(染色方法)
染色は以下の手順で行った。前記ファージの濃度を約1011PFU/ml(PFU:Plaque forming unit)に調整したファージ溶液(PBS:phosphate buffered saline)5μlを、カーボン蒸着および親水化処理を施したコロジオン膜張りCuグリッド(日新EM社製、製品番号:6511、200メッシュ)上にマイクロピペット3を用いて図4(a)に示すように滴下し、グリッドと3分間接触させた後、余分な溶液を5Cのろ紙で吸い取った。その後、試料に前記染色剤溶液5μlを、マイクロピペットを用いて図4(a)に示すように滴下し、3分間接触させた後、余分な溶液を5Cのろ紙により吸い取った。なお、ろ紙で余分な溶液を吸い取る際には、図4(b)に示すようにグリッド2とろ紙4との角度を30度に保った。その後、室温にて1時間定置乾燥させて観察用試料を得た。
【0046】
(電子顕微鏡観察)
前記観察用試料について電子顕微鏡観察を行った。電子顕微鏡観察は、広島大学自然科学研究支援開発センター遺伝子実験部門所有の透過型電子顕微鏡(JEM−1200EX、日本電子製、加速電圧80kV)を用いて行った。結果を図5(a)に示す。
【0047】
[実施例2] Preyssler/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(a)に示す。
【0048】
[実施例3] Preyssler/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(a)に示す。
【0049】
[比較例1] 酢酸ウラニル/T4
染色剤溶液として、酢酸ウラニルを蒸留水に溶かし、濃度を3質量%とした溶液を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図5(b)に示す。
【0050】
[比較例2] 酢酸ウラニル/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、比較例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(b)に示す。
【0051】
[比較例3] 酢酸ウラニル/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、比較例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(b)に示す。
【0052】
[比較例4] Keggin/T4
染色剤溶液として、Keggin型リンタングステン酸(TAAB社製)を蒸留水に溶かして濃度を0.5質量%とした後、KOH水溶液によりpHを6に調整した溶液を用いたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図5(c)に示す。
【0053】
[比較例5] Keggin/T7
ファージとして、T7ファージ(NBRC;NITE Biological Resource Centerより購入、T7(NBRC20007))を用いたこと以外は、比較例4と同様にして観察用試料を作製し、TEM観察を行った。結果を図6(c)に示す。
【0054】
[比較例6] Keggin/λ
ファージとして、λファージ(NBRC;NITE Biological Resource Centerより購入、λ(NBRC20016))を用いたこと以外は、比較例4と同様にして観察用試料を作製し、TEM観察を行った。結果を図7(c)に示す。
【0055】
[実施例4] Preyssler濃度0.3質量%/T4
染色剤溶液中のPreyssler型リンタングステン酸の濃度を0.3質量%としたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図8(a)に示す。
【0056】
[実施例5] Preyssler濃度2.0質量%/T4
染色剤溶液中のPreyssler型リンタングステン酸の濃度を2.0質量%としたこと以外は、実施例1と同様にして観察用試料を作製し、TEM観察を行った。結果を図8(b)に示す。
【0057】
[実施例6] Ca−Preyssler/T4
(Ca2+交換Preyssler型リンタングステン酸の合成)
実施例1と同様な方法で調製したK12.5Na1.5[NaP5W30O110]・15H2Oを純水に溶解し、1.2当量の塩化カルシウム(CaCl2、和光純薬製)を加え、既報(M.T.Popeら,Inorganic Chemistry,1993,32,1573−1578)に従って160℃で2日間反応させることにより、K13[CaP5W30O110]を合成し、単離した。元素分析(Mikroanalytisches Labor Pascher社により分析、所在地:An der Pulvermuhle 1,D−53424,Remagen−Bndorf,Germany)により、質量%での実測値(計算値)として、K:5.78(5.94)、Ca:0.48(0.46)、P:1.84(1.84)、W:65.4(65.4)、H:0.59(0.60)が得られ、本化合物がK13[CaP5W30O110]・25H2Oであることを確認した。また、実施例1と同様な方法で31P−NMRを測定し、−9.0および−11.1ppmに[CaP5W30O110]13-アニオン由来のシグナルが確認された。
【0058】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK13[CaP5W30O110]を用いたこと以外は、実施例1と同様な方法で行った。結果を図9に示す。
【0059】
[実施例7] Y−Preyssler/T4
(Y3+交換Preyssler型リンタングステン酸の合成)
塩化カルシウムの代わりに1.2当量の硝酸イットリウム・6水和物(Y(NO3)3・6H2O、アルドリッチ製)を用いたこと以外は、実施例6と同様にして、K12[YP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.78(5.74)、Y:1.05(1.04)、P:1.84(1.84)、W:65.4(65.4)、H:0.59(0.55)が得られ、本化合物がK12[YP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−10.1ppmに[YP5W30O110]12-アニオン由来のシグナルが確認された。
【0060】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[YP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図10に示す。
【0061】
[実施例8] Ce−Preyssler/T4
(Ce3+交換Preyssler型リンタングステン酸の合成)
溶媒として0.1mol/lの硝酸(HNO3)水溶液を用いたこと、塩化カルシウムの代わりに3当量の硝酸アンモニウムセリウム(IV)((NH4)2[Ce(NO3)6]、和光純薬製)を用いたことおよび反応温度を180℃としたこと以外は、実施例6と同様にして、K12[CeP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.74(5.78)、Ce:1.65(1.63)、P:1.83(1.81)、W:65.0(64.7)、H:0.59(0.60)が得られ、得られた化合物がK12[CeP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−15.9ppmに[CeP5W30O110]12-アニオン由来のシグナルが確認された。
【0062】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[CeP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図11に示す。
【0063】
[実施例9] Eu−Preyssler/T4
(Eu3+交換Preyssler型リンタングステン酸の合成)
塩化カルシウムの代わりに1.2当量の硝酸ユウロピウム(III)・6水和物(Eu(NO3)3・6H2O、和光純薬製)を用いたこと以外は、実施例6と同様にして、K12[EuP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.74(5.80)、Eu:1.79(1.81)、P:1.82(1.82)、W:64.9(64.8)、H:0.59(0.53)が得られ、本化合物がK12[EuP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、0.6ppmに[EuP5W30O110]12-アニオン由来のシグナルが確認された。
【0064】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[EuP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図12に示す。
【0065】
[実施例10] Bi−Preyssler/T4
(Bi3+交換Preyssler型リンタングステン酸の合成)
溶媒として0.1mol/lのHCl水溶液を用いたこと、塩化カルシウムの代わりに2当量の塩化ビスマス(III)(BiCl3、和光純薬製)を用いたこと以外は、実施例6と同様にして、K12[BiP5W30O110]を合成し、単離した。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:5.70(5.73)、Bi:2.44(2.41)、P:1.81(1.80)、W:64.5(64.6)、H:0.58(0.54)が得られ、本化合物がK12[BiP5W30O110]・25H2Oであることを確認した。31P−NMRにおいて、−8.2ppmに[BiP5W30O110]12-アニオン由来のシグナルが確認された。
【0066】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
染色剤としてK12[BiP5W30O110]を用いたこと以外は、実施例6と同様な方法で行った。結果を図13に示す。
【0067】
[実施例11] Eu−Preyssler/T7
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
実施例9の染色剤を用いたこと以外は、実施例2と同様な方法で行った。結果を図14に示す。
【0068】
[実施例12] Eu−Preyssler/λ
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
実施例3の観察対象を用いたこと以外は、実施例11と同様な方法で行った。結果を図15に示す。
【0069】
[実施例13] Preyssler−NH4塩/T4
(Preyssler型リンタングステン酸NH4塩の合成)
実施例1記載の既報に従って合成したK12.5Na1.5[NaP5W30O110]を原料とし、H14[NaP5W30O110]を経由して(NH4)14[NaP5W30O110]を合成した。具体的には、20gのK12.5Na1.5[NaP5W30O110]・15H2Oを300mlの純水に溶解し、50gのDowex50W×8(プロトン型陽イオン交換樹脂、和光純薬製)をつめたカラム(カラム内径:約15mm)にこの溶液を流通させることでH14[NaP5W30O110]へ変換した。得られた溶液をロータリーエバポレーター(32mbar、45℃)を用いて濃縮、乾燥し、固体を得た。実施例6と同様な方法で元素分析と31P−NMRを測定し、実施例1と同様な方法で183W−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:<0.0002(0.00)、Na:0.26(0.28)、P:1.72(1.88)、W:67.02(66.77)、H:1.10(1.24)が得られ、本化合物がH14[NaP5W30O110]・44H2Oであることを確認した。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。183W−NMRにより、−207.8、−209.7、−275.9および−288.3ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0070】
0.772gのH14[NaP5W30O110]・44H2Oと10mlの純水を、冷却管を取り付けた200ml二口フラスコに入れ、95℃に加熱したオイルバス中に30分間保持した。その溶液に0.12gの炭酸水素アンモニウム(NH4HCO3、和光純薬製)を55mlの純水に溶解した溶液を、滴下ロートを用いて30分かけて滴下した。滴下終了後、室温まで冷却し、ロータリーエバポレーター(32mbar、45℃)を用いて、3時間濃縮乾燥した。実施例1と同様な方法でFT−IRと31P−NMRを測定した。FT−IRスペクトルにおいては、784、912、935、984、1018、1079および1164cm-1に[NaP5W30O110]14-アニオンに特徴的な振動が、1401cm-1にNH4+カチオンに特徴的な振動が観測された。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0071】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
(NH4)14[NaP5W30O110]を染色剤として用いたこと以外は、実施例1と同様な方法で行った。結果を図16に示す。
【0072】
[実施例14] Preyssler−K塩/T4
(Preyssler型リンタングステン酸K塩の合成)
実施例1記載の既報に従い、K14[NaP5W30O110]を合成した。具体的には、タングステン酸ナトリウム・2水和物(Na2WO4・2H2O、和光純薬製)99gを純水90mlに溶解し、85質量%リン酸(85質量%H3PO4、和光純薬製)79.5mlを添加した。この溶液を、テフロン(登録商標)内筒型密閉容器(TAF−SR型、内容積300ml、耐圧硝子工業製)に入れて密閉後、120℃の水熱条件下で一晩静置した。容器を室温まで放冷して容器を開放し、純水45mlをゆっくりと添加、引き続いて塩化カリウム(和光純薬製)30gを添加した。生じた沈澱は、吸引ろ過によりろ別し、2mol/lの酢酸カリウム(和光純薬製)水溶液(150ml)およびメタノール(和光純薬製)(150ml)で洗浄した。吸引条件下で乾燥すると薄い黄白色固体が得られた(約60g)。得られた黄白色固体(約60g)を100度の熱水70mlに溶解し、静置してゆっくり室温まで放冷し、再結晶した。吸引ろ過して白色固体を得た(約25g)。この得られた白色固体(約25g)を100度の熱水20mlに溶解し、静置して室温までゆっくり放冷し、再結晶した。析出した固体を吸引ろ過して、白色固体を得た(約20g)。実施例6と同様な方法で元素分析と31P−NMRを測定した。元素分析により、質量%での実測値(計算値)として、K:6.31(6.50)、Na:0.28(0.27)、P:1.83(1.84)、W:65.5(65.5)、H:0.54(0.55)が得られ、本化合物がK14[NaP5W30O110]・23H2Oであることを確認した。31P−NMRにより、−9.4ppmに[NaP5W30O110]14-アニオン由来のシグナルが確認された。
【0073】
なお、前述したように、リンタングステン酸の水和水量(nH2O)は、乾燥状態や保管状態などにより変化するが、本発明においては、その変化は染色剤としての性能に影響を及ぼさない。また、本願発明者の検討により、K14-xNax[NaP5W30O110]・nH2OにおけるNaの含有率xは、同様な調製条件で合成された場合にも、元素分析結果におけるxが0〜1.5の間で変化する場合があることが分かった(例えば、実施例1と実施例6ではx=1.5、実施例14ではx=0)。この変化も、原料としての性質および染色剤としての性能に影響は与えないため、xおよびnの異なるK14-xNax[NaP5W30O110]・nH2Oは本発明において問題なく使用できる。
【0074】
(観察対象、染色剤溶液、染色方法および電子顕微鏡観察)
K14[NaP5W30O110]を染色剤として用いたこと以外は、実施例1と同様な方法で行った。結果を図17に示す。
【符号の説明】
【0075】
1 ピンセット
2 グリッド
3 マイクロピペット
4 ろ紙
【特許請求の範囲】
【請求項1】
一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]
(式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)
で表されるリンタングステン酸を含む電子顕微鏡観察用染色剤。
【請求項2】
前記一般式において、Aa+がH+、Li+、Na+、K+、Rb+、Cs+、Be2+、Mg2+、Ca2+、Sr2+、Ba2+、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであり、Zb+がNa+、Ca2+、Sr2+、Bi3+、Y3+、La3+、Ce3+、Eu3+、Gd3+、Lu3+、Am3+、Th4+およびU4+からなる群より選ばれる少なくとも一つのカチオンであり、M(d)がW(VI)、Mo(VI)およびV(IV)からなる群より選ばれる少なくとも一つの元素である請求項1に記載の電子顕微鏡観察用染色剤。
【請求項3】
請求項1または2に記載の電子顕微鏡観察用染色剤を用いる電子顕微鏡観察用試料の染色方法。
【請求項1】
一般式Aa+[(15-b)+c(6-d)]/a[Zb+P5W(30-c)M(d)cO110]
(式中、P、WおよびOは、それぞれリン、タングステンおよび酸素を示す。Aa+はa価のカチオン、Zb+はb価のカチオン、M(d)はd価の元素を示す。0<a、0<b、0≦c<30、0<d≦6である。)
で表されるリンタングステン酸を含む電子顕微鏡観察用染色剤。
【請求項2】
前記一般式において、Aa+がH+、Li+、Na+、K+、Rb+、Cs+、Be2+、Mg2+、Ca2+、Sr2+、Ba2+、NH4+、ピリジニウムカチオンおよび第4級アンモニウムカチオンからなる群より選ばれる少なくとも一つのカチオンであり、Zb+がNa+、Ca2+、Sr2+、Bi3+、Y3+、La3+、Ce3+、Eu3+、Gd3+、Lu3+、Am3+、Th4+およびU4+からなる群より選ばれる少なくとも一つのカチオンであり、M(d)がW(VI)、Mo(VI)およびV(IV)からなる群より選ばれる少なくとも一つの元素である請求項1に記載の電子顕微鏡観察用染色剤。
【請求項3】
請求項1または2に記載の電子顕微鏡観察用染色剤を用いる電子顕微鏡観察用試料の染色方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【公開番号】特開2012−247411(P2012−247411A)
【公開日】平成24年12月13日(2012.12.13)
【国際特許分類】
【出願番号】特願2012−99825(P2012−99825)
【出願日】平成24年4月25日(2012.4.25)
【出願人】(000006035)三菱レイヨン株式会社 (2,875)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
【公開日】平成24年12月13日(2012.12.13)
【国際特許分類】
【出願日】平成24年4月25日(2012.4.25)
【出願人】(000006035)三菱レイヨン株式会社 (2,875)
【出願人】(504136568)国立大学法人広島大学 (924)
【Fターム(参考)】
[ Back to top ]

