電極活物質、及び当該電極活物質を負極に含有する金属二次電池
【課題】金属二次電池に使用された際に、従来の負極活物質よりサイクル特性を向上させることができる電極活物質、及び当該電極活物質を負極に含有する金属二次電池を提供する。
【解決手段】下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする、電極活物質。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【解決手段】下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする、電極活物質。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、金属二次電池に使用された際に、従来の負極活物質を使用した金属二次電池よりサイクル特性を向上させることができる電極活物質、及び当該電極活物質を負極に含有する金属二次電池に関する。
【背景技術】
【0002】
二次電池は、化学反応に伴う化学エネルギーの減少分を電気エネルギーに変換し、放電を行うことができる他に、放電時と逆方向に電流を流すことにより、電気エネルギーを化学エネルギーに変換して蓄積(充電)することが可能な電池である。二次電池の中でも、リチウム二次電池に代表される金属二次電池は、エネルギー密度が高いため、ノート型のパーソナルコンピューターや、携帯電話機等の電源として幅広く応用されている。
【0003】
リチウム二次電池においては、負極活物質としてグラファイト(Cと表現する)を用いた場合、放電時において、負極では下記式(I)の反応が進行する。
LixC→C+xLi++xe− (I)
(上記式(I)中、0<x<1である。)
上記式(I)の反応で生じる電子は、外部回路を経由し、外部の負荷で仕事をした後、正極に到達する。そして、上記式(I)の反応で生じたリチウムイオン(Li+)は、負極と正極に挟持された電解質内を、負極側から正極側に電気浸透により移動する。
【0004】
また、正極活物質としてコバルト酸リチウム(Li1−xCoO2)を用いた場合、放電時において、正極では下記式(II)の反応が進行する。
Li1−xCoO2+xLi++xe−→LiCoO2 (II)
(上記式(II)中、0<x<1である。)
充電時においては、負極及び正極において、それぞれ上記式(I)及び式(II)の逆反応が進行し、負極においてはグラファイトインターカレーションによりリチウムが入り込んだグラファイト(LixC)が、正極においてはコバルト酸リチウム(Li1−xCoO2)が再生するため、再放電が可能となる。
【0005】
現在、リチウムイオン二次電池の負極材料には、一般にグラファイトをはじめとする炭素材料が用いられている。しかし、グラファイト系炭素材料には放電容量に理論的な限界があるため、電池の高容量化には不向きである。また、非黒鉛系の炭素材料は、放電容量は大きいものの、不可逆容量が大きく、電池設計の段階で大きなロスを生むという欠点がある。
一方、容量が大きく、炭素材料の代替材料となりうる負極材料も提案されてきた。例えば、Sn等を含む金属酸化物、Co、Mn等を含む金属窒化物を負極材料に応用した例が知られている。特許文献1には、Fe、Ni、Coのうち少なくとも1つの元素とSnを含み、かつ1種以上の化合物の相から構成される、急冷凝固法によって製造された非水系二次電池用負極材料が記載されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2006−236835号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
上記特許文献1に記載された負極材料は、当該文献の段落[0058][表1]からも分かるように、充放電の初期効率が極めて低い。これは、Snを含む合金は、リチウム二次電池に使用された際に、Liの挿入・脱離等の化学反応により結晶構造が大きく変化する結果、反応の可逆性に問題が生じるためと考えられる。
本発明は、上記実状を鑑みて成し遂げられたものであり、金属二次電池に使用された際に、従来の負極活物質を使用した金属二次電池よりサイクル特性を向上させることができる電極活物質、及び当該電極活物質を負極に含有する金属二次電池を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明の電極活物質は、下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【0009】
本発明の金属二次電池は、少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、前記負極が、上記電極活物質を含有することを特徴とする。
【発明の効果】
【0010】
本発明によれば、ハーフホイスラー構造を有することによりリチウムイオンの挿入サイトを確保でき、その結果、本発明に係る電極活物質を金属二次電池に使用した際に、電池のサイクル特性を向上させることができる。
【図面の簡単な説明】
【0011】
【図1】本発明の金属二次電池の一例を示す断面模式図である。
【図2】実施例2及び比較例1のリチウム二次電池の放電曲線である。
【図3】ハーフホイスラー化合物の結晶構造を示した図である。
【発明を実施するための形態】
【0012】
1.電極活物質
本発明の電極活物質は、下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【0013】
図3は、ハーフホイスラー化合物の結晶構造を示した図である。図3から分かるように、ハーフホイスラー化合物の結晶構造は、α原子11、β原子12及びγ原子13からなるC1b構造である。C1b構造の単位格子は、4つの面心立方格子から1つのα原子11を取り除いた構造である。
本発明の電極活物質は、図3に示すようなハーフホイスラー構造を有することにより、主に、図3中の破線の丸で示した空隙14にリチウムイオンの挿入サイトを確保でき、その結果、本発明に係る電極活物質を金属二次電池に使用した際に、電池のサイクル特性を向上させることができる。
【0014】
上記一般式(1)中のαは、第8族〜第12族元素であれば特に限定されないが、Fe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt又はAuであるのが好ましい。このうち、αは、Ni、Fe、Co又はCuであるのがより好ましい。
【0015】
上記一般式(1)中のβは、第3族〜第7族元素であれば特に限定されないが、Ti、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf又はTaであるのが好ましい。このうち、βは、Ti、V、Cr、Mn、Zr又はHfであるのがより好ましい。
【0016】
上記一般式(1)中のγは、第13族〜第15族元素であれば特に限定されないが、半導体元素又は非磁性金属元素であることが好ましく、Al、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd又はBiであることが好ましい。このうち、γは、Al、Ga、Ge、Sn又はSbであるのがより好ましい。
【0017】
上記一般式(1)で表される組成を有するハーフホイスラー化合物としては、具体的には、NiTiSn、NiZrSn、NiHfSn、CoTiSb、CoZrSn又はFeMoSbが挙げられる。
これらのハーフホイスラー化合物の中でも、本発明の電極活物質は、高エネルギー密度を有するという観点から、NiTiSnを含有することが特に好ましい。
【0018】
NiTiSn合金は、公知の方法により製造できる。すなわち、ニッケル(Ni)、チタン(Ti)、及びスズ(Sn)を等モル量用意し、均一に混合した混合物を焼成することにより、NiTiSn合金が得られる。
【0019】
2.金属二次電池
本発明の金属二次電池は、少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、前記負極が、上記電極活物質を含有することを特徴とする。
【0020】
図1は、本発明の金属二次電池の一例を示す断面模式図である。なお、本発明に係る電池は、必ずしもこの例のみに限定されるものではない。
金属二次電池100は、負極缶1の中に、当該缶の底から負極活物質層2、電解質3、正極活物質層4が順に収納され、さらに、電池の蓋として正極缶5がはめ込まれている。負極缶1、負極活物質層2及び電解質3と、正極缶5との間は、ガスケット6によってそれぞれ絶縁されている。図1に示すように、スペーサー7及びスプリング8を更に積層して、負極活物質層2、電解質3及び正極活物質層4に圧力をかけることにより互いに密着させてもよい。図1に示した例においては、負極缶1及び負極活物質層2によって負極が構成され、正極缶5、スプリング8、スペーサー7及び正極活物質層4によって正極が形成されている。なお、負極缶1は、負極集電体としての役割と電池ケースとしての役割を兼ね、正極缶5は、正極集電体としての役割と電池ケースとしての役割を兼ねる。さらに、スペーサー7及びスプリング8は、正極集電体としての役割も果たす。
図1に記載した金属二次電池100中、負極活物質層2は上述した電極活物質を含む。以下、本発明に係る金属二次電池を構成する、正極、負極及び電解質、並びに好適に使用されるセパレータ及び電池ケースについて、詳細に説明する。
【0021】
(正極)
本発明に係る金属二次電池の正極は、好ましくは正極活物質を含有する正極活物質層を有するものであり、通常、これに加えて、正極集電体、及び当該正極集電体に接続された正極リードを有するものである。
【0022】
(正極活物質層)
本発明がリチウム二次電池の場合には、本発明に用いられる正極活物質としては、具体的には、LiCoO2、LiNi1/3Mn1/3Co1/3O2、LiNiPO4、LiMnPO4、LiNiO2、LiMn2O4、LiCoMnO4、Li2NiMn3O8、Li3Fe2(PO4)3及びLi3V2(PO4)3等を挙げることができる。これらの中でも、本発明においては、LiCoO2を正極活物質として用いることが好ましい。
【0023】
本発明に用いられる正極活物質層の厚さは、目的とする金属二次電池の用途等により異なるものであるが、10〜250μmの範囲内であるのが好ましく、20〜200μmの範囲内であるのが特に好ましく、特に30〜150μmの範囲内であることが最も好ましい。
【0024】
正極活物質の平均粒径としては、例えば1〜50μmの範囲内、中でも1〜20μmの範囲内、特に3〜5μmの範囲内であることが好ましい。正極活物質の平均粒径が小さすぎると、取り扱い性が悪くなる可能性があり、正極活物質の平均粒径が大きすぎると、平坦な正極活物質層を得るのが困難になる場合があるからである。なお、正極活物質の平均粒径は、例えば走査型電子顕微鏡(SEM)により観察される活物質担体の粒径を測定して、平均することにより求めることができる。
【0025】
正極活物質層は、必要に応じて導電性材料及び結着剤等を含有していても良い。
本発明において用いられる正極活物質層が含有する導電性材料としては、正極活物質層の導電性を向上させることができれば特に限定されるものではないが、例えばアセチレンブラック、ケッチェンブラック等のカーボンブラック等を挙げることができる。また、正極活物質層における導電性材料の含有割合は、導電性材料の種類によって異なるものであるが、通常1質量%〜10質量%の範囲内である。
【0026】
本発明において用いられる正極活物質層が有する結着剤としては、例えばポリビニリデンフロライド(PVDF)、ポリテトラフルオロエチレン(PTFE)等を挙げることができる。また、正極活物質層における結着剤の含有割合は、正極活物質等を固定化できる程度の量であれば良く、より少ないことが好ましい。結着剤の含有割合は、通常1〜10質量%の範囲内である。
【0027】
(正極集電体)
本発明において用いられる正極集電体は、上記正極活物質層の集電を行う機能を有するものである。上記正極集電体の材料としては、例えばアルミニウム、SUS、ニッケル、鉄及びチタン等を挙げることができ、中でもアルミニウム及びSUSが好ましい。また、正極集電体の形状としては、例えば、箔状、板状、メッシュ状等を挙げることができ、中でも箔状が好ましい。
【0028】
本発明に用いられる正極を製造する方法は、上記正極を得ることができる方法であれば特に限定されるものではない。なお、正極活物質層を形成した後、電極密度を向上させるために、正極活物質層をプレスしても良い。
【0029】
(負極)
本発明に係る金属二次電池中の負極は、上述したハーフホイスラー化合物を負極活物質として含有する。負極は、好ましくは当該ハーフホイスラー化合物を含有する負極活物質層を備え、通常、これに加えて負極集電体、及び当該負極集電体に接続された負極リードを備えるものである。
【0030】
(負極活物質層)
本発明に係る金属二次電池中の負極活物質層は、上述したハーフホイスラー化合物を含有する。当該ハーフホイスラー化合物は、触媒として単独で用いてもよいし、他の触媒と混合して用いてもよい。
負極活物質層に用いられる他の触媒は、金属イオンを吸蔵・放出可能なものであれば特に限定されない。本発明がリチウム二次電池の場合には、本発明に用いられる負極活物質層中の他の触媒としては、例えば、金属リチウム、リチウム元素を含有する合金、リチウム元素を含有する金属酸化物、リチウム元素を含有する金属硫化物、リチウム元素を含有する金属窒化物、及びグラファイト等の炭素材料等を挙げることができる。また、負極活物質は、粉末状であっても良く、薄膜状であっても良い。
リチウム元素を含有する合金としては、例えばリチウムアルミニウム合金、リチウムスズ合金、リチウム鉛合金、リチウムケイ素合金等を挙げることができる。また、リチウム元素を含有する金属酸化物としては、例えばリチウムチタン酸化物等を挙げることができる。また、リチウム元素を含有する金属窒化物としては、例えばリチウムコバルト窒化物、リチウム鉄窒化物、リチウムマンガン窒化物等を挙げることができる。また、負極層には、固体電解質をコートしたリチウムを用いることもできる。
【0031】
また、上記負極活物質層は、負極活物質のみを含有するものであっても良く、負極活物質の他に、導電性材料及び結着剤の少なくとも一方を含有するものであっても良い。例えば、負極活物質が箔状である場合は、負極活物質のみを含有する負極活物質層とすることができる。一方、負極活物質が粉末状である場合は、負極活物質及び結着剤を有する負極層とすることができる。なお、導電性材料及び結着剤については、上述した「正極活物質層」の項に記載した内容と同様であるので、ここでの説明は省略する。
負極活物質層の膜厚としては、特に限定されるものではないが、例えば10〜100μmの範囲内、中でも10〜50μmの範囲内であることが好ましい。
【0032】
上記正極及び上記負極のうち少なくとも一方の電極の電極活物質層が、少なくとも電極活物質及び電極用電解質を含有するという構成をとることもできる。この場合、電極用電解質としては、固体酸化物電解質、固体硫化物電解質等の固体電解質や、後述するポリマー電解質、ゲル電解質等を用いることができる。
【0033】
(負極集電体)
負極集電体の材料及び形状としては、上述した正極集電体の材料及び形状と同様のものを採用することができる。
【0034】
(電解質)
本発明に係る金属二次電池中の電解質は、正極活物質層及び負極活物質層の間に保持され、正極活物質層及び負極活物質層との間で金属イオンを交換する働きを有する。
電解質としては、水系電解質及び非水系電解質を用いることができる。
【0035】
非水系電解質としては、非水系電解液及び非水ゲル電解質を用いることができる。
非水系電解液の種類は、伝導する金属イオンの種類に応じて、適宜選択することが好ましい。例えば、リチウム二次電池の非水系電解液は、通常、リチウム塩及び非水溶媒を含有する。上記リチウム塩としては、例えばLiPF6、LiBF4、LiClO4及びLiAsF6等の無機リチウム塩;LiCF3SO3、LiN(SO2CF3)2(Li−TFSI)、LiN(SO2C2F5)2及びLiC(SO2CF3)3等の有機リチウム塩等を挙げることができる。上記非水溶媒としては、例えばエチレンカーボネート(EC)、プロピレンカーボネート(PC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、エチルカーボネート、ブチレンカーボネート、γ−ブチロラクトン、スルホラン、アセトニトリル(AcN)、ジメトキシメタン、1,2−ジメトキシエタン(DME)、1,3−ジメトキシプロパン、ジエチルエーテル、テトラエチレングリコールジメチルエーテル(TEGDME)、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメチルスルホキシド(DMSO)及びこれらの混合物等を挙げることができる。非水系電解液におけるリチウム塩の濃度は、例えば0.5〜3mol/Lの範囲内である。
なお、本発明においては、非水系電解液又は非水溶媒として、例えば、N−メチル−N−プロピルピペリジニウム ビス(トリフルオロメタンスルホニル)イミド(PP13TFSI)、N−メチル−N−プロピルピロリジニウム ビス(トリフルオロメタンスルホニル)イミド(P13TFSI)、N−ブチル−N−メチルピロリジニウム ビス(トリフルオロメタンスルホニル)イミド(P14TFSI)、N,N−ジエチル−N−メチル−N−(2−メトキシエチル)アンモニウム ビス(トリフルオロメタンスルホニル)イミド(DEMETFSI)、N,N,N−トリメチル−N−プロピルアンモニウム ビス(トリフルオロメタンスルホニル)イミド(TMPATFSI)に代表されるような、イオン性液体等の低揮発性液体を用いても良い。
【0036】
また、本発明に用いられる非水ゲル電解質は、通常、非水系電解液にポリマーを添加してゲル化したものである。例えば、非水ゲル電解質は、上述した非水系電解液に、ポリエチレンオキシド(PEO)、ポリアクリルニトリル(PAN)またはポリメチルメタクリレート(PMMA)等のポリマーを添加し、ゲル化することにより、得ることができる。リチウム二次電池の非水ゲル電解質としては、例えば、LiTFSI(LiN(CF3SO2)2)−PEO系の非水ゲル電解質を用いることができる。
【0037】
水系電解液の種類は、伝導する金属イオンの種類に応じて、適宜選択することが好ましい。例えば、リチウム二次電池の水系電解液としては、通常、水にリチウム塩を含有させたものを用いる。リチウム塩としては、例えばLiOH、LiCl、LiNO3、CH3CO2Li等のリチウム塩等を挙げることができる。
【0038】
上記水系電解質及び非水系電解質中に、さらに固体電解質を混合して用いることができる。固体電解質としては、例えば、Li−La−Ti−O系固体電解質等を用いることができる。
【0039】
(セパレータ)
セパレータを本発明の金属二次電池に用いることができる。セパレータは、上述した正極集電体及び上記負極集電体の間に設けられるものであり、通常、正極活物質層と負極活物質層との接触を防止し、固体電解質を保持する機能を有する。上記セパレータの材料としては、例えばポリエチレン(PE)、ポリプロピレン(PP)、ポリエステル、セルロース及びポリアミド等の樹脂を挙げることができ、中でもポリエチレン及びポリプロピレンが好ましい。また、上記セパレータは、単層構造であっても良く、複層構造であっても良い。複層構造のセパレータとしては、例えばPE/PPの2層構造のセパレータ、PP/PE/PPの3層構造のセパレータ等を挙げることができる。さらに、本発明においては、上記セパレータが、樹脂不織布、ガラス繊維不織布等の不織布等であっても良い。また、上記セパレータの膜厚は、特に限定されるものではなく、一般的な金属二次電池に用いられるセパレータの膜厚と同様である。
セパレータに使用できるこれらの材料は、上述した電解液を含浸させることにより、電解液の支持材として使用することもできる。
【0040】
(電池ケース)
本発明に係る金属二次電池は、通常、正極、電解液及び負極等を収納する電池ケースを有する。電池ケースの形状としては、具体的にはコイン型、平板型、円筒型、ラミネート型等を挙げることができる。
【実施例】
【0041】
以下に、実施例及び比較例を挙げて、本発明をさらに具体的に説明する。なお、本発明は、これらの実施例のみに限定されるものではない。
【0042】
1.電極活物質の調製
[実施例1]
まず、ニッケル(Ni)0.59g、チタン(Ti)0.48g、及びスズ(Sn)1.19gを、乳鉢により均一に混合した。次に、当該混合物を不活性雰囲気下、12時間焼成し、実施例1の電極活物質を得た。
【0043】
2.電極活物質の構造解析
実施例1の電極活物質の化学構造を、粉末X線回折法(XRD)により調べた。測定には、粉末X線回折計(Rint 2200, Rigaku)を用いた。測定条件は、CuKα線を用い、加速電圧は40kVとし、印加電流は40mAとした。
【0044】
XRDによる構造解析の結果、XRDパターン中の2θ=26°、30°、43°、53°、62°、69°、71°、79°、85°付近にそれぞれ回折ピークが確認できた。したがって、実施例1の電極活物質の主成分は、ハーフホイスラー構造を有するNiTiSn合金であることが明らかとなった。しかし、XRD構造解析の結果からは、実施例1の電極活物質中には、不純物として未反応の原料(Sn、Ni及びTi)が体積比で4割程度残ることも分かった。
【0045】
3.リチウム二次電池の作製
リチウムを基準とした電極活物質の電位を測定するために、以下の実施例2及び比較例1のリチウム二次電池を作製した。なお、以下の各二次電池は、リチウム金属を負極活物質として、各電極活物質を正極活物質として用いるものとする。
【0046】
[実施例2]
まず、正極活物質として上記実施例1の電極活物質を、結着剤としてPTFEを、導電性材料としてアセチレンブラック(電気化学工業株式会社製、製品名HS−100)を、それぞれ用意した。正極活物質:結着剤:導電性材料=70質量%:5質量%:25質量%となるように混合し、正極合剤を調製した。
【0047】
次に、正極缶及び負極缶を用意した。負極缶の底にリチウム金属を貼り合わせて、負極を作製した。正極缶の内側に上記正極合剤を塗布し、正極を作製した。
エチレンカーボネート−ジエチレンカーボネート混合溶媒(EC−DEC)に、LiPF6を濃度1Mとなるように溶解させ、電解液とした。当該電解液を、上記正極と負極によって、負極缶−リチウム金属−電解液−正極合剤層−正極缶となるように挟持し、適宜ガスケットを用いて密閉し、実施例2のコイン型リチウム二次電池を作製した。
以上の工程は、全て窒素雰囲気下のグローブボックス内で行った。
【0048】
[比較例1]
正極活物質として、上記実施例1の電極活物質の替わりに、チタン酸リチウム(Li4Ti5O12;石原産業社製)を使用して正極合剤を調製したこと以外は、実施例2と同様に、比較例1のリチウム二次電池を作製した。
【0049】
4.リチウム二次電池の充放電特性の評価
実施例2及び比較例1のリチウム二次電池について、定電流充放電法により、電流0.02mA、充放電範囲0.5〜3.0Vの条件で放電を行った。
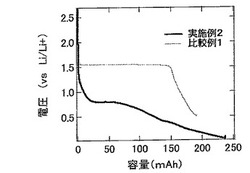
図2は、実施例2及び比較例1のリチウム二次電池の放電曲線である。図2中、太線のグラフは実施例2のデータを、細線のグラフは比較例1のデータを、それぞれ示す。
図2から分かるように、実施例2のグラフは、0.8Vに電圧の平行部(いわゆるプラトー)を有する。一方、比較例1のグラフは、1.5Vにプラトーを有する。すなわち、比較例1のグラフは、実施例2のグラフよりも0.7V高い電位にプラトーを有する。リチウム二次電池の負極材料は、リチウムに対する電位がより低い方が好ましいという観点から、実施例2に使用されたNiTiSn合金は、比較例1に使用されたLi4Ti5O12よりも負極材料として優れていることが分かる。
【0050】
構造解析の説明において述べたように、実施例1の電極活物質には、不純物として原料のSnが含まれる。0.5V以下の容量はSnに寄与するものであると考えられるので、合金を精製し、不純物を取り除いたNiTiSn合金を使用することにより、Li4Ti5O12を用いたリチウム二次電池よりも大きい容量のリチウム二次電池が得られることが示唆される。
【0051】
図2において、実施例2のグラフの0.8V付近のプラトーは、実施例2のリチウム二次電池の正極に使用されたNiTiSn合金が、リチウムイオンを挿入脱離するサイトを備えるハーフホイスラー構造を有することを示す。一般に、Snは電極材料として知られているが、Sn中にリチウムイオンが挿入脱離する反応は知られておらず、Snを電極材料として用いた電池の放電曲線は、このようなプラトーを有することはない。図2より、NiTiSn合金のリチウム挿入電位は1.0Vとなり、リチウム脱離電位は0.5Vとなることが分かる。また、図2より、O.6〜0.9Vの範囲内の容量は、NiTiSn合金に寄与するものであると考えられる。
上述したように、XRD構造解析の結果から、実施例1の電極活物質中には不純物として未反応の原料が残る。本願発明者は、この不純物が放電反応にどの程度寄与しているのかを見積もるために、実施例2のグラフの0.8V付近のプラトーが表す放電容量の変化を調べ、実施例2のリチウム二次電池のサイクル特性を評価した。
【0052】
実施例2のリチウム二次電池について、定電流充放電法により、電流0.02mA、充放電範囲0.5〜3.0Vの条件で放電を行い、実施例2のリチウム二次電池のサイクル特性を評価した。具体的には、実施例2のリチウム二次電池について、1サイクル目、2サイクル目、5サイクル目、10サイクル目及び50サイクル目の放電容量を測定した。
下記表1は、実施例2のリチウム二次電池の、0.8V付近のプラトーが表す、1サイクル目、2サイクル目、5サイクル目、10サイクル目及び50サイクル目の放電容量Cn(mAh/g)と、当該放電容量の維持率(%)をまとめた表である。なお、ここでいう放電容量の維持率とは、0.8V付近のプラトーが表す、1サイクル目の放電容量C1に対する各サイクルの放電容量Cnの割合と、100との積をいう。
【0053】
【表1】

【0054】
表1から分かるように、0.8V付近のプラトーが表す1サイクル目の放電容量は、50サイクル後も90%以上維持されることが分かる。この結果は、従来のSnを含む電極材料を用いた電池に比べて、実施例2のリチウム二次電池は、極めてサイクル特性が高いことを示す。また、実施例1の電極活物質中の不純物は、実施例2のリチウム二次電池のサイクル特性にはほとんど影響を及ぼしていないことも分かる。
各サイクルとも、放電容量Cnは40mAh/g以下であるが、これは実施例1のNiTiSn合金をさらに精製することにより、飛躍的に放電容量の向上が可能であることを示唆するものである。
【符号の説明】
【0055】
1 負極缶
2 負極活物質層
3 電解質
4 正極活物質層
5 正極缶
6 ガスケット
7 スペーサー
8 スプリング
11 α原子
12 β原子
13 γ原子
14 空隙
100 金属二次電池
【技術分野】
【0001】
本発明は、金属二次電池に使用された際に、従来の負極活物質を使用した金属二次電池よりサイクル特性を向上させることができる電極活物質、及び当該電極活物質を負極に含有する金属二次電池に関する。
【背景技術】
【0002】
二次電池は、化学反応に伴う化学エネルギーの減少分を電気エネルギーに変換し、放電を行うことができる他に、放電時と逆方向に電流を流すことにより、電気エネルギーを化学エネルギーに変換して蓄積(充電)することが可能な電池である。二次電池の中でも、リチウム二次電池に代表される金属二次電池は、エネルギー密度が高いため、ノート型のパーソナルコンピューターや、携帯電話機等の電源として幅広く応用されている。
【0003】
リチウム二次電池においては、負極活物質としてグラファイト(Cと表現する)を用いた場合、放電時において、負極では下記式(I)の反応が進行する。
LixC→C+xLi++xe− (I)
(上記式(I)中、0<x<1である。)
上記式(I)の反応で生じる電子は、外部回路を経由し、外部の負荷で仕事をした後、正極に到達する。そして、上記式(I)の反応で生じたリチウムイオン(Li+)は、負極と正極に挟持された電解質内を、負極側から正極側に電気浸透により移動する。
【0004】
また、正極活物質としてコバルト酸リチウム(Li1−xCoO2)を用いた場合、放電時において、正極では下記式(II)の反応が進行する。
Li1−xCoO2+xLi++xe−→LiCoO2 (II)
(上記式(II)中、0<x<1である。)
充電時においては、負極及び正極において、それぞれ上記式(I)及び式(II)の逆反応が進行し、負極においてはグラファイトインターカレーションによりリチウムが入り込んだグラファイト(LixC)が、正極においてはコバルト酸リチウム(Li1−xCoO2)が再生するため、再放電が可能となる。
【0005】
現在、リチウムイオン二次電池の負極材料には、一般にグラファイトをはじめとする炭素材料が用いられている。しかし、グラファイト系炭素材料には放電容量に理論的な限界があるため、電池の高容量化には不向きである。また、非黒鉛系の炭素材料は、放電容量は大きいものの、不可逆容量が大きく、電池設計の段階で大きなロスを生むという欠点がある。
一方、容量が大きく、炭素材料の代替材料となりうる負極材料も提案されてきた。例えば、Sn等を含む金属酸化物、Co、Mn等を含む金属窒化物を負極材料に応用した例が知られている。特許文献1には、Fe、Ni、Coのうち少なくとも1つの元素とSnを含み、かつ1種以上の化合物の相から構成される、急冷凝固法によって製造された非水系二次電池用負極材料が記載されている。
【先行技術文献】
【特許文献】
【0006】
【特許文献1】特開2006−236835号公報
【発明の概要】
【発明が解決しようとする課題】
【0007】
上記特許文献1に記載された負極材料は、当該文献の段落[0058][表1]からも分かるように、充放電の初期効率が極めて低い。これは、Snを含む合金は、リチウム二次電池に使用された際に、Liの挿入・脱離等の化学反応により結晶構造が大きく変化する結果、反応の可逆性に問題が生じるためと考えられる。
本発明は、上記実状を鑑みて成し遂げられたものであり、金属二次電池に使用された際に、従来の負極活物質を使用した金属二次電池よりサイクル特性を向上させることができる電極活物質、及び当該電極活物質を負極に含有する金属二次電池を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明の電極活物質は、下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【0009】
本発明の金属二次電池は、少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、前記負極が、上記電極活物質を含有することを特徴とする。
【発明の効果】
【0010】
本発明によれば、ハーフホイスラー構造を有することによりリチウムイオンの挿入サイトを確保でき、その結果、本発明に係る電極活物質を金属二次電池に使用した際に、電池のサイクル特性を向上させることができる。
【図面の簡単な説明】
【0011】
【図1】本発明の金属二次電池の一例を示す断面模式図である。
【図2】実施例2及び比較例1のリチウム二次電池の放電曲線である。
【図3】ハーフホイスラー化合物の結晶構造を示した図である。
【発明を実施するための形態】
【0012】
1.電極活物質
本発明の電極活物質は、下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【0013】
図3は、ハーフホイスラー化合物の結晶構造を示した図である。図3から分かるように、ハーフホイスラー化合物の結晶構造は、α原子11、β原子12及びγ原子13からなるC1b構造である。C1b構造の単位格子は、4つの面心立方格子から1つのα原子11を取り除いた構造である。
本発明の電極活物質は、図3に示すようなハーフホイスラー構造を有することにより、主に、図3中の破線の丸で示した空隙14にリチウムイオンの挿入サイトを確保でき、その結果、本発明に係る電極活物質を金属二次電池に使用した際に、電池のサイクル特性を向上させることができる。
【0014】
上記一般式(1)中のαは、第8族〜第12族元素であれば特に限定されないが、Fe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt又はAuであるのが好ましい。このうち、αは、Ni、Fe、Co又はCuであるのがより好ましい。
【0015】
上記一般式(1)中のβは、第3族〜第7族元素であれば特に限定されないが、Ti、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf又はTaであるのが好ましい。このうち、βは、Ti、V、Cr、Mn、Zr又はHfであるのがより好ましい。
【0016】
上記一般式(1)中のγは、第13族〜第15族元素であれば特に限定されないが、半導体元素又は非磁性金属元素であることが好ましく、Al、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd又はBiであることが好ましい。このうち、γは、Al、Ga、Ge、Sn又はSbであるのがより好ましい。
【0017】
上記一般式(1)で表される組成を有するハーフホイスラー化合物としては、具体的には、NiTiSn、NiZrSn、NiHfSn、CoTiSb、CoZrSn又はFeMoSbが挙げられる。
これらのハーフホイスラー化合物の中でも、本発明の電極活物質は、高エネルギー密度を有するという観点から、NiTiSnを含有することが特に好ましい。
【0018】
NiTiSn合金は、公知の方法により製造できる。すなわち、ニッケル(Ni)、チタン(Ti)、及びスズ(Sn)を等モル量用意し、均一に混合した混合物を焼成することにより、NiTiSn合金が得られる。
【0019】
2.金属二次電池
本発明の金属二次電池は、少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、前記負極が、上記電極活物質を含有することを特徴とする。
【0020】
図1は、本発明の金属二次電池の一例を示す断面模式図である。なお、本発明に係る電池は、必ずしもこの例のみに限定されるものではない。
金属二次電池100は、負極缶1の中に、当該缶の底から負極活物質層2、電解質3、正極活物質層4が順に収納され、さらに、電池の蓋として正極缶5がはめ込まれている。負極缶1、負極活物質層2及び電解質3と、正極缶5との間は、ガスケット6によってそれぞれ絶縁されている。図1に示すように、スペーサー7及びスプリング8を更に積層して、負極活物質層2、電解質3及び正極活物質層4に圧力をかけることにより互いに密着させてもよい。図1に示した例においては、負極缶1及び負極活物質層2によって負極が構成され、正極缶5、スプリング8、スペーサー7及び正極活物質層4によって正極が形成されている。なお、負極缶1は、負極集電体としての役割と電池ケースとしての役割を兼ね、正極缶5は、正極集電体としての役割と電池ケースとしての役割を兼ねる。さらに、スペーサー7及びスプリング8は、正極集電体としての役割も果たす。
図1に記載した金属二次電池100中、負極活物質層2は上述した電極活物質を含む。以下、本発明に係る金属二次電池を構成する、正極、負極及び電解質、並びに好適に使用されるセパレータ及び電池ケースについて、詳細に説明する。
【0021】
(正極)
本発明に係る金属二次電池の正極は、好ましくは正極活物質を含有する正極活物質層を有するものであり、通常、これに加えて、正極集電体、及び当該正極集電体に接続された正極リードを有するものである。
【0022】
(正極活物質層)
本発明がリチウム二次電池の場合には、本発明に用いられる正極活物質としては、具体的には、LiCoO2、LiNi1/3Mn1/3Co1/3O2、LiNiPO4、LiMnPO4、LiNiO2、LiMn2O4、LiCoMnO4、Li2NiMn3O8、Li3Fe2(PO4)3及びLi3V2(PO4)3等を挙げることができる。これらの中でも、本発明においては、LiCoO2を正極活物質として用いることが好ましい。
【0023】
本発明に用いられる正極活物質層の厚さは、目的とする金属二次電池の用途等により異なるものであるが、10〜250μmの範囲内であるのが好ましく、20〜200μmの範囲内であるのが特に好ましく、特に30〜150μmの範囲内であることが最も好ましい。
【0024】
正極活物質の平均粒径としては、例えば1〜50μmの範囲内、中でも1〜20μmの範囲内、特に3〜5μmの範囲内であることが好ましい。正極活物質の平均粒径が小さすぎると、取り扱い性が悪くなる可能性があり、正極活物質の平均粒径が大きすぎると、平坦な正極活物質層を得るのが困難になる場合があるからである。なお、正極活物質の平均粒径は、例えば走査型電子顕微鏡(SEM)により観察される活物質担体の粒径を測定して、平均することにより求めることができる。
【0025】
正極活物質層は、必要に応じて導電性材料及び結着剤等を含有していても良い。
本発明において用いられる正極活物質層が含有する導電性材料としては、正極活物質層の導電性を向上させることができれば特に限定されるものではないが、例えばアセチレンブラック、ケッチェンブラック等のカーボンブラック等を挙げることができる。また、正極活物質層における導電性材料の含有割合は、導電性材料の種類によって異なるものであるが、通常1質量%〜10質量%の範囲内である。
【0026】
本発明において用いられる正極活物質層が有する結着剤としては、例えばポリビニリデンフロライド(PVDF)、ポリテトラフルオロエチレン(PTFE)等を挙げることができる。また、正極活物質層における結着剤の含有割合は、正極活物質等を固定化できる程度の量であれば良く、より少ないことが好ましい。結着剤の含有割合は、通常1〜10質量%の範囲内である。
【0027】
(正極集電体)
本発明において用いられる正極集電体は、上記正極活物質層の集電を行う機能を有するものである。上記正極集電体の材料としては、例えばアルミニウム、SUS、ニッケル、鉄及びチタン等を挙げることができ、中でもアルミニウム及びSUSが好ましい。また、正極集電体の形状としては、例えば、箔状、板状、メッシュ状等を挙げることができ、中でも箔状が好ましい。
【0028】
本発明に用いられる正極を製造する方法は、上記正極を得ることができる方法であれば特に限定されるものではない。なお、正極活物質層を形成した後、電極密度を向上させるために、正極活物質層をプレスしても良い。
【0029】
(負極)
本発明に係る金属二次電池中の負極は、上述したハーフホイスラー化合物を負極活物質として含有する。負極は、好ましくは当該ハーフホイスラー化合物を含有する負極活物質層を備え、通常、これに加えて負極集電体、及び当該負極集電体に接続された負極リードを備えるものである。
【0030】
(負極活物質層)
本発明に係る金属二次電池中の負極活物質層は、上述したハーフホイスラー化合物を含有する。当該ハーフホイスラー化合物は、触媒として単独で用いてもよいし、他の触媒と混合して用いてもよい。
負極活物質層に用いられる他の触媒は、金属イオンを吸蔵・放出可能なものであれば特に限定されない。本発明がリチウム二次電池の場合には、本発明に用いられる負極活物質層中の他の触媒としては、例えば、金属リチウム、リチウム元素を含有する合金、リチウム元素を含有する金属酸化物、リチウム元素を含有する金属硫化物、リチウム元素を含有する金属窒化物、及びグラファイト等の炭素材料等を挙げることができる。また、負極活物質は、粉末状であっても良く、薄膜状であっても良い。
リチウム元素を含有する合金としては、例えばリチウムアルミニウム合金、リチウムスズ合金、リチウム鉛合金、リチウムケイ素合金等を挙げることができる。また、リチウム元素を含有する金属酸化物としては、例えばリチウムチタン酸化物等を挙げることができる。また、リチウム元素を含有する金属窒化物としては、例えばリチウムコバルト窒化物、リチウム鉄窒化物、リチウムマンガン窒化物等を挙げることができる。また、負極層には、固体電解質をコートしたリチウムを用いることもできる。
【0031】
また、上記負極活物質層は、負極活物質のみを含有するものであっても良く、負極活物質の他に、導電性材料及び結着剤の少なくとも一方を含有するものであっても良い。例えば、負極活物質が箔状である場合は、負極活物質のみを含有する負極活物質層とすることができる。一方、負極活物質が粉末状である場合は、負極活物質及び結着剤を有する負極層とすることができる。なお、導電性材料及び結着剤については、上述した「正極活物質層」の項に記載した内容と同様であるので、ここでの説明は省略する。
負極活物質層の膜厚としては、特に限定されるものではないが、例えば10〜100μmの範囲内、中でも10〜50μmの範囲内であることが好ましい。
【0032】
上記正極及び上記負極のうち少なくとも一方の電極の電極活物質層が、少なくとも電極活物質及び電極用電解質を含有するという構成をとることもできる。この場合、電極用電解質としては、固体酸化物電解質、固体硫化物電解質等の固体電解質や、後述するポリマー電解質、ゲル電解質等を用いることができる。
【0033】
(負極集電体)
負極集電体の材料及び形状としては、上述した正極集電体の材料及び形状と同様のものを採用することができる。
【0034】
(電解質)
本発明に係る金属二次電池中の電解質は、正極活物質層及び負極活物質層の間に保持され、正極活物質層及び負極活物質層との間で金属イオンを交換する働きを有する。
電解質としては、水系電解質及び非水系電解質を用いることができる。
【0035】
非水系電解質としては、非水系電解液及び非水ゲル電解質を用いることができる。
非水系電解液の種類は、伝導する金属イオンの種類に応じて、適宜選択することが好ましい。例えば、リチウム二次電池の非水系電解液は、通常、リチウム塩及び非水溶媒を含有する。上記リチウム塩としては、例えばLiPF6、LiBF4、LiClO4及びLiAsF6等の無機リチウム塩;LiCF3SO3、LiN(SO2CF3)2(Li−TFSI)、LiN(SO2C2F5)2及びLiC(SO2CF3)3等の有機リチウム塩等を挙げることができる。上記非水溶媒としては、例えばエチレンカーボネート(EC)、プロピレンカーボネート(PC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、エチルカーボネート、ブチレンカーボネート、γ−ブチロラクトン、スルホラン、アセトニトリル(AcN)、ジメトキシメタン、1,2−ジメトキシエタン(DME)、1,3−ジメトキシプロパン、ジエチルエーテル、テトラエチレングリコールジメチルエーテル(TEGDME)、テトラヒドロフラン、2−メチルテトラヒドロフラン、ジメチルスルホキシド(DMSO)及びこれらの混合物等を挙げることができる。非水系電解液におけるリチウム塩の濃度は、例えば0.5〜3mol/Lの範囲内である。
なお、本発明においては、非水系電解液又は非水溶媒として、例えば、N−メチル−N−プロピルピペリジニウム ビス(トリフルオロメタンスルホニル)イミド(PP13TFSI)、N−メチル−N−プロピルピロリジニウム ビス(トリフルオロメタンスルホニル)イミド(P13TFSI)、N−ブチル−N−メチルピロリジニウム ビス(トリフルオロメタンスルホニル)イミド(P14TFSI)、N,N−ジエチル−N−メチル−N−(2−メトキシエチル)アンモニウム ビス(トリフルオロメタンスルホニル)イミド(DEMETFSI)、N,N,N−トリメチル−N−プロピルアンモニウム ビス(トリフルオロメタンスルホニル)イミド(TMPATFSI)に代表されるような、イオン性液体等の低揮発性液体を用いても良い。
【0036】
また、本発明に用いられる非水ゲル電解質は、通常、非水系電解液にポリマーを添加してゲル化したものである。例えば、非水ゲル電解質は、上述した非水系電解液に、ポリエチレンオキシド(PEO)、ポリアクリルニトリル(PAN)またはポリメチルメタクリレート(PMMA)等のポリマーを添加し、ゲル化することにより、得ることができる。リチウム二次電池の非水ゲル電解質としては、例えば、LiTFSI(LiN(CF3SO2)2)−PEO系の非水ゲル電解質を用いることができる。
【0037】
水系電解液の種類は、伝導する金属イオンの種類に応じて、適宜選択することが好ましい。例えば、リチウム二次電池の水系電解液としては、通常、水にリチウム塩を含有させたものを用いる。リチウム塩としては、例えばLiOH、LiCl、LiNO3、CH3CO2Li等のリチウム塩等を挙げることができる。
【0038】
上記水系電解質及び非水系電解質中に、さらに固体電解質を混合して用いることができる。固体電解質としては、例えば、Li−La−Ti−O系固体電解質等を用いることができる。
【0039】
(セパレータ)
セパレータを本発明の金属二次電池に用いることができる。セパレータは、上述した正極集電体及び上記負極集電体の間に設けられるものであり、通常、正極活物質層と負極活物質層との接触を防止し、固体電解質を保持する機能を有する。上記セパレータの材料としては、例えばポリエチレン(PE)、ポリプロピレン(PP)、ポリエステル、セルロース及びポリアミド等の樹脂を挙げることができ、中でもポリエチレン及びポリプロピレンが好ましい。また、上記セパレータは、単層構造であっても良く、複層構造であっても良い。複層構造のセパレータとしては、例えばPE/PPの2層構造のセパレータ、PP/PE/PPの3層構造のセパレータ等を挙げることができる。さらに、本発明においては、上記セパレータが、樹脂不織布、ガラス繊維不織布等の不織布等であっても良い。また、上記セパレータの膜厚は、特に限定されるものではなく、一般的な金属二次電池に用いられるセパレータの膜厚と同様である。
セパレータに使用できるこれらの材料は、上述した電解液を含浸させることにより、電解液の支持材として使用することもできる。
【0040】
(電池ケース)
本発明に係る金属二次電池は、通常、正極、電解液及び負極等を収納する電池ケースを有する。電池ケースの形状としては、具体的にはコイン型、平板型、円筒型、ラミネート型等を挙げることができる。
【実施例】
【0041】
以下に、実施例及び比較例を挙げて、本発明をさらに具体的に説明する。なお、本発明は、これらの実施例のみに限定されるものではない。
【0042】
1.電極活物質の調製
[実施例1]
まず、ニッケル(Ni)0.59g、チタン(Ti)0.48g、及びスズ(Sn)1.19gを、乳鉢により均一に混合した。次に、当該混合物を不活性雰囲気下、12時間焼成し、実施例1の電極活物質を得た。
【0043】
2.電極活物質の構造解析
実施例1の電極活物質の化学構造を、粉末X線回折法(XRD)により調べた。測定には、粉末X線回折計(Rint 2200, Rigaku)を用いた。測定条件は、CuKα線を用い、加速電圧は40kVとし、印加電流は40mAとした。
【0044】
XRDによる構造解析の結果、XRDパターン中の2θ=26°、30°、43°、53°、62°、69°、71°、79°、85°付近にそれぞれ回折ピークが確認できた。したがって、実施例1の電極活物質の主成分は、ハーフホイスラー構造を有するNiTiSn合金であることが明らかとなった。しかし、XRD構造解析の結果からは、実施例1の電極活物質中には、不純物として未反応の原料(Sn、Ni及びTi)が体積比で4割程度残ることも分かった。
【0045】
3.リチウム二次電池の作製
リチウムを基準とした電極活物質の電位を測定するために、以下の実施例2及び比較例1のリチウム二次電池を作製した。なお、以下の各二次電池は、リチウム金属を負極活物質として、各電極活物質を正極活物質として用いるものとする。
【0046】
[実施例2]
まず、正極活物質として上記実施例1の電極活物質を、結着剤としてPTFEを、導電性材料としてアセチレンブラック(電気化学工業株式会社製、製品名HS−100)を、それぞれ用意した。正極活物質:結着剤:導電性材料=70質量%:5質量%:25質量%となるように混合し、正極合剤を調製した。
【0047】
次に、正極缶及び負極缶を用意した。負極缶の底にリチウム金属を貼り合わせて、負極を作製した。正極缶の内側に上記正極合剤を塗布し、正極を作製した。
エチレンカーボネート−ジエチレンカーボネート混合溶媒(EC−DEC)に、LiPF6を濃度1Mとなるように溶解させ、電解液とした。当該電解液を、上記正極と負極によって、負極缶−リチウム金属−電解液−正極合剤層−正極缶となるように挟持し、適宜ガスケットを用いて密閉し、実施例2のコイン型リチウム二次電池を作製した。
以上の工程は、全て窒素雰囲気下のグローブボックス内で行った。
【0048】
[比較例1]
正極活物質として、上記実施例1の電極活物質の替わりに、チタン酸リチウム(Li4Ti5O12;石原産業社製)を使用して正極合剤を調製したこと以外は、実施例2と同様に、比較例1のリチウム二次電池を作製した。
【0049】
4.リチウム二次電池の充放電特性の評価
実施例2及び比較例1のリチウム二次電池について、定電流充放電法により、電流0.02mA、充放電範囲0.5〜3.0Vの条件で放電を行った。
図2は、実施例2及び比較例1のリチウム二次電池の放電曲線である。図2中、太線のグラフは実施例2のデータを、細線のグラフは比較例1のデータを、それぞれ示す。
図2から分かるように、実施例2のグラフは、0.8Vに電圧の平行部(いわゆるプラトー)を有する。一方、比較例1のグラフは、1.5Vにプラトーを有する。すなわち、比較例1のグラフは、実施例2のグラフよりも0.7V高い電位にプラトーを有する。リチウム二次電池の負極材料は、リチウムに対する電位がより低い方が好ましいという観点から、実施例2に使用されたNiTiSn合金は、比較例1に使用されたLi4Ti5O12よりも負極材料として優れていることが分かる。
【0050】
構造解析の説明において述べたように、実施例1の電極活物質には、不純物として原料のSnが含まれる。0.5V以下の容量はSnに寄与するものであると考えられるので、合金を精製し、不純物を取り除いたNiTiSn合金を使用することにより、Li4Ti5O12を用いたリチウム二次電池よりも大きい容量のリチウム二次電池が得られることが示唆される。
【0051】
図2において、実施例2のグラフの0.8V付近のプラトーは、実施例2のリチウム二次電池の正極に使用されたNiTiSn合金が、リチウムイオンを挿入脱離するサイトを備えるハーフホイスラー構造を有することを示す。一般に、Snは電極材料として知られているが、Sn中にリチウムイオンが挿入脱離する反応は知られておらず、Snを電極材料として用いた電池の放電曲線は、このようなプラトーを有することはない。図2より、NiTiSn合金のリチウム挿入電位は1.0Vとなり、リチウム脱離電位は0.5Vとなることが分かる。また、図2より、O.6〜0.9Vの範囲内の容量は、NiTiSn合金に寄与するものであると考えられる。
上述したように、XRD構造解析の結果から、実施例1の電極活物質中には不純物として未反応の原料が残る。本願発明者は、この不純物が放電反応にどの程度寄与しているのかを見積もるために、実施例2のグラフの0.8V付近のプラトーが表す放電容量の変化を調べ、実施例2のリチウム二次電池のサイクル特性を評価した。
【0052】
実施例2のリチウム二次電池について、定電流充放電法により、電流0.02mA、充放電範囲0.5〜3.0Vの条件で放電を行い、実施例2のリチウム二次電池のサイクル特性を評価した。具体的には、実施例2のリチウム二次電池について、1サイクル目、2サイクル目、5サイクル目、10サイクル目及び50サイクル目の放電容量を測定した。
下記表1は、実施例2のリチウム二次電池の、0.8V付近のプラトーが表す、1サイクル目、2サイクル目、5サイクル目、10サイクル目及び50サイクル目の放電容量Cn(mAh/g)と、当該放電容量の維持率(%)をまとめた表である。なお、ここでいう放電容量の維持率とは、0.8V付近のプラトーが表す、1サイクル目の放電容量C1に対する各サイクルの放電容量Cnの割合と、100との積をいう。
【0053】
【表1】

【0054】
表1から分かるように、0.8V付近のプラトーが表す1サイクル目の放電容量は、50サイクル後も90%以上維持されることが分かる。この結果は、従来のSnを含む電極材料を用いた電池に比べて、実施例2のリチウム二次電池は、極めてサイクル特性が高いことを示す。また、実施例1の電極活物質中の不純物は、実施例2のリチウム二次電池のサイクル特性にはほとんど影響を及ぼしていないことも分かる。
各サイクルとも、放電容量Cnは40mAh/g以下であるが、これは実施例1のNiTiSn合金をさらに精製することにより、飛躍的に放電容量の向上が可能であることを示唆するものである。
【符号の説明】
【0055】
1 負極缶
2 負極活物質層
3 電解質
4 正極活物質層
5 正極缶
6 ガスケット
7 スペーサー
8 スプリング
11 α原子
12 β原子
13 γ原子
14 空隙
100 金属二次電池
【特許請求の範囲】
【請求項1】
下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする、電極活物質。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【請求項2】
少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、
前記負極が、前記請求項1に記載の電極活物質を含有することを特徴とする、金属二次電池。
【請求項1】
下記一般式(1)で表される組成を有するハーフホイスラー化合物を含有することを特徴とする、電極活物質。
αβγ 一般式(1)
(ただし、上記一般式(1)中、αはFe、Co、Ni、Cu、Zn、Ru、Rh、Pd、Ag、Cd、Ir、Pt及びAuからなる群から選ばれる元素であり、βはTi、V、Cr、Mn、Y、Zr、Nb、Gd、Tb、Dy、Ho、Er、Tm、Yb、Lu、Hf及びTaからなる群から選ばれる元素であり、γはAl、Si、Ga、Ge、As、In、Sn、Sb、Tl、Pd及びBiからなる群から選ばれる元素である。)
【請求項2】
少なくとも正極と、負極と、当該正極と当該負極との間に介在する電解質とを備える金属二次電池であって、
前記負極が、前記請求項1に記載の電極活物質を含有することを特徴とする、金属二次電池。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2012−174535(P2012−174535A)
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願番号】特願2011−36170(P2011−36170)
【出願日】平成23年2月22日(2011.2.22)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【Fターム(参考)】
【公開日】平成24年9月10日(2012.9.10)
【国際特許分類】
【出願日】平成23年2月22日(2011.2.22)
【出願人】(000003207)トヨタ自動車株式会社 (59,920)
【Fターム(参考)】
[ Back to top ]

