電極活物質材料およびその製造方法
【課題】レート特性が向上し、大電流による充放電を可能とする電極活物質材料およびその製造方法を提供する。
【解決手段】リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、前記一次粒子は単結晶であり、前記二次粒子中の前記一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴とする。
【解決手段】リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、前記一次粒子は単結晶であり、前記二次粒子中の前記一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、リチウムイオン二次電池に係り、特に、リチウムイオン二次電池の充放電レート特性を向上させる技術に関する。
【背景技術】
【0002】
車載用のリチウムイオン二次電池においては、それぞれ正極、負極および電解液を有する単電池(セル)が複数個直列に配置されて組電池を形成し、充放電制御のためのセルコントローラが接続され、必要な電圧が得られるようにバッテリーモジュールを形成する。
【0003】
このような二次電池の単電池には、電極シートとセパレータを重ね、扁平型や円筒型に巻回した後に潰した巻回型蓄電素子、あるいは、平板状に切り出した電極とセパレータを積層した積層型蓄電素子の2種類があり、これらを、円筒型のケースに収納したものや、角型、扁平型のケースに収納したものが知られている。
【0004】
単電池の構成要素のうち、正極または負極の電極シートは、薄い金属箔である集電箔の表面に、電極活物質粒子、バインダー、溶媒等を含む電極活物質のペーストが塗布および乾燥されてなる。
【0005】
単電池の充放電に際しては、リチウムイオンが電解液と電極活物質粒子との間を拡散して出入りする。そのため、従来、大電流にて充放電を行うと、リチウムイオンの出入りが円滑に行われず、レート特性(高レート充放電においても容量が維持される性能)が低下する原因となっていた。このレート特性を維持しながら大電流にて充放電を行なうためには、リチウムイオンの電極活物質粒子と電解液との間の出入りを迅速かつ円滑にする必要がある。
【0006】
しかしながら、従来、電極活物質粒子を構成する結晶は、結晶格子がランダムに配向した非晶質または多結晶質であるため、リチウムイオンの拡散のための移動経路が複雑となり、結果として、一定レベル以上の高レートの充放電は困難であった。
【0007】
このような問題を解決するため、リチウムイオン電池において、正極の電極活物質を単結晶の二酸化マンガンとして、さらに、電解液と電極活物質との間のリチウムイオンの拡散移動経路が最短となるように、すなわち、正極集電体に対して垂直となるように、この単結晶を配向させた正極構造が知られている(例えば、特許文献1参照)。
【0008】
しかしながら、特許文献1に記載の技術では、集電体上に単結晶を電気化学的に成長させる必要があるため、活物質の種類が限られるという問題や、結晶成長に著しく時間が掛かり単結晶の厚さを厚く形成することが困難であるという問題や、導電材およびバインダーの配合が制限されるという問題等がある。そのため、実現可能な寸法や仕様が限定され、実用化にはコストが高い。したがって、自動車用途に要求されるような、高レート特性を維持しつつ大電流による充放電を行う電池にこの技術を適用することは困難である。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2007−005281号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、以上述べた従来技術の課題を解決するためになされたもので、レート特性が向上し、大電流による充放電を可能とする電極活物質材料およびその製造方法を提供することを目的としている。
【課題を解決するための手段】
【0011】
本発明の電極活物質は、リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、一次粒子は単結晶であり、二次粒子中の一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴としている。
【0012】
上記構成の本発明にあっては、電極活物質を構成する二次粒子中の一次粒子が、リチウムイオン拡散方向が同一になるように配向しているので、充放電時におけるリチウムイオンの電解液と電極活物質との間の拡散移動経路が短縮される。これにより、リチウムイオンの迅速な挿入離脱が可能となり、電極表面での電気化学反応速度が向上することで、レート特性や出力密度が向上する。これにより、急速な充放電や大電流の充放電にも対応可能な電池を構成することができる。
【0013】
本発明においては、一次粒子は、長尺面と、それよりも短い短尺面を有し、長尺面は、リチウムイオン拡散方向と交差しており、短尺面は、リチウムイオン拡散方向と平行であることを好ましい態様としている。
【0014】
上記構成の本発明にあっては、長尺面がリチウムイオン拡散方向と交差し、短尺面がリチウムイオン拡散方向と平行である。すなわち、リチウムイオンの挿入離脱が起こる出入り口の面が長尺面となっていて相対的に広いので、よりスムーズにリチウムイオンが出入りし、電気化学反応速度が向上する。また、リチウムイオンの拡散移動が起こる方向に平行な面が短尺面となっているので、リチウムイオンの移動距離が相対的に短くなり、同様に、よりスムーズにリチウムイオンが出入りし、電気化学反応速度が向上する。
【0015】
本発明の電極活物質材料の製造方法は、リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質からなる単結晶の一次粒子を生成する工程と、一次粒子を金属アルコキシドにて被覆する工程と、被覆された一次粒子を凝集させ二次粒子を生成する工程とからなることを特徴としている。
【0016】
上記構成の本発明にあっては、電極活物質の単結晶である一次粒子の表面に多数のアルコキシ基が形成され、隣接する一次粒子表面のアルコキシ基が凝集し、脱水縮合してエーテル基を形成することにより隣接する一次粒子どうしが結合されて二次粒子が形成されるが、この際、短尺面に比較して長尺面の方がより多くのアルコキシ基を有するため、隣接する一次粒子の長尺面どうしがより選択的に凝集することになる。これにより、本発明のリチウムイオンの拡散方向が揃った二次粒子を成長させることができる。
【図面の簡単な説明】
【0017】
【図1】本発明の電極活物質を用いた正極構造を模式的に示す断面図である。
【図2】本発明の電極活物質二次粒子の拡大図である。
【図3】本発明の第1実施形態における電極活物質一次粒子の結晶構造を示す模式図である。
【図4】本発明の第2実施形態における電極活物質一次粒子の結晶構造を示す模式図である。
【図5】本発明の第1実施形態における層状化合物の結晶構造を示す模式図である。
【図6】本発明の第2実施形態におけるオリビン化合物の結晶構造を示す模式図である。
【図7】本発明の実施例および比較例(層状化合物)のX線回折分析結果を示すチャートである。
【図8】本発明の実施例および比較例(オリビン化合物)のX線回折分析結果を示すチャートである。
【発明を実施するための形態】
【0018】
以下、図面を参照して本発明の実施の形態を説明する。
図1は、本発明の実施形態に係るリチウムイオン電池における正極を模式的に示した断面図である。正極Eは、例えばアルミニウム等の金属箔の集電体1上に、電極活物質二次粒子2および導電材粒子3が、バインダー4により結着されて構成されている。電極Eは、例えば、電極活物質二次粒子2、導電材3およびバインダー4を溶媒と共に混練してペースト状としたものを集電体1上に塗布する公知の方法によって製造することができる。
【0019】
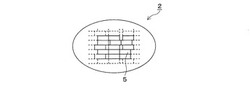
図2は、電極活物質二次粒子2の拡大図である。電極活物質二次粒子2は、多数の電極活物質一次粒子5が凝集して構成されている。本発明においては、図2に示すように、電極活物質一次粒子5は、長尺面と短尺面を有し、一次粒子5は、長尺面間で凝集して二次粒子を構成していると好ましく、また、長尺と短尺の比L/Dは、1.1以上になると好ましい。1.1未満であると長尺面と短尺面がほぼ同じとなってしまい、特に1未満であると、長尺面と短尺面が逆転してしまい好ましくない。また、一次粒子の粒径は、0.05〜100μm、特に0.1〜20μmの範囲が好ましい。
【0020】
第1実施形態(層状化合物)
図3は、電極活物質一次粒子5が、リチウムの層状化合物で構成されている本発明の第1実施形態を示し、図5は、層状化合物の結晶構造を説明する図である。本発明のリチウムの層状化合物は、一般式LixMO2±y(0.8≦x≦2.5、yはxに依存して変化)を取る複合酸化物であり、ここで、Mは、Al,Mg,V,Ti,Ni,Co,Mn,Fe,Cuのうち少なくとも一つを含む遷移金属である。
【0021】
図5に示すように、層状化合物の結晶は、遷移金属Mの酸化物層とリチウム層が交互に配列された構造を取る。そして、遷移金属Mの酸化物層とリチウム層の延在方向は、結晶格子の003面(00N面、N:整数、以下同じ)に一致し、110面(NN0面)に垂直に交わる。そのため、充放電に伴う電気化学反応に際しては、リチウムイオンは、003面に平行な方向に沿って拡散移動が行なわれる。
【0022】
したがって、本発明では、図3に示すように、電極活物質一次粒子5の長尺面Lが層状化合物の110面(NN0面)に一致し、かつ短尺面Dが003面(00N面)に一致するように一次粒子を構成し、かつ、一次粒子5を、それぞれの粒子におけるリチウムイオン拡散方向が一致するように、長尺面同士を結合させて二次粒子2を構成している。
【0023】
このように、本発明では、長尺面Lをリチウムイオンの出入り口とすることによってリチウムイオンの電極活物質内への挿入離脱をスムーズにすると共に、二次粒子2中の各一次粒子5のリチウムイオン拡散移動経路の方向を揃えることによって電気化学反応に際してのリチウムイオンの拡散移動経路に屈曲を無くし、最短距離とすることができる。
【0024】
第2実施形態(オリビン化合物)
図4は、電極活物質一次粒子5が、リチウムのオリビン化合物で構成されている本発明の第2実施形態を示し、図6は、オリビン化合物の結晶構造を説明する図である。本発明のリチウムのオリビン化合物は、一般式LiMPO4を取る複合酸化物であり、ここで、Mは、Al,Mg,V,Ti,Ni,Co,Mn,Fe,Cuのうち少なくとも一つを含む遷移金属である。
【0025】
図6に示すように、オリビン化合物の結晶は、MPO4の結晶構造の間にLiが層状に存在し、このLiの存在する層が200面(N00面)に一致した構造を取る。そして、リチウム層の延在方向は、結晶の020面(0N0面)に垂直に交わる。そのため、充放電に伴う電気化学反応に際しては、リチウムイオンは、200面に平行な方向に沿って拡散移動が行なわれる。
【0026】
したがって、本発明では、図4に示すように、電極活物質一次粒子5の長尺面Lが層状化合物の020面(0N0面)に一致し、かつ短尺面Dが200面(N00面)に一致するように一次粒子を構成し、かつ、一次粒子5を、それぞれの粒子におけるリチウムイオン拡散方向が一致するように長尺面同士を結合させて二次粒子2を構成している。
【0027】
このように、本発明では、長尺面Lをリチウムイオンの出入り口とすることによってリチウムイオンの電極活物質内への挿入離脱をスムーズにすると共に、二次粒子2中の各一次粒子5のリチウムイオン拡散移動経路の方向を揃えることによって電気化学反応に際してのリチウムイオンの拡散移動経路に屈曲を無くし、最短距離とすることができる。
【0028】
本発明の一次粒子および二次粒子の製造方法1:ゾルゲル法
上述した本発明における個々の一次粒子が特定の結晶面を揃えて整列した二次粒子は、下記の方法で作製することができる。
【0029】
<プロセス1:溶融塩中での結晶育成>
坩堝内に遷移金属酸化物を投入し、fluxかつLi源となるLi2OとLiClをそれぞれ投入する。大気雰囲気下、電気炉等を用いて300〜1000℃で焼成し、fluxを熔融させることで遷移金属酸化物のLi化および結晶育成を行う。これにより、電極活物質一次粒子の単結晶を成長させることができる。反応後、反応系を室温まで冷却を行う。結晶育成時間は、目的の単結晶の寸法に応じて任意に設定することができる。
【0030】
<プロセス2:過剰のflux除去>
次に、生成した結晶を蒸留水にて水洗し、上記工程で反応せずに残った過剰のfluxを除去する。用いるfluxの種類や量、結晶育成条件、坩堝に投入する遷移金属酸化物の粒子径を変化させることで、生成する一次粒子の大きさを0.05μm〜100μmの範囲で任意に制御することができる。flux水洗回数、時間は任意である。また、水洗温度も特に規定されないが温水を用いるとfluxの溶解度が増加するので効率的に除去できる。具体的には10〜90℃の範囲の水が使用可能である。
【0031】
<プロセス3:有機コート>
任意の複合酸化物を含む金属アルコキシドを用意しゾルゲル法を施す。複合酸化物がLiAlO2の場合、Li−OR、Al−ORを用いる。RO−は、エトキシ基であることが好ましい。これらダブルアルコキシド溶液をエタノールなどの溶媒にて準備する。撹拌しながらH2Oを滴定し、ゲル化を促進させた状態の溶液をスプレードライにて電極活物質一次粒子に噴霧塗布する。
【0032】
<プロセス4:二次粒子の形成>
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定していくと一次粒子の凝集体が形成される。これは活物質表面に結合している有機物同士がアルコキシド中の金属を介して活物質を長尺を含む面同士で結合していくことで配向した凝集が行なわれているのである。所望のサイズに凝集して成長したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスをかける。LiAlO2の場合、1トン/cm2の圧力を30秒保持する。これにより凝集体のアルコキシド金属を含む有機分が凝集体表面に押し出されながら更に凝集していく。最後にこれらの凝集体を焼結することで所望の二次粒子を得る。LiAlO2の場合、500度にて30分保持する。
【0033】
本発明の一次粒子および二次粒子の製造方法2:沈殿法
<プロセス1:遷移金属炭酸塩の沈殿>
遷移金属硝酸塩を蒸留水に溶解させる。その水溶液に炭酸ナトリウム水溶液と水酸化アンモニウム水溶液を滴下する。溶液が塩基性を帯びると遷移金属が炭酸塩として沈殿し、その沈殿物は微細な一次粒子から構成された球状の二次粒子となっている。遷移金属塩の種類は特に限定されず、硫酸塩や酢酸塩を用いても良いが、後の水洗・焼成工程で容易に除去できる硝酸塩が望ましい。
【0034】
<プロセス2:水洗>
生成した遷移金属炭酸塩の沈殿物を蒸留水にて水洗する。この工程で不純物として存在するNaイオンや硝酸イオンを除去する。水洗回数、時間は任意である。また、水洗温度も特に規定されないが温水を用いると効率的に不純物を除去できる。
【0035】
<プロセス3:沈殿物のLi化と一次粒子の結晶面整列化>
遷移金属炭酸塩の沈殿物を坩堝に投入し、fluxかつLi源となるLi2OとLiClをそれぞれ投入する。大気雰囲気下、電気炉等を用いて焼成し、fluxを熔融させることで炭酸塩のLi化と一次粒子結晶の整列化を行う。室温まで冷却する。
【0036】
焼成時に炭酸塩は脱炭酸するとともに、Liと反応し、Li含有遷移金属酸化物へと変化する。また多結晶体からなる個々の一次粒子は溶融塩中で一次粒子が単結晶化し、冷却過程で特定の結晶面が揃った二次粒子となる。用いるfluxの種類や量、結晶育成条件を変化させることで、揃う結晶面を制御できる。また、一次粒子の結晶面を揃える為に必要な冷却過程の時間は特に限定されないが、最高到達温度から室温までなるべく時間をかけて冷却することが望ましい。
【0037】
以下、本発明の各構成要素について詳細に説明する。
正極シート
リチウムイオン二次電池を構成する正極シートは、アルミニウムからなる正極集電体の両面に正極材料が結着した構造を有する。本発明の正極材料としては、本発明の電極活物質二次粒子を用い、導電フィラーとして、アセチレンブラック、ケッチエンブラック、VGCF等が挙げられる。正極および負極の導電フィラーは、同一でも、異なっていても良い。
【0038】
正極シートの結着材としては、電池内で化学的に安定なものであれば、熱可塑性樹脂、熱硬化性樹脂のいずれも使用できる。例えば、ポリエチレン、ポリプロピレン、ポリテトラフルオロエチレン(PTFE)、ポリフッ化ビニリデン(PVDF)、スチレンブタジエンゴムなどが挙げられ、これらを単独または複数混合して用いることができる。これらの中でも特に少量で結着力を発揮できるPVDFとPTFEが好ましい。
【0039】
負極シート
蓄電素子を構成する負極シートは、銅などからなる負極集電体の両面に負極材料が結着した構造を有する。本実施例の負極材料としては、リチウムイオンを吸蔵放出する炭素材料やSn、Si、Pb、Coを含む合金や酸化物を用いることができる。炭素材料としては、天然黒鉛、人造黒鉛、活性炭、600〜1200℃で焼成した低温炭素体(例えば、易黒鉛性炭素前駆体として、ピッチ、メソフェーズピッチ、または難黒鉛化性炭素前駆体として、フェノール樹脂、キシレン樹脂、PPS、セルロース等)を不活性雰囲気中で熱処理して合成した炭素などが挙げられる。中心部の素子と外周部の素子の電極活物質は、同一でも、異なっても良い。例えば、中心部の素子は、温度が高くなるので劣化が起こりやすいので、劣化タフネスが高く、膨張の小さい、ハードカーボンを中心部の負極に用い、外側の電極はソフトカーボン、黒鉛材料を用いることもできる。
【0040】
負極シートの結着材としては、前述の正極で用いた結着材と同様のものが使用でき、その中でも特にスチレンブタジエンゴム、ポリフッ化ビニリデンなどが好ましい。
【0041】
セパレータシート
蓄電素子を構成するセパレータシートは、ポリオレフィン系微多孔質セパレータ、例えば、ポリエチレン、ポリプロピレンや不織布セパレータ、例えば、ポリエステル繊維、アラミド繊維を用いることができる。
【0042】
電解液
溶媒としては、例えばエチレンカーボネート(EC)、プロピレンカーボネート(PC)、ブチレンカーボネート(BC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、γ−ブチロラクトン(γ−BL)、スルホラン、アセトニトリル、1,2−ジメトキシエタン、1,3−ジメトキシプロパン、ジメチルエーテル、テトラヒドロフラン(THF)、2−メチルテトラヒドロフラン等を挙げることができる。溶媒は、単独で使用しても、2種以上混合して使用しても良い。電解質としては、例えば過塩素酸リチウム(LiClO4)、六フッ化リン酸リチウム(LiPF6)、四フッ化ホウ素リチウム(LiBF4)、六フッ化砒素リチウム(LiAsF6)、トリフルオロメタンスルホン酸リチウム(LiCF3SO3)、ビストリフルオロメチルスルホニルイミドリチウム[LiN(CF3SO3)2]等のリチウム塩を挙げることができる。電解質は、単独で使用しても、2種以上混合して使用しても良い。電解質の溶媒に対する溶解量は、通常は0.2mol/L〜2mol/L程度である。種々のイオン性液体を混合してもよい。加えて、電解液の保持する、ゲル電解質としてもよくその保持材料としては、ポリエチレンオキサイド、ポリプロピレンオキサイド、ビニリデンフロライド(VdF)やヘキサフルオロプロピレン(HFP)またはその誘導体、または共重合体を用いることができる。
【0043】
電極端子
正極端子および負極端子の電極端子には、銅、ニッケル、アルミニウム、ステンレスといった金属またはこれらを含む合金やこれら金属を母材にしてニッケルメッキを施したものが使用可能である。集電箔と端子部分の接合面積を稼ぐためには、板状であることが好ましい。
【0044】
リード板
正極及び負極リード板には、銅、ニッケル、アルミニウム、ステンレスといった金属またはこれらを含む合金やこれら金属を母材にしてニッケルメッキを施したものが使用可能である。
【0045】
電池ケース
底面部の形状を加工するには、アルミ、ステンレス合金、樹脂を用いることができるが、インパクト成型、トランスファープレス加工によって作製したアルミニウム合金が好ましい。ケースは、蓄電素子と密着する構造が好ましく、これによりケースと蓄電素子との間の空間が少なくなり、電解液を注液した際の、液面が上昇するので蓄電素子吸収が改善され含浸時間を短くできる効果がある。
【実施例】
【0046】
以下、本発明の具体的な作製例について説明する。下記の方法で、本発明の実施例および比較例の電極活物質二次粒子を作製した。
[実施例1](製法1:ゾルゲル法)
坩堝内にCo酸化物(Co3O4)を1.0g投入し、fluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。大気雰囲気下、電気炉を用いて800℃で24時間焼成し、fluxを熔融させることでCo酸化物のLi化と結晶育成を行い、D50=15μmとなるまで成長させた。反応後、72時間かけて室温まで冷却した。生成したLiCoO2の結晶を蒸留水にて水洗し、上記工程で反応せずに残ったfluxを除去した。
【0047】
エタノール溶媒にて、LiアルコキシドおよびAlアルコキシドのダブルアルコキシド溶液を準備した。撹拌しながらH2Oを150ppm前後滴定し、ゲル化を促進させた状態の溶液をスプレードライにて上記LiCoO2の一次粒子に噴霧塗布した。
【0048】
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定して、結晶方位が一方向に配向した一次粒子の凝集体(二次粒子)を得た。所望のサイズに形成したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスを掛け、更に凝集させ、最後にこれらの凝集体を焼結することで表1に示す実施例1の二次粒子を得た。
【0049】
[実施例2](製法1:ゾルゲル法)
Co酸化物(Co3O4)の代わりに、1:1:1のモル比のNi/Co/Mn混合酸化物を用い、LiアルコキシドおよびAlアルコキシドのダブルアルコキシド溶液を用い、一次粒子の寸法をD50=10μmとした以外は同様にして、表1に示す実施例2の二次粒子を得た。
【0050】
[実施例3](製法2:沈殿法)
遷移金属硝酸塩(1:1:1のモル比のNi/Co/Mn硝酸塩混合物)を0.2Mとなるように蒸留水に溶解させた。この水溶液に、Na2CO3水溶液0.2MおよびNH4OH水溶液0.2Mを滴下し、上記遷移金属の炭酸塩を沈殿させ、微細な一次粒子から構成された球状の二次粒子を得た。生成した炭酸塩の沈殿物を蒸留水にて水洗し、不純物として存在するNaイオンや硝酸イオンを除去した。
【0051】
Ni/Co/Mn炭酸塩の沈殿物1.0gを坩堝に投入し、 fluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。大気雰囲気下、電気炉を用いて800℃で24時間焼成し、fluxを熔融させることで炭酸塩のLi化と一次粒子結晶の整列化を行った。72時間かけて室温まで冷却した。
【0052】
[実施例4〜8](製法2:沈殿法)
遷移金属硝酸塩の混合物のモル比および一次粒子の寸法を、表1に記載の各比および寸法に変更した以外は同様にして、表1に示す実施例4〜8の二次粒子を得た。
【0053】
[実施例9](製法1:ゾルゲル法)
Fe(NO2)3・9H2O、Na2HPO4・12H2Oをそれぞれ蒸留水に溶解して0.1mol/Lの溶液とし、これらの水溶液を混合した。得られた沈殿をろ過・水洗後に乾燥させて600℃で3時間空気中において焼成し、FePO4を得た。るつぼ内に1.0gのFePO4とfluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。また、FePO4の還元剤として0.1gのスクロースを加え、アルゴンと水素の混合ガス中で800℃で24時間焼成し、fluxを溶融させることでFePO4のLi化とD50=3μmとなるまで結晶育成を行った。反応後、72時間かけて室温まで冷却した。生成したLiFePO4の結晶を蒸留水にて水洗し、上記工程で反応せずに残ったfluxやスクロースを除去した。
【0054】
エタノール溶媒にて、金属アルコキシド(LiアルコキシドおよびAlアルコキシド)のダブルアルコキシド溶液を準備した。撹拌しながらH2Oを150ppm前後滴定し、ゲル化を促進させた状態の溶液をスプレードライにて上記LiFePO4の一次粒子に噴霧塗布した。
【0055】
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定して、結晶方位が一方向に配向した一次粒子の凝集体(二次粒子)を得た。所望のサイズに形成したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスを掛け、更に凝集させ、最後にこれらの凝集体を焼結することで表1に示す実施例9の二次粒子を得た。
【0056】
[比較例1](三元系)
反応容器に水酸化ナトリウムを添加してpHを約12に調整した2質量%のアンモニア水を用意した。Ni,Co,Mnのmol比が1/6:1/6:2/3となるよう調整した遷移金属硝酸塩を含む混合水溶液を反応容器内のアルカリ性溶液に滴下した。このとき反応溶液がpH約12に保たれるように25質量%のアンモニア水と水酸化ナトリウム水溶液も同時に滴下させた。反応溶液の温度は約50℃に保ち、反応雰囲気が不活性雰囲気となるよう窒素ガスをパージした。得られた生成物を濾過、水洗することでNi:Co:Mn=1/6:1/6:2/3のmol比で構成される水酸化物を得た。この水酸化物1molと水酸化リチウム一水和物1.4molを混合した。その混合物をアルミナるつぼに入れ、800℃で24時間焼成することでLi1.4(Ni1/6Co1/6Mn2/3)O2を合成した。
【0057】
[比較例2](鉄オリビン)
酢酸鉄(Fe(CH3COO)2)、リン酸水素二アンモニウム((NH4)2HPO4)、炭酸リチウム(Li2CO3)をリン酸鉄リチウム(LiFePO4)の化学両論比となるよう秤量した。秤量した原料にアセトンとジルコニアボールを加え、遊星型ボールミルを用いて混合した。混合物を乾燥し、アルゴンと水素の300℃で2時間予備焼成を行い、続いて800℃で24時間本焼成を行いリン酸鉄リチウム(LiFePO4)を合成した。
【0058】
X線回折分析
上記で作製した各実施例および比較例の電極活物質二次粒子について、X線回折分析を行った。その結果を、層状化合物については図7に、オリビン化合物については図8に示す。図7に示すように、層状化合物の実施例については、003のピークよりも110のピークが相対的に比較例よりも強まっており110配向していることが確認された。また、図8に示すように、オリビン化合物の実施例については、200ピークよりも020ピークが相対的に比較例よりも強まっており020配向が確認された。
【0059】
レート特性試験
各実施例および各比較例の電極活物質二次粒子を用いて、電池セルを作製した。負極の集電箔として厚さ14μmのCu箔を用い、正極の集電箔として厚さ20μmのAl箔を用いた。負極活物質は、粒径22μmの人造黒鉛粒子を用いた。PVDFバインダーを用いて電極を作製し、電極体プレス後の活物質層の厚みはそれぞれ100μmとした。負極の電極密度は1.5g/cm3、正極の電極密度は3.8g/cm3であった。正極側は塗工部110mm、未塗工部8mmとし、負極側は塗工部114mm、未塗工部8mmとし、セパレータは膜厚25μmのものを用いて正負極の間に挟んだ。
【0060】
セパレータ間に正、負極を挿入して、巻き芯で巻回した。終了後、巻き芯を抜き、素子厚み12mmの扁平型の蓄電素子を得た。集電箔として、正極、負極にそれぞれAlおよびCuの未塗工部を左右に出した。
【0061】
蓄電素子を80℃で24hr真空乾燥した後、グローブボックス内の含浸用の容器の中に、蓄電素子を投入し容器の内部を減圧、その後電解液1.0MのLiPF6/(EC+DMC+EMC)を注入して、含浸を行った。
【0062】
3003のアルミニウム合金を用いて、インパクト成型により、ケース板厚0.5mm、ケース外形寸法L130×W25×H80mmの電池ケースを作製した。上記で作製した蓄電素子は、電池ケース内に挿入した。この電池ケース内に挿入し、上部を電池蓋にて封止し、蓋とケースをYAG溶接で封口後、充放電装置で、4.2Vまで0.2Cの電流でCCCV充電を8時間行った。その後、減圧して脱泡して、注液口にゴム栓をしてセルを完成させた。SOC50%まで放電を行い、初期性能測定を行った。
【0063】
各電池について、高レート(5C)での放電および低レート(0.1C)での放電を行い、各放電から電池の容量を計算し、比率を求め、高レート容量維持率とした。結果を表1に示す。
【0064】
【表1】

【0065】
実施例は一次粒子がLiイオンの挿入離脱がスムーズな結晶面を揃えて二次粒子を形成しているため、急速充放電特性が高い。また、二次粒子を形成している一次粒子の一つ一つが微細なので固体内のLiイオン拡散パスが短く急速充放電に有利である。さらに、個々の一次粒子は単結晶で形成されているので格子欠陥などが存在せず、Liの固体内拡散を阻害するものが極めて少ないので、比較例よりも急速充放電特性が優れる(レート特性試験)。
【0066】
比較例のように固体内のLiイオン拡散パスを短くするために低温焼成して微粒子粉末を得ると、結晶性が低下する。そのような活物質を用いて充放電を繰り返すと徐々に非晶質化が進行し、充放電サイクル特性が悪化する。また、結晶性を上げるために高温で焼成させるだけでは粒子間で焼結が進行し、結晶性は高まるが大粒子化するので急速充放電特性が損なわれる。
【産業上の利用可能性】
【0067】
本発明によれば、大電流での充放電が可能となり、かつ、レート特性が向上するから、車載用リチウムイオン二次電池に適用して極めて有望である。
【符号の説明】
【0068】
E…正極、
1…正極集電体、
2…電極活物質二次粒子、
3…導電材、
4…バインダー、
5…電極活物質一次粒子。
【技術分野】
【0001】
本発明は、リチウムイオン二次電池に係り、特に、リチウムイオン二次電池の充放電レート特性を向上させる技術に関する。
【背景技術】
【0002】
車載用のリチウムイオン二次電池においては、それぞれ正極、負極および電解液を有する単電池(セル)が複数個直列に配置されて組電池を形成し、充放電制御のためのセルコントローラが接続され、必要な電圧が得られるようにバッテリーモジュールを形成する。
【0003】
このような二次電池の単電池には、電極シートとセパレータを重ね、扁平型や円筒型に巻回した後に潰した巻回型蓄電素子、あるいは、平板状に切り出した電極とセパレータを積層した積層型蓄電素子の2種類があり、これらを、円筒型のケースに収納したものや、角型、扁平型のケースに収納したものが知られている。
【0004】
単電池の構成要素のうち、正極または負極の電極シートは、薄い金属箔である集電箔の表面に、電極活物質粒子、バインダー、溶媒等を含む電極活物質のペーストが塗布および乾燥されてなる。
【0005】
単電池の充放電に際しては、リチウムイオンが電解液と電極活物質粒子との間を拡散して出入りする。そのため、従来、大電流にて充放電を行うと、リチウムイオンの出入りが円滑に行われず、レート特性(高レート充放電においても容量が維持される性能)が低下する原因となっていた。このレート特性を維持しながら大電流にて充放電を行なうためには、リチウムイオンの電極活物質粒子と電解液との間の出入りを迅速かつ円滑にする必要がある。
【0006】
しかしながら、従来、電極活物質粒子を構成する結晶は、結晶格子がランダムに配向した非晶質または多結晶質であるため、リチウムイオンの拡散のための移動経路が複雑となり、結果として、一定レベル以上の高レートの充放電は困難であった。
【0007】
このような問題を解決するため、リチウムイオン電池において、正極の電極活物質を単結晶の二酸化マンガンとして、さらに、電解液と電極活物質との間のリチウムイオンの拡散移動経路が最短となるように、すなわち、正極集電体に対して垂直となるように、この単結晶を配向させた正極構造が知られている(例えば、特許文献1参照)。
【0008】
しかしながら、特許文献1に記載の技術では、集電体上に単結晶を電気化学的に成長させる必要があるため、活物質の種類が限られるという問題や、結晶成長に著しく時間が掛かり単結晶の厚さを厚く形成することが困難であるという問題や、導電材およびバインダーの配合が制限されるという問題等がある。そのため、実現可能な寸法や仕様が限定され、実用化にはコストが高い。したがって、自動車用途に要求されるような、高レート特性を維持しつつ大電流による充放電を行う電池にこの技術を適用することは困難である。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2007−005281号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
本発明は、以上述べた従来技術の課題を解決するためになされたもので、レート特性が向上し、大電流による充放電を可能とする電極活物質材料およびその製造方法を提供することを目的としている。
【課題を解決するための手段】
【0011】
本発明の電極活物質は、リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、一次粒子は単結晶であり、二次粒子中の一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴としている。
【0012】
上記構成の本発明にあっては、電極活物質を構成する二次粒子中の一次粒子が、リチウムイオン拡散方向が同一になるように配向しているので、充放電時におけるリチウムイオンの電解液と電極活物質との間の拡散移動経路が短縮される。これにより、リチウムイオンの迅速な挿入離脱が可能となり、電極表面での電気化学反応速度が向上することで、レート特性や出力密度が向上する。これにより、急速な充放電や大電流の充放電にも対応可能な電池を構成することができる。
【0013】
本発明においては、一次粒子は、長尺面と、それよりも短い短尺面を有し、長尺面は、リチウムイオン拡散方向と交差しており、短尺面は、リチウムイオン拡散方向と平行であることを好ましい態様としている。
【0014】
上記構成の本発明にあっては、長尺面がリチウムイオン拡散方向と交差し、短尺面がリチウムイオン拡散方向と平行である。すなわち、リチウムイオンの挿入離脱が起こる出入り口の面が長尺面となっていて相対的に広いので、よりスムーズにリチウムイオンが出入りし、電気化学反応速度が向上する。また、リチウムイオンの拡散移動が起こる方向に平行な面が短尺面となっているので、リチウムイオンの移動距離が相対的に短くなり、同様に、よりスムーズにリチウムイオンが出入りし、電気化学反応速度が向上する。
【0015】
本発明の電極活物質材料の製造方法は、リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質からなる単結晶の一次粒子を生成する工程と、一次粒子を金属アルコキシドにて被覆する工程と、被覆された一次粒子を凝集させ二次粒子を生成する工程とからなることを特徴としている。
【0016】
上記構成の本発明にあっては、電極活物質の単結晶である一次粒子の表面に多数のアルコキシ基が形成され、隣接する一次粒子表面のアルコキシ基が凝集し、脱水縮合してエーテル基を形成することにより隣接する一次粒子どうしが結合されて二次粒子が形成されるが、この際、短尺面に比較して長尺面の方がより多くのアルコキシ基を有するため、隣接する一次粒子の長尺面どうしがより選択的に凝集することになる。これにより、本発明のリチウムイオンの拡散方向が揃った二次粒子を成長させることができる。
【図面の簡単な説明】
【0017】
【図1】本発明の電極活物質を用いた正極構造を模式的に示す断面図である。
【図2】本発明の電極活物質二次粒子の拡大図である。
【図3】本発明の第1実施形態における電極活物質一次粒子の結晶構造を示す模式図である。
【図4】本発明の第2実施形態における電極活物質一次粒子の結晶構造を示す模式図である。
【図5】本発明の第1実施形態における層状化合物の結晶構造を示す模式図である。
【図6】本発明の第2実施形態におけるオリビン化合物の結晶構造を示す模式図である。
【図7】本発明の実施例および比較例(層状化合物)のX線回折分析結果を示すチャートである。
【図8】本発明の実施例および比較例(オリビン化合物)のX線回折分析結果を示すチャートである。
【発明を実施するための形態】
【0018】
以下、図面を参照して本発明の実施の形態を説明する。
図1は、本発明の実施形態に係るリチウムイオン電池における正極を模式的に示した断面図である。正極Eは、例えばアルミニウム等の金属箔の集電体1上に、電極活物質二次粒子2および導電材粒子3が、バインダー4により結着されて構成されている。電極Eは、例えば、電極活物質二次粒子2、導電材3およびバインダー4を溶媒と共に混練してペースト状としたものを集電体1上に塗布する公知の方法によって製造することができる。
【0019】
図2は、電極活物質二次粒子2の拡大図である。電極活物質二次粒子2は、多数の電極活物質一次粒子5が凝集して構成されている。本発明においては、図2に示すように、電極活物質一次粒子5は、長尺面と短尺面を有し、一次粒子5は、長尺面間で凝集して二次粒子を構成していると好ましく、また、長尺と短尺の比L/Dは、1.1以上になると好ましい。1.1未満であると長尺面と短尺面がほぼ同じとなってしまい、特に1未満であると、長尺面と短尺面が逆転してしまい好ましくない。また、一次粒子の粒径は、0.05〜100μm、特に0.1〜20μmの範囲が好ましい。
【0020】
第1実施形態(層状化合物)
図3は、電極活物質一次粒子5が、リチウムの層状化合物で構成されている本発明の第1実施形態を示し、図5は、層状化合物の結晶構造を説明する図である。本発明のリチウムの層状化合物は、一般式LixMO2±y(0.8≦x≦2.5、yはxに依存して変化)を取る複合酸化物であり、ここで、Mは、Al,Mg,V,Ti,Ni,Co,Mn,Fe,Cuのうち少なくとも一つを含む遷移金属である。
【0021】
図5に示すように、層状化合物の結晶は、遷移金属Mの酸化物層とリチウム層が交互に配列された構造を取る。そして、遷移金属Mの酸化物層とリチウム層の延在方向は、結晶格子の003面(00N面、N:整数、以下同じ)に一致し、110面(NN0面)に垂直に交わる。そのため、充放電に伴う電気化学反応に際しては、リチウムイオンは、003面に平行な方向に沿って拡散移動が行なわれる。
【0022】
したがって、本発明では、図3に示すように、電極活物質一次粒子5の長尺面Lが層状化合物の110面(NN0面)に一致し、かつ短尺面Dが003面(00N面)に一致するように一次粒子を構成し、かつ、一次粒子5を、それぞれの粒子におけるリチウムイオン拡散方向が一致するように、長尺面同士を結合させて二次粒子2を構成している。
【0023】
このように、本発明では、長尺面Lをリチウムイオンの出入り口とすることによってリチウムイオンの電極活物質内への挿入離脱をスムーズにすると共に、二次粒子2中の各一次粒子5のリチウムイオン拡散移動経路の方向を揃えることによって電気化学反応に際してのリチウムイオンの拡散移動経路に屈曲を無くし、最短距離とすることができる。
【0024】
第2実施形態(オリビン化合物)
図4は、電極活物質一次粒子5が、リチウムのオリビン化合物で構成されている本発明の第2実施形態を示し、図6は、オリビン化合物の結晶構造を説明する図である。本発明のリチウムのオリビン化合物は、一般式LiMPO4を取る複合酸化物であり、ここで、Mは、Al,Mg,V,Ti,Ni,Co,Mn,Fe,Cuのうち少なくとも一つを含む遷移金属である。
【0025】
図6に示すように、オリビン化合物の結晶は、MPO4の結晶構造の間にLiが層状に存在し、このLiの存在する層が200面(N00面)に一致した構造を取る。そして、リチウム層の延在方向は、結晶の020面(0N0面)に垂直に交わる。そのため、充放電に伴う電気化学反応に際しては、リチウムイオンは、200面に平行な方向に沿って拡散移動が行なわれる。
【0026】
したがって、本発明では、図4に示すように、電極活物質一次粒子5の長尺面Lが層状化合物の020面(0N0面)に一致し、かつ短尺面Dが200面(N00面)に一致するように一次粒子を構成し、かつ、一次粒子5を、それぞれの粒子におけるリチウムイオン拡散方向が一致するように長尺面同士を結合させて二次粒子2を構成している。
【0027】
このように、本発明では、長尺面Lをリチウムイオンの出入り口とすることによってリチウムイオンの電極活物質内への挿入離脱をスムーズにすると共に、二次粒子2中の各一次粒子5のリチウムイオン拡散移動経路の方向を揃えることによって電気化学反応に際してのリチウムイオンの拡散移動経路に屈曲を無くし、最短距離とすることができる。
【0028】
本発明の一次粒子および二次粒子の製造方法1:ゾルゲル法
上述した本発明における個々の一次粒子が特定の結晶面を揃えて整列した二次粒子は、下記の方法で作製することができる。
【0029】
<プロセス1:溶融塩中での結晶育成>
坩堝内に遷移金属酸化物を投入し、fluxかつLi源となるLi2OとLiClをそれぞれ投入する。大気雰囲気下、電気炉等を用いて300〜1000℃で焼成し、fluxを熔融させることで遷移金属酸化物のLi化および結晶育成を行う。これにより、電極活物質一次粒子の単結晶を成長させることができる。反応後、反応系を室温まで冷却を行う。結晶育成時間は、目的の単結晶の寸法に応じて任意に設定することができる。
【0030】
<プロセス2:過剰のflux除去>
次に、生成した結晶を蒸留水にて水洗し、上記工程で反応せずに残った過剰のfluxを除去する。用いるfluxの種類や量、結晶育成条件、坩堝に投入する遷移金属酸化物の粒子径を変化させることで、生成する一次粒子の大きさを0.05μm〜100μmの範囲で任意に制御することができる。flux水洗回数、時間は任意である。また、水洗温度も特に規定されないが温水を用いるとfluxの溶解度が増加するので効率的に除去できる。具体的には10〜90℃の範囲の水が使用可能である。
【0031】
<プロセス3:有機コート>
任意の複合酸化物を含む金属アルコキシドを用意しゾルゲル法を施す。複合酸化物がLiAlO2の場合、Li−OR、Al−ORを用いる。RO−は、エトキシ基であることが好ましい。これらダブルアルコキシド溶液をエタノールなどの溶媒にて準備する。撹拌しながらH2Oを滴定し、ゲル化を促進させた状態の溶液をスプレードライにて電極活物質一次粒子に噴霧塗布する。
【0032】
<プロセス4:二次粒子の形成>
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定していくと一次粒子の凝集体が形成される。これは活物質表面に結合している有機物同士がアルコキシド中の金属を介して活物質を長尺を含む面同士で結合していくことで配向した凝集が行なわれているのである。所望のサイズに凝集して成長したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスをかける。LiAlO2の場合、1トン/cm2の圧力を30秒保持する。これにより凝集体のアルコキシド金属を含む有機分が凝集体表面に押し出されながら更に凝集していく。最後にこれらの凝集体を焼結することで所望の二次粒子を得る。LiAlO2の場合、500度にて30分保持する。
【0033】
本発明の一次粒子および二次粒子の製造方法2:沈殿法
<プロセス1:遷移金属炭酸塩の沈殿>
遷移金属硝酸塩を蒸留水に溶解させる。その水溶液に炭酸ナトリウム水溶液と水酸化アンモニウム水溶液を滴下する。溶液が塩基性を帯びると遷移金属が炭酸塩として沈殿し、その沈殿物は微細な一次粒子から構成された球状の二次粒子となっている。遷移金属塩の種類は特に限定されず、硫酸塩や酢酸塩を用いても良いが、後の水洗・焼成工程で容易に除去できる硝酸塩が望ましい。
【0034】
<プロセス2:水洗>
生成した遷移金属炭酸塩の沈殿物を蒸留水にて水洗する。この工程で不純物として存在するNaイオンや硝酸イオンを除去する。水洗回数、時間は任意である。また、水洗温度も特に規定されないが温水を用いると効率的に不純物を除去できる。
【0035】
<プロセス3:沈殿物のLi化と一次粒子の結晶面整列化>
遷移金属炭酸塩の沈殿物を坩堝に投入し、fluxかつLi源となるLi2OとLiClをそれぞれ投入する。大気雰囲気下、電気炉等を用いて焼成し、fluxを熔融させることで炭酸塩のLi化と一次粒子結晶の整列化を行う。室温まで冷却する。
【0036】
焼成時に炭酸塩は脱炭酸するとともに、Liと反応し、Li含有遷移金属酸化物へと変化する。また多結晶体からなる個々の一次粒子は溶融塩中で一次粒子が単結晶化し、冷却過程で特定の結晶面が揃った二次粒子となる。用いるfluxの種類や量、結晶育成条件を変化させることで、揃う結晶面を制御できる。また、一次粒子の結晶面を揃える為に必要な冷却過程の時間は特に限定されないが、最高到達温度から室温までなるべく時間をかけて冷却することが望ましい。
【0037】
以下、本発明の各構成要素について詳細に説明する。
正極シート
リチウムイオン二次電池を構成する正極シートは、アルミニウムからなる正極集電体の両面に正極材料が結着した構造を有する。本発明の正極材料としては、本発明の電極活物質二次粒子を用い、導電フィラーとして、アセチレンブラック、ケッチエンブラック、VGCF等が挙げられる。正極および負極の導電フィラーは、同一でも、異なっていても良い。
【0038】
正極シートの結着材としては、電池内で化学的に安定なものであれば、熱可塑性樹脂、熱硬化性樹脂のいずれも使用できる。例えば、ポリエチレン、ポリプロピレン、ポリテトラフルオロエチレン(PTFE)、ポリフッ化ビニリデン(PVDF)、スチレンブタジエンゴムなどが挙げられ、これらを単独または複数混合して用いることができる。これらの中でも特に少量で結着力を発揮できるPVDFとPTFEが好ましい。
【0039】
負極シート
蓄電素子を構成する負極シートは、銅などからなる負極集電体の両面に負極材料が結着した構造を有する。本実施例の負極材料としては、リチウムイオンを吸蔵放出する炭素材料やSn、Si、Pb、Coを含む合金や酸化物を用いることができる。炭素材料としては、天然黒鉛、人造黒鉛、活性炭、600〜1200℃で焼成した低温炭素体(例えば、易黒鉛性炭素前駆体として、ピッチ、メソフェーズピッチ、または難黒鉛化性炭素前駆体として、フェノール樹脂、キシレン樹脂、PPS、セルロース等)を不活性雰囲気中で熱処理して合成した炭素などが挙げられる。中心部の素子と外周部の素子の電極活物質は、同一でも、異なっても良い。例えば、中心部の素子は、温度が高くなるので劣化が起こりやすいので、劣化タフネスが高く、膨張の小さい、ハードカーボンを中心部の負極に用い、外側の電極はソフトカーボン、黒鉛材料を用いることもできる。
【0040】
負極シートの結着材としては、前述の正極で用いた結着材と同様のものが使用でき、その中でも特にスチレンブタジエンゴム、ポリフッ化ビニリデンなどが好ましい。
【0041】
セパレータシート
蓄電素子を構成するセパレータシートは、ポリオレフィン系微多孔質セパレータ、例えば、ポリエチレン、ポリプロピレンや不織布セパレータ、例えば、ポリエステル繊維、アラミド繊維を用いることができる。
【0042】
電解液
溶媒としては、例えばエチレンカーボネート(EC)、プロピレンカーボネート(PC)、ブチレンカーボネート(BC)、ジメチルカーボネート(DMC)、ジエチルカーボネート(DEC)、エチルメチルカーボネート(EMC)、γ−ブチロラクトン(γ−BL)、スルホラン、アセトニトリル、1,2−ジメトキシエタン、1,3−ジメトキシプロパン、ジメチルエーテル、テトラヒドロフラン(THF)、2−メチルテトラヒドロフラン等を挙げることができる。溶媒は、単独で使用しても、2種以上混合して使用しても良い。電解質としては、例えば過塩素酸リチウム(LiClO4)、六フッ化リン酸リチウム(LiPF6)、四フッ化ホウ素リチウム(LiBF4)、六フッ化砒素リチウム(LiAsF6)、トリフルオロメタンスルホン酸リチウム(LiCF3SO3)、ビストリフルオロメチルスルホニルイミドリチウム[LiN(CF3SO3)2]等のリチウム塩を挙げることができる。電解質は、単独で使用しても、2種以上混合して使用しても良い。電解質の溶媒に対する溶解量は、通常は0.2mol/L〜2mol/L程度である。種々のイオン性液体を混合してもよい。加えて、電解液の保持する、ゲル電解質としてもよくその保持材料としては、ポリエチレンオキサイド、ポリプロピレンオキサイド、ビニリデンフロライド(VdF)やヘキサフルオロプロピレン(HFP)またはその誘導体、または共重合体を用いることができる。
【0043】
電極端子
正極端子および負極端子の電極端子には、銅、ニッケル、アルミニウム、ステンレスといった金属またはこれらを含む合金やこれら金属を母材にしてニッケルメッキを施したものが使用可能である。集電箔と端子部分の接合面積を稼ぐためには、板状であることが好ましい。
【0044】
リード板
正極及び負極リード板には、銅、ニッケル、アルミニウム、ステンレスといった金属またはこれらを含む合金やこれら金属を母材にしてニッケルメッキを施したものが使用可能である。
【0045】
電池ケース
底面部の形状を加工するには、アルミ、ステンレス合金、樹脂を用いることができるが、インパクト成型、トランスファープレス加工によって作製したアルミニウム合金が好ましい。ケースは、蓄電素子と密着する構造が好ましく、これによりケースと蓄電素子との間の空間が少なくなり、電解液を注液した際の、液面が上昇するので蓄電素子吸収が改善され含浸時間を短くできる効果がある。
【実施例】
【0046】
以下、本発明の具体的な作製例について説明する。下記の方法で、本発明の実施例および比較例の電極活物質二次粒子を作製した。
[実施例1](製法1:ゾルゲル法)
坩堝内にCo酸化物(Co3O4)を1.0g投入し、fluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。大気雰囲気下、電気炉を用いて800℃で24時間焼成し、fluxを熔融させることでCo酸化物のLi化と結晶育成を行い、D50=15μmとなるまで成長させた。反応後、72時間かけて室温まで冷却した。生成したLiCoO2の結晶を蒸留水にて水洗し、上記工程で反応せずに残ったfluxを除去した。
【0047】
エタノール溶媒にて、LiアルコキシドおよびAlアルコキシドのダブルアルコキシド溶液を準備した。撹拌しながらH2Oを150ppm前後滴定し、ゲル化を促進させた状態の溶液をスプレードライにて上記LiCoO2の一次粒子に噴霧塗布した。
【0048】
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定して、結晶方位が一方向に配向した一次粒子の凝集体(二次粒子)を得た。所望のサイズに形成したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスを掛け、更に凝集させ、最後にこれらの凝集体を焼結することで表1に示す実施例1の二次粒子を得た。
【0049】
[実施例2](製法1:ゾルゲル法)
Co酸化物(Co3O4)の代わりに、1:1:1のモル比のNi/Co/Mn混合酸化物を用い、LiアルコキシドおよびAlアルコキシドのダブルアルコキシド溶液を用い、一次粒子の寸法をD50=10μmとした以外は同様にして、表1に示す実施例2の二次粒子を得た。
【0050】
[実施例3](製法2:沈殿法)
遷移金属硝酸塩(1:1:1のモル比のNi/Co/Mn硝酸塩混合物)を0.2Mとなるように蒸留水に溶解させた。この水溶液に、Na2CO3水溶液0.2MおよびNH4OH水溶液0.2Mを滴下し、上記遷移金属の炭酸塩を沈殿させ、微細な一次粒子から構成された球状の二次粒子を得た。生成した炭酸塩の沈殿物を蒸留水にて水洗し、不純物として存在するNaイオンや硝酸イオンを除去した。
【0051】
Ni/Co/Mn炭酸塩の沈殿物1.0gを坩堝に投入し、 fluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。大気雰囲気下、電気炉を用いて800℃で24時間焼成し、fluxを熔融させることで炭酸塩のLi化と一次粒子結晶の整列化を行った。72時間かけて室温まで冷却した。
【0052】
[実施例4〜8](製法2:沈殿法)
遷移金属硝酸塩の混合物のモル比および一次粒子の寸法を、表1に記載の各比および寸法に変更した以外は同様にして、表1に示す実施例4〜8の二次粒子を得た。
【0053】
[実施例9](製法1:ゾルゲル法)
Fe(NO2)3・9H2O、Na2HPO4・12H2Oをそれぞれ蒸留水に溶解して0.1mol/Lの溶液とし、これらの水溶液を混合した。得られた沈殿をろ過・水洗後に乾燥させて600℃で3時間空気中において焼成し、FePO4を得た。るつぼ内に1.0gのFePO4とfluxかつLi源となるLi2OとLiClをそれぞれ4.0g投入した。また、FePO4の還元剤として0.1gのスクロースを加え、アルゴンと水素の混合ガス中で800℃で24時間焼成し、fluxを溶融させることでFePO4のLi化とD50=3μmとなるまで結晶育成を行った。反応後、72時間かけて室温まで冷却した。生成したLiFePO4の結晶を蒸留水にて水洗し、上記工程で反応せずに残ったfluxやスクロースを除去した。
【0054】
エタノール溶媒にて、金属アルコキシド(LiアルコキシドおよびAlアルコキシド)のダブルアルコキシド溶液を準備した。撹拌しながらH2Oを150ppm前後滴定し、ゲル化を促進させた状態の溶液をスプレードライにて上記LiFePO4の一次粒子に噴霧塗布した。
【0055】
噴霧塗布された一次粒子をエタノール溶媒中にて撹拌しながら更にH2Oを滴定して、結晶方位が一方向に配向した一次粒子の凝集体(二次粒子)を得た。所望のサイズに形成したところで撹拌を止め、溶媒を静水圧プレスの容器に入れてプレスを掛け、更に凝集させ、最後にこれらの凝集体を焼結することで表1に示す実施例9の二次粒子を得た。
【0056】
[比較例1](三元系)
反応容器に水酸化ナトリウムを添加してpHを約12に調整した2質量%のアンモニア水を用意した。Ni,Co,Mnのmol比が1/6:1/6:2/3となるよう調整した遷移金属硝酸塩を含む混合水溶液を反応容器内のアルカリ性溶液に滴下した。このとき反応溶液がpH約12に保たれるように25質量%のアンモニア水と水酸化ナトリウム水溶液も同時に滴下させた。反応溶液の温度は約50℃に保ち、反応雰囲気が不活性雰囲気となるよう窒素ガスをパージした。得られた生成物を濾過、水洗することでNi:Co:Mn=1/6:1/6:2/3のmol比で構成される水酸化物を得た。この水酸化物1molと水酸化リチウム一水和物1.4molを混合した。その混合物をアルミナるつぼに入れ、800℃で24時間焼成することでLi1.4(Ni1/6Co1/6Mn2/3)O2を合成した。
【0057】
[比較例2](鉄オリビン)
酢酸鉄(Fe(CH3COO)2)、リン酸水素二アンモニウム((NH4)2HPO4)、炭酸リチウム(Li2CO3)をリン酸鉄リチウム(LiFePO4)の化学両論比となるよう秤量した。秤量した原料にアセトンとジルコニアボールを加え、遊星型ボールミルを用いて混合した。混合物を乾燥し、アルゴンと水素の300℃で2時間予備焼成を行い、続いて800℃で24時間本焼成を行いリン酸鉄リチウム(LiFePO4)を合成した。
【0058】
X線回折分析
上記で作製した各実施例および比較例の電極活物質二次粒子について、X線回折分析を行った。その結果を、層状化合物については図7に、オリビン化合物については図8に示す。図7に示すように、層状化合物の実施例については、003のピークよりも110のピークが相対的に比較例よりも強まっており110配向していることが確認された。また、図8に示すように、オリビン化合物の実施例については、200ピークよりも020ピークが相対的に比較例よりも強まっており020配向が確認された。
【0059】
レート特性試験
各実施例および各比較例の電極活物質二次粒子を用いて、電池セルを作製した。負極の集電箔として厚さ14μmのCu箔を用い、正極の集電箔として厚さ20μmのAl箔を用いた。負極活物質は、粒径22μmの人造黒鉛粒子を用いた。PVDFバインダーを用いて電極を作製し、電極体プレス後の活物質層の厚みはそれぞれ100μmとした。負極の電極密度は1.5g/cm3、正極の電極密度は3.8g/cm3であった。正極側は塗工部110mm、未塗工部8mmとし、負極側は塗工部114mm、未塗工部8mmとし、セパレータは膜厚25μmのものを用いて正負極の間に挟んだ。
【0060】
セパレータ間に正、負極を挿入して、巻き芯で巻回した。終了後、巻き芯を抜き、素子厚み12mmの扁平型の蓄電素子を得た。集電箔として、正極、負極にそれぞれAlおよびCuの未塗工部を左右に出した。
【0061】
蓄電素子を80℃で24hr真空乾燥した後、グローブボックス内の含浸用の容器の中に、蓄電素子を投入し容器の内部を減圧、その後電解液1.0MのLiPF6/(EC+DMC+EMC)を注入して、含浸を行った。
【0062】
3003のアルミニウム合金を用いて、インパクト成型により、ケース板厚0.5mm、ケース外形寸法L130×W25×H80mmの電池ケースを作製した。上記で作製した蓄電素子は、電池ケース内に挿入した。この電池ケース内に挿入し、上部を電池蓋にて封止し、蓋とケースをYAG溶接で封口後、充放電装置で、4.2Vまで0.2Cの電流でCCCV充電を8時間行った。その後、減圧して脱泡して、注液口にゴム栓をしてセルを完成させた。SOC50%まで放電を行い、初期性能測定を行った。
【0063】
各電池について、高レート(5C)での放電および低レート(0.1C)での放電を行い、各放電から電池の容量を計算し、比率を求め、高レート容量維持率とした。結果を表1に示す。
【0064】
【表1】

【0065】
実施例は一次粒子がLiイオンの挿入離脱がスムーズな結晶面を揃えて二次粒子を形成しているため、急速充放電特性が高い。また、二次粒子を形成している一次粒子の一つ一つが微細なので固体内のLiイオン拡散パスが短く急速充放電に有利である。さらに、個々の一次粒子は単結晶で形成されているので格子欠陥などが存在せず、Liの固体内拡散を阻害するものが極めて少ないので、比較例よりも急速充放電特性が優れる(レート特性試験)。
【0066】
比較例のように固体内のLiイオン拡散パスを短くするために低温焼成して微粒子粉末を得ると、結晶性が低下する。そのような活物質を用いて充放電を繰り返すと徐々に非晶質化が進行し、充放電サイクル特性が悪化する。また、結晶性を上げるために高温で焼成させるだけでは粒子間で焼結が進行し、結晶性は高まるが大粒子化するので急速充放電特性が損なわれる。
【産業上の利用可能性】
【0067】
本発明によれば、大電流での充放電が可能となり、かつ、レート特性が向上するから、車載用リチウムイオン二次電池に適用して極めて有望である。
【符号の説明】
【0068】
E…正極、
1…正極集電体、
2…電極活物質二次粒子、
3…導電材、
4…バインダー、
5…電極活物質一次粒子。
【特許請求の範囲】
【請求項1】
リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、
前記一次粒子は単結晶であり、
前記二次粒子中の前記一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴とする電極活物質材料。
【請求項2】
前記一次粒子は、長尺面と、それよりも短い短尺面を有し、
前記長尺面は、前記リチウムイオン拡散方向と交差しており、前記短尺面は、前記リチウムイオン拡散方向と平行であることを特徴とする請求項1に記載の電極活物質材料。
【請求項3】
リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質からなる単結晶の一次粒子を生成する工程と、
前記一次粒子を、金属アルコキシドにて被覆する工程と、
被覆された前記一次粒子を凝集させ二次粒子を生成する工程とからなることを特徴とする電極活物質材料の製造方法。
【請求項4】
前記金属アルコキシドの金属は、前記層状またはオリビン化合物の構成金属と同一であることを特徴とする請求項3に記載の電極活物質材料の製造方法。
【請求項5】
請求項1または2に記載の電極活物質材料を用いたリチウムイオン二次電池。
【請求項1】
リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質の一次粒子が集合した二次粒子から構成される電極活物質材料であって、
前記一次粒子は単結晶であり、
前記二次粒子中の前記一次粒子は、各一次粒子におけるリチウムイオン拡散方向が同一になるように、かつ、少なくともリチウムイオン拡散方向へ積層されたことを特徴とする電極活物質材料。
【請求項2】
前記一次粒子は、長尺面と、それよりも短い短尺面を有し、
前記長尺面は、前記リチウムイオン拡散方向と交差しており、前記短尺面は、前記リチウムイオン拡散方向と平行であることを特徴とする請求項1に記載の電極活物質材料。
【請求項3】
リチウムの層状化合物及びオリビン化合物のいずれかから選択される活物質からなる単結晶の一次粒子を生成する工程と、
前記一次粒子を、金属アルコキシドにて被覆する工程と、
被覆された前記一次粒子を凝集させ二次粒子を生成する工程とからなることを特徴とする電極活物質材料の製造方法。
【請求項4】
前記金属アルコキシドの金属は、前記層状またはオリビン化合物の構成金属と同一であることを特徴とする請求項3に記載の電極活物質材料の製造方法。
【請求項5】
請求項1または2に記載の電極活物質材料を用いたリチウムイオン二次電池。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【公開番号】特開2013−65397(P2013−65397A)
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願番号】特願2011−201791(P2011−201791)
【出願日】平成23年9月15日(2011.9.15)
【出願人】(000005326)本田技研工業株式会社 (23,863)
【Fターム(参考)】
【公開日】平成25年4月11日(2013.4.11)
【国際特許分類】
【出願日】平成23年9月15日(2011.9.15)
【出願人】(000005326)本田技研工業株式会社 (23,863)
【Fターム(参考)】
[ Back to top ]

