電解窒素固定法
【課題】窒素ガスと酸素ガスを原料とし電気化学反応を利用して窒素酸化物を生成する電解窒素固定法を提供する。
【解決手段】電解窒素固定法は、陽極21と陰極22とに接触する溶融塩からなる電解質23を準備するステップと、陰極22に窒素ガスを供給するステップと、電解質23中に酸素ガスを供給するステップと、陽極21と陰極22との間に、陰極22において窒化物イオンが生成し、陽極において酸素が発生する電圧を印加するステップと、生成された窒化物イオンと供給された酸素とを接触させるステップとを含む。また、さらに電解窒素固定法は、陽極と陰極との間に挟むように配置された電解質を準備するステップと、陽極に窒素ガスを接触させるステップと、陰極に酸素ガスを接触させるステップと、陽極と陰極との間に、陰極において酸化物イオンが生成し、陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加するステップとを含む。
【解決手段】電解窒素固定法は、陽極21と陰極22とに接触する溶融塩からなる電解質23を準備するステップと、陰極22に窒素ガスを供給するステップと、電解質23中に酸素ガスを供給するステップと、陽極21と陰極22との間に、陰極22において窒化物イオンが生成し、陽極において酸素が発生する電圧を印加するステップと、生成された窒化物イオンと供給された酸素とを接触させるステップとを含む。また、さらに電解窒素固定法は、陽極と陰極との間に挟むように配置された電解質を準備するステップと、陽極に窒素ガスを接触させるステップと、陰極に酸素ガスを接触させるステップと、陽極と陰極との間に、陰極において酸化物イオンが生成し、陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加するステップとを含む。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、一般的には窒素固定法に関し、特定的には、窒素酸化物として窒素を固定する方法に関する。
【背景技術】
【0002】
窒素固定とは、空気中に多量に存在する窒素分子を、窒素化合物(アンモニア、窒素酸化物など)に変換するプロセスをいう。
【0003】
この窒素固定については、自然界では、例えばニトロゲナーゼを持つ菌類によってアンモニアが生成されることにより行われる。あるいは、雷の放電や紫外線により窒素酸化物が形成され、これが雨水に溶けることで硝酸となって土壌に固定される。
【0004】
人工的に合成される窒素化合物の最たる例がアンモニアである。20世紀初頭に、このアンモニアの製造を人工的に行う方法が開発され、それ以降、特に食糧増産(窒素肥料製造)の観点から、人類に多大な恩恵をもたらしてきた。その製造法はハーバー・ボッシュ法と呼ばれ、現在も全世界のアンモニア製造を担っている。このプロセスでは窒素と水素を触媒のもとで高温・高圧で反応させてアンモニアを合成する。しかしながら、現行のハーバー・ボッシュ法によるアンモニア製造では、水素を炭化水素の水蒸気改質によって得ており、この際に多量のCO2を排出する。地球温暖化ガスの代表例とされるCO2の排出が世界的に問題視されている現状に鑑みると、現行のアンモニア製造プロセスは、人工的な窒素固定法として、必ずしも優れたプロセスであるとは言い得なくなってきている。
【0005】
一方、窒素酸化物もまた(近年では、内燃機関からの排出ガスに含まれる大気汚染物質としての側面ばかりが注目されているが)、硝酸や窒素肥料を製造するために不可欠な物質である。純粋な窒素酸化物を得るために、現行の製造プロセスでは上記のアンモニアを原料としている。このプロセスでは、アンモニアを白金や白金ロジウム合金などの高価な触媒のもとで燃焼させて一酸化窒素を得た後、さらに常温で酸素と反応させて二酸化窒素を得る。ここで得られた二酸化窒素と水との反応を経て、硝酸が得られる。この硝酸の製造方法はオストワルト法と呼ばれており、現在も大量の硝酸が工業的に生産されている。
【0006】
また、例えば、特開昭58−162276号公報(特許文献1)には、窒素ガスと酸素ガスとの混合気体をプラズマ化して窒素酸化物を生成する方法が記載されている。
【0007】
また、例えば、特開平11−92120号公報(特許文献2)には、窒素ガスと酸素ガスから、フラーレンを触媒として光化学的に窒素酸化物を生成する方法が記載されている。
【0008】
また、例えば、特開2002−338214号公報(特許文献3)には、オゾンと窒素を原料として、窒素がオゾンにより酸化されることにより、亜酸化窒素を生成する亜酸化窒素の生成方法および製造装置が記載されている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開昭58−162276号公報
【特許文献2】特開平11−92120号公報
【特許文献3】特開2002−338214号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
しかしながら、オストワルト法においては、窒素酸化物を製造するための原料としてアンモニアを製造する必要がある。
【0011】
また、特許文献1に記載の方法ではプラズマ発生のための高価で複雑な装置が必要であり、また量産性にも乏しいことから、窒素酸化物を使った滅菌等に利用が限られていた。
【0012】
特許文献2に記載の方法では、窒素酸化物の生成速度が遅く、大量生産には向かないと考えられた。
【0013】
特許文献3に記載の方法では、窒素酸化物を得るために酸素からオゾンを製造する必要があった。
【0014】
そこで、この発明の目的は、アンモニアやオゾンなどを原料として利用するのではなく、窒素ガスと酸素ガスから直接的に窒素酸化物を生成し、量産化にも容易に対応できる方法を提供することである。
【課題を解決するための手段】
【0015】
本発明者らは、鋭意検討を重ねた結果、窒素ガスと酸素ガスを原料とし、電気化学反応を利用して窒素酸化物を生成する、窒素固定の新しいプロセスを見出すに至った。
【0016】
本発明では、窒化物イオンと酸素ガスを用いる方法(以下、方法Aとする)と、窒素ガスと酸化物イオンを用いる方法(以下、方法Bとする)の二つの方法を提供する。
【0017】
この発明の一つの局面に従った電解窒素固定法(方法A)は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極と陰極と、陽極と陰極とに接触する溶融塩からなる電解質とを準備する。ステップ(a2)では、陰極に窒素ガスを供給する。ステップ(a3)では、電解質中に酸素ガスを供給する。ステップ(a4)では、陽極と陰極との間に、陰極において窒素が還元されて窒化物イオンが生成し、陽極において酸化物イオンが酸化されて酸素が発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極は、陰極に供給された窒素ガスを電解質にまで供給することが可能であるように構成されている。
【0018】
電解質と接するように固定された陰極(窒素ガス陰極)では、窒素ガスが電気化学的に還元されて窒化物イオンが電解質中に供給される。
1/2 N2 + 3 e− → N3−
【0019】
窒化物イオンを含む電解質中に酸素ガスを供給することにより、窒化物イオンと酸素ガスは直接反応して窒素酸化物NOnを生成する(以下では、この反応を反応Aと表記する)。ここでNOnとはNO、NO2の他、N2O、N2O3、N2O4、N2O5などを指すものとする。
(反応A) N3− + (2n+3)/4 O2 → NOn + 3/2 O2−
【0020】
このNOn生成反応により生成する酸化物イオンは、同じく電解質と接するように配置された陽極上で酸化され、酸素ガスを発生する。
3/2 O2− → 3/4 O2 + 3 e−
【0021】
全反応式は次のようになり、窒素ガスと酸素ガスから窒素酸化物NOnが生成する。
1/2 N2 +n/2 O2 → NOn
【0022】
陽極で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして利用するのが好ましい。
【0023】
この発明に従った方法Aの電解窒素固定法においては、ステップ(a5)は、溶融塩を、陰極から、ステップ(a3)によって酸素ガスが供給される位置を経て、陽極まで流動させることによって行われることが好ましい。
【0024】
この発明に従った方法Aの電解窒素固定法においては、陰極は、多孔質体によって形成されていることが好ましい。
【0025】
このようにすることにより、窒素ガスを陰極と電解質との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極を構成することができる。なお、陰極は、必ずしも多孔質体でなくてもよい。
【0026】
この発明の別の局面に従った電解窒素固定法(方法B)は、次のステップ(b1)〜(b4)を含む。ステップ(b1)では、陽極と陰極と、陽極と陰極との間に配置された電解質とを準備する。ステップ(b2)では、陽極に窒素ガスを接触させる。ステップ(b3)では、陰極に酸素ガスを接触させる。ステップ(b4)では、陽極と陰極との間に、陰極において酸素ガスが還元されて酸化物イオンが生成し、陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0027】
電解質は、陰極において酸素ガスを還元させることによって生成された酸化物イオンが陽極まで移動できるように構成されている。陽極は、陽極に接触した窒素ガスを陽極と電解質との界面にまで供給することが可能であるように構成されている。陰極は、陰極に接触した酸素ガスを陰極と電解質との界面にまで供給することが可能であるように構成されている。
【0028】
このように、方法Bでは、溶融塩もしくは酸化物イオン導電性の固体電解質を電解質として用いることが好ましい。電解質と接するように固定された酸素ガス陰極では、酸素ガスが電気化学的に還元されて酸化物イオンが電解質中に供給される。
n/2 O2 + 2n e− → nO2−
【0029】
ここで生成された酸化物イオンは、窒素ガスが供給される陽極で酸化され、NOnを生成する(以下では、この反応を反応Bと表記する)。
(反応B) 1/2 N2 + nO2− → NOn + 2ne−
【0030】
全反応式は方法Aと同じになる。
1/2 N2 +n/2 O2 → NOn
【0031】
以上より、この発明によれば、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0032】
この発明に従った方法Bの電解窒素固定法においては、電解質は、溶融塩または酸化物イオン伝導性の固体電解質であることが好ましい。
【0033】
この発明に従った方法Bの電解窒素固定法においては、陽極は、多孔質体によって形成されていることが好ましい。
【0034】
このようにすることにより、窒素ガスを陽極と電解質との界面にまで供給することが可能であるように陽極を構成することができる。なお、陽極は、必ずしも多孔質体でなくてもよい。
【0035】
この発明に従った方法Bの電解窒素固定法においては、陰極は、多孔質体によって形成されていることが好ましい。
【0036】
このようにすることにより、酸素ガスを陰極と電解質との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極を構成することができる。なお、陰極は、必ずしも多孔質体でなくてもよい。
【発明の効果】
【0037】
以上のように、この発明によれば、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【図面の簡単な説明】
【0038】
【図1】本発明の第1実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
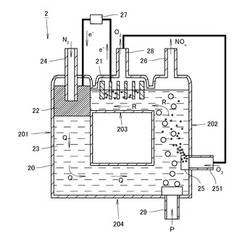
【図2】本発明の第2実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
【図3】本発明の第3実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
【発明を実施するための形態】
【0039】
以下、本発明の実施の形態を図面に基づいて説明する。
【0040】
(第1実施形態)
図1に示すように、方法Aによって窒素酸化物を製造するための窒素酸化物製造装置1は、陽極11と、陰極12と、溶融塩からなる電解質13と、窒素ガス供給部14と、酸素ガス供給部15と、酸素ガス供給管151と、窒素酸化物ガス排出部16と、電源部17と、酸素ガス排出部18とを備える。
【0041】
陽極11と陰極12とは電解質13に接触するように、電解質13を介して互いに対向するように配置されている。すなわち、電解質13は陽極11と陰極12との間に挟まれている。陰極12において電解質13に接触する面と反対側の面には窒素ガス供給部14によって窒素ガスが供給される。電解質13内の酸素ガス供給部15には酸素ガス供給管151を通して電解質13の外部から酸素ガスが供給される。電解質13には、電解質13中の窒素酸化物を電解質13の外部に排出するための窒素酸化物ガス排出部16が接続されている。陽極11において電解質13に接触する面と反対側の面には酸素ガス排出部18が接続されている。電源部17は陽極11と陰極12との間に電圧を印加する。
【0042】
陽極11では、NOn生成時に同時に生成した酸化物イオンが酸化され酸素ガスが生成する。したがって、溶融塩電解で通常用いられる酸素発生陽極が利用でき、ニッケルフェライトなどの導電性セラミクスや導電性ダイヤモンドが例示できる。ただし、電解開始直後などの電解質中の酸化物イオンの濃度が低い場合、電解電流の大きさによっては、たとえばLiCl−KClなどの溶融塩化物を溶融塩として用いる場合では、陽極が損耗する可能性がある。そのため、陽極反応に応じて黒鉛やグラッシーカーボンなどの炭素電極を使う、もしくは酸化リチウムや酸化カルシウムなどの添加により酸化物イオンをあらかじめ電解質中に供給しておくことで電解初期においても陽極反応が酸素発生となるようにする、などの措置を講じるのが好ましい。
【0043】
陰極12では、窒素ガスを還元して窒化物イオンを電解質中に供給する。従って、陰極の材質は、窒素ガスを安定して還元できる金属や合金、化合物であればよい。例えば、ニッケルや鉄を含むものが好ましく、特にニッケルを含むものが好ましい。陰極の形状としては、電解質との界面にまで窒素を供給するため、MCFC(Molten Carbonate Fuel Cell、溶融炭酸塩形燃料電池)の電極に用いられるような多孔質、金網状、メッシュ状が好ましく、陰極の表面にPt、Ir、Ru等の触媒を担持してもよい。このようにNOnを生成するための窒化物イオンは陰極から供給されるが、あらかじめ電解質中にLi3Nなどの窒化物イオン源を添加しておくことで、電解初期においても窒化物イオンが酸素ガスとスムーズに反応することができる。
【0044】
電解質13としては、窒化物イオン及び酸化物イオンが安定に存在できる溶融塩を用いることができる。溶融塩としては、例えば、アルカリ金属ハロゲン化物およびアルカリ土類金属ハロゲン化物の少なくとも一種が挙げられる。アルカリ金属ハロゲン化物としては、例えば、LiF、NaF、KF、RbF、CsF、LiCl、NaCl、KCl、RbCl、CsCl、LiBr、NaBr、KBr、RbBr、CsBr、LiI、NaI、KI、RbI、CsI等が挙げられる。アルカリ土類金属ハロゲン化物としては、例えば、MgF2、CaF2、SrF2、BaF2、MgCl2、CaCl2、SrCl2、BaCl2、MgBr2、CaBr2、SrBr2、BaBr2、MgI2、CaI2、SrI2、BaI2等が挙げられる。これらの化合物は単独または二種以上を組み合わせて溶融塩として使用できる。化合物の組み合わせや混合比は限定的ではなく、目的毎に定められた溶融塩の作動温度等に応じて適宜設定すればよい。
【0045】
方法Aでは、電解質13は、酸化リチウムや酸化カルシウムなどのアルカリ金属酸化物やアルカリ土類金属酸化物を含むことが好ましい。このようにすることにより、電解質13中に酸化物イオンを供給することができるので、電解開始直後から陽極11では酸化物イオンが酸化されて酸素ガスが発生する。この場合、陽極11に炭素電極を用いると炭素が消耗するので、電解初期の段階からニッケルフェライトなどの不溶性酸素発生陽極を用いることが好ましい。
【0046】
以上のように構成される窒素酸化物製造装置1の動作について説明する。
【0047】
窒素酸化物製造装置1においては、上述のように、陽極11と陰極12とが電解質13を挟むように配置されている。まず、窒素ガス供給部14に窒素ガスを供給することによって、陰極12に窒素ガスを接触させる。次に、陽極11と陰極12との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。また、酸素ガス供給管151から酸素ガス供給部15に酸素ガスを供給することによって電解質13中に酸素ガスが供給される。
【0048】
陰極12は、窒素ガスを供給できるように形成されているので、窒素ガスは陰極12の内部を通って、陰極12と電解質13との界面に到達する。陰極12と電解質13との界面では、次の反応が起きて窒化物イオンが生成する。
【0049】
(1/2)N2+3e− → N3−
生成した窒化物イオンは、電解質13中を移動して、酸素供給部15に到達する。
【0050】
酸素供給部15では、酸素ガスと、陰極12側から移動してきた窒化物イオンとが接触し、次の反応によって窒素酸化物と酸化物イオンとが生成される。
【0051】
(反応A)N3−+(2n+3)/4 O2 → NOn+3/2 O2−
【0052】
生成した窒素酸化物は窒素酸化物ガス排出部16から電解質13の外部に取り出される。酸化物イオンは、陽極11側へ移動する。陽極11では、次の反応によって酸素ガスが発生する。
【0053】
3/2 O2− → 3/4 O2 +3e−
【0054】
陽極11で発生した酸素ガスは、酸素ガス排出部18から電解質13の外部に排出される。陽極11で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして、酸素ガス供給管151から電解質13へ供給するように利用するのが好ましい。
【0055】
作動温度は、電解質13である溶融塩が安定に利用できる温度領域で作動させれば特に制限はされない。
【0056】
陽極11と陰極12との間に印加する電圧については、浴組成や作動温度などの条件に合わせて適宜調整すれば良いが、例えば450℃の溶融LiCl−KClを電解質に用いる場合には、陰極での窒素ガス還元反応はおよそ0.5V(vs.Li+/Li:同浴中で金属Liの示す電位を基準とする)よりも卑な電位領域で進行し、陽極での酸素ガス発生反応はおよそ2.5V(vs.Li+/Li)よりも貴な電位で進行することから、およそ2.0Vよりも大きい電圧を印加すれば良い。
【0057】
以上のように、窒素酸化物製造装置1において行われる電解窒素固定法は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極11と陰極12と、陽極11と陰極12とに接触する溶融塩からなる電解質13とを準備する。ステップ(a2)では、陰極12に窒素ガスを供給する。ステップ(a3)では、電解質13中に酸素ガスを供給する。ステップ(a4)では、陽極11と陰極12との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極12は、陰極12に供給された窒素ガスを電解質13にまで供給することが可能であるように構成されている。
【0058】
なお、ステップ(a2)とステップ(a3)とステップ(a4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0059】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0060】
また、窒素酸化物製造装置1においては、陰極12は、多孔質体によって形成されている。陰極12は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0061】
このようにすることにより、窒素ガスを陰極12と電解質13との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極12を構成することができる。
【0062】
ここで、方法Aによって窒素酸化物を合成する場合、例えば、陰極12で生成した窒化物イオンが、NOn生成部(酸素ガス供給部15)で消費しきれず未反応のまま陽極11に達した場合には、次式のように陽極11で酸化されて窒素ガスとなり、陽極11での酸素発生の電流分担率を低下させることになる。
N3− → 1/2 N2 + 3e−
【0063】
あるいは電解質13中に供給される酸素ガスが、未反応のまま陰極12に達した場合にも、例えば次に示すように陰極12で還元されて酸化物イオンを生成し、陰極12での窒素還元反応の電流分担率を低下させる。
3/2 O2 + 2 e− → O2−
【0064】
そのため、方法Aでは、陰極12で生成した窒化物イオンが全てNOn生成部(酸素ガス供給部15)へ供給され、またNOn生成部(酸素ガス供給部15)で生成した酸化物イオンが全て陽極11へ供給され、そして確実に消費される必要がある。そこで、電解質13である溶融塩を、電解槽内でループ状に循環させて、この溶融塩の循環に沿って、陰極12、NOn生成部(酸素ガス供給部15)、陽極11を配置するのが好ましい。このようにすることで、陰極12で生成した窒化物イオンを全てNOn生成部(酸素ガス供給部15)へ供給し、かつ、NOn生成部(酸素ガス供給部15)で生成した酸化物イオンを全て陽極11へ供給することができる。
【0065】
そこで、以下に、電解質をループ状に循環・流動させるように構成された窒素酸化物製造装置を用いて、方法Aによって窒素酸化物を製造する実施形態を説明する。
【0066】
(第2実施形態)
図2に示すように、第1実施形態の窒素酸化物製造装置1のより好ましい実施形態として、窒素酸化物製造装置2は、陽極21と、陰極22と、電解槽20と、電解槽20内に収容される、溶融塩からなる電解質23と、窒素ガス供給管24と、酸素ガス供給部25と酸素ガス供給管251と、窒素酸化物ガス排出部26と、電源部27と、酸素排出部28と、不活性ガス供給部29とを備える。陰極22は多孔質体によって形成されている。陰極22は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はなく、第1実施形態で述べたように、例えば、金網状、メッシュ状に形成されていてもよい。
【0067】
電解槽20は、この実施形態においては、鉛直方向に延びる第1流路201と第2流路202と、水平方向に延びる第3流路203と第4流路204とから構成されている。第1流路201と第2流路202とは、上部において第3流路203によって連結され、下部において第4流路204によって連結されている。
【0068】
電解槽20の内部の流路はまた、1つの流路が鉛直面内で円周形状に形成されているものなど、ループ状であればどのような形態であってもよく、必ず4つの流路が必要というわけではない。
【0069】
陽極21は、電解槽20の第3流路203内に配置される。陽極21では、NOn生成時に同時に生成した酸化物イオンが酸化され酸素ガスが生成する。陰極22は、電解槽20の第1流路201の上部に配置される。陰極22では、窒素ガスを還元して窒化物イオンを電解質中に供給する。窒素ガス供給管24は、電解槽20の外部から陰極22に窒素ガスを供給する。
【0070】
陽極21、陰極22、電解質23の構成や作動温度については、図1を用いて説明した通りである。
【0071】
電解質23の第2流路202中の下部の酸素ガス供給部25には、電解槽20の外部から、酸素ガス供給管251を通して酸素ガスが供給される。電解質中の窒化物イオンと酸素ガスとの反応は気液反応であることから、石英ガラス製や高純度アルミナ製などの多孔質ガス供給部を含むガス供給管などを利用して供給する場合には、供給される酸素ガスの気泡サイズを小さくする方が、反応がスムーズに進行するので好ましい。また、Ni製などの金属製の供給管や、上記のガラス製やアルミナ製の供給管に、触媒を担持した充填材を保持することなどは、触媒効果により電解質中の窒化物イオンと酸素ガスとの反応を促進させ得るので、より好ましい。
【0072】
第2流路202の上部の窒素酸化物ガス排出部26からは、窒素酸化物製造装置2で生成された窒素酸化物ガスが窒素酸化物製造装置2の外部に排出される。電源部27は、陽極21と陰極22との間に電圧を印加する。電源部27は、電源部27によって印加される電圧が、使用者によって制御されることが可能であるように構成されている。電解槽20の第3流路203の上部の酸素排出部28からは、電解槽20内で発生した酸素が電解槽20の外部に排出される。第2流路202の底部の不活性ガス供給部29は、図中に矢印Pで示すように、電解槽20の底部から電解質23中にアルゴン等の不活性ガスを供給する。
【0073】
以上のように構成される窒素酸化物製造装置2の動作について説明する。
【0074】
窒素酸化物製造装置2においては、上述のように、陽極21と陰極22とが電解質23に接触するように配置されている。まず、酸素ガス供給管251から酸素ガス供給部25に酸素ガスを供給することによって電解質23中に酸素ガスが供給される。窒素ガス供給管24に窒素ガスを供給することによって、陰極22に窒素ガスを接触させる。次に、陽極21と陰極22との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。
【0075】
陰極22は、窒素ガスを供給できるように形成されているので、窒素ガスは陰極22の内部を通って、陰極22と電解質23との界面に到達する。陰極22と電解質23との界面では、次の反応が起きて窒化物イオンが生成する。
【0076】
(1/2)N2+3e− → N3−
【0077】
電解質23には、底部の不活性ガス供給部29から不活性ガスが供給されている。このようにすることにより、ガスリフトによって電解質23の第2流路202内に上昇流が生じ、溶融塩が電解槽20のループ内を循環・流動される。溶融塩の流動には、プロペラ等を用いた機械的な方法を用いてもよいが、酸素ガスや不活性ガスの供給を利用したガスリフトを用いる方が、機械的な駆動部が不要であり、装置構成が単純になるので好ましい。生成した窒化物イオンは、図中に矢印Qで示す方向に移動して、第1流路201、第4流路204を通って、酸素ガス供給部25に到達する。
【0078】
酸素ガス供給部25では、酸素ガスと、陰極22側から移動してきた窒化物イオンとが接触し、次の反応によって窒素酸化物と酸化物イオンとが生成される。
【0079】
(反応A)N3−+(2n+3)/4 O2 → NOn+3/2 O2−
【0080】
生成した窒素酸化物と酸化物イオンとは、ガスリフトによって第2流路202内を下から上へ移動する。窒素酸化物は、第2流路202の上部の窒素酸化物ガス排出部26から電解槽20の外部に取り出される。酸化物イオンは、図中に矢印Rで示すように第2流路202内から第3流路203へ移動して、陽極21に到達する。陽極21では、次の反応によって酸素ガスが発生する。
【0081】
3/2 O2− → 3/4 O2 +3e−
【0082】
陽極21で発生した酸素ガスは、第3流路203の上部の酸素排出部28から電解槽20の外部に排出される。陽極21で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして、酸素ガス供給管251から電解質23へ供給するように利用するのが好ましい。
【0083】
このように、電解質23は、陰極22において窒素ガスを還元させることによって生成された窒化物イオンが酸素ガス供給部25にまで移動できるように、かつ、酸素ガス供給部25において窒素酸化物生成時に同時に生成する酸化物イオンが陽極21にまで移動できるように構成されており、陽極21は、生成した酸素ガスを陽極21の外部にまで排出することが可能であるように構成されており、陰極22は、窒素ガスを陰極22に接触する電解質23との界面(陰極−窒素ガス−電解質三相界面)にまで供給することが可能であるように構成されている。
【0084】
以上のように、窒素酸化物製造装置2において行われる電解窒素固定法は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極21と陰極22と、陽極21と陰極22とに接触する溶融塩からなる電解質23とを準備する。ステップ(a2)では、陰極22に窒素ガスを供給する。ステップ(a3)では、電解質23中に酸素ガスを供給する。ステップ(a4)では、陽極21と陰極22との間に、陰極22において窒素ガスが還元されて窒化物イオンが生成し、陽極21において酸化物イオンが酸化されて酸素が発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極22は、陰極22に供給された窒素ガスを電解質23にまで供給することが可能であるように構成されている。
【0085】
また、窒素酸化物製造装置2において行われる電解窒素固定法においては、ステップ(a5)は、電解質23を、ステップ(a3)によって酸素ガスが供給される位置を経て、陽極21まで流動させることによって行われる。
【0086】
なお、ステップ(a2)とステップ(a3)とステップ(a4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0087】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0088】
窒素酸化物製造装置2のその他の構成と効果は、窒素酸化物製造装置1(図1)と同様である。
【0089】
(第3実施形態)
図3に示すように、方法Bによって窒素酸化物を製造するための窒素酸化物製造装置3は、陽極(窒素極)31と、陰極(酸素極)32と、電解質33と、窒素ガス供給部34と、酸素ガス供給部35と、窒素酸化物ガス排出部36と、電源部37とを備える。
【0090】
陽極31と陰極32とは電解質33に接触するように、電解質33を介して互いに対向するように配置されている。すなわち、電解質33は陽極31と陰極32との間に挟まれている。陽極31も陰極32も多孔質体によって形成されている。陽極31と陰極32は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0091】
陽極31は、電解質33との界面にまで酸素を供給できるような形態であることが必要である。電解により陽極31に含まれる成分が溶出したり、生成する窒素酸化物によって変質して反応が進行しないようになったりしない限り、どのような材質であってもよい。電解質として溶融塩を含む場合には、ニッケルフェライトなどの導電性セラミクスや導電性ダイヤモンドが例示できる。この場合、方法Aと同じく、例えば酸化リチウムや酸化カルシウムなどの添加により酸化物イオンをあらかじめ電解質中に供給しておくことで電解初期においても陽極31反応が酸素発生となるようにする、などの措置を講じるのが好ましい。電解質として酸化物イオン伝導性の固体電解質を用いる場合には、例えば金属であればNiなどが利用できる。あるいは、上記のようにSOFC(Solid Oxide Fuel Cell、固体酸化物形燃料電池)で使用されるようなLa−Sr−MnO系や、La−Sr−CoO3系、Sm−Sr−CoO3系、(La,Sr)(Co,Fe)O3系などのMIEC(Mixed Ionic−Electronic Conductors、イオン・電子混合伝導体)などを利用することもできる。また、窒素酸化物の生成反応を促進させる目的で、PtやIr、Ru、Rh、Fe等の金属や化合物の触媒が担持されていてもよい。
【0092】
陰極32では、酸素ガスを還元して酸化物イオンを電解質33に供給する。従って、陰極32の材質は、酸素ガスを安定して還元できる金属や合金、化合物であればよく、例えば、SOFCで使用されるようなLa−Sr−MnO系や、La−Sr−CoO3系、Sm−Sr−CoO3系、(La,Sr)(Co,Fe)O3系などのMIECなどを利用することができる。また、電解質33との界面にまで酸素を供給するため、多孔質や金網状などのガス供給が可能な形態であることが必要である。また、純粋な酸素ガス以外にも、酸素を含む気体であって、酸素以外のガス成分の電気化学的な還元反応が進行しないのであれば使用でき、例えば乾燥空気などが例示できる。
【0093】
電解質33としては、酸化物イオンが安定に存在できる溶融塩や酸化物イオン伝導性の固体電解質を用いることができる。溶融塩としては、方法Aと同様の溶融塩が使用できる。酸化物イオン伝導性の固体電解質としては、具体的には、例えばSOFCで使用されるような、イットリア安定化ジルコニアやスカンジア安定化ジルコニアなどのジルコニア系セラミクスや、セリア系セラミクス、ランタンガレート系セラミクスなどが利用できる。
【0094】
窒素ガス供給部34には、窒素ガスが供給される。
【0095】
酸素ガス供給部35には、酸素ガスが供給される。酸素ガス供給部35には、純粋な酸素ではなく、乾燥空気など酸素を含む気体が供給されていてもよい。
【0096】
窒素酸化物ガス排出部36からは、窒素酸化物製造装置3で生成された窒素酸化物ガスが窒素酸化物製造装置3の外部に排出される。
【0097】
電源部37は、陰極32と陽極31との間に電圧を印加する。電源部37は、電源部37によって印加される電圧が、使用者によって制御されることが可能であるように構成されている。
【0098】
以上のように構成される窒素酸化物製造装置3の動作について説明する。
【0099】
窒素酸化物製造装置3においては、上述のように、陽極31と陰極32とが電解質33を挟むように配置されている。まず、窒素ガス供給部34に窒素ガスを供給することによって、陽極31に窒素ガスを接触させる。酸素ガス供給部35に酸素ガスを供給することによって、陰極32に酸素ガスを接触させる。次に、陽極31と陰極32との間に、陰極32において酸素が還元されて酸化物イオンが生成し、陽極31において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0100】
陰極32は、酸素ガスを供給するように形成されているので、酸素ガスは陰極32の内部を通って、陰極32と電解質33との界面に到達する。陰極32と電解質33との界面では、次の反応が起きて酸化物イオンが生成する。
【0101】
(1/2)n O2 + 2ne− → n
O2−
【0102】
生成した酸化物イオンは、電解質33中を移動して、陽極31に到達する。
【0103】
一方、陽極31は窒素ガスを供給するように形成されているので、窒素ガスは陽極31の内部を通って、陽極31と電解質33との界面に到達する。陽極31と電解質33との界面では、窒素ガスと、陰極32側から移動してきた酸化物イオンとの間で、次の反応が進行する。
【0104】
(B) 1/2 N2 + n O2− → NOn + 2n e−
【0105】
このようにして、窒素酸化物が生成される。生成した窒素酸化物は、陽極31を通過して、窒素酸化物ガス排出部36から排出される。
【0106】
作動温度としては、溶融塩が安定に利用できる温度領域、もしくは酸化物イオン伝導性が発現する温度領域で作動させれば特に制限はされない。上記のような固体酸化物電解質を使用する場合は、400〜1000℃、好ましくは500〜800℃で作動させるのがよい。
【0107】
陽極31と陰極32との間に印加する電圧については、浴組成作動温度などの条件に合わせて適宜調整すれば良い。例えば450℃の溶融LiCl−KClを用いる場合には、熱力学計算を参考にして、陽極電位がおよそ3V(vs.Li+/Li)よりも貴な電位領域となるように、陽極31と陰極32との間に印加する電圧を設定すれば良い。
【0108】
以上のように、窒素酸化物製造装置3において行われる電解窒素固定法は、次のステップ(b1)〜(b4)を含む。ステップ(b1)では、陽極31と陰極32と、陽極31と陰極32との間に挟むように配置された電解質33とを準備する。ステップ(b2)では、陽極31に窒素ガスを接触させる。ステップ(b3)では、陰極32に酸素ガスを接触させる。ステップ(b4)では、陽極31と陰極32との間に、陰極32において酸素が還元されて酸化物イオンが生成し、陽極31において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0109】
電解質33は、溶融塩または酸化物イオン伝導性の固体電解質であり、陰極32において酸素ガスを還元させることによって生成された酸化物イオンが陽極まで移動できるように構成されている。陽極31は、陽極31に接触した窒素ガスを電解質33にまで供給することが可能であるように構成されている。陰極32は、陰極32に接触した酸素ガスを電解質33にまで供給することが可能であるように構成されている。
【0110】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0111】
なお、ステップ(b2)とステップ(b3)とステップ(b4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0112】
窒素酸化物製造装置3においては、陽極31は、多孔質体によって形成されている。陽極31は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0113】
このようにすることにより、陽極31に接触した窒素ガスを電解質33にまで供給することが可能であるように陽極31を構成することができる。
【0114】
窒素酸化物製造装置3においては、陰極32は、多孔質体によって形成されている。陽極32は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0115】
このようにすることにより、陰極32に接触した酸素ガスを電解質33にまで供給することが可能であるように陰極32を構成することができる。
【実施例】
【0116】
(実施例1)
この発明の方法Aにおけるステップ(a2)〜(a4)では、陰極において窒素が還元されて窒化物イオンが生成し、陰極において陽極において酸化物イオンが酸化されて酸素が発生するが、これらの反応については、これまで発明者らが行ってきた溶融塩中での窒素ガスや酸素ガスの電極反応に関する研究成果などにより明らかとなっている。
【0117】
従って、この発明の方法Aによって窒素酸化物が生成されることは、ステップ(a5)において窒化物イオンと酸素とが反応して窒素酸化物が生成するNOn生成反応Aを示すことにより、確認することができる。
【0118】
方法AにおけるNOn生成反応Aを確認するための実施例として、次のような検討を行った。共融組成のLiCl−KClをAr雰囲気下の高純度アルミナ製坩堝内で450℃に保持し、N3−源として0.2mol%のLi3Nを添加したものを溶融塩として用いた。この溶融塩中に10vol%のO2を含むArガスを100cc・min−1でアルミナ管により吹き込み、溶融塩中のN3−と反応させた。所定時間経過後、生成したガスを回収し、NO及びNO2については北川式ガス検知管により生成ガスの評価を行った。表1は、サンプリングを行った時間(O2吹き込み開始後の経過時間)と、生成ガスとの関係を示す。
【0119】
【表1】

【0120】
溶融塩中にArのみを吹き込んでいる場合(表1ではblankと表記)ではNO及びNO2の生成は確認されなかった。溶融塩中へのO2吹き込み開始後すぐにNOの生成が確認されており、約1000秒経過後以降は、検知管の測定可能な濃度上限以上のNO及びNO2が確認された。この結果から、反応AによるNOn生成が確認されたので、既に公知である溶融塩中での窒素ガス陰極還元反応や陽極での酸素ガス発生反応と合わせ、方法Aによる電気化学的なNOn生成が確認できた。
【0121】
(実施例2)
この発明の方法Bにおけるステップ(b3)では、陰極において酸素が還元されて酸化物イオンが生成するが、この反応についてもこれまで発明者らが行ってきた溶融塩中での酸素ガスの電極挙動に関する研究成果により明らかとなっている。
【0122】
従って、この発明の方法Bによって窒素酸化物が生成されることは、ステップ(b2)および(b4)において陽極反応により酸化物イオンと窒素とから窒素酸化物を生成するNOn生成反応Bを示すことにより、確認することができる。
【0123】
方法BにおけるNOn生成反応Bを確認するための実施例として、次のような検討を行った。共融組成のLiCl−KClをAr雰囲気下の高純度アルミナ製坩堝内で450℃に保持し、O2−源として0.2mol%のLi2Oを添加したものを溶融塩として用いた。陽極には角棒状のニッケルフェライト(Ni0.75Fe2.25O4)を用い、これを石英製円筒内部に配置してセル内雰囲気と隔離しつつ溶融塩中に浸漬させ、この管内にN2ガスを100cc・min−1で供給した。陰極にはAl板を用い、電解時、Li+の陰極還元反応により生成するLiをAl−Li合金とすることで陰極内に保持させた。参照極にはAg+/Ag電極を用い、同電極電位はNi線電極上に析出させた金属Liの開回路電位(Li+/Li電位、以下同電位基準で表記する)で較正した。前記円筒内陽極へのN2供給を開始した後、陽極電位3.4Vで定電位電解を行った。電解時に陽極から発生したガスは、前記円筒内から外部へと取り出して回収し、実施例1と同じく、NO及びNO2については北川式ガス検知管により生成ガスの評価を行った。電解開始後すぐにサンプリングした場合ではNOnの生成は確認できなかったが、およそ2,000秒経過後にサンプリングを行ったところ、約5ppmのNOの生成が確認された。この結果から、反応BによるNOn生成が確認されたので、既に公知である溶融塩中での酸素ガス陰極還元反応と合わせ、方法Bによる電気化学的なNOn生成が確認できた。
【0124】
以上に開示された実施の形態はすべての点で例示であって制限的なものではないと考慮されるべきである。本発明の範囲は、以上の説明ではなく、特許請求の範囲によって示され、特許請求の範囲と均等の意味および範囲内でのすべての変形を含むものである。
【符号の説明】
【0125】
11,21,31:陽極、12,22,32:陰極、13,23,33:電解質。
【技術分野】
【0001】
本発明は、一般的には窒素固定法に関し、特定的には、窒素酸化物として窒素を固定する方法に関する。
【背景技術】
【0002】
窒素固定とは、空気中に多量に存在する窒素分子を、窒素化合物(アンモニア、窒素酸化物など)に変換するプロセスをいう。
【0003】
この窒素固定については、自然界では、例えばニトロゲナーゼを持つ菌類によってアンモニアが生成されることにより行われる。あるいは、雷の放電や紫外線により窒素酸化物が形成され、これが雨水に溶けることで硝酸となって土壌に固定される。
【0004】
人工的に合成される窒素化合物の最たる例がアンモニアである。20世紀初頭に、このアンモニアの製造を人工的に行う方法が開発され、それ以降、特に食糧増産(窒素肥料製造)の観点から、人類に多大な恩恵をもたらしてきた。その製造法はハーバー・ボッシュ法と呼ばれ、現在も全世界のアンモニア製造を担っている。このプロセスでは窒素と水素を触媒のもとで高温・高圧で反応させてアンモニアを合成する。しかしながら、現行のハーバー・ボッシュ法によるアンモニア製造では、水素を炭化水素の水蒸気改質によって得ており、この際に多量のCO2を排出する。地球温暖化ガスの代表例とされるCO2の排出が世界的に問題視されている現状に鑑みると、現行のアンモニア製造プロセスは、人工的な窒素固定法として、必ずしも優れたプロセスであるとは言い得なくなってきている。
【0005】
一方、窒素酸化物もまた(近年では、内燃機関からの排出ガスに含まれる大気汚染物質としての側面ばかりが注目されているが)、硝酸や窒素肥料を製造するために不可欠な物質である。純粋な窒素酸化物を得るために、現行の製造プロセスでは上記のアンモニアを原料としている。このプロセスでは、アンモニアを白金や白金ロジウム合金などの高価な触媒のもとで燃焼させて一酸化窒素を得た後、さらに常温で酸素と反応させて二酸化窒素を得る。ここで得られた二酸化窒素と水との反応を経て、硝酸が得られる。この硝酸の製造方法はオストワルト法と呼ばれており、現在も大量の硝酸が工業的に生産されている。
【0006】
また、例えば、特開昭58−162276号公報(特許文献1)には、窒素ガスと酸素ガスとの混合気体をプラズマ化して窒素酸化物を生成する方法が記載されている。
【0007】
また、例えば、特開平11−92120号公報(特許文献2)には、窒素ガスと酸素ガスから、フラーレンを触媒として光化学的に窒素酸化物を生成する方法が記載されている。
【0008】
また、例えば、特開2002−338214号公報(特許文献3)には、オゾンと窒素を原料として、窒素がオゾンにより酸化されることにより、亜酸化窒素を生成する亜酸化窒素の生成方法および製造装置が記載されている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開昭58−162276号公報
【特許文献2】特開平11−92120号公報
【特許文献3】特開2002−338214号公報
【発明の概要】
【発明が解決しようとする課題】
【0010】
しかしながら、オストワルト法においては、窒素酸化物を製造するための原料としてアンモニアを製造する必要がある。
【0011】
また、特許文献1に記載の方法ではプラズマ発生のための高価で複雑な装置が必要であり、また量産性にも乏しいことから、窒素酸化物を使った滅菌等に利用が限られていた。
【0012】
特許文献2に記載の方法では、窒素酸化物の生成速度が遅く、大量生産には向かないと考えられた。
【0013】
特許文献3に記載の方法では、窒素酸化物を得るために酸素からオゾンを製造する必要があった。
【0014】
そこで、この発明の目的は、アンモニアやオゾンなどを原料として利用するのではなく、窒素ガスと酸素ガスから直接的に窒素酸化物を生成し、量産化にも容易に対応できる方法を提供することである。
【課題を解決するための手段】
【0015】
本発明者らは、鋭意検討を重ねた結果、窒素ガスと酸素ガスを原料とし、電気化学反応を利用して窒素酸化物を生成する、窒素固定の新しいプロセスを見出すに至った。
【0016】
本発明では、窒化物イオンと酸素ガスを用いる方法(以下、方法Aとする)と、窒素ガスと酸化物イオンを用いる方法(以下、方法Bとする)の二つの方法を提供する。
【0017】
この発明の一つの局面に従った電解窒素固定法(方法A)は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極と陰極と、陽極と陰極とに接触する溶融塩からなる電解質とを準備する。ステップ(a2)では、陰極に窒素ガスを供給する。ステップ(a3)では、電解質中に酸素ガスを供給する。ステップ(a4)では、陽極と陰極との間に、陰極において窒素が還元されて窒化物イオンが生成し、陽極において酸化物イオンが酸化されて酸素が発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極は、陰極に供給された窒素ガスを電解質にまで供給することが可能であるように構成されている。
【0018】
電解質と接するように固定された陰極(窒素ガス陰極)では、窒素ガスが電気化学的に還元されて窒化物イオンが電解質中に供給される。
1/2 N2 + 3 e− → N3−
【0019】
窒化物イオンを含む電解質中に酸素ガスを供給することにより、窒化物イオンと酸素ガスは直接反応して窒素酸化物NOnを生成する(以下では、この反応を反応Aと表記する)。ここでNOnとはNO、NO2の他、N2O、N2O3、N2O4、N2O5などを指すものとする。
(反応A) N3− + (2n+3)/4 O2 → NOn + 3/2 O2−
【0020】
このNOn生成反応により生成する酸化物イオンは、同じく電解質と接するように配置された陽極上で酸化され、酸素ガスを発生する。
3/2 O2− → 3/4 O2 + 3 e−
【0021】
全反応式は次のようになり、窒素ガスと酸素ガスから窒素酸化物NOnが生成する。
1/2 N2 +n/2 O2 → NOn
【0022】
陽極で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして利用するのが好ましい。
【0023】
この発明に従った方法Aの電解窒素固定法においては、ステップ(a5)は、溶融塩を、陰極から、ステップ(a3)によって酸素ガスが供給される位置を経て、陽極まで流動させることによって行われることが好ましい。
【0024】
この発明に従った方法Aの電解窒素固定法においては、陰極は、多孔質体によって形成されていることが好ましい。
【0025】
このようにすることにより、窒素ガスを陰極と電解質との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極を構成することができる。なお、陰極は、必ずしも多孔質体でなくてもよい。
【0026】
この発明の別の局面に従った電解窒素固定法(方法B)は、次のステップ(b1)〜(b4)を含む。ステップ(b1)では、陽極と陰極と、陽極と陰極との間に配置された電解質とを準備する。ステップ(b2)では、陽極に窒素ガスを接触させる。ステップ(b3)では、陰極に酸素ガスを接触させる。ステップ(b4)では、陽極と陰極との間に、陰極において酸素ガスが還元されて酸化物イオンが生成し、陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0027】
電解質は、陰極において酸素ガスを還元させることによって生成された酸化物イオンが陽極まで移動できるように構成されている。陽極は、陽極に接触した窒素ガスを陽極と電解質との界面にまで供給することが可能であるように構成されている。陰極は、陰極に接触した酸素ガスを陰極と電解質との界面にまで供給することが可能であるように構成されている。
【0028】
このように、方法Bでは、溶融塩もしくは酸化物イオン導電性の固体電解質を電解質として用いることが好ましい。電解質と接するように固定された酸素ガス陰極では、酸素ガスが電気化学的に還元されて酸化物イオンが電解質中に供給される。
n/2 O2 + 2n e− → nO2−
【0029】
ここで生成された酸化物イオンは、窒素ガスが供給される陽極で酸化され、NOnを生成する(以下では、この反応を反応Bと表記する)。
(反応B) 1/2 N2 + nO2− → NOn + 2ne−
【0030】
全反応式は方法Aと同じになる。
1/2 N2 +n/2 O2 → NOn
【0031】
以上より、この発明によれば、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0032】
この発明に従った方法Bの電解窒素固定法においては、電解質は、溶融塩または酸化物イオン伝導性の固体電解質であることが好ましい。
【0033】
この発明に従った方法Bの電解窒素固定法においては、陽極は、多孔質体によって形成されていることが好ましい。
【0034】
このようにすることにより、窒素ガスを陽極と電解質との界面にまで供給することが可能であるように陽極を構成することができる。なお、陽極は、必ずしも多孔質体でなくてもよい。
【0035】
この発明に従った方法Bの電解窒素固定法においては、陰極は、多孔質体によって形成されていることが好ましい。
【0036】
このようにすることにより、酸素ガスを陰極と電解質との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極を構成することができる。なお、陰極は、必ずしも多孔質体でなくてもよい。
【発明の効果】
【0037】
以上のように、この発明によれば、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【図面の簡単な説明】
【0038】
【図1】本発明の第1実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
【図2】本発明の第2実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
【図3】本発明の第3実施形態の窒素酸化物の製造装置の全体の構成を模式的に示す図である。
【発明を実施するための形態】
【0039】
以下、本発明の実施の形態を図面に基づいて説明する。
【0040】
(第1実施形態)
図1に示すように、方法Aによって窒素酸化物を製造するための窒素酸化物製造装置1は、陽極11と、陰極12と、溶融塩からなる電解質13と、窒素ガス供給部14と、酸素ガス供給部15と、酸素ガス供給管151と、窒素酸化物ガス排出部16と、電源部17と、酸素ガス排出部18とを備える。
【0041】
陽極11と陰極12とは電解質13に接触するように、電解質13を介して互いに対向するように配置されている。すなわち、電解質13は陽極11と陰極12との間に挟まれている。陰極12において電解質13に接触する面と反対側の面には窒素ガス供給部14によって窒素ガスが供給される。電解質13内の酸素ガス供給部15には酸素ガス供給管151を通して電解質13の外部から酸素ガスが供給される。電解質13には、電解質13中の窒素酸化物を電解質13の外部に排出するための窒素酸化物ガス排出部16が接続されている。陽極11において電解質13に接触する面と反対側の面には酸素ガス排出部18が接続されている。電源部17は陽極11と陰極12との間に電圧を印加する。
【0042】
陽極11では、NOn生成時に同時に生成した酸化物イオンが酸化され酸素ガスが生成する。したがって、溶融塩電解で通常用いられる酸素発生陽極が利用でき、ニッケルフェライトなどの導電性セラミクスや導電性ダイヤモンドが例示できる。ただし、電解開始直後などの電解質中の酸化物イオンの濃度が低い場合、電解電流の大きさによっては、たとえばLiCl−KClなどの溶融塩化物を溶融塩として用いる場合では、陽極が損耗する可能性がある。そのため、陽極反応に応じて黒鉛やグラッシーカーボンなどの炭素電極を使う、もしくは酸化リチウムや酸化カルシウムなどの添加により酸化物イオンをあらかじめ電解質中に供給しておくことで電解初期においても陽極反応が酸素発生となるようにする、などの措置を講じるのが好ましい。
【0043】
陰極12では、窒素ガスを還元して窒化物イオンを電解質中に供給する。従って、陰極の材質は、窒素ガスを安定して還元できる金属や合金、化合物であればよい。例えば、ニッケルや鉄を含むものが好ましく、特にニッケルを含むものが好ましい。陰極の形状としては、電解質との界面にまで窒素を供給するため、MCFC(Molten Carbonate Fuel Cell、溶融炭酸塩形燃料電池)の電極に用いられるような多孔質、金網状、メッシュ状が好ましく、陰極の表面にPt、Ir、Ru等の触媒を担持してもよい。このようにNOnを生成するための窒化物イオンは陰極から供給されるが、あらかじめ電解質中にLi3Nなどの窒化物イオン源を添加しておくことで、電解初期においても窒化物イオンが酸素ガスとスムーズに反応することができる。
【0044】
電解質13としては、窒化物イオン及び酸化物イオンが安定に存在できる溶融塩を用いることができる。溶融塩としては、例えば、アルカリ金属ハロゲン化物およびアルカリ土類金属ハロゲン化物の少なくとも一種が挙げられる。アルカリ金属ハロゲン化物としては、例えば、LiF、NaF、KF、RbF、CsF、LiCl、NaCl、KCl、RbCl、CsCl、LiBr、NaBr、KBr、RbBr、CsBr、LiI、NaI、KI、RbI、CsI等が挙げられる。アルカリ土類金属ハロゲン化物としては、例えば、MgF2、CaF2、SrF2、BaF2、MgCl2、CaCl2、SrCl2、BaCl2、MgBr2、CaBr2、SrBr2、BaBr2、MgI2、CaI2、SrI2、BaI2等が挙げられる。これらの化合物は単独または二種以上を組み合わせて溶融塩として使用できる。化合物の組み合わせや混合比は限定的ではなく、目的毎に定められた溶融塩の作動温度等に応じて適宜設定すればよい。
【0045】
方法Aでは、電解質13は、酸化リチウムや酸化カルシウムなどのアルカリ金属酸化物やアルカリ土類金属酸化物を含むことが好ましい。このようにすることにより、電解質13中に酸化物イオンを供給することができるので、電解開始直後から陽極11では酸化物イオンが酸化されて酸素ガスが発生する。この場合、陽極11に炭素電極を用いると炭素が消耗するので、電解初期の段階からニッケルフェライトなどの不溶性酸素発生陽極を用いることが好ましい。
【0046】
以上のように構成される窒素酸化物製造装置1の動作について説明する。
【0047】
窒素酸化物製造装置1においては、上述のように、陽極11と陰極12とが電解質13を挟むように配置されている。まず、窒素ガス供給部14に窒素ガスを供給することによって、陰極12に窒素ガスを接触させる。次に、陽極11と陰極12との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。また、酸素ガス供給管151から酸素ガス供給部15に酸素ガスを供給することによって電解質13中に酸素ガスが供給される。
【0048】
陰極12は、窒素ガスを供給できるように形成されているので、窒素ガスは陰極12の内部を通って、陰極12と電解質13との界面に到達する。陰極12と電解質13との界面では、次の反応が起きて窒化物イオンが生成する。
【0049】
(1/2)N2+3e− → N3−
生成した窒化物イオンは、電解質13中を移動して、酸素供給部15に到達する。
【0050】
酸素供給部15では、酸素ガスと、陰極12側から移動してきた窒化物イオンとが接触し、次の反応によって窒素酸化物と酸化物イオンとが生成される。
【0051】
(反応A)N3−+(2n+3)/4 O2 → NOn+3/2 O2−
【0052】
生成した窒素酸化物は窒素酸化物ガス排出部16から電解質13の外部に取り出される。酸化物イオンは、陽極11側へ移動する。陽極11では、次の反応によって酸素ガスが発生する。
【0053】
3/2 O2− → 3/4 O2 +3e−
【0054】
陽極11で発生した酸素ガスは、酸素ガス排出部18から電解質13の外部に排出される。陽極11で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして、酸素ガス供給管151から電解質13へ供給するように利用するのが好ましい。
【0055】
作動温度は、電解質13である溶融塩が安定に利用できる温度領域で作動させれば特に制限はされない。
【0056】
陽極11と陰極12との間に印加する電圧については、浴組成や作動温度などの条件に合わせて適宜調整すれば良いが、例えば450℃の溶融LiCl−KClを電解質に用いる場合には、陰極での窒素ガス還元反応はおよそ0.5V(vs.Li+/Li:同浴中で金属Liの示す電位を基準とする)よりも卑な電位領域で進行し、陽極での酸素ガス発生反応はおよそ2.5V(vs.Li+/Li)よりも貴な電位で進行することから、およそ2.0Vよりも大きい電圧を印加すれば良い。
【0057】
以上のように、窒素酸化物製造装置1において行われる電解窒素固定法は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極11と陰極12と、陽極11と陰極12とに接触する溶融塩からなる電解質13とを準備する。ステップ(a2)では、陰極12に窒素ガスを供給する。ステップ(a3)では、電解質13中に酸素ガスを供給する。ステップ(a4)では、陽極11と陰極12との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極12は、陰極12に供給された窒素ガスを電解質13にまで供給することが可能であるように構成されている。
【0058】
なお、ステップ(a2)とステップ(a3)とステップ(a4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0059】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0060】
また、窒素酸化物製造装置1においては、陰極12は、多孔質体によって形成されている。陰極12は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0061】
このようにすることにより、窒素ガスを陰極12と電解質13との界面にまで供給することが可能であり、かつ、反応面積を大きくするように陰極12を構成することができる。
【0062】
ここで、方法Aによって窒素酸化物を合成する場合、例えば、陰極12で生成した窒化物イオンが、NOn生成部(酸素ガス供給部15)で消費しきれず未反応のまま陽極11に達した場合には、次式のように陽極11で酸化されて窒素ガスとなり、陽極11での酸素発生の電流分担率を低下させることになる。
N3− → 1/2 N2 + 3e−
【0063】
あるいは電解質13中に供給される酸素ガスが、未反応のまま陰極12に達した場合にも、例えば次に示すように陰極12で還元されて酸化物イオンを生成し、陰極12での窒素還元反応の電流分担率を低下させる。
3/2 O2 + 2 e− → O2−
【0064】
そのため、方法Aでは、陰極12で生成した窒化物イオンが全てNOn生成部(酸素ガス供給部15)へ供給され、またNOn生成部(酸素ガス供給部15)で生成した酸化物イオンが全て陽極11へ供給され、そして確実に消費される必要がある。そこで、電解質13である溶融塩を、電解槽内でループ状に循環させて、この溶融塩の循環に沿って、陰極12、NOn生成部(酸素ガス供給部15)、陽極11を配置するのが好ましい。このようにすることで、陰極12で生成した窒化物イオンを全てNOn生成部(酸素ガス供給部15)へ供給し、かつ、NOn生成部(酸素ガス供給部15)で生成した酸化物イオンを全て陽極11へ供給することができる。
【0065】
そこで、以下に、電解質をループ状に循環・流動させるように構成された窒素酸化物製造装置を用いて、方法Aによって窒素酸化物を製造する実施形態を説明する。
【0066】
(第2実施形態)
図2に示すように、第1実施形態の窒素酸化物製造装置1のより好ましい実施形態として、窒素酸化物製造装置2は、陽極21と、陰極22と、電解槽20と、電解槽20内に収容される、溶融塩からなる電解質23と、窒素ガス供給管24と、酸素ガス供給部25と酸素ガス供給管251と、窒素酸化物ガス排出部26と、電源部27と、酸素排出部28と、不活性ガス供給部29とを備える。陰極22は多孔質体によって形成されている。陰極22は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はなく、第1実施形態で述べたように、例えば、金網状、メッシュ状に形成されていてもよい。
【0067】
電解槽20は、この実施形態においては、鉛直方向に延びる第1流路201と第2流路202と、水平方向に延びる第3流路203と第4流路204とから構成されている。第1流路201と第2流路202とは、上部において第3流路203によって連結され、下部において第4流路204によって連結されている。
【0068】
電解槽20の内部の流路はまた、1つの流路が鉛直面内で円周形状に形成されているものなど、ループ状であればどのような形態であってもよく、必ず4つの流路が必要というわけではない。
【0069】
陽極21は、電解槽20の第3流路203内に配置される。陽極21では、NOn生成時に同時に生成した酸化物イオンが酸化され酸素ガスが生成する。陰極22は、電解槽20の第1流路201の上部に配置される。陰極22では、窒素ガスを還元して窒化物イオンを電解質中に供給する。窒素ガス供給管24は、電解槽20の外部から陰極22に窒素ガスを供給する。
【0070】
陽極21、陰極22、電解質23の構成や作動温度については、図1を用いて説明した通りである。
【0071】
電解質23の第2流路202中の下部の酸素ガス供給部25には、電解槽20の外部から、酸素ガス供給管251を通して酸素ガスが供給される。電解質中の窒化物イオンと酸素ガスとの反応は気液反応であることから、石英ガラス製や高純度アルミナ製などの多孔質ガス供給部を含むガス供給管などを利用して供給する場合には、供給される酸素ガスの気泡サイズを小さくする方が、反応がスムーズに進行するので好ましい。また、Ni製などの金属製の供給管や、上記のガラス製やアルミナ製の供給管に、触媒を担持した充填材を保持することなどは、触媒効果により電解質中の窒化物イオンと酸素ガスとの反応を促進させ得るので、より好ましい。
【0072】
第2流路202の上部の窒素酸化物ガス排出部26からは、窒素酸化物製造装置2で生成された窒素酸化物ガスが窒素酸化物製造装置2の外部に排出される。電源部27は、陽極21と陰極22との間に電圧を印加する。電源部27は、電源部27によって印加される電圧が、使用者によって制御されることが可能であるように構成されている。電解槽20の第3流路203の上部の酸素排出部28からは、電解槽20内で発生した酸素が電解槽20の外部に排出される。第2流路202の底部の不活性ガス供給部29は、図中に矢印Pで示すように、電解槽20の底部から電解質23中にアルゴン等の不活性ガスを供給する。
【0073】
以上のように構成される窒素酸化物製造装置2の動作について説明する。
【0074】
窒素酸化物製造装置2においては、上述のように、陽極21と陰極22とが電解質23に接触するように配置されている。まず、酸素ガス供給管251から酸素ガス供給部25に酸素ガスを供給することによって電解質23中に酸素ガスが供給される。窒素ガス供給管24に窒素ガスを供給することによって、陰極22に窒素ガスを接触させる。次に、陽極21と陰極22との間に、陰極12において窒素ガスが還元されて窒化物イオンが生成し、陽極11において酸化物イオンが酸化されて酸素ガスが発生する電圧を印加する。
【0075】
陰極22は、窒素ガスを供給できるように形成されているので、窒素ガスは陰極22の内部を通って、陰極22と電解質23との界面に到達する。陰極22と電解質23との界面では、次の反応が起きて窒化物イオンが生成する。
【0076】
(1/2)N2+3e− → N3−
【0077】
電解質23には、底部の不活性ガス供給部29から不活性ガスが供給されている。このようにすることにより、ガスリフトによって電解質23の第2流路202内に上昇流が生じ、溶融塩が電解槽20のループ内を循環・流動される。溶融塩の流動には、プロペラ等を用いた機械的な方法を用いてもよいが、酸素ガスや不活性ガスの供給を利用したガスリフトを用いる方が、機械的な駆動部が不要であり、装置構成が単純になるので好ましい。生成した窒化物イオンは、図中に矢印Qで示す方向に移動して、第1流路201、第4流路204を通って、酸素ガス供給部25に到達する。
【0078】
酸素ガス供給部25では、酸素ガスと、陰極22側から移動してきた窒化物イオンとが接触し、次の反応によって窒素酸化物と酸化物イオンとが生成される。
【0079】
(反応A)N3−+(2n+3)/4 O2 → NOn+3/2 O2−
【0080】
生成した窒素酸化物と酸化物イオンとは、ガスリフトによって第2流路202内を下から上へ移動する。窒素酸化物は、第2流路202の上部の窒素酸化物ガス排出部26から電解槽20の外部に取り出される。酸化物イオンは、図中に矢印Rで示すように第2流路202内から第3流路203へ移動して、陽極21に到達する。陽極21では、次の反応によって酸素ガスが発生する。
【0081】
3/2 O2− → 3/4 O2 +3e−
【0082】
陽極21で発生した酸素ガスは、第3流路203の上部の酸素排出部28から電解槽20の外部に排出される。陽極21で発生した酸素ガスは、回収して再度NOn生成のための原料ガスとして、酸素ガス供給管251から電解質23へ供給するように利用するのが好ましい。
【0083】
このように、電解質23は、陰極22において窒素ガスを還元させることによって生成された窒化物イオンが酸素ガス供給部25にまで移動できるように、かつ、酸素ガス供給部25において窒素酸化物生成時に同時に生成する酸化物イオンが陽極21にまで移動できるように構成されており、陽極21は、生成した酸素ガスを陽極21の外部にまで排出することが可能であるように構成されており、陰極22は、窒素ガスを陰極22に接触する電解質23との界面(陰極−窒素ガス−電解質三相界面)にまで供給することが可能であるように構成されている。
【0084】
以上のように、窒素酸化物製造装置2において行われる電解窒素固定法は、次のステップ(a1)〜(a5)を含む。ステップ(a1)では、陽極21と陰極22と、陽極21と陰極22とに接触する溶融塩からなる電解質23とを準備する。ステップ(a2)では、陰極22に窒素ガスを供給する。ステップ(a3)では、電解質23中に酸素ガスを供給する。ステップ(a4)では、陽極21と陰極22との間に、陰極22において窒素ガスが還元されて窒化物イオンが生成し、陽極21において酸化物イオンが酸化されて酸素が発生する電圧を印加する。ステップ(a5)では、ステップ(a4)で生成される窒化物イオンとステップ(a3)で供給される酸素とを接触させる。陰極22は、陰極22に供給された窒素ガスを電解質23にまで供給することが可能であるように構成されている。
【0085】
また、窒素酸化物製造装置2において行われる電解窒素固定法においては、ステップ(a5)は、電解質23を、ステップ(a3)によって酸素ガスが供給される位置を経て、陽極21まで流動させることによって行われる。
【0086】
なお、ステップ(a2)とステップ(a3)とステップ(a4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0087】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0088】
窒素酸化物製造装置2のその他の構成と効果は、窒素酸化物製造装置1(図1)と同様である。
【0089】
(第3実施形態)
図3に示すように、方法Bによって窒素酸化物を製造するための窒素酸化物製造装置3は、陽極(窒素極)31と、陰極(酸素極)32と、電解質33と、窒素ガス供給部34と、酸素ガス供給部35と、窒素酸化物ガス排出部36と、電源部37とを備える。
【0090】
陽極31と陰極32とは電解質33に接触するように、電解質33を介して互いに対向するように配置されている。すなわち、電解質33は陽極31と陰極32との間に挟まれている。陽極31も陰極32も多孔質体によって形成されている。陽極31と陰極32は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0091】
陽極31は、電解質33との界面にまで酸素を供給できるような形態であることが必要である。電解により陽極31に含まれる成分が溶出したり、生成する窒素酸化物によって変質して反応が進行しないようになったりしない限り、どのような材質であってもよい。電解質として溶融塩を含む場合には、ニッケルフェライトなどの導電性セラミクスや導電性ダイヤモンドが例示できる。この場合、方法Aと同じく、例えば酸化リチウムや酸化カルシウムなどの添加により酸化物イオンをあらかじめ電解質中に供給しておくことで電解初期においても陽極31反応が酸素発生となるようにする、などの措置を講じるのが好ましい。電解質として酸化物イオン伝導性の固体電解質を用いる場合には、例えば金属であればNiなどが利用できる。あるいは、上記のようにSOFC(Solid Oxide Fuel Cell、固体酸化物形燃料電池)で使用されるようなLa−Sr−MnO系や、La−Sr−CoO3系、Sm−Sr−CoO3系、(La,Sr)(Co,Fe)O3系などのMIEC(Mixed Ionic−Electronic Conductors、イオン・電子混合伝導体)などを利用することもできる。また、窒素酸化物の生成反応を促進させる目的で、PtやIr、Ru、Rh、Fe等の金属や化合物の触媒が担持されていてもよい。
【0092】
陰極32では、酸素ガスを還元して酸化物イオンを電解質33に供給する。従って、陰極32の材質は、酸素ガスを安定して還元できる金属や合金、化合物であればよく、例えば、SOFCで使用されるようなLa−Sr−MnO系や、La−Sr−CoO3系、Sm−Sr−CoO3系、(La,Sr)(Co,Fe)O3系などのMIECなどを利用することができる。また、電解質33との界面にまで酸素を供給するため、多孔質や金網状などのガス供給が可能な形態であることが必要である。また、純粋な酸素ガス以外にも、酸素を含む気体であって、酸素以外のガス成分の電気化学的な還元反応が進行しないのであれば使用でき、例えば乾燥空気などが例示できる。
【0093】
電解質33としては、酸化物イオンが安定に存在できる溶融塩や酸化物イオン伝導性の固体電解質を用いることができる。溶融塩としては、方法Aと同様の溶融塩が使用できる。酸化物イオン伝導性の固体電解質としては、具体的には、例えばSOFCで使用されるような、イットリア安定化ジルコニアやスカンジア安定化ジルコニアなどのジルコニア系セラミクスや、セリア系セラミクス、ランタンガレート系セラミクスなどが利用できる。
【0094】
窒素ガス供給部34には、窒素ガスが供給される。
【0095】
酸素ガス供給部35には、酸素ガスが供給される。酸素ガス供給部35には、純粋な酸素ではなく、乾燥空気など酸素を含む気体が供給されていてもよい。
【0096】
窒素酸化物ガス排出部36からは、窒素酸化物製造装置3で生成された窒素酸化物ガスが窒素酸化物製造装置3の外部に排出される。
【0097】
電源部37は、陰極32と陽極31との間に電圧を印加する。電源部37は、電源部37によって印加される電圧が、使用者によって制御されることが可能であるように構成されている。
【0098】
以上のように構成される窒素酸化物製造装置3の動作について説明する。
【0099】
窒素酸化物製造装置3においては、上述のように、陽極31と陰極32とが電解質33を挟むように配置されている。まず、窒素ガス供給部34に窒素ガスを供給することによって、陽極31に窒素ガスを接触させる。酸素ガス供給部35に酸素ガスを供給することによって、陰極32に酸素ガスを接触させる。次に、陽極31と陰極32との間に、陰極32において酸素が還元されて酸化物イオンが生成し、陽極31において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0100】
陰極32は、酸素ガスを供給するように形成されているので、酸素ガスは陰極32の内部を通って、陰極32と電解質33との界面に到達する。陰極32と電解質33との界面では、次の反応が起きて酸化物イオンが生成する。
【0101】
(1/2)n O2 + 2ne− → n
O2−
【0102】
生成した酸化物イオンは、電解質33中を移動して、陽極31に到達する。
【0103】
一方、陽極31は窒素ガスを供給するように形成されているので、窒素ガスは陽極31の内部を通って、陽極31と電解質33との界面に到達する。陽極31と電解質33との界面では、窒素ガスと、陰極32側から移動してきた酸化物イオンとの間で、次の反応が進行する。
【0104】
(B) 1/2 N2 + n O2− → NOn + 2n e−
【0105】
このようにして、窒素酸化物が生成される。生成した窒素酸化物は、陽極31を通過して、窒素酸化物ガス排出部36から排出される。
【0106】
作動温度としては、溶融塩が安定に利用できる温度領域、もしくは酸化物イオン伝導性が発現する温度領域で作動させれば特に制限はされない。上記のような固体酸化物電解質を使用する場合は、400〜1000℃、好ましくは500〜800℃で作動させるのがよい。
【0107】
陽極31と陰極32との間に印加する電圧については、浴組成作動温度などの条件に合わせて適宜調整すれば良い。例えば450℃の溶融LiCl−KClを用いる場合には、熱力学計算を参考にして、陽極電位がおよそ3V(vs.Li+/Li)よりも貴な電位領域となるように、陽極31と陰極32との間に印加する電圧を設定すれば良い。
【0108】
以上のように、窒素酸化物製造装置3において行われる電解窒素固定法は、次のステップ(b1)〜(b4)を含む。ステップ(b1)では、陽極31と陰極32と、陽極31と陰極32との間に挟むように配置された電解質33とを準備する。ステップ(b2)では、陽極31に窒素ガスを接触させる。ステップ(b3)では、陰極32に酸素ガスを接触させる。ステップ(b4)では、陽極31と陰極32との間に、陰極32において酸素が還元されて酸化物イオンが生成し、陽極31において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加する。
【0109】
電解質33は、溶融塩または酸化物イオン伝導性の固体電解質であり、陰極32において酸素ガスを還元させることによって生成された酸化物イオンが陽極まで移動できるように構成されている。陽極31は、陽極31に接触した窒素ガスを電解質33にまで供給することが可能であるように構成されている。陰極32は、陰極32に接触した酸素ガスを電解質33にまで供給することが可能であるように構成されている。
【0110】
このようにすることにより、窒素ガスと酸素ガスから直接的に窒素酸化物を生成する方法を提供することができる。
【0111】
なお、ステップ(b2)とステップ(b3)とステップ(b4)とは同時に行われてもよいし、いずれか一つが先に行われてもよい。
【0112】
窒素酸化物製造装置3においては、陽極31は、多孔質体によって形成されている。陽極31は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0113】
このようにすることにより、陽極31に接触した窒素ガスを電解質33にまで供給することが可能であるように陽極31を構成することができる。
【0114】
窒素酸化物製造装置3においては、陰極32は、多孔質体によって形成されている。陽極32は、ガス供給が可能な形態であれば、必ずしも多孔質である必要はない。
【0115】
このようにすることにより、陰極32に接触した酸素ガスを電解質33にまで供給することが可能であるように陰極32を構成することができる。
【実施例】
【0116】
(実施例1)
この発明の方法Aにおけるステップ(a2)〜(a4)では、陰極において窒素が還元されて窒化物イオンが生成し、陰極において陽極において酸化物イオンが酸化されて酸素が発生するが、これらの反応については、これまで発明者らが行ってきた溶融塩中での窒素ガスや酸素ガスの電極反応に関する研究成果などにより明らかとなっている。
【0117】
従って、この発明の方法Aによって窒素酸化物が生成されることは、ステップ(a5)において窒化物イオンと酸素とが反応して窒素酸化物が生成するNOn生成反応Aを示すことにより、確認することができる。
【0118】
方法AにおけるNOn生成反応Aを確認するための実施例として、次のような検討を行った。共融組成のLiCl−KClをAr雰囲気下の高純度アルミナ製坩堝内で450℃に保持し、N3−源として0.2mol%のLi3Nを添加したものを溶融塩として用いた。この溶融塩中に10vol%のO2を含むArガスを100cc・min−1でアルミナ管により吹き込み、溶融塩中のN3−と反応させた。所定時間経過後、生成したガスを回収し、NO及びNO2については北川式ガス検知管により生成ガスの評価を行った。表1は、サンプリングを行った時間(O2吹き込み開始後の経過時間)と、生成ガスとの関係を示す。
【0119】
【表1】

【0120】
溶融塩中にArのみを吹き込んでいる場合(表1ではblankと表記)ではNO及びNO2の生成は確認されなかった。溶融塩中へのO2吹き込み開始後すぐにNOの生成が確認されており、約1000秒経過後以降は、検知管の測定可能な濃度上限以上のNO及びNO2が確認された。この結果から、反応AによるNOn生成が確認されたので、既に公知である溶融塩中での窒素ガス陰極還元反応や陽極での酸素ガス発生反応と合わせ、方法Aによる電気化学的なNOn生成が確認できた。
【0121】
(実施例2)
この発明の方法Bにおけるステップ(b3)では、陰極において酸素が還元されて酸化物イオンが生成するが、この反応についてもこれまで発明者らが行ってきた溶融塩中での酸素ガスの電極挙動に関する研究成果により明らかとなっている。
【0122】
従って、この発明の方法Bによって窒素酸化物が生成されることは、ステップ(b2)および(b4)において陽極反応により酸化物イオンと窒素とから窒素酸化物を生成するNOn生成反応Bを示すことにより、確認することができる。
【0123】
方法BにおけるNOn生成反応Bを確認するための実施例として、次のような検討を行った。共融組成のLiCl−KClをAr雰囲気下の高純度アルミナ製坩堝内で450℃に保持し、O2−源として0.2mol%のLi2Oを添加したものを溶融塩として用いた。陽極には角棒状のニッケルフェライト(Ni0.75Fe2.25O4)を用い、これを石英製円筒内部に配置してセル内雰囲気と隔離しつつ溶融塩中に浸漬させ、この管内にN2ガスを100cc・min−1で供給した。陰極にはAl板を用い、電解時、Li+の陰極還元反応により生成するLiをAl−Li合金とすることで陰極内に保持させた。参照極にはAg+/Ag電極を用い、同電極電位はNi線電極上に析出させた金属Liの開回路電位(Li+/Li電位、以下同電位基準で表記する)で較正した。前記円筒内陽極へのN2供給を開始した後、陽極電位3.4Vで定電位電解を行った。電解時に陽極から発生したガスは、前記円筒内から外部へと取り出して回収し、実施例1と同じく、NO及びNO2については北川式ガス検知管により生成ガスの評価を行った。電解開始後すぐにサンプリングした場合ではNOnの生成は確認できなかったが、およそ2,000秒経過後にサンプリングを行ったところ、約5ppmのNOの生成が確認された。この結果から、反応BによるNOn生成が確認されたので、既に公知である溶融塩中での酸素ガス陰極還元反応と合わせ、方法Bによる電気化学的なNOn生成が確認できた。
【0124】
以上に開示された実施の形態はすべての点で例示であって制限的なものではないと考慮されるべきである。本発明の範囲は、以上の説明ではなく、特許請求の範囲によって示され、特許請求の範囲と均等の意味および範囲内でのすべての変形を含むものである。
【符号の説明】
【0125】
11,21,31:陽極、12,22,32:陰極、13,23,33:電解質。
【特許請求の範囲】
【請求項1】
陽極と陰極と、陽極と陰極とに接触する溶融塩からなる電解質とを準備するステップ(a1)と、
前記陰極に窒素ガスを供給するステップ(a2)と、
前記電解質中に酸素ガスを供給するステップ(a3)と、
前記陽極と前記陰極との間に、前記陰極において窒素が還元されて窒化物イオンが生成し、前記陽極において酸化物イオンが酸化されて酸素が発生する電圧を印加するステップ(a4)と、
前記ステップ(a4)で生成される窒化物イオンと前記ステップ(a3)で供給される酸素とを接触させるステップ(a5)とを含み、
前記陰極は、前記陰極に供給された前記窒素ガスを前記電解質にまで供給することが可能であるように構成されている、電解窒素固定法。
【請求項2】
前記ステップ(a5)は、前記溶融塩を、前記陰極から、前記ステップ(a3)によって酸素ガスが供給される位置を経て、前記陽極まで流動させることによって行われる、請求項1に記載の電解窒素固定法。
【請求項3】
陽極と陰極と、前記陽極と前記陰極との間に配置された電解質とを準備するステップ(b1)と、
前記陽極に窒素ガスを接触させるステップ(b2)と、
前記陰極に酸素ガスを接触させるステップ(b3)と、
前記陽極と前記陰極との間に、前記陰極において前記酸素ガスが還元されて酸化物イオンが生成し、前記陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加するステップ(b4)とを含み、
前記電解質は、前記陰極において前記酸素ガスを還元させることによって生成された酸化物イオンが陽極にまで移動できるように構成されており、
前記陽極は、前記陽極に接触した前記窒素ガスを前記電解質との界面にまで供給することが可能であるように構成されており、
前記陰極は、前記陰極に接触した前記酸素ガスを前記電解質との界面にまで供給することが可能であるように構成されている、電解窒素固定法。
【請求項4】
前記電解質は溶融塩または酸化物イオン伝導性の固体電解質である、請求項3に記載の電解窒素固定法。
【請求項5】
前記陽極は、多孔質体によって形成されている、請求項3または請求項4に記載の電解窒素固定法。
【請求項6】
前記陰極は、多孔質体によって形成されている、請求項1から請求項5までのいずれか1項に記載の電解窒素固定法。
【請求項1】
陽極と陰極と、陽極と陰極とに接触する溶融塩からなる電解質とを準備するステップ(a1)と、
前記陰極に窒素ガスを供給するステップ(a2)と、
前記電解質中に酸素ガスを供給するステップ(a3)と、
前記陽極と前記陰極との間に、前記陰極において窒素が還元されて窒化物イオンが生成し、前記陽極において酸化物イオンが酸化されて酸素が発生する電圧を印加するステップ(a4)と、
前記ステップ(a4)で生成される窒化物イオンと前記ステップ(a3)で供給される酸素とを接触させるステップ(a5)とを含み、
前記陰極は、前記陰極に供給された前記窒素ガスを前記電解質にまで供給することが可能であるように構成されている、電解窒素固定法。
【請求項2】
前記ステップ(a5)は、前記溶融塩を、前記陰極から、前記ステップ(a3)によって酸素ガスが供給される位置を経て、前記陽極まで流動させることによって行われる、請求項1に記載の電解窒素固定法。
【請求項3】
陽極と陰極と、前記陽極と前記陰極との間に配置された電解質とを準備するステップ(b1)と、
前記陽極に窒素ガスを接触させるステップ(b2)と、
前記陰極に酸素ガスを接触させるステップ(b3)と、
前記陽極と前記陰極との間に、前記陰極において前記酸素ガスが還元されて酸化物イオンが生成し、前記陽極において酸化物イオンが酸化されて窒素酸化物が生成する電圧を印加するステップ(b4)とを含み、
前記電解質は、前記陰極において前記酸素ガスを還元させることによって生成された酸化物イオンが陽極にまで移動できるように構成されており、
前記陽極は、前記陽極に接触した前記窒素ガスを前記電解質との界面にまで供給することが可能であるように構成されており、
前記陰極は、前記陰極に接触した前記酸素ガスを前記電解質との界面にまで供給することが可能であるように構成されている、電解窒素固定法。
【請求項4】
前記電解質は溶融塩または酸化物イオン伝導性の固体電解質である、請求項3に記載の電解窒素固定法。
【請求項5】
前記陽極は、多孔質体によって形成されている、請求項3または請求項4に記載の電解窒素固定法。
【請求項6】
前記陰極は、多孔質体によって形成されている、請求項1から請求項5までのいずれか1項に記載の電解窒素固定法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2013−95961(P2013−95961A)
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願番号】特願2011−239478(P2011−239478)
【出願日】平成23年10月31日(2011.10.31)
【出願人】(506360310)アイ’エムセップ株式会社 (17)
【Fターム(参考)】
【公開日】平成25年5月20日(2013.5.20)
【国際特許分類】
【出願日】平成23年10月31日(2011.10.31)
【出願人】(506360310)アイ’エムセップ株式会社 (17)
【Fターム(参考)】
[ Back to top ]

