非常に高い皮膚浸透率を有するプロスタグランジン及び関連化合物の正荷電水溶性プロドラッグ
構造(2)で表される、プロスタグランジン、プロスタサイクリン、及び関連化合物の新規な正荷電プロドラッグを合成した。これらのプロドラッグの正に荷電されたアミノ基は、薬物の水中での溶解性を大いに増大させるだけでなく、膜のホスファート頭基上の負電荷と結合し、プロドラッグを細胞質ゾルの中に押し込む。プロドラッグは、プロスタグランジン、プロスタサイクリン、及び関連化合物よりも〜1000倍速く、人の皮膚を通して拡散する。血漿中、数分で、90%を超えるこれらのプロドラッグが変化して親薬物に戻り得る。プロドラッグは、人又は動物における、プロスタグランジン、プロスタサイクリン、及び関連化合物治療可能な状態の治療に医薬的に使用され得る。プロドラッグは、種々の薬物治療のために経皮投与され得、プロスタグランジン、プロスタサイクリン、及び関連化合物のたいていの副作用を回避し得る。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の正に荷電された水溶性プロドラッグの調製剤、並びに人又は動物において、プロスタグランジン、プロスタサイクリン、及び関連化合物治療可能な状態を治療する際のその医薬用途に関する。より具体的に言うと、本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の迅速な皮膚浸透を可能にするためにある。
【背景技術】
【0002】
天然のプロスタグランジン及びプロスタサイクリンは、膜リン脂質に由来するオータコイドのグループのうちの一つである、エイコサノイドの分類に属する。これらは、本質的に身体のどの領域でも見出される。プロスタグランジンの一般的な構造は構造1で示される。
【化1】

【0003】
全ての天然プロスタグランジンは、15α−ヒドロキシ基及びC−13でのトランス二重結合を有する(William O. Foyeなど、Principles of Medicinal Chemistry, fourth edition, Williams及びWilkins, 1995, pg 538)。カルボキシルを有する鎖はアルファ鎖と呼ばれ、ヒドロキシルを有する鎖はオメガ鎖と呼ばれる。プロスタグランジン(PG)は、9−及び11−位での酸素置換基の性質並びに立体化学に依存して、大文字A、B、C、D、E、F、G、H及びIにより分類される。様々なプロスタグランジンの作用は多種多様である。膣内に投与されると、PGE2は、妊娠子宮の子宮内膜を刺激して、分娩中に観察される子宮収縮と同じように収縮させるだろう。従って、PGE2は、堕胎薬として使用することを目的としたジノプロストン(プロスチンE2、Upjohn)として治療上利用できる。PGE2はまた、消化(GI)管平滑筋の有効な刺激剤であり、ほとんどの血管組織において有効な血管拡張作用を有し、特定の部位では収縮作用をまた有することに加えて、体温を上げ得る。PGF2αは、多くのPGEの作用を共有し、また堕胎薬として治療上利用できる(プロスチンF2アルファ、Upjohn)。PGF2αの合成15−メチル誘導体、カルボプロストもまた、堕胎薬として治療上利用できる(プロスチン15/M、Upjohn)。PGD2は、血管拡張と血管収縮の両方を引き起こす。PGEは、気管支及び気管平滑筋の弛緩をもたらす一方、PGF及びPGD2は収縮を引き起こす。PGE1は、先天性心疾患を治療するために手術が行われ得るまで、アルプロスタジルとして、新生児において動脈管の能力を維持するために利用できる。PGE1及びその類似体は、男性の勃起不全の治療のため(Yeager, James L. 米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, Nathan Earl, 米国特許第6,291,528号明細書)に使用されてもよい。プロスタグランジン類似体は、眼圧を調節することに対する安全性及び有効性が証明された緑内障薬の主要な分類である。それらは、ビマトプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[1E,3S]−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−5−N−エチルヘプテンアミド}、ラタノプロスト(13,14−ジヒドロ−17−フェニル−18,19,20−トリノルPGF2αイソプロピルエステル)、トラボプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル]−5−ヘプテノアート}、及びウノプロストン(13,14−ジヒドロ−15−ケト−20−エチルPGF2α)を含む。
【0004】
残念ながら、プロスタグランジン、プロスタサイクリン、及び関連化合物は、様々な酸化的及び還元的経路によって急速に代謝され、不活性化される。プロスタグランジンを経口的に服用すると、肝臓及び消化管での化合物の化学分解に言及する初回通過代謝によって、プロスタグランジンは数秒で破壊され、不活性化され得る。注射によりプロスタグランジンを投与する場合、有痛性であり、多くの場合、慢性症状を治療するために頻繁で金のかかる来院が必要とされ、かつほとんどのプロスタグランジン、プロスタサイクリン、及び関連化合物は、意図した作用部位に到達する前に血中及び肝臓で破壊され、不活性化され得る。
【0005】
薬物を投与する一代替方法は、局所的な送達である。局所的な薬物送達はいくつかの利点を有する。この方法は、肝臓及び消化管での初回通過代謝により引き起こされる薬物の不活性化を回避するのに役立つ。それは、全身に曝露されることなく、意図した作用部位に、適切な濃度の薬物の局所的な送達を供給し得る。Fishman(Fishman; Robert, 米国特許第7,052,715号明細書)は、経口薬物治療と関連した追加的な課題を指摘した。それは、疼痛又は炎症のある末端部を効果的に治療するためには、血流中で達成されなければならない濃度レベルが、有意でなければならないということである。これらのレベルはしばしば、疼痛又は損傷のある特定部位を正確に標的とすることが可能である場合に必要となるレベルよりもずっと高い。Yeagerは、男性の勃起不全の治療を目的にPGE1を送達するため、浸透エンハンサーを使用することを試みた(Yeager, James L. 米国特許第6,693,135号明細書)。Susan Milosovichらは、テストステロニル−4−ジメチルアミノブチラート塩酸塩(testosteronyl-4-dimethylaminobutyrate.HCl)(TSBH)を設計し、調製した。これは、親油性部分及び生理学的pHではプロトン化された形態で存在する第3級アミン基を有する。彼らは、プロドラッグ(TSBH)は、薬物(TS)それ自体よりも〜60倍速く人の皮膚を通して拡散することを見出した[Susan Milosovichなど、J. Pharm. Sci., 82,227(1993)]。
【発明の概要】
【発明が解決しようとする課題】
【0006】
様々なプロスタグランジンの作用は多種多様である。プロスタグランジンは多くの医薬用途を有する。PGE2及びPGF2αは治療上利用できる。PGF2αの合成15−メチル誘導体、カルボプロストはまた、堕胎薬として治療上利用できる(プロスチン15/M、Upjohn)。PGE1は、先天性心疾患を治療するために手術が行われ得るまで、アルプロスタジルとして、新生児において動脈管の能力を維持するために利用できる。PGE1及びその類似体は、男性の勃起不全の治療のため(Yeager, James L. 米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, Nathan Earl, 米国特許第6,291,528号明細書)に使用されてもよい。プロスタグランジン類似体は、眼圧を調節することに対する安全性及び有効性が証明された緑内障薬の主要な分類である。それらは、ビマトプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[1E,3S]−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−5−N−エチルヘプテンアミド}、ラタノプロスト(13,14−ジヒドロ−17−フェニル−18,19,20−トリノルPGF2αイソプロピルエステル)、トラボプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル]−5−ヘプテノアート}、及びウノプロストン(13,14−ジヒドロ−15−ケト−20−エチルプロスタグランジンF2α)を含む。
【0007】
残念ながら、プロスタグランジン、プロスタサイクリン、及び関連化合物は、様々な酸化的及び還元的経路によって急速に代謝され、不活性化される。プロスタグランジンを経口的に服用すると、肝臓及び消化管での化合物の化学分解に言及する初回通過代謝によって、プロスタグランジンは数秒で破壊され、不活性化され得る。注射の場合、プロスタグランジンの投与は有痛性であり、多くの場合、慢性症状を治療するために頻繁で金のかかる来院が必要とされ、かつほとんどのプロスタグランジン、プロスタサイクリン、及び関連化合物は、意図した作用部位に到達する前に血中及び肝臓で破壊され、不活性化され得る。プロスタグランジンが、緑内障及び高眼圧を治療するために局所的に眼に適用されると、プロスタグランジンは眼の膜を通してゆっくり浸透するため、かすみ目、眼若しくは眼瞼の炎症又は感染、ヒリヒリ感(burning)、チクチク感(stinging)、又は不快感を引き起こすかもしれない。
【課題を解決するための手段】
【0008】
本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の、新規な正に荷電された水溶性プロドラッグの調製剤、並びにそれらの医薬用途に関する。プロスタグランジン、プロスタサイクリン、及び関連化合物のプロドラッグは、次式の構造(2)を有する。
【化2】

【0009】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zは-(CH2)6-、-(CH2)n-、-(CH2)m-O-CH2-、-(CH2)m-S-CH2-、-CH2C≡C-(CH2)n-、-CH2C≡C-(CH2)n-O-CH2-、-CH2C≡C-(CH2)n-S-CH2-、-CH2-CO-(CH2)n-、-CH2-CH=C=CH-(CH2)n-、-CH2-CH=C=CH-O-(CH2)n-、-CH2-CH=C=CH-S-(CH2)n-、又は以下のものを表す。
【化3】

【0010】
式中、X3及びX4はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、m及びnは0〜8の全てを含む値を有し、Cx−Cyは-CH2-CH2-、-S-CH2-、-O-CH2-、-C≡C-、又は-CH=CH-を表し、R4は以下のものを表す。
【化4】

【化5】

【0011】
式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X3、X4及びX5はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、Y3及びY4は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH3、CH2OH、CH2OCOCH3、CH2OCOC2H5、CH2OCOC3H7、CH2OCOC4H9、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素である。Y5はCH2、NH、S、又はOであり、m及びnは0〜6の全てを含む値を有する。
【0012】

【化6】

【化7】

【0013】
式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X1及びY1は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、X2及びY2は単独でみて、相違しており、H、OH、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、I、若しくは何もなし(破線が二重結合であるとき)であるか、又は一緒にみて、酸素又は2つの水素であり、Z1及びZ2はH、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、又はClを表す。WはH、CH3、Cl、F、Br、I、又はOHを表し、破線は単結合又は二重結合を表し、全てのR、-(CH2)n-又は-(CH2)m-基は分枝鎖又は直鎖であり、C、H、O、S、又はN原子を含んでもよく、単結合、二重結合、及び三重結合を有してもよい。いずれのCH2基はO、S又はNHと置換されてもよい。
【0014】
薬物吸収は、胃腸管からであろうと他の部位からであろうと、薬物が分子形で障壁膜を横断して通過することを必要とする。薬物は初めに溶解しなければならず、もし薬物が望ましい生物薬剤的性質を有しているならば、高濃度の領域から低濃度の領域へと膜を横断して通過し、血液循環又は体循環に入るだろう。全ての生物学的膜は、主要な構成成分として脂質を含有している。膜形成について主要な役割を果たしている分子は、全てホスファート含有高極性頭基(head group)を有し、たいていの場合、2つの高疎水性炭化水素尾部(tail)を有している。膜は2分子膜であり、その親水性頭基は、両側にある水性領域へと外側を向いている。非常に親水性な薬物は膜の疎水性層を通過することができず、非常に疎水性な薬物はそれらの類似性のため膜の一部として疎水性層に留まり、内側にある細胞質ゾルに能率的に入ることができないだろう。
【0015】
本発明の目的は、皮膚表面で利用できる水分中でのプロスタグランジン、プロスタサイクリン、及び関連化合物の溶解性、並びに膜及び皮膚障壁を通してのそれらの浸透率を増大させることによって、プロスタグランジン、プロスタサイクリン、及び関連化合物を経皮投与(局所適用)可能にすることである。プロスタグランジン、プロスタサイクリン、及び関連化合物の新規なプロドラッグは、共通して2つの構造的特徴を有している。すなわち、これらは、親油性部分及び生理学的pHではプロトン化された形態で存在する第1級、第2級、又は第3級アミン基(親水性部分)を有している。膜障壁を通して能率的に通過するためには、このような親水性親油性バランスが必要とされる[Susan Milosovichなど、J. Pharm. Sci., 82,227(1993)]。正に荷電されたアミノ基は薬物の水中での溶解性を大きく増大させる。プロスタグランジン、プロスタサイクリン、及び関連化合物のこれらのプロドラッグの溶解性は>100mg/mlであり、プロスタグランジン、プロスタサイクリン、及び関連化合物の溶解性は<0.01mg/mlである。多くの例では、一連の中での最も遅い又は律速段階は薬物の溶解である。プロスタグランジン、プロスタサイクリン、及び関連化合物は、皮膚表面で利用できる水分中で非常に低い溶解性を有し、分子形では皮膚障壁を横断して通過しないだろう。それらは眼又は皮膚の膜の外側に長時間残留するため、眼若しくは皮膚の痛み、痒み又は腫れを引き起こすかもしれない。これらの新規なプロドラッグは、溶液、スプレー、ローション、軟膏、エマルジョン又はゲルのような投与形態で経皮投与されると、眼又は皮膚表面で利用できる水分中で直ちに溶解するだろう。これらのプロドラッグのアミノ基上にある正電荷は、膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、半液体状濃縮水溶液又は懸濁液である細胞質ゾルの中にプロドラッグを押し込むだろう。眼又は皮膚の膜の外側での短い残留のため、プロドラッグは眼若しくは皮膚のヒリヒリ感、痛み、痒み、又は腫れを引き起こさないだろう。
【0016】
これらのプロドラッグの人の皮膚を通しての浸透率を、修正フランツ(Franz)細胞を使用することによって試験管内で測定した。修正フランツ細胞は前大腿部及び後大腿部のヒト皮膚組織(厚さ360〜400μm)から単離した。受容液(receiving fluid)は生理食塩水中2%ウシ血清アルブミン2mlからなり、600rpmで撹拌した。時間に対する、皮膚に浸透するこれらのプロドラッグ及びその親薬物の累積量を、特異的な高速液体クロマトグラフィー法により測定した。pH7.4ホスファート緩衝液(0.2M)0.2mL中、いくつかのプロドラッグの10%溶液、又はいくつかのプロスタグランジン、プロスタサイクリン、及び関連化合物の10%懸濁液のどちらかからなるドナーを使用して得た結果を図1、図2及び図3に示す。それぞれ、人の皮膚を通して拡散する、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(N,N-diethylaminoethyl 11,15-dihydroxy-9-oxoprost-13-en-1-oate.AcOH)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスト−13−エン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−4,5,13−トリエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(9,11−ジヒドロキシ−15−ケト−20−エチルプロスタグランジンF2α N,N−ジエチルアミノエチルエステル)、N,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−メチルプロスト−13−エン−1−オアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−16,16−ジメチル−9−オキソプロスタ−2,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 7−[3−ヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル)−5−オキソシクロペンチル]−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 6,9−エポキシ−11,15−ジヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 7−{3,5−ジヒドロキシ−2−[3−ヒドロキシ−4−(3−トリフルオロメチルフェノキシ)−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 7−{2−[4−(3−クロロフェノキシ)−3−ヒドロキシ−1−ブテニル]−3,5−ジヒドロキシシクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 7−[3,5−ジヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル]シクロペンチル]−4,5−ヘプタジエン−1−オアート酢酸塩、PGE1、PGE2、PGF1α、PGF2α、カルボプロスト、プロスタレン、ウノプロストン、ミソプロストール、トラボプロスト、ラタノプロスト、ビマトプロスト、ゲメプロスト、スルプロストン、PGI2、フルプロステノール、クロプロステノール、及びフェンプロスタレンに対して、1.01 mg、1.10 mg、0.85 mg、0.94 mg、0.80 mg、0.90 mg、1.05 mg、1.09 mg、0.91 mg、0.95 mg、0.85 mg、0.88 mg、1.01 mg、1.11 mg、0.86 mg、0.92 mg、0.81 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、及び0.001 mg/cm2/hという明白な流速値を計算した。本結果は、プロドラッグは、プロスタグランジン、プロスタサイクリン、及び関連化合物よりも〜1000倍速く人の皮膚を通して拡散するということを示す。本結果は、ジアルキルアミノエチル基上の正電荷は、薬物が膜及び皮膚障壁を横断して通過することにおいて非常に重要な役割を有しているということを示す。構造(2)で表される他のプロドラッグは、非常に高い浸透率を有し、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩の浸透率と非常に近似している。
【0017】
プロスタグランジンは、非常に有効な降眼圧薬であり、緑内障の長期医療管理に理想的に適している(Woodward, D.F.など、米国特許第5,688,819号明細書)。このようなプロスタグランジンは、PGA、PGB、PGD、PGF2α、PGF1α、PGE2、PGE1を含む。それらのアルキルエステルは、降眼圧活性を有していることが報告されたが、結膜の充血及び浮腫により特徴付けられる表面刺激と同様に、一般的に炎症も引き起こす。ヨーロッパ特許出願0,364,417号に開示された、特定のフェニル及びフェノキシモノ、トリ及びテトラノルプロスタグランジン並びにそれらのエステルは、緑内障又は高眼圧の治療に有益である。Buchmannら(Buchmannなど、米国特許第5,756,818号明細書)は、眼圧を下げるのに適していると言われる特定種のシクロペンタンヘプタン酸、2−シクロアルキル、又はアリールアルキル(aryalkyl)化合物を開示した。Woodwardら(Woodward, D.F.など、米国特許第5688819号明細書)は、シクロペンタンヘプタン酸、2−シクロアルキル、又はアリールアルキル化合物は、緑内障又は高眼圧の治療に有益であるということを開示した。最近、ウノプロストン、トラボプロスト、ラタノプロスト、及びビマトプロストは緑内障薬の主要な分類になっている。これらの薬物は、非常に浸透率が低いため、全て副作用を有している。これらの副作用には、かすみ目、発赤、異物感、虹彩の変色、痒み、ヒリヒリ感、チクチク感、眼の乾燥、流涙の増加(increased tearing)、眼痛及び他の眼に関連した不快感が含まれた。
【0018】
本発明の特定の化合物の眼圧(IOP)を下げる能力を、前もって行われたレーザー線維柱帯形成術(laser trabeculoplastry)によりもたらされた高眼圧なネコにおいて評価した。希薄なプロパラカインで軽い角膜麻酔をかけた後、IOPを空気眼圧計(pneumatonometer)で測定した。試験化合物水溶液で処置する前に、ベースラインIOPを(mmHgで)測定した。3日間に渡って、6回に分けて(12時間に1回)投与した。最初の投与から24時間後、次いで12時間に1回、IOPを測定した。典型的には、治療有効量は、pH7.2ホスファート緩衝液(0.1M)中0.001〜0.01%である。組成物1滴(約30マイクロリットル)でもって処置を行った。N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(A)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(B)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(C)、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(9,11−ジヒドロキシ−15−ケト−20−エチルプロスタグランジンF2α N,N−ジエチルアミノエチルエステル)(D)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(E)、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩(F)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩(G)の結果を表1に示す。
【0019】
表1:ネコにおいて測定された、天然プロスタグランジン及び修飾類似体のプロドラッグによる眼圧低下。

【0020】
ネコの眼における、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグの刺激作用又は眼の不快感を、それぞれの試験薬物の局所適用後の最初の数時間中で評価した。眼の不快感を0〜4段階に段階分けした。0は、不快感の徴候が全く何もないことを示し、4は、完全な眼瞼閉鎖から明らかなように、最大の刺激を示す。結果を表2に示す。
【0021】
表2:それぞれの試験薬物の局所適用後、最初の2時間中の、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグの刺激作用。

【0022】
ウサギの眼における、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグによる結膜の充血を、それぞれの試験薬物の局所適用後の最初の2時間中で評価した。結膜の充血を0〜4段階に段階分けした。0は、充血が全く何もないことを示し、4は、結膜浮腫を伴った顕著な充血を示す。結果を表3に示す。
【0023】
表3:それぞれの試験薬物の局所適用後、最初の2時間中の、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグによる、ウサギの眼における結膜の充血。

【0024】
本結果は、これらのプロドラッグは、高眼圧及び緑内障の治療においてその親薬物よりも優れている、ということを示す。それらは優れた眼圧低下作用を示し、副作用を引き起こさないか、又は非常に軽度の副作用しか引き起こさない。プロスタグランジン及び関連化合物は非常に親油性である。プロスタグランジンが眼に局所適用されても、それらは眼の眼房水中に溶解しない。それらは眼の膜の外側に長時間残留するため、眼の痛み、痒み、又は腫れを引き起こすかもしれない。プロスタグランジンが眼の膜に入ると、それらは、その類似性のため膜の一部として疎水性層に留まると考えられ、内側にある細胞質ゾルに能率的に入ることができない。プロスタグランジンのプロドラッグが眼に局所適用されると、それらは眼の眼房水中に直ちに溶解するだろう。これらのプロドラッグのアミノ基上にある正電荷は、眼の膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、細胞質ゾルの中にプロドラッグを押し込むだろう。眼又は皮膚の膜の外側での短い残留のため、プロドラッグは眼のヒリヒリ感、痛み、痒み、又は腫れを引き起こさないだろう。
【0025】
プロスタグランジンは、男性の勃起不全の治療のため(Yeager; J.L.など、米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, N.E.など、米国特許第6291528号明細書)に使用され得る。しかしながら、プロスタグランジン製剤を単独で用いると、薬物濃度レベルを提供するのに十分には皮膚に浸透しない。市販の一形態(MUSE.RTM, Vivus, Menlo Park Calif.)では、アルプロスタジル(PGE1)は、長さ3.2cmで直径3.5mmの中空ステムを有するアプリケーター(Padma-Nathan, H.など、N. Engl. J. Med., 336: 1-7 (1997))を使用して、インポテンスの治療のために、尿道中に蓄積したペレット中に投与される。この治療の副作用は、陰茎の痛み及び軽度な尿道の外傷である。PGE1又はPGE2の経尿道的な送達は、インポテンスを治療する非常に有効な手段であるが、尿道のヒリヒリとした又は痛みの感覚、及び生殖器部中の海綿静脈洞弓状化(arching)を含む、望ましくない副作用がある。プロスタグランジンの経尿道的な送達は、組成物の送達を終えるための除去に関するまた別の問題を有し、パートナーの膣への過剰なプロスタグランジンの送達同様、結果として過量投与をもたらす可能性がある。
【0026】
市販の一形態では、PGE1は陰茎海綿体内注射(intracavernosal injection)により投与される。アルプロスタジル(PGE1)の陰茎海綿体内注射の主要な副作用は、投与部位での痛み、線維症の発生及び瘢痕形成である。
【0027】
本発明における新規なプロドラッグは、非常に高率(〜1mg/h/cm2)で人の皮膚を通して拡散し得て、勃起不全を治療する、又は女性の性的刺激を増強する、ほとんど副作用のない方法を提供し得る。pH7.0リン酸緩衝液(0.1M)中、0.0005%[〜0.05μg(マイクログラム)]N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩約0.01mlを、5日間、1日に1回、雄ラット(30匹)の生殖器部に塗布した。結果、薬物が与えられたラットでは、薬物が与えられなかったラットに比べて、勧誘(solicitation)において6倍の増加を示し、交尾において4倍の増加を示した。
【0028】
pH7.0リン酸緩衝液(0.1M)中、同量のN,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩を、5日間、1日に1回、雄ラット(30匹)と雌ラット(30匹)の両方の生殖器部に塗布した。結果、薬物が与えられたラットでは、薬物が与えられなかったラットに比べて、勧誘において6倍の増加を示し、交尾において6倍の増加を示した。
【0029】
PGE、PGA、及びPGFの天然並びに合成類似体からなる群から選択されたプロスタグランジンは、全身血圧を低下させるのに有益である。pH7.0リン酸緩衝液(0.1M)0.3ml中、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(A)、及びN,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−ビニルプロスタ−5,13−エン−1−オアート酢酸塩(B)0.02mgを、タングステン豊富な食餌の摂取後の、自然発症高血圧ラットの背中に塗布した。血圧をマルチチャンネルフィジオグラフで連続的に記録した。結果を表4に示す。
【0030】
表4:自然発症高血圧ラットにおける、平均動脈圧に対するプロスタグランジンのプロドラッグの作用。全ての数値は、平均±標準偏差として報告される。

【0031】
プロスタグランジンのプロドラッグの経皮投与後、自然発症高血圧ラットにおける平均動脈圧は著しく低下し、かつ薬物が与えられたラットは何ら不快感を示さなかった。
【0032】
上記の構造(2)で表される化合物は、保護されたプロスタグランジン、プロスタサイクリン、及び関連化合物から、カップリング試薬、例えば、N,N’−ジシクロヘキシルカルボジイミド、N,N’−ジイソプロピルカルボジイミド、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムテトラフルオロボラート、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロホスファート、ベンゾトリアゾール−1−イル−オキシ−トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスファート等を使用することにより、構造(3)で表される化合物との反応によって調製され得る。
【化8】

【0033】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、XはO、S又はNHを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【0034】
XがOを表すとき、上記の構造(2)で表される化合物は、プロスタグランジン、プロスタサイクリン及び関連化合物の金属塩、有機塩基塩、又は固定化された塩基塩から、構造(4)で表される化合物との反応によって調製され得る。
【化9】

【0035】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはハロゲン、又はp−トルエンスルホニルを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表す。
【発明の効果】
【0036】
本発明における、これらのプロスタグランジン、プロスタサイクリン、及び関連化合物のプロドラッグは、親油性部分及び親水性部分(生理学的pHではプロトン化された形態で存在するアミン基)を有する。これらのプロドラッグの正に荷電されたアミノ基は、2つの優れた利点を有する。第一に、薬物の水中での溶解性を大きく増大させる。すなわち、これらの新規なプロドラッグが、溶液、スプレー、ローション、軟膏、エマルジョン又はゲルのような投与形態で経皮投与されると、皮膚、眼、生殖器部、口、鼻、又は身体の他の部分上の水分と直ちに混合されるだろう。第二に、これらのプロドラッグのアミノ基上にある正電荷は、膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、半液体状濃縮水溶液又は懸濁液である細胞質ゾルの中にプロドラッグを押し込むだろう。皮膚、眼、生殖器部、口、鼻、又は身体の他の部分での短い残留のため、プロドラッグは痒み、ヒリヒリ感又は痛みを引き起こさないだろう。実験結果は、数分で、90%を超えるプロドラッグが変化して親薬物に戻ったということを示す。プロドラッグははるかに良い吸収率を有し、経皮投与は初回通過代謝を回避するため、プロドラッグは同用量でプロスタグランジン、プロスタサイクリン、及び関連化合物よりも強い作用を有するだろう。これらのプロドラッグの経皮投与におけるもう一つの大きな利点は、特に子供への、薬物投与がいっそう容易になるだろうということである。
【図面の簡単な説明】
【0037】
【図1】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスト−13−エン−1−オアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩(E、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−4,5,13−トリエン−1−オアート酢酸塩(F、10%溶液)、PGE1(G、10%懸濁液)、PGE2(H、10%懸濁液)、PGF1α(I、10%懸濁液)、PGF2α(J、10%懸濁液)、カルボプロスト(K、10%懸濁液)、プロスタレン(L、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
【図2】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−メチルプロスト−13−エン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩(E、10%溶液)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−16,16−ジメチル−9−オキソプロスタ−2,13−ジエン−1−オアート酢酸塩(F、10%溶液)、ウノプロストン(G、10%懸濁液)、ミソプロストール(H、10%懸濁液)、トラボプロスト(I、10%懸濁液)、ラタノプロスト(J、10%懸濁液)、ビマトプロスト(K、10%懸濁液)、ゲメプロスト(L、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
【図3】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 7−[3−ヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル)−5−オキソシクロペンチル]−5−ヘプテノアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 6,9−エポキシ−11,15−ジヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル 7−{3,5−ジヒドロキシ−2−[3−ヒドロキシ−4−(3−トリフルオロメチルフェノキシ)−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル 7−{2−[4−(3−クロロフェノキシ)−3−ヒドロキシ−1−ブテニル]−3,5−ジヒドロキシシクロペンチル}−5−ヘプテノアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル 7−[3,5−ジヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル]シクロペンチル]−4,5−ヘプタジエン−1−オアート酢酸塩(E、10%溶液)、スルプロストン(F、10%懸濁液)、PGI2(G、10%懸濁液)、フルプロステノール(H、10%懸濁液)、クロプロステノール(I、10%懸濁液)、及びフェンプロスタレン(J、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
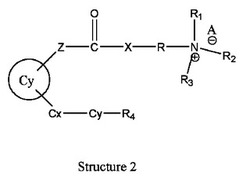
【図4】式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはアルファ鎖を表し、かつCx-Cy-R4はオメガ鎖を表す。Cyはプロスタグランジンのシクロペンチル系を表す。
【発明を実施するための形態】
【0038】
(最良の形態)
N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩の調製
11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−酸ナトリウム(sodium 11,15-dihydroxy-9-oxoprost-13-en-1-oate)37.7g(0.1mol)をアセトニトリル100mlに溶解した。2−ブロモ−N,N−ジエチルエチルアミン臭化水素酸塩(2-Bromo-N,N-diethylethylamine.HBr)26.1g(0.1mol)及び重炭酸ナトリウム8.6gを反応混合物に加えた。混合物を室温で一晩中撹拌した。溶媒を蒸発させた。酢酸エチル250mlを反応混合物に加え、混合物を水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物42g(81.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:513.37、計算% C: 65.47; H: 10.01; N: 2.73; O: 21.80、実測% C: 65.42; H: 10.03; N: 2.70; O: 21.85、1H-NMR (400MHz,D2O): δ: 0.96 (t, 3H), 1.25-1.33 (m, 12H), 1.48-1.53 (m, 4H) 1.55 (t, 6H), 1.68 (m, 2H), 2.08 (m, 1H), 2.18 (s, 3H), 2.21 (m, 2H), 2.25 (t, 2H), 2.77 (m, 1H), 3.22 (m, 4H), 3.50 (m, 2H), 3.76 (m, 1H), 3.90 (m, 1H), 4.52 (m, 2H), 5.65-5.69 (m, 2H)。
【0039】
(発明の形態)
N,N−ジエチルアミノエチル 11,15−ジアセトキシ−9−オキソプロスタ−5,13−ジエン−1−オアミド酢酸塩の調製
11,15−ジアセトキシ−9−オキソプロスタ−5,13−ジエン−1−酸43.7g(0.1mol)をクロロホルム300mlに溶解した。N,N’−ジシクロヘキシルカルボジイミド20.6gを反応混合物に加えた。N,N−ジエチルアミノエチルアミン11.7gを反応混合物に加えた。混合物を室温で3時間撹拌した。固形物を濾過により除去した。該クロロホルム溶液を5%NaHCO3(2×100ml)及び水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(85.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C34H59NO9S、分子量:657.90、計算% C: 62.07; H: 9.04; N: 2.13; O: 21.89; S: 4.87、実測% C: 62.02; H: 9.06; N: 2.11, O: 21.95; S: 4.86、1H-NMR (400MHz,D2O): δ: 0.95 (t, 3H), 1.25-1.33 (m, 14H), 1.54 (m, 2H) 1.56 (t, 6H), 1.62 (m, 2H), 1.99 (m, 2H), 2.01 (s, 3H), 2.02 (s, 3H), 2.05 (s, 3H), 2.10 (m, 1H), 2.18 (s, 3H), 2.35 (t, 2H), 2.77 (m, 1H), 3.22 (m, 4H), 3.35 (m, 2H), 3.89 (m, 2H), 3.97 (m, 1H), 4.02 (m, 1H), 4.60 (m, 1H), 5.45-5.69 (m, 2H)。
【0040】
S−(N,N−ジメチルアミノエチル)9,11,15−トリアセトキシチオプロスト−13−エン−1−オアート酢酸塩の調製
9,11,15−トリアセトキシプロスト−13−エン−1−酸49.9g(0.1mol)をクロロホルム300mlに溶解した。N,N’−ジシクロヘキシルカルボジイミド20.6gを反応混合物に加えた。ジメチルアミノエチルメルカプタン13.1gを反応混合物に加えた。混合物を室温で3時間撹拌した。固形物を濾過により除去した。該クロロホルム溶液を5%NaHCO3(2×100ml)及び水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(85.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C32H53NO9、分子量:657.9、計算% C: 64.51; H: 8.97; N: 2.35; O: 24.17、実測% C: 64.47; H: 8.99; N: 2.34, O: 24.20、1H-NMR (400MHz,D2O): δ:0.95 (t, 3H), 1.25-1.31 (m, 6H), 1.54 (m, 2H) 1.56 (t, 6H), 1.72 (m, 2H), 1.95 (m, 2H), 2.01 (s, 3H), 2.02 (s, 3H), 2.10 (m, 1H), 2.18 (s, 3H), 2.20 (m, 2H), 2.25 (t, 2H), 2.30 (m, 2H), 3.18 (m, 1H), 3.22 (m, 4H), 3.50 (m, 2H), 4.50 (m, 1H), 4.52 (m, 2H), 4.58 (m, 1H), 5.45-5.69 (m, 4H)。
【0041】
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩の調製
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−酸ナトリウム37.7g(0.1mol)をアセトニトリル100mlに溶解した。2−ブロモ−N,N−ジエチルエチルアミン臭化水素酸塩39g(0.15mol)を反応混合物に加えた。混合物を室温で3時間撹拌した。次いで、重炭酸ナトリウム8gを反応混合物に加えた。混合物を室温でまた別に2時間撹拌する。溶媒を蒸発させた。酢酸エチル250mlを反応混合物に加え、混合物を水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(87.6%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:513.71、計算% C: 65.47; H: 10.01; N: 2.73; O: 21.80、実測% C: 65.42; H: 10.03; N: 2.70; O: 21.85、1H-NMR (400MHz,D2O): δ: 0.96 (t, 3H), 1.25-1.33 (m, 6H), 1.48 (m, 2H), 1.55 (t, 6H), 1.65 (m, 1H), 1.72 (m, 2H), 1.81 (m, 2H), 1.92 (m, 2H), 1.96 (m, 2H), 2.26 (m, 1H), 2.18 (s, 3H), 2.25 (t, 2H), 3.21 (m, 1H), 3.23 (m, 1H), 3.25 (m, 4H), 3.52 (m, 2H), 3.86 (m, 1H), 4.52 (m, 2H), 5.65-5.69 (m, 4H)。
【0042】
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩の調製
高分子結合トリエチルアミン(3mol/g、100〜200メッシュ)60gをクロロホルム180mlに懸濁した。N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−酸29.6g(0.1mol)を撹拌しながら混合物に加えた。N,N−ジエチルアミノエチルブロミド臭化水素酸塩(N,N-diethylaminoethyl bromide.HBr)43g(0.15mol)を混合物に加え、混合物を室温で5時間撹拌した。高分子を濾過により除去し、テトラヒドロフラン(3×50ml)で洗浄した。酢酸ナトリウム8.2g(0.1mol)を撹拌しながら反応混合物に加えた。混合物を2時間撹拌した。固形物を濾過により除去し、クロロホルム(3×50ml)で洗浄した。溶液を真空中で100mlに濃縮した。次いでヘキサン300mlを溶液に加えた。固形生成物を濾過により集め、ヘキサン(3×100ml)で洗浄した。乾燥後、目的生成物47g(87.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:527.73、計算% C: 66.00; H: 10.12; N: 2.65; O: 21.22、実測% C: 65.96; H: 10.15; N: 2.64; O: 21.24、1H-NMR (400MHz,D2O): δ: 0.95 (t, 3H), 1.24-1.34 (m, 6H), 1.41 (s, 3H), 1.47 (m, 2H), 1.56 (t, 6H), 1.65 (m, 1H), 1.72 (m, 2H), 1.82 (m, 2H), 1.92 (m, 2H), 1.97 (m, 2H), 2.26 (m, 1H), 2.18 (s, 3H), 2.25 (t, 2H), 3.21 (m, 1H), 3.23 (m, 1H), 3.25 (m, 4H), 3.52 (m, 2H), 4.52 (m, 2H), 5.64-5.68 (m, 4H)。
【産業上の利用可能性】
【0043】
構造(2)で表されるプロドラッグは、プロスタグランジン、プロスタサイクリン及び関連化合物よりも優れている。これらは、人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態の治療に医薬的に使用され得る。これらは、緑内障又は高眼圧の治療、男性の勃起不全の治療、女性の性的刺激の増強、全身血圧の低減、堕胎、降圧コントロール(hypotensive control)、血小板凝集の阻害、肺疾患の治療、消化器疾患の治療、ショック状態の治療、生殖治療、受精能治療などのために使用されてもよい。
【技術分野】
【0001】
本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の正に荷電された水溶性プロドラッグの調製剤、並びに人又は動物において、プロスタグランジン、プロスタサイクリン、及び関連化合物治療可能な状態を治療する際のその医薬用途に関する。より具体的に言うと、本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の迅速な皮膚浸透を可能にするためにある。
【背景技術】
【0002】
天然のプロスタグランジン及びプロスタサイクリンは、膜リン脂質に由来するオータコイドのグループのうちの一つである、エイコサノイドの分類に属する。これらは、本質的に身体のどの領域でも見出される。プロスタグランジンの一般的な構造は構造1で示される。
【化1】

【0003】
全ての天然プロスタグランジンは、15α−ヒドロキシ基及びC−13でのトランス二重結合を有する(William O. Foyeなど、Principles of Medicinal Chemistry, fourth edition, Williams及びWilkins, 1995, pg 538)。カルボキシルを有する鎖はアルファ鎖と呼ばれ、ヒドロキシルを有する鎖はオメガ鎖と呼ばれる。プロスタグランジン(PG)は、9−及び11−位での酸素置換基の性質並びに立体化学に依存して、大文字A、B、C、D、E、F、G、H及びIにより分類される。様々なプロスタグランジンの作用は多種多様である。膣内に投与されると、PGE2は、妊娠子宮の子宮内膜を刺激して、分娩中に観察される子宮収縮と同じように収縮させるだろう。従って、PGE2は、堕胎薬として使用することを目的としたジノプロストン(プロスチンE2、Upjohn)として治療上利用できる。PGE2はまた、消化(GI)管平滑筋の有効な刺激剤であり、ほとんどの血管組織において有効な血管拡張作用を有し、特定の部位では収縮作用をまた有することに加えて、体温を上げ得る。PGF2αは、多くのPGEの作用を共有し、また堕胎薬として治療上利用できる(プロスチンF2アルファ、Upjohn)。PGF2αの合成15−メチル誘導体、カルボプロストもまた、堕胎薬として治療上利用できる(プロスチン15/M、Upjohn)。PGD2は、血管拡張と血管収縮の両方を引き起こす。PGEは、気管支及び気管平滑筋の弛緩をもたらす一方、PGF及びPGD2は収縮を引き起こす。PGE1は、先天性心疾患を治療するために手術が行われ得るまで、アルプロスタジルとして、新生児において動脈管の能力を維持するために利用できる。PGE1及びその類似体は、男性の勃起不全の治療のため(Yeager, James L. 米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, Nathan Earl, 米国特許第6,291,528号明細書)に使用されてもよい。プロスタグランジン類似体は、眼圧を調節することに対する安全性及び有効性が証明された緑内障薬の主要な分類である。それらは、ビマトプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[1E,3S]−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−5−N−エチルヘプテンアミド}、ラタノプロスト(13,14−ジヒドロ−17−フェニル−18,19,20−トリノルPGF2αイソプロピルエステル)、トラボプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル]−5−ヘプテノアート}、及びウノプロストン(13,14−ジヒドロ−15−ケト−20−エチルPGF2α)を含む。
【0004】
残念ながら、プロスタグランジン、プロスタサイクリン、及び関連化合物は、様々な酸化的及び還元的経路によって急速に代謝され、不活性化される。プロスタグランジンを経口的に服用すると、肝臓及び消化管での化合物の化学分解に言及する初回通過代謝によって、プロスタグランジンは数秒で破壊され、不活性化され得る。注射によりプロスタグランジンを投与する場合、有痛性であり、多くの場合、慢性症状を治療するために頻繁で金のかかる来院が必要とされ、かつほとんどのプロスタグランジン、プロスタサイクリン、及び関連化合物は、意図した作用部位に到達する前に血中及び肝臓で破壊され、不活性化され得る。
【0005】
薬物を投与する一代替方法は、局所的な送達である。局所的な薬物送達はいくつかの利点を有する。この方法は、肝臓及び消化管での初回通過代謝により引き起こされる薬物の不活性化を回避するのに役立つ。それは、全身に曝露されることなく、意図した作用部位に、適切な濃度の薬物の局所的な送達を供給し得る。Fishman(Fishman; Robert, 米国特許第7,052,715号明細書)は、経口薬物治療と関連した追加的な課題を指摘した。それは、疼痛又は炎症のある末端部を効果的に治療するためには、血流中で達成されなければならない濃度レベルが、有意でなければならないということである。これらのレベルはしばしば、疼痛又は損傷のある特定部位を正確に標的とすることが可能である場合に必要となるレベルよりもずっと高い。Yeagerは、男性の勃起不全の治療を目的にPGE1を送達するため、浸透エンハンサーを使用することを試みた(Yeager, James L. 米国特許第6,693,135号明細書)。Susan Milosovichらは、テストステロニル−4−ジメチルアミノブチラート塩酸塩(testosteronyl-4-dimethylaminobutyrate.HCl)(TSBH)を設計し、調製した。これは、親油性部分及び生理学的pHではプロトン化された形態で存在する第3級アミン基を有する。彼らは、プロドラッグ(TSBH)は、薬物(TS)それ自体よりも〜60倍速く人の皮膚を通して拡散することを見出した[Susan Milosovichなど、J. Pharm. Sci., 82,227(1993)]。
【発明の概要】
【発明が解決しようとする課題】
【0006】
様々なプロスタグランジンの作用は多種多様である。プロスタグランジンは多くの医薬用途を有する。PGE2及びPGF2αは治療上利用できる。PGF2αの合成15−メチル誘導体、カルボプロストはまた、堕胎薬として治療上利用できる(プロスチン15/M、Upjohn)。PGE1は、先天性心疾患を治療するために手術が行われ得るまで、アルプロスタジルとして、新生児において動脈管の能力を維持するために利用できる。PGE1及びその類似体は、男性の勃起不全の治療のため(Yeager, James L. 米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, Nathan Earl, 米国特許第6,291,528号明細書)に使用されてもよい。プロスタグランジン類似体は、眼圧を調節することに対する安全性及び有効性が証明された緑内障薬の主要な分類である。それらは、ビマトプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[1E,3S]−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−5−N−エチルヘプテンアミド}、ラタノプロスト(13,14−ジヒドロ−17−フェニル−18,19,20−トリノルPGF2αイソプロピルエステル)、トラボプロスト{(Z)−7−[(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル]−5−ヘプテノアート}、及びウノプロストン(13,14−ジヒドロ−15−ケト−20−エチルプロスタグランジンF2α)を含む。
【0007】
残念ながら、プロスタグランジン、プロスタサイクリン、及び関連化合物は、様々な酸化的及び還元的経路によって急速に代謝され、不活性化される。プロスタグランジンを経口的に服用すると、肝臓及び消化管での化合物の化学分解に言及する初回通過代謝によって、プロスタグランジンは数秒で破壊され、不活性化され得る。注射の場合、プロスタグランジンの投与は有痛性であり、多くの場合、慢性症状を治療するために頻繁で金のかかる来院が必要とされ、かつほとんどのプロスタグランジン、プロスタサイクリン、及び関連化合物は、意図した作用部位に到達する前に血中及び肝臓で破壊され、不活性化され得る。プロスタグランジンが、緑内障及び高眼圧を治療するために局所的に眼に適用されると、プロスタグランジンは眼の膜を通してゆっくり浸透するため、かすみ目、眼若しくは眼瞼の炎症又は感染、ヒリヒリ感(burning)、チクチク感(stinging)、又は不快感を引き起こすかもしれない。
【課題を解決するための手段】
【0008】
本発明は、プロスタグランジン、プロスタサイクリン、及び関連化合物の、新規な正に荷電された水溶性プロドラッグの調製剤、並びにそれらの医薬用途に関する。プロスタグランジン、プロスタサイクリン、及び関連化合物のプロドラッグは、次式の構造(2)を有する。
【化2】

【0009】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zは-(CH2)6-、-(CH2)n-、-(CH2)m-O-CH2-、-(CH2)m-S-CH2-、-CH2C≡C-(CH2)n-、-CH2C≡C-(CH2)n-O-CH2-、-CH2C≡C-(CH2)n-S-CH2-、-CH2-CO-(CH2)n-、-CH2-CH=C=CH-(CH2)n-、-CH2-CH=C=CH-O-(CH2)n-、-CH2-CH=C=CH-S-(CH2)n-、又は以下のものを表す。
【化3】

【0010】
式中、X3及びX4はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、m及びnは0〜8の全てを含む値を有し、Cx−Cyは-CH2-CH2-、-S-CH2-、-O-CH2-、-C≡C-、又は-CH=CH-を表し、R4は以下のものを表す。
【化4】

【化5】

【0011】
式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X3、X4及びX5はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、Y3及びY4は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH3、CH2OH、CH2OCOCH3、CH2OCOC2H5、CH2OCOC3H7、CH2OCOC4H9、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素である。Y5はCH2、NH、S、又はOであり、m及びnは0〜6の全てを含む値を有する。
【0012】

【化6】

【化7】

【0013】
式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X1及びY1は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、X2及びY2は単独でみて、相違しており、H、OH、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、I、若しくは何もなし(破線が二重結合であるとき)であるか、又は一緒にみて、酸素又は2つの水素であり、Z1及びZ2はH、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、又はClを表す。WはH、CH3、Cl、F、Br、I、又はOHを表し、破線は単結合又は二重結合を表し、全てのR、-(CH2)n-又は-(CH2)m-基は分枝鎖又は直鎖であり、C、H、O、S、又はN原子を含んでもよく、単結合、二重結合、及び三重結合を有してもよい。いずれのCH2基はO、S又はNHと置換されてもよい。
【0014】
薬物吸収は、胃腸管からであろうと他の部位からであろうと、薬物が分子形で障壁膜を横断して通過することを必要とする。薬物は初めに溶解しなければならず、もし薬物が望ましい生物薬剤的性質を有しているならば、高濃度の領域から低濃度の領域へと膜を横断して通過し、血液循環又は体循環に入るだろう。全ての生物学的膜は、主要な構成成分として脂質を含有している。膜形成について主要な役割を果たしている分子は、全てホスファート含有高極性頭基(head group)を有し、たいていの場合、2つの高疎水性炭化水素尾部(tail)を有している。膜は2分子膜であり、その親水性頭基は、両側にある水性領域へと外側を向いている。非常に親水性な薬物は膜の疎水性層を通過することができず、非常に疎水性な薬物はそれらの類似性のため膜の一部として疎水性層に留まり、内側にある細胞質ゾルに能率的に入ることができないだろう。
【0015】
本発明の目的は、皮膚表面で利用できる水分中でのプロスタグランジン、プロスタサイクリン、及び関連化合物の溶解性、並びに膜及び皮膚障壁を通してのそれらの浸透率を増大させることによって、プロスタグランジン、プロスタサイクリン、及び関連化合物を経皮投与(局所適用)可能にすることである。プロスタグランジン、プロスタサイクリン、及び関連化合物の新規なプロドラッグは、共通して2つの構造的特徴を有している。すなわち、これらは、親油性部分及び生理学的pHではプロトン化された形態で存在する第1級、第2級、又は第3級アミン基(親水性部分)を有している。膜障壁を通して能率的に通過するためには、このような親水性親油性バランスが必要とされる[Susan Milosovichなど、J. Pharm. Sci., 82,227(1993)]。正に荷電されたアミノ基は薬物の水中での溶解性を大きく増大させる。プロスタグランジン、プロスタサイクリン、及び関連化合物のこれらのプロドラッグの溶解性は>100mg/mlであり、プロスタグランジン、プロスタサイクリン、及び関連化合物の溶解性は<0.01mg/mlである。多くの例では、一連の中での最も遅い又は律速段階は薬物の溶解である。プロスタグランジン、プロスタサイクリン、及び関連化合物は、皮膚表面で利用できる水分中で非常に低い溶解性を有し、分子形では皮膚障壁を横断して通過しないだろう。それらは眼又は皮膚の膜の外側に長時間残留するため、眼若しくは皮膚の痛み、痒み又は腫れを引き起こすかもしれない。これらの新規なプロドラッグは、溶液、スプレー、ローション、軟膏、エマルジョン又はゲルのような投与形態で経皮投与されると、眼又は皮膚表面で利用できる水分中で直ちに溶解するだろう。これらのプロドラッグのアミノ基上にある正電荷は、膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、半液体状濃縮水溶液又は懸濁液である細胞質ゾルの中にプロドラッグを押し込むだろう。眼又は皮膚の膜の外側での短い残留のため、プロドラッグは眼若しくは皮膚のヒリヒリ感、痛み、痒み、又は腫れを引き起こさないだろう。
【0016】
これらのプロドラッグの人の皮膚を通しての浸透率を、修正フランツ(Franz)細胞を使用することによって試験管内で測定した。修正フランツ細胞は前大腿部及び後大腿部のヒト皮膚組織(厚さ360〜400μm)から単離した。受容液(receiving fluid)は生理食塩水中2%ウシ血清アルブミン2mlからなり、600rpmで撹拌した。時間に対する、皮膚に浸透するこれらのプロドラッグ及びその親薬物の累積量を、特異的な高速液体クロマトグラフィー法により測定した。pH7.4ホスファート緩衝液(0.2M)0.2mL中、いくつかのプロドラッグの10%溶液、又はいくつかのプロスタグランジン、プロスタサイクリン、及び関連化合物の10%懸濁液のどちらかからなるドナーを使用して得た結果を図1、図2及び図3に示す。それぞれ、人の皮膚を通して拡散する、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(N,N-diethylaminoethyl 11,15-dihydroxy-9-oxoprost-13-en-1-oate.AcOH)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスト−13−エン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−4,5,13−トリエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(9,11−ジヒドロキシ−15−ケト−20−エチルプロスタグランジンF2α N,N−ジエチルアミノエチルエステル)、N,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−メチルプロスト−13−エン−1−オアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−16,16−ジメチル−9−オキソプロスタ−2,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 7−[3−ヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル)−5−オキソシクロペンチル]−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 6,9−エポキシ−11,15−ジヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩、N,N−ジエチルアミノエチル 7−{3,5−ジヒドロキシ−2−[3−ヒドロキシ−4−(3−トリフルオロメチルフェノキシ)−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 7−{2−[4−(3−クロロフェノキシ)−3−ヒドロキシ−1−ブテニル]−3,5−ジヒドロキシシクロペンチル}−5−ヘプテノアート酢酸塩、N,N−ジエチルアミノエチル 7−[3,5−ジヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル]シクロペンチル]−4,5−ヘプタジエン−1−オアート酢酸塩、PGE1、PGE2、PGF1α、PGF2α、カルボプロスト、プロスタレン、ウノプロストン、ミソプロストール、トラボプロスト、ラタノプロスト、ビマトプロスト、ゲメプロスト、スルプロストン、PGI2、フルプロステノール、クロプロステノール、及びフェンプロスタレンに対して、1.01 mg、1.10 mg、0.85 mg、0.94 mg、0.80 mg、0.90 mg、1.05 mg、1.09 mg、0.91 mg、0.95 mg、0.85 mg、0.88 mg、1.01 mg、1.11 mg、0.86 mg、0.92 mg、0.81 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、0.001 mg、及び0.001 mg/cm2/hという明白な流速値を計算した。本結果は、プロドラッグは、プロスタグランジン、プロスタサイクリン、及び関連化合物よりも〜1000倍速く人の皮膚を通して拡散するということを示す。本結果は、ジアルキルアミノエチル基上の正電荷は、薬物が膜及び皮膚障壁を横断して通過することにおいて非常に重要な役割を有しているということを示す。構造(2)で表される他のプロドラッグは、非常に高い浸透率を有し、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩の浸透率と非常に近似している。
【0017】
プロスタグランジンは、非常に有効な降眼圧薬であり、緑内障の長期医療管理に理想的に適している(Woodward, D.F.など、米国特許第5,688,819号明細書)。このようなプロスタグランジンは、PGA、PGB、PGD、PGF2α、PGF1α、PGE2、PGE1を含む。それらのアルキルエステルは、降眼圧活性を有していることが報告されたが、結膜の充血及び浮腫により特徴付けられる表面刺激と同様に、一般的に炎症も引き起こす。ヨーロッパ特許出願0,364,417号に開示された、特定のフェニル及びフェノキシモノ、トリ及びテトラノルプロスタグランジン並びにそれらのエステルは、緑内障又は高眼圧の治療に有益である。Buchmannら(Buchmannなど、米国特許第5,756,818号明細書)は、眼圧を下げるのに適していると言われる特定種のシクロペンタンヘプタン酸、2−シクロアルキル、又はアリールアルキル(aryalkyl)化合物を開示した。Woodwardら(Woodward, D.F.など、米国特許第5688819号明細書)は、シクロペンタンヘプタン酸、2−シクロアルキル、又はアリールアルキル化合物は、緑内障又は高眼圧の治療に有益であるということを開示した。最近、ウノプロストン、トラボプロスト、ラタノプロスト、及びビマトプロストは緑内障薬の主要な分類になっている。これらの薬物は、非常に浸透率が低いため、全て副作用を有している。これらの副作用には、かすみ目、発赤、異物感、虹彩の変色、痒み、ヒリヒリ感、チクチク感、眼の乾燥、流涙の増加(increased tearing)、眼痛及び他の眼に関連した不快感が含まれた。
【0018】
本発明の特定の化合物の眼圧(IOP)を下げる能力を、前もって行われたレーザー線維柱帯形成術(laser trabeculoplastry)によりもたらされた高眼圧なネコにおいて評価した。希薄なプロパラカインで軽い角膜麻酔をかけた後、IOPを空気眼圧計(pneumatonometer)で測定した。試験化合物水溶液で処置する前に、ベースラインIOPを(mmHgで)測定した。3日間に渡って、6回に分けて(12時間に1回)投与した。最初の投与から24時間後、次いで12時間に1回、IOPを測定した。典型的には、治療有効量は、pH7.2ホスファート緩衝液(0.1M)中0.001〜0.01%である。組成物1滴(約30マイクロリットル)でもって処置を行った。N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(A)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(B)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(C)、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(9,11−ジヒドロキシ−15−ケト−20−エチルプロスタグランジンF2α N,N−ジエチルアミノエチルエステル)(D)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(E)、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩(F)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩(G)の結果を表1に示す。
【0019】
表1:ネコにおいて測定された、天然プロスタグランジン及び修飾類似体のプロドラッグによる眼圧低下。

【0020】
ネコの眼における、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグの刺激作用又は眼の不快感を、それぞれの試験薬物の局所適用後の最初の数時間中で評価した。眼の不快感を0〜4段階に段階分けした。0は、不快感の徴候が全く何もないことを示し、4は、完全な眼瞼閉鎖から明らかなように、最大の刺激を示す。結果を表2に示す。
【0021】
表2:それぞれの試験薬物の局所適用後、最初の2時間中の、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグの刺激作用。

【0022】
ウサギの眼における、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグによる結膜の充血を、それぞれの試験薬物の局所適用後の最初の2時間中で評価した。結膜の充血を0〜4段階に段階分けした。0は、充血が全く何もないことを示し、4は、結膜浮腫を伴った顕著な充血を示す。結果を表3に示す。
【0023】
表3:それぞれの試験薬物の局所適用後、最初の2時間中の、天然に存在するプロスタグランジン及び修飾プロスタグランジン、並びにそれらの新規なプロドッグによる、ウサギの眼における結膜の充血。

【0024】
本結果は、これらのプロドラッグは、高眼圧及び緑内障の治療においてその親薬物よりも優れている、ということを示す。それらは優れた眼圧低下作用を示し、副作用を引き起こさないか、又は非常に軽度の副作用しか引き起こさない。プロスタグランジン及び関連化合物は非常に親油性である。プロスタグランジンが眼に局所適用されても、それらは眼の眼房水中に溶解しない。それらは眼の膜の外側に長時間残留するため、眼の痛み、痒み、又は腫れを引き起こすかもしれない。プロスタグランジンが眼の膜に入ると、それらは、その類似性のため膜の一部として疎水性層に留まると考えられ、内側にある細胞質ゾルに能率的に入ることができない。プロスタグランジンのプロドラッグが眼に局所適用されると、それらは眼の眼房水中に直ちに溶解するだろう。これらのプロドラッグのアミノ基上にある正電荷は、眼の膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、細胞質ゾルの中にプロドラッグを押し込むだろう。眼又は皮膚の膜の外側での短い残留のため、プロドラッグは眼のヒリヒリ感、痛み、痒み、又は腫れを引き起こさないだろう。
【0025】
プロスタグランジンは、男性の勃起不全の治療のため(Yeager; J.L.など、米国特許第6,693,135号明細書)、及び女性の性的刺激を増強するため(Scott, N.E.など、米国特許第6291528号明細書)に使用され得る。しかしながら、プロスタグランジン製剤を単独で用いると、薬物濃度レベルを提供するのに十分には皮膚に浸透しない。市販の一形態(MUSE.RTM, Vivus, Menlo Park Calif.)では、アルプロスタジル(PGE1)は、長さ3.2cmで直径3.5mmの中空ステムを有するアプリケーター(Padma-Nathan, H.など、N. Engl. J. Med., 336: 1-7 (1997))を使用して、インポテンスの治療のために、尿道中に蓄積したペレット中に投与される。この治療の副作用は、陰茎の痛み及び軽度な尿道の外傷である。PGE1又はPGE2の経尿道的な送達は、インポテンスを治療する非常に有効な手段であるが、尿道のヒリヒリとした又は痛みの感覚、及び生殖器部中の海綿静脈洞弓状化(arching)を含む、望ましくない副作用がある。プロスタグランジンの経尿道的な送達は、組成物の送達を終えるための除去に関するまた別の問題を有し、パートナーの膣への過剰なプロスタグランジンの送達同様、結果として過量投与をもたらす可能性がある。
【0026】
市販の一形態では、PGE1は陰茎海綿体内注射(intracavernosal injection)により投与される。アルプロスタジル(PGE1)の陰茎海綿体内注射の主要な副作用は、投与部位での痛み、線維症の発生及び瘢痕形成である。
【0027】
本発明における新規なプロドラッグは、非常に高率(〜1mg/h/cm2)で人の皮膚を通して拡散し得て、勃起不全を治療する、又は女性の性的刺激を増強する、ほとんど副作用のない方法を提供し得る。pH7.0リン酸緩衝液(0.1M)中、0.0005%[〜0.05μg(マイクログラム)]N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩約0.01mlを、5日間、1日に1回、雄ラット(30匹)の生殖器部に塗布した。結果、薬物が与えられたラットでは、薬物が与えられなかったラットに比べて、勧誘(solicitation)において6倍の増加を示し、交尾において4倍の増加を示した。
【0028】
pH7.0リン酸緩衝液(0.1M)中、同量のN,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩を、5日間、1日に1回、雄ラット(30匹)と雌ラット(30匹)の両方の生殖器部に塗布した。結果、薬物が与えられたラットでは、薬物が与えられなかったラットに比べて、勧誘において6倍の増加を示し、交尾において6倍の増加を示した。
【0029】
PGE、PGA、及びPGFの天然並びに合成類似体からなる群から選択されたプロスタグランジンは、全身血圧を低下させるのに有益である。pH7.0リン酸緩衝液(0.1M)0.3ml中、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(A)、及びN,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−ビニルプロスタ−5,13−エン−1−オアート酢酸塩(B)0.02mgを、タングステン豊富な食餌の摂取後の、自然発症高血圧ラットの背中に塗布した。血圧をマルチチャンネルフィジオグラフで連続的に記録した。結果を表4に示す。
【0030】
表4:自然発症高血圧ラットにおける、平均動脈圧に対するプロスタグランジンのプロドラッグの作用。全ての数値は、平均±標準偏差として報告される。

【0031】
プロスタグランジンのプロドラッグの経皮投与後、自然発症高血圧ラットにおける平均動脈圧は著しく低下し、かつ薬物が与えられたラットは何ら不快感を示さなかった。
【0032】
上記の構造(2)で表される化合物は、保護されたプロスタグランジン、プロスタサイクリン、及び関連化合物から、カップリング試薬、例えば、N,N’−ジシクロヘキシルカルボジイミド、N,N’−ジイソプロピルカルボジイミド、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムテトラフルオロボラート、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロホスファート、ベンゾトリアゾール−1−イル−オキシ−トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスファート等を使用することにより、構造(3)で表される化合物との反応によって調製され得る。
【化8】

【0033】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、XはO、S又はNHを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【0034】
XがOを表すとき、上記の構造(2)で表される化合物は、プロスタグランジン、プロスタサイクリン及び関連化合物の金属塩、有機塩基塩、又は固定化された塩基塩から、構造(4)で表される化合物との反応によって調製され得る。
【化9】

【0035】
式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはハロゲン、又はp−トルエンスルホニルを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表す。
【発明の効果】
【0036】
本発明における、これらのプロスタグランジン、プロスタサイクリン、及び関連化合物のプロドラッグは、親油性部分及び親水性部分(生理学的pHではプロトン化された形態で存在するアミン基)を有する。これらのプロドラッグの正に荷電されたアミノ基は、2つの優れた利点を有する。第一に、薬物の水中での溶解性を大きく増大させる。すなわち、これらの新規なプロドラッグが、溶液、スプレー、ローション、軟膏、エマルジョン又はゲルのような投与形態で経皮投与されると、皮膚、眼、生殖器部、口、鼻、又は身体の他の部分上の水分と直ちに混合されるだろう。第二に、これらのプロドラッグのアミノ基上にある正電荷は、膜のホスファート頭基上にある負電荷と結合するだろう。従って、膜の外側の局所的な濃度が非常に高くなり、高濃度の領域から低濃度の領域へのこれらのプロドラッグの通過を促進するだろう。これらのプロドラッグが膜に入るとき、親水性部分は、半液体状濃縮水溶液又は懸濁液である細胞質ゾルの中にプロドラッグを押し込むだろう。皮膚、眼、生殖器部、口、鼻、又は身体の他の部分での短い残留のため、プロドラッグは痒み、ヒリヒリ感又は痛みを引き起こさないだろう。実験結果は、数分で、90%を超えるプロドラッグが変化して親薬物に戻ったということを示す。プロドラッグははるかに良い吸収率を有し、経皮投与は初回通過代謝を回避するため、プロドラッグは同用量でプロスタグランジン、プロスタサイクリン、及び関連化合物よりも強い作用を有するだろう。これらのプロドラッグの経皮投与におけるもう一つの大きな利点は、特に子供への、薬物投与がいっそう容易になるだろうということである。
【図面の簡単な説明】
【0037】
【図1】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスタ−5,13−ジエン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスト−13−エン−1−オアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩(E、10%溶液)、N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−4,5,13−トリエン−1−オアート酢酸塩(F、10%溶液)、PGE1(G、10%懸濁液)、PGE2(H、10%懸濁液)、PGF1α(I、10%懸濁液)、PGF2α(J、10%懸濁液)、カルボプロスト(K、10%懸濁液)、プロスタレン(L、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
【図2】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 9,11−ジヒドロキシ−15−ケト−20−エチルプロスト−5,13−ジエン−1−オアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 11,16−ジヒドロキシ−9−オキソ−16−メチルプロスト−13−エン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3R)−3−ヒドロキシ−4−[(α,α,α−トリフルオロ−m−トリル)オキシ]−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル(Z)−7{(1R,2R,3R,5S)3,5−ジヒドロキシ−2−[(3R)−3−ヒドロキシ−5−フェニルペンチル]シクロペンチル}−5−ヘプテノアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル(Z)−7−{(1R,2R,3R,5S)−3,5−ジヒドロキシ−2−[(1E,3S)−3−ヒドロキシ−5−フェニル−1−ペンテニル]シクロペンチル}−ヘプテノアート酢酸塩(E、10%溶液)、N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−16,16−ジメチル−9−オキソプロスタ−2,13−ジエン−1−オアート酢酸塩(F、10%溶液)、ウノプロストン(G、10%懸濁液)、ミソプロストール(H、10%懸濁液)、トラボプロスト(I、10%懸濁液)、ラタノプロスト(J、10%懸濁液)、ビマトプロスト(K、10%懸濁液)、ゲメプロスト(L、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
【図3】フランツ細胞(n=5)での、単離されたヒト皮膚組織を横断する、N,N−ジエチルアミノエチル 7−[3−ヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル)−5−オキソシクロペンチル]−5−ヘプテノアート酢酸塩(A、10%溶液)、N,N−ジエチルアミノエチル 6,9−エポキシ−11,15−ジヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩(B、10%溶液)、N,N−ジエチルアミノエチル 7−{3,5−ジヒドロキシ−2−[3−ヒドロキシ−4−(3−トリフルオロメチルフェノキシ)−1−ブテニル]シクロペンチル}−5−ヘプテノアート酢酸塩(C、10%溶液)、N,N−ジエチルアミノエチル 7−{2−[4−(3−クロロフェノキシ)−3−ヒドロキシ−1−ブテニル]−3,5−ジヒドロキシシクロペンチル}−5−ヘプテノアート酢酸塩(D、10%溶液)、N,N−ジエチルアミノエチル 7−[3,5−ジヒドロキシ−2−(3−ヒドロキシ−4−フェノキシ−1−ブテニル]シクロペンチル]−4,5−ヘプタジエン−1−オアート酢酸塩(E、10%溶液)、スルプロストン(F、10%懸濁液)、PGI2(G、10%懸濁液)、フルプロステノール(H、10%懸濁液)、クロプロステノール(I、10%懸濁液)、及びフェンプロスタレン(J、10%懸濁液)の累積量。それぞれの場合において、媒体はpH7.4ホスファート緩衝液(0.2M)であった。
【図4】式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはアルファ鎖を表し、かつCx-Cy-R4はオメガ鎖を表す。Cyはプロスタグランジンのシクロペンチル系を表す。
【発明を実施するための形態】
【0038】
(最良の形態)
N,N−ジエチルアミノエチル 11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−オアート酢酸塩の調製
11,15−ジヒドロキシ−9−オキソプロスト−13−エン−1−酸ナトリウム(sodium 11,15-dihydroxy-9-oxoprost-13-en-1-oate)37.7g(0.1mol)をアセトニトリル100mlに溶解した。2−ブロモ−N,N−ジエチルエチルアミン臭化水素酸塩(2-Bromo-N,N-diethylethylamine.HBr)26.1g(0.1mol)及び重炭酸ナトリウム8.6gを反応混合物に加えた。混合物を室温で一晩中撹拌した。溶媒を蒸発させた。酢酸エチル250mlを反応混合物に加え、混合物を水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物42g(81.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:513.37、計算% C: 65.47; H: 10.01; N: 2.73; O: 21.80、実測% C: 65.42; H: 10.03; N: 2.70; O: 21.85、1H-NMR (400MHz,D2O): δ: 0.96 (t, 3H), 1.25-1.33 (m, 12H), 1.48-1.53 (m, 4H) 1.55 (t, 6H), 1.68 (m, 2H), 2.08 (m, 1H), 2.18 (s, 3H), 2.21 (m, 2H), 2.25 (t, 2H), 2.77 (m, 1H), 3.22 (m, 4H), 3.50 (m, 2H), 3.76 (m, 1H), 3.90 (m, 1H), 4.52 (m, 2H), 5.65-5.69 (m, 2H)。
【0039】
(発明の形態)
N,N−ジエチルアミノエチル 11,15−ジアセトキシ−9−オキソプロスタ−5,13−ジエン−1−オアミド酢酸塩の調製
11,15−ジアセトキシ−9−オキソプロスタ−5,13−ジエン−1−酸43.7g(0.1mol)をクロロホルム300mlに溶解した。N,N’−ジシクロヘキシルカルボジイミド20.6gを反応混合物に加えた。N,N−ジエチルアミノエチルアミン11.7gを反応混合物に加えた。混合物を室温で3時間撹拌した。固形物を濾過により除去した。該クロロホルム溶液を5%NaHCO3(2×100ml)及び水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(85.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C34H59NO9S、分子量:657.90、計算% C: 62.07; H: 9.04; N: 2.13; O: 21.89; S: 4.87、実測% C: 62.02; H: 9.06; N: 2.11, O: 21.95; S: 4.86、1H-NMR (400MHz,D2O): δ: 0.95 (t, 3H), 1.25-1.33 (m, 14H), 1.54 (m, 2H) 1.56 (t, 6H), 1.62 (m, 2H), 1.99 (m, 2H), 2.01 (s, 3H), 2.02 (s, 3H), 2.05 (s, 3H), 2.10 (m, 1H), 2.18 (s, 3H), 2.35 (t, 2H), 2.77 (m, 1H), 3.22 (m, 4H), 3.35 (m, 2H), 3.89 (m, 2H), 3.97 (m, 1H), 4.02 (m, 1H), 4.60 (m, 1H), 5.45-5.69 (m, 2H)。
【0040】
S−(N,N−ジメチルアミノエチル)9,11,15−トリアセトキシチオプロスト−13−エン−1−オアート酢酸塩の調製
9,11,15−トリアセトキシプロスト−13−エン−1−酸49.9g(0.1mol)をクロロホルム300mlに溶解した。N,N’−ジシクロヘキシルカルボジイミド20.6gを反応混合物に加えた。ジメチルアミノエチルメルカプタン13.1gを反応混合物に加えた。混合物を室温で3時間撹拌した。固形物を濾過により除去した。該クロロホルム溶液を5%NaHCO3(2×100ml)及び水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(85.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C32H53NO9、分子量:657.9、計算% C: 64.51; H: 8.97; N: 2.35; O: 24.17、実測% C: 64.47; H: 8.99; N: 2.34, O: 24.20、1H-NMR (400MHz,D2O): δ:0.95 (t, 3H), 1.25-1.31 (m, 6H), 1.54 (m, 2H) 1.56 (t, 6H), 1.72 (m, 2H), 1.95 (m, 2H), 2.01 (s, 3H), 2.02 (s, 3H), 2.10 (m, 1H), 2.18 (s, 3H), 2.20 (m, 2H), 2.25 (t, 2H), 2.30 (m, 2H), 3.18 (m, 1H), 3.22 (m, 4H), 3.50 (m, 2H), 4.50 (m, 1H), 4.52 (m, 2H), 4.58 (m, 1H), 5.45-5.69 (m, 4H)。
【0041】
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−オアート酢酸塩の調製
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシプロスタ−5,13−ジエン−1−酸ナトリウム37.7g(0.1mol)をアセトニトリル100mlに溶解した。2−ブロモ−N,N−ジエチルエチルアミン臭化水素酸塩39g(0.15mol)を反応混合物に加えた。混合物を室温で3時間撹拌した。次いで、重炭酸ナトリウム8gを反応混合物に加えた。混合物を室温でまた別に2時間撹拌する。溶媒を蒸発させた。酢酸エチル250mlを反応混合物に加え、混合物を水(3×100ml)で洗浄した。得られた有機溶液を無水硫酸ナトリウム上で乾燥させた。硫酸ナトリウムを濾過により除去した。酢酸6gを撹拌しながら反応混合物に加えた。ヘキサン(200ml)を加えた。固形生成物を濾過により集めた。乾燥後、目的生成物45g(87.6%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:513.71、計算% C: 65.47; H: 10.01; N: 2.73; O: 21.80、実測% C: 65.42; H: 10.03; N: 2.70; O: 21.85、1H-NMR (400MHz,D2O): δ: 0.96 (t, 3H), 1.25-1.33 (m, 6H), 1.48 (m, 2H), 1.55 (t, 6H), 1.65 (m, 1H), 1.72 (m, 2H), 1.81 (m, 2H), 1.92 (m, 2H), 1.96 (m, 2H), 2.26 (m, 1H), 2.18 (s, 3H), 2.25 (t, 2H), 3.21 (m, 1H), 3.23 (m, 1H), 3.25 (m, 4H), 3.52 (m, 2H), 3.86 (m, 1H), 4.52 (m, 2H), 5.65-5.69 (m, 4H)。
【0042】
N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−オアート酢酸塩の調製
高分子結合トリエチルアミン(3mol/g、100〜200メッシュ)60gをクロロホルム180mlに懸濁した。N,N−ジエチルアミノエチル 9,11,15−トリヒドロキシ−15−メチルプロスタ−5,13−ジエン−1−酸29.6g(0.1mol)を撹拌しながら混合物に加えた。N,N−ジエチルアミノエチルブロミド臭化水素酸塩(N,N-diethylaminoethyl bromide.HBr)43g(0.15mol)を混合物に加え、混合物を室温で5時間撹拌した。高分子を濾過により除去し、テトラヒドロフラン(3×50ml)で洗浄した。酢酸ナトリウム8.2g(0.1mol)を撹拌しながら反応混合物に加えた。混合物を2時間撹拌した。固形物を濾過により除去し、クロロホルム(3×50ml)で洗浄した。溶液を真空中で100mlに濃縮した。次いでヘキサン300mlを溶液に加えた。固形生成物を濾過により集め、ヘキサン(3×100ml)で洗浄した。乾燥後、目的生成物47g(87.8%)を得た。吸湿性生成物、水中での溶解性:100mg/ml、元素分析:C28H51NO7、分子量:527.73、計算% C: 66.00; H: 10.12; N: 2.65; O: 21.22、実測% C: 65.96; H: 10.15; N: 2.64; O: 21.24、1H-NMR (400MHz,D2O): δ: 0.95 (t, 3H), 1.24-1.34 (m, 6H), 1.41 (s, 3H), 1.47 (m, 2H), 1.56 (t, 6H), 1.65 (m, 1H), 1.72 (m, 2H), 1.82 (m, 2H), 1.92 (m, 2H), 1.97 (m, 2H), 2.26 (m, 1H), 2.18 (s, 3H), 2.25 (t, 2H), 3.21 (m, 1H), 3.23 (m, 1H), 3.25 (m, 4H), 3.52 (m, 2H), 4.52 (m, 2H), 5.64-5.68 (m, 4H)。
【産業上の利用可能性】
【0043】
構造(2)で表されるプロドラッグは、プロスタグランジン、プロスタサイクリン及び関連化合物よりも優れている。これらは、人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態の治療に医薬的に使用され得る。これらは、緑内障又は高眼圧の治療、男性の勃起不全の治療、女性の性的刺激の増強、全身血圧の低減、堕胎、降圧コントロール(hypotensive control)、血小板凝集の阻害、肺疾患の治療、消化器疾患の治療、ショック状態の治療、生殖治療、受精能治療などのために使用されてもよい。
【特許請求の範囲】
【請求項1】
次式の構造(2)で表される化合物。
【化1】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Cx−Cyは-CH2-CH2-、-S-CH2-、-O-CH2-、-C≡C-、又は-CH=CH-を表し、Zは-(CH2)6-、-(CH2)n-、-(CH2)m-O-CH2-、-(CH2)m-S-CH2-、-CH2C≡C-(CH2)n-、-CH2C≡C-(CH2)n-O-CH2-、-CH2C≡C-(CH2)n-S-CH2-、-CH2-CO-(CH2)n-、-CH2-CH=C=CH-(CH2)n-、-CH2-CH=C=CH-O-(CH2)n-、-CH2-CH=C=CH-S-(CH2)n-、又は以下のものを表し、
【化2】

式中、m及びnは0〜6の全てを含む値を有し、R4は以下のものを表し、
【化3】

【化4】

式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X3、X4及びX5はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、Y3及びY4は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH3、CH2OH、CH2OCOCH3、CH2OCOC2H5、CH2OCOC3H7、CH2OCOC4H9、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、Y5はCH2、NH、S、又はOであり、m及びnは0〜8の全てを含む値を有し、

【化5】

【化6】

式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X1及びY1は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、X2及びY2は単独でみて、相違しており、H、OH、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、I、若しくは何もなし(破線が二重結合であるとき)であるか、又は一緒にみて、酸素又は2つの水素であり、Z1及びZ2はH、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、又はClを表し、WはH、CH3、Cl、F、Br、I、又はOHを表し、破線は単結合又は二重結合を表し、全てのR、-(CH2)n-又は-(CH2)m-基は分枝鎖又は直鎖であり、C、H、O、S、又はN原子を含んでもよく、単結合、二重結合、及び三重結合を有してもよく、いずれのCH2基はO、S又はNHと置換されてもよい。
【請求項2】
請求項1に記載の、構造(2)で表される化合物を調製する方法であって、該化合物を、保護されたプロスタグランジン、プロスタサイクリン、及び関連化合物から、カップリング試薬、例えば、N,N’−ジシクロヘキシルカルボジイミド、N,N’−ジイソプロピルカルボジイミド、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムテトラフルオロボラート、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロホスファート、ベンゾトリアゾール−1−イル−オキシ−トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスファート等を使用することにより、以下の構造(3)で表される化合物と反応させることにより得ることを特徴とする方法。
【化7】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、XはO、S又はNHを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【請求項3】
請求項1に記載の、構造(2)で表される化合物を調製する方法であって、該化合物を、プロスタグランジン、プロスタサイクリン及び関連化合物の金属塩、有機塩基塩、又は固定化された塩基塩から、以下の構造(4)で表される化合物と反応させて得ることを特徴とする方法。
【化8】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはハロゲン、又はp−トルエンスルホニルを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【請求項4】
請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物であって、人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療するために、経口投与又は経皮投与可能である化合物又は組成物であって、前記プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態が、緑内障又は高眼圧、男性の勃起不全及び女性の性機能不全、全身高血圧、堕胎、降圧コントロール、血小板凝集の阻害、肺疾患、消化器疾患、炎症、ショック状態、生殖、受精能等を含むが、これに限定されるものではない化合物又は組成物。
【請求項5】
人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療する方法であって、身体の一部に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することにより、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物の治療有効血漿レベルを送達することを特徴とする方法。
【請求項6】
男性の勃起不全又は女性の性機能不全を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、男性若しくは女性、又は動物の生殖器部に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項7】
緑内障又は高眼圧を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の眼に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項8】
全身高血圧を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の一部分に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項9】
請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物であって、堕胎薬として、女性の膣に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与され得る化合物又は組成物。
【請求項10】
胃腸潰瘍及び皮膚潰瘍を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の一部分に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項11】
炎症を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人若しくは動物の眼又は身体の別の部分に経皮投与することを特徴とする方法。
【請求項12】
人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療するための、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物の経皮治療応用システムであって、活性物質含有マトリックス層及び非透過性支持層からなる包帯又はパッチであり得、最も好ましくは、活性物質貯蔵庫であり、これが皮膚に面する透過性底面を有し、放出の割合を制御することによって、プロスタグランジン、プロスタサイクリン及び関連化合物が絶えず最適治療血中レベルに達することを可能にし、効能を増大させ、プロスタグランジン、プロスタサイクリン及び関連化合物の副作用を減少させることを可能にすることを特徴とするシステム。
【請求項1】
次式の構造(2)で表される化合物。
【化1】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、XはO、S、又はNHを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Cx−Cyは-CH2-CH2-、-S-CH2-、-O-CH2-、-C≡C-、又は-CH=CH-を表し、Zは-(CH2)6-、-(CH2)n-、-(CH2)m-O-CH2-、-(CH2)m-S-CH2-、-CH2C≡C-(CH2)n-、-CH2C≡C-(CH2)n-O-CH2-、-CH2C≡C-(CH2)n-S-CH2-、-CH2-CO-(CH2)n-、-CH2-CH=C=CH-(CH2)n-、-CH2-CH=C=CH-O-(CH2)n-、-CH2-CH=C=CH-S-(CH2)n-、又は以下のものを表し、
【化2】

式中、m及びnは0〜6の全てを含む値を有し、R4は以下のものを表し、
【化3】

【化4】

式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X3、X4及びX5はH、OH、Cl、F、OCH3、S-CH3、CH3、C2H5、CH=CH2、CH2CH=CH2、及びCF3を表し、Y3及びY4は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH3、CH2OH、CH2OCOCH3、CH2OCOC2H5、CH2OCOC3H7、CH2OCOC4H9、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、Y5はCH2、NH、S、又はOであり、m及びnは0〜8の全てを含む値を有し、

【化5】

【化6】

式中、R5はH、OH、アセチル、プロピオニル、イソブチリル、ブチリル、ピバロイル、バレリル、及びイソバレリルを表し、X1及びY1は単独でみて、相違しており、H、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、Iであるか、又は一緒にみて、酸素又は2つの水素であり、X2及びY2は単独でみて、相違しており、H、OH、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、Cl、F、Br、I、若しくは何もなし(破線が二重結合であるとき)であるか、又は一緒にみて、酸素又は2つの水素であり、Z1及びZ2はH、OH、OR5、OOH、OCOCH3、OCOC2H5、OCOC3H7、OCOC4H9、OCOC5H11、OCOC6H13、CH2-OH、又はClを表し、WはH、CH3、Cl、F、Br、I、又はOHを表し、破線は単結合又は二重結合を表し、全てのR、-(CH2)n-又は-(CH2)m-基は分枝鎖又は直鎖であり、C、H、O、S、又はN原子を含んでもよく、単結合、二重結合、及び三重結合を有してもよく、いずれのCH2基はO、S又はNHと置換されてもよい。
【請求項2】
請求項1に記載の、構造(2)で表される化合物を調製する方法であって、該化合物を、保護されたプロスタグランジン、プロスタサイクリン、及び関連化合物から、カップリング試薬、例えば、N,N’−ジシクロヘキシルカルボジイミド、N,N’−ジイソプロピルカルボジイミド、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムテトラフルオロボラート、O−(ベンゾトリアゾール−1−イル)−N,N,N’,N’−テトラメチルウロニウムヘキサフルオロホスファート、ベンゾトリアゾール−1−イル−オキシ−トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスファート等を使用することにより、以下の構造(3)で表される化合物と反応させることにより得ることを特徴とする方法。
【化7】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、XはO、S又はNHを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【請求項3】
請求項1に記載の、構造(2)で表される化合物を調製する方法であって、該化合物を、プロスタグランジン、プロスタサイクリン及び関連化合物の金属塩、有機塩基塩、又は固定化された塩基塩から、以下の構造(4)で表される化合物と反応させて得ることを特徴とする方法。
【化8】

式中、R1はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R2はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、R3はH、1〜12炭素原子を有するアルキル、アルキルオキシ、アルケニル、若しくはアルキニル残基のいずれか一つ、アリール又はヘテロアリール残基を表し、Rは分枝鎖若しくは直鎖、-(CH2)n-であってn=0、1、2、3、4、5、6、7、8、9、10……、アリール又はヘテロアリール基を表し、Zはハロゲン、又はp−トルエンスルホニルを表し、A-はCl-、Br-、F-、I-、AcO-、シトラート、又は陰イオンを表し、n=0、1、2、3、4、5、6、7、8、9、10……である。
【請求項4】
請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物であって、人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療するために、経口投与又は経皮投与可能である化合物又は組成物であって、前記プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態が、緑内障又は高眼圧、男性の勃起不全及び女性の性機能不全、全身高血圧、堕胎、降圧コントロール、血小板凝集の阻害、肺疾患、消化器疾患、炎症、ショック状態、生殖、受精能等を含むが、これに限定されるものではない化合物又は組成物。
【請求項5】
人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療する方法であって、身体の一部に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することにより、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物の治療有効血漿レベルを送達することを特徴とする方法。
【請求項6】
男性の勃起不全又は女性の性機能不全を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、男性若しくは女性、又は動物の生殖器部に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項7】
緑内障又は高眼圧を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の眼に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項8】
全身高血圧を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の一部分に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項9】
請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物であって、堕胎薬として、女性の膣に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与され得る化合物又は組成物。
【請求項10】
胃腸潰瘍及び皮膚潰瘍を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人又は動物の一部分に(溶液、スプレー、ローション、軟膏、エマルジョン又はゲルの形態で)経皮投与することを特徴とする方法。
【請求項11】
炎症を治療する方法であって、治療有効量の、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物を、人若しくは動物の眼又は身体の別の部分に経皮投与することを特徴とする方法。
【請求項12】
人又は動物において、プロスタグランジン、プロスタサイクリン及び関連化合物治療可能な状態を治療するための、請求項1に記載の、構造(2)で表される化合物、又は少なくとも構造(2)で表される化合物を活性成分として含む組成物の経皮治療応用システムであって、活性物質含有マトリックス層及び非透過性支持層からなる包帯又はパッチであり得、最も好ましくは、活性物質貯蔵庫であり、これが皮膚に面する透過性底面を有し、放出の割合を制御することによって、プロスタグランジン、プロスタサイクリン及び関連化合物が絶えず最適治療血中レベルに達することを可能にし、効能を増大させ、プロスタグランジン、プロスタサイクリン及び関連化合物の副作用を減少させることを可能にすることを特徴とするシステム。
【図1】


【図2】


【図3】


【図4】




【図2】


【図3】


【図4】


【公表番号】特表2010−505808(P2010−505808A)
【公表日】平成22年2月25日(2010.2.25)
【国際特許分類】
【出願番号】特願2009−530953(P2009−530953)
【出願日】平成18年10月2日(2006.10.2)
【国際出願番号】PCT/IB2006/053594
【国際公開番号】WO2008/041054
【国際公開日】平成20年4月10日(2008.4.10)
【出願人】(509011581)テックフィールズ バイオケム カンパニー リミテッド (10)
【出願人】(509023539)
【Fターム(参考)】
【公表日】平成22年2月25日(2010.2.25)
【国際特許分類】
【出願日】平成18年10月2日(2006.10.2)
【国際出願番号】PCT/IB2006/053594
【国際公開番号】WO2008/041054
【国際公開日】平成20年4月10日(2008.4.10)
【出願人】(509011581)テックフィールズ バイオケム カンパニー リミテッド (10)
【出願人】(509023539)

【Fターム(参考)】
[ Back to top ]

