骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材
【課題】患者への負担を軽減しながら十分な量の心筋細胞を得る。
【解決手段】骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップS3を備える骨格筋芽細胞の心筋細胞への分化方法を提供する。また、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップS3と、該培養ステップS3によって骨格筋芽細胞から分化した心筋細胞を回収する回収ステップS4とを備える心筋移植材の製造方法を提供する。また、上記心筋移植材の製造方法により製造された心筋移植材を提供する。
【解決手段】骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップS3を備える骨格筋芽細胞の心筋細胞への分化方法を提供する。また、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップS3と、該培養ステップS3によって骨格筋芽細胞から分化した心筋細胞を回収する回収ステップS4とを備える心筋移植材の製造方法を提供する。また、上記心筋移植材の製造方法により製造された心筋移植材を提供する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材に関するものである。
【背景技術】
【0002】
従来、脂肪由来幹細胞を目的の部位の分化した細胞(成熟細胞)と混合して培養することにより、脂肪由来幹細胞を分化させる方法が知られている(例えば、特許文献1参照。)。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特表2007−507202号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
しかしながら、成熟細胞の数に対して分化させることができる幹細胞の数は限られている。したがって、特許文献1の場合、例えば、目的の部位が病変していて正常な成熟細胞の存在する領域が限られていたり、目的の部位の成熟細胞が元々わずかしか存在しなかったりする場合、必要な量の成熟細胞を確保することが難しいため、幹細胞から分化させて得られる細胞の量に限界がある。また、そのような部位から成熟細胞を採取することによる患者の負担も大きい。特に、必要な成熟細胞が、心筋細胞のように体外で培養して増殖させることが困難な細胞である場合、必要な量の細胞を幹細胞から分化させて得ることが非常に難しい。
【0005】
本発明は、上述した事情に鑑みてなされたものであって、患者への負担を軽減しながら十分な量の心筋細胞を得ることができる骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材を提供することを目的とする。
【課題を解決するための手段】
【0006】
上記目的を達成するため、本発明は以下の手段を提供する。
本発明は、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップを備える骨格筋芽細胞の心筋細胞への分化方法を提供する。
本発明によれば、培養ステップにおいて脂肪由来幹細胞が骨格筋芽細胞の心筋細胞への分化を誘導することにより、心筋細胞を得ることができる。このように、心筋以外の部位に比較的豊富に存在する骨格筋芽細胞から心筋細胞が分化させられるので、患者への負担を軽減しながら、十分な量の心筋細胞を得ることができる。
【0007】
上記発明においては、前記間葉系幹細胞が、脂肪組織から分離された脂肪由来幹細胞であってもよい。
このようにすることで、脂肪組織は、生体内に豊富に存在するうえ採取が比較的容易であり、さらに間葉系幹細胞である脂肪由来幹細胞を比較的豊富に含んでいるので、間葉系幹細胞の採取に伴う患者への負担を軽減することができる。
【0008】
また、本発明は、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップと、該培養ステップによって前記骨格筋芽細胞から分化した心筋細胞を回収する回収ステップとを備える心筋移植材の製造方法を提供する。
本発明によれば、培養ステップによって骨格筋芽細胞から分化した心筋細胞を回収ステップにおいて回収することにより、患者への負担を軽減しながら十分な量の心筋細胞を含む心筋移植材を製造することができる。
【0009】
上記発明においては、前記培養ステップの前に、培養容器の底面上に骨格筋芽細胞からなる骨格筋芽細胞層を形成する骨格筋芽細胞層形成ステップを備え、前記培養ステップが、前記培養容器内に前記間葉系幹細胞を播種して培養してもよい。
このようにすることで、骨格筋芽細胞を脂肪由来幹細胞と効率良く接触させて骨格筋芽細胞の分化効率を向上することができる。
【0010】
また、上記発明においては、前記培養ステップが、培養温度より低い下限臨界溶解温度を有するポリマにより底面が被覆された培養容器内で前記骨格筋芽細胞を前記培養温度で培養し、前記回収ステップが、前記培養容器を前記培養温度より低い温度に冷却させることにより前記心筋細胞を前記底面から剥離させて回収してもよい。
【0011】
このようにすることで、タンパク質分解酵素などの薬剤を添加することなく心筋移植材を製造することができる。また、これにより培養中に細胞が分泌した細胞外基質が分解されることなく残るので、生体に移植されたときに細胞外基質が接着剤として働くことにより生体への生着効率を向上することができる。また、培養容器内に骨格筋芽細胞層を形成した場合には、シート形状の心筋移植材を容易に製造できる。
【0012】
また、上記発明においては、前記培養ステップが、細胞非接着性の底面を有する培養容器内で前記骨格筋芽細胞を培養してもよい。
このようにすることで、骨格筋芽細胞および脂肪由来幹細胞は底面に接着せずに細胞同士で互いに接着して細胞凝集塊を形成する。これにより、骨格筋芽細胞および脂肪由来幹細胞の細胞外基質の分泌が促されるとともに、分化した心筋細胞がタンパク質分解酵素を使用せずに培養容器内から回収されるので、生体に移植したときの生着効率を向上することができる。
【0013】
また、上記発明においては、前記培養容器が、略均一に分布する複数の凹部を底面に有していてもよい。
このようにすることで、略均一な数の骨格筋芽細胞および脂肪由来幹細胞が各凹部に集合するので、各細胞凝集塊に含まれる心筋細胞の数を略均一に揃えることができる。また、心筋移植材として細胞凝集塊の分散液が製造されるので、心筋移植材を注射によって容易に移植できる。
【0014】
また、上記発明においては、前記培養容器は、前記骨格筋芽細胞および前記脂肪由来幹細胞の移動を制限する仕切りによって底面が複数の区画に分画されていてもよい。
このようにすることで、比較的小さく分割されたシート形状で、または、細胞凝集塊の分散液として心筋移植材が製造されるので、心筋移植材を注射によって容易に移植することができる。
【0015】
また、上記発明においては、前記培養ステップの後に前記脂肪由来幹細胞を除去する脂肪由来幹細胞除去ステップを備えていてもよい。
このようにすることで、心筋細胞の純度を向上し、移植したときの治療効果を向上することができる。
また、本発明は、上記いずれかに記載の心筋移植材の製造方法により製造された心筋移植材を提供する。
【発明の効果】
【0016】
本発明によれば、患者への負担を軽減しながら十分な量の心筋細胞を得ることができるという効果を奏する。
【図面の簡単な説明】
【0017】
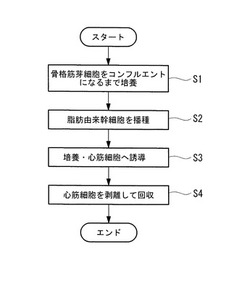
【図1】本発明の一実施形態に係る骨格筋芽細胞の心筋細胞への分化方法を示すフローチャートである。
【図2】播種ステップにおける培養容器内を模式的に示した図である。
【図3】培養ステップにおける培養容器内を模式的に示した図である。
【図4】骨格筋芽細胞層の変形例および培養容器の変形例を示す図である。
【図5】培養容器のもう1つ変形例を示す図である。
【図6】骨格筋芽細胞を脂肪由来幹細胞と共に4日間培養したときの脂肪由来幹細胞の蛍光染色画像である。
【図7】骨格筋芽細胞を脂肪由来幹細胞と共に4日間培養したときのトロポニンの蛍光染色画像である。
【発明を実施するための形態】
【0018】
以下に、本発明の一実施形態に係る骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材について、図1〜図5を参照して説明する。
本実施形態に係る心筋移植材の製造方法は、図1に示されるように、培養容器1の底面上に骨格筋芽細胞層2を形成する骨格筋芽細胞層形成ステップS1と、培養容器1に間葉系幹細胞Aを播種する播種ステップS2と、培養容器1内で間葉系幹細胞Aと共に骨格筋芽細胞Bを培養する培養ステップS3と、該培養ステップS3において骨格筋芽細胞Bから分化した心筋細胞Cを回収する回収ステップS4とを備えている。
【0019】
本実施形態に係る骨格筋芽細胞の心筋細胞への分化方法は、培養ステップS3に相当する。
本実施形態においては、間葉系幹細胞Aとして、患者の脂肪組織から抽出した脂肪由来幹細胞Aを用いることとするが、例えば、患者の骨髄などの他の組織由来の間葉系幹細胞も同様に用いることができる。脂肪由来幹細胞Aは、脂肪組織を消化酵素で分解することにより脂肪組織から脂肪由来細胞群を分離し、分離した脂肪由来細胞群から抗CD34抗体に陰性かつ抗CD90抗体に陽性の細胞を選択することにより、脂肪組織から抽出できる。
【0020】
骨格筋芽細胞層形成ステップS1は、骨格筋芽細胞Bを培養容器1内でコンフルエントな状態まで培養することにより行われる。骨格筋芽細胞Bは、通常の培養条件、すなわち、培養温度37℃、二酸化炭素濃度5%の環境で培養される。これにより、培養容器1の底面が略全体にわたって骨格筋芽細胞層2により覆われる。骨格筋芽細胞Bとしては、患者の骨格筋組織から抽出して培養により増殖させたものが用いられる。
【0021】
ここで、培養容器1としては、温度応答性培養容器が用いられる。温度応答性培養容器は、骨格筋芽細胞層形成ステップS1および後述する培養ステップS3における培養温度より低い下限臨界溶解温度を有する温度応答性ポリマにより、底面が被覆されている。温度応答性培養容器内で骨格筋芽細胞Bをコンフルエントな状態まで増殖させた後、温度応答性培養容器の温度を下限臨界溶解温度より低い温度まで下降させることにより、骨格筋芽細胞層2が底面上に浮いた状態となる。これにより、骨格筋芽細胞層2をシート形状のまま底面から容易に剥がして回収することができる。
【0022】
また、培養容器1の底面は、細胞非接着性の材料からなる格子状のグリッド(仕切り)3が設けられている。骨格筋芽細胞Bおよび脂肪由来幹細胞Aは、グリッド3上を避けて移動および増殖するので、後述する培養ステップS3において、グリッド3によって分画された各区画内において増殖する。これにより、培養容器1の温度を温度応答性ポリマの下限臨界溶解温度より低い温度まで下降させたときに、小さく分割された複数の細胞シートが底面上に浮く。細胞非接着性の材料としては、例えば、エチレングリコール誘導体が用いられる。
【0023】
播種ステップS2は、骨格筋芽細胞層形成ステップS1により形成された骨格筋芽細胞層2上に脂肪由来幹細胞Aを播種した後、骨格筋芽細胞層2上に接着した脂肪由来幹細胞Aの上から骨格筋芽細胞Bからなる細胞シートをかぶせることにより行われる。これにより、図2に示されるように、骨格筋芽細胞Bの間に脂肪由来幹細胞Aが挟まれ、骨格筋芽細胞Bが脂肪由来幹細胞Aと密に接触させられた状態になる。骨格筋芽細胞Bからなる細胞シートは、他の温度応答性培養容器内で骨格筋芽細胞Bをコンフルエントな状態まで増殖させた後に、形成された骨格筋芽細胞層を温度応答性培養容器の底面から剥離することにより作成される。
【0024】
培養ステップS3は、通常の細胞培養に用いられる条件で骨格筋芽細胞Bと脂肪由来幹細胞Aを培養することにより行われる。具体的には、培地Dとして10%FBSを添加したDMEM(ダルベッコ改変イーグル培地)を用い、培養温度37℃、二酸化炭素濃度5%の環境で、骨格筋芽細胞Bと脂肪由来幹細胞Aを培養する。これにより、図3に示されるように、骨格筋芽細胞Bは、脂肪由来幹細胞Aによって心筋細胞Cへの分化が誘導される。
【0025】
ここで、骨格筋芽細胞Bおよび脂肪由来幹細胞Aが互いに密に接着した状態で培養されることにより、これらの細胞A,Bから細胞外基質が盛んに分泌される。分泌された細胞外基質は、生体内に移植されたときに生体内の組織との接着剤として働くことにより、心筋移植材の生着効率を向上させる。
【0026】
回収ステップS4は、培養容器1内の培地Dを生理食塩水などの溶媒に交換した後、培養容器1の温度を下限臨界溶解温度より低い温度まで下降させ、溶媒中に浮いた細胞シートを溶媒と共に注射器などで吸引することにより行われる。これにより、心筋細胞Cを含む比較的小さな細胞シートが溶媒に懸濁された本実施形態に係る心筋移植材を製造することができる。
【0027】
このようにして製造された心筋移植材の移植は、例えば、心筋に注射することにより行われる。このときに、細胞シートが比較的小さく分割されているので、細径の注射針を使用した場合でもスムーズに心筋移植材を移植することができる。
【0028】
ここで、心筋の一部が病変していたりその一部を切除したりした場合など、同じ部位から心筋細胞を採取することは患者の負担を増大させるため、採取できる心筋細胞の量は少量に限られる。また、心筋細胞の場合、採取後に体外で培養により増殖させることは困難である。したがって、従来の、患者から採取した心筋細胞により幹細胞の心筋細胞への分化を誘導させる方法では、分化させることができる幹細胞の量が少量に限られ、十分な量の心筋細胞を得ることが難しかった。
【0029】
これに対して、本実施形態によれば、生体内に比較的豊富に存在し生体内からの採取が比較的容易な骨格筋組織および脂肪組織からそれぞれ抽出された骨格筋芽細胞Bおよび脂肪由来幹細胞Aを使用して心筋移植材が製造される。したがって、患者の体内から心筋細胞を採取することが困難な場合でも、治療に十分な量の心筋細胞Cを含んだ心筋移植材を製造することができるとともに、細胞の採取による患者への負担を軽減することができる。
【0030】
また、温度応答性培養容器を使用することにより、トリプシンなどのタンパク質分解酵素を使用せずに、細胞A,Cを培養容器1から回収することができる。したがって、培養ステップS3において細胞A,Bから分泌された細胞外基質が分解されることなく残されるので、生体内に移植したときの心筋移植材の生着効率を向上することができる。
【0031】
なお、本実施形態においては、骨格筋芽細胞層形成ステップS1において、脂肪由来幹細胞Aをコンフルエントな状態まで増殖させることにより骨格筋芽細胞層2を形成することとしたが、これに代えて、図4に示されるように、細胞外基質からなるゲルEに骨格筋芽細胞Bを包埋することにより骨格筋芽細胞層2を形成してもよい。ゲルEとしては、細胞外基質を主成分とし、ゾル−ゲル転移温度が37℃より低いもの、例えば、コラーゲンゲル、アルギン酸ゲル、フィブリンゲルなどが用いられる。
【0032】
この場合、骨格筋芽細胞層2は、骨格筋芽細胞Bを懸濁したゾルを培養容器1内に収容した後、温度を37℃まで上昇させることにより形成することができる。
このようにすることで、骨格筋芽細胞Bをコンフルエントになるまで培養する必要がなくなり、骨格筋芽細胞層2の形成に要する時間を短縮することができる。
また、この場合、回収ステップS4において、心筋細胞Cを含むゲルEを小さく分割した状態で回収できるように、培養容器1内を複数の区画に分画する仕切り4が設けられていてもよい。
【0033】
また、本実施形態においては、播種ステップS2において、脂肪由来幹細胞Aを骨格筋芽細胞層2と脂肪由来幹細胞シートとの間に挟むこととしたが、骨格筋芽細胞Bを脂肪由来幹細胞Aと効率的に接触させることができれば、他の方法によりこれらの細胞A,Bを播種してもよい。
例えば、骨格筋芽細胞Bと脂肪由来幹細胞Aとを予め混合し、これらの細胞A,Bを同時に培養容器1内に播種してもよい。この場合、細胞A,B同士が効率良く接着するように、コラーゲン、アルギン酸またはフィブリンなどの細胞外基質の成分からなるゲルに細胞A,Bを混合した状態で播種することが好ましい。
【0034】
また、本実施形態においては、培養容器1として、温度応答性培養容器を使用することとしたが、これに代えて、少なくとも底面が、細胞が接着しにくい非細胞接着性の材料でコートされたものを用いることとしてもよい。このようにすることで、培養容器1内に播種された骨格筋芽細胞Bおよび脂肪由来幹細胞Aは、底面に接着せずに、細胞A,B同士で互いに接着して細胞凝集塊を形成する。この場合、心筋移植材として、細胞凝集塊が溶媒に懸濁されたものが製造される。
【0035】
これにより、骨格筋芽細胞層2を形成しなくても、骨格筋芽細胞Bと脂肪由来幹細胞Aとを効率良く接触させた状態で培養して骨格筋芽細胞Bの心筋細胞Cへの分化を効率良く誘導することができるとともに、骨格筋芽細胞Bと脂肪由来幹細胞Aによる細胞外基質の分泌を促すことができる。また、回収ステップS4においてタンパク質分解酵素を使用せずに細胞A,Cを回収できるので、温度応答性培養容器を使用したときと同様に、心筋移植材の生着効率を向上することができる。
【0036】
細胞非接着性の材料で底面が被覆された培養容器1を使用する場合、細胞凝集塊の大きさが比較的小さな寸法で略均一に揃うように、図4に示されるように、培養容器1内に仕切り4が設けられている、または、図5に示されるように、底面に略均一に分布する凹部5を形成されていることが好ましい。これにより、心筋移植材を注射器を使用して生体に移植する場合に、注射針が詰ったりすることなく、スムーズに移植することができる。
【0037】
また、本実施形態においては、回収ステップS4の後に脂肪由来細胞を除去する脂肪由来幹細胞除去ステップが行われてもよい。これにより、心筋移植材に含まれる心筋細胞Cの純度を高め、移植したときの治療効果を向上することができる。
【0038】
脂肪由来幹細胞を除去する方法としては、例えば、回収ステップS4において回収した細胞シートをトリプシンなどのタンパク質分解酵素で処理することにより単一細胞に分散させた後、新しい培養容器内で短時間、例えば、30〜60分間培養する。これにより、接着力の強い脂肪由来幹細胞Aは培養容器1の底面に十分に強く接着し、脂肪由来幹細胞Aに比べて接着力の弱い心筋細胞Cは培養容器1の底面に接着せずに培地D内で浮遊したままとなる。したがって、短時間の培養の後に培地Dを回収することにより、脂肪由来幹細胞Aを培養容器1内に残して心筋細胞Cを選択的に回収することができる。
【0039】
あるいは、脂肪由来幹細胞除去ステップは、回収ステップS4で回収した細胞群から、抗体を使用して脂肪由来幹細胞Aを除去することにより行われてもよい。この場合は、抗CD34抗体に陰性かつ抗CD90抗体に陽性の細胞を脂肪由来幹細胞Aとして除去すればよい。
【0040】
また、本実施形態においては、間葉系幹細胞として脂肪由来幹細胞を用いることとしたが、これに代えて、脂肪組織から分離された脂肪由来細胞群を用いることとしてもよい。脂肪由来細胞群には、脂肪由来幹細胞が十分に豊富に含まれているので、脂肪由来細胞群をそのまま播種ステップS2において播種しても、骨格筋芽細胞Bを十分に効率良く分化させることができる。
【実施例】
【0041】
次に、上述した実施形態の実施例について、図6及び図7を参照して説明する。
脂肪由来幹細胞により骨格筋芽細胞の心筋細胞への分化が誘導されることを確かめるため、以下の実験を行った。
【0042】
まず、24ウェルのプレートの各ウェル内で骨格筋芽細胞を2〜4日間、コンフルエントになるまで培養し、各ウェルの底面上に形成された骨格筋芽細胞層を層状のまま剥離することにより、骨格筋芽細胞シートを作成した。作成した骨格筋芽細胞シートを、直径35mmの培養容器内に敷き、その上にGFP(緑色蛍光タンパク質)で標識した脂肪由来幹細胞の懸濁液を5〜10μl滴下し、滴下した懸濁液の上からもう1枚の骨格筋芽細胞シートをかぶせた。そして、10%FBSを添加したDMEM内で、温度37℃、二酸化炭素濃度5%の環境で培養した。
【0043】
培養後、心筋細胞に特異的に発現するタンパク質であるトロポニンを蛍光色素で標識し、蛍光顕微鏡で観察した。その観察結果を図6および図7に示す。図6および図7はそれぞれ、4日間培養した後の脂肪由来幹細胞の蛍光画像またはトロポニンの蛍光画像である。なお、本実施例においては、心筋細胞のマーカとしてトロポニンを蛍光標識したが、これに代えて、Nkx2.5、α−MHCまたはGATA−4を蛍光標識してもよい。
【0044】
図6及び図7に示されるように、骨格筋芽細胞を脂肪由来幹細胞と共に培養することにより、骨格筋芽細胞シートを敷いた領域全体にわたってトロポニンの蛍光が観察された。このことから、脂肪由来幹細胞により骨格筋芽細胞の心筋細胞への分化が誘導されることが確認された。
【符号の説明】
【0045】
1 培養容器
2 骨格筋芽細胞層
3 グリッド(仕切り)
4 仕切り
5 凹部
S1 骨格筋芽細胞層形成ステップ
S2 播種ステップ
S3 培養ステップ
S4 回収ステップ
A 脂肪由来幹細胞(間葉系幹細胞)
B 骨格筋芽細胞
C 心筋細胞
D 培地
E ゲル
【技術分野】
【0001】
本発明は、骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材に関するものである。
【背景技術】
【0002】
従来、脂肪由来幹細胞を目的の部位の分化した細胞(成熟細胞)と混合して培養することにより、脂肪由来幹細胞を分化させる方法が知られている(例えば、特許文献1参照。)。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特表2007−507202号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
しかしながら、成熟細胞の数に対して分化させることができる幹細胞の数は限られている。したがって、特許文献1の場合、例えば、目的の部位が病変していて正常な成熟細胞の存在する領域が限られていたり、目的の部位の成熟細胞が元々わずかしか存在しなかったりする場合、必要な量の成熟細胞を確保することが難しいため、幹細胞から分化させて得られる細胞の量に限界がある。また、そのような部位から成熟細胞を採取することによる患者の負担も大きい。特に、必要な成熟細胞が、心筋細胞のように体外で培養して増殖させることが困難な細胞である場合、必要な量の細胞を幹細胞から分化させて得ることが非常に難しい。
【0005】
本発明は、上述した事情に鑑みてなされたものであって、患者への負担を軽減しながら十分な量の心筋細胞を得ることができる骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材を提供することを目的とする。
【課題を解決するための手段】
【0006】
上記目的を達成するため、本発明は以下の手段を提供する。
本発明は、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップを備える骨格筋芽細胞の心筋細胞への分化方法を提供する。
本発明によれば、培養ステップにおいて脂肪由来幹細胞が骨格筋芽細胞の心筋細胞への分化を誘導することにより、心筋細胞を得ることができる。このように、心筋以外の部位に比較的豊富に存在する骨格筋芽細胞から心筋細胞が分化させられるので、患者への負担を軽減しながら、十分な量の心筋細胞を得ることができる。
【0007】
上記発明においては、前記間葉系幹細胞が、脂肪組織から分離された脂肪由来幹細胞であってもよい。
このようにすることで、脂肪組織は、生体内に豊富に存在するうえ採取が比較的容易であり、さらに間葉系幹細胞である脂肪由来幹細胞を比較的豊富に含んでいるので、間葉系幹細胞の採取に伴う患者への負担を軽減することができる。
【0008】
また、本発明は、骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップと、該培養ステップによって前記骨格筋芽細胞から分化した心筋細胞を回収する回収ステップとを備える心筋移植材の製造方法を提供する。
本発明によれば、培養ステップによって骨格筋芽細胞から分化した心筋細胞を回収ステップにおいて回収することにより、患者への負担を軽減しながら十分な量の心筋細胞を含む心筋移植材を製造することができる。
【0009】
上記発明においては、前記培養ステップの前に、培養容器の底面上に骨格筋芽細胞からなる骨格筋芽細胞層を形成する骨格筋芽細胞層形成ステップを備え、前記培養ステップが、前記培養容器内に前記間葉系幹細胞を播種して培養してもよい。
このようにすることで、骨格筋芽細胞を脂肪由来幹細胞と効率良く接触させて骨格筋芽細胞の分化効率を向上することができる。
【0010】
また、上記発明においては、前記培養ステップが、培養温度より低い下限臨界溶解温度を有するポリマにより底面が被覆された培養容器内で前記骨格筋芽細胞を前記培養温度で培養し、前記回収ステップが、前記培養容器を前記培養温度より低い温度に冷却させることにより前記心筋細胞を前記底面から剥離させて回収してもよい。
【0011】
このようにすることで、タンパク質分解酵素などの薬剤を添加することなく心筋移植材を製造することができる。また、これにより培養中に細胞が分泌した細胞外基質が分解されることなく残るので、生体に移植されたときに細胞外基質が接着剤として働くことにより生体への生着効率を向上することができる。また、培養容器内に骨格筋芽細胞層を形成した場合には、シート形状の心筋移植材を容易に製造できる。
【0012】
また、上記発明においては、前記培養ステップが、細胞非接着性の底面を有する培養容器内で前記骨格筋芽細胞を培養してもよい。
このようにすることで、骨格筋芽細胞および脂肪由来幹細胞は底面に接着せずに細胞同士で互いに接着して細胞凝集塊を形成する。これにより、骨格筋芽細胞および脂肪由来幹細胞の細胞外基質の分泌が促されるとともに、分化した心筋細胞がタンパク質分解酵素を使用せずに培養容器内から回収されるので、生体に移植したときの生着効率を向上することができる。
【0013】
また、上記発明においては、前記培養容器が、略均一に分布する複数の凹部を底面に有していてもよい。
このようにすることで、略均一な数の骨格筋芽細胞および脂肪由来幹細胞が各凹部に集合するので、各細胞凝集塊に含まれる心筋細胞の数を略均一に揃えることができる。また、心筋移植材として細胞凝集塊の分散液が製造されるので、心筋移植材を注射によって容易に移植できる。
【0014】
また、上記発明においては、前記培養容器は、前記骨格筋芽細胞および前記脂肪由来幹細胞の移動を制限する仕切りによって底面が複数の区画に分画されていてもよい。
このようにすることで、比較的小さく分割されたシート形状で、または、細胞凝集塊の分散液として心筋移植材が製造されるので、心筋移植材を注射によって容易に移植することができる。
【0015】
また、上記発明においては、前記培養ステップの後に前記脂肪由来幹細胞を除去する脂肪由来幹細胞除去ステップを備えていてもよい。
このようにすることで、心筋細胞の純度を向上し、移植したときの治療効果を向上することができる。
また、本発明は、上記いずれかに記載の心筋移植材の製造方法により製造された心筋移植材を提供する。
【発明の効果】
【0016】
本発明によれば、患者への負担を軽減しながら十分な量の心筋細胞を得ることができるという効果を奏する。
【図面の簡単な説明】
【0017】
【図1】本発明の一実施形態に係る骨格筋芽細胞の心筋細胞への分化方法を示すフローチャートである。
【図2】播種ステップにおける培養容器内を模式的に示した図である。
【図3】培養ステップにおける培養容器内を模式的に示した図である。
【図4】骨格筋芽細胞層の変形例および培養容器の変形例を示す図である。
【図5】培養容器のもう1つ変形例を示す図である。
【図6】骨格筋芽細胞を脂肪由来幹細胞と共に4日間培養したときの脂肪由来幹細胞の蛍光染色画像である。
【図7】骨格筋芽細胞を脂肪由来幹細胞と共に4日間培養したときのトロポニンの蛍光染色画像である。
【発明を実施するための形態】
【0018】
以下に、本発明の一実施形態に係る骨格筋芽細胞の心筋細胞への分化方法、心筋移植材の製造方法および心筋移植材について、図1〜図5を参照して説明する。
本実施形態に係る心筋移植材の製造方法は、図1に示されるように、培養容器1の底面上に骨格筋芽細胞層2を形成する骨格筋芽細胞層形成ステップS1と、培養容器1に間葉系幹細胞Aを播種する播種ステップS2と、培養容器1内で間葉系幹細胞Aと共に骨格筋芽細胞Bを培養する培養ステップS3と、該培養ステップS3において骨格筋芽細胞Bから分化した心筋細胞Cを回収する回収ステップS4とを備えている。
【0019】
本実施形態に係る骨格筋芽細胞の心筋細胞への分化方法は、培養ステップS3に相当する。
本実施形態においては、間葉系幹細胞Aとして、患者の脂肪組織から抽出した脂肪由来幹細胞Aを用いることとするが、例えば、患者の骨髄などの他の組織由来の間葉系幹細胞も同様に用いることができる。脂肪由来幹細胞Aは、脂肪組織を消化酵素で分解することにより脂肪組織から脂肪由来細胞群を分離し、分離した脂肪由来細胞群から抗CD34抗体に陰性かつ抗CD90抗体に陽性の細胞を選択することにより、脂肪組織から抽出できる。
【0020】
骨格筋芽細胞層形成ステップS1は、骨格筋芽細胞Bを培養容器1内でコンフルエントな状態まで培養することにより行われる。骨格筋芽細胞Bは、通常の培養条件、すなわち、培養温度37℃、二酸化炭素濃度5%の環境で培養される。これにより、培養容器1の底面が略全体にわたって骨格筋芽細胞層2により覆われる。骨格筋芽細胞Bとしては、患者の骨格筋組織から抽出して培養により増殖させたものが用いられる。
【0021】
ここで、培養容器1としては、温度応答性培養容器が用いられる。温度応答性培養容器は、骨格筋芽細胞層形成ステップS1および後述する培養ステップS3における培養温度より低い下限臨界溶解温度を有する温度応答性ポリマにより、底面が被覆されている。温度応答性培養容器内で骨格筋芽細胞Bをコンフルエントな状態まで増殖させた後、温度応答性培養容器の温度を下限臨界溶解温度より低い温度まで下降させることにより、骨格筋芽細胞層2が底面上に浮いた状態となる。これにより、骨格筋芽細胞層2をシート形状のまま底面から容易に剥がして回収することができる。
【0022】
また、培養容器1の底面は、細胞非接着性の材料からなる格子状のグリッド(仕切り)3が設けられている。骨格筋芽細胞Bおよび脂肪由来幹細胞Aは、グリッド3上を避けて移動および増殖するので、後述する培養ステップS3において、グリッド3によって分画された各区画内において増殖する。これにより、培養容器1の温度を温度応答性ポリマの下限臨界溶解温度より低い温度まで下降させたときに、小さく分割された複数の細胞シートが底面上に浮く。細胞非接着性の材料としては、例えば、エチレングリコール誘導体が用いられる。
【0023】
播種ステップS2は、骨格筋芽細胞層形成ステップS1により形成された骨格筋芽細胞層2上に脂肪由来幹細胞Aを播種した後、骨格筋芽細胞層2上に接着した脂肪由来幹細胞Aの上から骨格筋芽細胞Bからなる細胞シートをかぶせることにより行われる。これにより、図2に示されるように、骨格筋芽細胞Bの間に脂肪由来幹細胞Aが挟まれ、骨格筋芽細胞Bが脂肪由来幹細胞Aと密に接触させられた状態になる。骨格筋芽細胞Bからなる細胞シートは、他の温度応答性培養容器内で骨格筋芽細胞Bをコンフルエントな状態まで増殖させた後に、形成された骨格筋芽細胞層を温度応答性培養容器の底面から剥離することにより作成される。
【0024】
培養ステップS3は、通常の細胞培養に用いられる条件で骨格筋芽細胞Bと脂肪由来幹細胞Aを培養することにより行われる。具体的には、培地Dとして10%FBSを添加したDMEM(ダルベッコ改変イーグル培地)を用い、培養温度37℃、二酸化炭素濃度5%の環境で、骨格筋芽細胞Bと脂肪由来幹細胞Aを培養する。これにより、図3に示されるように、骨格筋芽細胞Bは、脂肪由来幹細胞Aによって心筋細胞Cへの分化が誘導される。
【0025】
ここで、骨格筋芽細胞Bおよび脂肪由来幹細胞Aが互いに密に接着した状態で培養されることにより、これらの細胞A,Bから細胞外基質が盛んに分泌される。分泌された細胞外基質は、生体内に移植されたときに生体内の組織との接着剤として働くことにより、心筋移植材の生着効率を向上させる。
【0026】
回収ステップS4は、培養容器1内の培地Dを生理食塩水などの溶媒に交換した後、培養容器1の温度を下限臨界溶解温度より低い温度まで下降させ、溶媒中に浮いた細胞シートを溶媒と共に注射器などで吸引することにより行われる。これにより、心筋細胞Cを含む比較的小さな細胞シートが溶媒に懸濁された本実施形態に係る心筋移植材を製造することができる。
【0027】
このようにして製造された心筋移植材の移植は、例えば、心筋に注射することにより行われる。このときに、細胞シートが比較的小さく分割されているので、細径の注射針を使用した場合でもスムーズに心筋移植材を移植することができる。
【0028】
ここで、心筋の一部が病変していたりその一部を切除したりした場合など、同じ部位から心筋細胞を採取することは患者の負担を増大させるため、採取できる心筋細胞の量は少量に限られる。また、心筋細胞の場合、採取後に体外で培養により増殖させることは困難である。したがって、従来の、患者から採取した心筋細胞により幹細胞の心筋細胞への分化を誘導させる方法では、分化させることができる幹細胞の量が少量に限られ、十分な量の心筋細胞を得ることが難しかった。
【0029】
これに対して、本実施形態によれば、生体内に比較的豊富に存在し生体内からの採取が比較的容易な骨格筋組織および脂肪組織からそれぞれ抽出された骨格筋芽細胞Bおよび脂肪由来幹細胞Aを使用して心筋移植材が製造される。したがって、患者の体内から心筋細胞を採取することが困難な場合でも、治療に十分な量の心筋細胞Cを含んだ心筋移植材を製造することができるとともに、細胞の採取による患者への負担を軽減することができる。
【0030】
また、温度応答性培養容器を使用することにより、トリプシンなどのタンパク質分解酵素を使用せずに、細胞A,Cを培養容器1から回収することができる。したがって、培養ステップS3において細胞A,Bから分泌された細胞外基質が分解されることなく残されるので、生体内に移植したときの心筋移植材の生着効率を向上することができる。
【0031】
なお、本実施形態においては、骨格筋芽細胞層形成ステップS1において、脂肪由来幹細胞Aをコンフルエントな状態まで増殖させることにより骨格筋芽細胞層2を形成することとしたが、これに代えて、図4に示されるように、細胞外基質からなるゲルEに骨格筋芽細胞Bを包埋することにより骨格筋芽細胞層2を形成してもよい。ゲルEとしては、細胞外基質を主成分とし、ゾル−ゲル転移温度が37℃より低いもの、例えば、コラーゲンゲル、アルギン酸ゲル、フィブリンゲルなどが用いられる。
【0032】
この場合、骨格筋芽細胞層2は、骨格筋芽細胞Bを懸濁したゾルを培養容器1内に収容した後、温度を37℃まで上昇させることにより形成することができる。
このようにすることで、骨格筋芽細胞Bをコンフルエントになるまで培養する必要がなくなり、骨格筋芽細胞層2の形成に要する時間を短縮することができる。
また、この場合、回収ステップS4において、心筋細胞Cを含むゲルEを小さく分割した状態で回収できるように、培養容器1内を複数の区画に分画する仕切り4が設けられていてもよい。
【0033】
また、本実施形態においては、播種ステップS2において、脂肪由来幹細胞Aを骨格筋芽細胞層2と脂肪由来幹細胞シートとの間に挟むこととしたが、骨格筋芽細胞Bを脂肪由来幹細胞Aと効率的に接触させることができれば、他の方法によりこれらの細胞A,Bを播種してもよい。
例えば、骨格筋芽細胞Bと脂肪由来幹細胞Aとを予め混合し、これらの細胞A,Bを同時に培養容器1内に播種してもよい。この場合、細胞A,B同士が効率良く接着するように、コラーゲン、アルギン酸またはフィブリンなどの細胞外基質の成分からなるゲルに細胞A,Bを混合した状態で播種することが好ましい。
【0034】
また、本実施形態においては、培養容器1として、温度応答性培養容器を使用することとしたが、これに代えて、少なくとも底面が、細胞が接着しにくい非細胞接着性の材料でコートされたものを用いることとしてもよい。このようにすることで、培養容器1内に播種された骨格筋芽細胞Bおよび脂肪由来幹細胞Aは、底面に接着せずに、細胞A,B同士で互いに接着して細胞凝集塊を形成する。この場合、心筋移植材として、細胞凝集塊が溶媒に懸濁されたものが製造される。
【0035】
これにより、骨格筋芽細胞層2を形成しなくても、骨格筋芽細胞Bと脂肪由来幹細胞Aとを効率良く接触させた状態で培養して骨格筋芽細胞Bの心筋細胞Cへの分化を効率良く誘導することができるとともに、骨格筋芽細胞Bと脂肪由来幹細胞Aによる細胞外基質の分泌を促すことができる。また、回収ステップS4においてタンパク質分解酵素を使用せずに細胞A,Cを回収できるので、温度応答性培養容器を使用したときと同様に、心筋移植材の生着効率を向上することができる。
【0036】
細胞非接着性の材料で底面が被覆された培養容器1を使用する場合、細胞凝集塊の大きさが比較的小さな寸法で略均一に揃うように、図4に示されるように、培養容器1内に仕切り4が設けられている、または、図5に示されるように、底面に略均一に分布する凹部5を形成されていることが好ましい。これにより、心筋移植材を注射器を使用して生体に移植する場合に、注射針が詰ったりすることなく、スムーズに移植することができる。
【0037】
また、本実施形態においては、回収ステップS4の後に脂肪由来細胞を除去する脂肪由来幹細胞除去ステップが行われてもよい。これにより、心筋移植材に含まれる心筋細胞Cの純度を高め、移植したときの治療効果を向上することができる。
【0038】
脂肪由来幹細胞を除去する方法としては、例えば、回収ステップS4において回収した細胞シートをトリプシンなどのタンパク質分解酵素で処理することにより単一細胞に分散させた後、新しい培養容器内で短時間、例えば、30〜60分間培養する。これにより、接着力の強い脂肪由来幹細胞Aは培養容器1の底面に十分に強く接着し、脂肪由来幹細胞Aに比べて接着力の弱い心筋細胞Cは培養容器1の底面に接着せずに培地D内で浮遊したままとなる。したがって、短時間の培養の後に培地Dを回収することにより、脂肪由来幹細胞Aを培養容器1内に残して心筋細胞Cを選択的に回収することができる。
【0039】
あるいは、脂肪由来幹細胞除去ステップは、回収ステップS4で回収した細胞群から、抗体を使用して脂肪由来幹細胞Aを除去することにより行われてもよい。この場合は、抗CD34抗体に陰性かつ抗CD90抗体に陽性の細胞を脂肪由来幹細胞Aとして除去すればよい。
【0040】
また、本実施形態においては、間葉系幹細胞として脂肪由来幹細胞を用いることとしたが、これに代えて、脂肪組織から分離された脂肪由来細胞群を用いることとしてもよい。脂肪由来細胞群には、脂肪由来幹細胞が十分に豊富に含まれているので、脂肪由来細胞群をそのまま播種ステップS2において播種しても、骨格筋芽細胞Bを十分に効率良く分化させることができる。
【実施例】
【0041】
次に、上述した実施形態の実施例について、図6及び図7を参照して説明する。
脂肪由来幹細胞により骨格筋芽細胞の心筋細胞への分化が誘導されることを確かめるため、以下の実験を行った。
【0042】
まず、24ウェルのプレートの各ウェル内で骨格筋芽細胞を2〜4日間、コンフルエントになるまで培養し、各ウェルの底面上に形成された骨格筋芽細胞層を層状のまま剥離することにより、骨格筋芽細胞シートを作成した。作成した骨格筋芽細胞シートを、直径35mmの培養容器内に敷き、その上にGFP(緑色蛍光タンパク質)で標識した脂肪由来幹細胞の懸濁液を5〜10μl滴下し、滴下した懸濁液の上からもう1枚の骨格筋芽細胞シートをかぶせた。そして、10%FBSを添加したDMEM内で、温度37℃、二酸化炭素濃度5%の環境で培養した。
【0043】
培養後、心筋細胞に特異的に発現するタンパク質であるトロポニンを蛍光色素で標識し、蛍光顕微鏡で観察した。その観察結果を図6および図7に示す。図6および図7はそれぞれ、4日間培養した後の脂肪由来幹細胞の蛍光画像またはトロポニンの蛍光画像である。なお、本実施例においては、心筋細胞のマーカとしてトロポニンを蛍光標識したが、これに代えて、Nkx2.5、α−MHCまたはGATA−4を蛍光標識してもよい。
【0044】
図6及び図7に示されるように、骨格筋芽細胞を脂肪由来幹細胞と共に培養することにより、骨格筋芽細胞シートを敷いた領域全体にわたってトロポニンの蛍光が観察された。このことから、脂肪由来幹細胞により骨格筋芽細胞の心筋細胞への分化が誘導されることが確認された。
【符号の説明】
【0045】
1 培養容器
2 骨格筋芽細胞層
3 グリッド(仕切り)
4 仕切り
5 凹部
S1 骨格筋芽細胞層形成ステップ
S2 播種ステップ
S3 培養ステップ
S4 回収ステップ
A 脂肪由来幹細胞(間葉系幹細胞)
B 骨格筋芽細胞
C 心筋細胞
D 培地
E ゲル
【特許請求の範囲】
【請求項1】
骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップを備える骨格筋芽細胞の心筋細胞への分化方法。
【請求項2】
前記間葉系幹細胞が、脂肪組織から分離された脂肪由来幹細胞である請求項1に記載の骨格筋芽細胞の心筋細胞への分化方法。
【請求項3】
骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップと、
該培養ステップによって前記骨格筋芽細胞から分化した心筋細胞を回収する回収ステップとを備える心筋移植材の製造方法。
【請求項4】
前記培養ステップの前に、培養容器の底面上に骨格筋芽細胞からなる骨格筋芽細胞層を形成する骨格筋芽細胞層形成ステップを備え、
前記培養ステップが、前記培養容器内に前記間葉系幹細胞を播種して培養する請求項3に記載の心筋移植材の製造方法。
【請求項5】
前記培養ステップが、培養温度より低い下限臨界溶解温度を有するポリマにより底面が被覆された培養容器内で前記骨格筋芽細胞を前記培養温度で培養し、
前記回収ステップが、前記培養容器を前記培養温度より低い温度に冷却させることにより前記心筋細胞を前記底面から剥離させて回収する請求項3または請求項4に記載の心筋移植材の製造方法。
【請求項6】
前記培養ステップが、細胞非接着性の底面を有する培養容器内で前記骨格筋芽細胞を培養する請求項3に記載の心筋移植材の製造方法。
【請求項7】
前記培養容器が、略均一に分布する複数の凹部を底面に有する請求項6に記載の心筋移植材の製造方法。
【請求項8】
前記培養容器は、前記骨格筋芽細胞および前記脂肪由来幹細胞の移動を制限する仕切りによって底面が複数の区画に分画されている請求項5または請求項6に記載の心筋移植材の製造方法。
【請求項9】
前記培養ステップの後に前記脂肪由来幹細胞を除去する脂肪由来幹細胞除去ステップを備える請求項3に記載の心筋移植材の製造方法。
【請求項10】
請求項3から請求項9のいずれかに記載の心筋移植材の製造方法により製造された心筋移植材。
【請求項1】
骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップを備える骨格筋芽細胞の心筋細胞への分化方法。
【請求項2】
前記間葉系幹細胞が、脂肪組織から分離された脂肪由来幹細胞である請求項1に記載の骨格筋芽細胞の心筋細胞への分化方法。
【請求項3】
骨格筋芽細胞を間葉系幹細胞と接触させた状態で培養する培養ステップと、
該培養ステップによって前記骨格筋芽細胞から分化した心筋細胞を回収する回収ステップとを備える心筋移植材の製造方法。
【請求項4】
前記培養ステップの前に、培養容器の底面上に骨格筋芽細胞からなる骨格筋芽細胞層を形成する骨格筋芽細胞層形成ステップを備え、
前記培養ステップが、前記培養容器内に前記間葉系幹細胞を播種して培養する請求項3に記載の心筋移植材の製造方法。
【請求項5】
前記培養ステップが、培養温度より低い下限臨界溶解温度を有するポリマにより底面が被覆された培養容器内で前記骨格筋芽細胞を前記培養温度で培養し、
前記回収ステップが、前記培養容器を前記培養温度より低い温度に冷却させることにより前記心筋細胞を前記底面から剥離させて回収する請求項3または請求項4に記載の心筋移植材の製造方法。
【請求項6】
前記培養ステップが、細胞非接着性の底面を有する培養容器内で前記骨格筋芽細胞を培養する請求項3に記載の心筋移植材の製造方法。
【請求項7】
前記培養容器が、略均一に分布する複数の凹部を底面に有する請求項6に記載の心筋移植材の製造方法。
【請求項8】
前記培養容器は、前記骨格筋芽細胞および前記脂肪由来幹細胞の移動を制限する仕切りによって底面が複数の区画に分画されている請求項5または請求項6に記載の心筋移植材の製造方法。
【請求項9】
前記培養ステップの後に前記脂肪由来幹細胞を除去する脂肪由来幹細胞除去ステップを備える請求項3に記載の心筋移植材の製造方法。
【請求項10】
請求項3から請求項9のいずれかに記載の心筋移植材の製造方法により製造された心筋移植材。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【公開番号】特開2012−235731(P2012−235731A)
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願番号】特願2011−106552(P2011−106552)
【出願日】平成23年5月11日(2011.5.11)
【出願人】(591173198)学校法人東京女子医科大学 (48)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
【公開日】平成24年12月6日(2012.12.6)
【国際特許分類】
【出願日】平成23年5月11日(2011.5.11)
【出願人】(591173198)学校法人東京女子医科大学 (48)
【出願人】(000000376)オリンパス株式会社 (11,466)
【Fターム(参考)】
[ Back to top ]

