高分子システムを変性する方法
【課題】高分子を変性する方法を提供する。
【解決手段】(i);高分子を提供する工程、(ii);式(I)を有する化合物を提供する工程、および(iii);式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程、を包含する高分子を変性する方法。

(Nは保護基Pで保護されたアミノ基で、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され、Xは反応性基である。)
【解決手段】(i);高分子を提供する工程、(ii);式(I)を有する化合物を提供する工程、および(iii);式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程、を包含する高分子を変性する方法。

(Nは保護基Pで保護されたアミノ基で、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され、Xは反応性基である。)
【発明の詳細な説明】
【技術分野】
【0001】
本発明は高分子を変性する方法、特に反応性部分、アルキレンオキシドスペーサーアームおよび保護された第1級アミンを有する官能性基を有する分子体との官能化によってポリマーマトリックスを変性する方法に関する。
【背景技術】
【0002】
大きな生体分子およびポリマー材料を包含する種々の高分子システム(macromolecular system)(要するに高分子物(macromolecules))を特殊な官能化をする必要性が高い。第1級アミンは大変有用な官能性基であって、種々の化学反応の反応点のみならず高分子システムの物理化学性能を変性するのに用いられ得る。
【0003】
多くの用途において、官能基に好適なアクセスを確保するために、官能基を長い化学的なスペーサーを介して高分子系に付加することが要求されることがある。ポリ−またはオリゴ−アルキレンオキシドはそのような官能性アームのために用いられ得る分子フラグメントの一群であって、用途による生物学的または化学的環境に対する高い適合性を示す。
【0004】
そのような分子体がアミン官能化された生成物を形成するのに有用な高分子システムには、生物分子(例えば、タンパク質やヌクレオチド)、ペプチド合成のためのビーズ材料、クロマトグラフィーのための樹脂、濾過用ポリマー材料ならびに医学用成分に用いられる表面層、生体内および生体外診断成分、分析システムなどが挙げられる。
【0005】
文献中には、固体相合成やクロマトグラフィーなどの用途に用いられるポリマー樹脂に第1級アミンを官能性基として導入する多くの方法が存在する。これらの方法の多くはアミン基をポリマー骨格に直接または短い(10原子以下)つなぎを介して結合する。その例としては脱プロトン化されたフタルイミドと第1級アルキルハライドとを反応した後、イミドをヒドラジン分解(hydrazinolysis)する方法およびアジドとアルキルハライドまたはトシレートを反応した後還元する方法である。また、ブロモエチルフタルイミドと高分子上のアルコキシド残基とを反応した後、ヒドラジン分解する方法も多くの場合有用であることが分かっている。多くの場合、第1級アミン官能性はポリマー樹脂に付加された長いアルコキシドスペーサーアーム上の末端官能基として得られる。これらの場合は、第1級アミン−アルコキシドスペーサーアーム部分は段階的方法、すなわちアルコキシドスペーサーアームを付加して、その後第1級アミンを上記反応を用いてアルコキシドスペーサーアームに付加することにより形成されている。上記方法を包含する化学は異常に厳しい条件が必要であり、しばしば高分子システムと不適合であったりする。特に、生物学的高分子は劣下し、またクロマトグラフィーに用いる樹脂はそのような条件下で損害を受ける。後者の場合、多孔性樹脂にとって特に重要であって、厳しい条件が樹脂の多孔性を変化する。また、上記反応はほとんど定量的でなく、不必要な副生成物を形成する。
【0006】
一端がアミンで一端がヒドロキシドであるエチレングリコールから調製された非対称アルキレンオキシドも存在する。これらの化合物は主として短いオリゴマー状で存在し、対称アルキレンオキシドからの分離が可能である。さらに、これらの化合物の高い製造コストや高分子システムに強く反応する反応基にヒドロキシル基を選択的に変更することの難しさが、高分子システムの官能化のためにこれらの化合物を工業的に用いることを非常に制限する。
【0007】
エタノールアミンをアミドまたはイミド保護基と直接エトキシ化することによって調製される非対称pegの例が以下の文献に記載されている。
【0008】
ランジ・アンド・ワール(Lange and Wahl)(Bull.Chim.Soc.Fr.1951、340−342)には、N−アセチルエタノールアミンのエトキシル化からモノおよびジエタノール化誘導体を形成することが記載されている。ロントジェンツ(Lontjens)ら(Polym.Bull.30、1933、pp489−494)には、モノアミノポリエチレングリコールを高温のエトキシル化反応で合成することが記載されているが、多くの副生成物を生成する。Y−Iフアング(Y−I Huang)(J.polym.Sci.23、1985、pp.795−799)には、エタノールアミン−ベンズアルデヒドシッフ塩基をエトキシル化した後、加水分解してモノアミン置換ポリエチレングリコールを形成することが記載されている。後者の2つの例は、生成物を第1級アミンと反応して遊離のヒドロキシル基を有するポリマーを形成してしまう。いずれの場合も、第1級アミン誘導体が得られない。
【0009】
従って、高分子システムをアルコキシドスペーサーアームおよび第1級アミン官能性で効果的かつ安価に官能化することが可能な分子材料が望まれている。
【図面の簡単な説明】
【0010】
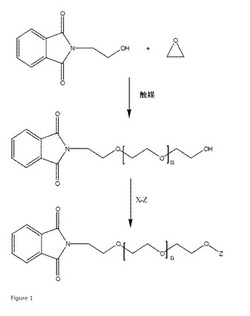
【図1】一般式(I)の化合物の調製を示す図であり、mは1であり、nは式(I)中、n−1に対応し、かつ図1中Zは式(I)中Xに相当する。
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明は高分子、特に合成もしくはクロマトグラフィー用途の固体状支持体として用いられるポリマーマトリックスを変性する方法に関する。
【0012】
特に、本発明は
(i)高分子を提供する工程;
(ii)一般式(I):
【化1】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含し、;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程;
を包含する高分子を変性する方法
に関する。
【0013】
(一般式(I)の化合物)
高分子、特にポリマーマトリックスの変性に有用な化合物は一般式(I):
【化2】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含するものであり;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基を示す。)
によって表わされる化合物であり得る。
【0014】
一般式(I)の化合物は「保護アミノ」−ポリ(オキシアミキレン)型を有すると認識される。従って、本発明の方法は高分子(例えば、ポリマーマトリックス)に一般に親水結合体を介して第1級アミノ基を導入するのに好適である。
【0015】
一般式(I)の化合物は保護基Pで保護された第1級アミノ基である{P}−N部分を含有し、該保護基は第1級アミノ基の2つの自由原子化を包含する。
【0016】
第1級アミノ基の2つの自由原子化を包含する保護基は典型的にはイミド型(RC(=O))2N−]およびイミン型[R−C=N−]で表わされるものである。
【0017】
例えば、イミド型保護基はコハク酸無水物/コハク酸(コハク酸イミド)およびフタル酸無水物/フタル酸(フタル酸イミド)から選択されるものであってよい。
【0018】
好ましい態様では、保護基はイミド型であり、最も好ましい保護基はコハク酸無水物/コハク酸(コハク酸イミド)およびフタル酸無水物/フタル酸(フタル酸イミド)、特にフタル酸無水物/フタル酸(フタルイミド)である。
【0019】
mは1〜12、例えば1〜6、具体的には1〜4、または1〜3、または1〜2の整数であり、特に1である。nは1〜2000、より典型的には1〜100、または1〜50、または1〜10または1〜8、例えば1〜6、または1〜5、または1〜4、または1〜3、または1〜2、または2〜6、または2〜4、または1である。
【0020】
R1およびR2は独立して水素またはC1−4−アルキルからなる群から選択される。
【0021】
C1−4−アルキルはメチル、エチル、1−プロピル、2−プロピル、1−ブチル、2−ブチル、t−ブチルおよび(2−メチル)−プロプ−1−イルを包含する。
【0022】
特定の例はR1およびR2が水素およびメチルから選択されているもの、即ちエチレングリコールおよびプロピレングリコール部分を有する化合物である。現在最も好ましい態様ではR1およびR2は全て水素であるものであり、すなわちエチレングリコール部分を有する化合物である。
【0023】
反応性基は高分子(例えばポリマーマトリックス)上の単純官能基、例えばアミン、アルコールおよびチオール官能性、必要であればそれらの基の活性化されたものと反応し得るものであってよい。この目的のためには、小さな環状エーテル、例えばオキシラン(エポキシド)およびオキシエタンを包含する反応性基を用いてもよく、官能基、例えばイソシアネート、カルボン酸、酸無水物または活性化ビニル化合物を用いてもよい。特定の例としてはオキシランまたはオキセタンを有する反応性基であり、好適なオキシラン含有反応性基(X)はエピクロロヒドリンから誘導されたものであってよい(実施例5)。反応性基の別の例としてはカルボン酸−含有反応性基(例えば実施例7に記載したもの)である。これらの実施例のいずれも、CH2基は反応性基Xの一部(実施例5におけるCH2(O)CHCH2−および実施例7におけるHOOCCH2−参照)として包含する。
【0024】
(一般式(I)の化合物の調製)
本発明の好ましい態様では、分子体はN−保護ヒドロキシアルキルアミンのポリアルコキシル化およびその後反応性部分をC−O結合を介しての付加することによって形成される。これは非対称ポリアルキレンオキシドに対するコスト効果の優れたルートであり、触媒および反応時間を注意深く選択することによって鎖長および純度の調整も得られる。さらに、アルキレンオキシド、例えばエチレンオキシドおよびプロピレンオキシドの含有量を調節することにより、生成物の分子構造および親水性をコントロールすることもできる。
【0025】
(保護ポリエチレングリコール−アルキルアミンの合成)
この合成の出発点は保護ヒドロキシアルキルアミン(b)である。簡単で有用なアルキルアミンの例は、エタノールアミン、3−ヒドロキシプロピルアミン、2−ヒドロキシプロピルアミンである。またより複雑なアミン、例えば3−オキシ−5−ヒドロキシ−1−ペンタンアミンまたは4−ヒドロキシメチル−ベンジルアミンを用いてもよい。
【0026】
ヒドロキシアルキルアミン(a)上のアミン基はエトキシル化およびその後の反応性部分への付加を可能にする保護基で保護される。保護基、例えばイミド、アミド、イミンまたは尿素誘導体がこの目的には有用である。エタノールアミンおよびフタル酸無水物から形成されたフタルイミド保護アミンが市販されている。単純なアミド保護と比べて窒素原子上に水素原子が存在せず、その結果その後の変性における求核攻撃に対して安定であるという利点を有する。一般のアミド保護アミン中のアミドプロトンがポリアルコキシド中の末端ヒドロキシル基と同等の酸性力を有し、それが不明確な置換反応を引き起こすので、このことは特に重要である。
【0027】
アミン基が保護されたら、遊離ヒドロキシル基が触媒の存在下にオキシランと反応して、ポリアルコキシ誘導体(c)を形成することができる。一般に使用されるオキシランには、エチレンオキシドおよびプロピレンオキシドまたはそれらの混合物が含まれる。触媒の選択および反応条件の選択は特に重要である。2−ヒドロキシエチルフタルイミドおよびエチレンオキシドとの間の反応に以前報告されている条件は、高濃度の水酸化ナトリウム触媒で160℃以上の温度を包含し、大きな分子量分布と高い濃度の不純物を有する濃い着色された生成物を形成する。本発明に例示されたように、温度および触媒の濃度を低くすることは許容される純度の生成物を提供する。ランタまたはランタニドベースの触媒を適用することは分子量分布の小さい非常に純粋な、ほとんど着色のない生成物を提供する。
【0028】
エチレンオキシドに基づくポリアルコキシドは親水性が高く生物的適合性が高い。エチレンオキシドの代わりにプロピレンオキシドを使用することは、水に比較的に溶けにくく、生物分子との疎水的相互反応をある程度を示す分子になる。2つのモノマーが共重合して、さらに親水性を制御してもよい。
【0029】
次に、ポリアルコキシ誘導体を反応性部分で官能化して、所望の分子体を得て、それが高分子システムを変性するのに用いられる。反応部分は高分子システム上の官能基、例えば前述のアミン、アルコール、チオールなどとの反応し得るべきである。
【0030】
本発明は、ある態様では一般式(I):
【化3】

(式中、{P}−Nはフタルイミド基であり、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は共に水素であり、およびXは反応性基である。)の化合物の調製方法を提供し、この方法は(a)フタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13−アルカンを提供する工程;(b)上記アルカンとエチレンオキシドとを触媒の存在下に反応する工程;および(c)工程(b)で得られた生成物の末端OH基を官能化することによる変性する工程を包含する。
【0031】
工程(b)中の反応は好ましくは大気(特に酸素)の不存在下で行われる。さらに、反応は典型的には圧力下、例えば2〜10バールおよび高温、例えば80〜200℃、具体的には100〜190℃で行われる。触媒の量は典型的にはフタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13−アルカンの量に基づいて1〜3%であり、この量はエチレンオキシドの当量で変化し、すなわちより高い量のエチレンオキシドを用いると、より高い触媒の量が必要である。使用されるエチレンオキシドの当量数は所望の鎖長、すなわち一般式(I)中の数字「n」に対応する。好適な触媒はNaOH、KOH、KOCH3、MEO−3およびMEO−LAから選択されるものである。
【0032】
工程(c)中の転換は反応性基の分子への酸素原子を介してのカップリング化または末端ヒドロキシ官能を対応するカルボン酸に、例えば酸化によって変更することによって、反応性基Xを導入するために行われる。これは実施例の部分に例示的に記載している。
【0033】
(一般式(I)の化合物の高分子へのグラフト化)
完全な分子体を次いで高分子システム(高分子)、例えばポリマーマトリックス、生体分子(酵素、タンパク質など)および材料表面を変性するために用い得る。高分子システム上での反応性基がアミン基である場合、反応が触媒なしでも進行し得るが、ヒドロキシル基(すなわち、アルコール)との反応においては触媒がしばしば用いられる。
【0034】
適当なポリマーマトリックスの例としては、PS、POEPS、POEPOP、SPOCC、PEGA、CLEAR、HYDRA、PEG−ポリアクリレート共重合体、ポリエーテル−ポリアミン共重合体および架橋ポリエチレンジ−アミン、エキスパンシン(Expansin)、ポリアミド、ジャンダゲル(Jandagel)、PS−BDODMA、PS−HDODA、PS−TTEGDA、PS−TEGDA、GDMA−PMMA、PS−TRPGDA、アルゴゲル(ArgoGel)、アルゴポール(Argopore)樹脂、トーヨーパール(Toyopearl)、他の架橋ポリアクリレート高容量PEGA、グラフトゲル(Fractogel)、セファデックス(Sephadex)、セファロース(Sepharose)、他の架橋アガロースおよび上記の誘導体から選択されるものである。
【0035】
最終段階で、アルコキシド側鎖上の末端第1級アミンの保護基を除去してもよい。フタルイミド保護基をヒドラジンまたはエチレンジアミンを含有する溶液で処理することによって外してもよく、イミンタイプの保護基は水中で低濃度の酸または塩基を用いる緩やかな条件下で加水分解してもよい。アミド型保護基はまた高温下に強塩基処理を必要とし、あまり好ましくない。
【0036】
上記方法を用いる場合、高分子システムを末端基として容易に入手できる第1級アミンで所望の親水性の官能化側鎖としてもよい。そのような高分子システムはそのように、またアミン基の化学変性によりさらに変性してもよい。
【0037】
アミン基を固体相化学のための出発点として用いてもよく、また、より複雑な分子、例えばタンパク質、ヌクレオチド、または親和リガンドに対する付着点として用いてもよい。そのような高分子システムはアミノ基の化学変性を介してそのようなまたは更に変性されてもよい。
【0038】
要するに、本発明は特定の高分子体の形成、およびそのような高分子体の高分子システムの変性への利用からなる。形成は以下の4つの工程からなる:
1.N−保護ヒドロキシアルキルアミンのアルコキシル化。
2.反応部分のポリアルキレンオキシドの遊離ヒドロキシ末端を介する付加。
3.反応性部分の高分子システムの官能基との反応。
4.N−保護基の解離による第1級アミンの放出。
【0039】
(特定の態様)
特定の態様において、本発明は高分子、特に高分子マトリックスの変性方法に関し、その方法は:
(i)高分子(例えば、ポリマーマトリックス)を提供する工程:
(ii)一般式(I):
【化4】

(式中、{P}−Nはフタルイミド基であり;
mは1であり、nは1〜100の整数を示し;
R1およびR2は両方とも水素であり;かつ
Xが反応性基、例えばオキシラン含有反応性基およびオキシラン含有オキセタン含有反応性基から選択され、特にオキセタン含有反応性基またはオキシタン含有反応性基である。)
の化合物を提供する工程;および
(iii)一般式(I)の化合物を高分子(例えば、ポリマーマトリックス)と反応させて、高分子上にグラフトを形成する工程;
を包含する。
【0040】
さらに特定の態様では、本発明は一般式(I)
【化5】

(式中、{P}−Nがフタルイミド基であり;
mが1で、nが1〜100の整数であり;
R1およびR2が共に水素であり;および
Xがオキセタン含有反応基またはオキシラン含有反応基である。)
で表わされる化合物を提供する。
【0041】
この態様では、Xは好ましくはCH2(O)CHCH2−(オキシラニル−メチル)を示す。
【0042】
(別の態様)
高分子は本明細書中において有機分子から誘導される骨格に基づくものを言うが、また本発明の方法はガラス基材(例えば、プレート、ビーズ、スティックなど)を変性するのにも有用である。そのような場合、反応性基(一般式(I)化合物におけるX)は問題のガラス基材のSi−OH表面基またはすでに変性されたガラス基材の表面基と反応し得るべきである。従って、好適な反応性基は時にはシラン型であってもよい。
【0043】
さらに別の態様でおいては、一般式(I)の化合物の反応性基Xはポリアルキレンオキシド鎖の脱水素末端−CH2−OHに対応する電子ペア、すなわち−CH2−O−Xが−CH2−O−であるものであってもよい。そのような反応性基は高分子のエポキシド基と反応してもよい。
【実施例】
【0044】
実施例1−N−(2−ヒドロキシエチル)−フタルイミドのアルコキシル化
合成を加熱マントル、内部冷却コイルおよび機械的攪拌装置を備えた3リットルオートクレーブ中で行う。
【0045】
触媒をN−(2−ヒドロキシエチル)−フタルイミド(HPI、Katwijk Chemie bv、オランダ)300gに添加した。反応器の内容物を130℃で窒素パージによって20分間乾燥した。その後、エチレンオキシドを選択した温度で3〜5バールのレベルで加圧をキープして加えた(以下参照)。エチレンオキシド(EO)640gを導入した後、生成物を反応温度で30分間処理した。得られたエトキシレートを40℃で取り出し、秤量した。
【0046】
【表1】

【0047】
MEO−3およびMEO−LA触媒はメキセオ(Mexeo)、PIによって開発された不均質ランタン触媒である。純度はMaldi Tofスペクトルに基づいて推測した。
【0048】
実施例2−アルコキシル化N−(2−ヒドロキシエチル)−フタルイミドのエピクロルヒドリンによる官能化
MEO−3触媒を用いて実施例1により調製したアルコキシル化N−(2−ヒドロキシエチル)−フタルイミドをアセトニトリル(5mL/gPEG、2x)の共沸蒸留により乾燥し、攪拌下におよび水分排出下にTHF中に溶解した。ナトリウムヒドリド(ミネラルオイル中60重量%分散体)を攪拌下に湿度を除去してPEG溶液に小さく区切って加えた。脱プロトン化反応が室温で2時間攪拌し、エピクロルヒドリンを滴下し、反応を40℃で12時間攪拌した。溶液を真空中で蒸気蒸留し、残渣をアセトニトリル(25mL)と混合した。沈殿したナトリウム塩を8000r.p.mの遠心分離により20分間分離し、上澄み液を真空中で蒸留した。得られた生成物をヘプタン(3×25mL)で洗って、ミネラルオイルを除去し、高真空下に乾燥した。
【0049】
実施例3−ポリマーマトリックス上へのグラフト化
実施例2で得られた生成物を実施例9の記載の通りポリマーマトリックス上にグラフト化した。
【0050】
実施例4−フタルイミド誘導ポリマーマトリックスの加水分解
実施例3で得られたポリマーマトリックスをガラスフィルター漏斗中で150mLメタノールで洗浄し、次いでブタノール150mLで洗浄した。溶媒を取除いた後、さらに50mLのブタノールをビーカーに加えて室温で2時間放置した。ブタノールを取除いた後、樹脂を丸底フラスコに移した。樹脂に対しエチレンジアミン11mLを加えた後、ブタノール30mLを加えた。混合物を90℃で15時間不活性雰囲気下に攪拌および加熱した。得られた生成物を水で洗浄した後、0.5M塩酸でpH約1〜2になるまで加えた。次いで樹脂を溶媒から取除き、2M塩酸で処理した。混合物を90℃で2時間攪拌および加熱した。最後に、樹脂を1M水酸化ナトリウムで完全に洗浄し、水でまた洗浄した。
【0051】
実施例5−オキシラン−PEGフタルイミドの調製
【化6】

MEO−3触媒(1当量)を用いて実施例1で記載のように調製したPEG−フタルイミドをTHF(5mL)に溶解し、攪拌下にナトリウムヒドリド(60%オイル)(1当量)を添加した。6時間後、エピクロロヒドリン(1.5当量)を反応混合物に45℃で滴下し、16時間攪拌した。DCMを反応混合物に加え、非溶解不純物を濾過した。溶媒を真空中で除去し、生成物を得た。
【0052】
実施例6−VO−2000−PEG−アミンの調製
【化7】

VO−2000樹脂(バーサマトリックスA/Sから市販のオキセタン架橋PEベース樹脂)(0.5ミリモルOH)をDMFで水洗し、DMF(5mL)中KOBut(4当量)を添加した。反応混合物を100℃に保持し、アルゴンでフラッシュした。MEO−3触媒(4当量)を用いて実施例1で記載のように調製したDMF(5mL)中反応混合物オキシラン−PEGフタルイミドを添加し、反応を1夜続けた。樹脂を濾過し、DMF、エタノール、水、エタノールおよびブタノールで洗浄した。エチレンジアミン(5当量)をブタノール中の樹脂に添加し、反応混合物を90℃1夜保持した。樹脂をブタノール、エタノール、水、エタノール、DMFおよびDCMで洗浄した。
【0053】
分析:カイザーテストはポジティブであった。
ローディング:Fmoc−Gly−OHを樹脂にTBTU/NEM活性方法で付加した。予め測定した樹脂上のFmoc基をDMF中の20%ピペリジンで解離し、ピペリジン−フルビーン(fulvene)付加物の吸収を290nmで測定し、樹脂のアミノ量をOD値から計算した。測定値は=0.69ミリモル/gであった。
【0054】
実施例7−カルボキシルPEG−フタルイミドの調製
【化8】

実施例1の記載のようにMEO−3触媒で調製されたPEG−フタルイミド(1当量)を25mL水/8mL濃硫酸に溶解し、水5mL中CrO3を添加した。溶液を室温で16時間攪拌した。水25mLを反応混合物に添加し、DCM(3x)に抽出した。有機層を加えて水(2x)で洗浄し、NaOH(2x)で飽和し、有機部分を硫酸ナトリウムで乾燥し、真空中で濃縮した。
【0055】
実施例8−VA−1900PEG−アミンの調製
【化9】

VA−1900樹脂(バーサマトリックスA/Sによって市販されている1900ダルトンを有する平均PEG鎖長を有するアクリルアミド架橋PEGベース樹脂)(0.17ミリモルNH2)をDMFで洗浄し、実施例7で得られたカルボキシル−PEGフタルイミド(10当量)、TBTU(9.6当量)およびNEM(13.3当量)をDMF中で樹脂に添加し、反応を3時間継続した。樹脂を濾過し、DMF、エタノール、水、エタノールおよびブタノールで洗浄した。エチレンジアミン(5当量)を樹脂にブタノール中で添加し、反応混合物を90℃で1夜保持した。樹脂をブタノール、エタノール、水、エタノール、DMFおよびDCMで洗浄した。
【0056】
分析:カイザーテストがポジティブであった。
ローディング:Fmoc−Gly−OHを樹脂にTBTU/NEM活性方法で付加した。予め測定した樹脂上のFmoc基をDMF中の20%ピペリジンで解離し、ピペリジン−フルビーン(fulvene)付加物の吸収を290nmで測定し、樹脂のアミノ量をOD値から計算した。測定値は=0.27ミリモル/gであった。
【0057】
実施例9−アクリレート樹脂の誘導
15mLエポキシアクリレート樹脂を蒸留水、エタノールおよびTHFで洗浄し、さらにTHFを吸引除去した。PEG−フタルイミド11.4g(4当量)をTHF6mL中に溶解し、ナトリウムヒトリド720mg(4当量)を添加した。反応は激しく、多くの泡が形成された。溶液を次いで樹脂+4mLTHFに添加した。カップリングを45℃で1夜行った。樹脂をTHF、エタノール、水、エタノールおよびブタノールで洗浄した。1.5mLエチレンジアミンを9mLブタノールに添加し、樹脂に添加した。反応を90℃で1夜継続した。樹脂をブタノール、エタノールおよび水で洗浄した。
【0058】
分析:カイザーテストをいくつかのビーズ上で行い、青に変化し、正であることは樹脂上に第1級アミンの存在を示す。
ローディング:15mLアミノ−PEG−樹脂を水、エタノールおよびDMFで洗浄したが、格子間のDMFは吸引では除去されなかった。Fmoc−Gly5.3g(4当量)およびTBTU5.78g(4当量)およびNEM2.27mL(4当量)を18mL中に混合し、樹脂に加えた。カップリングを室温で週末の内行った。週末後、ビーズの100μLアリコートをFmoc−付加テストのために取り出し、307μモルNH2/g乾燥樹脂の量を得た。
【技術分野】
【0001】
本発明は高分子を変性する方法、特に反応性部分、アルキレンオキシドスペーサーアームおよび保護された第1級アミンを有する官能性基を有する分子体との官能化によってポリマーマトリックスを変性する方法に関する。
【背景技術】
【0002】
大きな生体分子およびポリマー材料を包含する種々の高分子システム(macromolecular system)(要するに高分子物(macromolecules))を特殊な官能化をする必要性が高い。第1級アミンは大変有用な官能性基であって、種々の化学反応の反応点のみならず高分子システムの物理化学性能を変性するのに用いられ得る。
【0003】
多くの用途において、官能基に好適なアクセスを確保するために、官能基を長い化学的なスペーサーを介して高分子系に付加することが要求されることがある。ポリ−またはオリゴ−アルキレンオキシドはそのような官能性アームのために用いられ得る分子フラグメントの一群であって、用途による生物学的または化学的環境に対する高い適合性を示す。
【0004】
そのような分子体がアミン官能化された生成物を形成するのに有用な高分子システムには、生物分子(例えば、タンパク質やヌクレオチド)、ペプチド合成のためのビーズ材料、クロマトグラフィーのための樹脂、濾過用ポリマー材料ならびに医学用成分に用いられる表面層、生体内および生体外診断成分、分析システムなどが挙げられる。
【0005】
文献中には、固体相合成やクロマトグラフィーなどの用途に用いられるポリマー樹脂に第1級アミンを官能性基として導入する多くの方法が存在する。これらの方法の多くはアミン基をポリマー骨格に直接または短い(10原子以下)つなぎを介して結合する。その例としては脱プロトン化されたフタルイミドと第1級アルキルハライドとを反応した後、イミドをヒドラジン分解(hydrazinolysis)する方法およびアジドとアルキルハライドまたはトシレートを反応した後還元する方法である。また、ブロモエチルフタルイミドと高分子上のアルコキシド残基とを反応した後、ヒドラジン分解する方法も多くの場合有用であることが分かっている。多くの場合、第1級アミン官能性はポリマー樹脂に付加された長いアルコキシドスペーサーアーム上の末端官能基として得られる。これらの場合は、第1級アミン−アルコキシドスペーサーアーム部分は段階的方法、すなわちアルコキシドスペーサーアームを付加して、その後第1級アミンを上記反応を用いてアルコキシドスペーサーアームに付加することにより形成されている。上記方法を包含する化学は異常に厳しい条件が必要であり、しばしば高分子システムと不適合であったりする。特に、生物学的高分子は劣下し、またクロマトグラフィーに用いる樹脂はそのような条件下で損害を受ける。後者の場合、多孔性樹脂にとって特に重要であって、厳しい条件が樹脂の多孔性を変化する。また、上記反応はほとんど定量的でなく、不必要な副生成物を形成する。
【0006】
一端がアミンで一端がヒドロキシドであるエチレングリコールから調製された非対称アルキレンオキシドも存在する。これらの化合物は主として短いオリゴマー状で存在し、対称アルキレンオキシドからの分離が可能である。さらに、これらの化合物の高い製造コストや高分子システムに強く反応する反応基にヒドロキシル基を選択的に変更することの難しさが、高分子システムの官能化のためにこれらの化合物を工業的に用いることを非常に制限する。
【0007】
エタノールアミンをアミドまたはイミド保護基と直接エトキシ化することによって調製される非対称pegの例が以下の文献に記載されている。
【0008】
ランジ・アンド・ワール(Lange and Wahl)(Bull.Chim.Soc.Fr.1951、340−342)には、N−アセチルエタノールアミンのエトキシル化からモノおよびジエタノール化誘導体を形成することが記載されている。ロントジェンツ(Lontjens)ら(Polym.Bull.30、1933、pp489−494)には、モノアミノポリエチレングリコールを高温のエトキシル化反応で合成することが記載されているが、多くの副生成物を生成する。Y−Iフアング(Y−I Huang)(J.polym.Sci.23、1985、pp.795−799)には、エタノールアミン−ベンズアルデヒドシッフ塩基をエトキシル化した後、加水分解してモノアミン置換ポリエチレングリコールを形成することが記載されている。後者の2つの例は、生成物を第1級アミンと反応して遊離のヒドロキシル基を有するポリマーを形成してしまう。いずれの場合も、第1級アミン誘導体が得られない。
【0009】
従って、高分子システムをアルコキシドスペーサーアームおよび第1級アミン官能性で効果的かつ安価に官能化することが可能な分子材料が望まれている。
【図面の簡単な説明】
【0010】
【図1】一般式(I)の化合物の調製を示す図であり、mは1であり、nは式(I)中、n−1に対応し、かつ図1中Zは式(I)中Xに相当する。
【発明の開示】
【発明が解決しようとする課題】
【0011】
本発明は高分子、特に合成もしくはクロマトグラフィー用途の固体状支持体として用いられるポリマーマトリックスを変性する方法に関する。
【0012】
特に、本発明は
(i)高分子を提供する工程;
(ii)一般式(I):
【化1】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含し、;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程;
を包含する高分子を変性する方法
に関する。
【0013】
(一般式(I)の化合物)
高分子、特にポリマーマトリックスの変性に有用な化合物は一般式(I):
【化2】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含するものであり;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基を示す。)
によって表わされる化合物であり得る。
【0014】
一般式(I)の化合物は「保護アミノ」−ポリ(オキシアミキレン)型を有すると認識される。従って、本発明の方法は高分子(例えば、ポリマーマトリックス)に一般に親水結合体を介して第1級アミノ基を導入するのに好適である。
【0015】
一般式(I)の化合物は保護基Pで保護された第1級アミノ基である{P}−N部分を含有し、該保護基は第1級アミノ基の2つの自由原子化を包含する。
【0016】
第1級アミノ基の2つの自由原子化を包含する保護基は典型的にはイミド型(RC(=O))2N−]およびイミン型[R−C=N−]で表わされるものである。
【0017】
例えば、イミド型保護基はコハク酸無水物/コハク酸(コハク酸イミド)およびフタル酸無水物/フタル酸(フタル酸イミド)から選択されるものであってよい。
【0018】
好ましい態様では、保護基はイミド型であり、最も好ましい保護基はコハク酸無水物/コハク酸(コハク酸イミド)およびフタル酸無水物/フタル酸(フタル酸イミド)、特にフタル酸無水物/フタル酸(フタルイミド)である。
【0019】
mは1〜12、例えば1〜6、具体的には1〜4、または1〜3、または1〜2の整数であり、特に1である。nは1〜2000、より典型的には1〜100、または1〜50、または1〜10または1〜8、例えば1〜6、または1〜5、または1〜4、または1〜3、または1〜2、または2〜6、または2〜4、または1である。
【0020】
R1およびR2は独立して水素またはC1−4−アルキルからなる群から選択される。
【0021】
C1−4−アルキルはメチル、エチル、1−プロピル、2−プロピル、1−ブチル、2−ブチル、t−ブチルおよび(2−メチル)−プロプ−1−イルを包含する。
【0022】
特定の例はR1およびR2が水素およびメチルから選択されているもの、即ちエチレングリコールおよびプロピレングリコール部分を有する化合物である。現在最も好ましい態様ではR1およびR2は全て水素であるものであり、すなわちエチレングリコール部分を有する化合物である。
【0023】
反応性基は高分子(例えばポリマーマトリックス)上の単純官能基、例えばアミン、アルコールおよびチオール官能性、必要であればそれらの基の活性化されたものと反応し得るものであってよい。この目的のためには、小さな環状エーテル、例えばオキシラン(エポキシド)およびオキシエタンを包含する反応性基を用いてもよく、官能基、例えばイソシアネート、カルボン酸、酸無水物または活性化ビニル化合物を用いてもよい。特定の例としてはオキシランまたはオキセタンを有する反応性基であり、好適なオキシラン含有反応性基(X)はエピクロロヒドリンから誘導されたものであってよい(実施例5)。反応性基の別の例としてはカルボン酸−含有反応性基(例えば実施例7に記載したもの)である。これらの実施例のいずれも、CH2基は反応性基Xの一部(実施例5におけるCH2(O)CHCH2−および実施例7におけるHOOCCH2−参照)として包含する。
【0024】
(一般式(I)の化合物の調製)
本発明の好ましい態様では、分子体はN−保護ヒドロキシアルキルアミンのポリアルコキシル化およびその後反応性部分をC−O結合を介しての付加することによって形成される。これは非対称ポリアルキレンオキシドに対するコスト効果の優れたルートであり、触媒および反応時間を注意深く選択することによって鎖長および純度の調整も得られる。さらに、アルキレンオキシド、例えばエチレンオキシドおよびプロピレンオキシドの含有量を調節することにより、生成物の分子構造および親水性をコントロールすることもできる。
【0025】
(保護ポリエチレングリコール−アルキルアミンの合成)
この合成の出発点は保護ヒドロキシアルキルアミン(b)である。簡単で有用なアルキルアミンの例は、エタノールアミン、3−ヒドロキシプロピルアミン、2−ヒドロキシプロピルアミンである。またより複雑なアミン、例えば3−オキシ−5−ヒドロキシ−1−ペンタンアミンまたは4−ヒドロキシメチル−ベンジルアミンを用いてもよい。
【0026】
ヒドロキシアルキルアミン(a)上のアミン基はエトキシル化およびその後の反応性部分への付加を可能にする保護基で保護される。保護基、例えばイミド、アミド、イミンまたは尿素誘導体がこの目的には有用である。エタノールアミンおよびフタル酸無水物から形成されたフタルイミド保護アミンが市販されている。単純なアミド保護と比べて窒素原子上に水素原子が存在せず、その結果その後の変性における求核攻撃に対して安定であるという利点を有する。一般のアミド保護アミン中のアミドプロトンがポリアルコキシド中の末端ヒドロキシル基と同等の酸性力を有し、それが不明確な置換反応を引き起こすので、このことは特に重要である。
【0027】
アミン基が保護されたら、遊離ヒドロキシル基が触媒の存在下にオキシランと反応して、ポリアルコキシ誘導体(c)を形成することができる。一般に使用されるオキシランには、エチレンオキシドおよびプロピレンオキシドまたはそれらの混合物が含まれる。触媒の選択および反応条件の選択は特に重要である。2−ヒドロキシエチルフタルイミドおよびエチレンオキシドとの間の反応に以前報告されている条件は、高濃度の水酸化ナトリウム触媒で160℃以上の温度を包含し、大きな分子量分布と高い濃度の不純物を有する濃い着色された生成物を形成する。本発明に例示されたように、温度および触媒の濃度を低くすることは許容される純度の生成物を提供する。ランタまたはランタニドベースの触媒を適用することは分子量分布の小さい非常に純粋な、ほとんど着色のない生成物を提供する。
【0028】
エチレンオキシドに基づくポリアルコキシドは親水性が高く生物的適合性が高い。エチレンオキシドの代わりにプロピレンオキシドを使用することは、水に比較的に溶けにくく、生物分子との疎水的相互反応をある程度を示す分子になる。2つのモノマーが共重合して、さらに親水性を制御してもよい。
【0029】
次に、ポリアルコキシ誘導体を反応性部分で官能化して、所望の分子体を得て、それが高分子システムを変性するのに用いられる。反応部分は高分子システム上の官能基、例えば前述のアミン、アルコール、チオールなどとの反応し得るべきである。
【0030】
本発明は、ある態様では一般式(I):
【化3】

(式中、{P}−Nはフタルイミド基であり、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は共に水素であり、およびXは反応性基である。)の化合物の調製方法を提供し、この方法は(a)フタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13−アルカンを提供する工程;(b)上記アルカンとエチレンオキシドとを触媒の存在下に反応する工程;および(c)工程(b)で得られた生成物の末端OH基を官能化することによる変性する工程を包含する。
【0031】
工程(b)中の反応は好ましくは大気(特に酸素)の不存在下で行われる。さらに、反応は典型的には圧力下、例えば2〜10バールおよび高温、例えば80〜200℃、具体的には100〜190℃で行われる。触媒の量は典型的にはフタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13−アルカンの量に基づいて1〜3%であり、この量はエチレンオキシドの当量で変化し、すなわちより高い量のエチレンオキシドを用いると、より高い触媒の量が必要である。使用されるエチレンオキシドの当量数は所望の鎖長、すなわち一般式(I)中の数字「n」に対応する。好適な触媒はNaOH、KOH、KOCH3、MEO−3およびMEO−LAから選択されるものである。
【0032】
工程(c)中の転換は反応性基の分子への酸素原子を介してのカップリング化または末端ヒドロキシ官能を対応するカルボン酸に、例えば酸化によって変更することによって、反応性基Xを導入するために行われる。これは実施例の部分に例示的に記載している。
【0033】
(一般式(I)の化合物の高分子へのグラフト化)
完全な分子体を次いで高分子システム(高分子)、例えばポリマーマトリックス、生体分子(酵素、タンパク質など)および材料表面を変性するために用い得る。高分子システム上での反応性基がアミン基である場合、反応が触媒なしでも進行し得るが、ヒドロキシル基(すなわち、アルコール)との反応においては触媒がしばしば用いられる。
【0034】
適当なポリマーマトリックスの例としては、PS、POEPS、POEPOP、SPOCC、PEGA、CLEAR、HYDRA、PEG−ポリアクリレート共重合体、ポリエーテル−ポリアミン共重合体および架橋ポリエチレンジ−アミン、エキスパンシン(Expansin)、ポリアミド、ジャンダゲル(Jandagel)、PS−BDODMA、PS−HDODA、PS−TTEGDA、PS−TEGDA、GDMA−PMMA、PS−TRPGDA、アルゴゲル(ArgoGel)、アルゴポール(Argopore)樹脂、トーヨーパール(Toyopearl)、他の架橋ポリアクリレート高容量PEGA、グラフトゲル(Fractogel)、セファデックス(Sephadex)、セファロース(Sepharose)、他の架橋アガロースおよび上記の誘導体から選択されるものである。
【0035】
最終段階で、アルコキシド側鎖上の末端第1級アミンの保護基を除去してもよい。フタルイミド保護基をヒドラジンまたはエチレンジアミンを含有する溶液で処理することによって外してもよく、イミンタイプの保護基は水中で低濃度の酸または塩基を用いる緩やかな条件下で加水分解してもよい。アミド型保護基はまた高温下に強塩基処理を必要とし、あまり好ましくない。
【0036】
上記方法を用いる場合、高分子システムを末端基として容易に入手できる第1級アミンで所望の親水性の官能化側鎖としてもよい。そのような高分子システムはそのように、またアミン基の化学変性によりさらに変性してもよい。
【0037】
アミン基を固体相化学のための出発点として用いてもよく、また、より複雑な分子、例えばタンパク質、ヌクレオチド、または親和リガンドに対する付着点として用いてもよい。そのような高分子システムはアミノ基の化学変性を介してそのようなまたは更に変性されてもよい。
【0038】
要するに、本発明は特定の高分子体の形成、およびそのような高分子体の高分子システムの変性への利用からなる。形成は以下の4つの工程からなる:
1.N−保護ヒドロキシアルキルアミンのアルコキシル化。
2.反応部分のポリアルキレンオキシドの遊離ヒドロキシ末端を介する付加。
3.反応性部分の高分子システムの官能基との反応。
4.N−保護基の解離による第1級アミンの放出。
【0039】
(特定の態様)
特定の態様において、本発明は高分子、特に高分子マトリックスの変性方法に関し、その方法は:
(i)高分子(例えば、ポリマーマトリックス)を提供する工程:
(ii)一般式(I):
【化4】

(式中、{P}−Nはフタルイミド基であり;
mは1であり、nは1〜100の整数を示し;
R1およびR2は両方とも水素であり;かつ
Xが反応性基、例えばオキシラン含有反応性基およびオキシラン含有オキセタン含有反応性基から選択され、特にオキセタン含有反応性基またはオキシタン含有反応性基である。)
の化合物を提供する工程;および
(iii)一般式(I)の化合物を高分子(例えば、ポリマーマトリックス)と反応させて、高分子上にグラフトを形成する工程;
を包含する。
【0040】
さらに特定の態様では、本発明は一般式(I)
【化5】

(式中、{P}−Nがフタルイミド基であり;
mが1で、nが1〜100の整数であり;
R1およびR2が共に水素であり;および
Xがオキセタン含有反応基またはオキシラン含有反応基である。)
で表わされる化合物を提供する。
【0041】
この態様では、Xは好ましくはCH2(O)CHCH2−(オキシラニル−メチル)を示す。
【0042】
(別の態様)
高分子は本明細書中において有機分子から誘導される骨格に基づくものを言うが、また本発明の方法はガラス基材(例えば、プレート、ビーズ、スティックなど)を変性するのにも有用である。そのような場合、反応性基(一般式(I)化合物におけるX)は問題のガラス基材のSi−OH表面基またはすでに変性されたガラス基材の表面基と反応し得るべきである。従って、好適な反応性基は時にはシラン型であってもよい。
【0043】
さらに別の態様でおいては、一般式(I)の化合物の反応性基Xはポリアルキレンオキシド鎖の脱水素末端−CH2−OHに対応する電子ペア、すなわち−CH2−O−Xが−CH2−O−であるものであってもよい。そのような反応性基は高分子のエポキシド基と反応してもよい。
【実施例】
【0044】
実施例1−N−(2−ヒドロキシエチル)−フタルイミドのアルコキシル化
合成を加熱マントル、内部冷却コイルおよび機械的攪拌装置を備えた3リットルオートクレーブ中で行う。
【0045】
触媒をN−(2−ヒドロキシエチル)−フタルイミド(HPI、Katwijk Chemie bv、オランダ)300gに添加した。反応器の内容物を130℃で窒素パージによって20分間乾燥した。その後、エチレンオキシドを選択した温度で3〜5バールのレベルで加圧をキープして加えた(以下参照)。エチレンオキシド(EO)640gを導入した後、生成物を反応温度で30分間処理した。得られたエトキシレートを40℃で取り出し、秤量した。
【0046】
【表1】

【0047】
MEO−3およびMEO−LA触媒はメキセオ(Mexeo)、PIによって開発された不均質ランタン触媒である。純度はMaldi Tofスペクトルに基づいて推測した。
【0048】
実施例2−アルコキシル化N−(2−ヒドロキシエチル)−フタルイミドのエピクロルヒドリンによる官能化
MEO−3触媒を用いて実施例1により調製したアルコキシル化N−(2−ヒドロキシエチル)−フタルイミドをアセトニトリル(5mL/gPEG、2x)の共沸蒸留により乾燥し、攪拌下におよび水分排出下にTHF中に溶解した。ナトリウムヒドリド(ミネラルオイル中60重量%分散体)を攪拌下に湿度を除去してPEG溶液に小さく区切って加えた。脱プロトン化反応が室温で2時間攪拌し、エピクロルヒドリンを滴下し、反応を40℃で12時間攪拌した。溶液を真空中で蒸気蒸留し、残渣をアセトニトリル(25mL)と混合した。沈殿したナトリウム塩を8000r.p.mの遠心分離により20分間分離し、上澄み液を真空中で蒸留した。得られた生成物をヘプタン(3×25mL)で洗って、ミネラルオイルを除去し、高真空下に乾燥した。
【0049】
実施例3−ポリマーマトリックス上へのグラフト化
実施例2で得られた生成物を実施例9の記載の通りポリマーマトリックス上にグラフト化した。
【0050】
実施例4−フタルイミド誘導ポリマーマトリックスの加水分解
実施例3で得られたポリマーマトリックスをガラスフィルター漏斗中で150mLメタノールで洗浄し、次いでブタノール150mLで洗浄した。溶媒を取除いた後、さらに50mLのブタノールをビーカーに加えて室温で2時間放置した。ブタノールを取除いた後、樹脂を丸底フラスコに移した。樹脂に対しエチレンジアミン11mLを加えた後、ブタノール30mLを加えた。混合物を90℃で15時間不活性雰囲気下に攪拌および加熱した。得られた生成物を水で洗浄した後、0.5M塩酸でpH約1〜2になるまで加えた。次いで樹脂を溶媒から取除き、2M塩酸で処理した。混合物を90℃で2時間攪拌および加熱した。最後に、樹脂を1M水酸化ナトリウムで完全に洗浄し、水でまた洗浄した。
【0051】
実施例5−オキシラン−PEGフタルイミドの調製
【化6】

MEO−3触媒(1当量)を用いて実施例1で記載のように調製したPEG−フタルイミドをTHF(5mL)に溶解し、攪拌下にナトリウムヒドリド(60%オイル)(1当量)を添加した。6時間後、エピクロロヒドリン(1.5当量)を反応混合物に45℃で滴下し、16時間攪拌した。DCMを反応混合物に加え、非溶解不純物を濾過した。溶媒を真空中で除去し、生成物を得た。
【0052】
実施例6−VO−2000−PEG−アミンの調製
【化7】

VO−2000樹脂(バーサマトリックスA/Sから市販のオキセタン架橋PEベース樹脂)(0.5ミリモルOH)をDMFで水洗し、DMF(5mL)中KOBut(4当量)を添加した。反応混合物を100℃に保持し、アルゴンでフラッシュした。MEO−3触媒(4当量)を用いて実施例1で記載のように調製したDMF(5mL)中反応混合物オキシラン−PEGフタルイミドを添加し、反応を1夜続けた。樹脂を濾過し、DMF、エタノール、水、エタノールおよびブタノールで洗浄した。エチレンジアミン(5当量)をブタノール中の樹脂に添加し、反応混合物を90℃1夜保持した。樹脂をブタノール、エタノール、水、エタノール、DMFおよびDCMで洗浄した。
【0053】
分析:カイザーテストはポジティブであった。
ローディング:Fmoc−Gly−OHを樹脂にTBTU/NEM活性方法で付加した。予め測定した樹脂上のFmoc基をDMF中の20%ピペリジンで解離し、ピペリジン−フルビーン(fulvene)付加物の吸収を290nmで測定し、樹脂のアミノ量をOD値から計算した。測定値は=0.69ミリモル/gであった。
【0054】
実施例7−カルボキシルPEG−フタルイミドの調製
【化8】

実施例1の記載のようにMEO−3触媒で調製されたPEG−フタルイミド(1当量)を25mL水/8mL濃硫酸に溶解し、水5mL中CrO3を添加した。溶液を室温で16時間攪拌した。水25mLを反応混合物に添加し、DCM(3x)に抽出した。有機層を加えて水(2x)で洗浄し、NaOH(2x)で飽和し、有機部分を硫酸ナトリウムで乾燥し、真空中で濃縮した。
【0055】
実施例8−VA−1900PEG−アミンの調製
【化9】

VA−1900樹脂(バーサマトリックスA/Sによって市販されている1900ダルトンを有する平均PEG鎖長を有するアクリルアミド架橋PEGベース樹脂)(0.17ミリモルNH2)をDMFで洗浄し、実施例7で得られたカルボキシル−PEGフタルイミド(10当量)、TBTU(9.6当量)およびNEM(13.3当量)をDMF中で樹脂に添加し、反応を3時間継続した。樹脂を濾過し、DMF、エタノール、水、エタノールおよびブタノールで洗浄した。エチレンジアミン(5当量)を樹脂にブタノール中で添加し、反応混合物を90℃で1夜保持した。樹脂をブタノール、エタノール、水、エタノール、DMFおよびDCMで洗浄した。
【0056】
分析:カイザーテストがポジティブであった。
ローディング:Fmoc−Gly−OHを樹脂にTBTU/NEM活性方法で付加した。予め測定した樹脂上のFmoc基をDMF中の20%ピペリジンで解離し、ピペリジン−フルビーン(fulvene)付加物の吸収を290nmで測定し、樹脂のアミノ量をOD値から計算した。測定値は=0.27ミリモル/gであった。
【0057】
実施例9−アクリレート樹脂の誘導
15mLエポキシアクリレート樹脂を蒸留水、エタノールおよびTHFで洗浄し、さらにTHFを吸引除去した。PEG−フタルイミド11.4g(4当量)をTHF6mL中に溶解し、ナトリウムヒトリド720mg(4当量)を添加した。反応は激しく、多くの泡が形成された。溶液を次いで樹脂+4mLTHFに添加した。カップリングを45℃で1夜行った。樹脂をTHF、エタノール、水、エタノールおよびブタノールで洗浄した。1.5mLエチレンジアミンを9mLブタノールに添加し、樹脂に添加した。反応を90℃で1夜継続した。樹脂をブタノール、エタノールおよび水で洗浄した。
【0058】
分析:カイザーテストをいくつかのビーズ上で行い、青に変化し、正であることは樹脂上に第1級アミンの存在を示す。
ローディング:15mLアミノ−PEG−樹脂を水、エタノールおよびDMFで洗浄したが、格子間のDMFは吸引では除去されなかった。Fmoc−Gly5.3g(4当量)およびTBTU5.78g(4当量)およびNEM2.27mL(4当量)を18mL中に混合し、樹脂に加えた。カップリングを室温で週末の内行った。週末後、ビーズの100μLアリコートをFmoc−付加テストのために取り出し、307μモルNH2/g乾燥樹脂の量を得た。
【特許請求の範囲】
【請求項1】
(i)高分子を提供する工程;
(ii)一般式(I):
【化1】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含し、;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程;
を包含する高分子を変性する方法。
【請求項2】
高分子がポリマーマトリックスである請求項1記載の方法。
【請求項3】
保護基{P}−Nがフルミド基である請求項1または2記載の方法。
【請求項4】
保護基{P}−Nがフタルイミド基であり、mが1であり、nが1〜10であり、Xがオキセタン−含有反応性基およびオキシラン−含有反応性基から選択される、請求項1〜3いずれかに記載の方法。
【請求項5】
(i)高分子を提供する工程;
(ii)一般式(I):
【化2】

(式中、{P}−Nはフタルイミド基であり;
mは1で、nは1〜100の整数であり;
R1およびR2は共に水素であり;および
Xは反応性基、例えばオキセタン−含有反応性基およびオキシラン−含有反応性基から選択される反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程:
を包含する請求項1記載の方法。
【請求項6】
一般式(I):
【化3】

(式中、{P}−Nがフタルイミド基であり;mが1で、nが1〜100の整数であり;
R1およびR2が共に水素であり;およびXがオキセタン−含有反応性基またはオキシラン−含有反応性基である。)
で表わされる化合物。
【請求項7】
(a)フタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13アルカンを提供する工程;
(b)該アルカンを触媒の存在下にエチレンオキシドと反応する工程;および
(c)工程(b)で得られた生成物の末端OH基を官能化して転換する工程、
を含有する一般式(I):
【化4】

(式中、{P}−Nはフタルイミド基であり、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は共に水素であり、Xは反応性基である。)
で表される化合物の調製方法。
【請求項1】
(i)高分子を提供する工程;
(ii)一般式(I):
【化1】

(式中、Nは保護基Pで保護された第1級アミノ基であって、保護基は第1級アミノ基の2つの自由原子化を包含し、;
mは1〜12の整数であり、nは1〜2000の整数であり;
R1およびR2は独立して水素およびC1−4−アルキルからなる群から選択され;および
Xは反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程;
を包含する高分子を変性する方法。
【請求項2】
高分子がポリマーマトリックスである請求項1記載の方法。
【請求項3】
保護基{P}−Nがフルミド基である請求項1または2記載の方法。
【請求項4】
保護基{P}−Nがフタルイミド基であり、mが1であり、nが1〜10であり、Xがオキセタン−含有反応性基およびオキシラン−含有反応性基から選択される、請求項1〜3いずれかに記載の方法。
【請求項5】
(i)高分子を提供する工程;
(ii)一般式(I):
【化2】

(式中、{P}−Nはフタルイミド基であり;
mは1で、nは1〜100の整数であり;
R1およびR2は共に水素であり;および
Xは反応性基、例えばオキセタン−含有反応性基およびオキシラン−含有反応性基から選択される反応性基である。)
を有する化合物を提供する工程;および
(iii)一般式(I)の化合物を前記高分子と反応させて高分子にグラフトを形成する工程:
を包含する請求項1記載の方法。
【請求項6】
一般式(I):
【化3】

(式中、{P}−Nがフタルイミド基であり;mが1で、nが1〜100の整数であり;
R1およびR2が共に水素であり;およびXがオキセタン−含有反応性基またはオキシラン−含有反応性基である。)
で表わされる化合物。
【請求項7】
(a)フタルイミドN−保護a−ヒドロキシ−ω−アミノ−C2−13アルカンを提供する工程;
(b)該アルカンを触媒の存在下にエチレンオキシドと反応する工程;および
(c)工程(b)で得られた生成物の末端OH基を官能化して転換する工程、
を含有する一般式(I):
【化4】

(式中、{P}−Nはフタルイミド基であり、mは1〜12の整数であり、nは1〜2000の整数であり、R1およびR2は共に水素であり、Xは反応性基である。)
で表される化合物の調製方法。
【図1】




【公開番号】特開2012−180518(P2012−180518A)
【公開日】平成24年9月20日(2012.9.20)
【国際特許分類】
【外国語出願】
【出願番号】特願2012−62338(P2012−62338)
【出願日】平成24年3月19日(2012.3.19)
【分割の表示】特願2008−527308(P2008−527308)の分割
【原出願日】平成18年8月25日(2006.8.25)
【出願人】(395018066)ノヴォ ノルディスク アクティーゼルスカブ (7)
【Fターム(参考)】
【公開日】平成24年9月20日(2012.9.20)
【国際特許分類】
【出願番号】特願2012−62338(P2012−62338)
【出願日】平成24年3月19日(2012.3.19)
【分割の表示】特願2008−527308(P2008−527308)の分割
【原出願日】平成18年8月25日(2006.8.25)
【出願人】(395018066)ノヴォ ノルディスク アクティーゼルスカブ (7)
【Fターム(参考)】
[ Back to top ]

