高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池
【課題】側鎖のメソゲンのスタッキングを促進させ、また、薄膜化を可能とするため主鎖に剛直な骨格を用いることで、プロトン伝導性に優れ、発電性能を向上させた高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池を提供する。
【解決手段】側鎖のビフェニルをジフェニルアセチレンに変更し、メソゲン同士のスタッキングを促進することで、プロトンのネットワーク形成を促進させ、プロトン伝導度を向上させた。また、主鎖をアクリルもしくメタクリル骨格からフェニレン骨格に変更し、剛直な骨格のため、薄膜化が可能となり、発電性能を向上させた。
【解決手段】側鎖のビフェニルをジフェニルアセチレンに変更し、メソゲン同士のスタッキングを促進することで、プロトンのネットワーク形成を促進させ、プロトン伝導度を向上させた。また、主鎖をアクリルもしくメタクリル骨格からフェニレン骨格に変更し、剛直な骨格のため、薄膜化が可能となり、発電性能を向上させた。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池に関し、特に、固体高分子形燃料電池に用いられる高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池に関する。
【背景技術】
【0002】
固体高分子形燃料電池(以下、「PEFC(Polymer Electrolyte Fuel Cell)」と記す。)は、環境負荷ガスの放出を削減することに貢献することができるため、燃料電池自動車や、定置用コジェネレーション、携帯電話の電源として研究開発が進められている。PEFCでは、電池内でプロトンの伝導が起こることによって発電反応が進行する。PEFCにおけるプロトン伝導には水の存在が必須であり、それ故にPEFCの発電反応を進行させるためには加湿器が必要となる。車両などに燃料電池を適用する場合、車載性の観点からは加湿器は小さいことが望まれるため、低加湿下でもプロトン伝導が良好に行われる電解質が求められている。ナフィオン(登録商標、デュポン社製)、アシプレックス(登録商標、旭化成株式会社製)に代表されるフッ素系樹脂電解質は、低加湿下におけるプロトン伝導性に優れており、PEFCにおいて汎用されている材料である。
【0003】
しかしながら、フッ素系樹脂電解質は、フッ素からなる高分子材料であるため、リサイクル性が低いという問題があった。燃料電池自動車の普及を考えた場合、燃料電池をリサイクルすることができるかどうかという点が非常に重要であり、リサイクルができない材料の環境への負荷を無視することができない。
さらに、フッ素系樹脂電解質を単独で電解質膜として適用した場合、耐久性が低くなるという問題があった。このようなことから、フッ素系樹脂電解質の代替となる新たな材料の必要性が高まってきている。
【0004】
具体的な代替材料の一つとして炭化水素系電解質があり、この炭化水素系電解質の開発が近年行われてきている。炭化水素系材料は、一般的にフッ素系樹脂電解質よりも耐久性に優れ、フッ素系樹脂電解質の代替として期待される。
例えば、特許文献1には、炭化水素系電解質を用いて、低加湿で高いプロトン伝導性を得るために、液晶骨格を有する材料を用いて、スルホン酸基のネットワークを形成させることにより、低加湿で高いプロトン伝導性が得られることについて記載されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2003−55337号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1に記載のスルホン酸型液晶モノマー材料を高分子量化したスルホン化液晶ポリマー材料は、側鎖のメソゲンがビフェニルである。このビフェニルは、オルソ位の水素原子同士が電子反発を起こし、2つの環がねじれるためにメソゲン同士のスタッキングが不安定になる。それに伴い、酸基のネットワーク形成が阻害され、より高いプロトン伝導度が達成できなくなることが懸念される。また、主鎖がメタクリル基、もしくはアクリル骨格のため、高分子電解質膜を薄膜化したことにより性能が向上しにくくなることがあった。
【0007】
そこで、本発明は、上記の課題を解決するものであって、側鎖のメソゲンのスタッキングを促進させ、また、薄膜化を可能とするため主鎖に剛直な骨格を用いることで、プロトン伝導性に優れ、発電性能を向上させた高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明による高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池は、上記の目的を達成するために、次のように構成される。
本発明のある態様による第1の高分子電解質は、下記の化学一般式(1)(A1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。)で表わされる高分子単位を有することを特徴とする。
【0009】
【化1】

【0010】
本発明によれば、高いプロトン伝導度を有し、かつ薄膜化が可能であって、高い発電性能を有する高分子電解質を提供することが可能となる。
本発明のある態様による第2の高分子電解質は、前記アルキル基は、−(CH2)m−(mは1以上の整数とする。)であることを特徴とする。
【0011】
本発明によれば、アルキル基を−(CH2)m−とすることで、高分子電解質からなる高分子電解質膜の柔軟性を維持しつつ、酸価の高い高分子電解質膜を得ることが可能となる。
本発明のある態様による第3の高分子電解質は、前記プロトン酸基は、スルホン酸基またはホスホン酸基であることを特徴とする。
【0012】
本発明によれば、プロトンの解離を促進させて、プロトン伝導度を向上することが可能となる。
本発明のある態様による第4の高分子電解質は、前記化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する下記の化学一般式(2)(X1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子を示す。)で表されるイオン性材料を含んで形成されたことを特徴とする。
【0013】
【化2】

【0014】
本発明によれば、イオン性材料を含んで形成されているため、高分子電解質膜を薄膜化して際にも、膜電極接合体を形成することのできる十分な機械強度を得ることが可能となる。
本発明のある態様による第5の高分子電解質は、イオン交換容量は、2.1meq/g以上2.4meq/g以下であることを特徴とする。
本発明によれば、イオン交換容量を上記のようにすることにより、上記で説明したような高分子電解質膜の性能を最も高めることが可能となる。
本発明のある態様による高分子電解質膜は、第1〜4のいずれか1つの高分子電解質を用いて形成されたことを特徴とする。
【0015】
本発明によれば、高いプロトン伝導度、発電性能を兼ね備えた高分子電解質膜を提供することが可能となる。
本発明のある態様による固体高分子形燃料電池は、上記の高分子電解質膜を用いて形成されたことを特徴とする。
本発明によれば、上記の高分子電解質膜を用いて形成された固体高分子形燃料電池であり、高い発電性能を備えた固体高分子形燃料電池を提供することが可能となる。
【発明の効果】
【0016】
本発明によれば、上記の化学一般式(1)で表される高分子単位を有することにより、高いプロトン伝導度を有し、かつ薄膜化が可能であって、高い発電性能を有する高分子電解質を提供することができる。
また、本発明によれば、プロトン酸基が、スルホン酸基またはホスホン酸基であることを特徴とする高分子電解質により、プロトンの解離を促進させ、プロトン伝導度を向上させることができる。
【0017】
また、本発明によれば、上記の高分子電解質から高分子電解質膜を形成することにより、高いプロトン伝導度、および発電性能を兼ね備えた高分子電解質膜を提供することができる。
また、本発明によれば、上記の化学一般式(2)で表されるX1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子である高分子電解質(イオン性材料)であり、高分子電解質膜を薄膜化しても、膜電極接合体を形成するために必要な機械強度を十分に得ることができる。
【0018】
また、本発明によれば、上記の高分子電解質膜を用いて固体高分子形燃料電池を構成することにより、高い発電性能を備えた固体高分子形燃料電池を提供することができる。
【図面の簡単な説明】
【0019】
【図1】本発明の高分子電解質膜1の両面に電極触媒層が形成された膜電極接合体12を装着した固体高分子形燃料電池の単セル11の構成を示す分解断面図である。
【図2】図1に示した膜電極結合体12の構成を示す要部断面図である。
【図3】ベンゼン環のπスタックの構造の概念を示す模式図である。
【図4】ビフェニルの構造を示す一般式である。
【図5】ジフェニルアセチレンの構造を示す一般式である。
【発明を実施するための形態】
【0020】
以下に、添付した図面を参照して、本発明の高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池について詳細に説明する。
なお、本発明は、以下に記載する各実施の形態に限定されるものではなく、当業者の知識に基づいて設計の変更等の変形を加えることも可能であり、そのような変形が加えられた実施の形態も本発明の範囲に含まれうるものである。
【0021】
まず、図1および図2を参照して、本実施形態に係る固体高分子形燃料電池の単セル11の全体の構成を説明する。
図1は、本発明の高分子電解質膜(高分子電解質)1の両面に電極触媒層が形成された膜電極接合体12を装着した固体高分子形燃料電池の単セル11の構成を示す分解断面図である。
【0022】
図1に示す固体高分子形燃料電池の単セル11は、その上下部を保護する2つのセパレータ10に膜電極結合体12が挟まれて形成される。なお、2つのセパレータ10のうちの一方のセパレータと膜電極結合体12との間には、ガス拡散層として空気極側ガス拡散層4が形成される。また、他方のセパレータと膜電極結合体12との間にも、同様にガス拡散層として燃料極側ガス拡散層5が形成される。
【0023】
そして、膜電極結合体12は、高分子電解質膜1の空気極側ガス拡散層4の面に空気極側電極触媒層2が形成される。また、膜電極結合体12は、高分子電解質膜1の燃料極側ガス拡散層5の面に燃料極側電極触媒層3が形成される。
上記の空気極側電極触媒層2と空気極側ガス拡散層4とで、電極として機能する空気極6が形成される。さらに、燃料極側電極触媒層3と燃料極側ガス拡散層5とで、同じく電極として機能する燃料極7が形成される。この空気極6と燃料極7とに、図示しない外部の負荷が接続されることで、負荷を駆動することができる。
【0024】
また、セパレータ10には、一方の面にはガスが流れる経路としてガス流路8が形成され、他方の面には冷却水が流れる経路として冷却水流路9が形成されている。
また、図2は、図1に示した膜電極結合体12の構成を示す要部断面図である。図2に示す膜電極結合体12は、高分子電解質膜1の空気極6側の面に、空気極側電極触媒層2が形成されている。また、膜電極結合体12は、高分子電解質膜1の燃料極7側の面に、空気極側電極触媒層3が形成されている。
【0025】
続いて、図3〜図5を参照して、プロトン伝導度を向上させるための方法について説明する。
図3は、ベンゼン環のπスタックの構造の概念を示す模式図である。一般的に、芳香族化合物は、図3に示すように、芳香環上に非局在化したπ電子同士が相互作用することで、芳香環の面と面を重ね合わせるように分子間でのスタック(πスタック)を形成することが知られている。この図3では、上下のベンゼン環の炭素原子同士が、互いに重なり合う配座の例を具体的に示している。
【0026】
液晶分子のメソゲンはこのスタックの形成を利用し、秩序構造を形成している。すなわち、液晶分子が集合体を形成する上では、スタックの形成を促進することが重要である。
本実施形態では、メソゲンにプロトン酸基が、連結基を通して結合しており、メソゲンのネットワークが直接プロトンのネットワークになりうる。従って、メソゲンのスタックの形成をさらに促進することで、分子内でのプロトンの輸送を効率よく行うことができ、プロトン伝導度を向上させることができる。
【0027】
また、図4は、ビフェニルの構造を示す一般式である。また、ジフェニルアセチレンの構造を示す一般式である。通常、メソゲンとして用いられることが多いビフェニルは、図4に示すように、ベンゼン環同士が結合している炭素の隣(オルソ位)の炭素に結合した水素同士が電子反発を起こし、隣り合う環同士(図4中に矢印Aで示す箇所)が約50°ねじれることが知られている。よりスタックを形成しやすくするためには、このねじれを解消する必要がある。
【0028】
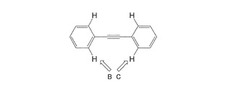
本実施形態における高分子電解質膜1は、メソゲンのビフェニルをジフェニルアセチレンに変更している。ジフェニルアセチレンは、図5に示すように、ビフェニルの環同士の間に、3重結合をスペーサーとして挿入した構造をしている。このため、ビフェニルに見られる水素同士の電子反発を起こすことがないため、隣り合う環同士(図5中に矢印B,Cで示す箇所)のねじれは殆ど起こらずに、環同士はほぼ同一平面状にある。
【0029】
以下に、本発明の固体高分子形燃料電池の薄膜化が可能であって、さらに耐久性に優れた高分子電解質膜の製造方法について説明する。なお、本発明は、以下に記載する各実施の形態に限定されうるものではなく、当業者の知識に基づいて設計の変更等の変形を加えることも可能であり、そのような変形が加えられた実施の形態も本発明の範囲に含まれうるものである。
(化合物の合成)
下記の化学一般式(1)におけるA1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。
【0030】
【化3】

【0031】
また、下記の化学一般式(2)におけるA1,A2,Bは、上記の化学一般式(1)で定義されたものと同義であるが、X1およびX2はそれぞれ独立して塩素原子、臭素原子、またはヨウ素原子のいずれかである。X1およびX2は同一であっても、異なってもよいが、同一であることが好ましい。
【0032】
ここで、ポリマー化が可能な基とは、具体的に、X1またはX2を含む基のことをいう。また、イオン性材料とは、Yで表されるプロトン酸基を有する材料のことをいう。
【0033】
【化4】

【0034】
つまり、上記の高分子電解質膜(高分子電解質)1は、上記の化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する上記の化学一般式(2)で表わされるイオン性材料を重合させることによって得られる。
上記の化学一般式(2)中のA1,A2で表されるアルキル基は、−(CH2)m−(mは1以上の整数である。)であることが好ましく、mが3または4であることが特に好ましい。mが3または4であることによって、その高分子電解質からなる高分子電解質膜の柔軟性を維持しつつ、酸価の高い高分子電解質膜を得ることができる。
なお、高分子電解質1のイオン交換容量は、上記で説明したような高分子電解質膜の性能を高める観点から、2.1meq/g以上2.4meq/g以下であることが特に好ましい。
【0035】
上記の化学一般式(2)のモノマー製造方法は特に限定されないが、例えばA1がエチレン基−(CH2)2−、A2がプロピレン基−(CH2)3−、およびBがスルホン酸基である場合、以下のようにして合成できる。なお、本実施形態においては、Bがスルホン酸基である場合について説明するが、Bはスルホン酸基に限定されない。例えば、Bは、ホスホン酸基であってもよい。
【0036】
まず、1,2−ジ(4−ヒドロキシフェニル)アセチレンを用意し、これと無機塩基およびプロパンスルトンを反応させることにより、下記の化学一般式(3)で表される化合物を得ることができる。
【0037】
【化5】

【0038】
この際の反応条件は、特に限定されるものではないが、反応温度は好ましくは、25℃以上80℃以下であることが好ましい。反応時間は、好ましくは、10時間以上48時間以下で行われる。また、化合物を反応させるのは、大気雰囲気下であってもよいし、窒素雰囲気下であってもよい。
【0039】
反応溶媒としては、良溶媒であることが望ましく、より好ましくは、アルコール系溶媒であることが望ましい。具体的な反応溶媒として、例えば、エタノール、メタノール、1−プロパノール、2−プロパノール、1−ブタノールが挙げられる。
また、塩基としては、強塩基であることが望ましく、例えば、水酸化ナトリウム、水酸化カリウムなどが挙げられる。塩基の量は、1,2−ジ(4−ヒドロキシフェニル)アセチレン100モル%に対して、50モル%以上100モル%以下であることが好ましく、70モル%以上90モル%以下であることが好ましい。
【0040】
次に、下記の化学一般式(4)で表わされる化合物を用意する。ここで、Xはそれぞれ塩素原子、臭素原子またはヨウ素原子のいずれかである。
【0041】
【化6】

【0042】
さらに、下記の化学一般式(3)で表わされる化合物を無機塩基で処理した後に、化学一般式(4)に示される化合物を反応させることで、下記の化学一般式(5)で表わされるモノマー化合物を得ることができる。
【0043】
【化7】

【0044】
この際の反応条件は、特に限定されるものではないが、反応温度は好ましくは、25℃以上80℃以下が好ましい。また、反応時間は、好ましくは、10時間以上48時間以下で行われる。化合物を反応させるのは、大気雰囲気下であってもよいし、窒素雰囲気下であってもよい。
【0045】
反応溶媒としては、良溶媒であることが望ましく、より好ましくは、極性の高い溶媒であることが望ましい。例えば、ジメチルスルホキシド、ジメチルホルムアミド、ジメチルアセトアミド、N−メチルピロリドンなどが挙げられる。
塩基としては、強塩基であることが望ましく、例えば、水酸化ナトリウム、水酸化カリウムなどが挙げられる。塩基の量は、上記の化学一般式(4)で表わされる化合物100モル%に対して、50モル%以上100モル%以下であることが好ましく、80モル%以上100モル%以下であることが好ましい。
【0046】
該モノマーの重合は、特に限定されるものではないが、特定の触媒の存在下に反応させることが好ましい。また、この際に使用される触媒は、遷移金属化合物を含む触媒系である。また、この触媒系としては、配位子成分、配位子が配位された遷移金属錯体、および還元剤を必須成分とし、さらに、重合速度を上げるために塩を添加してもよい。
配位子成分としては、トリフェニルホスフィン、2,2’−ビピリジン、1,5−シクロオクタジエン、または1,3−ビス(ジフェニルホスフィノ)プロパンなどが挙げられる。これらのうち、トリフェニルホスフィン、2,2’−ビピリジンが好ましい。上記配位子成分である化合物は、1種単独で用いてもよく、2種以上を併用してもよい。配位子成分は、上記モノマー100モル%に対して、1モル%以上100モル%以下であることが好ましく、1モル%以上20モル%以下であることがより好ましい。
【0047】
配位子が配位された遷移金属錯体としては、例えば、塩化ニッケルビス(トリフェニルホスフィン)、臭化ニッケルビス(トリフェニルホスフィン)、ヨウ化ニッケルビス(トリフェニルホスフィン)、硝酸ニッケルビス(トリフェニルホスフィン)、塩化ニッケル(2,2’−ビピリジン)、臭化ニッケル(2,2’−ビピリジン)、ビス(1,5−シクロオクタジエン)ニッケル、テトラキス(トリフェニルホスフィン)ニッケル、テトラキス(トリフェニルホスファイト)ニッケル、またはテトラキス(トリフェニルホスフィン)パラジウムなどが挙げられる。これらのうち、塩化ニッケルビス(トリフェニルホスフィン)、塩化ニッケル(2,2’−ビピリジン)が好ましい。遷移金属錯体は、上記モノマー100モル%に対して、1モル%以上100モル%以下であることが好ましく、1モル%以上20モル%以下であることがより好ましい。
【0048】
上記の触媒系に使用することができる還元剤としては、例えば、鉄、亜鉛、マンガン、アルミニウム、マグネシウム、ナトリウム、またはカルシウムなどが挙げられる。これらのうち、亜鉛、マグネシウム、マンガンが好ましい。これらの還元剤は、有機酸などの酸に接触させることにより、より活性化して用いることができる。還元剤は、上記モノマー100モル%に対して、1モル%以上100モル%以下であること好ましく、10モル%以上30モル%以下であることが好ましい。
【0049】
また、上記の触媒系において使用することのできる塩としては、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、ヨウ化ナトリウム、硫酸ナトリウムなどのナトリウム化合物;フッ化カリウム、塩化カリウム、臭化カリウム、ヨウ化カリウム、硫酸カリウムなどのカリウム化合物;フッ化テトラエチルアンモニウム、塩化テトラエチルアンモニウム、臭化テトラエチルアンモニウム、ヨウ化テトラエチルアンモニウム、硫酸テトラエチルアンモニウムなどのアンモニウム化合物が挙げられる。これらのうち、臭化ナトリウム、ヨウ化ナトリウム、臭化カリウム、臭化テトラエチルアンモニウム、ヨウ化テトラエチルアンモニウムが好ましい。塩は、上記モノマー100モル%に対して、1以上100モル%以下であることが好ましく、10モル%以上30モル%以下であることが好ましい。
【0050】
また、該重合の際に用いられる溶媒としては、例えばテトラヒドロフラン、シクロヘキサノン、ジメチルスルホキシド、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチル−2−ピロリドン、γ−ブチロラクトン、N,N−ジメチルイミダゾリジノンなどが挙げられる。これらのうち、テトラヒドロフラン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチル−2−ピロリドン、N,N’−ジメチルイミダゾリジノンが好ましい。これらの重合溶媒は、十分に乾燥してから用いることが好ましい。
【0051】
重合の際の重合温度および重合時間は、特に限定されるものではなく、分子量や、重合の濃度等によって適宜設定すればよい。例えば、重量平均分子量が10万以上50万以下の重合体を得ることを目的とする場合、反応効率の点から、重合温度が好ましくは25℃以上80℃以下、より好ましくは40℃以上70℃以下、重合時間が好ましくは8時間以上40時間以下、より好ましくは16時間以上32時間以下で重合が行われる。重合の際の重合圧力は、特に限定されず、加圧下、常圧(大気)下、減圧下のいずれかでよく、場合により適宜設定すればよいが、常圧下であることが好ましい。
【0052】
このようにして得られた高分子電解質を用いて高分子電解質膜を製造する方法としては、特に限定されないが、例えば、本発明のポリフェニレン系電解質を溶剤に溶解して溶液とした後、キャスティングにより、基材上に塗布し、フィルム状に形成する方法や、所定のギャップに制御されたアプリケータを用いて塗工、成膜する方法、ダイコータを用いて成膜する方法等が挙げられる。
【0053】
また、成膜にあたっては、粘度を10mPa・s以上10000mPa・s以下とすることが好ましく、10mPa・s以上1000mPa・s以下とすることがより好ましい。上記の範囲内であると、溶剤の残留量が少なく、また溶液を乾燥する際に多量の気泡が発生する確率が低い。このため、レべリング効果により厚みのむらを低減することができるため、安定したプロトン伝導性を確保することができる。
この際の電解質濃度は、分子量にもよるが、通常、2.5質量%以上50質量%以下、好ましくは7質量%以上25質量%以下である。上記の範囲内であれば、成膜性に優れる。
【0054】
また、この際に用いられる溶媒としては、例えば、N−メチル−2−ピロリドン、N,N−ジメチルホルムアミド、γ−ブチルラクトン、N,N−ジメチルアセトアミド、ジメチルスルホキシド、ジメチル尿素、ジメチルイミダゾリジノンなどの非プロトン系極性溶剤、メタノール、エタノール、プロピルアルコール、isо−プロピルアルコール、sec−ブチルアルコール、tert−ブチルアルコールなどのアルコール系溶媒およびアセトン、メチルエチルケトン、シクロヘキサノンなどのケトン系溶媒などが挙げられる。これらの溶媒は、単独で用いてもよく、あるいは2種以上混合させてもよい。またこれらの溶媒に水を添加したものを用いてもよい。
【0055】
粘度を調整したポリマー溶液は、例えば、基材にキャストされる。キャストする基材としては、金属材料、ガラス、セラミックス、プラスチックなどが挙げられる。なお、基材の形状は、特に限定されるものではないため、任意の形状に形成することができる。
基材上に形成されたフィルムは、好ましくは25℃以上140℃以下、0.1時間以上24時間以下、加熱することにより、高分子電解質膜を得ることができる。
【0056】
以下に、実施例および比較例について示す。
以下、本発明を実施例により詳細に説明するが、本発明はこれらに限定されるものではない。
(実施例)
(化学一般式(3)の合成)
窒素雰囲気下、1,2−ジ(4−ヒドロキシフェニル)アセチレン105g(0.5mol)を用意し、プロパンスルトンを61g(0.5mol)および水酸化ナトリウム16g(0.4mol)、メタノールを200ml加えて、48時間撹拌した。その後、ジエチルエーテルで再沈殿させ、ろ過した。ろ過物をメタノールにて洗いこみ、上記の化学一般式(3)で表される化合物を得た。
(化学一般式(6)の合成)
窒素雰囲気下、上記の化学一般式(3)で表される化合物177g(0.5mol)に、2−(2,5−ジクロロフェニル)−1−ブロモエタン127g(0.5mol)および水酸化ナトリウム20g(0.5mol)、ジメチルスルホキシドを200mlを加えて、48時間撹拌した。その後、メタノールで再沈殿させ、ろ過した。ろ過物をメタノールにて洗いこみ、下記の化学一般式(6)で表される化合物を得た。
【0057】
【化8】

【0058】
(化学一般式(7)の合成)
窒素雰囲気下、化学一般式(6)で表される化合物を7.9g(15mmol)に、トリフェニルホスフィン1.5g(5.6mmol)、ヨウ化ナトリウム0.3g(2mmol)、亜鉛1.3g(20mmol)、ビス(トリフェニルホスフィン)ニッケル(II)ジクロリド0.31g(0.48mmol)を加えて、さらに、溶媒として、20mlのジメチルホルムアミドを加えて、60℃で24時間撹拌した。反応物をメタノールで再沈し、固体を濾別したのち、濃塩酸でプロトンフォームした。さらに純水で濾液のpHが7になるまで洗浄したのち、固体を減圧乾燥し、下記の化学一般式(7)で表される化合物を得た。
【0059】
【化9】

【0060】
以下、本発明を比較例により詳細に説明するが、本発明はこれらに限定されるものではない。
(9−ブロモ−1−デセンの合成)
500mlの三角フラスコにベンゼン100mlおよびピリジン1.0gを加えて、9−デセン−1−オール25g(0.16mol)を溶解した。次に三臭化リン43.2g(0.16mol)を溶解させたベンゼン溶液100mlを氷冷下でゆっくりと滴下した後、室温で18時間撹拌した。その後、反応液を氷水中に注ぎ、ジエチルエーテル300mlで抽出した。ここで得たエーテル−ベンゼン混合液は無水硫酸ナトリウムで一晩脱水した。吸引ろ過により硫酸ナトリウムを除き、エーテル−ベンゼンを減圧除去し、残渣を減圧蒸留して目的物9−ブロモ−1−デセンを得た。
【0061】
(4−(9−デセニルオキシフェニル)フェノールの合成)
水酸化ナトリウム3.40g(0.08mol)を100mlのエタノールに溶解させた。この溶液を4,4’−ビフェノール14.9g(0.08mol)を溶解させた100mlエタノールに少量ずつ加えて、エタノールを減圧除去した。残渣を150mlジメチルホルムアミドに窒素気流下で加温して溶解させた(A液)。上記で調整した9−ブロモ−1−デセン15.8g(0.072mol)、フェノチアジン0.1gを30mlのDMFに溶解させた(B液)。窒素雰囲気下でよく撹拌しながら、A液にB液を30分程度かけて加えて、40℃で24時間反応させた。反応終了後、反応液を冷却し、300mlの10%冷却塩酸で洗浄した後、300mlのエーテルで抽出し、次いで100ml冷蒸留水で洗浄した。エーテル層は無水硫酸ナトリウムで一晩脱水する。残渣に300mlのヘキサンを加えて、ろ過により沈殿物を得る。次いで200mlベンゼンを加えて、ベンゼン可溶部分をベンゼンを用いたカラムクロマトグラフィーで精製して4−(9−デセニルオキシフェニル)フェノールを得た。
【0062】
(3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸の合成)
ジメチルホルムアミド30ml中に重合禁止剤フェノチアジン0.05gを溶解させた。そこへ、1,8−ジアザビシクロ[5,4,0]−7−ウンデンセン(DBU)1.22g(0.008mol)と4−(9−デセニルオキシフェニル)フェノール0.65g(0.002mol)、3−ブロモプロパンスルホン酸ナトリウム1.8g(0.008mol)を溶解させ、窒素雰囲気下、50℃で48時間撹拌した。反応終了後、溶媒を濃縮しジエチルエーテルを加えて、ろ過することにより沈殿を得た。次に、沈殿を蒸留水でよく洗浄した。次に、洗浄後の沈殿を6mol/LのHCl中で24時間撹拌後、遠心分離機により沈殿を得て、この沈殿をジエチルエーテルで洗浄後、乾燥して3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸を得た。
【0063】
(比較例)
(3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸の高分子量化)
窒素雰囲気下、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロプルスルホン酸を488mg(1mmol)、開始剤であるAIBNを6.6mg(0.04mmol)加えて、ジメチルスルホキシドを4.8ml加えた。その後、60℃で60時間熱重合して高分子量化させた。その後、アセトンで再沈殿させ、ポリマーを得た。
【0064】
(ポリマーの製膜)
化学一般式(7)、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸ポリマーをジメチルスルホキシドに溶解させ、ガラスにキャストし、45℃で12時間、80℃で12時間、80℃で1時間真空乾燥させることで、膜を得た。
(薄膜化)
化学一般式(7)で表わされるポリマー膜は、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸ポリマーから得られる膜に比較して、薄膜化しても膜電極接合体が作製できる機械強度を有していた。
(プロトン伝導度の測定)
電解質膜の交流抵抗は、10mm幅の短冊状のプロトン伝導膜試料の表面に、白金線を押し当て、恒温恒湿装置中に試料を保持し、白金線間の交流インピーダンス測定から求めた。すなわち、温度80℃、相対湿度30%の環境下でインピーダンスを測定した。実施例のプロトン伝導度は、比較例と比べて大きく向上した。
【産業上の利用可能性】
【0065】
本発明は、電気自動車、燃料電池自動車などの自動車や、ノートパソコン、携帯電話、携帯情報端末などのモバイル機器、家庭用発電装置などの発電源として用いられる固体高分子形燃料電池を構成する高分子電解質膜として利用することができる。
【符号の説明】
【0066】
1……高分子電解質膜(高分子電解質)
2……空気極側電極触媒層
3……燃料極側電極触媒層
4……空気極側ガス拡散層
5……燃料極側ガス拡散層
6……空気極
7……燃料極
8……ガス流路
9……冷却水流路
10……セパレータ
11……固体高分子形燃料電池の単セル
12……膜電極結合体
【技術分野】
【0001】
本発明は、高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池に関し、特に、固体高分子形燃料電池に用いられる高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池に関する。
【背景技術】
【0002】
固体高分子形燃料電池(以下、「PEFC(Polymer Electrolyte Fuel Cell)」と記す。)は、環境負荷ガスの放出を削減することに貢献することができるため、燃料電池自動車や、定置用コジェネレーション、携帯電話の電源として研究開発が進められている。PEFCでは、電池内でプロトンの伝導が起こることによって発電反応が進行する。PEFCにおけるプロトン伝導には水の存在が必須であり、それ故にPEFCの発電反応を進行させるためには加湿器が必要となる。車両などに燃料電池を適用する場合、車載性の観点からは加湿器は小さいことが望まれるため、低加湿下でもプロトン伝導が良好に行われる電解質が求められている。ナフィオン(登録商標、デュポン社製)、アシプレックス(登録商標、旭化成株式会社製)に代表されるフッ素系樹脂電解質は、低加湿下におけるプロトン伝導性に優れており、PEFCにおいて汎用されている材料である。
【0003】
しかしながら、フッ素系樹脂電解質は、フッ素からなる高分子材料であるため、リサイクル性が低いという問題があった。燃料電池自動車の普及を考えた場合、燃料電池をリサイクルすることができるかどうかという点が非常に重要であり、リサイクルができない材料の環境への負荷を無視することができない。
さらに、フッ素系樹脂電解質を単独で電解質膜として適用した場合、耐久性が低くなるという問題があった。このようなことから、フッ素系樹脂電解質の代替となる新たな材料の必要性が高まってきている。
【0004】
具体的な代替材料の一つとして炭化水素系電解質があり、この炭化水素系電解質の開発が近年行われてきている。炭化水素系材料は、一般的にフッ素系樹脂電解質よりも耐久性に優れ、フッ素系樹脂電解質の代替として期待される。
例えば、特許文献1には、炭化水素系電解質を用いて、低加湿で高いプロトン伝導性を得るために、液晶骨格を有する材料を用いて、スルホン酸基のネットワークを形成させることにより、低加湿で高いプロトン伝導性が得られることについて記載されている。
【先行技術文献】
【特許文献】
【0005】
【特許文献1】特開2003−55337号公報
【発明の概要】
【発明が解決しようとする課題】
【0006】
しかしながら、特許文献1に記載のスルホン酸型液晶モノマー材料を高分子量化したスルホン化液晶ポリマー材料は、側鎖のメソゲンがビフェニルである。このビフェニルは、オルソ位の水素原子同士が電子反発を起こし、2つの環がねじれるためにメソゲン同士のスタッキングが不安定になる。それに伴い、酸基のネットワーク形成が阻害され、より高いプロトン伝導度が達成できなくなることが懸念される。また、主鎖がメタクリル基、もしくはアクリル骨格のため、高分子電解質膜を薄膜化したことにより性能が向上しにくくなることがあった。
【0007】
そこで、本発明は、上記の課題を解決するものであって、側鎖のメソゲンのスタッキングを促進させ、また、薄膜化を可能とするため主鎖に剛直な骨格を用いることで、プロトン伝導性に優れ、発電性能を向上させた高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池を提供することを目的とする。
【課題を解決するための手段】
【0008】
本発明による高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池は、上記の目的を達成するために、次のように構成される。
本発明のある態様による第1の高分子電解質は、下記の化学一般式(1)(A1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。)で表わされる高分子単位を有することを特徴とする。
【0009】
【化1】

【0010】
本発明によれば、高いプロトン伝導度を有し、かつ薄膜化が可能であって、高い発電性能を有する高分子電解質を提供することが可能となる。
本発明のある態様による第2の高分子電解質は、前記アルキル基は、−(CH2)m−(mは1以上の整数とする。)であることを特徴とする。
【0011】
本発明によれば、アルキル基を−(CH2)m−とすることで、高分子電解質からなる高分子電解質膜の柔軟性を維持しつつ、酸価の高い高分子電解質膜を得ることが可能となる。
本発明のある態様による第3の高分子電解質は、前記プロトン酸基は、スルホン酸基またはホスホン酸基であることを特徴とする。
【0012】
本発明によれば、プロトンの解離を促進させて、プロトン伝導度を向上することが可能となる。
本発明のある態様による第4の高分子電解質は、前記化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する下記の化学一般式(2)(X1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子を示す。)で表されるイオン性材料を含んで形成されたことを特徴とする。
【0013】
【化2】

【0014】
本発明によれば、イオン性材料を含んで形成されているため、高分子電解質膜を薄膜化して際にも、膜電極接合体を形成することのできる十分な機械強度を得ることが可能となる。
本発明のある態様による第5の高分子電解質は、イオン交換容量は、2.1meq/g以上2.4meq/g以下であることを特徴とする。
本発明によれば、イオン交換容量を上記のようにすることにより、上記で説明したような高分子電解質膜の性能を最も高めることが可能となる。
本発明のある態様による高分子電解質膜は、第1〜4のいずれか1つの高分子電解質を用いて形成されたことを特徴とする。
【0015】
本発明によれば、高いプロトン伝導度、発電性能を兼ね備えた高分子電解質膜を提供することが可能となる。
本発明のある態様による固体高分子形燃料電池は、上記の高分子電解質膜を用いて形成されたことを特徴とする。
本発明によれば、上記の高分子電解質膜を用いて形成された固体高分子形燃料電池であり、高い発電性能を備えた固体高分子形燃料電池を提供することが可能となる。
【発明の効果】
【0016】
本発明によれば、上記の化学一般式(1)で表される高分子単位を有することにより、高いプロトン伝導度を有し、かつ薄膜化が可能であって、高い発電性能を有する高分子電解質を提供することができる。
また、本発明によれば、プロトン酸基が、スルホン酸基またはホスホン酸基であることを特徴とする高分子電解質により、プロトンの解離を促進させ、プロトン伝導度を向上させることができる。
【0017】
また、本発明によれば、上記の高分子電解質から高分子電解質膜を形成することにより、高いプロトン伝導度、および発電性能を兼ね備えた高分子電解質膜を提供することができる。
また、本発明によれば、上記の化学一般式(2)で表されるX1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子である高分子電解質(イオン性材料)であり、高分子電解質膜を薄膜化しても、膜電極接合体を形成するために必要な機械強度を十分に得ることができる。
【0018】
また、本発明によれば、上記の高分子電解質膜を用いて固体高分子形燃料電池を構成することにより、高い発電性能を備えた固体高分子形燃料電池を提供することができる。
【図面の簡単な説明】
【0019】
【図1】本発明の高分子電解質膜1の両面に電極触媒層が形成された膜電極接合体12を装着した固体高分子形燃料電池の単セル11の構成を示す分解断面図である。
【図2】図1に示した膜電極結合体12の構成を示す要部断面図である。
【図3】ベンゼン環のπスタックの構造の概念を示す模式図である。
【図4】ビフェニルの構造を示す一般式である。
【図5】ジフェニルアセチレンの構造を示す一般式である。
【発明を実施するための形態】
【0020】
以下に、添付した図面を参照して、本発明の高分子電解質、それを用いた高分子電解質膜および固体高分子形燃料電池について詳細に説明する。
なお、本発明は、以下に記載する各実施の形態に限定されるものではなく、当業者の知識に基づいて設計の変更等の変形を加えることも可能であり、そのような変形が加えられた実施の形態も本発明の範囲に含まれうるものである。
【0021】
まず、図1および図2を参照して、本実施形態に係る固体高分子形燃料電池の単セル11の全体の構成を説明する。
図1は、本発明の高分子電解質膜(高分子電解質)1の両面に電極触媒層が形成された膜電極接合体12を装着した固体高分子形燃料電池の単セル11の構成を示す分解断面図である。
【0022】
図1に示す固体高分子形燃料電池の単セル11は、その上下部を保護する2つのセパレータ10に膜電極結合体12が挟まれて形成される。なお、2つのセパレータ10のうちの一方のセパレータと膜電極結合体12との間には、ガス拡散層として空気極側ガス拡散層4が形成される。また、他方のセパレータと膜電極結合体12との間にも、同様にガス拡散層として燃料極側ガス拡散層5が形成される。
【0023】
そして、膜電極結合体12は、高分子電解質膜1の空気極側ガス拡散層4の面に空気極側電極触媒層2が形成される。また、膜電極結合体12は、高分子電解質膜1の燃料極側ガス拡散層5の面に燃料極側電極触媒層3が形成される。
上記の空気極側電極触媒層2と空気極側ガス拡散層4とで、電極として機能する空気極6が形成される。さらに、燃料極側電極触媒層3と燃料極側ガス拡散層5とで、同じく電極として機能する燃料極7が形成される。この空気極6と燃料極7とに、図示しない外部の負荷が接続されることで、負荷を駆動することができる。
【0024】
また、セパレータ10には、一方の面にはガスが流れる経路としてガス流路8が形成され、他方の面には冷却水が流れる経路として冷却水流路9が形成されている。
また、図2は、図1に示した膜電極結合体12の構成を示す要部断面図である。図2に示す膜電極結合体12は、高分子電解質膜1の空気極6側の面に、空気極側電極触媒層2が形成されている。また、膜電極結合体12は、高分子電解質膜1の燃料極7側の面に、空気極側電極触媒層3が形成されている。
【0025】
続いて、図3〜図5を参照して、プロトン伝導度を向上させるための方法について説明する。
図3は、ベンゼン環のπスタックの構造の概念を示す模式図である。一般的に、芳香族化合物は、図3に示すように、芳香環上に非局在化したπ電子同士が相互作用することで、芳香環の面と面を重ね合わせるように分子間でのスタック(πスタック)を形成することが知られている。この図3では、上下のベンゼン環の炭素原子同士が、互いに重なり合う配座の例を具体的に示している。
【0026】
液晶分子のメソゲンはこのスタックの形成を利用し、秩序構造を形成している。すなわち、液晶分子が集合体を形成する上では、スタックの形成を促進することが重要である。
本実施形態では、メソゲンにプロトン酸基が、連結基を通して結合しており、メソゲンのネットワークが直接プロトンのネットワークになりうる。従って、メソゲンのスタックの形成をさらに促進することで、分子内でのプロトンの輸送を効率よく行うことができ、プロトン伝導度を向上させることができる。
【0027】
また、図4は、ビフェニルの構造を示す一般式である。また、ジフェニルアセチレンの構造を示す一般式である。通常、メソゲンとして用いられることが多いビフェニルは、図4に示すように、ベンゼン環同士が結合している炭素の隣(オルソ位)の炭素に結合した水素同士が電子反発を起こし、隣り合う環同士(図4中に矢印Aで示す箇所)が約50°ねじれることが知られている。よりスタックを形成しやすくするためには、このねじれを解消する必要がある。
【0028】
本実施形態における高分子電解質膜1は、メソゲンのビフェニルをジフェニルアセチレンに変更している。ジフェニルアセチレンは、図5に示すように、ビフェニルの環同士の間に、3重結合をスペーサーとして挿入した構造をしている。このため、ビフェニルに見られる水素同士の電子反発を起こすことがないため、隣り合う環同士(図5中に矢印B,Cで示す箇所)のねじれは殆ど起こらずに、環同士はほぼ同一平面状にある。
【0029】
以下に、本発明の固体高分子形燃料電池の薄膜化が可能であって、さらに耐久性に優れた高分子電解質膜の製造方法について説明する。なお、本発明は、以下に記載する各実施の形態に限定されうるものではなく、当業者の知識に基づいて設計の変更等の変形を加えることも可能であり、そのような変形が加えられた実施の形態も本発明の範囲に含まれうるものである。
(化合物の合成)
下記の化学一般式(1)におけるA1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。
【0030】
【化3】

【0031】
また、下記の化学一般式(2)におけるA1,A2,Bは、上記の化学一般式(1)で定義されたものと同義であるが、X1およびX2はそれぞれ独立して塩素原子、臭素原子、またはヨウ素原子のいずれかである。X1およびX2は同一であっても、異なってもよいが、同一であることが好ましい。
【0032】
ここで、ポリマー化が可能な基とは、具体的に、X1またはX2を含む基のことをいう。また、イオン性材料とは、Yで表されるプロトン酸基を有する材料のことをいう。
【0033】
【化4】

【0034】
つまり、上記の高分子電解質膜(高分子電解質)1は、上記の化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する上記の化学一般式(2)で表わされるイオン性材料を重合させることによって得られる。
上記の化学一般式(2)中のA1,A2で表されるアルキル基は、−(CH2)m−(mは1以上の整数である。)であることが好ましく、mが3または4であることが特に好ましい。mが3または4であることによって、その高分子電解質からなる高分子電解質膜の柔軟性を維持しつつ、酸価の高い高分子電解質膜を得ることができる。
なお、高分子電解質1のイオン交換容量は、上記で説明したような高分子電解質膜の性能を高める観点から、2.1meq/g以上2.4meq/g以下であることが特に好ましい。
【0035】
上記の化学一般式(2)のモノマー製造方法は特に限定されないが、例えばA1がエチレン基−(CH2)2−、A2がプロピレン基−(CH2)3−、およびBがスルホン酸基である場合、以下のようにして合成できる。なお、本実施形態においては、Bがスルホン酸基である場合について説明するが、Bはスルホン酸基に限定されない。例えば、Bは、ホスホン酸基であってもよい。
【0036】
まず、1,2−ジ(4−ヒドロキシフェニル)アセチレンを用意し、これと無機塩基およびプロパンスルトンを反応させることにより、下記の化学一般式(3)で表される化合物を得ることができる。
【0037】
【化5】

【0038】
この際の反応条件は、特に限定されるものではないが、反応温度は好ましくは、25℃以上80℃以下であることが好ましい。反応時間は、好ましくは、10時間以上48時間以下で行われる。また、化合物を反応させるのは、大気雰囲気下であってもよいし、窒素雰囲気下であってもよい。
【0039】
反応溶媒としては、良溶媒であることが望ましく、より好ましくは、アルコール系溶媒であることが望ましい。具体的な反応溶媒として、例えば、エタノール、メタノール、1−プロパノール、2−プロパノール、1−ブタノールが挙げられる。
また、塩基としては、強塩基であることが望ましく、例えば、水酸化ナトリウム、水酸化カリウムなどが挙げられる。塩基の量は、1,2−ジ(4−ヒドロキシフェニル)アセチレン100モル%に対して、50モル%以上100モル%以下であることが好ましく、70モル%以上90モル%以下であることが好ましい。
【0040】
次に、下記の化学一般式(4)で表わされる化合物を用意する。ここで、Xはそれぞれ塩素原子、臭素原子またはヨウ素原子のいずれかである。
【0041】
【化6】

【0042】
さらに、下記の化学一般式(3)で表わされる化合物を無機塩基で処理した後に、化学一般式(4)に示される化合物を反応させることで、下記の化学一般式(5)で表わされるモノマー化合物を得ることができる。
【0043】
【化7】

【0044】
この際の反応条件は、特に限定されるものではないが、反応温度は好ましくは、25℃以上80℃以下が好ましい。また、反応時間は、好ましくは、10時間以上48時間以下で行われる。化合物を反応させるのは、大気雰囲気下であってもよいし、窒素雰囲気下であってもよい。
【0045】
反応溶媒としては、良溶媒であることが望ましく、より好ましくは、極性の高い溶媒であることが望ましい。例えば、ジメチルスルホキシド、ジメチルホルムアミド、ジメチルアセトアミド、N−メチルピロリドンなどが挙げられる。
塩基としては、強塩基であることが望ましく、例えば、水酸化ナトリウム、水酸化カリウムなどが挙げられる。塩基の量は、上記の化学一般式(4)で表わされる化合物100モル%に対して、50モル%以上100モル%以下であることが好ましく、80モル%以上100モル%以下であることが好ましい。
【0046】
該モノマーの重合は、特に限定されるものではないが、特定の触媒の存在下に反応させることが好ましい。また、この際に使用される触媒は、遷移金属化合物を含む触媒系である。また、この触媒系としては、配位子成分、配位子が配位された遷移金属錯体、および還元剤を必須成分とし、さらに、重合速度を上げるために塩を添加してもよい。
配位子成分としては、トリフェニルホスフィン、2,2’−ビピリジン、1,5−シクロオクタジエン、または1,3−ビス(ジフェニルホスフィノ)プロパンなどが挙げられる。これらのうち、トリフェニルホスフィン、2,2’−ビピリジンが好ましい。上記配位子成分である化合物は、1種単独で用いてもよく、2種以上を併用してもよい。配位子成分は、上記モノマー100モル%に対して、1モル%以上100モル%以下であることが好ましく、1モル%以上20モル%以下であることがより好ましい。
【0047】
配位子が配位された遷移金属錯体としては、例えば、塩化ニッケルビス(トリフェニルホスフィン)、臭化ニッケルビス(トリフェニルホスフィン)、ヨウ化ニッケルビス(トリフェニルホスフィン)、硝酸ニッケルビス(トリフェニルホスフィン)、塩化ニッケル(2,2’−ビピリジン)、臭化ニッケル(2,2’−ビピリジン)、ビス(1,5−シクロオクタジエン)ニッケル、テトラキス(トリフェニルホスフィン)ニッケル、テトラキス(トリフェニルホスファイト)ニッケル、またはテトラキス(トリフェニルホスフィン)パラジウムなどが挙げられる。これらのうち、塩化ニッケルビス(トリフェニルホスフィン)、塩化ニッケル(2,2’−ビピリジン)が好ましい。遷移金属錯体は、上記モノマー100モル%に対して、1モル%以上100モル%以下であることが好ましく、1モル%以上20モル%以下であることがより好ましい。
【0048】
上記の触媒系に使用することができる還元剤としては、例えば、鉄、亜鉛、マンガン、アルミニウム、マグネシウム、ナトリウム、またはカルシウムなどが挙げられる。これらのうち、亜鉛、マグネシウム、マンガンが好ましい。これらの還元剤は、有機酸などの酸に接触させることにより、より活性化して用いることができる。還元剤は、上記モノマー100モル%に対して、1モル%以上100モル%以下であること好ましく、10モル%以上30モル%以下であることが好ましい。
【0049】
また、上記の触媒系において使用することのできる塩としては、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、ヨウ化ナトリウム、硫酸ナトリウムなどのナトリウム化合物;フッ化カリウム、塩化カリウム、臭化カリウム、ヨウ化カリウム、硫酸カリウムなどのカリウム化合物;フッ化テトラエチルアンモニウム、塩化テトラエチルアンモニウム、臭化テトラエチルアンモニウム、ヨウ化テトラエチルアンモニウム、硫酸テトラエチルアンモニウムなどのアンモニウム化合物が挙げられる。これらのうち、臭化ナトリウム、ヨウ化ナトリウム、臭化カリウム、臭化テトラエチルアンモニウム、ヨウ化テトラエチルアンモニウムが好ましい。塩は、上記モノマー100モル%に対して、1以上100モル%以下であることが好ましく、10モル%以上30モル%以下であることが好ましい。
【0050】
また、該重合の際に用いられる溶媒としては、例えばテトラヒドロフラン、シクロヘキサノン、ジメチルスルホキシド、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチル−2−ピロリドン、γ−ブチロラクトン、N,N−ジメチルイミダゾリジノンなどが挙げられる。これらのうち、テトラヒドロフラン、N,N−ジメチルホルムアミド、N,N−ジメチルアセトアミド、N−メチル−2−ピロリドン、N,N’−ジメチルイミダゾリジノンが好ましい。これらの重合溶媒は、十分に乾燥してから用いることが好ましい。
【0051】
重合の際の重合温度および重合時間は、特に限定されるものではなく、分子量や、重合の濃度等によって適宜設定すればよい。例えば、重量平均分子量が10万以上50万以下の重合体を得ることを目的とする場合、反応効率の点から、重合温度が好ましくは25℃以上80℃以下、より好ましくは40℃以上70℃以下、重合時間が好ましくは8時間以上40時間以下、より好ましくは16時間以上32時間以下で重合が行われる。重合の際の重合圧力は、特に限定されず、加圧下、常圧(大気)下、減圧下のいずれかでよく、場合により適宜設定すればよいが、常圧下であることが好ましい。
【0052】
このようにして得られた高分子電解質を用いて高分子電解質膜を製造する方法としては、特に限定されないが、例えば、本発明のポリフェニレン系電解質を溶剤に溶解して溶液とした後、キャスティングにより、基材上に塗布し、フィルム状に形成する方法や、所定のギャップに制御されたアプリケータを用いて塗工、成膜する方法、ダイコータを用いて成膜する方法等が挙げられる。
【0053】
また、成膜にあたっては、粘度を10mPa・s以上10000mPa・s以下とすることが好ましく、10mPa・s以上1000mPa・s以下とすることがより好ましい。上記の範囲内であると、溶剤の残留量が少なく、また溶液を乾燥する際に多量の気泡が発生する確率が低い。このため、レべリング効果により厚みのむらを低減することができるため、安定したプロトン伝導性を確保することができる。
この際の電解質濃度は、分子量にもよるが、通常、2.5質量%以上50質量%以下、好ましくは7質量%以上25質量%以下である。上記の範囲内であれば、成膜性に優れる。
【0054】
また、この際に用いられる溶媒としては、例えば、N−メチル−2−ピロリドン、N,N−ジメチルホルムアミド、γ−ブチルラクトン、N,N−ジメチルアセトアミド、ジメチルスルホキシド、ジメチル尿素、ジメチルイミダゾリジノンなどの非プロトン系極性溶剤、メタノール、エタノール、プロピルアルコール、isо−プロピルアルコール、sec−ブチルアルコール、tert−ブチルアルコールなどのアルコール系溶媒およびアセトン、メチルエチルケトン、シクロヘキサノンなどのケトン系溶媒などが挙げられる。これらの溶媒は、単独で用いてもよく、あるいは2種以上混合させてもよい。またこれらの溶媒に水を添加したものを用いてもよい。
【0055】
粘度を調整したポリマー溶液は、例えば、基材にキャストされる。キャストする基材としては、金属材料、ガラス、セラミックス、プラスチックなどが挙げられる。なお、基材の形状は、特に限定されるものではないため、任意の形状に形成することができる。
基材上に形成されたフィルムは、好ましくは25℃以上140℃以下、0.1時間以上24時間以下、加熱することにより、高分子電解質膜を得ることができる。
【0056】
以下に、実施例および比較例について示す。
以下、本発明を実施例により詳細に説明するが、本発明はこれらに限定されるものではない。
(実施例)
(化学一般式(3)の合成)
窒素雰囲気下、1,2−ジ(4−ヒドロキシフェニル)アセチレン105g(0.5mol)を用意し、プロパンスルトンを61g(0.5mol)および水酸化ナトリウム16g(0.4mol)、メタノールを200ml加えて、48時間撹拌した。その後、ジエチルエーテルで再沈殿させ、ろ過した。ろ過物をメタノールにて洗いこみ、上記の化学一般式(3)で表される化合物を得た。
(化学一般式(6)の合成)
窒素雰囲気下、上記の化学一般式(3)で表される化合物177g(0.5mol)に、2−(2,5−ジクロロフェニル)−1−ブロモエタン127g(0.5mol)および水酸化ナトリウム20g(0.5mol)、ジメチルスルホキシドを200mlを加えて、48時間撹拌した。その後、メタノールで再沈殿させ、ろ過した。ろ過物をメタノールにて洗いこみ、下記の化学一般式(6)で表される化合物を得た。
【0057】
【化8】

【0058】
(化学一般式(7)の合成)
窒素雰囲気下、化学一般式(6)で表される化合物を7.9g(15mmol)に、トリフェニルホスフィン1.5g(5.6mmol)、ヨウ化ナトリウム0.3g(2mmol)、亜鉛1.3g(20mmol)、ビス(トリフェニルホスフィン)ニッケル(II)ジクロリド0.31g(0.48mmol)を加えて、さらに、溶媒として、20mlのジメチルホルムアミドを加えて、60℃で24時間撹拌した。反応物をメタノールで再沈し、固体を濾別したのち、濃塩酸でプロトンフォームした。さらに純水で濾液のpHが7になるまで洗浄したのち、固体を減圧乾燥し、下記の化学一般式(7)で表される化合物を得た。
【0059】
【化9】

【0060】
以下、本発明を比較例により詳細に説明するが、本発明はこれらに限定されるものではない。
(9−ブロモ−1−デセンの合成)
500mlの三角フラスコにベンゼン100mlおよびピリジン1.0gを加えて、9−デセン−1−オール25g(0.16mol)を溶解した。次に三臭化リン43.2g(0.16mol)を溶解させたベンゼン溶液100mlを氷冷下でゆっくりと滴下した後、室温で18時間撹拌した。その後、反応液を氷水中に注ぎ、ジエチルエーテル300mlで抽出した。ここで得たエーテル−ベンゼン混合液は無水硫酸ナトリウムで一晩脱水した。吸引ろ過により硫酸ナトリウムを除き、エーテル−ベンゼンを減圧除去し、残渣を減圧蒸留して目的物9−ブロモ−1−デセンを得た。
【0061】
(4−(9−デセニルオキシフェニル)フェノールの合成)
水酸化ナトリウム3.40g(0.08mol)を100mlのエタノールに溶解させた。この溶液を4,4’−ビフェノール14.9g(0.08mol)を溶解させた100mlエタノールに少量ずつ加えて、エタノールを減圧除去した。残渣を150mlジメチルホルムアミドに窒素気流下で加温して溶解させた(A液)。上記で調整した9−ブロモ−1−デセン15.8g(0.072mol)、フェノチアジン0.1gを30mlのDMFに溶解させた(B液)。窒素雰囲気下でよく撹拌しながら、A液にB液を30分程度かけて加えて、40℃で24時間反応させた。反応終了後、反応液を冷却し、300mlの10%冷却塩酸で洗浄した後、300mlのエーテルで抽出し、次いで100ml冷蒸留水で洗浄した。エーテル層は無水硫酸ナトリウムで一晩脱水する。残渣に300mlのヘキサンを加えて、ろ過により沈殿物を得る。次いで200mlベンゼンを加えて、ベンゼン可溶部分をベンゼンを用いたカラムクロマトグラフィーで精製して4−(9−デセニルオキシフェニル)フェノールを得た。
【0062】
(3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸の合成)
ジメチルホルムアミド30ml中に重合禁止剤フェノチアジン0.05gを溶解させた。そこへ、1,8−ジアザビシクロ[5,4,0]−7−ウンデンセン(DBU)1.22g(0.008mol)と4−(9−デセニルオキシフェニル)フェノール0.65g(0.002mol)、3−ブロモプロパンスルホン酸ナトリウム1.8g(0.008mol)を溶解させ、窒素雰囲気下、50℃で48時間撹拌した。反応終了後、溶媒を濃縮しジエチルエーテルを加えて、ろ過することにより沈殿を得た。次に、沈殿を蒸留水でよく洗浄した。次に、洗浄後の沈殿を6mol/LのHCl中で24時間撹拌後、遠心分離機により沈殿を得て、この沈殿をジエチルエーテルで洗浄後、乾燥して3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸を得た。
【0063】
(比較例)
(3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸の高分子量化)
窒素雰囲気下、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロプルスルホン酸を488mg(1mmol)、開始剤であるAIBNを6.6mg(0.04mmol)加えて、ジメチルスルホキシドを4.8ml加えた。その後、60℃で60時間熱重合して高分子量化させた。その後、アセトンで再沈殿させ、ポリマーを得た。
【0064】
(ポリマーの製膜)
化学一般式(7)、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸ポリマーをジメチルスルホキシドに溶解させ、ガラスにキャストし、45℃で12時間、80℃で12時間、80℃で1時間真空乾燥させることで、膜を得た。
(薄膜化)
化学一般式(7)で表わされるポリマー膜は、3−[6−(9−デセニルオキシ)ビフェニルオキシ]プロピルスルホン酸ポリマーから得られる膜に比較して、薄膜化しても膜電極接合体が作製できる機械強度を有していた。
(プロトン伝導度の測定)
電解質膜の交流抵抗は、10mm幅の短冊状のプロトン伝導膜試料の表面に、白金線を押し当て、恒温恒湿装置中に試料を保持し、白金線間の交流インピーダンス測定から求めた。すなわち、温度80℃、相対湿度30%の環境下でインピーダンスを測定した。実施例のプロトン伝導度は、比較例と比べて大きく向上した。
【産業上の利用可能性】
【0065】
本発明は、電気自動車、燃料電池自動車などの自動車や、ノートパソコン、携帯電話、携帯情報端末などのモバイル機器、家庭用発電装置などの発電源として用いられる固体高分子形燃料電池を構成する高分子電解質膜として利用することができる。
【符号の説明】
【0066】
1……高分子電解質膜(高分子電解質)
2……空気極側電極触媒層
3……燃料極側電極触媒層
4……空気極側ガス拡散層
5……燃料極側ガス拡散層
6……空気極
7……燃料極
8……ガス流路
9……冷却水流路
10……セパレータ
11……固体高分子形燃料電池の単セル
12……膜電極結合体
【特許請求の範囲】
【請求項1】
下記の化学一般式(1)(A1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。)で表わされる高分子単位を有することを特徴とする高分子電解質。
【化10】

【請求項2】
前記アルキル基は、−(CH2)m−(mは1以上の整数とする。)であることを特徴とする請求項1に記載の高分子電解質。
【請求項3】
前記プロトン酸基は、スルホン酸基またはホスホン酸基であることを特徴とする請求項1または2に記載の高分子電解質。
【請求項4】
前記化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する下記の化学一般式(2)(X1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子を示す。)で表されるイオン性材料を含んで形成されたことを特徴とする請求項1〜3のいずれか1項に記載の高分子電解質。
【化11】

【請求項5】
イオン交換容量は、2.1meq/g以上2.4meq/g以下であることを特徴とする請求項1〜4のいずれか1項に記載の高分子電解質。
【請求項6】
請求項1〜5のいずれか1項に記載の高分子電解質を用いて形成されたことを特徴とする高分子電解質膜。
【請求項7】
請求項6に記載の高分子電解質膜を用いて形成されたことを特徴とする固体高分子形燃料電池。
【請求項1】
下記の化学一般式(1)(A1,A2はアルキル基を示し、Bはプロトン酸基を示し、nを10以上10000以下の整数とする。)で表わされる高分子単位を有することを特徴とする高分子電解質。
【化10】

【請求項2】
前記アルキル基は、−(CH2)m−(mは1以上の整数とする。)であることを特徴とする請求項1に記載の高分子電解質。
【請求項3】
前記プロトン酸基は、スルホン酸基またはホスホン酸基であることを特徴とする請求項1または2に記載の高分子電解質。
【請求項4】
前記化学一般式(1)に対して、ポリマー化が可能な基としてX1,X2を有する下記の化学一般式(2)(X1,X2はそれぞれ独立して、塩素原子、臭素原子、またはヨウ素原子を示す。)で表されるイオン性材料を含んで形成されたことを特徴とする請求項1〜3のいずれか1項に記載の高分子電解質。
【化11】

【請求項5】
イオン交換容量は、2.1meq/g以上2.4meq/g以下であることを特徴とする請求項1〜4のいずれか1項に記載の高分子電解質。
【請求項6】
請求項1〜5のいずれか1項に記載の高分子電解質を用いて形成されたことを特徴とする高分子電解質膜。
【請求項7】
請求項6に記載の高分子電解質膜を用いて形成されたことを特徴とする固体高分子形燃料電池。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−67702(P2013−67702A)
【公開日】平成25年4月18日(2013.4.18)
【国際特許分類】
【出願番号】特願2011−206084(P2011−206084)
【出願日】平成23年9月21日(2011.9.21)
【出願人】(000003193)凸版印刷株式会社 (10,630)
【Fターム(参考)】
【公開日】平成25年4月18日(2013.4.18)
【国際特許分類】
【出願日】平成23年9月21日(2011.9.21)
【出願人】(000003193)凸版印刷株式会社 (10,630)
【Fターム(参考)】
[ Back to top ]

