高純度シリカの製造方法
【課題】高純度のシリカを、簡易にかつ低コストで製造しうる方法を提供する。
【解決手段】(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【解決手段】(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、高純度シリカの製造方法に関する。
【背景技術】
【0002】
高純度シリコンは、半導体デバイス、触媒担体等に用いられている。
高純度シリコンの製造方法として、例えば、金属シリコンから製造された高純度のシリコン塩化物(トリクロロシラン)を原料として用いる方法が提案されている(特許文献1)。
特許文献1に記載の方法によると、非常に高純度のシリコンを得ることができる。しかし、この方法は、工程が煩雑でかつ高コストであるという問題がある。このような事情下において、高純度のシリコンを、低コストかつ大量に製造することのできる技術が望まれている。
これを解決すべく、二酸化ケイ素を含有しかつ多孔質で微細構造を有する原料を精製して高純度シリカを製造し、次いで、この高純度シリカを原料としてシリコンを生成し、得られたシリコンにレーザを照射することなどによって、高純度シリコンを製造する方法が提案されている(特許文献2)。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2006−001804号公報
【特許文献2】特開2006−188367号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
特許文献2に記載の方法によると、従来技術に比して、低コストでかつ簡易に、高純度のシリコンを得ることができる。シリコンの原料となる高純度シリカを、より低コストでかつ簡易に得ることができれば、好都合である。
そこで、本発明は、高純度シリカを、簡易にかつ低コストで製造することのできる方法を提供することを目的とする。
【課題を解決するための手段】
【0005】
本発明者は、上記課題を解決するために鋭意検討した結果、ケイ酸アルカリ水溶液と鉱酸を混合して、非ゲル状の沈降性シリカとして析出するとともに、製造工程において原料と過酸化水素を混合することによって、前記の目的を達成することができることを見出し、本発明を完成した。
【0006】
すなわち、本発明は、以下の[1]〜[12]を提供するものである。
[1](B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
[2](C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含む前記[1]に記載の高純度シリカの製造方法。
[3](B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程と、(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含み、前記工程(C)において、鉱酸と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
[4]工程(B)において、ケイ酸アルカリ水溶液と鉱酸の混合が、ケイ酸アルカリ水溶液を鉱酸に添加することによって行われる、前記[1]〜[3]のいずれかに記載の高純度シリカの製造方法。
[5]工程(B)において、ケイ酸アルカリ水溶液と鉱酸を、pH1.0以下に保ちながら混合する、前記[1]〜[4]のいずれかに記載の高純度シリカの製造方法。
[6]工程(B)において、ケイ酸アルカリ水溶液のSi濃度が10.0〜20.0質量%である、前記[1]〜[5]のいずれかに記載の高純度シリカの製造方法。
[7]過酸化水素の添加量が、シリカ(SiO2)100質量%に対して、0.1〜15.0質量%である前記[1]〜[6]のいずれかに記載の高純度シリカの製造方法。
[8]工程(B)の前に、(A)シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程を含む、前記[1]〜[7]のいずれかに記載の高純度シリカの製造方法。
[9]工程(A)と工程(B)の間に、(B1)工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中の不純物を析出させた後、固液分離を行い、ケイ酸アルカリ水溶液と、固形分を得る不純物回収工程、を含む、前記[8]に記載の高純度シリカの製造方法。
[10]工程(A)の前に、(A1)シリカ含有鉱物を水洗して、粘土分及び有機物を除去する原料水洗工程、を含む前記[8]または[9]に記載の高純度シリカの製造方法。
[11]工程(A)の前に、(A2)シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成して、有機物を除去する原料焼成工程、を含む前記[8]〜[10]のいずれかに記載の高純度シリカの製造方法。
[12](D)前工程で得られたSiO2を含む固形分と水を混合して、上記固形分中に残存する不純物を溶解させた後、上記スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る水洗浄工程、を含む前記[1]〜[11]のいずれかに記載の高純度シリカの製造方法。
【発明の効果】
【0007】
本発明の高純度シリカの製造方法によると、操作が簡易であり、処理効率が高いことなどに起因して、従来技術に比して低い製造コストで高純度シリカを得ることができる。
さらに、本発明の製造方法により得られる高純度シリカは、シリカの含有率が高く、またアルミニウム(Al)、鉄(Fe)、チタン(Ti)、ホウ素(B)、リン(P)、有機物(C)などの不純物、特にチタン(Ti)の含有率が低いという特長がある。
【図面の簡単な説明】
【0008】
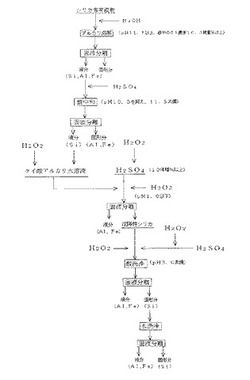
【図1】本発明の高純度シリカの製造方法の実施形態の一例を示すフロー図である。
【図2】珪質頁岩の一例についてのCu−Kα線による粉末X線の回折強度を示すグラフである。
【図3】珪質頁岩の一例についてのオパールCTの半値幅を示すグラフである。
【発明を実施するための形態】
【0009】
以下、本発明の高純度シリカの製造方法を詳しく説明する。
なお、以下の工程(A1)〜工程(D)中、工程(B)は、本発明において必須の工程であるが、工程(A)は、シリカ含有鉱物を原料としてケイ酸アルカリ水溶液を調製する場合に追加される工程であり、工程(A1)、(A2)、(B1)、(C)及び(D)は、本発明において必須ではなく、任意で追加可能な工程である。
[工程(A1);原料水洗工程]
工程(A1)は、シリカ含有鉱物(岩石状又は粉末状)を水洗して、粘土分及び有機物を除去する工程である。水洗後のシリカ含有鉱物は、通常、フィルタープレス等を用いて、さらに脱水させる。
シリカ含有鉱物としては、珪藻土、珪質頁岩等が挙げられる。シリカ含有鉱物は、アルカリに対する溶解性が高いことが望ましい。
ここで、珪藻土とは、珪藻が海底や湖底に沈積し、長い年月の間に体内の原形質その他の有機物が分解し、非晶質シリカを主体とした珪藻殻が集積して堆積したものである。
珪質頁岩とは、珪質の生物遺骸等に由来する頁岩である。すなわち、海域には、珪質の殻を有する珪藻などのプランクトンが生息するが、このプランクトンの死骸が海底中に堆積すると、死骸中の有機物の部分は徐々に分解され、珪質(SiO2;シリカ)の殻のみが残る。この珪質の殻(珪質堆積物)が、時間の経過や温度・圧力の変化などに伴い、続成作用により変質して、硬岩化することにより珪質頁岩となる。なお、珪質堆積物中のシリカは、続成作用によって、非晶質シリカから、結晶化してクリストバライト、トリデイマイトへ、さらに石英へと変化する。
【0010】
珪藻土は、主に非晶質シリカであるオパールAからなる。珪質頁岩は、オパールAより結晶化が進んだオパールCTまたはオパールCを主に含む。オパールCTとは、クリストバライト構造とトリディマイト構造からなるシリカ鉱物である。オパールCとは、クリストバライト構造からなるシリカ鉱物である。このうち、本発明では、オパールCTを主とする珪質頁岩が好ましく用いられる。
さらに、Cu−Kα線による粉末X線回折において、石英の2θ=26.6degのピーク頂部の回折強度に対するオパールCTの2θ=21.5〜21.9degの回折強度は、石英を1とした場合の比率で0.2〜2.0の範囲が好ましく、0.4〜1.8の範囲がより好ましく、0.5〜1.5の範囲が特に好ましい。該値が0.2に満たない場合には、反応性に富むオパールCTの量が少ないため、シリカの収量が低下する。一方、該値が2.0を超える場合には、オパールCTの量が石英よりはるかに多くなり、このような珪質頁岩は資源的に少なく、経済性に劣る。
なお、石英に対するオパールCTの回折強度の比率は、以下の式で求める。
石英に対するオパールCTの回折強度の比率=(21.5〜21.9degのピーク頂部の回折強度)/(26.6degのピーク頂部の回折強度)
また、珪質頁岩のCu−Kα線による粉末X線回折において、オパールCTの2θ=21.5〜21.9degの間に存在するピークの半値幅は0.5°以上が好ましく、0.75°以上がより好ましく、1.0°以上がさらに好ましい。該値が0.5°未満では、オパールCTの結晶の結合力が増大し、アルカリとの反応性が低下して、シリカの収量が減少する。ここで、半値幅とは、ピーク頂部の回折強度の1/2に位置する回折線の幅をいう。
本発明で用いる珪質頁岩は、シリカ含有率が70質量%以上であることが好ましく、75質量%以上であることがより好ましい。このような珪質頁岩を用いることにより、より高純度のシリカを低コストで製造することができる。
シリカ含有鉱物は、例えば、珪質頁岩等のシリカ含有鉱物を粉砕装置(例えば、ジョークラッシャー、トップグラインダーミル、クロスビーターミル、ボールミル等)で粉砕することによって得ることができる。
[工程(A2);原料焼成工程]
工程(A2)は、シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成し、有機物を除去する工程である。
なお、工程(A1)と工程(A2)の双方を実施する場合、その順序は特に限定されないが、有機物の除去効率の観点から工程(A1)を先に行うことが好ましい。
【0011】
[工程(A);アルカリ溶解工程]
工程(A)は、シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程である。
ここで、ケイ酸アルカリ水溶液とは、化学式中にケイ酸(SiO2)を含む物質を含有するアルカリ性の水溶液をいう。
シリカ含有鉱物とアルカリ水溶液を混合してなるアルカリ性スラリーのpHは、11.5以上、好ましくは12.5以上、より好ましくは13.0以上となるように調整される。該pHが11.5未満であると、シリカを十分に溶解させることができず、シリカが固形分中に残存してしまうため、得られるシリカの収量が減少する。
pHを上記数値範囲内に調整するためのアルカリ水溶液としては、水酸化ナトリウム水溶液、水酸化カリウム水溶液等が用いられる。
スラリーの固液比(アルカリ水溶液1リットルに対するシリカ含有鉱物の質量)は、好ましくは100〜500g/リットル、より好ましくは200〜400g/リットルである。該固液比が100g/リットル未満では、スラリーの固液分離に要する時間が増大するなど、処理効率が低下する。該固液比が400g/リットルを超えると、シリカ等を十分に溶出させることができないことがある。
スラリーは、通常、所定時間(例えば、30〜90分間)攪拌される。
攪拌後のスラリーは、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離される。液分は、Si及び他の成分(Al、Fe等の不純物)を含むケイ酸アルカリ水溶液であり、次の工程(B1)または工程(B)で処理される。液分中に含まれるSiの濃度は、10.0質量%以上、好ましくは10.0〜20.0質量%、より好ましくは12.0〜18.0質量%、特に好ましくは13.0〜16.0質量%である。Si濃度が10.0質量%未満であると、後述する工程(B)においてシリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
なお、本工程においてアルカリ性スラリーを得る際の液温は、エネルギーコストの観点から、5〜100℃に保持されることが好ましく、10〜80℃に保持されることがより好ましく、10〜40℃に保持されることが特に好ましい。液温を上記範囲内とすることにより、処理効率を高めることができる。
【0012】
[工程(B1);不純物回収工程]
本工程は、工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中のSi以外の不純物(例えば、Al及びFe)を析出させた後、固液分離を行い、Siを含むケイ酸アルカリ水溶液と、固形分を得る工程である。
なお、本工程で回収されずに液分中に残存する不純物は、工程(B)以降の工程で回収される。
本工程において、酸との混合後の液分のpHは、10.3を超え、11.5未満、好ましくは10.4以上、11.0以下、特に好ましくは10.5以上、10.8以下である。該pHが10.3以下であると、不純物(例えば、Al及びFe)と共にSiも析出してしまう。一方、該pHが11.5以上では、十分に析出せずに液分中に残存する不純物(例えば、Al及びFe)の量が多くなる。
pHを上記数値範囲内に調整するための酸としては、硫酸、塩酸、シュウ酸等が用いられる。
pH調整後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
このうち、固形分(ケーキ)は、不純物(例えば、Al及びFe)を含むものである。
液分は、Siを含むものであり、次の工程(B)で処理される。
なお、本工程においてpH調整を行う際の液温は、エネルギーコストの観点から、5
〜100℃に保持されることが好ましく、10〜80℃に保持されることがより好ましく、10〜40℃に保持されることが特に好ましい。液温を上記範囲内とすることにより、処理効率を高めることができる。
【0013】
[工程(B);シリカ回収工程]
本工程は、液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得る工程である。
なお、沈降性シリカは、ケイ酸アルカリ水溶液と鉱酸との混合と同時に生成する。
本工程において用いられるケイ酸アルカリ水溶液は、特に限定されないが、具体的には前工程(工程(A)または工程(B1))で得られたケイ酸アルカリ水溶液、及び水ガラス等が挙げられる。
本発明で用いられる水ガラスは、市販のものを使用することができ、JIS規格により規定される1号、2号、3号の他に各水ガラスメーカーで製造販売されているJIS規格外の製品も使用することができる。
ケイ酸アルカリ水溶液中に含まれるSiの濃度は、10.0質量%以上、好ましくは
10.0〜20.0質量%、より好ましくは12.0〜18.0質量%、特に好ましくは13.0〜16.0質量%である。Si濃度が10.0質量%未満であると、シリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
Si濃度が20質量%を超えると、ケイ酸アルカリ水溶液のハンドリング(輸送等)が悪化するとともに、不純物の除去が不十分となる場合がある。
本工程において用いられる鉱酸は、例えば硫酸、塩酸、硝酸等が挙げられ、硫酸を用いることが薬剤コスト低減の理由で好ましい。
鉱酸の濃度は、10.0体積%以上、より好ましくは10.0〜20.0体積%、特に好ましくは10.0〜15.0体積%である。鉱酸の濃度が、10.0体積%未満の場合には、沈降性シリカが生成しない、あるいは沈降性シリカとゲル状シリカの両方が生成するおそれがある。このゲル状シリカが生成すると、最終シリカ生成物中の不純物濃度が高くなる。20.0体積%を超えるとコストの面から好ましくない。
ケイ酸アルカリ水溶液と鉱酸の混合方法は、特に限定されるものではないが、沈降性シリカのみを生成させる観点から、ケイ酸アルカリ水溶液を鉱酸に添加する方法が好ましい。具体的には、ケイ酸アルカリ水溶液を鉱酸に滴下する方法や、ケイ酸アルカリ水溶液を、1.0mmφ以上、好ましくは4.0mmφ以上のチューブ等から、鉱酸中に直接押し出す方法等が挙げられる。
また、混合する際のpHは好ましくは1.0以下、より好ましくは0.9以下に保つことが望ましい。pHが1.0を超えるとシリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
また、ケイ酸アルカリ水溶液の鉱酸中への流出速度は限定されないが、混合する際にpHが1.0を超え、かつ流出速度が大きい場合には、沈降性シリカが生成しない、あるいは沈降性シリカとゲル状シリカの両方が生成するおそれがある。
本工程において、ケイ酸アルカリ水溶液と鉱酸を混合する際の沈降性シリカの析出温度は、特に限定されるものではないが、好ましくは10〜80℃、より好ましくは15〜40℃、特に好ましくは20〜30℃であり、通常、常温(例えば10〜40℃)である。80℃を超えると、エネルギーコストが上昇するとともに、設備の腐食が生じ易くなる。
上記ケイ酸アルカリ水溶液中のSiを沈降性シリカとして析出させた後、フィルタープレス等の固液分離手段を用いて、SiO2を含む固形分と、不純物を含む液分に分離する。得られた沈降性シリカはゲル状ではなく、粒子状であるため、固液分離に要する時間を短くすることができる。
【0014】
本発明では、工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することで、不純物(特にTi)が低減された高純度シリカを得ることができる。
混合方法は特に限定されるものではなく、(1)ケイ酸アルカリ水溶液と過酸化水素を混合し、次いで得られた混合物と鉱酸を混合する方法、(2)鉱酸と過酸化水素を混合し、次いで得られた混合物とケイ酸アルカリ水溶液を混合する方法、(3)ケイ酸アルカリ水溶液と鉱酸を混合し、次いで得られた混合物と過酸化水素を混合する方法、(4)ケイ酸アルカリ水溶液と、鉱酸と、過酸化水素を同時に混合する方法が挙げられる。中でも、工程の上流側で不純物(特にTi)の低減を図るという観点から(1)が好ましい。
過酸化水素の添加量は、シリカ(SiO2)の質量(100質量%)に対して、好ましくは0.1〜15.0質量%、より好ましくは0.1〜10.0質量%、特に好ましくは0.1〜5.0質量%である。過酸化水素の添加量が0.1質量%未満では、不純物(例えばTi)の低減効果が十分ではなく、15.0質量%を超えると、不純物(例えばTi)の低減効果が飽和状態となる。
【0015】
工程(B)において用いられる鉱酸が硫酸である場合、工程(B)で得られた不純物を含む液分を中和処理することで、液分中の不純物を石膏として析出し、セメントの原料として再利用してもよい。
【0016】
[工程(C);酸洗浄工程]
工程(B)で得られたSiO2を含む固形分は、Al、Fe、Ti、B、P等の不純物が低減された高純度シリカである。
工程(B)で得られたSiO2を含む固形分に対して、適宜、工程(C)(酸洗浄工程)を行うことができる。酸洗浄工程を行うことにより、より高純度のシリカを得ることができる。
工程(C)は、工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物(例えば、Al、Fe)を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物(例えば、Al、Fe)を含む液分を得る工程である。
本工程における酸性スラリーのpHは、3.0未満、好ましくは2.0以下である。酸性スラリーのpHを上記範囲内に調整して酸洗浄を行うことにより、工程(B)で得られた固形分にわずかに残存するアルミニウム分、鉄分等の不純物を溶解して液分中へ移行させることができ、固形分中のシリカ含有率を上昇させることができるため、さらに高純度のシリカを得ることができる。
pHを上記数値範囲内に調整するための鉱酸としては、硫酸、塩酸、シュウ酸等が用いられる。
pH調整後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
なお、本工程においてpH調整を行う際の液温は、特に限定されるものではないが、エネルギーコストの観点から、好ましくは10〜80℃、より好ましくは15〜40℃、特に好ましくは20℃〜30℃であり、通常、常温(例えば10〜40℃)である。液温を上記範囲内とすることにより、処理効率を高めることができる。
また、酸洗浄工程後の液分を回収し、工程(B)に用いられる鉱酸、および工程(C)に用いられる鉱酸として再利用してもよい。
【0017】
本発明では、工程(B)における過酸化水素の使用に代えて、または、工程(B)における過酸化水素の使用とともに、工程(C)において、鉱酸と過酸化水素を混合することで、不純物(特にTi)が低減された高純度シリカを得ることができる。
混合方法は特に限定されるものではなく、(1)工程(B)で得られたSiO2を含む固形分と過酸化水素を混合し、次いで得られた混合物と鉱酸を混合する方法、(2)鉱酸と過酸化水素を混合し、次いで得られた混合物と工程(B)で得られたSiO2を含む固形分を混合する方法、(3)工程(B)で得られたSiO2を含む固形分と鉱酸を混合し、次いで得られた混合物と過酸化水素を混合する方法、(4)工程(B)で得られたSiO2を含む固形分と、鉱酸と、過酸化水素を同時に混合する方法が挙げられる。中でも、工程の上流側で不純物(特にTi)の低減を図るという観点から(1)が好ましい。
過酸化水素の添加量は、シリカ(SiO2)の質量(100質量%)に対して、好ましくは0.1〜15.0質量%、より好ましくは0.1〜10.0質量%、特に好ましくは0.1〜5.0質量%である。過酸化水素の添加量が0.1質量%未満では不純物(例えばTi)の低減効果が十分ではなく、15.0質量%を超えると、不純物(例えばTi)低減効果が飽和状態となる。
本発明においては、本明細書の段落0014、及び、段落0017に記載された方法に従い、工程(B)及び工程(C)の少なくともいずれか一方において過酸化水素を混合することで、本発明の効果を得ることができる。
【0018】
[工程(D);水洗浄工程]
本工程は、前工程(工程(B)または工程(C))で得られたSiO2を含む固形分に対して、適宜、水洗浄を行うことにより、より高純度のシリカを得る工程である。水洗浄を行うことにより、前工程で得られた固形分にわずかに残存するナトリウム、硫黄等の不純物を溶解して液分中へ移行させることができ、固形分中のシリカ含有率を上昇させることができるため、さらに高純度のシリカを得ることができる。
水洗浄後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
また、水洗浄工程後の液分を回収し、工程(A1)、工程(A)、工程(B)、工程(C)、及び工程(D)に用いられる水として再利用してもよい。
【0019】
さらに、工程(A)と工程(B)の間で、適宜、イオン交換処理及び/又は活性炭処理を行うことができる。
イオン交換処理及び/又は活性炭処理で回収される不純物は、ホウ素(B)、リン(P)、アルミニウム(Al)、鉄(Fe)、ナトリウム(Na)、チタン(Ti)、カルシウム(Ca)、カリウム(K)、マグネシウム(Mg)、及び有機物(C)からなる群より選ばれる一種以上である。
イオン交換処理は、キレート樹脂、イオン交換樹脂等のイオン交換媒体を用いて行なうことができる。
イオン交換媒体の種類は、除去対象元素に対する選択性を考慮して、適宜定めればよい。例えば、ホウ素を除去する場合、グルカミン基を有するキレート樹脂や、N−メチルグルカミン基を有するイオン交換樹脂等を用いることができる。
イオン交換媒体の形態は、特に限定されるものではなく、ビーズ状、繊維状、クロス状等が挙げられる。イオン交換媒体への液分の通液方法もなんら限定されるものではなく、例えばカラムにキレート樹脂またはイオン交換樹脂を充填して連続的に通液する方法などを用いることができる。
イオン交換処理及び/又は活性炭処理を行う際の液温は、各処理に用いる材料の耐用温度以下であれば、特に限定されない。
【0020】
本発明の製造方法によって最終的に得られたシリカを含む固形分は、適宜、乾燥処理及び/又は焼成処理を行うことができる。乾燥処理及び/又は焼成処理の条件は、例えば、100〜1000℃で1〜5時間である。
また、最終的に得られたシリカを含む固形分をアルカリ溶液(例えば水酸化ナトリウム)に溶解させ、工程(B)のケイ酸アルカリ水溶液として用い、工程(B)から工程(D)を複数回繰り返すことによって、より高純度のシリカを得ることができる。
【0021】
本発明の製造方法で得られるシリカは、シリカの含有率が高く、またアルミニウム(Al)、鉄(Fe)、チタン(Ti)、ホウ素(B)、リン(P)等の不純物の含有量が低いものである。
本発明の製造方法で得られる高純度シリカ中のSiO2の含有率は、好ましくは99.0質量%以上である。また、高純度シリカ中のNa、S、Al、Fe、Ca、B、P、Tiの含有率は、各々、好ましくは5.0ppm以下、5.0ppm以下、1.0ppm以下、1.0ppm以下、1.0ppm以下、0.1ppm以下、1.0ppm以下、1.0ppm以下である。
【実施例】
【0022】
以下、本発明を実施例により具体的に説明するが、本発明はこれら実施例に限定されるものではない。
[実施例1]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水4.7mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%(水165.6mlに濃硫酸20mlを混合したもの)の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
なお、表1中、「過酸化水素の添加量」は、SiO2の質量(100質量%)に対する過酸化水素水中の過酸化水素(H2O2)の量(質量%)を示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.1ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.7ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0023】
[実施例2]
35質量%の過酸化水素水の添加量を4.7mlから3.4mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:3.6ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.6ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0024】
[実施例3]
35質量%の過酸化水素水の添加量を4.7mlから2.1mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:3.9ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.8ppm、Ca:0.6ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0025】
[実施例4]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更する以外は実施例1と同様にして精製シリカ9.9gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0026】
[実施例5]
35質量%の過酸化水素水の添加量を4.7mlから0.2mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.5ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.5ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0027】
[実施例6]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
一方、水165.6mlに濃硫酸20mlを加えて混合し、次いで35質量%の過酸化水素水1.0mlを添加することによって、過酸化水素が添加された硫酸濃度10.7体積%の鉱酸を得た。
前記Si濃度10.0質量%の水ガラス溶液66.2gを前記鉱酸に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.9gと、不純物を含む液分246.3gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.9gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.7ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0028】
[実施例7]
水の量を165.6mlから166.1mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.5mlに変更する以外は実施例6と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.5ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.8ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0029】
[実施例8]
水の量を165.6mlから166.5mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.1mlに変更する以外は実施例6と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.4ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.7ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0030】
[実施例9]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
一方、水165.6mlに濃硫酸20mlを加えて混合し、次いで35質量%の過酸化水素水1.0mlを添加することによって硫酸濃度10.7体積%の鉱酸を得た。この鉱酸を常温(25℃)下で前記の固形分(沈降性シリカ)に対して、200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:0.5ppm、Fe:0.8ppm、Ca:0.5ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0031】
[実施例10]
水の量を165.6mlから166.1mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.5mlに変更する以外は実施例9と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.9ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0032】
[実施例11]
水の量を165.6mlから166.5mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.1mlに変更する以外は実施例9と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.8ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:1.0ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0033】
[実施例12]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更し、かつ、蒸留水を用いた水洗を行わない以外は実施例1と同様にして精製シリカ9.8gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:310ppm、S:425ppm、Al:0.9ppm、Fe:0.9ppm、Ca:1.0ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0034】
[実施例13]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水1.1mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%(水165.6mlに濃硫酸20mlを混合したもの)の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.5gと、不純物を含む液分246.7gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:3.9ppm、Fe:4.0ppm、Ca:1.1ppm、B:0.1ppm、P:1.2ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0035】
[実施例14]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水1.1mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:246ppm、S:308ppm、Al:9.5ppm、Fe:8.2ppm、Ca:2.6ppm、B:0.5ppm、P:1.3ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0036】
[実施例15]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)100gに含まれる水分を乾燥機にて蒸発させて、Si濃度16.4質量%に調製した水ガラス溶液80.5gを得た。次いで35質量%の過酸化水素水0.8mlを添加することによって、過酸化水素が添加されたSi濃度16.4質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)47gと、不純物を含む液分219gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ23.2gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.9質量%、Na:205ppm、S:354ppm、Al:1.8ppm、Fe:2.2ppm、Ca:1.3ppm、B:0.6ppm、P:1.2ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0037】
[実施例16]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更し、かつ、pHを滴下終了時まで2.0に保った以外は実施例1と同様にして精製シリカ9.8gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:62ppm、S:91ppm、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0038】
[実施例17]
珪質頁岩(成分組成;SiO2:80質量%、Al2O3:10質量%、Fe2O3:5質量%、B:150ppm、P:330ppm)を、ボールミルを用いて粉砕し、珪質頁岩粉末(最大粒径:0.5mm)を得た。
原料として使用した珪質頁岩について、Cu−Kα線による粉末X線の回折強度、オパールCTの半値幅を、粉末X線回折装置(株式会社リガク製、RINT2000)を用いて測定した。回折強度を図2に、半値幅を図3にそれぞれ示す。使用した珪質頁岩は、石英の2θ=26.6degのピーク頂部の回折強度に対するオパールCTの2θ=21.5〜21.9degのピーク頂部の回折強度の比率が、0.68であった。また、オパールCTの半値幅は、1.4°であった。
次いで、得られた珪質頁岩粉末250gと、2.5N水酸化ナトリウム水溶液1000gを混合して、70℃に加温した後に、60分間混合撹拌し、pHが13.5であるスラリーを得た。
このスラリーを減圧下でブフナー漏斗で固液分離し、Siの濃度が10.0質量%の液分700gを得た。
【0039】
得られた液分(ケイ酸アルカリ水溶液)に35質量%の過酸化水素水4.4mlを添加し、次いで、過酸化水素が添加されたケイ酸アルカリ水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、析出温度を20℃に保ちながら沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)14.6gと、不純物を含む液分251.6gを得た。なお、pHは滴下終了まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ7.3gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.2ppm、S:2.4ppm、Al:検出限界未満(0.5ppm未満)、Fe:0.4ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は49%であった。
【0040】
[比較例1]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.99質量%、Na:1.8ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0041】
【表1】

【0042】
実施例1〜17の結果から、本発明の製造方法により得られたシリカは、シリカの含有率が高いと共に、比較例1に比べて、不純物の一つであるチタンの含有率が少ない。また、他の不純物(Na、S、Al、Fe、Ca、B、P)の含有率も少ないことがわかる。
【技術分野】
【0001】
本発明は、高純度シリカの製造方法に関する。
【背景技術】
【0002】
高純度シリコンは、半導体デバイス、触媒担体等に用いられている。
高純度シリコンの製造方法として、例えば、金属シリコンから製造された高純度のシリコン塩化物(トリクロロシラン)を原料として用いる方法が提案されている(特許文献1)。
特許文献1に記載の方法によると、非常に高純度のシリコンを得ることができる。しかし、この方法は、工程が煩雑でかつ高コストであるという問題がある。このような事情下において、高純度のシリコンを、低コストかつ大量に製造することのできる技術が望まれている。
これを解決すべく、二酸化ケイ素を含有しかつ多孔質で微細構造を有する原料を精製して高純度シリカを製造し、次いで、この高純度シリカを原料としてシリコンを生成し、得られたシリコンにレーザを照射することなどによって、高純度シリコンを製造する方法が提案されている(特許文献2)。
【先行技術文献】
【特許文献】
【0003】
【特許文献1】特開2006−001804号公報
【特許文献2】特開2006−188367号公報
【発明の概要】
【発明が解決しようとする課題】
【0004】
特許文献2に記載の方法によると、従来技術に比して、低コストでかつ簡易に、高純度のシリコンを得ることができる。シリコンの原料となる高純度シリカを、より低コストでかつ簡易に得ることができれば、好都合である。
そこで、本発明は、高純度シリカを、簡易にかつ低コストで製造することのできる方法を提供することを目的とする。
【課題を解決するための手段】
【0005】
本発明者は、上記課題を解決するために鋭意検討した結果、ケイ酸アルカリ水溶液と鉱酸を混合して、非ゲル状の沈降性シリカとして析出するとともに、製造工程において原料と過酸化水素を混合することによって、前記の目的を達成することができることを見出し、本発明を完成した。
【0006】
すなわち、本発明は、以下の[1]〜[12]を提供するものである。
[1](B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
[2](C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含む前記[1]に記載の高純度シリカの製造方法。
[3](B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程と、(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含み、前記工程(C)において、鉱酸と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
[4]工程(B)において、ケイ酸アルカリ水溶液と鉱酸の混合が、ケイ酸アルカリ水溶液を鉱酸に添加することによって行われる、前記[1]〜[3]のいずれかに記載の高純度シリカの製造方法。
[5]工程(B)において、ケイ酸アルカリ水溶液と鉱酸を、pH1.0以下に保ちながら混合する、前記[1]〜[4]のいずれかに記載の高純度シリカの製造方法。
[6]工程(B)において、ケイ酸アルカリ水溶液のSi濃度が10.0〜20.0質量%である、前記[1]〜[5]のいずれかに記載の高純度シリカの製造方法。
[7]過酸化水素の添加量が、シリカ(SiO2)100質量%に対して、0.1〜15.0質量%である前記[1]〜[6]のいずれかに記載の高純度シリカの製造方法。
[8]工程(B)の前に、(A)シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程を含む、前記[1]〜[7]のいずれかに記載の高純度シリカの製造方法。
[9]工程(A)と工程(B)の間に、(B1)工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中の不純物を析出させた後、固液分離を行い、ケイ酸アルカリ水溶液と、固形分を得る不純物回収工程、を含む、前記[8]に記載の高純度シリカの製造方法。
[10]工程(A)の前に、(A1)シリカ含有鉱物を水洗して、粘土分及び有機物を除去する原料水洗工程、を含む前記[8]または[9]に記載の高純度シリカの製造方法。
[11]工程(A)の前に、(A2)シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成して、有機物を除去する原料焼成工程、を含む前記[8]〜[10]のいずれかに記載の高純度シリカの製造方法。
[12](D)前工程で得られたSiO2を含む固形分と水を混合して、上記固形分中に残存する不純物を溶解させた後、上記スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る水洗浄工程、を含む前記[1]〜[11]のいずれかに記載の高純度シリカの製造方法。
【発明の効果】
【0007】
本発明の高純度シリカの製造方法によると、操作が簡易であり、処理効率が高いことなどに起因して、従来技術に比して低い製造コストで高純度シリカを得ることができる。
さらに、本発明の製造方法により得られる高純度シリカは、シリカの含有率が高く、またアルミニウム(Al)、鉄(Fe)、チタン(Ti)、ホウ素(B)、リン(P)、有機物(C)などの不純物、特にチタン(Ti)の含有率が低いという特長がある。
【図面の簡単な説明】
【0008】
【図1】本発明の高純度シリカの製造方法の実施形態の一例を示すフロー図である。
【図2】珪質頁岩の一例についてのCu−Kα線による粉末X線の回折強度を示すグラフである。
【図3】珪質頁岩の一例についてのオパールCTの半値幅を示すグラフである。
【発明を実施するための形態】
【0009】
以下、本発明の高純度シリカの製造方法を詳しく説明する。
なお、以下の工程(A1)〜工程(D)中、工程(B)は、本発明において必須の工程であるが、工程(A)は、シリカ含有鉱物を原料としてケイ酸アルカリ水溶液を調製する場合に追加される工程であり、工程(A1)、(A2)、(B1)、(C)及び(D)は、本発明において必須ではなく、任意で追加可能な工程である。
[工程(A1);原料水洗工程]
工程(A1)は、シリカ含有鉱物(岩石状又は粉末状)を水洗して、粘土分及び有機物を除去する工程である。水洗後のシリカ含有鉱物は、通常、フィルタープレス等を用いて、さらに脱水させる。
シリカ含有鉱物としては、珪藻土、珪質頁岩等が挙げられる。シリカ含有鉱物は、アルカリに対する溶解性が高いことが望ましい。
ここで、珪藻土とは、珪藻が海底や湖底に沈積し、長い年月の間に体内の原形質その他の有機物が分解し、非晶質シリカを主体とした珪藻殻が集積して堆積したものである。
珪質頁岩とは、珪質の生物遺骸等に由来する頁岩である。すなわち、海域には、珪質の殻を有する珪藻などのプランクトンが生息するが、このプランクトンの死骸が海底中に堆積すると、死骸中の有機物の部分は徐々に分解され、珪質(SiO2;シリカ)の殻のみが残る。この珪質の殻(珪質堆積物)が、時間の経過や温度・圧力の変化などに伴い、続成作用により変質して、硬岩化することにより珪質頁岩となる。なお、珪質堆積物中のシリカは、続成作用によって、非晶質シリカから、結晶化してクリストバライト、トリデイマイトへ、さらに石英へと変化する。
【0010】
珪藻土は、主に非晶質シリカであるオパールAからなる。珪質頁岩は、オパールAより結晶化が進んだオパールCTまたはオパールCを主に含む。オパールCTとは、クリストバライト構造とトリディマイト構造からなるシリカ鉱物である。オパールCとは、クリストバライト構造からなるシリカ鉱物である。このうち、本発明では、オパールCTを主とする珪質頁岩が好ましく用いられる。
さらに、Cu−Kα線による粉末X線回折において、石英の2θ=26.6degのピーク頂部の回折強度に対するオパールCTの2θ=21.5〜21.9degの回折強度は、石英を1とした場合の比率で0.2〜2.0の範囲が好ましく、0.4〜1.8の範囲がより好ましく、0.5〜1.5の範囲が特に好ましい。該値が0.2に満たない場合には、反応性に富むオパールCTの量が少ないため、シリカの収量が低下する。一方、該値が2.0を超える場合には、オパールCTの量が石英よりはるかに多くなり、このような珪質頁岩は資源的に少なく、経済性に劣る。
なお、石英に対するオパールCTの回折強度の比率は、以下の式で求める。
石英に対するオパールCTの回折強度の比率=(21.5〜21.9degのピーク頂部の回折強度)/(26.6degのピーク頂部の回折強度)
また、珪質頁岩のCu−Kα線による粉末X線回折において、オパールCTの2θ=21.5〜21.9degの間に存在するピークの半値幅は0.5°以上が好ましく、0.75°以上がより好ましく、1.0°以上がさらに好ましい。該値が0.5°未満では、オパールCTの結晶の結合力が増大し、アルカリとの反応性が低下して、シリカの収量が減少する。ここで、半値幅とは、ピーク頂部の回折強度の1/2に位置する回折線の幅をいう。
本発明で用いる珪質頁岩は、シリカ含有率が70質量%以上であることが好ましく、75質量%以上であることがより好ましい。このような珪質頁岩を用いることにより、より高純度のシリカを低コストで製造することができる。
シリカ含有鉱物は、例えば、珪質頁岩等のシリカ含有鉱物を粉砕装置(例えば、ジョークラッシャー、トップグラインダーミル、クロスビーターミル、ボールミル等)で粉砕することによって得ることができる。
[工程(A2);原料焼成工程]
工程(A2)は、シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成し、有機物を除去する工程である。
なお、工程(A1)と工程(A2)の双方を実施する場合、その順序は特に限定されないが、有機物の除去効率の観点から工程(A1)を先に行うことが好ましい。
【0011】
[工程(A);アルカリ溶解工程]
工程(A)は、シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程である。
ここで、ケイ酸アルカリ水溶液とは、化学式中にケイ酸(SiO2)を含む物質を含有するアルカリ性の水溶液をいう。
シリカ含有鉱物とアルカリ水溶液を混合してなるアルカリ性スラリーのpHは、11.5以上、好ましくは12.5以上、より好ましくは13.0以上となるように調整される。該pHが11.5未満であると、シリカを十分に溶解させることができず、シリカが固形分中に残存してしまうため、得られるシリカの収量が減少する。
pHを上記数値範囲内に調整するためのアルカリ水溶液としては、水酸化ナトリウム水溶液、水酸化カリウム水溶液等が用いられる。
スラリーの固液比(アルカリ水溶液1リットルに対するシリカ含有鉱物の質量)は、好ましくは100〜500g/リットル、より好ましくは200〜400g/リットルである。該固液比が100g/リットル未満では、スラリーの固液分離に要する時間が増大するなど、処理効率が低下する。該固液比が400g/リットルを超えると、シリカ等を十分に溶出させることができないことがある。
スラリーは、通常、所定時間(例えば、30〜90分間)攪拌される。
攪拌後のスラリーは、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離される。液分は、Si及び他の成分(Al、Fe等の不純物)を含むケイ酸アルカリ水溶液であり、次の工程(B1)または工程(B)で処理される。液分中に含まれるSiの濃度は、10.0質量%以上、好ましくは10.0〜20.0質量%、より好ましくは12.0〜18.0質量%、特に好ましくは13.0〜16.0質量%である。Si濃度が10.0質量%未満であると、後述する工程(B)においてシリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
なお、本工程においてアルカリ性スラリーを得る際の液温は、エネルギーコストの観点から、5〜100℃に保持されることが好ましく、10〜80℃に保持されることがより好ましく、10〜40℃に保持されることが特に好ましい。液温を上記範囲内とすることにより、処理効率を高めることができる。
【0012】
[工程(B1);不純物回収工程]
本工程は、工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中のSi以外の不純物(例えば、Al及びFe)を析出させた後、固液分離を行い、Siを含むケイ酸アルカリ水溶液と、固形分を得る工程である。
なお、本工程で回収されずに液分中に残存する不純物は、工程(B)以降の工程で回収される。
本工程において、酸との混合後の液分のpHは、10.3を超え、11.5未満、好ましくは10.4以上、11.0以下、特に好ましくは10.5以上、10.8以下である。該pHが10.3以下であると、不純物(例えば、Al及びFe)と共にSiも析出してしまう。一方、該pHが11.5以上では、十分に析出せずに液分中に残存する不純物(例えば、Al及びFe)の量が多くなる。
pHを上記数値範囲内に調整するための酸としては、硫酸、塩酸、シュウ酸等が用いられる。
pH調整後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
このうち、固形分(ケーキ)は、不純物(例えば、Al及びFe)を含むものである。
液分は、Siを含むものであり、次の工程(B)で処理される。
なお、本工程においてpH調整を行う際の液温は、エネルギーコストの観点から、5
〜100℃に保持されることが好ましく、10〜80℃に保持されることがより好ましく、10〜40℃に保持されることが特に好ましい。液温を上記範囲内とすることにより、処理効率を高めることができる。
【0013】
[工程(B);シリカ回収工程]
本工程は、液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得る工程である。
なお、沈降性シリカは、ケイ酸アルカリ水溶液と鉱酸との混合と同時に生成する。
本工程において用いられるケイ酸アルカリ水溶液は、特に限定されないが、具体的には前工程(工程(A)または工程(B1))で得られたケイ酸アルカリ水溶液、及び水ガラス等が挙げられる。
本発明で用いられる水ガラスは、市販のものを使用することができ、JIS規格により規定される1号、2号、3号の他に各水ガラスメーカーで製造販売されているJIS規格外の製品も使用することができる。
ケイ酸アルカリ水溶液中に含まれるSiの濃度は、10.0質量%以上、好ましくは
10.0〜20.0質量%、より好ましくは12.0〜18.0質量%、特に好ましくは13.0〜16.0質量%である。Si濃度が10.0質量%未満であると、シリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
Si濃度が20質量%を超えると、ケイ酸アルカリ水溶液のハンドリング(輸送等)が悪化するとともに、不純物の除去が不十分となる場合がある。
本工程において用いられる鉱酸は、例えば硫酸、塩酸、硝酸等が挙げられ、硫酸を用いることが薬剤コスト低減の理由で好ましい。
鉱酸の濃度は、10.0体積%以上、より好ましくは10.0〜20.0体積%、特に好ましくは10.0〜15.0体積%である。鉱酸の濃度が、10.0体積%未満の場合には、沈降性シリカが生成しない、あるいは沈降性シリカとゲル状シリカの両方が生成するおそれがある。このゲル状シリカが生成すると、最終シリカ生成物中の不純物濃度が高くなる。20.0体積%を超えるとコストの面から好ましくない。
ケイ酸アルカリ水溶液と鉱酸の混合方法は、特に限定されるものではないが、沈降性シリカのみを生成させる観点から、ケイ酸アルカリ水溶液を鉱酸に添加する方法が好ましい。具体的には、ケイ酸アルカリ水溶液を鉱酸に滴下する方法や、ケイ酸アルカリ水溶液を、1.0mmφ以上、好ましくは4.0mmφ以上のチューブ等から、鉱酸中に直接押し出す方法等が挙げられる。
また、混合する際のpHは好ましくは1.0以下、より好ましくは0.9以下に保つことが望ましい。pHが1.0を超えるとシリカがゲル状で析出する場合があり、固液分離に時間がかかるとともに、得られるシリカの量が低下する。
また、ケイ酸アルカリ水溶液の鉱酸中への流出速度は限定されないが、混合する際にpHが1.0を超え、かつ流出速度が大きい場合には、沈降性シリカが生成しない、あるいは沈降性シリカとゲル状シリカの両方が生成するおそれがある。
本工程において、ケイ酸アルカリ水溶液と鉱酸を混合する際の沈降性シリカの析出温度は、特に限定されるものではないが、好ましくは10〜80℃、より好ましくは15〜40℃、特に好ましくは20〜30℃であり、通常、常温(例えば10〜40℃)である。80℃を超えると、エネルギーコストが上昇するとともに、設備の腐食が生じ易くなる。
上記ケイ酸アルカリ水溶液中のSiを沈降性シリカとして析出させた後、フィルタープレス等の固液分離手段を用いて、SiO2を含む固形分と、不純物を含む液分に分離する。得られた沈降性シリカはゲル状ではなく、粒子状であるため、固液分離に要する時間を短くすることができる。
【0014】
本発明では、工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することで、不純物(特にTi)が低減された高純度シリカを得ることができる。
混合方法は特に限定されるものではなく、(1)ケイ酸アルカリ水溶液と過酸化水素を混合し、次いで得られた混合物と鉱酸を混合する方法、(2)鉱酸と過酸化水素を混合し、次いで得られた混合物とケイ酸アルカリ水溶液を混合する方法、(3)ケイ酸アルカリ水溶液と鉱酸を混合し、次いで得られた混合物と過酸化水素を混合する方法、(4)ケイ酸アルカリ水溶液と、鉱酸と、過酸化水素を同時に混合する方法が挙げられる。中でも、工程の上流側で不純物(特にTi)の低減を図るという観点から(1)が好ましい。
過酸化水素の添加量は、シリカ(SiO2)の質量(100質量%)に対して、好ましくは0.1〜15.0質量%、より好ましくは0.1〜10.0質量%、特に好ましくは0.1〜5.0質量%である。過酸化水素の添加量が0.1質量%未満では、不純物(例えばTi)の低減効果が十分ではなく、15.0質量%を超えると、不純物(例えばTi)の低減効果が飽和状態となる。
【0015】
工程(B)において用いられる鉱酸が硫酸である場合、工程(B)で得られた不純物を含む液分を中和処理することで、液分中の不純物を石膏として析出し、セメントの原料として再利用してもよい。
【0016】
[工程(C);酸洗浄工程]
工程(B)で得られたSiO2を含む固形分は、Al、Fe、Ti、B、P等の不純物が低減された高純度シリカである。
工程(B)で得られたSiO2を含む固形分に対して、適宜、工程(C)(酸洗浄工程)を行うことができる。酸洗浄工程を行うことにより、より高純度のシリカを得ることができる。
工程(C)は、工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物(例えば、Al、Fe)を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物(例えば、Al、Fe)を含む液分を得る工程である。
本工程における酸性スラリーのpHは、3.0未満、好ましくは2.0以下である。酸性スラリーのpHを上記範囲内に調整して酸洗浄を行うことにより、工程(B)で得られた固形分にわずかに残存するアルミニウム分、鉄分等の不純物を溶解して液分中へ移行させることができ、固形分中のシリカ含有率を上昇させることができるため、さらに高純度のシリカを得ることができる。
pHを上記数値範囲内に調整するための鉱酸としては、硫酸、塩酸、シュウ酸等が用いられる。
pH調整後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
なお、本工程においてpH調整を行う際の液温は、特に限定されるものではないが、エネルギーコストの観点から、好ましくは10〜80℃、より好ましくは15〜40℃、特に好ましくは20℃〜30℃であり、通常、常温(例えば10〜40℃)である。液温を上記範囲内とすることにより、処理効率を高めることができる。
また、酸洗浄工程後の液分を回収し、工程(B)に用いられる鉱酸、および工程(C)に用いられる鉱酸として再利用してもよい。
【0017】
本発明では、工程(B)における過酸化水素の使用に代えて、または、工程(B)における過酸化水素の使用とともに、工程(C)において、鉱酸と過酸化水素を混合することで、不純物(特にTi)が低減された高純度シリカを得ることができる。
混合方法は特に限定されるものではなく、(1)工程(B)で得られたSiO2を含む固形分と過酸化水素を混合し、次いで得られた混合物と鉱酸を混合する方法、(2)鉱酸と過酸化水素を混合し、次いで得られた混合物と工程(B)で得られたSiO2を含む固形分を混合する方法、(3)工程(B)で得られたSiO2を含む固形分と鉱酸を混合し、次いで得られた混合物と過酸化水素を混合する方法、(4)工程(B)で得られたSiO2を含む固形分と、鉱酸と、過酸化水素を同時に混合する方法が挙げられる。中でも、工程の上流側で不純物(特にTi)の低減を図るという観点から(1)が好ましい。
過酸化水素の添加量は、シリカ(SiO2)の質量(100質量%)に対して、好ましくは0.1〜15.0質量%、より好ましくは0.1〜10.0質量%、特に好ましくは0.1〜5.0質量%である。過酸化水素の添加量が0.1質量%未満では不純物(例えばTi)の低減効果が十分ではなく、15.0質量%を超えると、不純物(例えばTi)低減効果が飽和状態となる。
本発明においては、本明細書の段落0014、及び、段落0017に記載された方法に従い、工程(B)及び工程(C)の少なくともいずれか一方において過酸化水素を混合することで、本発明の効果を得ることができる。
【0018】
[工程(D);水洗浄工程]
本工程は、前工程(工程(B)または工程(C))で得られたSiO2を含む固形分に対して、適宜、水洗浄を行うことにより、より高純度のシリカを得る工程である。水洗浄を行うことにより、前工程で得られた固形分にわずかに残存するナトリウム、硫黄等の不純物を溶解して液分中へ移行させることができ、固形分中のシリカ含有率を上昇させることができるため、さらに高純度のシリカを得ることができる。
水洗浄後、フィルタープレス等の固液分離手段を用いて、固形分と液分に分離する。
また、水洗浄工程後の液分を回収し、工程(A1)、工程(A)、工程(B)、工程(C)、及び工程(D)に用いられる水として再利用してもよい。
【0019】
さらに、工程(A)と工程(B)の間で、適宜、イオン交換処理及び/又は活性炭処理を行うことができる。
イオン交換処理及び/又は活性炭処理で回収される不純物は、ホウ素(B)、リン(P)、アルミニウム(Al)、鉄(Fe)、ナトリウム(Na)、チタン(Ti)、カルシウム(Ca)、カリウム(K)、マグネシウム(Mg)、及び有機物(C)からなる群より選ばれる一種以上である。
イオン交換処理は、キレート樹脂、イオン交換樹脂等のイオン交換媒体を用いて行なうことができる。
イオン交換媒体の種類は、除去対象元素に対する選択性を考慮して、適宜定めればよい。例えば、ホウ素を除去する場合、グルカミン基を有するキレート樹脂や、N−メチルグルカミン基を有するイオン交換樹脂等を用いることができる。
イオン交換媒体の形態は、特に限定されるものではなく、ビーズ状、繊維状、クロス状等が挙げられる。イオン交換媒体への液分の通液方法もなんら限定されるものではなく、例えばカラムにキレート樹脂またはイオン交換樹脂を充填して連続的に通液する方法などを用いることができる。
イオン交換処理及び/又は活性炭処理を行う際の液温は、各処理に用いる材料の耐用温度以下であれば、特に限定されない。
【0020】
本発明の製造方法によって最終的に得られたシリカを含む固形分は、適宜、乾燥処理及び/又は焼成処理を行うことができる。乾燥処理及び/又は焼成処理の条件は、例えば、100〜1000℃で1〜5時間である。
また、最終的に得られたシリカを含む固形分をアルカリ溶液(例えば水酸化ナトリウム)に溶解させ、工程(B)のケイ酸アルカリ水溶液として用い、工程(B)から工程(D)を複数回繰り返すことによって、より高純度のシリカを得ることができる。
【0021】
本発明の製造方法で得られるシリカは、シリカの含有率が高く、またアルミニウム(Al)、鉄(Fe)、チタン(Ti)、ホウ素(B)、リン(P)等の不純物の含有量が低いものである。
本発明の製造方法で得られる高純度シリカ中のSiO2の含有率は、好ましくは99.0質量%以上である。また、高純度シリカ中のNa、S、Al、Fe、Ca、B、P、Tiの含有率は、各々、好ましくは5.0ppm以下、5.0ppm以下、1.0ppm以下、1.0ppm以下、1.0ppm以下、0.1ppm以下、1.0ppm以下、1.0ppm以下である。
【実施例】
【0022】
以下、本発明を実施例により具体的に説明するが、本発明はこれら実施例に限定されるものではない。
[実施例1]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水4.7mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%(水165.6mlに濃硫酸20mlを混合したもの)の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
なお、表1中、「過酸化水素の添加量」は、SiO2の質量(100質量%)に対する過酸化水素水中の過酸化水素(H2O2)の量(質量%)を示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.1ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.7ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0023】
[実施例2]
35質量%の過酸化水素水の添加量を4.7mlから3.4mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:3.6ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.6ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0024】
[実施例3]
35質量%の過酸化水素水の添加量を4.7mlから2.1mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:3.9ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.8ppm、Ca:0.6ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0025】
[実施例4]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更する以外は実施例1と同様にして精製シリカ9.9gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0026】
[実施例5]
35質量%の過酸化水素水の添加量を4.7mlから0.2mlに変更する以外は実施例1と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.5ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.5ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0027】
[実施例6]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
一方、水165.6mlに濃硫酸20mlを加えて混合し、次いで35質量%の過酸化水素水1.0mlを添加することによって、過酸化水素が添加された硫酸濃度10.7体積%の鉱酸を得た。
前記Si濃度10.0質量%の水ガラス溶液66.2gを前記鉱酸に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.9gと、不純物を含む液分246.3gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.9gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.7ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0028】
[実施例7]
水の量を165.6mlから166.1mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.5mlに変更する以外は実施例6と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.5ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.8ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0029】
[実施例8]
水の量を165.6mlから166.5mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.1mlに変更する以外は実施例6と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.4ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.7ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0030】
[実施例9]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
一方、水165.6mlに濃硫酸20mlを加えて混合し、次いで35質量%の過酸化水素水1.0mlを添加することによって硫酸濃度10.7体積%の鉱酸を得た。この鉱酸を常温(25℃)下で前記の固形分(沈降性シリカ)に対して、200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:0.5ppm、Fe:0.8ppm、Ca:0.5ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0031】
[実施例10]
水の量を165.6mlから166.1mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.5mlに変更する以外は実施例9と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.9ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0032】
[実施例11]
水の量を165.6mlから166.5mlに変更し、かつ、35質量%の過酸化水素水の添加量を1.0mlから0.1mlに変更する以外は実施例9と同様にして精製シリカ10.0gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.8ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:1.0ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は67%であった。
【0033】
[実施例12]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更し、かつ、蒸留水を用いた水洗を行わない以外は実施例1と同様にして精製シリカ9.8gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:310ppm、S:425ppm、Al:0.9ppm、Fe:0.9ppm、Ca:1.0ppm、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0034】
[実施例13]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水1.1mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%(水165.6mlに濃硫酸20mlを混合したもの)の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.5gと、不純物を含む液分246.7gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:2.0ppm、S:検出限界未満(3.3ppm未満)、Al:3.9ppm、Fe:4.0ppm、Ca:1.1ppm、B:0.1ppm、P:1.2ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0035】
[実施例14]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに、水35gを加えて混合し、次いで35質量%の過酸化水素水1.1mlを添加することによって、過酸化水素が添加されたSi濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:246ppm、S:308ppm、Al:9.5ppm、Fe:8.2ppm、Ca:2.6ppm、B:0.5ppm、P:1.3ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0036】
[実施例15]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)100gに含まれる水分を乾燥機にて蒸発させて、Si濃度16.4質量%に調製した水ガラス溶液80.5gを得た。次いで35質量%の過酸化水素水0.8mlを添加することによって、過酸化水素が添加されたSi濃度16.4質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)47gと、不純物を含む液分219gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ23.2gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.9質量%、Na:205ppm、S:354ppm、Al:1.8ppm、Fe:2.2ppm、Ca:1.3ppm、B:0.6ppm、P:1.2ppmの成分組成を有していた。また、Siの回収率は65%であった。
【0037】
[実施例16]
35質量%の過酸化水素水の添加量を4.7mlから1.1mlに変更し、かつ、pHを滴下終了時まで2.0に保った以外は実施例1と同様にして精製シリカ9.8gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:62ppm、S:91ppm、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は66%であった。
【0038】
[実施例17]
珪質頁岩(成分組成;SiO2:80質量%、Al2O3:10質量%、Fe2O3:5質量%、B:150ppm、P:330ppm)を、ボールミルを用いて粉砕し、珪質頁岩粉末(最大粒径:0.5mm)を得た。
原料として使用した珪質頁岩について、Cu−Kα線による粉末X線の回折強度、オパールCTの半値幅を、粉末X線回折装置(株式会社リガク製、RINT2000)を用いて測定した。回折強度を図2に、半値幅を図3にそれぞれ示す。使用した珪質頁岩は、石英の2θ=26.6degのピーク頂部の回折強度に対するオパールCTの2θ=21.5〜21.9degのピーク頂部の回折強度の比率が、0.68であった。また、オパールCTの半値幅は、1.4°であった。
次いで、得られた珪質頁岩粉末250gと、2.5N水酸化ナトリウム水溶液1000gを混合して、70℃に加温した後に、60分間混合撹拌し、pHが13.5であるスラリーを得た。
このスラリーを減圧下でブフナー漏斗で固液分離し、Siの濃度が10.0質量%の液分700gを得た。
【0039】
得られた液分(ケイ酸アルカリ水溶液)に35質量%の過酸化水素水4.4mlを添加し、次いで、過酸化水素が添加されたケイ酸アルカリ水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、析出温度を20℃に保ちながら沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)14.6gと、不純物を含む液分251.6gを得た。なお、pHは滴下終了まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ7.3gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.999質量%、Na:1.2ppm、S:2.4ppm、Al:検出限界未満(0.5ppm未満)、Fe:0.4ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は49%であった。
【0040】
[比較例1]
水ガラス溶液(富士化学(株)製:SiO2/Na2O(モル比)=3.20)140gに水35gを加えて、Si濃度10.0質量%の水ガラス溶液を得た。
得られた水ガラス水溶液66.2gを硫酸濃度10.7体積%の硫酸200g中に滴下し、常温(25℃)下で沈降性シリカを析出させた後、減圧下でブフナー漏斗を用いて固液分離し、SiO2を含む固形分(沈降性シリカ)19.4gと、不純物を含む液分246.8gを得た。なお、pHは滴下終了時まで1.0以下に保った。
得られたSiO2を含む固形分(沈降性シリカ)に対して、常温(25℃)下で硫酸濃度10.7体積%の硫酸を200g添加してpHが3.0未満のスラリーとした。このスラリーを固液分離した後に、得られた固形分を、蒸留水を用いて水洗した。その後、105℃で1日乾燥させ、精製シリカ9.7gを得た。
得られた精製シリカ中のチタン(Ti)の濃度を測定した。その結果を表1に示す。
得られた精製シリカは、乾燥後に、SiO2:99.99質量%、Na:1.8ppm、S:検出限界未満(3.3ppm未満)、Al:検出限界未満(0.5ppm未満)、Fe:0.9ppm、Ca:検出限界未満(0.5ppm未満)、B:検出限界未満(0.05ppm未満)、P:検出限界未満(1.0ppm未満)の成分組成を有していた。また、Siの回収率は65%であった。
【0041】
【表1】

【0042】
実施例1〜17の結果から、本発明の製造方法により得られたシリカは、シリカの含有率が高いと共に、比較例1に比べて、不純物の一つであるチタンの含有率が少ない。また、他の不純物(Na、S、Al、Fe、Ca、B、P)の含有率も少ないことがわかる。
【特許請求の範囲】
【請求項1】
(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、
前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【請求項2】
(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含む請求項1に記載の高純度シリカの製造方法。
【請求項3】
(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程と、
(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含み、
前記工程(C)において、鉱酸と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【請求項4】
工程(B)において、ケイ酸アルカリ水溶液と鉱酸の混合が、ケイ酸アルカリ水溶液を鉱酸に添加することによって行われる、請求項1〜3のいずれか1項に記載の高純度シリカの製造方法。
【請求項5】
工程(B)において、ケイ酸アルカリ水溶液と鉱酸を、pH1.0以下に保ちながら混合する、請求項1〜4のいずれか1項に記載の高純度シリカの製造方法。
【請求項6】
工程(B)において、ケイ酸アルカリ水溶液のSi濃度が10.0〜20.0質量%である、請求項1〜5のいずれか1項に記載の高純度シリカの製造方法。
【請求項7】
過酸化水素の添加量が、シリカ(SiO2)100質量%に対して、0.1〜15.0質量%である請求項1〜6のいずれか1項に記載の高純度シリカの製造方法。
【請求項8】
工程(B)の前に、(A)シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程を含む、請求項1〜7のいずれか1項に記載の高純度シリカの製造方法。
【請求項9】
工程(A)と工程(B)の間に、(B1)工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中の不純物を析出させた後、固液分離を行い、ケイ酸アルカリ水溶液と、固形分を得る不純物回収工程、を含む、請求項8に記載の高純度シリカの製造方法。
【請求項10】
工程(A)の前に、(A1)シリカ含有鉱物を水洗して、粘土分及び有機物を除去する原料水洗工程、を含む請求項8または9に記載の高純度シリカの製造方法。
【請求項11】
工程(A)の前に、(A2)シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成して、有機物を除去する原料焼成工程、を含む請求項8〜10のいずれか1項に記載の高純度シリカの製造方法。
【請求項12】
(D)前工程で得られたSiO2を含む固形分と水を混合して、上記固形分中に残存する不純物を溶解させた後、上記スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る水洗浄工程、
を含む請求項1〜11のいずれか1項に記載の高純度シリカの製造方法。
【請求項1】
(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程、を含み、
前記工程(B)において、ケイ酸アルカリ水溶液、及び鉱酸の少なくともいずれか一方と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【請求項2】
(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含む請求項1に記載の高純度シリカの製造方法。
【請求項3】
(B)液分中のSi濃度が10.0質量%以上のケイ酸アルカリ水溶液と10.0体積%以上の濃度の鉱酸を混合して、液分中のSiを非ゲル状の沈降性シリカとして析出させた後、固液分離を行い、SiO2を含む固形分と、不純物を含む液分を得るシリカ回収工程と、
(C)工程(B)で得られたSiO2を含む固形分と鉱酸を混合して、pHが3.0未満の酸性スラリーを調製し、上記固形分中に残存する不純物を溶解させた後、上記酸性スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る酸洗浄工程、を含み、
前記工程(C)において、鉱酸と過酸化水素を混合することを特徴とする高純度シリカの製造方法。
【請求項4】
工程(B)において、ケイ酸アルカリ水溶液と鉱酸の混合が、ケイ酸アルカリ水溶液を鉱酸に添加することによって行われる、請求項1〜3のいずれか1項に記載の高純度シリカの製造方法。
【請求項5】
工程(B)において、ケイ酸アルカリ水溶液と鉱酸を、pH1.0以下に保ちながら混合する、請求項1〜4のいずれか1項に記載の高純度シリカの製造方法。
【請求項6】
工程(B)において、ケイ酸アルカリ水溶液のSi濃度が10.0〜20.0質量%である、請求項1〜5のいずれか1項に記載の高純度シリカの製造方法。
【請求項7】
過酸化水素の添加量が、シリカ(SiO2)100質量%に対して、0.1〜15.0質量%である請求項1〜6のいずれか1項に記載の高純度シリカの製造方法。
【請求項8】
工程(B)の前に、(A)シリカ含有鉱物とアルカリ水溶液を混合して、pHが11.5以上のアルカリ性スラリーを調製し、液分中のSi濃度が10.0質量%以上となるように、上記シリカ含有鉱物中のSiを液分中に溶解させた後、上記アルカリ性スラリーを固液分離して、Siを含むケイ酸アルカリ水溶液と、固形分を得るアルカリ溶解工程を含む、請求項1〜7のいずれか1項に記載の高純度シリカの製造方法。
【請求項9】
工程(A)と工程(B)の間に、(B1)工程(A)で得られたケイ酸アルカリ水溶液と酸を混合して、pHを10.3を超え、11.5未満に調整し、液分中の不純物を析出させた後、固液分離を行い、ケイ酸アルカリ水溶液と、固形分を得る不純物回収工程、を含む、請求項8に記載の高純度シリカの製造方法。
【請求項10】
工程(A)の前に、(A1)シリカ含有鉱物を水洗して、粘土分及び有機物を除去する原料水洗工程、を含む請求項8または9に記載の高純度シリカの製造方法。
【請求項11】
工程(A)の前に、(A2)シリカ含有鉱物を300〜1000℃で0.5〜2時間焼成して、有機物を除去する原料焼成工程、を含む請求項8〜10のいずれか1項に記載の高純度シリカの製造方法。
【請求項12】
(D)前工程で得られたSiO2を含む固形分と水を混合して、上記固形分中に残存する不純物を溶解させた後、上記スラリーを固液分離して、SiO2を含む固形分と、不純物を含む液分を得る水洗浄工程、
を含む請求項1〜11のいずれか1項に記載の高純度シリカの製造方法。
【図1】


【図2】


【図3】




【図2】


【図3】


【公開番号】特開2012−158486(P2012−158486A)
【公開日】平成24年8月23日(2012.8.23)
【国際特許分類】
【出願番号】特願2011−18223(P2011−18223)
【出願日】平成23年1月31日(2011.1.31)
【出願人】(000000240)太平洋セメント株式会社 (1,449)
【Fターム(参考)】
【公開日】平成24年8月23日(2012.8.23)
【国際特許分類】
【出願日】平成23年1月31日(2011.1.31)
【出願人】(000000240)太平洋セメント株式会社 (1,449)
【Fターム(参考)】
[ Back to top ]

