(オキシ)ナイトライド蛍光体、それを含む白色発光素子及び蛍光体の製造方法
【課題】(オキシ)ナイトライド蛍光体、それを含む白色発光素子及び蛍光体の製造方法を提供する。
【解決手段】下記化学式1の化合物で表示されるオキシナイトライド蛍光体である:

前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。これにより、UV−LED及び青色LED型の白色発光素子に使用するのに優秀な赤色を具現し、優秀な効率を具現する。
【解決手段】下記化学式1の化合物で表示されるオキシナイトライド蛍光体である:

前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。これにより、UV−LED及び青色LED型の白色発光素子に使用するのに優秀な赤色を具現し、優秀な効率を具現する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、(オキシ)ナイトライド蛍光体、それを含む白色発光素子及びナイトライド蛍光体の製造方法に係り、特に優秀な赤色及び優秀な発光効率を具現する(オキシ)ナイトライド蛍光体、それを含む白色発光素子及びマイルドな工程条件を有する蛍光体の製造方法に関する。
【背景技術】
【0002】
従来の光システムとして蛍光灯及び白熱灯が広く使われる。しかし、蛍光灯で使われるHgは、環境問題をもたらす。また、前記従来の光システムは、寿命が非常に短いだけでなく、その効率も非常に低いため、節電の側面から望ましくない。これに対し、最近多くの研究により白色発光素子の効率が向上している。
【0003】
かかる白色発光素子を具現する方法は、UV発光ダイオード(Light Emitting Diode:LED、以下、UV−LEDとも称する)を光源として利用し、光の三原色である三原色蛍光体を励起させて白色を具現する方式、青色発光ダイオード(以下、青色LEDとも称する)を光源として使用して赤色及び緑色蛍光体を励起させて白色を具現する方式、または青色LEDを光源として使用して黄色蛍光体を励起させることによって白色を具現する方式に区分される。
【0004】
前記三つの方法のうち、青色LEDを光源として使用して黄色蛍光体を励起させることによって白色を具現する方式は、赤色の強度が低下して色再現の側面で問題がある。
【0005】
したがって、前記三つの方式のうち、残りのUV及び青色LED及び蛍光体を使用して光システムを開発しようとする研究が増加している。しかし、それらの方式は、色再現には優れているが、効率が低下するという短所がある。
【0006】
一方、従来の公知の赤色蛍光体は、白色発光素子に適用するのに適していない。それらは、カソードレイ、VUV(Vacuum Ultraviolet)レイ及び短波長光に対しては発光効率が優れているが、前記白色発光素子で使われるUV及び青色光に対する発光効率に劣る。したがって、白色発光素子の技術分野で、UV及び青色光に対して高効率を有する赤色蛍光体の開発が強く要求されている。
【0007】
かかる状況で、ナイトライド蛍光体の開発が進められている。
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、従来のナイトライド蛍光体は、UV及び青色光に対して発光するものの、白色発光素子として商業化されるには発光強度が十分な程度ではない。また、公知のナイトライド蛍光体の製造方法は、高い温度、0.1MP以上の高い窒素ガス圧力の工程条件が必要となる。したがって、かかる高温、高圧に耐えるように考案された特別な装置が必要となり、また、出発物質として不安定な物質を使用しているため、それらの出発物質の取扱時に要求される条件が厳しい。このように、現在までは商業化するのに適した赤色蛍光体が開発されていないのが実情である。
【0009】
本発明が解決しようとする課題は、前述した問題点を解決した赤色蛍光体として(オキシ)ナイトライド蛍光体を提供するところにある。
【0010】
本発明が解決しようとする他の課題は、前記(オキシ)ナイトライド蛍光体を含む白色発光素子を提供するところにある。
【0011】
本発明が解決しようとするさらに他の課題は、安定かつマイルドな工程条件を有する蛍光体の製造方法を提供するところにある。
【課題を解決するための手段】
【0012】
前記課題を解決するために、本発明では、下記化学式1の化合物で表示される(オキシ)ナイトライド蛍光体を提供する。
【0013】
【化1】

【0014】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【0015】
前記化学式1の化合物の(オキシ)ナイトライド蛍光体は、ポアを含みうる。
【0016】
前記他の課題を解決するために、本発明では、UV−LEDと、前記本発明による(オキシ)ナイトライド赤色蛍光体と、を含む白色発光素子を提供する。
【0017】
前記さらに他の課題を解決するために、本発明では、(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、(b)前記ゲル状態の混合物を乾燥及び1次焼成する工程と、(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含む蛍光体の製造方法を提供する。
【発明の効果】
【0018】
本発明の(オキシ)ナイトライド蛍光体は、UV−LED及び青色LED型白色発光素子に使用するのに優れた赤色を具現し、優秀な効率を具現する。また、本発明による蛍光体の製造方法は、安定した物質を出発物質として使用し、工程条件がマイルドかつ環境親和的であるので、商業的に活用するのに有効である。
【図面の簡単な説明】
【0019】
【図1】本発明の一具現例によるLEDの構造を示す概略図である。
【図2】本発明の他の具現例による(オキシ)ナイトライド蛍光体の励起スペクトルを示す図面である。
【図3】本発明のさらに他の具現例による(オキシ)ナイトライド蛍光体の発光スペクトルを示す図面である。
【図4】本発明のさらに他の具現例による(オキシ)ナイトライド蛍光体に対する発光スペクトルを示す図面である。
【図5】本発明の蛍光体の製造方法の一具現例において、中間産物として生成されるSr2+キレート化合物の構造式を示す図面である。
【図6】本発明の蛍光体の製造方法によって中間過程で形成されるゲル状態の混合物を図式化した図面である。
【図7】本発明の蛍光体の製造方法の他の具現例において、1次焼成過程を通じた変化を概略的に示す図面である。
【図8】本発明の蛍光体の製造方法のさらに他の具現例において、2次焼成過程を通じた蛍光体の形成過程を概略的に示す図面である。
【図9】本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【図10】アルカリ土類金属としてSrを使用し、酸としてクエン酸を使用した場合を例とした本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【図11】本発明の一具現例による(オキシ)ナイトライド蛍光体のSEM写真である。
【発明を実施するための形態】
【0020】
以下、本発明をさらに詳細に説明する。
【0021】
本発明は、下記化学式1の(オキシ)ナイトライド系蛍光体を提供する。
【0022】
【化2】

【0023】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【0024】
前記化学式1の化合物の例として下記の化学式が挙げられる。
【0025】
【化3】

【0026】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8及び0<c+d≦8である。
【0027】
前記(オキシ)ナイトライド蛍光体は、ポアを含みうる。
【0028】
前記化学式1の(オキシ)ナイトライド蛍光体は、赤色蛍光体であって、UV及び青色光に対して励起され、赤色発光時に高効率を表す物質である。したがって、前記化学式1の(オキシ)ナイトライド蛍光体を含む白色発光素子は、UV−LED及び青色−LEDを励起光源として使用できる。
【0029】
本発明による化学式1の(オキシ)ナイトライド蛍光体は、従来の赤色蛍光体が有する色々な短所を効果的に改善する。例えば、発光元素が窒素と結合することによって、消光と関連した熱活性化エネルギーが非常に大きくなる。このため、赤色発光の熱損失を減らすことができ、赤色発光の高い効率が得られる。また、既存の赤色蛍光体には、空気中の水分に敏感である、バインダと予期せぬ反応を起こす、熱に対する耐久性が弱いといった問題点があった。オキシナイトライド蛍光体は、従来の赤色蛍光体が有するかような問題を解決しうる物質であるため、白色発光素子用の赤色蛍光体として非常に有効である。
【0030】
したがって、本発明による(オキシ)ナイトライド赤色蛍光体は、UV−LEDを光源として利用し、赤色、緑色、青色を有する3個の蛍光体を組み合わせて白色を具現する方式、及び青色LEDを光源として使用して赤色及び緑色蛍光体を励起させることによって白色を具現する方式の白色発光素子の類型に非常に適している。かかる白色発光素子は、良好な白色発光を実現し、かつ高い効率を具現できる。
【0031】
一方、前記本発明による(オキシ)ナイトライド蛍光体は、人の目に対する敏感度が高い赤色を再現できる。
【0032】
また、本発明は、ポアを含む(オキシ)ナイトライド蛍光体を提供する。ポアを有するオキシナイトライド蛍光体の製造過程で、活性窒素(N*)がポア内に浸透して窒化を起こす。オキシナイトライド蛍光体がポアを有すると、ポアを通じて円滑なガスの出入が行われる。したがって窒化の観点から見るとき、ポアが蛍光体の合成過程上、肯定的な役割を行う側面があると見られる。
【0033】
本発明による(オキシ)ナイトライド蛍光体がポアを含む場合、前記ポアは、平均直径が0.6μm以下であり、望ましくは、約0.2μmないし0.6μmである。ポアの平均直径が0.2μm未満の場合、Nの含量が少なくなる可能性がある。これは、蛍光体の製造過程で前述したように活性窒素(N*)がポア内に浸透して窒化を起こすが、ポアが小さくなれば、かかる作用が不十分になるためである。また、ポアの平均直径が0.6μmを超える場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。なお、ポアが概略円形以外の場合、平均直径を算出する際の直径とは、楕円形の場合、長径を指し、多角形の場合、各頂点を結んだ長さのうち最大径を指す。
【0034】
また、ポアは、(オキシ)ナイトライド蛍光体の断面1μm2当たり約0.01個以下、望ましくは、約0.005個ないし0.01個を含む。前記単位面積当たりポアの個数、すなわち(オキシ)ナイトライド蛍光体の断面1μm2当たりポアが0.005個未満の場合、Nの含量が少なくなる虞れがある。これも、蛍光体の製造過程で活性窒素(N*)がポア内に浸透して窒化を起こすが、ポアの個数が少なくなれば、かかる作用が不十分になるためである。前記単位面積当たりポアの個数、すなわち(オキシ)ナイトライド蛍光体の断面1μm2当たりポアが0.01個を超える場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。
【0035】
ポア間の平均距離は、約1μm以上、望ましくは、約1μmないし3μmである。ポア間の平均距離が1μm未満で形成される場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。3μmを超えて形成される場合、Nの含量が少なくなる可能性がある。これも、前記蛍光体の製造過程で活性窒素(N*)がポア内に浸透して窒化を起こすが、ポア間の平均距離が大きくなれば、かかる作用が不十分になるためである。
【0036】
ポアは、色々な形態を有するところ、その断面が円形、楕円形、多角形などでありうる。
【0037】
化学式1において、Mはアルカリ土類金属であり、好ましくはBa、SrまたはCaである。ここでMは、1種のアルカリ土類金属であっても、あるいは2種以上のアルカリ土類金属を表すものであってもよい。
【0038】
前記化学式1の化合物の具体例としては、(Sr1−xEux)aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0≦c<8及び0<c+d≦8、望ましくは、(Sr1−xEux)2Si5N8(0<x≦0.1)が挙げられる。
【0039】
前記化学式1の化合物の他の具体例としては、(Sr1−xEux)2Si5N8(0<x<1)、(Sr1−xEux)1.99Si5N8(0<x<1)、(Ba1−x−ySrxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Sr1−x−yCaxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Ba0.5Sr1−xCa0.5Eux)Si5N8(0<x<1)、(Sr1−xEux)2Si5O0.32N7.68(0<x<1)),または(Sr1−xEux)2Si5O0.30N7.70(0<x<1))のような化合物でありうる。
【0040】
本発明は、また、UV−LEDと、本発明による(オキシ)ナイトライド赤色蛍光体(ポアを有する場合及びポアを有さない場合いずれも可能である)と、を含む白色発光素子を提供する。
【0041】
望ましくは、UV−LEDは、励起光源が紫外線または近紫外線領域の電磁波である。
【0042】
さらに望ましくは、白色発光素子において、UV−LEDの励起光源の波長帯域が390〜460nmの範囲である。
【0043】
UV−LEDと、本発明によるオキシナイトライド赤色蛍光体を含む白色発光素子は、青色蛍光体および/または緑色蛍光体をさらに含む。
【0044】
前記青色蛍光体の例としては、(Sr,Ba,Ca)5(PO4)3Cl:Eu2+;BaMg2Al16O27:Eu2+;Sr4Al14O25:Eu2+;BaAl8O13:Eu2+;(Sr,Mg,Ca,Ba)5(PO4)3Cl:Eu2+;BaMgAl10O17:Eu2+及びSr2Si3O82SrCl2:Eu2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0045】
前記緑色蛍光体の例としては、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+及びBaMg2Al16O27:Eu2+,Mn2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0046】
望ましくは、前記赤色蛍光体の放出スペクトル(蛍光スペクトル)でピークの波長は、610〜650nmである。望ましくは、前記緑色蛍光体の放出スペクトルでピークの波長は、510〜560nmである。望ましくは、前記青色蛍光体の放出スペクトルでピークの波長は、440〜460nmである。
【0047】
また、本発明は、青色LEDと、本発明による(オキシ)ナイトライド赤色蛍光体と、を含む白色発光素子を提供する。望ましくは、青色LEDは、励起光源であって、420〜480nmの波長帯域を有する。
【0048】
青色LEDと、本発明によるオキシナイトライド赤色蛍光体を含む白色発光素子は、緑色蛍光体をさらに含むことが好ましい。
【0049】
緑色蛍光体の例としては、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+及びBaMg2Al16O27:Eu2+,Mn2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0050】
望ましくは、前記赤色蛍光体の放出スペクトルでピークの波長は、610〜650nmである。望ましくは、前記緑色蛍光体の放出スペクトルでピークの波長は、510〜560nmである。
【0051】
本発明の白色発光素子は、信号灯、通信機器、ディスプレイ装置のバックライトまたは照明用として用いることができる。
【0052】
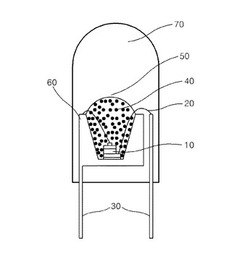
図1は、本発明の一実施形態によるLEDの構造を示す概略図であって、高分子レンズタイプの表面実装型LEDを示すものである。ここで、高分子レンズの一実施例としてエポキシレンズを使用する。
【0053】
図1に示すように、UV LEDチップ10は、金ワイヤー20を通じて電気リード線30とダイボンディングされ、本発明による赤色蛍光体を含有する蛍光体組成物40を含むようにエポキシモールド層50が形成されている。そして、図1において、成形モールド60の内部は、アルミニウムまたは銀でコーティングされた反射膜からなり、これは、ダイオードから放出された光を上方に反射させる役割及び適当量のエポキシを溜める役割を行う。
【0054】
前記エポキシモールド層50の上部には、エポキシドームレンズ70が形成されており、このエポキシドームレンズ70は、所望の配向角によって形態が変化しうる。
【0055】
本発明のLEDは、図1の構造にのみ限定されることを意味するものではなく、その他の構造、例えばLEDに蛍光体が実装されるタイプ、砲弾型、PCBタイプの表面実装型の構造を有するLEDでありうる。
【0056】
一方、本発明の化学式1で表示されるオキシナイトライド蛍光体は、前述したLED以外に水銀ランプ、キセノンランプのようなランプまたは自発光液晶表示素子(LCD)にも適用可能である。
【0057】
また、本発明は、(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、(b)前記(a)工程で得られる混合物を乾燥及び1次焼成する工程と、(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含む蛍光体の製造方法を提供する。
【0058】
上記方法を本発明の一具現例によってさらに具体的に説明すれば、次の通りである。
【0059】
まず、アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物を準備する。アルカリ土類金属前駆体化合物は、望ましくは、Ba前駆体化合物、Sr前駆体化合物、Ca前駆体化合物などを使用できる。Ba前駆体化合物の例として、BaCO3,Ba(NO3)2,BaCl2,BaOなどがある。Sr前駆体化合物の例として、SrCO3,Sr(NO3)2,SrCl2,SrOなどがある。Ca前駆体化合物の例として、CaCO3,Ca(NO3)2,CaCl2,CaOなどがある。また、前記Eu前駆体化合物として、Eu2O3,Eu(NO3)3,EuCl3などを使用できる。前記各前駆体化合物は、それぞれ1種単独で用いてもよいし、2種以上併用してもよい。
【0060】
次いで、前記アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物を酸に溶解させる。このとき、使用可能な酸は、無機酸または有機酸などが広く使われ、その例としては、HNO3、HCl、H2SO4、酢酸、酪酸、パルミチン酸、シュウ酸、酒石酸などがある。これらは1種単独で用いてもよいし、2種以上併用してもよい。望ましくは、前記酸は、0.1ないし10mol/lの濃度である。
【0061】
次いで、前記アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物が溶解された酸にSi3N4粉末を添加する。
【0062】
次いで、前記アルカリ土類金属前駆体化合物、Eu前駆体化合物の混合物が溶解された酸及びSi3N4粉末の混合物にキレート化合物を添加してゲル状態に形成する。前記キレート化合物の例は、クエン酸、グリシン、尿素、エチレンジアミン四酢酸(EDTA)などでありうる。キレート剤の添加量は、混合物全体に対して25〜30質量%であることが好ましい。前記キレート化合物は、それぞれ1種単独で用いてもよいし、2種以上併用してもよい。
【0063】
前記キレート化合物を混合すれば、下記反応式によって反応してSr2+キレート化合物、Eu3+キレート化合物が形成される。
【0064】
前記Sr2+キレート化合物、Eu3+キレート化合物の反応経路を、アルカリ土類金属前駆体化合物としてSrCO3を、Eu前駆体化合物としてEu2O3を使用し、酸として硝酸を、キレート化合物としてクエン酸を使用した場合を例として説明すれば、次の通りである。この場合、下記反応式1のような反応が起こる。
【0065】
【化4】

【0066】
さらに詳しくは、前記Sr2+キレート化合物は、まず、SrCO3が硝酸と反応してSr2+を形成し、次いで、クエン酸と反応して形成される。
【0067】
【化5】

【0068】
このように形成されたSr2+キレート化合物は、図5で示した通りである。
【0069】
また、前記Eu3+キレート化合物も、まず、Eu2O3が硝酸と反応してEu3+を形成し、次いで、クエン酸と反応して形成される。
【0070】
【化6】

【0071】
図6は、前記のような過程で形成されたゲル状態の混合物を図式化したものである。図6において、Si3N4間に介在されたキレート化合物は、Sr2+キレート化合物及びEu3+キレート化合物がランダムに分布したことを意味する。
【0072】
次いで、前記ゲル状態の結果物を乾燥した後、1次焼成する。望ましくは、前記焼成は、300ないし700℃の空気雰囲気下で行う。焼成時間は特に限定されるものではないが、好ましくは0.5〜5時間、より好ましくは1〜5時間である。かかる1次焼成によりアルカリ土類金属キレート化合物及びEu3+キレート化合物が酸化されて、アルカリ土類金属酸化物及びEu2O3が合成される。このように生成されたアルカリ土類金属酸化物は、前記酸化時に共に発生するCO2及びH2Oガスにより生成された複数のポアを有する。
【0073】
図7は、前記反応式1の例で1次焼成過程を通じた変化を概略的に示す図面である。
【0074】
次いで、前記のように1次焼成を行って得た結果物を粉砕し、2次焼成を行う。このとき、焼成は、1300〜1700℃で行うことが好ましい。また焼成時間は、10〜100時間で行うことが好ましい。さらに焼成雰囲気は、NH3及び/またはH2/N2混合ガス雰囲気下で行うことが好ましい。H2/N2混合ガスの混合割合は、好ましくはH2:N2=0.05:1〜0.2:1である。なお、工程中の一部に前記好適な条件を具備する焼結工程が少なくとも含まれて入ればよい。かような2次焼成を行うことによって、ナイトライド化合物が得られる。
【0075】
前記NH3及び/またはH2/N2混合物ガス雰囲気下での2次焼成過程をさらに詳細に説明すれば、まず、高温でNH3またはN2は分解されて活性窒素(N*)を生成する。
【0076】
N*は、ポアを通過できる。一般的に、酸化物は、前記のようなポアを有さないため、酸化物粒子の表面積が非常に小さい。一方、本発明の蛍光体の製造過程では、ポアが生成されるため、表面積が非常に広くなる。窒化反応は、気体及び固体の反応であるため、活性表面が広いほどさらに望ましい。したがって、本発明の蛍光体の製造過程では、ポアの生成により広い活性表面を提供できるので、窒化反応に対して非常に有利である。
【0077】
前記1次焼成後に生成されたアルカリ土類金属酸化物及びEu2O3のN*との窒化反応により、アルカリ土類金属窒化物、Eu3N2(このとき、E3+は、E2+に還元される)が生成される。前述したように、前記アルカリ土類金属がSrである場合、アルカリ土類金属窒化物はSr3N2である。このように生成されたアルカリ土類金属窒化物及びEu3N2は、空気中では不安定であるが、前記本発明の蛍光体の製造方法による環境では安定している。次いで、さらなる反応によりナイトライド蛍光体が製造される。また、前記アルカリ土類金属がSrである場合の例を挙げれば、前記生成されたナイトライド蛍光体は(Sr1−xEux)2Si5N8(0<x<1)でありうる。
【0078】
図8は、これまで詳述した2次焼成過程を通じた蛍光体の形成過程をアルカリ土類金属がSrである場合の例として挙げて概略的に示す図面である。
【0079】
図9は、本発明の他の具現例による蛍光体の製造方法の概略的なフローチャートである。フローチャート中、使用される化合物および記載のない製造条件としては、上述したものと同様のものを用いることができる。
【0080】
図10は、アルカリ土類金属としてSrを使用し、酸としてクエン酸を使用した場合を例として本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【0081】
選択的に、前記のように得た結果物は、粉砕及び焼成する段階を反復して優秀な結晶性を有するナイトライド蛍光体が得られる。このとき、焼成は、望ましくは、1300〜1700℃で10〜100時間、NH3及び/またはH2/N2混合ガス雰囲気下で行える。
【0082】
次いで、前記結果物を洗浄して、最終粉末状態の蛍光体結果物が得られる。
【0083】
図11は、本発明の一具現例による(オキシ)ナイトライド蛍光体のSEM写真を示す。前記図11から分かるように、前記(オキシ)ナイトライド蛍光体は、ポアを有し、前記ポアの平均直径は、0.6μm以下であり、前記ポアの数は、単位面積(1μm2)当たり0.01以下であり、前記ポア間の平均距離は、1μm以上であり、前記ポアの断面積は、円形、楕円形、長方形、正方形、多角形などの形態を有する。
【0084】
前記本発明による蛍光体の製造方法は、特にナイトライド蛍光体の製造に有利である。すなわち、従来技術は、不安定な一部のナイトレートを前駆体として使用するところ、グローブボックスのように特別な装置の使用が要求されることと異なり、本発明による蛍光体の製造方法は、Sr,Ba,Ca,Euのそれぞれの前駆体としてSrCO3,SrO,Sr(NO3)2,SrCl2,BaCO3,BaO,Ba(NO3)2,BaCl2,CaCO3,CaO,Ca(NO3)2,CaCl2,Eu2O3,Eu(NO3)3,EuCl3のようにカーボネートまたはオキサイドなどの非常に安定な粉末を使用し、一方、Siの前駆体は、大気で安定なSi3N4を使用するので、グローブボックスのような特別な装置を要求しない。
【0085】
このように、本発明による蛍光体の製造方法は、安定な物質を出発物質として使用し、また、マイルドな工程条件で可能であるので、商業的に応用するのに非常に適している。すなわち、従来の公知のナイトライド系蛍光体の製造方法は、高温、高圧の窒素雰囲気を要求したが、前記本発明によるナイトライド蛍光体の製造方法は、それをいずれも解決した方法である。したがって、高温、高圧の工程条件を組成し、また、かかる高温、高圧の工程条件に耐えるために特別に設備された装置を要求しない。
【0086】
また、本発明によるナイトライド蛍光体の製造方法は、環境問題をもたらす物質を使用しないために環境にやさしい。
【0087】
本発明は、また、前記本発明による蛍光体の製造方法によって製造されたナイトライド蛍光体を提供する。
【実施例】
【0088】
以下、本発明を下記実施例を挙げて詳細に説明するが、本発明が下記実施例にのみ限定されるものではない。
【0089】
実施例1
SrCO3 5.0g及びEu2O3 0.06gを10質量%硝酸水溶液100cc(混合物中、1.7N)に溶解した。前記混合溶液にSi3N4 4.0gを添加した。クエン酸4.8gを前記混合溶液と混ぜて乾燥させた。前記乾燥された混合物を空気雰囲気下で700℃で1時間焼成した。焼成された混合物を、めのう乳鉢を利用して粉砕した。前記粉砕して得た粉末をペレット形態に得た後、それをアルミナるつぼに入れ、それを電気炉に入れて炭素と共にNH3雰囲気で1100℃まで加熱し(1100℃での維持時間;3時間)、その後5%のH2及び95%のN2雰囲気で1600℃まで加熱する。1600℃での焼成時間は、5時間行った。前記炭素は、ナイトライド出発物質の酸化を防止するために使われる。このように得た焼結体を粉末に粉砕し、蒸溜水で洗浄した後、オーブンで乾燥して蛍光体サンプル1(Sr0.99Eu0.01)2Si5N8を得た。
【0090】
実施例2
出発物質としてSrCO3 5.0g及びEu2O3 0.12gを10質量%硝酸100ccに溶解して使用した点を除いては、実施例1と同様に行って蛍光体サンプル2(Sr0.98Eu0.02)2Si5N8を得た。
【0091】
実施例3
出発物質としてSrCO3 5.0g及びEu2O3 0.18gを10質量%硝酸100ccに溶解した後、前記混合溶液にSi3N4 4.1gを添加して使用した点を除いては、実施例1と同様に行って蛍光体サンプル3(Sr0.97Eu0.03)2Si5N8を得た。
【0092】
実施例4
SrCO3 5.0g及びEu2O3 0.12gを10質量%硝酸水溶液100ccに溶解し、ここにSi3N4 4.0gを添加した。前記混合溶液をクエン酸4.8gと混合して得られた溶液を乾燥した。乾燥させた結果物を700℃の大気中で1時間1次焼成した。めのう乳鉢を利用して前記焼成結果物を粉砕して粉末化した。得られた粉末をペレットに製造した。前記ペレットをるつぼに入れた後、それを電気炉に位置させた。前記電気炉でカーボンと共に前記ペレットをNH3大気下で1時間1100℃まで加熱し、その後5%のH2及び95%のN2大気下で5時間1600℃まで加熱した。前記カーボンは、窒化出発物の酸化を防止するために添加した。加熱時間は1ないし60時間であり、望ましくは、3ないし50時間である。焼成結果物を粉砕して粉末化した後、得られた粉末を蒸溜水で洗浄し、オーブンで乾燥してSr1.96Eu0.04Si5O0.32N7.68の化学式を有する蛍光体を製造した。
【0093】
実施例5
SrCO3 5.0g及びEu2O3 0.06gを10質量%硝酸水溶液100ccに溶解し、ここにSi3N4 4.0gを添加した。前記混合溶液をクエン酸4.8gと混合して得られた溶液を乾燥した。乾燥させた結果物を700℃の大気中で1時間1次焼成した。めのう乳鉢を利用して前記焼成結果物を粉砕して粉末化した。得られた粉末をペレットに製造した。前記ペレットをるつぼに入れた後、それを電気炉に位置させた。前記電気炉でカーボンと共に前記ペレットをNH3大気下で1時間1100℃まで加熱し、その後5%のH2及び95%のN2大気下で5時間1600℃まで加熱した。前記カーボンは、窒化出発物の酸化を防止するために添加した。加熱時間は1ないし60時間であり、望ましくは、3ないし50時間である。焼成結果物を粉砕して粉末化した後、得られた粉末を蒸溜水で洗浄し、オーブンで乾燥してSr1.98Eu0.02Si5O0.30N7.70の化学式を有する蛍光体を製造した。
【0094】
図2は、蛍光体サンプル1の励起スペクトルを示す。UVから青色までの広い領域で光を吸収するので、本発明の蛍光体サンプルは、UV−LEDや青色LEDにいずれも適用可能である。
【0095】
図3は、蛍光体サンプル1の発光スペクトルを示す。
【0096】
図4は、サンプル1、2及び3に対する発光スペクトルを示す図面である。これから、EuのSrに対する相対的な含量が多くなるほどピーク波長が長くなることを確認した。
【産業上の利用可能性】
【0097】
本発明は、発光素子関連の技術分野に適用可能である。
【符号の説明】
【0098】
10 LEDチップ
20 金ワイヤー
30 電気リード線
40 蛍光体組成物
50 エポキシモールド層
60 成形モールド
70 エポキシドームレンズ
【技術分野】
【0001】
本発明は、(オキシ)ナイトライド蛍光体、それを含む白色発光素子及びナイトライド蛍光体の製造方法に係り、特に優秀な赤色及び優秀な発光効率を具現する(オキシ)ナイトライド蛍光体、それを含む白色発光素子及びマイルドな工程条件を有する蛍光体の製造方法に関する。
【背景技術】
【0002】
従来の光システムとして蛍光灯及び白熱灯が広く使われる。しかし、蛍光灯で使われるHgは、環境問題をもたらす。また、前記従来の光システムは、寿命が非常に短いだけでなく、その効率も非常に低いため、節電の側面から望ましくない。これに対し、最近多くの研究により白色発光素子の効率が向上している。
【0003】
かかる白色発光素子を具現する方法は、UV発光ダイオード(Light Emitting Diode:LED、以下、UV−LEDとも称する)を光源として利用し、光の三原色である三原色蛍光体を励起させて白色を具現する方式、青色発光ダイオード(以下、青色LEDとも称する)を光源として使用して赤色及び緑色蛍光体を励起させて白色を具現する方式、または青色LEDを光源として使用して黄色蛍光体を励起させることによって白色を具現する方式に区分される。
【0004】
前記三つの方法のうち、青色LEDを光源として使用して黄色蛍光体を励起させることによって白色を具現する方式は、赤色の強度が低下して色再現の側面で問題がある。
【0005】
したがって、前記三つの方式のうち、残りのUV及び青色LED及び蛍光体を使用して光システムを開発しようとする研究が増加している。しかし、それらの方式は、色再現には優れているが、効率が低下するという短所がある。
【0006】
一方、従来の公知の赤色蛍光体は、白色発光素子に適用するのに適していない。それらは、カソードレイ、VUV(Vacuum Ultraviolet)レイ及び短波長光に対しては発光効率が優れているが、前記白色発光素子で使われるUV及び青色光に対する発光効率に劣る。したがって、白色発光素子の技術分野で、UV及び青色光に対して高効率を有する赤色蛍光体の開発が強く要求されている。
【0007】
かかる状況で、ナイトライド蛍光体の開発が進められている。
【発明の概要】
【発明が解決しようとする課題】
【0008】
しかしながら、従来のナイトライド蛍光体は、UV及び青色光に対して発光するものの、白色発光素子として商業化されるには発光強度が十分な程度ではない。また、公知のナイトライド蛍光体の製造方法は、高い温度、0.1MP以上の高い窒素ガス圧力の工程条件が必要となる。したがって、かかる高温、高圧に耐えるように考案された特別な装置が必要となり、また、出発物質として不安定な物質を使用しているため、それらの出発物質の取扱時に要求される条件が厳しい。このように、現在までは商業化するのに適した赤色蛍光体が開発されていないのが実情である。
【0009】
本発明が解決しようとする課題は、前述した問題点を解決した赤色蛍光体として(オキシ)ナイトライド蛍光体を提供するところにある。
【0010】
本発明が解決しようとする他の課題は、前記(オキシ)ナイトライド蛍光体を含む白色発光素子を提供するところにある。
【0011】
本発明が解決しようとするさらに他の課題は、安定かつマイルドな工程条件を有する蛍光体の製造方法を提供するところにある。
【課題を解決するための手段】
【0012】
前記課題を解決するために、本発明では、下記化学式1の化合物で表示される(オキシ)ナイトライド蛍光体を提供する。
【0013】
【化1】

【0014】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【0015】
前記化学式1の化合物の(オキシ)ナイトライド蛍光体は、ポアを含みうる。
【0016】
前記他の課題を解決するために、本発明では、UV−LEDと、前記本発明による(オキシ)ナイトライド赤色蛍光体と、を含む白色発光素子を提供する。
【0017】
前記さらに他の課題を解決するために、本発明では、(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、(b)前記ゲル状態の混合物を乾燥及び1次焼成する工程と、(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含む蛍光体の製造方法を提供する。
【発明の効果】
【0018】
本発明の(オキシ)ナイトライド蛍光体は、UV−LED及び青色LED型白色発光素子に使用するのに優れた赤色を具現し、優秀な効率を具現する。また、本発明による蛍光体の製造方法は、安定した物質を出発物質として使用し、工程条件がマイルドかつ環境親和的であるので、商業的に活用するのに有効である。
【図面の簡単な説明】
【0019】
【図1】本発明の一具現例によるLEDの構造を示す概略図である。
【図2】本発明の他の具現例による(オキシ)ナイトライド蛍光体の励起スペクトルを示す図面である。
【図3】本発明のさらに他の具現例による(オキシ)ナイトライド蛍光体の発光スペクトルを示す図面である。
【図4】本発明のさらに他の具現例による(オキシ)ナイトライド蛍光体に対する発光スペクトルを示す図面である。
【図5】本発明の蛍光体の製造方法の一具現例において、中間産物として生成されるSr2+キレート化合物の構造式を示す図面である。
【図6】本発明の蛍光体の製造方法によって中間過程で形成されるゲル状態の混合物を図式化した図面である。
【図7】本発明の蛍光体の製造方法の他の具現例において、1次焼成過程を通じた変化を概略的に示す図面である。
【図8】本発明の蛍光体の製造方法のさらに他の具現例において、2次焼成過程を通じた蛍光体の形成過程を概略的に示す図面である。
【図9】本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【図10】アルカリ土類金属としてSrを使用し、酸としてクエン酸を使用した場合を例とした本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【図11】本発明の一具現例による(オキシ)ナイトライド蛍光体のSEM写真である。
【発明を実施するための形態】
【0020】
以下、本発明をさらに詳細に説明する。
【0021】
本発明は、下記化学式1の(オキシ)ナイトライド系蛍光体を提供する。
【0022】
【化2】

【0023】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【0024】
前記化学式1の化合物の例として下記の化学式が挙げられる。
【0025】
【化3】

【0026】
前記式で、Mは、アルカリ土類金属であり、0<x<1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8及び0<c+d≦8である。
【0027】
前記(オキシ)ナイトライド蛍光体は、ポアを含みうる。
【0028】
前記化学式1の(オキシ)ナイトライド蛍光体は、赤色蛍光体であって、UV及び青色光に対して励起され、赤色発光時に高効率を表す物質である。したがって、前記化学式1の(オキシ)ナイトライド蛍光体を含む白色発光素子は、UV−LED及び青色−LEDを励起光源として使用できる。
【0029】
本発明による化学式1の(オキシ)ナイトライド蛍光体は、従来の赤色蛍光体が有する色々な短所を効果的に改善する。例えば、発光元素が窒素と結合することによって、消光と関連した熱活性化エネルギーが非常に大きくなる。このため、赤色発光の熱損失を減らすことができ、赤色発光の高い効率が得られる。また、既存の赤色蛍光体には、空気中の水分に敏感である、バインダと予期せぬ反応を起こす、熱に対する耐久性が弱いといった問題点があった。オキシナイトライド蛍光体は、従来の赤色蛍光体が有するかような問題を解決しうる物質であるため、白色発光素子用の赤色蛍光体として非常に有効である。
【0030】
したがって、本発明による(オキシ)ナイトライド赤色蛍光体は、UV−LEDを光源として利用し、赤色、緑色、青色を有する3個の蛍光体を組み合わせて白色を具現する方式、及び青色LEDを光源として使用して赤色及び緑色蛍光体を励起させることによって白色を具現する方式の白色発光素子の類型に非常に適している。かかる白色発光素子は、良好な白色発光を実現し、かつ高い効率を具現できる。
【0031】
一方、前記本発明による(オキシ)ナイトライド蛍光体は、人の目に対する敏感度が高い赤色を再現できる。
【0032】
また、本発明は、ポアを含む(オキシ)ナイトライド蛍光体を提供する。ポアを有するオキシナイトライド蛍光体の製造過程で、活性窒素(N*)がポア内に浸透して窒化を起こす。オキシナイトライド蛍光体がポアを有すると、ポアを通じて円滑なガスの出入が行われる。したがって窒化の観点から見るとき、ポアが蛍光体の合成過程上、肯定的な役割を行う側面があると見られる。
【0033】
本発明による(オキシ)ナイトライド蛍光体がポアを含む場合、前記ポアは、平均直径が0.6μm以下であり、望ましくは、約0.2μmないし0.6μmである。ポアの平均直径が0.2μm未満の場合、Nの含量が少なくなる可能性がある。これは、蛍光体の製造過程で前述したように活性窒素(N*)がポア内に浸透して窒化を起こすが、ポアが小さくなれば、かかる作用が不十分になるためである。また、ポアの平均直径が0.6μmを超える場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。なお、ポアが概略円形以外の場合、平均直径を算出する際の直径とは、楕円形の場合、長径を指し、多角形の場合、各頂点を結んだ長さのうち最大径を指す。
【0034】
また、ポアは、(オキシ)ナイトライド蛍光体の断面1μm2当たり約0.01個以下、望ましくは、約0.005個ないし0.01個を含む。前記単位面積当たりポアの個数、すなわち(オキシ)ナイトライド蛍光体の断面1μm2当たりポアが0.005個未満の場合、Nの含量が少なくなる虞れがある。これも、蛍光体の製造過程で活性窒素(N*)がポア内に浸透して窒化を起こすが、ポアの個数が少なくなれば、かかる作用が不十分になるためである。前記単位面積当たりポアの個数、すなわち(オキシ)ナイトライド蛍光体の断面1μm2当たりポアが0.01個を超える場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。
【0035】
ポア間の平均距離は、約1μm以上、望ましくは、約1μmないし3μmである。ポア間の平均距離が1μm未満で形成される場合、蛍光体の密度が減少して発光強度が低下するという問題点がありうる。3μmを超えて形成される場合、Nの含量が少なくなる可能性がある。これも、前記蛍光体の製造過程で活性窒素(N*)がポア内に浸透して窒化を起こすが、ポア間の平均距離が大きくなれば、かかる作用が不十分になるためである。
【0036】
ポアは、色々な形態を有するところ、その断面が円形、楕円形、多角形などでありうる。
【0037】
化学式1において、Mはアルカリ土類金属であり、好ましくはBa、SrまたはCaである。ここでMは、1種のアルカリ土類金属であっても、あるいは2種以上のアルカリ土類金属を表すものであってもよい。
【0038】
前記化学式1の化合物の具体例としては、(Sr1−xEux)aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0≦c<8及び0<c+d≦8、望ましくは、(Sr1−xEux)2Si5N8(0<x≦0.1)が挙げられる。
【0039】
前記化学式1の化合物の他の具体例としては、(Sr1−xEux)2Si5N8(0<x<1)、(Sr1−xEux)1.99Si5N8(0<x<1)、(Ba1−x−ySrxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Sr1−x−yCaxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Ba0.5Sr1−xCa0.5Eux)Si5N8(0<x<1)、(Sr1−xEux)2Si5O0.32N7.68(0<x<1)),または(Sr1−xEux)2Si5O0.30N7.70(0<x<1))のような化合物でありうる。
【0040】
本発明は、また、UV−LEDと、本発明による(オキシ)ナイトライド赤色蛍光体(ポアを有する場合及びポアを有さない場合いずれも可能である)と、を含む白色発光素子を提供する。
【0041】
望ましくは、UV−LEDは、励起光源が紫外線または近紫外線領域の電磁波である。
【0042】
さらに望ましくは、白色発光素子において、UV−LEDの励起光源の波長帯域が390〜460nmの範囲である。
【0043】
UV−LEDと、本発明によるオキシナイトライド赤色蛍光体を含む白色発光素子は、青色蛍光体および/または緑色蛍光体をさらに含む。
【0044】
前記青色蛍光体の例としては、(Sr,Ba,Ca)5(PO4)3Cl:Eu2+;BaMg2Al16O27:Eu2+;Sr4Al14O25:Eu2+;BaAl8O13:Eu2+;(Sr,Mg,Ca,Ba)5(PO4)3Cl:Eu2+;BaMgAl10O17:Eu2+及びSr2Si3O82SrCl2:Eu2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0045】
前記緑色蛍光体の例としては、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+及びBaMg2Al16O27:Eu2+,Mn2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0046】
望ましくは、前記赤色蛍光体の放出スペクトル(蛍光スペクトル)でピークの波長は、610〜650nmである。望ましくは、前記緑色蛍光体の放出スペクトルでピークの波長は、510〜560nmである。望ましくは、前記青色蛍光体の放出スペクトルでピークの波長は、440〜460nmである。
【0047】
また、本発明は、青色LEDと、本発明による(オキシ)ナイトライド赤色蛍光体と、を含む白色発光素子を提供する。望ましくは、青色LEDは、励起光源であって、420〜480nmの波長帯域を有する。
【0048】
青色LEDと、本発明によるオキシナイトライド赤色蛍光体を含む白色発光素子は、緑色蛍光体をさらに含むことが好ましい。
【0049】
緑色蛍光体の例としては、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+及びBaMg2Al16O27:Eu2+,Mn2+などが挙げられる。これらは1種単独で用いてもよいし、2種以上併用してもよい。
【0050】
望ましくは、前記赤色蛍光体の放出スペクトルでピークの波長は、610〜650nmである。望ましくは、前記緑色蛍光体の放出スペクトルでピークの波長は、510〜560nmである。
【0051】
本発明の白色発光素子は、信号灯、通信機器、ディスプレイ装置のバックライトまたは照明用として用いることができる。
【0052】
図1は、本発明の一実施形態によるLEDの構造を示す概略図であって、高分子レンズタイプの表面実装型LEDを示すものである。ここで、高分子レンズの一実施例としてエポキシレンズを使用する。
【0053】
図1に示すように、UV LEDチップ10は、金ワイヤー20を通じて電気リード線30とダイボンディングされ、本発明による赤色蛍光体を含有する蛍光体組成物40を含むようにエポキシモールド層50が形成されている。そして、図1において、成形モールド60の内部は、アルミニウムまたは銀でコーティングされた反射膜からなり、これは、ダイオードから放出された光を上方に反射させる役割及び適当量のエポキシを溜める役割を行う。
【0054】
前記エポキシモールド層50の上部には、エポキシドームレンズ70が形成されており、このエポキシドームレンズ70は、所望の配向角によって形態が変化しうる。
【0055】
本発明のLEDは、図1の構造にのみ限定されることを意味するものではなく、その他の構造、例えばLEDに蛍光体が実装されるタイプ、砲弾型、PCBタイプの表面実装型の構造を有するLEDでありうる。
【0056】
一方、本発明の化学式1で表示されるオキシナイトライド蛍光体は、前述したLED以外に水銀ランプ、キセノンランプのようなランプまたは自発光液晶表示素子(LCD)にも適用可能である。
【0057】
また、本発明は、(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、(b)前記(a)工程で得られる混合物を乾燥及び1次焼成する工程と、(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含む蛍光体の製造方法を提供する。
【0058】
上記方法を本発明の一具現例によってさらに具体的に説明すれば、次の通りである。
【0059】
まず、アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物を準備する。アルカリ土類金属前駆体化合物は、望ましくは、Ba前駆体化合物、Sr前駆体化合物、Ca前駆体化合物などを使用できる。Ba前駆体化合物の例として、BaCO3,Ba(NO3)2,BaCl2,BaOなどがある。Sr前駆体化合物の例として、SrCO3,Sr(NO3)2,SrCl2,SrOなどがある。Ca前駆体化合物の例として、CaCO3,Ca(NO3)2,CaCl2,CaOなどがある。また、前記Eu前駆体化合物として、Eu2O3,Eu(NO3)3,EuCl3などを使用できる。前記各前駆体化合物は、それぞれ1種単独で用いてもよいし、2種以上併用してもよい。
【0060】
次いで、前記アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物を酸に溶解させる。このとき、使用可能な酸は、無機酸または有機酸などが広く使われ、その例としては、HNO3、HCl、H2SO4、酢酸、酪酸、パルミチン酸、シュウ酸、酒石酸などがある。これらは1種単独で用いてもよいし、2種以上併用してもよい。望ましくは、前記酸は、0.1ないし10mol/lの濃度である。
【0061】
次いで、前記アルカリ土類金属前駆体化合物及びEu前駆体化合物の混合物が溶解された酸にSi3N4粉末を添加する。
【0062】
次いで、前記アルカリ土類金属前駆体化合物、Eu前駆体化合物の混合物が溶解された酸及びSi3N4粉末の混合物にキレート化合物を添加してゲル状態に形成する。前記キレート化合物の例は、クエン酸、グリシン、尿素、エチレンジアミン四酢酸(EDTA)などでありうる。キレート剤の添加量は、混合物全体に対して25〜30質量%であることが好ましい。前記キレート化合物は、それぞれ1種単独で用いてもよいし、2種以上併用してもよい。
【0063】
前記キレート化合物を混合すれば、下記反応式によって反応してSr2+キレート化合物、Eu3+キレート化合物が形成される。
【0064】
前記Sr2+キレート化合物、Eu3+キレート化合物の反応経路を、アルカリ土類金属前駆体化合物としてSrCO3を、Eu前駆体化合物としてEu2O3を使用し、酸として硝酸を、キレート化合物としてクエン酸を使用した場合を例として説明すれば、次の通りである。この場合、下記反応式1のような反応が起こる。
【0065】
【化4】

【0066】
さらに詳しくは、前記Sr2+キレート化合物は、まず、SrCO3が硝酸と反応してSr2+を形成し、次いで、クエン酸と反応して形成される。
【0067】
【化5】

【0068】
このように形成されたSr2+キレート化合物は、図5で示した通りである。
【0069】
また、前記Eu3+キレート化合物も、まず、Eu2O3が硝酸と反応してEu3+を形成し、次いで、クエン酸と反応して形成される。
【0070】
【化6】

【0071】
図6は、前記のような過程で形成されたゲル状態の混合物を図式化したものである。図6において、Si3N4間に介在されたキレート化合物は、Sr2+キレート化合物及びEu3+キレート化合物がランダムに分布したことを意味する。
【0072】
次いで、前記ゲル状態の結果物を乾燥した後、1次焼成する。望ましくは、前記焼成は、300ないし700℃の空気雰囲気下で行う。焼成時間は特に限定されるものではないが、好ましくは0.5〜5時間、より好ましくは1〜5時間である。かかる1次焼成によりアルカリ土類金属キレート化合物及びEu3+キレート化合物が酸化されて、アルカリ土類金属酸化物及びEu2O3が合成される。このように生成されたアルカリ土類金属酸化物は、前記酸化時に共に発生するCO2及びH2Oガスにより生成された複数のポアを有する。
【0073】
図7は、前記反応式1の例で1次焼成過程を通じた変化を概略的に示す図面である。
【0074】
次いで、前記のように1次焼成を行って得た結果物を粉砕し、2次焼成を行う。このとき、焼成は、1300〜1700℃で行うことが好ましい。また焼成時間は、10〜100時間で行うことが好ましい。さらに焼成雰囲気は、NH3及び/またはH2/N2混合ガス雰囲気下で行うことが好ましい。H2/N2混合ガスの混合割合は、好ましくはH2:N2=0.05:1〜0.2:1である。なお、工程中の一部に前記好適な条件を具備する焼結工程が少なくとも含まれて入ればよい。かような2次焼成を行うことによって、ナイトライド化合物が得られる。
【0075】
前記NH3及び/またはH2/N2混合物ガス雰囲気下での2次焼成過程をさらに詳細に説明すれば、まず、高温でNH3またはN2は分解されて活性窒素(N*)を生成する。
【0076】
N*は、ポアを通過できる。一般的に、酸化物は、前記のようなポアを有さないため、酸化物粒子の表面積が非常に小さい。一方、本発明の蛍光体の製造過程では、ポアが生成されるため、表面積が非常に広くなる。窒化反応は、気体及び固体の反応であるため、活性表面が広いほどさらに望ましい。したがって、本発明の蛍光体の製造過程では、ポアの生成により広い活性表面を提供できるので、窒化反応に対して非常に有利である。
【0077】
前記1次焼成後に生成されたアルカリ土類金属酸化物及びEu2O3のN*との窒化反応により、アルカリ土類金属窒化物、Eu3N2(このとき、E3+は、E2+に還元される)が生成される。前述したように、前記アルカリ土類金属がSrである場合、アルカリ土類金属窒化物はSr3N2である。このように生成されたアルカリ土類金属窒化物及びEu3N2は、空気中では不安定であるが、前記本発明の蛍光体の製造方法による環境では安定している。次いで、さらなる反応によりナイトライド蛍光体が製造される。また、前記アルカリ土類金属がSrである場合の例を挙げれば、前記生成されたナイトライド蛍光体は(Sr1−xEux)2Si5N8(0<x<1)でありうる。
【0078】
図8は、これまで詳述した2次焼成過程を通じた蛍光体の形成過程をアルカリ土類金属がSrである場合の例として挙げて概略的に示す図面である。
【0079】
図9は、本発明の他の具現例による蛍光体の製造方法の概略的なフローチャートである。フローチャート中、使用される化合物および記載のない製造条件としては、上述したものと同様のものを用いることができる。
【0080】
図10は、アルカリ土類金属としてSrを使用し、酸としてクエン酸を使用した場合を例として本発明のさらに他の具現例による蛍光体の製造方法の概略的な工程図である。
【0081】
選択的に、前記のように得た結果物は、粉砕及び焼成する段階を反復して優秀な結晶性を有するナイトライド蛍光体が得られる。このとき、焼成は、望ましくは、1300〜1700℃で10〜100時間、NH3及び/またはH2/N2混合ガス雰囲気下で行える。
【0082】
次いで、前記結果物を洗浄して、最終粉末状態の蛍光体結果物が得られる。
【0083】
図11は、本発明の一具現例による(オキシ)ナイトライド蛍光体のSEM写真を示す。前記図11から分かるように、前記(オキシ)ナイトライド蛍光体は、ポアを有し、前記ポアの平均直径は、0.6μm以下であり、前記ポアの数は、単位面積(1μm2)当たり0.01以下であり、前記ポア間の平均距離は、1μm以上であり、前記ポアの断面積は、円形、楕円形、長方形、正方形、多角形などの形態を有する。
【0084】
前記本発明による蛍光体の製造方法は、特にナイトライド蛍光体の製造に有利である。すなわち、従来技術は、不安定な一部のナイトレートを前駆体として使用するところ、グローブボックスのように特別な装置の使用が要求されることと異なり、本発明による蛍光体の製造方法は、Sr,Ba,Ca,Euのそれぞれの前駆体としてSrCO3,SrO,Sr(NO3)2,SrCl2,BaCO3,BaO,Ba(NO3)2,BaCl2,CaCO3,CaO,Ca(NO3)2,CaCl2,Eu2O3,Eu(NO3)3,EuCl3のようにカーボネートまたはオキサイドなどの非常に安定な粉末を使用し、一方、Siの前駆体は、大気で安定なSi3N4を使用するので、グローブボックスのような特別な装置を要求しない。
【0085】
このように、本発明による蛍光体の製造方法は、安定な物質を出発物質として使用し、また、マイルドな工程条件で可能であるので、商業的に応用するのに非常に適している。すなわち、従来の公知のナイトライド系蛍光体の製造方法は、高温、高圧の窒素雰囲気を要求したが、前記本発明によるナイトライド蛍光体の製造方法は、それをいずれも解決した方法である。したがって、高温、高圧の工程条件を組成し、また、かかる高温、高圧の工程条件に耐えるために特別に設備された装置を要求しない。
【0086】
また、本発明によるナイトライド蛍光体の製造方法は、環境問題をもたらす物質を使用しないために環境にやさしい。
【0087】
本発明は、また、前記本発明による蛍光体の製造方法によって製造されたナイトライド蛍光体を提供する。
【実施例】
【0088】
以下、本発明を下記実施例を挙げて詳細に説明するが、本発明が下記実施例にのみ限定されるものではない。
【0089】
実施例1
SrCO3 5.0g及びEu2O3 0.06gを10質量%硝酸水溶液100cc(混合物中、1.7N)に溶解した。前記混合溶液にSi3N4 4.0gを添加した。クエン酸4.8gを前記混合溶液と混ぜて乾燥させた。前記乾燥された混合物を空気雰囲気下で700℃で1時間焼成した。焼成された混合物を、めのう乳鉢を利用して粉砕した。前記粉砕して得た粉末をペレット形態に得た後、それをアルミナるつぼに入れ、それを電気炉に入れて炭素と共にNH3雰囲気で1100℃まで加熱し(1100℃での維持時間;3時間)、その後5%のH2及び95%のN2雰囲気で1600℃まで加熱する。1600℃での焼成時間は、5時間行った。前記炭素は、ナイトライド出発物質の酸化を防止するために使われる。このように得た焼結体を粉末に粉砕し、蒸溜水で洗浄した後、オーブンで乾燥して蛍光体サンプル1(Sr0.99Eu0.01)2Si5N8を得た。
【0090】
実施例2
出発物質としてSrCO3 5.0g及びEu2O3 0.12gを10質量%硝酸100ccに溶解して使用した点を除いては、実施例1と同様に行って蛍光体サンプル2(Sr0.98Eu0.02)2Si5N8を得た。
【0091】
実施例3
出発物質としてSrCO3 5.0g及びEu2O3 0.18gを10質量%硝酸100ccに溶解した後、前記混合溶液にSi3N4 4.1gを添加して使用した点を除いては、実施例1と同様に行って蛍光体サンプル3(Sr0.97Eu0.03)2Si5N8を得た。
【0092】
実施例4
SrCO3 5.0g及びEu2O3 0.12gを10質量%硝酸水溶液100ccに溶解し、ここにSi3N4 4.0gを添加した。前記混合溶液をクエン酸4.8gと混合して得られた溶液を乾燥した。乾燥させた結果物を700℃の大気中で1時間1次焼成した。めのう乳鉢を利用して前記焼成結果物を粉砕して粉末化した。得られた粉末をペレットに製造した。前記ペレットをるつぼに入れた後、それを電気炉に位置させた。前記電気炉でカーボンと共に前記ペレットをNH3大気下で1時間1100℃まで加熱し、その後5%のH2及び95%のN2大気下で5時間1600℃まで加熱した。前記カーボンは、窒化出発物の酸化を防止するために添加した。加熱時間は1ないし60時間であり、望ましくは、3ないし50時間である。焼成結果物を粉砕して粉末化した後、得られた粉末を蒸溜水で洗浄し、オーブンで乾燥してSr1.96Eu0.04Si5O0.32N7.68の化学式を有する蛍光体を製造した。
【0093】
実施例5
SrCO3 5.0g及びEu2O3 0.06gを10質量%硝酸水溶液100ccに溶解し、ここにSi3N4 4.0gを添加した。前記混合溶液をクエン酸4.8gと混合して得られた溶液を乾燥した。乾燥させた結果物を700℃の大気中で1時間1次焼成した。めのう乳鉢を利用して前記焼成結果物を粉砕して粉末化した。得られた粉末をペレットに製造した。前記ペレットをるつぼに入れた後、それを電気炉に位置させた。前記電気炉でカーボンと共に前記ペレットをNH3大気下で1時間1100℃まで加熱し、その後5%のH2及び95%のN2大気下で5時間1600℃まで加熱した。前記カーボンは、窒化出発物の酸化を防止するために添加した。加熱時間は1ないし60時間であり、望ましくは、3ないし50時間である。焼成結果物を粉砕して粉末化した後、得られた粉末を蒸溜水で洗浄し、オーブンで乾燥してSr1.98Eu0.02Si5O0.30N7.70の化学式を有する蛍光体を製造した。
【0094】
図2は、蛍光体サンプル1の励起スペクトルを示す。UVから青色までの広い領域で光を吸収するので、本発明の蛍光体サンプルは、UV−LEDや青色LEDにいずれも適用可能である。
【0095】
図3は、蛍光体サンプル1の発光スペクトルを示す。
【0096】
図4は、サンプル1、2及び3に対する発光スペクトルを示す図面である。これから、EuのSrに対する相対的な含量が多くなるほどピーク波長が長くなることを確認した。
【産業上の利用可能性】
【0097】
本発明は、発光素子関連の技術分野に適用可能である。
【符号の説明】
【0098】
10 LEDチップ
20 金ワイヤー
30 電気リード線
40 蛍光体組成物
50 エポキシモールド層
60 成形モールド
70 エポキシドームレンズ
【特許請求の範囲】
【請求項1】
下記化学式で表示されるオキシナイトライド蛍光体:
【化1】

前記式で、
Mは、アルカリ土類金属であり、
0<x<1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8及び0<c+d≦8である。
【請求項2】
前記化学式で、Mは、Ba、SrおよびCaからなる群から選ばれる少なくとも1種である、請求項1に記載のオキシナイトライド蛍光体。
【請求項3】
前記化学式の化合物は、{Sr(1−x)Eux}aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8)である、請求項1に記載のオキシナイトライド蛍光体。
【請求項4】
下記化学式で表示され、ポアを有するナイトライド蛍光体。
【化2】

前記式で、
Mは、アルカリ土類金属であり、
0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【請求項5】
前記化学式の化合物は、{Sr(1−x)Eux}aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8)である、請求項4に記載のナイトライド蛍光体。
【請求項6】
前記化学式の化合物は、(Sr(1−x)Eux)2Si5N8(0<x≦0.1)である、請求項4に記載のナイトライド蛍光体。
【請求項7】
前記化学式の化合物は、(Sr1−xEux)2Si5N8(0<x<1)、(Sr1−xEux)1.99Si5N8(0<x<1)、(Ba1−x−ySrxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Sr1−x−yCaxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)または(Ba0.5Sr1−xCa0.5Eux)Si5N8(0<x<1)である、請求項4に記載のナイトライド蛍光体。
【請求項8】
前記ポアは、平均直径が0.6μm以下である、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項9】
前記ナイトライド蛍光体の断面1μm2当たり0.01個以下のポア個数を有する、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項10】
前記ポア間の平均距離は、1μm以上である、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項11】
前記ポアの断面は、円形、楕円形または多角形である、請求項4〜7のいずれか1項に記載のナイトライド蛍光体。
【請求項12】
UV発光ダイオードと、
請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体と、を含むことを特徴とする白色発光素子。
【請求項13】
前記UV発光ダイオードは、励起光源が紫外または近紫外線領域の電磁波である、請求項12に記載の白色発光素子。
【請求項14】
前記UV発光ダイオードの励起光源は、390ないし460nmの範囲の波長帯域を有する、請求項12に記載の白色発光素子。
【請求項15】
青色蛍光体及び緑色蛍光体から選択された一つ以上をさらに含む、請求項12に記載の白色発光素子。
【請求項16】
前記青色蛍光体は、(Sr,Ba,Ca)5(PO4)3Cl:Eu2+;BaMg2Al16O27:Eu2+;Sr4Al14O25:Eu2+;BaAl8O13:Eu2+;(Sr,Mg,Ca,Ba)5(PO4)3Cl:Eu2+;BaMgAl10O17:Eu2+及びSr2Si3O82SrCl2:Eu2+からなる群から選択された一つ以上である、請求項15に記載の白色発光素子。
【請求項17】
前記緑色蛍光体は、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+;及びBaMg2Al16O27:Eu2+,Mn2+からなる群から選択された一つ以上である、請求項15に記載の白色発光素子。
【請求項18】
前記請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体の放出スペクトルピーク波長が610ないし650nmであり、前記青色蛍光体の放出スペクトルピーク波長が440ないし460nmであり、前記緑色蛍光体の放出スペクトルピーク波長が510ないし560nmであることを特徴とする請求項15に記載の白色発光素子。
【請求項19】
青色発光ダイオードと、
前記請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体と、を含む、白色発光素子。
【請求項20】
緑色蛍光体をさらに含む、請求項19に記載の白色発光素子。
【請求項21】
前記白色発光素子は、信号灯、通信機器、ディスプレイ装置のバックライトまたは照明用である、請求項12ないし20のうちいずれか一項に記載の白色発光素子。
【請求項22】
(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、
(b)前記(a)工程で得られる混合物を乾燥及び1次焼成する工程と、
(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含むことを特徴とする蛍光体の製造方法。
【請求項23】
前記(a)工程で、前記アルカリ土類金属前駆体化合物は、BaCO3,BaO,Ba(NO3)2,BaCl2,SrCO3,SrO,Sr(NO3)2,SrCl2,CaCO3,CaO,Ca(NO3)2およびCaCl2からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項24】
前記(a)工程で、前記Eu前駆体化合物は、Eu2O3,Eu(NO3)3およびEuCl3からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項25】
前記(a)工程で、前記酸は、塩酸、硫酸、硝酸、酢酸、酪酸、パルミチン酸、シュウ酸および酒石酸からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項26】
前記(a)工程で、前記酸は、混合物中、0.1ないし10mol/lの濃度である、請求項22に記載の蛍光体の製造方法。
【請求項27】
前記(a)工程で、前記キレート化合物は、クエン酸、グリシン、尿素およびエチレンジアミン四酢酸からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項28】
前記(b)工程の1次焼成過程を空気雰囲気下で300ないし700℃で行う、請求項22に記載の蛍光体の製造方法。
【請求項29】
前記(c)工程の2次焼成過程を1300ないし1700℃で10ないし100時間の間にNH3、H2及びN2の混合ガス、またはNH3、H2及びN2の混合ガス雰囲気下で行う、請求項22に記載の蛍光体の製造方法。
【請求項30】
請求項22〜29のいずれか一項に記載の方法で製造されたナイトライド蛍光体。
【請求項1】
下記化学式で表示されるオキシナイトライド蛍光体:
【化1】

前記式で、
Mは、アルカリ土類金属であり、
0<x<1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8及び0<c+d≦8である。
【請求項2】
前記化学式で、Mは、Ba、SrおよびCaからなる群から選ばれる少なくとも1種である、請求項1に記載のオキシナイトライド蛍光体。
【請求項3】
前記化学式の化合物は、{Sr(1−x)Eux}aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0<c<8、0<d≦8)である、請求項1に記載のオキシナイトライド蛍光体。
【請求項4】
下記化学式で表示され、ポアを有するナイトライド蛍光体。
【化2】

前記式で、
Mは、アルカリ土類金属であり、
0<x<1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8及び0<c+d≦8である。
【請求項5】
前記化学式の化合物は、{Sr(1−x)Eux}aSibOcNd(0<x≦0.1、1.8<a<2.2、4.5<b<5.5、0≦c<8、0<d≦8)である、請求項4に記載のナイトライド蛍光体。
【請求項6】
前記化学式の化合物は、(Sr(1−x)Eux)2Si5N8(0<x≦0.1)である、請求項4に記載のナイトライド蛍光体。
【請求項7】
前記化学式の化合物は、(Sr1−xEux)2Si5N8(0<x<1)、(Sr1−xEux)1.99Si5N8(0<x<1)、(Ba1−x−ySrxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)、(Sr1−x−yCaxEuy)2Si5N8(0<x<1、0<y<1及び0<x+y<1)または(Ba0.5Sr1−xCa0.5Eux)Si5N8(0<x<1)である、請求項4に記載のナイトライド蛍光体。
【請求項8】
前記ポアは、平均直径が0.6μm以下である、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項9】
前記ナイトライド蛍光体の断面1μm2当たり0.01個以下のポア個数を有する、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項10】
前記ポア間の平均距離は、1μm以上である、請求項4ないし7のいずれか1項に記載のナイトライド蛍光体。
【請求項11】
前記ポアの断面は、円形、楕円形または多角形である、請求項4〜7のいずれか1項に記載のナイトライド蛍光体。
【請求項12】
UV発光ダイオードと、
請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体と、を含むことを特徴とする白色発光素子。
【請求項13】
前記UV発光ダイオードは、励起光源が紫外または近紫外線領域の電磁波である、請求項12に記載の白色発光素子。
【請求項14】
前記UV発光ダイオードの励起光源は、390ないし460nmの範囲の波長帯域を有する、請求項12に記載の白色発光素子。
【請求項15】
青色蛍光体及び緑色蛍光体から選択された一つ以上をさらに含む、請求項12に記載の白色発光素子。
【請求項16】
前記青色蛍光体は、(Sr,Ba,Ca)5(PO4)3Cl:Eu2+;BaMg2Al16O27:Eu2+;Sr4Al14O25:Eu2+;BaAl8O13:Eu2+;(Sr,Mg,Ca,Ba)5(PO4)3Cl:Eu2+;BaMgAl10O17:Eu2+及びSr2Si3O82SrCl2:Eu2+からなる群から選択された一つ以上である、請求項15に記載の白色発光素子。
【請求項17】
前記緑色蛍光体は、(Ba,Sr,Ca)2SiO4:Eu2+;Ba2MgSi2O7:Eu2+;Ba2ZnSi2O7:Eu2+;BaAl2O4:Eu2+;SrAl2O4:Eu2+;BaMgAl10O17:Eu2+,Mn2+;及びBaMg2Al16O27:Eu2+,Mn2+からなる群から選択された一つ以上である、請求項15に記載の白色発光素子。
【請求項18】
前記請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体の放出スペクトルピーク波長が610ないし650nmであり、前記青色蛍光体の放出スペクトルピーク波長が440ないし460nmであり、前記緑色蛍光体の放出スペクトルピーク波長が510ないし560nmであることを特徴とする請求項15に記載の白色発光素子。
【請求項19】
青色発光ダイオードと、
前記請求項1ないし3のうちいずれか一項に記載のオキシナイトライド蛍光体、または請求項4ないし11のうちいずれか一項に記載のナイトライド蛍光体と、を含む、白色発光素子。
【請求項20】
緑色蛍光体をさらに含む、請求項19に記載の白色発光素子。
【請求項21】
前記白色発光素子は、信号灯、通信機器、ディスプレイ装置のバックライトまたは照明用である、請求項12ないし20のうちいずれか一項に記載の白色発光素子。
【請求項22】
(a)アルカリ土類金属前駆体化合物、Eu前駆体化合物、酸、Si3N4粉末及びキレート化合物の混合物をゲル状態に形成する工程と、
(b)前記(a)工程で得られる混合物を乾燥及び1次焼成する工程と、
(c)前記(b)工程の結果物を粉砕及び2次焼成する工程と、を含むことを特徴とする蛍光体の製造方法。
【請求項23】
前記(a)工程で、前記アルカリ土類金属前駆体化合物は、BaCO3,BaO,Ba(NO3)2,BaCl2,SrCO3,SrO,Sr(NO3)2,SrCl2,CaCO3,CaO,Ca(NO3)2およびCaCl2からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項24】
前記(a)工程で、前記Eu前駆体化合物は、Eu2O3,Eu(NO3)3およびEuCl3からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項25】
前記(a)工程で、前記酸は、塩酸、硫酸、硝酸、酢酸、酪酸、パルミチン酸、シュウ酸および酒石酸からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項26】
前記(a)工程で、前記酸は、混合物中、0.1ないし10mol/lの濃度である、請求項22に記載の蛍光体の製造方法。
【請求項27】
前記(a)工程で、前記キレート化合物は、クエン酸、グリシン、尿素およびエチレンジアミン四酢酸からなる群から選ばれる少なくとも1種である、請求項22に記載の蛍光体の製造方法。
【請求項28】
前記(b)工程の1次焼成過程を空気雰囲気下で300ないし700℃で行う、請求項22に記載の蛍光体の製造方法。
【請求項29】
前記(c)工程の2次焼成過程を1300ないし1700℃で10ないし100時間の間にNH3、H2及びN2の混合ガス、またはNH3、H2及びN2の混合ガス雰囲気下で行う、請求項22に記載の蛍光体の製造方法。
【請求項30】
請求項22〜29のいずれか一項に記載の方法で製造されたナイトライド蛍光体。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【公開番号】特開2009−287027(P2009−287027A)
【公開日】平成21年12月10日(2009.12.10)
【国際特許分類】
【出願番号】特願2009−132554(P2009−132554)
【出願日】平成21年6月1日(2009.6.1)
【出願人】(591003770)三星電機株式会社 (982)
【Fターム(参考)】
【公開日】平成21年12月10日(2009.12.10)
【国際特許分類】
【出願日】平成21年6月1日(2009.6.1)
【出願人】(591003770)三星電機株式会社 (982)
【Fターム(参考)】
[ Back to top ]

