1つの画像データからの解剖学的構造を含む対象物のモデルの領域を、診断的又は治療的介入に用いられる画像にマッピングするための方法、そのシステム及びコンピューター読み取り可能な媒体
プランニング画像における解剖学的構造を含む対象物のモデル、及びその中の介入標的領域を、介入がガイドする画像データにマッピング(写影)するための、方法、システム及びコンピューター読み取り可能な媒体を開示する。一つの方法によると、解剖学的構造を含む対象物の初期内側表現(メディアルリプレゼンテーション)対象物モデル(m-rep)は、対象物の少なくとも第1事例の画像データに基づいて作り出される。対象物の少なくとも第2事例は患者と結びつくが、この少なくとも第2事例のプランニング画像データに基づいて初期m−repを変形して、患者に特異的m−repが作り出される。m−rep内の介入標的領域はプランニング画像に記録された画像内に特定される。患者特異的m−repは、プランニング画像から変形した対象物の少なくとも第2事例の介入がガイドする画像データと関係づけられる。プランニング画像におけるm−rep、及び介入がガイドする画像におけるm−repの間の変換に従い、介入標的領域は、介入がガイドする画像に送られる。
【発明の詳細な説明】
【技術分野】
【0001】
この特許出願は、2007年10月18日に出願された米国仮特許出願60/999,420、及び2008年8月7日に出願された米国仮特許出願61/087,026に基づく優先権を有し、そこに記載された内容は本明細書に取り込まれている。
この発明完成に関与する幾つかの仕事は米国NCI及びNIBIB助成金P01 EB002779により支援された。従って、米国政府は本発明について一定の権利を有する。
本明細書に記載される発明は、医学的画像セグメンテーション(分節)及び解析に関し、より詳細には、診断的又は治療的介入に用いられる画像に用意されている1つの画像データから、対象物のモデル(模型)における解剖学的構造を含む領域をマッピング(写影)する方法、システム及びコンピューター読み取り可能な媒体に関する。
【背景技術】
【0002】
前立腺癌(CaP)は、米国における主要な健康問題であり、2005年には240,000診断例及び30,000死亡例がある。前立腺癌は、米国男性人口の非皮膚性癌の全新規発生率の33%を占めており、全非皮膚性癌の中で最大の発生率であり、毎年の死亡率は、結果的に肺/気管支癌に次いで第2位である。前立腺癌の広がり及び深刻な結果により、米国の130〜150万人の患者は、通常バイオプシ(biopsy、生検)を伴う、経直腸的超音波断層イメージング(TRUS)によりガイドされた前立腺介入処置を毎年受ける。他の処置としては、放射性シードの挿入(ブラキ療法−小線源療法)及び組織を凍結又は加熱する方法による組織切除がある。
【0003】
バイオプシの間、小ゲージの中空の注射針を前立腺に導入し、TRUSの視覚的誘導の下にコア組織試料を集める。TRUSは前立腺の全体の形態を良く示すが、大きな短所として、前立腺内の正常及び癌組織を区別することができない。この限界があるので、全ての患者に適用される所定のグリッドパターン(格子模様)に基づいて組織試料を集める。不幸なことに、このアプローチの偽陰性率は高い(約25〜30%)。さらに、バイオプシが陽性の場合においてすら、腫瘍が不完全にサンプリングされるかも知れず、誤って低いGleasonスコア(腫瘍グレード)を導き、また恐らく不適切な治療決定を導く。偽陰性の結果、多年にわたる多数回繰り返すバイオプシがおこなわれ、増殖を続け恐らく転移可能性のある癌が見逃され、かつ患者に不安が生まれる。これらの誤診は著しく患者のクオリティオブライフ(QOL、生活の質)に影響を与え、医療保険負担及び医療費に影響を与える。
【0004】
経直腸的超音波断層イメージング(TRUS)がガイドするバイオプシには、医師が癌の疑いのある前立腺内部の組織から充分正確にバイオプシ試料を取り出すことができないという問題がある。これらの問題を克服するために、画像セグメンテーション(分節化)を用いて、解剖学的対象物及び解剖学的構造の潜在的癌部位のような、解剖学的対象物の中の介入標的領域を特定してもよい。ここで用いるように、"画像セグメンテーション"は、医学的処置に関わる解剖学的実体を見出すために、デジタル画像を領域(即ち、ヴォクセル又はピクセル)に区分する過程を表す。画像セグメンテーションを用いて、磁気共鳴画像(MRI)及びコンピューター断層撮影(CT)に限らず、様々な種類の医学的画像に表れる対象物及び境界(線、曲線、その他)を探し出すことができる。
【0005】
従って、画像を分節化することは、画像を様々な領域に分けることであり、ここで対象物領域又は諸領域の内部及び外部に位置するヴォクセルは、色、強度、又はテクスチャーのような幾つかの特徴又は性質に関するアトラス(地図帳)における対応する位置(即ち、症例内のばらつきに関する情報を備えた可能性を有する鋳型(テンプレート)画像)に似ている。画像セグメンテーションにおける見せかけの情報の使用に加えて、モデルをベースとした分節化は、検討すべき対象物(即ち、器官、腫瘍その他)が、繰り返しのあるジオメトリー(幾何学的配列)を有すると仮定し、従って、対象物のモデルを作成し、用いて、画像のセグメンテーション上に確率的制約を課すことができて、それにより精度が増す。
【0006】
前立腺癌スクリーニング及び治療を含む医学的目的のために、画像セグメンテーションを行うために用いることができる2つの画像例は、磁気共鳴画像(MRI)及び超音波(US)画像である。バイオプシのために針を向けること、又は治療用に放射性シードの挿入のような、重大な治療計画及び治療開始の決定を助けるために、人は、このような画像から、患者内部の解剖学的構造のジオメトリックモデル(幾何学的な模型)を抽出できる。しかしながら、臨床的処置を導くために用いる超音波画像から対象物モデルを抽出するための現在の方法、及び処置を計画するために用いられるMRIのような画像からの抽出でさえ、熟練した人とのやりとりを必要とし、従って非常に時間を要し、高価である。さらに、同様な訓練を受けた熟練者でさえ、人は臨床的決定に不利に影響する使用者内及び使用者間のばらつきを示すことが知られている。
【0007】
バイオプシのような介入を計画するために用いられる幾つかの画像は、前立腺のような、検討すべき対象物の情報ばかりではなく、介入標的領域が対象物内の何処に位置しているかの情報も含む。あるいは、検討すべき対象物、及び介入の位置を示す画像に完全に記録された別々の画像を得ることができるかも知れない。最近の研究によると、MR画像と同時に得られ、また完全に記録された磁気共鳴分光画像(MRSI)は、前立腺癌が疑われる前立腺内部の領域、即ち介入標的領域、を高感度に検出することができる。
【発明の概要】
【発明が解決しようとする課題】
【0008】
不幸なことに、日常的にバイオプシや治療処置を、一定の癌の疑いがあることを示す、画像の直接の視覚的ガイダンス(誘導)の下に行うことは非現実的である。その理由は、このようなガイダンス(誘導)は、経直腸的超音波断層イメージング(TRUS)のようなリアルタイム画像技術を必要とするが、これらは解剖学的対象物を示すが、一定の疾患の疑いについての情報を与えないからである。
従ってこれらの困難を考慮して、介入標的領域由来の画像から、介入標的領域を、介入がガイドする画像に移動させるための、改良された方法、システム、コンピューター読み取り可能な媒体を望む要求が存在する。この要求は、診断的又は治療的介入をガイドするために用いられる画像データに、(プランニング画像に由来する)解剖学的構造を含む対象物のモデルを、マッピング(写影)することにより充足される。
【課題を解決するための手段】
【0009】
プランニング画像から分節化された解剖学的構造を含む対象物のモデルを、対象物が導かれるとは異なる種類の介入がガイドする(導く)画像にマッピング(写影)するための;及びその結果、対象物に含まれる領域を、介入がガイドする画像にマッピングするための;方法、システム及びコンピューター読み取り可能な媒体を開示する。一つの方法によると、解剖学的構造を含む対象物の初期内側表現(メディアルリプレゼンテーション;medial representation)対象物モデル(m-rep)は、対象物の少なくとも第1事例の画像データに基づいて作り出される。対象物の少なくとも第2事例は患者と結びつくが、この少なくとも第2事例のプランニング画像データに基づいて初期m−repを変形して、及びプランニング画像データに記録した介入標的領域を特定して、患者に特異的m−repが作り出される。患者特異的m−repは、対象物の少なくとも第2事例の介入がガイドする画像データと関係づけられるが、対象物の少なくとも第2事例は、プランニング画像データにおける対象物の状態から変形したものである。プランニング画像データにおけるm−rep、及び介入がガイドする画像データにおけるm−rep、の両者の間の変換に由来するマッピングにより、介入標的領域は、特定できる。
【0010】
解剖学的構造を含む対象物のモデルを、介入がガイドする画像データにマッピングするためのシステムもまた開示する。このシステムは、対象物のプランニング画像データに基づく解剖学的構造を含む対象物の内側表現対象物モデル(m−rep)を作り出す対象物モデルジェネレーター(生成系)を含む。次に、ある対象物モデル変形及びマッピングモジュール(要素)は、対象物の介入がガイドする画像に対するm−repと関係づけられる。
【0011】
一つの態様によると、このシステムは、対象物の無数の事例の画像データに由来する確率的情報を含むことができて、各々は異なる患者個人(患者間確率的情報)、及び同一個人の無数の画像データの事例に由来する確率的情報(患者内確率的情報)である。ある患者特異的内側表現対象物モデル(m−rep)は、ある患者に対するプランニング画像データの少なくとも一部に基づくが、ここで画像データの少なくとも一部は、前立腺のような、対象物の種類と関連する。他の個人に由来する確率的情報を用いて、この患者に対するプランニング画像に当てはめられたm−rep、即ちこの患者特異的m−rep、を得ることができる。介入の際、介入がガイドする画像が、同じ器官について得られ、また患者内確率的情報を用いて、この患者特異的m−repは変形されて介入がガイドする画像になる。この変形は、対象物内の介入標的領域に適用される。バイオプシのために、バイオプシ針をガイドして、対象物内の介入標的領域から組織試料を取り出す。このガイダンスは、介入がガイドする画像データ上に重ね合わされた介入標的領域の表示により行われる。
【0012】
他の態様により、このm−repの対象物の介入がガイドする画像データへの変形は、ある目的関数の最適化を含むが、その目的関数は、このm−repを介入がガイドする画像データに関係づける成分を含む。
【0013】
本明細書で用いられる用語"対象物"はモデル化することを希望する解剖学的構造のような、実世界の構造を示す。例えば、対象物としては、腎臓、心臓、肺、膀胱及び前立腺を含むことができる。
【0014】
用語"介入標的領域"は、疾病が疑われマークされている領域又は治療の標的のような、医療介入のための標的を示す。
【0015】
用語"対象物画像データ"は、対象物からセンサーにより集められ、コンピューター上に保存された一組のデータを示す。対象物画像データの例としては、CT走査データ;MRIデータ;X−線データ;デジタル写真;又は、一組のピクセル強度及び位置で表すことができる、実世界から集められたあらゆる他の種類のデータ;を含む。
【0016】
本明細書で用いられる用語"メディアルアトム(medial atom、内側の原子)"は、お互い、及びモデル中の1又は2以上の中心軸に関して、所定の関係を有するベクトルの位置及び集積を示す。メディアルアトムは、互いにグループ化してモデルを形成することができる。例えば、格子の成分がメディアルアトムと呼ばれる、空間的に正則格子から、メディアルマニホールド(内部多様体)をサンプリング抽出することができる。
【0017】
本明細書で用いられる用語"メディアルアクシス(medial axis、中心軸)"は、あるモデルの反対側の表面上の接点から等距離の一組のポイント(地点)を示し、表面上の接点から直行直線の交差点に位置する。
【0018】
本明細書で用いられる用語"対象物モデル"は、表面、内部及び形態的ばらつきを含むが、それらに制限されない、対象物の数学的表現を示す。
【0019】
本明細書で用いられる用語"m−rep"は、対象物又は対象物画像データのメディアルアトム表現を示す。あるm−repは、一組の連結した連続メディアルマニホールドとして、幾何学的な対象物を表す、Riemannian空間内の対象物のジオメトリーの明示的な数学的表現(即ちモデル)である。3D対象物に対して、対象物の内部にあり、また2又は3以上の点において対象物の境界に接する全ての球体の中心により、これらのメディアルマニホールドを作ることができる。このメディアルの記載は、内接する球体の中心、及び球体中心から対象物境界上の2個のそれぞれの接点に向かう、「スポーク」と呼ばれる、対応するベクトルにより定義される。対象物の表面境界を表現することに加えて、m−repは、局部の位置、配向、及びサイズに関して内部の対象物を表すことができて、また単一形状又は多数のフィギュア(形状)を含むことができることは評価される。また、あるm−repを、対象物をベースとした座標システム、即ち、作成している対象画像データの対象物の座標システム、において定義することができる。
【0020】
本明細書で用いられる用語"フィギュア(figure、形状)"は、モデルの成分又は下位成分を表す。あるメディアルマニホールドの各連続セグメント(部分)は、メディアルフィギュアを表す。例えば、幾つかのモデルは、単一フィギュアだけを有することができる。単一フィギュアで代表することができる対象物の例は、腎臓のように、比較的単純な形態を持つ対象物である。正確なモデリング(モデル(模型)を組み立てること)のために多数のフィギュアを必要とする対象物の例は、ヒトの手である。メディアルアトムをベースとした手のモデルは、手の掌からなる主要なフィギュア及び手の各指からなる下位フィギュアを含むことができる。
【0021】
本明細書で用いられる用語"ヴォクセル(voxel)"は、3D空間での規則的グリッド上のある値を表す体積(ボリューム)成分を示す。
【0022】
介入がガイドする対象物画像データに解剖学的構造を含む対象物のプランニング画像をマッピングするために、またそれによりプランニング画像に記録した介入標的領域を、介入がガイドする画像に送るために、本発明を、コンピュータープログラム製品を用いて実行することができるが、このコンピュータープログラム製品は、コンピューターが実行できる指令を含み、この指令は、コンピュータープロセッサー(処理装置)により行われる具体的なコンピューターが読み取り可能な媒体に埋め込まれている。本発明を実行する上で適切な、典型的コンピューター読み取り可能媒体には、ディスク記憶装置、プログラム可能な論理装置、及び応用に特異的な集積回路が含まれる。ある実行において、コンピューター読み取り可能な媒体として、処理装置がアクセス可能なメモリー(記憶装置)を含むことができる。このメモリーは、本明細書に記載した要求を探し出すための全ての方法を実行するために、処理装置により実行可能な指令を含むことができる。さらに、本発明を実行するコンピューター読み取り可能な媒体は、多数の物理的装置及び/又は計算プラットフォームを通して配布することができる。
【図面の簡単な説明】
【0023】
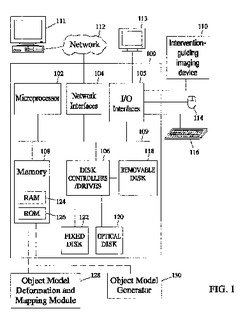
【図1】一般目的の計算プラットフォームのブロックダイアグラム(概略ブロック図)を示す図である。本発明の実施態様に従い、一部の方法とシステムをその一般目的の計算プラットフォーム上で実行することにより、モデル及び介入標的領域は、介入がガイドする画像に変換される。
【図2】本発明の実施態様に従い、MR/MRS画像データをTRUS画像にマッピングする典型的過程を示すフローチャートを示す図である。
【図3】本発明の実施態様に従い、それぞれ、熟練者が作成した膀胱及び前立腺の境界を描写する一対の分節化したCT画像を示す図である。
【図4】本発明の実施態様に従い、あるm−rep対象物モデルの3次元表現を示す図である。
【図5】本発明の実施態様に従い、画像強度値をサンプリングするために適切なCT画像における前立腺の3直交性表現を示す図である。
【図6】本発明の実施態様に従い、RIQF解析が実行される前及び後の、典型的m−rep対象物モデルの表現を示す図である。
【図7】本発明の実施態様に従い、膀胱に当てはめたRIQF画像の様々な統計的指標の連続したプロットを示す図である。
【図8】本発明の実施態様に従い、様々な方法を用いて作成した前立腺境界を描写する一連の典型的なTRUS画像を示す図である。
【図9A】本発明の実施態様に従い、膀胱及び前立腺表面の表現を示す図である。
【図9B】本発明の実施態様に従い、超音波走査における膀胱及び前立腺の正中矢状面の切片を示す図である。
【図10A】本発明の実施態様に従い、膀胱の表面表現を示す図である。
【図10B】本発明の実施態様に従い、熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、膀胱の表現を示す図である。
【図10C】本発明の実施態様に従い、コンピューターをベースとしたセグメンテーションを示す膀胱の正軸性(ミッドアクシアル;midaxial)切片を示す図である。
【図11A】本発明の実施態様に従い、熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、前立腺の3次元表現を示す図である。
【図11B】本発明の実施態様に従い、コンピューターをベースとしたセグメンテーションを示すCT走査における前立腺の切片を示す図である。
【図12】熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、前立腺の3次元表現を示す図である。
【図13】本発明の実施態様に従い、画像当て嵌の様々な統計的指標を描写する連続したプロットを示す図である。
【図14】本発明の実施態様に従い、ヒトが生成したコントゥア(輪郭)に当てはめた複数のm−repから計算した2個の初期固有モード(様式)からの一連の試料を示す図である。
【図15】本発明の実施態様に従い、男性骨盤ファントム(模型)のCT走査を示す図である。
【図16】本発明の実施態様に従い、バイオプシ処置過程において、医師の針をガイドするために、前立腺のTRUS画像に重ね合わせた3Dm−repモデルの典型的表示を示す図である。
【図17】本発明の実施態様に従い、プランニング画像データから解剖学的構造を含む対象物を、介入がガイドする画像データに、マッピングさせる典型的システムを示す図である。
【発明を実施するための最良の形態】
【0024】
本発明は、プランニング画像における解剖学的構造を含む対象物を;及びプランニング画像に記録した画像由来の介入標的領域を;対象物を示す介入がガイドする画像データにマッピングするための方法及びシステムを含む。本発明の方法及びシステムを、ハードウェア、ファームウェア、ソフトウェア又はこれらの全ての組合せにおいて実行することができる。1つの典型的実施態様において、プランニング画像における解剖学的構造を含む対象物モデルを、介入がガイドする画像データにマッピングするための、対象物モデリングを行うこの方法及びシステムを、一般目的のコンピューター上で実行するように適合させた応用ソフトウェアとして実行できる。図1は、本発明の実施態様に従い、プランニング画像における解剖学的構造を含む対象物モデルを、介入がガイドする画像データにマッピングするための、この方法及びシステムのための典型的操作環境を描写する。図1を参照すると、コンピューター100は、バス(母線)109に接続したマイクロプロセッサー(超小型演算装置)102,ネットワークインターフェース104,I/Oインターフェース105,ディスクコントローラー/ドライブ106,及びメモリー108を含む。従って、コンピューター100は、例えば検討すべき解剖学的対象物の画像データを受けとるために、I/Oインターフェース105を経由して介入がガイドするイメージング装置110に接続できる。
【0025】
マイクロプロセッサー102は、応用ソフトウェアの実行に適切な全ての種類の一般目的用の演算装置であることができる。本発明の実施態様の使用のために適した典型的なマイクロプロセッサーは、Intel(R)会社から入手できるいずれのPentium(R)ファミリーのプロセッサーでもよい。
【0026】
ネットワークインターフェース104は、ネットワーク112を経由して1又は2以上の遠隔のコンピューター111と連絡する1又は2以上のネットワークアダプターカードを含むことができる。例えば、ネットワークインターフェース104は、Ethernet又はATMカードであることができる。
【0027】
I/Oインターフェース105は、ディスプレイデバイス(表示装置)113,マウス114及びキーボード116のような、外部デバイスと連絡する直列ポートを提供できる。I/Oインターフェース105は、またマイクロホン及びスピーカーのような、他の種類の入力及び出力デバイスのためのインターフェースを含むことができる。
【0028】
ディスクコントローラー/ドライブ106は、取りだし可能ディスク118,光学ディスク120及び固定ディスク122のような、記憶装置の読み、書きのためのハードウェア部品を含むことができる。
【0029】
メモリー(記憶装置)108は、マイクロプロセッサー102により実行される指令を記憶するために、ランダムアクセスメモリー124及び読み出し専用メモリー126を含むことができる。本発明に従い、メモリー108は、対象物モデルを変形して対象物の特定の例に当てはめ、及び対象物モデルを対象物の1又は2以上の超音波画像にマッピングするために、ソフトウェア128の特定の例を記憶し、及び対象物の高分解画像データに基づく解剖学的構造を含む対象物の内部表現対象物モデルを作成するために、対象物モデルジェネレーター130の一例を記憶することができる。ソフトウェア128及び130は、Windows(R)オペレーティングシステムの下で現代のPC上で走行できる。又、ソフトウェア128及び130は、自動的にメディアルアトムモデルを変形して、画像データに変えることができて、その後介入標的領域を介入がガイドする画像に送ることができる。ソフトウェア128及び130により行うことができる典型的操作を以下により詳細に記載する。
【0030】
発明の概要
本発明の1態様により、対象物モデルを、標的画像に自動的に埋め込み;対応する標的対象物に厳格に記録し;その後変形して特定の標的対象物の形態に密接に適合させることができる。図2は、本発明の実施態様に従い、外科処置の際医師のバイオプシ針をガイドするために、対象物のプランニング画像に基づいて、前立腺の、患者特異的で、統計的に調整可能(トレイナブル)で、変形可能である、形態モデルを作り出し;及びプランニング画像に記録した画像から介入標的領域を作りだし;及び対象物モデル、従ってこの介入標的領域、を一連の介入がガイドする画像にマッピングする;典型的な過程のフローチャートである。図2を参照すると、ブロック200において解剖学的構造を含む対象物の初期内側表現対象物モデル(m−rep)は、対象物の少なくとも第1事例の画像データに基づいて作成される。対象物モデルは、対象物のその種類に対して一般的であるが、後にその対象物(例えば、患者)の特定の事例に対して、特注作成することができる。あるm−repは対象物の1又は2以上のバイオプシ前画像(例えば、MR,CT,その他)に基づいて作られる。例えば、医師は、存在する全ての小結節を含む、前立腺の詳細なジオメトリーを示すバイオプシ前のMR画像を得ることができる。更に、前立腺モデルに相対的な領域の、前立腺の形態の確率分布及び画像強度パターンを得ることができる。
【0031】
ブロック202において、患者特異的m−repは、対象物の少なくとも第2事例のプランニング画像データに基づき、初期m−repを変形することにより作られるが、ここで対象物の少なくとも第2事例は患者に関係する。例えば、前立腺形態の患者特異的アトラスは、恐らく、画像強度が関係する統計的調整(トレイニング)方法の使用と組み合わせて、プランニング画像のピクセル強度を解析することにより作り出すことができる。また、介入標的領域は、プランニング画像から抽出される;又はプランニング画像に完全に記録され、また介入標的領域についての情報を表現する他の画像から抽出される。
【0032】
ブロック204において、この患者特異的m−repは、プランニング画像から変形した対象物の少なくとも第2事例の介入がガイドする画像データと関係する;及び介入標的領域は、誘導されたm−rep変形を用いた介入がガイドする画像データにマッピングされる。例えば、対象物の境界/輪郭は、超音波画像において正確に定義することができる;及び、癌の可能性がある、又は他の疾患が疑われる領域のような、対象物内の介入標的領域を、プランニング画像から、介入がガイドする画像に送ることができるが、この際プランニング画像における患者特異的m−rep、及び介入がガイドする画像における患者特異的モデルとの間の関係を用いて送る。バイオプシ応用(例えば、医師が標的領域を通した、針の軌跡(トラジェクトリー;trajectory)を計画し、実行させることを可能にすること)に加えて、変形した対象物モデルを用いて、対象物の非―超音波画像を対象物の超音波画像にマッピングすることは、治療上の及び/又は他の診断上の使用にも可能である。確率的分布によって導かれた最適過程により、相関関係を得ることができること;及び検討すべき解剖学的対象物の解剖学的モデルと関係して、前立腺形態の変化、及びプランニングの基本的特徴と介入がガイドする画像技術の間の差異、及び各々の確率分布に気を配ることができること;は評価できる。
【0033】
さらに、対象物モデル、及び介入標的領域は、同時に表示できて、また外科的処置の際に医師をガイドするために、対象物の介入がガイドする画像と重ね合わせることができる。例えば、前立腺バイオプシの間に、正確に針を配置するために、m−rep及び介入標的領域を、前立腺のTRUS画像上にマッピングし、また重ね合わすことができる。
【0034】
他の態様によると、本発明は、患者特異的m−repをTRUS画像にマッピングするための目的関数に表れる、画像位置合わせ項のテクスチャー解析に基づく方法を含む。
【0035】
他の態様によると、MR/MRS及びTRUSデータセットの間の変形可能なマッピングを可能にするために、本発明は、MR/MRSイメージング及びTRUSイメージングの間の患者内変形についての統計を作成する方法;及び前立腺/嫌疑体積モデルに相対的なTRUS画像強度及びテクスチャーを表現する方法;を含む。これらの態様の各々を、今や、より詳細に記載する。
【0036】
初期M−rep対象物モデルの作成
対象物の画像データ
上述のように、様々な種類の対象物は、異なった種類のデジタル画像で表現できる。これらの画像は、MRI,MRSI及びCT画像のような、プランニング画像を含むことができる;又は超音波画像(例えばTRUS)のような介入がガイドする画像であることもできる。デジタル画像に表現される、異なる解剖学的対象物の境界を正確に特定するための一つの方法は、マニュアル(手作業)2D画像セグメンテーションを含み、このセグメンテーションでは、熟練者が、画像の各切片に表現される対象物の境界を決定する。
【0037】
画像セグメンテーションにより2D画像における対象物の境界の特定に加えて、対象物ジオメトリーの異なる特徴を捕捉する対象物の複数の画像を用いて、対象物の3Dモデルを作ることができる。例えば、異なる患者から得た前立腺の画像、異なる時間に得た個々の患者の前立腺画像、異なる角度から得た前立腺の画像、及び/又は異なるイメージング技術を用いて得た前立腺の画像を用いて、前立腺の3Dモデルを作ることができる。以下により詳細に記載する様に、モデルをベースとする方法は、外観をベースとしたモデル、解剖が知らせるモデル、機械的モデル、統計的モデル、及びこれらの組合せに分けることができる。
【0038】
対象物モデルの作成に適したある種類のデジタル画像の一例は、磁気共鳴画像(MRI)である。対象物の画像表現を作成するために、電磁場を用いて体中の原子の核磁化を並べることにより、MRIは生み出される。初期配列の後に、ラジオ周波数場を用いて、スキャナ(走査器)により検知可能な回転磁場を対象物中の核に引き起こし、システマティックにこの配列を変化させることができる。充分な情報を作り出して、対象物の画像を再構成するために、追加的な磁場を用いて、さらに配列を動かすことができる。例えば、MRIスキャナー内に人が横たわる時、水素核(例えばプロトン)は、強い主磁場に沿って並ぶことができる。主磁場に垂直に、ラジオ周波数で振動する第2の電磁場を、パルスして、幾つかのプロトンを主磁場に沿った並びから外すことができる。これらのプロトンが主磁場に沿った並びにドリフトバックする時、これらのプロトンは、検出可能なラジオ周波数信号を発信する。身体の異なる組織のプロトン(例えば、筋肉に対する脂肪)は、異なる速度で再配列するので、身体の異なる構造を、MRIに示すことができる。
【0039】
MRIに類似して、磁気共鳴分光イメージング(MRSI)を画像データとして用いることができて、ここから癌の疑いのレベルを知ることができる。MRSIを分光学及びイメージング法と組み合わせて、対象物の中から空間的に局在するスペクトルを作ることができる。例えば、磁気共鳴分光を用いて、体組織中の異なる代謝物のレベルを測定することができる。MRシグナルは"励起した"同位体の異なる分子配置に対応する共鳴スペクトル作ることができるので、共鳴スペクトル標識を測定することができて、また様々な疾患の診断又は治療計画をするために用いることができる。
【0040】
本発明に従い対象物モデルを作成するために適したデジタル画像の第3番目の典型的な種類の例は、コンピューター断層撮影(CT)画像である。従来型のCTイメージングとしては、回転軸の周りから取り込まれた複数の2次元(2D)X線画像から、対象物の3次元(3D)画像を作り出すためのデジタルジオメトリープロセッシングの使用がある。しかしながら、他の種類のCTイメージングとして、本発明の範囲を離れることなく、ダイナミックボリュームCT,アクシアル(断層)CT、シネCT,ヘリカル/スパイラルCT,デジタル再構成写真(DRR)CT,電子ビームCT,多切片CT,デュアル線源CT,インバースジオメトリーCT,末梢定量的コンピューター断層撮影(pQCT),シンクロトロンX線断層撮影顕微鏡、及びX線CTがあり、これらに制限されないことを評価する。
【0041】
図3A及び3Bは、本発明の実施態様に従い、それぞれ、熟練者が作成した膀胱と前立腺の境界を描写する一対の分節化したCT画像である。図3Aを参照すると、境界300は、例えば、画像におけるピクセル強度の目視検査により医師が決定したヒト男性の膀胱の境界に対応することができる。同様に、図3Bにおいて、境界302は、画像におけるピクセル強度パターンに基づくヒト男性の前立腺の境界である。図3A及び3Bに描写したマニュアル2Dセグメンテーションは、3D領域を提供することができるが、この3D領域に、モデルが当てはめられ、及び更に、解剖学的形態の形態上で、及び対象物に関連した画像情報上で、確率分布を学習する過程でさらに用いられることができる;あるいはそれは標的又はゴールを表すことができて、この標的又はゴールは、ゆっくりした煩雑なマニュアル法で為し遂げることができるが、同様に(又はより正確でさえあるが)自動化した画像処理を用いて;及び本明細書に記載する統計的対象物モデリング法を用いて;為し遂げることができるものである。従って本明細書に記載した、プランニング及び介入がガイドする解剖学的構造のデジタル画像を分節化するための方法の精度の指標としては、画像フィッティング(当てはめ)解析、又は図3A及び図3Bに示すような、熟練者が作成したマニュアルセグメンテーションとの比較が含まれる。
【0042】
対象物モデルの作成
2D画像において、対象物の2D境界を決定することに加えて、対象物の複数の2D画像を用いて対象物の3Dモデルを作成することができる。従って、既に紹介した1又は2以上の高分解能デジタル画像を用いて、初期対象物モデルを作成することができる。以下により詳細に記載するように、対象物モデルを、様々な方法に従って作成することができる。しかしながら、これら全ての方法のゴールは、形態及び対象物の可能な形態変化の最も正確な記述(表面及び体積)を作り出すことである。
【0043】
良い−静止モデル
対象物の静止モデルは、対象物の数学的表現であり、ここで、モデルの各部分の関係は、他の部分との関係で変化しない(即ち、変形しない)。
しかしながら、(前立腺のような)解剖学的対象物は、長時間にわたってめったに同一の形態及びサイズではない(静止してない)ので、もしこのような対象物の正確なモデルを提供することを望むのであれば、解剖学的対象物のモデルは、静止であるべきでない。
【0044】
より良い−変形可能形態モデル
変形可能形態モデル(DSM)は、解剖学的構造を含む対象物の形態、及び形態的ばらつきの両者の表現である。しかしながら、DSMのカテゴリーの中で、m−repと呼ばれる特別な部類のDSMは、前立腺のような解剖学的対象物と結びついた特定のジオメトリーを最も良く表現することができる。
【0045】
上述のように、"m−rep"は、一組の連結した連続メディアルマニホールドを用いた対象物のジオメトリーの明示的な数学的表現(即ち、モデル)である、メディアルアクシス(中心軸)表現対象物モデルを示し、ここでメディアルマニホールドの各連続セグメントはメディアル(内部)形状を表す。このメディアルマニホールドは、空間的に正則格子からサンプリングできて、ここでこの格子の成分はメディアルアトムと呼ばれる。この格子は、2Dメッシュの形であることができて、又は各々1サイクルのスポークからなるアトムの1D鎖であることもできる。結果として、m−repは解剖学的対象物の幾何学的ばらつきの有効なパラメーター化であり、またそれにより、画像セグメンテーションの際の形態的な制約を提供することができる。
【0046】
図4は、本発明の実施態様に従い、m−rep対象物モデルの3次元表現である。図4を参照すると、メディアルジオメトリーは中心及び幅の観点から対象物を記載できる。ある3D対象物(例えば、前立腺)を、対象物の対向表面の間の途中に横たわる2D湾曲型のシート、及びシートの両サイドから対象物の境界まで達するスポークにより表すことができる。ハブ(hub)と呼ばれる、メディアルシート上の位置、及び2本のスポークは、メディアルアトムと呼ばれる。従って、m−repを用いて、完全な対象物表面を、アトムスポーク端から再現することができる。
【0047】
図4において、ハブ400を、2D湾曲表面402及び404と、それぞれスポーク406及び408を経由して接続することができる、またこれらを合わせてm−rep410を表わす。複数のm−rep410を連結して、対象物412のような対象物の体積のあるジオメトリーを作ることができる。最後に対象物の表面を示すために、ワイアメッシュ(金網)414を、m−repモデル412に適用できる。m−repのより詳細な考察及びm−rep作成過程は、本明細書に参考文献としてその全体を取り込んだ、US特許番号7,200,251に含まれる。
【0048】
上記のように、初期m−repが、対象物の1又は2以上の高分解能デジタル画像を用いて作られた後、対象物のジオメトリー及び/又は対象物を様々な条件下で変形できる方法をより正確に表すために、このm−repは、統計的調整を受ける。一連の変形及び統計的計算によるm−rep調整の過程については、以下により詳しく記載する。
【0049】
DSM−外観をベースとした
外観モデルは、ジオメトリックモデルと関連して取得された場所における画像を記載する。セグメンテーションに用いられる外観モデルは、画像強度値に基づく。例えば、ヴォクセル目録(リスト)及び局所的な強度変位値関数(RIQF)法は、画像強度をベースとした画像セグメンテーション法である。RIQF構成要素は、対象物の特定領域の強度の累積ヒストグラム(度数分布)の逆関数を表す。RIQFはこのような構成要素により作ることができる。各構成要素は、例えば、1D配列の変位値関数値であり、この各値は、与えられた変位値に対する強度値である。例えば、CT又は超音波のような、画像における単一強度ような;又は、ある種のMR画像のような、複数の強度画像において測定される複数の強度のような;異なる強度に各構成要素は対応することができる。さらに、テクスチャーフィルターを用いることで得られた強度のような、測定した画像由来の1又は2以上の強度はRIQF構成要素の基礎であることができる。幾つかの数の異なった、重なっている可能性がある対象物−モデル−関係の領域に対するRIQFも存在することができる。図5に示す実施態様において、内部領域502及び外部領域504が存在する。図6に示した他の実施態様において、606内部領域及びm−repモデルの各スポークに中心のある外部がある。
【0050】
DSM−統計的調整可能
統計的調整可能な変形可能な形態モデル(SDSM)処理法は、解剖学的対象物の内在的なジオメトリーを表し;及び統計解析を用いて、ジオメトリーの可変性を記載する。幾つかの異なったジオメトリー表現を用いて解剖学的対象物を形作ることができるが、最も簡単なこのようなジオメトリーは、Euclideanベクトル空間における内在的ジオメトリーの表現を含むことは評価される。
【0051】
一度、対象物が形作られると、統計的形態解析を用いて、その対象物のばらつき様式を数学的に表現できる(即ち、幾何学的な対象物の集団の可変性を記載する)。主成分解析(PCA)は、Euclideanベクトル空間をベースとした対象物モデルの可変性の有効なパラメーター化を提供するための統計的形態解析ツールの一例である。
【0052】
PCAは、解析のために多次元データセットを低次元に下げるために使われるベクトル空間変形である。しかしながら、PCAは、Euclidean空間に存在する幾何学的モデルを記載するためにのみ有用であることができる(例えば、一組のEuclidean目印又は境界点によりパラメーター化される)。その結果として、PCAは、m−repの様に、形態の非Euclidean表現を記載するためには、適切でない可能性がある。m−repで用いられるメディアルパラメーターはEuclidean空間の成分ではないので、標準的な形態解析技術(例えば、PCA)は適合しない。従って、PCAの修正型(即ち、一般化した)を用いて、これらの種類の対象物の可変性を記載しなければならない。
【0053】
このようなPCAの修正形の一つを主ジオデシック(測地学)解析(PGA)と呼ぶ。PGAは湾曲したマニホールドのためのPCAの一般化である、またPCAの様に、PGAは解析のために多次元データセットを低次元に下げるために、データ共分散マトリクスの固有値分解の計算を含むことができる。例えば、対象物のジオメトリーを、mにより表すことができて、対象物の形態の可変性を確率密度p(m)で表すことができ、また画像知識をp(mに相対的なl)により捕捉できて、p(m)の見積をPGAにより行うことができるが、このPGAは対象物及び対象物間の相互関係手段を(配向及びサイズの指標である特別の非Euclidean数学的特徴を認識する遣り方で)計算し、またこのPGAはm−repの抽象的湾曲空間に平均して接する抽象的平坦(Euclidean)空間上のばらつき様式を計算する。
【0054】
上記のように、m−repは対象物の幾何学的な可変性を、曲げ、捻れ、及び拡大という点から記載することができるが、メディアルパラメーターは、Euclideanベクトル空間の成分ではない。その結果として、m−repモデルを変形する従来型の方法は、非Euclideanベクトル空間に適用するためにやはり修正する必要があるかも知れない。
【0055】
統計的に調整した外観モデル
調整した画像lに当てはめたDSMmに由来する外観モデルを、主成分解析により解析して、コンピューターをベースとしたセグメンテーションに用いられる外観p(mに相対的なl)上の確率分布を学習することができる。このような確率分布を、プランニング画像に関連して、及び介入がガイドする画像に関連して、学習することができる。
【0056】
最善の統計的調整をした(バイオプシ前)患者特異的M−Rep及び外観モデル
一組の調整した画像が与えられると、m−rep対象物モデルを調整させる第1のゴールは、対象物の幾何学的可変性を正確に形に表すことである。従って、m−repを熟練者により作られたモデルで調整し、検討すべきヒト集合を横断した医学的画像における対象物の形態(例えば、前立腺、膀胱及び直腸)の範囲、及び各対象物の強度パターンの範囲を定義する統計的確率分布を作ることができる。結果として、m−repを調整させることにより、m−repモデルの画像への当てはめの質を高めることができる。
【0057】
初期m−repモデルを、1又は2以上のメディアルアトムを変えることにより、自動的に変形して、標的画像データに一致させることができて、その結果log p(m)、log p(mに相対的なl)の総和、及びDSMの初期設定に忠実性を与える、他の項により作られる関数を最適化することができる。メディアルアトム上に行うことができる典型的変化は、初期モデルのガース(周囲の寸法)の増加、又は減少するようメディアルアトムのサイズを変更すること;メディアルアトムの各スポークを、一緒に又は別々に回転させて、初期モデルの表面を捻ること;及びメディアルアトムを動かして初期モデルを曲げる又は伸ばすこと;を含む。初期モデルは、伸長、曲げ、回転、捻り、及びモデルのガースの増加又は減少のような自然な操作に対応して変形できるので、m−repを変形して、標的画像データに当てはめるに必要な時間及び処理量は減少する。
【0058】
一つのシナリオにおいて、m−rep調整はm−repモデルを既知の対象物の調整集団に当てはめること、及びPGAの計算を含むことができるが、ここでPGAを用いて、対象物の統計的に可能な事例にモデルの形態を制限することができる。
【0059】
p(m)が与えられた対象物のジオメトリー、及びp(mに相対的なl)が与えられた対画像ジオメトリー適合(geometry-to image match)に対する調整過程は、熟練者により作られた注意深いマニュアルによる対象物(単数又は複数)のセグメンテーションの調整例を用いるが、このマニュアルセグメンテーションよりモノクロ2値画像を作ることができる。各調整例において、m−repは、各対象物に対するモノクロ2値画像に密接に当て嵌まり;及びアラインドフィット(位置合わせによる当てはめ)のPGAはp(m)をもたらす。p(mに相対的なl)を見出すために、得られた当てはめを用いて、前立腺に関係するRIQFを抽出するが、これは対応する調整(トレイニング)画像から全てのモデルに関係する領域のためである。モノクロ2値画像にmを当てはめる方法は、上記のグレースケール(白黒画像)セグメンテーション法の変形である:目標関数、log p(mに相対的l) + log p(m)、は同一型の関数、画像マッチ(適合)+ジオメトリックティピカリティ(幾何学的典型性)により置き換えられるが、ここで、2値画像マッチは、mにより示されるモノクロ2値及び境界の間の距離から計算される、またここでジオメトリックティピカリティは、mの滑らかさ、畳み込み無し、及び幾何学的規則性を与える。
【0060】
m−repが初期化された後、即ち対象物に対して大雑把に位置づけられ、また方向付けられた後、このm−repは、例えば、画像強度を含む目標関数、及び/又は変形したDSM及び標的画像の間の適合の度合いの指標を計算する非強度項を最適化することにより変形できる。
【0061】
セグメンテーション−ステップ1:初期化
形態は、しばしば、全体的な平行移動、回転、拡大縮小で不変な対象物のジオメトリーとして定義される。従って、計算される可変性が形態変化のみであることを保証するために、調整目標を通例の位置、配向及び大きさにアライン(位置あわせ)しなければならない。一つの通例のアラインメント技術は、全体としての平行移動、回転、拡大縮小に関して、対応するデータ地点間の距離の二乗の和を最小化することを含む。
【0062】
従って、典型的m−rep初期化のアルゴリズムは、(1)平行移動、(2)回転及び拡大縮小、及び(3)反復からなるステップを含むことができる。従って、例えば、平行移動は、各モデルを平行移動することによる、複数のm−repモデルの画像への集中化を含み、その結果メディアルアトム位置の平均は、任意の原点に局在する。その後、特定のモデルを選択し、残りのモデルの平均に揃えることができる。この処理は、繰り返され、アラインメントの基準をさらに小さくできなくなるまで繰り返すことができる。
【0063】
他の典型的なm−rep初期化アルゴリズムは、平行移動、回転、及び拡大縮小だけではなく、次項に記載するように、その後、対象物の統計的に可能な事例内での変形を含むことができて、しかも一方において、平行移動、回転、拡大縮小間の繰り返し、他方において、変形の繰り返しを伴う。
【0064】
セグメンテーション−ステップ2:変形
形態ばらつきの解析に基づく方法は、医学的イメージングにおいて、広範囲に及びつつある。これらの方法により、画像情報自体はしばしば充分強くない、タスク(課題)以前の形態知識の統計的モデリングが、タスクを自動的に解決することを可能にする。セグメンテーションにおける変形可能なモデル使用の一例は、統計的形態モデルによる、好ましい変形の決定を含む。他の重要なタスクは、形態解析と分類であるが、ここで統計的形態モデルは、診断方法のために健康な器官及び疾患の器官の分布を提供する。
【0065】
統計的形態モデルの最も一般的な形式は、変形を伴う平均形態である。平均及び対応する変形は、調整データの収集からの形態の統計的解析を通して構築された。調整セットにおける各形態は選択された形態表現により示され、表現のパラメーター解析により平均、及びばらつきが得られる。
【0066】
統計的形態モデルの他の形式はある平均からの前変形を初期化すること、及びその初期化からの変形を含む。プランニング画像から分節化したm−repから、介入がガイドする画像から分節化したm−repへの変形が一例である。
【0067】
m−repを、同一患者の異なる画像由来の形態上で、及び/又は異なる患者の画像を横断して、調整できることは評価される。同一患者による調整により、例えば、異なる程度の直腸、及び/又は膀胱の貯留のような、前立腺に働く機械的な力による;及び患者間で生ずる自然の差異による;形態差異を記載する統計が提供される。異なる患者からの画像による調整により、個々の患者間の解剖学的な差異を記載する統計が提供される。
【0068】
変形:外観をベースとする:ピクセル強度
上記のように、PGAは、m−repに適用できるが、ここでm−repはp(m)と言う形で対象物のジオメトリーを表現できる。PCAはmに相対的な領域に対するRIQFに適用できるが、ここでRIQFはp(mに相対的なl)という形で対象物に相対的な外観を表現する。従って、mに相対的なl、をPCAに従わせるために、対象物境界に隣接した外部及び内部領域に対するピクセル強度は、mにより示される対象物境界に対して近く、また内部の領域を記載するRIQFにより表現できるが、ここでこのRIQFはその領域の強度の累積ヒストグラムの逆関数を表す。
【0069】
図5は、本発明の実施態様に従い、画像強度値のサンプリングに適した、CT画像における前立腺の3直交線表現である。図5を参照すると、3直交線CT表示500は、前立腺内の画像強度をサンプリングするための領域502及び前立腺の外側の画像強度をサンプリングするための領域504を含む。画像強度のサンプリングは、対象物境界近く及び内部の領域を対象物に対するRIQFで記載する関数を用いるが、対象物境界に隣接した内部及び外部領域における画像強度のサンプリングは、対象物のジオメトリーをPCAに対して適切にするために必要であろう。
【0070】
図6は、本明細書に記載した実施態様に従い、RIQF解析のために準備した典型的なm−rep対象物モデルの表現を含む。右側に、膀胱m−rep対象物モデル600を示す。左側に、対象物600を、このm−repに基づいて定義された境界及びスポーク関連領域602により定義することができる。その後、スポーク関連領域602を用いて、各スポークに対応する内部及び外部領域を作ることができて、及びこれらの領域を用いて、各領域に対するRIQFに基づく外観モデルを提供することができる。このアイデアは、均一組織の領域は、異なる患者における標的対象物に関して同一位置であり、また類似の組織組成を持つであろうと言うことである。対象物境界の外部領域がそのRIQFが画像マッチに貢献する外部領域を定義するために用いられる際、調整においてこれらのクラスターで定義される対象物境界上の外部領域が、スライドし(滑り)回ることを可能にすることにより、改善された外観モデルを、得ることができるであろう。
【0071】
図7は、本明細書に記載した実施態様に従い、調整画像に由来する膀胱、及び前立腺に対するRIQF(上部)、及びそこに由来するヒストグラム(下部)の一連のプロットである。図7を参照すると、一対の画像700は、膀胱対象物に対するRIQFを描写し、また一対の画像702は、前立腺対象物に対するRIQFを描写するが、他方第1及び第3コラムは、調整画像からのRIQF及びヒストグラムを示す、また第2及び第4カラムにおける破線曲線は平均からの±1.5σ(実線で表す)を示す。一対の画像704及び706は、それぞれ、RIQF700及び702に対するヒストグラムを表す。
【0072】
変形:外観をベースとした:テクスチャー特性
強度変量のみを用いただけは背景から対象物を分離することは不可能であるが、ある画像に対する一つの例において、テクスチャー特性は、背景から対象物を分離する重要なセパレーター(分離手段)を提供する。本明細書で用いるように、一つの態様に依れば、用語"テクスチャー"及び"テクスチャー特性"は、関係する成分を有するデジタル画像において1又は2以上のピクセルの収集を含む。他の態様によると、テクスチャーは、周期的に配列した初期テクスチャーの空間的配列を含むことができるが、ここで初期テクスチャーは、最も単純な又は基本的な下位パターンを表す一群のピクセルである。例えば、あるテクスチャーは、ピクセル強度及び/又は初期テクスチャー間の空間的関係により、細かい、粗い、滑らか、又は粒状であることができる。
【0073】
例えば、CTにおいて、肺葉内の気管支及び血管のパターンは、肺葉又は肺を心臓から分節化する上で重要であることができる。m−repの後部の最適化によるセグメンテーションによると、テクスチャー変量上のRIQFが、強度変量上にRIQFとコンカテネートした(結びついた)幾つかの場合、改良されたセグメンテーションが、得られることが示唆される。
【0074】
一つの実施態様によると、超音波プローブに垂直な面における6個の2Dの回転しても不変なテクスチャー特性を用いることができる。次に、Gaussian又はLaplacianフィルターを含むがこれらに限られない、フィルターをテクスチャー特性に適用できる。さらに、第1微分又は第2微分Gaussianの複数の配向に関して、最大応答を得ることができる。平均外部記載に対する平均内部記載のMahalanobis距離、又はその逆関数に基づき、各テクスチャー特性を、前立腺の内部と外部を識別する能力により評価することができる。
【0075】
例えば、本明細書に記載した実験データを用いて、全体規模で最善を行うテクスチャー特性は、小規模2次微分Gaussianフィルターに基づく。全体としての内部及び外部領域に対して、この(テクスチャー)特性の感度が、強度のみを用いるより、2.9倍高いことは評価できる。従って、テクスチャーRIQFと共に強度RIQFは、本明細書に記載された目的関数に対して、強く識別する画像位置合わせ項に対する基礎を提供できる。
【0076】
この場合テクスチャー特性は、Gaussianの方向付けられた2次微分を伴うコンボリューション(畳み込み演算)の結果の画像平面における配向に関して最大であった。この指標を選んだ理由は、これが、前立腺に対して外部の全体的領域に対するRIQFと、全体の内部領域を良く分離することを示したからである。
【0077】
変形:情報に基づく解剖
画像強度パターンのみを用いることに加えて、画像の成功したセグメンテーションは、解剖の知識及び解剖に関連した画像強度パターンの両者によることができる。従って、セグメンテーションは、標的対象物ジオメトリーの解剖学的に妥当な例に制限することができる。問題となる対象物のジオメトリーの表現m上の確率密度p(m)により、解剖の知識は獲得され;及び、我々の理解では、条件付き確率(下式)
【数1】

に等しいp(mに相対的なl)により、画像知識は獲得される。
【0078】
そこで、セグメンテーションは、
(i)mを、問題となる器官を妥当に表す、幾何学的に折り畳まれてない、滑らかな構造に対応する、初期モードのみをカバーする空間Sに制限すること;及び
(ii)lにより表される画像強度パターンが与えられた時、そのような最も有望なmを見出すこと;
を含む。
【0079】
即ち、mにより表されている解剖学的対象物(複数も可能)を分節化するために、下式
【数2】

は、p(m)において表されているばらつきの初期様式の係数について、下式
【数3】

の共役勾配(コンジュゲートグラディエント)最適化により計算できる。あるいは関数最適化は、初期化の際提供された情報からの変位を反映する項をさらに含むことができる。
【0080】
関数、p(m)及びp(mに相対的なl)、の見積を可能にするために、m及びmに相対的なlの両者の表現は、PGAに対して妥当であること;及び両関数が、それぞれ、ジオメトリー及び画像強度パターンを充分に記載すること;が必要である。従って、上記のように、mはm−repを用いて表すことができる;及びlは本発明に従い、RIQFを用いて記載することができる。
【0081】
実験結果
図8は、本発明の実施態様に従い、様々な方法を用いて作成した前立腺境界を描写する一連の典型的なTRUS画像である。図8を参照すると、TRUS画像800は、前立腺の中央を薄切りした前立腺の分節化してない画像であり;画像802はマニュアルセグメンテーション境界808を描写し;画像804は、マニュアルセグメンテーション境界810に相対的なGaussianをベースとしたテクスチャーパラメーターの2次微分を描写し;及び画像806は強度及びテクスチャーRIQFをベースとした外観モデルを伴う、m−repの後部最適化を経由したセグメンテーション境界812を描写する。画像806で示されたセグメンテーション境界812の不正確さは、画像において前立腺のカットオフを考慮しない結果であると評価される。
【0082】
図9Aは、膀胱及び前立腺の表面表現である。図9Bは、それぞれ自動化したセグメンテーションを含む前立腺及び膀胱の表現である。
図10Aは、膀胱の表面表現である。図10Bは、熟練者によるセグメンテーション;及びコンピューターをベースとしたセグメンテーション;を含む膀胱の表現である。図10Cは、自動化したセグメンテーションを含む膀胱の正中軸切片である。
【0083】
図11Aは、熟練者によるセグメンテーション;及びコンピューターベースのセグメンテーション;を含む前立腺の3D表現である。図11Aを参照すると、ワイアーメッシュ1100は、本発明の実施態様に従い、ソフトウェア128により自動的に作り出した、3D前立腺境界を描写する。表面1102は、熟練者によりマニュアルで作られた前立腺の表面境界を描写する。図11Bは、前立腺のCT切片であり、ここで前立腺境界1104は、図11Aに示した境界1100に対応する。同様に、図12は、自動化したセグメンテーション境界1200;及び熟練者セグメンテーション境界1202;を含む前立腺の3D表現である。
【0084】
図13は、本発明の実施態様に従う、一連のRIQFのプロットである。図13を参照すると、図Aは、前立腺の内部及び外部全体領域に対するテクスチャーRIQFを描写する。図Bは、前立腺の平均RIQFを描写する。図C及びDは、平均RIQF及び平均からの±1.5σを表す。
【0085】
図14は、本発明の実施態様に従い、熟練者の作ったコントゥアに当てはめられた複数のm−repから計算した、一連の2個の初期固有モードからの試料である。図14を参照すると、PGAの結果が描写されており、ここで平均m−repはm−rep1408である。列(m−rep1400〜1404,1406〜1410,及び1412〜1416)は、第1モードに沿って−1.5σから+1.5σの範囲であり、行(m−rep1400,1406,1412;1402,1408,1414;及び1404,1410,1416)は、第2モードに沿って−1.5σから+1.5σまで広がる。第1モードは、患者を横断する全体規模を捕捉し;他方第2モードは、前立腺/直腸境界のサドルバッグ様の外観を捕捉する。
【0086】
図15A〜15Cは、男性骨盤の一連のCT走査である。図15Aを参照すると、CT切片は、収縮した直腸のバルーンを伴う男性骨盤ファントムである。図15Bは、膨張した直腸バルーンを伴うFEM計算の切片を描写する。図15Cは、膨張した直腸バルーンを伴う、現実のCT切片を描写する。
【0087】
変形:機械的シミュレーション
上記のように、m−repは、前立腺のような解剖学的対象物のジオメトリーを表すために自動的に組み立てた3D6面体メッシュ(網目)に対する枠組みを提供する。m−repの多くの可能な変形をシミュレートするために、身体的に正しい機械的変形を計算することができて、その一つの例として、有限要素法(FEM)がある。本明細書で用いる様に、FEMは、完全に微分方程式を使わない;又は標準的な技術を用いて解かれる常微分方程式を用いて式を近似する;のいずれかにより、偏微分方程式及び積分方程式に対する近似解を見出すための数値技術である。本発明の範囲から離れることなく、他の技術も用いることができる。
【0088】
m−repを形成するメディアルアトムメッシュ内の各四辺形は、メディアルシートの各側に1個の、スポークの2個の四辺形を形成する。スポークの各四辺形は、6面のエンティティ(実体)を形成し、これは更にスポーク再分割及び内挿により再分割できる。得られた正確なメッシュを、他の対象物も恐らく含め、解剖学的対象物の外部に当て嵌まるようにメッシュに埋め込むことができる。この領域への力の効果をシミュレートするために;又は機械的に妥当な変形に当てはめるために;全体としてのメッシュを用いて、確立したFEM法の機械的微分方程式を解くことができる。
【0089】
従って、内部の力により引き起こされた対象物モデルの変形は、FEMのような機械的モデリング法により学習されることができる;及び結果としての変形の統計は、FEMの結果から抽出したm−repに導くことができる。
【0090】
この可能性は、前立腺に埋め込まれた金属シード及び直腸内バルーンカテーテルを伴う組織に等価な骨盤ファントムのCT走査を用いて正当と確認された。計算は3Dであったが、明確にさせるために2D結果を示すことは評価できる。非変形の前立腺のシードは、膨張したバルーンにより変形した前立腺に対応する位置に、CTヴォクセルサイズのみにより制限される精度で、マップできる。この方法は、調整画像に当てはめたm−rep上の身体的に正しい変形を計算するために適用して、ジオメトリックな調整に対する付加的なm−repを作ることができる;及び調整したm−repを経由してマップしたアトラスの空間的な精度を有効と確認することができる。
【0091】
介入標的領域を介入がガイドする画像に送る
プランニング画像、又はそこに記録した他の画像から抽出した介入標的領域は、プランニング画像から分節化した解剖学的対象物のm−repの下位領域を作る。一つの例において、プランニング画像は、MRIであり;解剖学的対象物は前立腺であり;及び介入標的領域は、MRS画像において癌の疑いありと描写された組織である。プランニング画像において分節化したその形;及び介入がガイドする画像におけるその形;の間のm−repの変形は、対象物の内部の全てのポイントの変換をもたらすが、ここで対応するスポーク上の長さの割合に従って対応する位置は、互いにマップすると言う規則に従って変形する。この変形を、プランニング画像から分節化した解剖学的対象物における介入標的領域に適用し、介入がガイドする画像における、予想された介入標的領域をもたらすことができる。
【0092】
調整とセグメンテーション
介入がガイドする画像上にM−repを重ね合わせ
図16は、本発明の実施態様に従い、検討すべき対象物のm−rep境界の重ね合わされた画像を含む典型的なTRUS画像である。図9を参照すると、前立腺の3DTRUS画像が示され、ここでm−repを、画像に対するヒト・コントゥアに当てはめて、96.6%のメディアン体積重なり(即ち、Dice係数)及び0.36mmのメディアン平均表面分離をもたらす。本明細書で用いるように、Dice類似係数(DSC)は、A及びBセットの間の面積/体積重なりを下式
【数4】

で定義する。雑音の多いTRUS画像に由来する形態モデル表現は、等しく良い重なりを狙うべきである。図9に示した当てはめは、素晴らしく、解剖学的構造を含む対象物のプランニング画像を、介入をガイドする対象物画像データにマッピングさせるための要件;及びそれにより、プランニング画像からの解剖学的構造内の介入標的領域を、介入がガイドする画像にマッピングさせるための要件;をかなえる。
【0093】
可能な応用例
一つの態様によると、介入をガイドして、画像により針をガイドするために、本発明を用いることができる。例えば、1又は2以上の画像が与えられると、あるm−repモデルをプランニング画像内(例えば、前立腺)の対象物に当てはめる。そして、このm−repモデルは、介入がガイドする画像中の対象物に当てはめられる。そして、これらの画像間の介入標的領域のマッピングを用いて、バイオプシ又は手術の際医師のバイオプシ針をガイドする。
【0094】
例えば、図17は、本発明の実施態様に従い、TRUS画像に重ね合わされた、患者特異的な前立腺m−rep及び介入標的領域のガイドの下に、バイオプシ針の前立腺へのガイドを描写する。図17を参照すると、経直腸の超音波プローブ1700を、患者の直腸1702に挿入する。その結果、プローブ1700は、患者の前立腺を囲む領域のTRUS画像1704を作り、表示装置上に画像を表示できる。次に、患者の前立腺のm−repモデルは、TRUS画像1704に重ね合わせることができて、ここでこのm−repは前立腺境界1706を定義することを助ける。前立腺境界1706内において、介入標的領域1708を描写することができる。例えば、癌の疑いのある前立腺の一部に、針1710を用いてバイオプシできる。上記で詳細に述べたように、m−repを用いて、TRUS画像1704のような、介入がガイドする画像上に、対象物境界1706を正確に示して、バイオプシ針1710を、標的対象物1708まで正確にガイドすることができる。そのため他の組織を乱すことがない。
【0095】
他の例において、癌治療のために、ブラキ療法(brachytherapy、小線源療法)と呼ばれる処置において、放射活性のあるシードを置くために用いられる針を、上述のバイオプシ例と同様な技術によりガイドすることができる。
他の例において、本発明を、大脳皮質又は皮質下脳構造の形態測定のために用いることができる。脳における幾つかの構造の形態は、ある神経状態と相関すると考えられている。MR画像で見られる皮質下脳構造又は大脳皮質の体積及び形態の特徴は、成人早発性痴呆症及び統合失調症と関係する。例えば、本発明を用いて、自閉症のリスクがあると判断された、個人の子供時代に開始した長期にわたるMR画像の皮質下脳構造の吟味をすることができる。時間経過による形態の変化の観察のために、及びこれらの変化と臨床的症状を関係づけるために、及び疾病の改善された治療のために、研究が行われている。
【0096】
他の例において、本発明を用いて、MRIで画像化された膝軟骨の深さのパターン及び湾曲への関節炎薬剤の効果の測定法の開発のような、関節炎の膝軟骨の治療を改善することができる。
【0097】
他の例において、本発明を用いて、筋肉損傷を見積もるために、心拍モデルを作成できる。一つのシナリオにおいて、虚血疾患(心筋への血流の減少)を持った患者の心拍のm−repモデルを用いて、血流が減少している筋肉の領域を限定することができて、また正常心拍の調整したm−repモデルと比較して、どの程度深刻に筋肉が冒されているのか判断できる。特殊なCT,MR及びUS技術により作ることができる、所謂4D画像(3Dプラス時間)から作られたモデルは、研究されるであろう。もし成功したならば、虚血疾患の患者を判断し、また適切な治療を計画するための安全な非浸襲的手技であろう。
【0098】
他の例において、本発明を用いて、慢性閉塞性呼吸器系疾患(COPD)を研究し、また治療することができる。m−repを用いて、呼吸サイクルの様々な部分で獲得したm−rep及びCT画像を用いて肺の画像を自動分節化することにより、患者のCOPDの進行を研究できる。m−repの形態測定特性を用いて、閉塞した肺組織の体積を限定し、測定することができる。
【0099】
他の例において、本発明を用いて、治療の間患者の呼吸による運動及び形態変化をする、肺及び肝臓における腫瘍の治療を改善できる。m−repを用いて、複数の呼吸サイクルの間、複数の間隔で取り込んだCT画像における、標的対象物及び近接した器官を分節化できる。その後、セグメンテーションにより4Dモデルを構築して、患者の呼吸サイクルの間の変化を予想することができる;及び治療計画及び治療実施の間のこれらの変化を説明できる。
【0100】
更に他の例において、本発明を用いて、頭頚部における癌の放射線治療計画を改善できる。例えば、m−repを用いて、リンパシステム下位領域と共に、頭頚部の両側の15又はそれ以上の対象物が、臨床的に重要な解剖学的構造である領域である、頭頚部の腫瘍の放射線治療を計画することができる。
【0101】
他の可能な応用として、コンピューター支援のデザイン、重要な製作及び構造物部品のシミュレートされたストレス検査、及び漫画製作を含むが、これらに限られない。本明細書で述べたこれらの応用は、広い範囲の可能な製品分野を強調するだけである。前述した事柄は、幾つかの進行中の又は計画中の医学研究プロジェクトを含むが、本発明を、医学的画像における解剖学的対象を抽出するための方法として、統計的に調整した形態物指し、即ち、形態統計に基づいて測定し、識別する方法、例えば、(正常な)1クラス(部類)の形態を他の(疾病の)クラスから区別する方法として、あるいはその両者として、用いることができる。
【0102】
本発明の有利な効果
本発明は、可視標的を示すために、非超音波画像からの癌領域をTRUSバイオプシ画像にマッピングを行い、医師がより正確に彼/彼女の器具を向けることを可能にすることにより、公知技術の短所を克服できる。患者にとっての正味の恩恵は、バイオプシの繰り返し回数の減少;ネガティブバイオプシが偽りであるかどうか、又は低いGleasonスコアは偽りで低いかどうかの不確かさに関係する心理的ストレスの安楽化;治療法決定の基礎となるより良いデータ;及びクオリティオブライフ(生活の質)の全体としての改善であろう。更に、バイオプシの繰り返しに伴う医療費も減少させるべきである。
【0103】
本発明は、自動的に患者モデルを抽出することにより殆ど全ての人間の介入を取り除くことができる、またこれは、使用者の好ましくない変動性が無いやり方で行われる。
本発明は、イメージング研究、及びバイオプシ処置の際、直腸内プローブにより引き起こされた前立腺の変形を正確に形に表すことができる、またTRUS及びMR画像の間の異なる画像特性を扱うことができる。
【0104】
更に、本発明は、診断のための、手術のための、及び他の治療のための介入の全てに対して応用できることは評価される。
本発明の様々な詳細は、本発明の範囲を離れることなく、変更可能であることは、理解されるであろう。更に、前述の記載は本発明は別に述べたクレイムにより定義されたように、描写のみを目的としており、制限付けを目的にしたものではない。
【符号の説明】
【0105】
100 コンピューター
109 バス(母線)
111 遠隔のコンピューター
113 表示装置
114 マウス
116 キーボード
128、130 ソフトウェア
1700 超音波プローブ
1702 患者の直腸
1704 TRUS画像
1706 前立腺境界
1708 介入標的領域
1710 バイオプシ針
【技術分野】
【0001】
この特許出願は、2007年10月18日に出願された米国仮特許出願60/999,420、及び2008年8月7日に出願された米国仮特許出願61/087,026に基づく優先権を有し、そこに記載された内容は本明細書に取り込まれている。
この発明完成に関与する幾つかの仕事は米国NCI及びNIBIB助成金P01 EB002779により支援された。従って、米国政府は本発明について一定の権利を有する。
本明細書に記載される発明は、医学的画像セグメンテーション(分節)及び解析に関し、より詳細には、診断的又は治療的介入に用いられる画像に用意されている1つの画像データから、対象物のモデル(模型)における解剖学的構造を含む領域をマッピング(写影)する方法、システム及びコンピューター読み取り可能な媒体に関する。
【背景技術】
【0002】
前立腺癌(CaP)は、米国における主要な健康問題であり、2005年には240,000診断例及び30,000死亡例がある。前立腺癌は、米国男性人口の非皮膚性癌の全新規発生率の33%を占めており、全非皮膚性癌の中で最大の発生率であり、毎年の死亡率は、結果的に肺/気管支癌に次いで第2位である。前立腺癌の広がり及び深刻な結果により、米国の130〜150万人の患者は、通常バイオプシ(biopsy、生検)を伴う、経直腸的超音波断層イメージング(TRUS)によりガイドされた前立腺介入処置を毎年受ける。他の処置としては、放射性シードの挿入(ブラキ療法−小線源療法)及び組織を凍結又は加熱する方法による組織切除がある。
【0003】
バイオプシの間、小ゲージの中空の注射針を前立腺に導入し、TRUSの視覚的誘導の下にコア組織試料を集める。TRUSは前立腺の全体の形態を良く示すが、大きな短所として、前立腺内の正常及び癌組織を区別することができない。この限界があるので、全ての患者に適用される所定のグリッドパターン(格子模様)に基づいて組織試料を集める。不幸なことに、このアプローチの偽陰性率は高い(約25〜30%)。さらに、バイオプシが陽性の場合においてすら、腫瘍が不完全にサンプリングされるかも知れず、誤って低いGleasonスコア(腫瘍グレード)を導き、また恐らく不適切な治療決定を導く。偽陰性の結果、多年にわたる多数回繰り返すバイオプシがおこなわれ、増殖を続け恐らく転移可能性のある癌が見逃され、かつ患者に不安が生まれる。これらの誤診は著しく患者のクオリティオブライフ(QOL、生活の質)に影響を与え、医療保険負担及び医療費に影響を与える。
【0004】
経直腸的超音波断層イメージング(TRUS)がガイドするバイオプシには、医師が癌の疑いのある前立腺内部の組織から充分正確にバイオプシ試料を取り出すことができないという問題がある。これらの問題を克服するために、画像セグメンテーション(分節化)を用いて、解剖学的対象物及び解剖学的構造の潜在的癌部位のような、解剖学的対象物の中の介入標的領域を特定してもよい。ここで用いるように、"画像セグメンテーション"は、医学的処置に関わる解剖学的実体を見出すために、デジタル画像を領域(即ち、ヴォクセル又はピクセル)に区分する過程を表す。画像セグメンテーションを用いて、磁気共鳴画像(MRI)及びコンピューター断層撮影(CT)に限らず、様々な種類の医学的画像に表れる対象物及び境界(線、曲線、その他)を探し出すことができる。
【0005】
従って、画像を分節化することは、画像を様々な領域に分けることであり、ここで対象物領域又は諸領域の内部及び外部に位置するヴォクセルは、色、強度、又はテクスチャーのような幾つかの特徴又は性質に関するアトラス(地図帳)における対応する位置(即ち、症例内のばらつきに関する情報を備えた可能性を有する鋳型(テンプレート)画像)に似ている。画像セグメンテーションにおける見せかけの情報の使用に加えて、モデルをベースとした分節化は、検討すべき対象物(即ち、器官、腫瘍その他)が、繰り返しのあるジオメトリー(幾何学的配列)を有すると仮定し、従って、対象物のモデルを作成し、用いて、画像のセグメンテーション上に確率的制約を課すことができて、それにより精度が増す。
【0006】
前立腺癌スクリーニング及び治療を含む医学的目的のために、画像セグメンテーションを行うために用いることができる2つの画像例は、磁気共鳴画像(MRI)及び超音波(US)画像である。バイオプシのために針を向けること、又は治療用に放射性シードの挿入のような、重大な治療計画及び治療開始の決定を助けるために、人は、このような画像から、患者内部の解剖学的構造のジオメトリックモデル(幾何学的な模型)を抽出できる。しかしながら、臨床的処置を導くために用いる超音波画像から対象物モデルを抽出するための現在の方法、及び処置を計画するために用いられるMRIのような画像からの抽出でさえ、熟練した人とのやりとりを必要とし、従って非常に時間を要し、高価である。さらに、同様な訓練を受けた熟練者でさえ、人は臨床的決定に不利に影響する使用者内及び使用者間のばらつきを示すことが知られている。
【0007】
バイオプシのような介入を計画するために用いられる幾つかの画像は、前立腺のような、検討すべき対象物の情報ばかりではなく、介入標的領域が対象物内の何処に位置しているかの情報も含む。あるいは、検討すべき対象物、及び介入の位置を示す画像に完全に記録された別々の画像を得ることができるかも知れない。最近の研究によると、MR画像と同時に得られ、また完全に記録された磁気共鳴分光画像(MRSI)は、前立腺癌が疑われる前立腺内部の領域、即ち介入標的領域、を高感度に検出することができる。
【発明の概要】
【発明が解決しようとする課題】
【0008】
不幸なことに、日常的にバイオプシや治療処置を、一定の癌の疑いがあることを示す、画像の直接の視覚的ガイダンス(誘導)の下に行うことは非現実的である。その理由は、このようなガイダンス(誘導)は、経直腸的超音波断層イメージング(TRUS)のようなリアルタイム画像技術を必要とするが、これらは解剖学的対象物を示すが、一定の疾患の疑いについての情報を与えないからである。
従ってこれらの困難を考慮して、介入標的領域由来の画像から、介入標的領域を、介入がガイドする画像に移動させるための、改良された方法、システム、コンピューター読み取り可能な媒体を望む要求が存在する。この要求は、診断的又は治療的介入をガイドするために用いられる画像データに、(プランニング画像に由来する)解剖学的構造を含む対象物のモデルを、マッピング(写影)することにより充足される。
【課題を解決するための手段】
【0009】
プランニング画像から分節化された解剖学的構造を含む対象物のモデルを、対象物が導かれるとは異なる種類の介入がガイドする(導く)画像にマッピング(写影)するための;及びその結果、対象物に含まれる領域を、介入がガイドする画像にマッピングするための;方法、システム及びコンピューター読み取り可能な媒体を開示する。一つの方法によると、解剖学的構造を含む対象物の初期内側表現(メディアルリプレゼンテーション;medial representation)対象物モデル(m-rep)は、対象物の少なくとも第1事例の画像データに基づいて作り出される。対象物の少なくとも第2事例は患者と結びつくが、この少なくとも第2事例のプランニング画像データに基づいて初期m−repを変形して、及びプランニング画像データに記録した介入標的領域を特定して、患者に特異的m−repが作り出される。患者特異的m−repは、対象物の少なくとも第2事例の介入がガイドする画像データと関係づけられるが、対象物の少なくとも第2事例は、プランニング画像データにおける対象物の状態から変形したものである。プランニング画像データにおけるm−rep、及び介入がガイドする画像データにおけるm−rep、の両者の間の変換に由来するマッピングにより、介入標的領域は、特定できる。
【0010】
解剖学的構造を含む対象物のモデルを、介入がガイドする画像データにマッピングするためのシステムもまた開示する。このシステムは、対象物のプランニング画像データに基づく解剖学的構造を含む対象物の内側表現対象物モデル(m−rep)を作り出す対象物モデルジェネレーター(生成系)を含む。次に、ある対象物モデル変形及びマッピングモジュール(要素)は、対象物の介入がガイドする画像に対するm−repと関係づけられる。
【0011】
一つの態様によると、このシステムは、対象物の無数の事例の画像データに由来する確率的情報を含むことができて、各々は異なる患者個人(患者間確率的情報)、及び同一個人の無数の画像データの事例に由来する確率的情報(患者内確率的情報)である。ある患者特異的内側表現対象物モデル(m−rep)は、ある患者に対するプランニング画像データの少なくとも一部に基づくが、ここで画像データの少なくとも一部は、前立腺のような、対象物の種類と関連する。他の個人に由来する確率的情報を用いて、この患者に対するプランニング画像に当てはめられたm−rep、即ちこの患者特異的m−rep、を得ることができる。介入の際、介入がガイドする画像が、同じ器官について得られ、また患者内確率的情報を用いて、この患者特異的m−repは変形されて介入がガイドする画像になる。この変形は、対象物内の介入標的領域に適用される。バイオプシのために、バイオプシ針をガイドして、対象物内の介入標的領域から組織試料を取り出す。このガイダンスは、介入がガイドする画像データ上に重ね合わされた介入標的領域の表示により行われる。
【0012】
他の態様により、このm−repの対象物の介入がガイドする画像データへの変形は、ある目的関数の最適化を含むが、その目的関数は、このm−repを介入がガイドする画像データに関係づける成分を含む。
【0013】
本明細書で用いられる用語"対象物"はモデル化することを希望する解剖学的構造のような、実世界の構造を示す。例えば、対象物としては、腎臓、心臓、肺、膀胱及び前立腺を含むことができる。
【0014】
用語"介入標的領域"は、疾病が疑われマークされている領域又は治療の標的のような、医療介入のための標的を示す。
【0015】
用語"対象物画像データ"は、対象物からセンサーにより集められ、コンピューター上に保存された一組のデータを示す。対象物画像データの例としては、CT走査データ;MRIデータ;X−線データ;デジタル写真;又は、一組のピクセル強度及び位置で表すことができる、実世界から集められたあらゆる他の種類のデータ;を含む。
【0016】
本明細書で用いられる用語"メディアルアトム(medial atom、内側の原子)"は、お互い、及びモデル中の1又は2以上の中心軸に関して、所定の関係を有するベクトルの位置及び集積を示す。メディアルアトムは、互いにグループ化してモデルを形成することができる。例えば、格子の成分がメディアルアトムと呼ばれる、空間的に正則格子から、メディアルマニホールド(内部多様体)をサンプリング抽出することができる。
【0017】
本明細書で用いられる用語"メディアルアクシス(medial axis、中心軸)"は、あるモデルの反対側の表面上の接点から等距離の一組のポイント(地点)を示し、表面上の接点から直行直線の交差点に位置する。
【0018】
本明細書で用いられる用語"対象物モデル"は、表面、内部及び形態的ばらつきを含むが、それらに制限されない、対象物の数学的表現を示す。
【0019】
本明細書で用いられる用語"m−rep"は、対象物又は対象物画像データのメディアルアトム表現を示す。あるm−repは、一組の連結した連続メディアルマニホールドとして、幾何学的な対象物を表す、Riemannian空間内の対象物のジオメトリーの明示的な数学的表現(即ちモデル)である。3D対象物に対して、対象物の内部にあり、また2又は3以上の点において対象物の境界に接する全ての球体の中心により、これらのメディアルマニホールドを作ることができる。このメディアルの記載は、内接する球体の中心、及び球体中心から対象物境界上の2個のそれぞれの接点に向かう、「スポーク」と呼ばれる、対応するベクトルにより定義される。対象物の表面境界を表現することに加えて、m−repは、局部の位置、配向、及びサイズに関して内部の対象物を表すことができて、また単一形状又は多数のフィギュア(形状)を含むことができることは評価される。また、あるm−repを、対象物をベースとした座標システム、即ち、作成している対象画像データの対象物の座標システム、において定義することができる。
【0020】
本明細書で用いられる用語"フィギュア(figure、形状)"は、モデルの成分又は下位成分を表す。あるメディアルマニホールドの各連続セグメント(部分)は、メディアルフィギュアを表す。例えば、幾つかのモデルは、単一フィギュアだけを有することができる。単一フィギュアで代表することができる対象物の例は、腎臓のように、比較的単純な形態を持つ対象物である。正確なモデリング(モデル(模型)を組み立てること)のために多数のフィギュアを必要とする対象物の例は、ヒトの手である。メディアルアトムをベースとした手のモデルは、手の掌からなる主要なフィギュア及び手の各指からなる下位フィギュアを含むことができる。
【0021】
本明細書で用いられる用語"ヴォクセル(voxel)"は、3D空間での規則的グリッド上のある値を表す体積(ボリューム)成分を示す。
【0022】
介入がガイドする対象物画像データに解剖学的構造を含む対象物のプランニング画像をマッピングするために、またそれによりプランニング画像に記録した介入標的領域を、介入がガイドする画像に送るために、本発明を、コンピュータープログラム製品を用いて実行することができるが、このコンピュータープログラム製品は、コンピューターが実行できる指令を含み、この指令は、コンピュータープロセッサー(処理装置)により行われる具体的なコンピューターが読み取り可能な媒体に埋め込まれている。本発明を実行する上で適切な、典型的コンピューター読み取り可能媒体には、ディスク記憶装置、プログラム可能な論理装置、及び応用に特異的な集積回路が含まれる。ある実行において、コンピューター読み取り可能な媒体として、処理装置がアクセス可能なメモリー(記憶装置)を含むことができる。このメモリーは、本明細書に記載した要求を探し出すための全ての方法を実行するために、処理装置により実行可能な指令を含むことができる。さらに、本発明を実行するコンピューター読み取り可能な媒体は、多数の物理的装置及び/又は計算プラットフォームを通して配布することができる。
【図面の簡単な説明】
【0023】
【図1】一般目的の計算プラットフォームのブロックダイアグラム(概略ブロック図)を示す図である。本発明の実施態様に従い、一部の方法とシステムをその一般目的の計算プラットフォーム上で実行することにより、モデル及び介入標的領域は、介入がガイドする画像に変換される。
【図2】本発明の実施態様に従い、MR/MRS画像データをTRUS画像にマッピングする典型的過程を示すフローチャートを示す図である。
【図3】本発明の実施態様に従い、それぞれ、熟練者が作成した膀胱及び前立腺の境界を描写する一対の分節化したCT画像を示す図である。
【図4】本発明の実施態様に従い、あるm−rep対象物モデルの3次元表現を示す図である。
【図5】本発明の実施態様に従い、画像強度値をサンプリングするために適切なCT画像における前立腺の3直交性表現を示す図である。
【図6】本発明の実施態様に従い、RIQF解析が実行される前及び後の、典型的m−rep対象物モデルの表現を示す図である。
【図7】本発明の実施態様に従い、膀胱に当てはめたRIQF画像の様々な統計的指標の連続したプロットを示す図である。
【図8】本発明の実施態様に従い、様々な方法を用いて作成した前立腺境界を描写する一連の典型的なTRUS画像を示す図である。
【図9A】本発明の実施態様に従い、膀胱及び前立腺表面の表現を示す図である。
【図9B】本発明の実施態様に従い、超音波走査における膀胱及び前立腺の正中矢状面の切片を示す図である。
【図10A】本発明の実施態様に従い、膀胱の表面表現を示す図である。
【図10B】本発明の実施態様に従い、熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、膀胱の表現を示す図である。
【図10C】本発明の実施態様に従い、コンピューターをベースとしたセグメンテーションを示す膀胱の正軸性(ミッドアクシアル;midaxial)切片を示す図である。
【図11A】本発明の実施態様に従い、熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、前立腺の3次元表現を示す図である。
【図11B】本発明の実施態様に従い、コンピューターをベースとしたセグメンテーションを示すCT走査における前立腺の切片を示す図である。
【図12】熟練者セグメンテーション及びコンピューターをベースとしたセグメンテーションを含む、前立腺の3次元表現を示す図である。
【図13】本発明の実施態様に従い、画像当て嵌の様々な統計的指標を描写する連続したプロットを示す図である。
【図14】本発明の実施態様に従い、ヒトが生成したコントゥア(輪郭)に当てはめた複数のm−repから計算した2個の初期固有モード(様式)からの一連の試料を示す図である。
【図15】本発明の実施態様に従い、男性骨盤ファントム(模型)のCT走査を示す図である。
【図16】本発明の実施態様に従い、バイオプシ処置過程において、医師の針をガイドするために、前立腺のTRUS画像に重ね合わせた3Dm−repモデルの典型的表示を示す図である。
【図17】本発明の実施態様に従い、プランニング画像データから解剖学的構造を含む対象物を、介入がガイドする画像データに、マッピングさせる典型的システムを示す図である。
【発明を実施するための最良の形態】
【0024】
本発明は、プランニング画像における解剖学的構造を含む対象物を;及びプランニング画像に記録した画像由来の介入標的領域を;対象物を示す介入がガイドする画像データにマッピングするための方法及びシステムを含む。本発明の方法及びシステムを、ハードウェア、ファームウェア、ソフトウェア又はこれらの全ての組合せにおいて実行することができる。1つの典型的実施態様において、プランニング画像における解剖学的構造を含む対象物モデルを、介入がガイドする画像データにマッピングするための、対象物モデリングを行うこの方法及びシステムを、一般目的のコンピューター上で実行するように適合させた応用ソフトウェアとして実行できる。図1は、本発明の実施態様に従い、プランニング画像における解剖学的構造を含む対象物モデルを、介入がガイドする画像データにマッピングするための、この方法及びシステムのための典型的操作環境を描写する。図1を参照すると、コンピューター100は、バス(母線)109に接続したマイクロプロセッサー(超小型演算装置)102,ネットワークインターフェース104,I/Oインターフェース105,ディスクコントローラー/ドライブ106,及びメモリー108を含む。従って、コンピューター100は、例えば検討すべき解剖学的対象物の画像データを受けとるために、I/Oインターフェース105を経由して介入がガイドするイメージング装置110に接続できる。
【0025】
マイクロプロセッサー102は、応用ソフトウェアの実行に適切な全ての種類の一般目的用の演算装置であることができる。本発明の実施態様の使用のために適した典型的なマイクロプロセッサーは、Intel(R)会社から入手できるいずれのPentium(R)ファミリーのプロセッサーでもよい。
【0026】
ネットワークインターフェース104は、ネットワーク112を経由して1又は2以上の遠隔のコンピューター111と連絡する1又は2以上のネットワークアダプターカードを含むことができる。例えば、ネットワークインターフェース104は、Ethernet又はATMカードであることができる。
【0027】
I/Oインターフェース105は、ディスプレイデバイス(表示装置)113,マウス114及びキーボード116のような、外部デバイスと連絡する直列ポートを提供できる。I/Oインターフェース105は、またマイクロホン及びスピーカーのような、他の種類の入力及び出力デバイスのためのインターフェースを含むことができる。
【0028】
ディスクコントローラー/ドライブ106は、取りだし可能ディスク118,光学ディスク120及び固定ディスク122のような、記憶装置の読み、書きのためのハードウェア部品を含むことができる。
【0029】
メモリー(記憶装置)108は、マイクロプロセッサー102により実行される指令を記憶するために、ランダムアクセスメモリー124及び読み出し専用メモリー126を含むことができる。本発明に従い、メモリー108は、対象物モデルを変形して対象物の特定の例に当てはめ、及び対象物モデルを対象物の1又は2以上の超音波画像にマッピングするために、ソフトウェア128の特定の例を記憶し、及び対象物の高分解画像データに基づく解剖学的構造を含む対象物の内部表現対象物モデルを作成するために、対象物モデルジェネレーター130の一例を記憶することができる。ソフトウェア128及び130は、Windows(R)オペレーティングシステムの下で現代のPC上で走行できる。又、ソフトウェア128及び130は、自動的にメディアルアトムモデルを変形して、画像データに変えることができて、その後介入標的領域を介入がガイドする画像に送ることができる。ソフトウェア128及び130により行うことができる典型的操作を以下により詳細に記載する。
【0030】
発明の概要
本発明の1態様により、対象物モデルを、標的画像に自動的に埋め込み;対応する標的対象物に厳格に記録し;その後変形して特定の標的対象物の形態に密接に適合させることができる。図2は、本発明の実施態様に従い、外科処置の際医師のバイオプシ針をガイドするために、対象物のプランニング画像に基づいて、前立腺の、患者特異的で、統計的に調整可能(トレイナブル)で、変形可能である、形態モデルを作り出し;及びプランニング画像に記録した画像から介入標的領域を作りだし;及び対象物モデル、従ってこの介入標的領域、を一連の介入がガイドする画像にマッピングする;典型的な過程のフローチャートである。図2を参照すると、ブロック200において解剖学的構造を含む対象物の初期内側表現対象物モデル(m−rep)は、対象物の少なくとも第1事例の画像データに基づいて作成される。対象物モデルは、対象物のその種類に対して一般的であるが、後にその対象物(例えば、患者)の特定の事例に対して、特注作成することができる。あるm−repは対象物の1又は2以上のバイオプシ前画像(例えば、MR,CT,その他)に基づいて作られる。例えば、医師は、存在する全ての小結節を含む、前立腺の詳細なジオメトリーを示すバイオプシ前のMR画像を得ることができる。更に、前立腺モデルに相対的な領域の、前立腺の形態の確率分布及び画像強度パターンを得ることができる。
【0031】
ブロック202において、患者特異的m−repは、対象物の少なくとも第2事例のプランニング画像データに基づき、初期m−repを変形することにより作られるが、ここで対象物の少なくとも第2事例は患者に関係する。例えば、前立腺形態の患者特異的アトラスは、恐らく、画像強度が関係する統計的調整(トレイニング)方法の使用と組み合わせて、プランニング画像のピクセル強度を解析することにより作り出すことができる。また、介入標的領域は、プランニング画像から抽出される;又はプランニング画像に完全に記録され、また介入標的領域についての情報を表現する他の画像から抽出される。
【0032】
ブロック204において、この患者特異的m−repは、プランニング画像から変形した対象物の少なくとも第2事例の介入がガイドする画像データと関係する;及び介入標的領域は、誘導されたm−rep変形を用いた介入がガイドする画像データにマッピングされる。例えば、対象物の境界/輪郭は、超音波画像において正確に定義することができる;及び、癌の可能性がある、又は他の疾患が疑われる領域のような、対象物内の介入標的領域を、プランニング画像から、介入がガイドする画像に送ることができるが、この際プランニング画像における患者特異的m−rep、及び介入がガイドする画像における患者特異的モデルとの間の関係を用いて送る。バイオプシ応用(例えば、医師が標的領域を通した、針の軌跡(トラジェクトリー;trajectory)を計画し、実行させることを可能にすること)に加えて、変形した対象物モデルを用いて、対象物の非―超音波画像を対象物の超音波画像にマッピングすることは、治療上の及び/又は他の診断上の使用にも可能である。確率的分布によって導かれた最適過程により、相関関係を得ることができること;及び検討すべき解剖学的対象物の解剖学的モデルと関係して、前立腺形態の変化、及びプランニングの基本的特徴と介入がガイドする画像技術の間の差異、及び各々の確率分布に気を配ることができること;は評価できる。
【0033】
さらに、対象物モデル、及び介入標的領域は、同時に表示できて、また外科的処置の際に医師をガイドするために、対象物の介入がガイドする画像と重ね合わせることができる。例えば、前立腺バイオプシの間に、正確に針を配置するために、m−rep及び介入標的領域を、前立腺のTRUS画像上にマッピングし、また重ね合わすことができる。
【0034】
他の態様によると、本発明は、患者特異的m−repをTRUS画像にマッピングするための目的関数に表れる、画像位置合わせ項のテクスチャー解析に基づく方法を含む。
【0035】
他の態様によると、MR/MRS及びTRUSデータセットの間の変形可能なマッピングを可能にするために、本発明は、MR/MRSイメージング及びTRUSイメージングの間の患者内変形についての統計を作成する方法;及び前立腺/嫌疑体積モデルに相対的なTRUS画像強度及びテクスチャーを表現する方法;を含む。これらの態様の各々を、今や、より詳細に記載する。
【0036】
初期M−rep対象物モデルの作成
対象物の画像データ
上述のように、様々な種類の対象物は、異なった種類のデジタル画像で表現できる。これらの画像は、MRI,MRSI及びCT画像のような、プランニング画像を含むことができる;又は超音波画像(例えばTRUS)のような介入がガイドする画像であることもできる。デジタル画像に表現される、異なる解剖学的対象物の境界を正確に特定するための一つの方法は、マニュアル(手作業)2D画像セグメンテーションを含み、このセグメンテーションでは、熟練者が、画像の各切片に表現される対象物の境界を決定する。
【0037】
画像セグメンテーションにより2D画像における対象物の境界の特定に加えて、対象物ジオメトリーの異なる特徴を捕捉する対象物の複数の画像を用いて、対象物の3Dモデルを作ることができる。例えば、異なる患者から得た前立腺の画像、異なる時間に得た個々の患者の前立腺画像、異なる角度から得た前立腺の画像、及び/又は異なるイメージング技術を用いて得た前立腺の画像を用いて、前立腺の3Dモデルを作ることができる。以下により詳細に記載する様に、モデルをベースとする方法は、外観をベースとしたモデル、解剖が知らせるモデル、機械的モデル、統計的モデル、及びこれらの組合せに分けることができる。
【0038】
対象物モデルの作成に適したある種類のデジタル画像の一例は、磁気共鳴画像(MRI)である。対象物の画像表現を作成するために、電磁場を用いて体中の原子の核磁化を並べることにより、MRIは生み出される。初期配列の後に、ラジオ周波数場を用いて、スキャナ(走査器)により検知可能な回転磁場を対象物中の核に引き起こし、システマティックにこの配列を変化させることができる。充分な情報を作り出して、対象物の画像を再構成するために、追加的な磁場を用いて、さらに配列を動かすことができる。例えば、MRIスキャナー内に人が横たわる時、水素核(例えばプロトン)は、強い主磁場に沿って並ぶことができる。主磁場に垂直に、ラジオ周波数で振動する第2の電磁場を、パルスして、幾つかのプロトンを主磁場に沿った並びから外すことができる。これらのプロトンが主磁場に沿った並びにドリフトバックする時、これらのプロトンは、検出可能なラジオ周波数信号を発信する。身体の異なる組織のプロトン(例えば、筋肉に対する脂肪)は、異なる速度で再配列するので、身体の異なる構造を、MRIに示すことができる。
【0039】
MRIに類似して、磁気共鳴分光イメージング(MRSI)を画像データとして用いることができて、ここから癌の疑いのレベルを知ることができる。MRSIを分光学及びイメージング法と組み合わせて、対象物の中から空間的に局在するスペクトルを作ることができる。例えば、磁気共鳴分光を用いて、体組織中の異なる代謝物のレベルを測定することができる。MRシグナルは"励起した"同位体の異なる分子配置に対応する共鳴スペクトル作ることができるので、共鳴スペクトル標識を測定することができて、また様々な疾患の診断又は治療計画をするために用いることができる。
【0040】
本発明に従い対象物モデルを作成するために適したデジタル画像の第3番目の典型的な種類の例は、コンピューター断層撮影(CT)画像である。従来型のCTイメージングとしては、回転軸の周りから取り込まれた複数の2次元(2D)X線画像から、対象物の3次元(3D)画像を作り出すためのデジタルジオメトリープロセッシングの使用がある。しかしながら、他の種類のCTイメージングとして、本発明の範囲を離れることなく、ダイナミックボリュームCT,アクシアル(断層)CT、シネCT,ヘリカル/スパイラルCT,デジタル再構成写真(DRR)CT,電子ビームCT,多切片CT,デュアル線源CT,インバースジオメトリーCT,末梢定量的コンピューター断層撮影(pQCT),シンクロトロンX線断層撮影顕微鏡、及びX線CTがあり、これらに制限されないことを評価する。
【0041】
図3A及び3Bは、本発明の実施態様に従い、それぞれ、熟練者が作成した膀胱と前立腺の境界を描写する一対の分節化したCT画像である。図3Aを参照すると、境界300は、例えば、画像におけるピクセル強度の目視検査により医師が決定したヒト男性の膀胱の境界に対応することができる。同様に、図3Bにおいて、境界302は、画像におけるピクセル強度パターンに基づくヒト男性の前立腺の境界である。図3A及び3Bに描写したマニュアル2Dセグメンテーションは、3D領域を提供することができるが、この3D領域に、モデルが当てはめられ、及び更に、解剖学的形態の形態上で、及び対象物に関連した画像情報上で、確率分布を学習する過程でさらに用いられることができる;あるいはそれは標的又はゴールを表すことができて、この標的又はゴールは、ゆっくりした煩雑なマニュアル法で為し遂げることができるが、同様に(又はより正確でさえあるが)自動化した画像処理を用いて;及び本明細書に記載する統計的対象物モデリング法を用いて;為し遂げることができるものである。従って本明細書に記載した、プランニング及び介入がガイドする解剖学的構造のデジタル画像を分節化するための方法の精度の指標としては、画像フィッティング(当てはめ)解析、又は図3A及び図3Bに示すような、熟練者が作成したマニュアルセグメンテーションとの比較が含まれる。
【0042】
対象物モデルの作成
2D画像において、対象物の2D境界を決定することに加えて、対象物の複数の2D画像を用いて対象物の3Dモデルを作成することができる。従って、既に紹介した1又は2以上の高分解能デジタル画像を用いて、初期対象物モデルを作成することができる。以下により詳細に記載するように、対象物モデルを、様々な方法に従って作成することができる。しかしながら、これら全ての方法のゴールは、形態及び対象物の可能な形態変化の最も正確な記述(表面及び体積)を作り出すことである。
【0043】
良い−静止モデル
対象物の静止モデルは、対象物の数学的表現であり、ここで、モデルの各部分の関係は、他の部分との関係で変化しない(即ち、変形しない)。
しかしながら、(前立腺のような)解剖学的対象物は、長時間にわたってめったに同一の形態及びサイズではない(静止してない)ので、もしこのような対象物の正確なモデルを提供することを望むのであれば、解剖学的対象物のモデルは、静止であるべきでない。
【0044】
より良い−変形可能形態モデル
変形可能形態モデル(DSM)は、解剖学的構造を含む対象物の形態、及び形態的ばらつきの両者の表現である。しかしながら、DSMのカテゴリーの中で、m−repと呼ばれる特別な部類のDSMは、前立腺のような解剖学的対象物と結びついた特定のジオメトリーを最も良く表現することができる。
【0045】
上述のように、"m−rep"は、一組の連結した連続メディアルマニホールドを用いた対象物のジオメトリーの明示的な数学的表現(即ち、モデル)である、メディアルアクシス(中心軸)表現対象物モデルを示し、ここでメディアルマニホールドの各連続セグメントはメディアル(内部)形状を表す。このメディアルマニホールドは、空間的に正則格子からサンプリングできて、ここでこの格子の成分はメディアルアトムと呼ばれる。この格子は、2Dメッシュの形であることができて、又は各々1サイクルのスポークからなるアトムの1D鎖であることもできる。結果として、m−repは解剖学的対象物の幾何学的ばらつきの有効なパラメーター化であり、またそれにより、画像セグメンテーションの際の形態的な制約を提供することができる。
【0046】
図4は、本発明の実施態様に従い、m−rep対象物モデルの3次元表現である。図4を参照すると、メディアルジオメトリーは中心及び幅の観点から対象物を記載できる。ある3D対象物(例えば、前立腺)を、対象物の対向表面の間の途中に横たわる2D湾曲型のシート、及びシートの両サイドから対象物の境界まで達するスポークにより表すことができる。ハブ(hub)と呼ばれる、メディアルシート上の位置、及び2本のスポークは、メディアルアトムと呼ばれる。従って、m−repを用いて、完全な対象物表面を、アトムスポーク端から再現することができる。
【0047】
図4において、ハブ400を、2D湾曲表面402及び404と、それぞれスポーク406及び408を経由して接続することができる、またこれらを合わせてm−rep410を表わす。複数のm−rep410を連結して、対象物412のような対象物の体積のあるジオメトリーを作ることができる。最後に対象物の表面を示すために、ワイアメッシュ(金網)414を、m−repモデル412に適用できる。m−repのより詳細な考察及びm−rep作成過程は、本明細書に参考文献としてその全体を取り込んだ、US特許番号7,200,251に含まれる。
【0048】
上記のように、初期m−repが、対象物の1又は2以上の高分解能デジタル画像を用いて作られた後、対象物のジオメトリー及び/又は対象物を様々な条件下で変形できる方法をより正確に表すために、このm−repは、統計的調整を受ける。一連の変形及び統計的計算によるm−rep調整の過程については、以下により詳しく記載する。
【0049】
DSM−外観をベースとした
外観モデルは、ジオメトリックモデルと関連して取得された場所における画像を記載する。セグメンテーションに用いられる外観モデルは、画像強度値に基づく。例えば、ヴォクセル目録(リスト)及び局所的な強度変位値関数(RIQF)法は、画像強度をベースとした画像セグメンテーション法である。RIQF構成要素は、対象物の特定領域の強度の累積ヒストグラム(度数分布)の逆関数を表す。RIQFはこのような構成要素により作ることができる。各構成要素は、例えば、1D配列の変位値関数値であり、この各値は、与えられた変位値に対する強度値である。例えば、CT又は超音波のような、画像における単一強度ような;又は、ある種のMR画像のような、複数の強度画像において測定される複数の強度のような;異なる強度に各構成要素は対応することができる。さらに、テクスチャーフィルターを用いることで得られた強度のような、測定した画像由来の1又は2以上の強度はRIQF構成要素の基礎であることができる。幾つかの数の異なった、重なっている可能性がある対象物−モデル−関係の領域に対するRIQFも存在することができる。図5に示す実施態様において、内部領域502及び外部領域504が存在する。図6に示した他の実施態様において、606内部領域及びm−repモデルの各スポークに中心のある外部がある。
【0050】
DSM−統計的調整可能
統計的調整可能な変形可能な形態モデル(SDSM)処理法は、解剖学的対象物の内在的なジオメトリーを表し;及び統計解析を用いて、ジオメトリーの可変性を記載する。幾つかの異なったジオメトリー表現を用いて解剖学的対象物を形作ることができるが、最も簡単なこのようなジオメトリーは、Euclideanベクトル空間における内在的ジオメトリーの表現を含むことは評価される。
【0051】
一度、対象物が形作られると、統計的形態解析を用いて、その対象物のばらつき様式を数学的に表現できる(即ち、幾何学的な対象物の集団の可変性を記載する)。主成分解析(PCA)は、Euclideanベクトル空間をベースとした対象物モデルの可変性の有効なパラメーター化を提供するための統計的形態解析ツールの一例である。
【0052】
PCAは、解析のために多次元データセットを低次元に下げるために使われるベクトル空間変形である。しかしながら、PCAは、Euclidean空間に存在する幾何学的モデルを記載するためにのみ有用であることができる(例えば、一組のEuclidean目印又は境界点によりパラメーター化される)。その結果として、PCAは、m−repの様に、形態の非Euclidean表現を記載するためには、適切でない可能性がある。m−repで用いられるメディアルパラメーターはEuclidean空間の成分ではないので、標準的な形態解析技術(例えば、PCA)は適合しない。従って、PCAの修正型(即ち、一般化した)を用いて、これらの種類の対象物の可変性を記載しなければならない。
【0053】
このようなPCAの修正形の一つを主ジオデシック(測地学)解析(PGA)と呼ぶ。PGAは湾曲したマニホールドのためのPCAの一般化である、またPCAの様に、PGAは解析のために多次元データセットを低次元に下げるために、データ共分散マトリクスの固有値分解の計算を含むことができる。例えば、対象物のジオメトリーを、mにより表すことができて、対象物の形態の可変性を確率密度p(m)で表すことができ、また画像知識をp(mに相対的なl)により捕捉できて、p(m)の見積をPGAにより行うことができるが、このPGAは対象物及び対象物間の相互関係手段を(配向及びサイズの指標である特別の非Euclidean数学的特徴を認識する遣り方で)計算し、またこのPGAはm−repの抽象的湾曲空間に平均して接する抽象的平坦(Euclidean)空間上のばらつき様式を計算する。
【0054】
上記のように、m−repは対象物の幾何学的な可変性を、曲げ、捻れ、及び拡大という点から記載することができるが、メディアルパラメーターは、Euclideanベクトル空間の成分ではない。その結果として、m−repモデルを変形する従来型の方法は、非Euclideanベクトル空間に適用するためにやはり修正する必要があるかも知れない。
【0055】
統計的に調整した外観モデル
調整した画像lに当てはめたDSMmに由来する外観モデルを、主成分解析により解析して、コンピューターをベースとしたセグメンテーションに用いられる外観p(mに相対的なl)上の確率分布を学習することができる。このような確率分布を、プランニング画像に関連して、及び介入がガイドする画像に関連して、学習することができる。
【0056】
最善の統計的調整をした(バイオプシ前)患者特異的M−Rep及び外観モデル
一組の調整した画像が与えられると、m−rep対象物モデルを調整させる第1のゴールは、対象物の幾何学的可変性を正確に形に表すことである。従って、m−repを熟練者により作られたモデルで調整し、検討すべきヒト集合を横断した医学的画像における対象物の形態(例えば、前立腺、膀胱及び直腸)の範囲、及び各対象物の強度パターンの範囲を定義する統計的確率分布を作ることができる。結果として、m−repを調整させることにより、m−repモデルの画像への当てはめの質を高めることができる。
【0057】
初期m−repモデルを、1又は2以上のメディアルアトムを変えることにより、自動的に変形して、標的画像データに一致させることができて、その結果log p(m)、log p(mに相対的なl)の総和、及びDSMの初期設定に忠実性を与える、他の項により作られる関数を最適化することができる。メディアルアトム上に行うことができる典型的変化は、初期モデルのガース(周囲の寸法)の増加、又は減少するようメディアルアトムのサイズを変更すること;メディアルアトムの各スポークを、一緒に又は別々に回転させて、初期モデルの表面を捻ること;及びメディアルアトムを動かして初期モデルを曲げる又は伸ばすこと;を含む。初期モデルは、伸長、曲げ、回転、捻り、及びモデルのガースの増加又は減少のような自然な操作に対応して変形できるので、m−repを変形して、標的画像データに当てはめるに必要な時間及び処理量は減少する。
【0058】
一つのシナリオにおいて、m−rep調整はm−repモデルを既知の対象物の調整集団に当てはめること、及びPGAの計算を含むことができるが、ここでPGAを用いて、対象物の統計的に可能な事例にモデルの形態を制限することができる。
【0059】
p(m)が与えられた対象物のジオメトリー、及びp(mに相対的なl)が与えられた対画像ジオメトリー適合(geometry-to image match)に対する調整過程は、熟練者により作られた注意深いマニュアルによる対象物(単数又は複数)のセグメンテーションの調整例を用いるが、このマニュアルセグメンテーションよりモノクロ2値画像を作ることができる。各調整例において、m−repは、各対象物に対するモノクロ2値画像に密接に当て嵌まり;及びアラインドフィット(位置合わせによる当てはめ)のPGAはp(m)をもたらす。p(mに相対的なl)を見出すために、得られた当てはめを用いて、前立腺に関係するRIQFを抽出するが、これは対応する調整(トレイニング)画像から全てのモデルに関係する領域のためである。モノクロ2値画像にmを当てはめる方法は、上記のグレースケール(白黒画像)セグメンテーション法の変形である:目標関数、log p(mに相対的l) + log p(m)、は同一型の関数、画像マッチ(適合)+ジオメトリックティピカリティ(幾何学的典型性)により置き換えられるが、ここで、2値画像マッチは、mにより示されるモノクロ2値及び境界の間の距離から計算される、またここでジオメトリックティピカリティは、mの滑らかさ、畳み込み無し、及び幾何学的規則性を与える。
【0060】
m−repが初期化された後、即ち対象物に対して大雑把に位置づけられ、また方向付けられた後、このm−repは、例えば、画像強度を含む目標関数、及び/又は変形したDSM及び標的画像の間の適合の度合いの指標を計算する非強度項を最適化することにより変形できる。
【0061】
セグメンテーション−ステップ1:初期化
形態は、しばしば、全体的な平行移動、回転、拡大縮小で不変な対象物のジオメトリーとして定義される。従って、計算される可変性が形態変化のみであることを保証するために、調整目標を通例の位置、配向及び大きさにアライン(位置あわせ)しなければならない。一つの通例のアラインメント技術は、全体としての平行移動、回転、拡大縮小に関して、対応するデータ地点間の距離の二乗の和を最小化することを含む。
【0062】
従って、典型的m−rep初期化のアルゴリズムは、(1)平行移動、(2)回転及び拡大縮小、及び(3)反復からなるステップを含むことができる。従って、例えば、平行移動は、各モデルを平行移動することによる、複数のm−repモデルの画像への集中化を含み、その結果メディアルアトム位置の平均は、任意の原点に局在する。その後、特定のモデルを選択し、残りのモデルの平均に揃えることができる。この処理は、繰り返され、アラインメントの基準をさらに小さくできなくなるまで繰り返すことができる。
【0063】
他の典型的なm−rep初期化アルゴリズムは、平行移動、回転、及び拡大縮小だけではなく、次項に記載するように、その後、対象物の統計的に可能な事例内での変形を含むことができて、しかも一方において、平行移動、回転、拡大縮小間の繰り返し、他方において、変形の繰り返しを伴う。
【0064】
セグメンテーション−ステップ2:変形
形態ばらつきの解析に基づく方法は、医学的イメージングにおいて、広範囲に及びつつある。これらの方法により、画像情報自体はしばしば充分強くない、タスク(課題)以前の形態知識の統計的モデリングが、タスクを自動的に解決することを可能にする。セグメンテーションにおける変形可能なモデル使用の一例は、統計的形態モデルによる、好ましい変形の決定を含む。他の重要なタスクは、形態解析と分類であるが、ここで統計的形態モデルは、診断方法のために健康な器官及び疾患の器官の分布を提供する。
【0065】
統計的形態モデルの最も一般的な形式は、変形を伴う平均形態である。平均及び対応する変形は、調整データの収集からの形態の統計的解析を通して構築された。調整セットにおける各形態は選択された形態表現により示され、表現のパラメーター解析により平均、及びばらつきが得られる。
【0066】
統計的形態モデルの他の形式はある平均からの前変形を初期化すること、及びその初期化からの変形を含む。プランニング画像から分節化したm−repから、介入がガイドする画像から分節化したm−repへの変形が一例である。
【0067】
m−repを、同一患者の異なる画像由来の形態上で、及び/又は異なる患者の画像を横断して、調整できることは評価される。同一患者による調整により、例えば、異なる程度の直腸、及び/又は膀胱の貯留のような、前立腺に働く機械的な力による;及び患者間で生ずる自然の差異による;形態差異を記載する統計が提供される。異なる患者からの画像による調整により、個々の患者間の解剖学的な差異を記載する統計が提供される。
【0068】
変形:外観をベースとする:ピクセル強度
上記のように、PGAは、m−repに適用できるが、ここでm−repはp(m)と言う形で対象物のジオメトリーを表現できる。PCAはmに相対的な領域に対するRIQFに適用できるが、ここでRIQFはp(mに相対的なl)という形で対象物に相対的な外観を表現する。従って、mに相対的なl、をPCAに従わせるために、対象物境界に隣接した外部及び内部領域に対するピクセル強度は、mにより示される対象物境界に対して近く、また内部の領域を記載するRIQFにより表現できるが、ここでこのRIQFはその領域の強度の累積ヒストグラムの逆関数を表す。
【0069】
図5は、本発明の実施態様に従い、画像強度値のサンプリングに適した、CT画像における前立腺の3直交線表現である。図5を参照すると、3直交線CT表示500は、前立腺内の画像強度をサンプリングするための領域502及び前立腺の外側の画像強度をサンプリングするための領域504を含む。画像強度のサンプリングは、対象物境界近く及び内部の領域を対象物に対するRIQFで記載する関数を用いるが、対象物境界に隣接した内部及び外部領域における画像強度のサンプリングは、対象物のジオメトリーをPCAに対して適切にするために必要であろう。
【0070】
図6は、本明細書に記載した実施態様に従い、RIQF解析のために準備した典型的なm−rep対象物モデルの表現を含む。右側に、膀胱m−rep対象物モデル600を示す。左側に、対象物600を、このm−repに基づいて定義された境界及びスポーク関連領域602により定義することができる。その後、スポーク関連領域602を用いて、各スポークに対応する内部及び外部領域を作ることができて、及びこれらの領域を用いて、各領域に対するRIQFに基づく外観モデルを提供することができる。このアイデアは、均一組織の領域は、異なる患者における標的対象物に関して同一位置であり、また類似の組織組成を持つであろうと言うことである。対象物境界の外部領域がそのRIQFが画像マッチに貢献する外部領域を定義するために用いられる際、調整においてこれらのクラスターで定義される対象物境界上の外部領域が、スライドし(滑り)回ることを可能にすることにより、改善された外観モデルを、得ることができるであろう。
【0071】
図7は、本明細書に記載した実施態様に従い、調整画像に由来する膀胱、及び前立腺に対するRIQF(上部)、及びそこに由来するヒストグラム(下部)の一連のプロットである。図7を参照すると、一対の画像700は、膀胱対象物に対するRIQFを描写し、また一対の画像702は、前立腺対象物に対するRIQFを描写するが、他方第1及び第3コラムは、調整画像からのRIQF及びヒストグラムを示す、また第2及び第4カラムにおける破線曲線は平均からの±1.5σ(実線で表す)を示す。一対の画像704及び706は、それぞれ、RIQF700及び702に対するヒストグラムを表す。
【0072】
変形:外観をベースとした:テクスチャー特性
強度変量のみを用いただけは背景から対象物を分離することは不可能であるが、ある画像に対する一つの例において、テクスチャー特性は、背景から対象物を分離する重要なセパレーター(分離手段)を提供する。本明細書で用いるように、一つの態様に依れば、用語"テクスチャー"及び"テクスチャー特性"は、関係する成分を有するデジタル画像において1又は2以上のピクセルの収集を含む。他の態様によると、テクスチャーは、周期的に配列した初期テクスチャーの空間的配列を含むことができるが、ここで初期テクスチャーは、最も単純な又は基本的な下位パターンを表す一群のピクセルである。例えば、あるテクスチャーは、ピクセル強度及び/又は初期テクスチャー間の空間的関係により、細かい、粗い、滑らか、又は粒状であることができる。
【0073】
例えば、CTにおいて、肺葉内の気管支及び血管のパターンは、肺葉又は肺を心臓から分節化する上で重要であることができる。m−repの後部の最適化によるセグメンテーションによると、テクスチャー変量上のRIQFが、強度変量上にRIQFとコンカテネートした(結びついた)幾つかの場合、改良されたセグメンテーションが、得られることが示唆される。
【0074】
一つの実施態様によると、超音波プローブに垂直な面における6個の2Dの回転しても不変なテクスチャー特性を用いることができる。次に、Gaussian又はLaplacianフィルターを含むがこれらに限られない、フィルターをテクスチャー特性に適用できる。さらに、第1微分又は第2微分Gaussianの複数の配向に関して、最大応答を得ることができる。平均外部記載に対する平均内部記載のMahalanobis距離、又はその逆関数に基づき、各テクスチャー特性を、前立腺の内部と外部を識別する能力により評価することができる。
【0075】
例えば、本明細書に記載した実験データを用いて、全体規模で最善を行うテクスチャー特性は、小規模2次微分Gaussianフィルターに基づく。全体としての内部及び外部領域に対して、この(テクスチャー)特性の感度が、強度のみを用いるより、2.9倍高いことは評価できる。従って、テクスチャーRIQFと共に強度RIQFは、本明細書に記載された目的関数に対して、強く識別する画像位置合わせ項に対する基礎を提供できる。
【0076】
この場合テクスチャー特性は、Gaussianの方向付けられた2次微分を伴うコンボリューション(畳み込み演算)の結果の画像平面における配向に関して最大であった。この指標を選んだ理由は、これが、前立腺に対して外部の全体的領域に対するRIQFと、全体の内部領域を良く分離することを示したからである。
【0077】
変形:情報に基づく解剖
画像強度パターンのみを用いることに加えて、画像の成功したセグメンテーションは、解剖の知識及び解剖に関連した画像強度パターンの両者によることができる。従って、セグメンテーションは、標的対象物ジオメトリーの解剖学的に妥当な例に制限することができる。問題となる対象物のジオメトリーの表現m上の確率密度p(m)により、解剖の知識は獲得され;及び、我々の理解では、条件付き確率(下式)
【数1】

に等しいp(mに相対的なl)により、画像知識は獲得される。
【0078】
そこで、セグメンテーションは、
(i)mを、問題となる器官を妥当に表す、幾何学的に折り畳まれてない、滑らかな構造に対応する、初期モードのみをカバーする空間Sに制限すること;及び
(ii)lにより表される画像強度パターンが与えられた時、そのような最も有望なmを見出すこと;
を含む。
【0079】
即ち、mにより表されている解剖学的対象物(複数も可能)を分節化するために、下式
【数2】

は、p(m)において表されているばらつきの初期様式の係数について、下式
【数3】

の共役勾配(コンジュゲートグラディエント)最適化により計算できる。あるいは関数最適化は、初期化の際提供された情報からの変位を反映する項をさらに含むことができる。
【0080】
関数、p(m)及びp(mに相対的なl)、の見積を可能にするために、m及びmに相対的なlの両者の表現は、PGAに対して妥当であること;及び両関数が、それぞれ、ジオメトリー及び画像強度パターンを充分に記載すること;が必要である。従って、上記のように、mはm−repを用いて表すことができる;及びlは本発明に従い、RIQFを用いて記載することができる。
【0081】
実験結果
図8は、本発明の実施態様に従い、様々な方法を用いて作成した前立腺境界を描写する一連の典型的なTRUS画像である。図8を参照すると、TRUS画像800は、前立腺の中央を薄切りした前立腺の分節化してない画像であり;画像802はマニュアルセグメンテーション境界808を描写し;画像804は、マニュアルセグメンテーション境界810に相対的なGaussianをベースとしたテクスチャーパラメーターの2次微分を描写し;及び画像806は強度及びテクスチャーRIQFをベースとした外観モデルを伴う、m−repの後部最適化を経由したセグメンテーション境界812を描写する。画像806で示されたセグメンテーション境界812の不正確さは、画像において前立腺のカットオフを考慮しない結果であると評価される。
【0082】
図9Aは、膀胱及び前立腺の表面表現である。図9Bは、それぞれ自動化したセグメンテーションを含む前立腺及び膀胱の表現である。
図10Aは、膀胱の表面表現である。図10Bは、熟練者によるセグメンテーション;及びコンピューターをベースとしたセグメンテーション;を含む膀胱の表現である。図10Cは、自動化したセグメンテーションを含む膀胱の正中軸切片である。
【0083】
図11Aは、熟練者によるセグメンテーション;及びコンピューターベースのセグメンテーション;を含む前立腺の3D表現である。図11Aを参照すると、ワイアーメッシュ1100は、本発明の実施態様に従い、ソフトウェア128により自動的に作り出した、3D前立腺境界を描写する。表面1102は、熟練者によりマニュアルで作られた前立腺の表面境界を描写する。図11Bは、前立腺のCT切片であり、ここで前立腺境界1104は、図11Aに示した境界1100に対応する。同様に、図12は、自動化したセグメンテーション境界1200;及び熟練者セグメンテーション境界1202;を含む前立腺の3D表現である。
【0084】
図13は、本発明の実施態様に従う、一連のRIQFのプロットである。図13を参照すると、図Aは、前立腺の内部及び外部全体領域に対するテクスチャーRIQFを描写する。図Bは、前立腺の平均RIQFを描写する。図C及びDは、平均RIQF及び平均からの±1.5σを表す。
【0085】
図14は、本発明の実施態様に従い、熟練者の作ったコントゥアに当てはめられた複数のm−repから計算した、一連の2個の初期固有モードからの試料である。図14を参照すると、PGAの結果が描写されており、ここで平均m−repはm−rep1408である。列(m−rep1400〜1404,1406〜1410,及び1412〜1416)は、第1モードに沿って−1.5σから+1.5σの範囲であり、行(m−rep1400,1406,1412;1402,1408,1414;及び1404,1410,1416)は、第2モードに沿って−1.5σから+1.5σまで広がる。第1モードは、患者を横断する全体規模を捕捉し;他方第2モードは、前立腺/直腸境界のサドルバッグ様の外観を捕捉する。
【0086】
図15A〜15Cは、男性骨盤の一連のCT走査である。図15Aを参照すると、CT切片は、収縮した直腸のバルーンを伴う男性骨盤ファントムである。図15Bは、膨張した直腸バルーンを伴うFEM計算の切片を描写する。図15Cは、膨張した直腸バルーンを伴う、現実のCT切片を描写する。
【0087】
変形:機械的シミュレーション
上記のように、m−repは、前立腺のような解剖学的対象物のジオメトリーを表すために自動的に組み立てた3D6面体メッシュ(網目)に対する枠組みを提供する。m−repの多くの可能な変形をシミュレートするために、身体的に正しい機械的変形を計算することができて、その一つの例として、有限要素法(FEM)がある。本明細書で用いる様に、FEMは、完全に微分方程式を使わない;又は標準的な技術を用いて解かれる常微分方程式を用いて式を近似する;のいずれかにより、偏微分方程式及び積分方程式に対する近似解を見出すための数値技術である。本発明の範囲から離れることなく、他の技術も用いることができる。
【0088】
m−repを形成するメディアルアトムメッシュ内の各四辺形は、メディアルシートの各側に1個の、スポークの2個の四辺形を形成する。スポークの各四辺形は、6面のエンティティ(実体)を形成し、これは更にスポーク再分割及び内挿により再分割できる。得られた正確なメッシュを、他の対象物も恐らく含め、解剖学的対象物の外部に当て嵌まるようにメッシュに埋め込むことができる。この領域への力の効果をシミュレートするために;又は機械的に妥当な変形に当てはめるために;全体としてのメッシュを用いて、確立したFEM法の機械的微分方程式を解くことができる。
【0089】
従って、内部の力により引き起こされた対象物モデルの変形は、FEMのような機械的モデリング法により学習されることができる;及び結果としての変形の統計は、FEMの結果から抽出したm−repに導くことができる。
【0090】
この可能性は、前立腺に埋め込まれた金属シード及び直腸内バルーンカテーテルを伴う組織に等価な骨盤ファントムのCT走査を用いて正当と確認された。計算は3Dであったが、明確にさせるために2D結果を示すことは評価できる。非変形の前立腺のシードは、膨張したバルーンにより変形した前立腺に対応する位置に、CTヴォクセルサイズのみにより制限される精度で、マップできる。この方法は、調整画像に当てはめたm−rep上の身体的に正しい変形を計算するために適用して、ジオメトリックな調整に対する付加的なm−repを作ることができる;及び調整したm−repを経由してマップしたアトラスの空間的な精度を有効と確認することができる。
【0091】
介入標的領域を介入がガイドする画像に送る
プランニング画像、又はそこに記録した他の画像から抽出した介入標的領域は、プランニング画像から分節化した解剖学的対象物のm−repの下位領域を作る。一つの例において、プランニング画像は、MRIであり;解剖学的対象物は前立腺であり;及び介入標的領域は、MRS画像において癌の疑いありと描写された組織である。プランニング画像において分節化したその形;及び介入がガイドする画像におけるその形;の間のm−repの変形は、対象物の内部の全てのポイントの変換をもたらすが、ここで対応するスポーク上の長さの割合に従って対応する位置は、互いにマップすると言う規則に従って変形する。この変形を、プランニング画像から分節化した解剖学的対象物における介入標的領域に適用し、介入がガイドする画像における、予想された介入標的領域をもたらすことができる。
【0092】
調整とセグメンテーション
介入がガイドする画像上にM−repを重ね合わせ
図16は、本発明の実施態様に従い、検討すべき対象物のm−rep境界の重ね合わされた画像を含む典型的なTRUS画像である。図9を参照すると、前立腺の3DTRUS画像が示され、ここでm−repを、画像に対するヒト・コントゥアに当てはめて、96.6%のメディアン体積重なり(即ち、Dice係数)及び0.36mmのメディアン平均表面分離をもたらす。本明細書で用いるように、Dice類似係数(DSC)は、A及びBセットの間の面積/体積重なりを下式
【数4】

で定義する。雑音の多いTRUS画像に由来する形態モデル表現は、等しく良い重なりを狙うべきである。図9に示した当てはめは、素晴らしく、解剖学的構造を含む対象物のプランニング画像を、介入をガイドする対象物画像データにマッピングさせるための要件;及びそれにより、プランニング画像からの解剖学的構造内の介入標的領域を、介入がガイドする画像にマッピングさせるための要件;をかなえる。
【0093】
可能な応用例
一つの態様によると、介入をガイドして、画像により針をガイドするために、本発明を用いることができる。例えば、1又は2以上の画像が与えられると、あるm−repモデルをプランニング画像内(例えば、前立腺)の対象物に当てはめる。そして、このm−repモデルは、介入がガイドする画像中の対象物に当てはめられる。そして、これらの画像間の介入標的領域のマッピングを用いて、バイオプシ又は手術の際医師のバイオプシ針をガイドする。
【0094】
例えば、図17は、本発明の実施態様に従い、TRUS画像に重ね合わされた、患者特異的な前立腺m−rep及び介入標的領域のガイドの下に、バイオプシ針の前立腺へのガイドを描写する。図17を参照すると、経直腸の超音波プローブ1700を、患者の直腸1702に挿入する。その結果、プローブ1700は、患者の前立腺を囲む領域のTRUS画像1704を作り、表示装置上に画像を表示できる。次に、患者の前立腺のm−repモデルは、TRUS画像1704に重ね合わせることができて、ここでこのm−repは前立腺境界1706を定義することを助ける。前立腺境界1706内において、介入標的領域1708を描写することができる。例えば、癌の疑いのある前立腺の一部に、針1710を用いてバイオプシできる。上記で詳細に述べたように、m−repを用いて、TRUS画像1704のような、介入がガイドする画像上に、対象物境界1706を正確に示して、バイオプシ針1710を、標的対象物1708まで正確にガイドすることができる。そのため他の組織を乱すことがない。
【0095】
他の例において、癌治療のために、ブラキ療法(brachytherapy、小線源療法)と呼ばれる処置において、放射活性のあるシードを置くために用いられる針を、上述のバイオプシ例と同様な技術によりガイドすることができる。
他の例において、本発明を、大脳皮質又は皮質下脳構造の形態測定のために用いることができる。脳における幾つかの構造の形態は、ある神経状態と相関すると考えられている。MR画像で見られる皮質下脳構造又は大脳皮質の体積及び形態の特徴は、成人早発性痴呆症及び統合失調症と関係する。例えば、本発明を用いて、自閉症のリスクがあると判断された、個人の子供時代に開始した長期にわたるMR画像の皮質下脳構造の吟味をすることができる。時間経過による形態の変化の観察のために、及びこれらの変化と臨床的症状を関係づけるために、及び疾病の改善された治療のために、研究が行われている。
【0096】
他の例において、本発明を用いて、MRIで画像化された膝軟骨の深さのパターン及び湾曲への関節炎薬剤の効果の測定法の開発のような、関節炎の膝軟骨の治療を改善することができる。
【0097】
他の例において、本発明を用いて、筋肉損傷を見積もるために、心拍モデルを作成できる。一つのシナリオにおいて、虚血疾患(心筋への血流の減少)を持った患者の心拍のm−repモデルを用いて、血流が減少している筋肉の領域を限定することができて、また正常心拍の調整したm−repモデルと比較して、どの程度深刻に筋肉が冒されているのか判断できる。特殊なCT,MR及びUS技術により作ることができる、所謂4D画像(3Dプラス時間)から作られたモデルは、研究されるであろう。もし成功したならば、虚血疾患の患者を判断し、また適切な治療を計画するための安全な非浸襲的手技であろう。
【0098】
他の例において、本発明を用いて、慢性閉塞性呼吸器系疾患(COPD)を研究し、また治療することができる。m−repを用いて、呼吸サイクルの様々な部分で獲得したm−rep及びCT画像を用いて肺の画像を自動分節化することにより、患者のCOPDの進行を研究できる。m−repの形態測定特性を用いて、閉塞した肺組織の体積を限定し、測定することができる。
【0099】
他の例において、本発明を用いて、治療の間患者の呼吸による運動及び形態変化をする、肺及び肝臓における腫瘍の治療を改善できる。m−repを用いて、複数の呼吸サイクルの間、複数の間隔で取り込んだCT画像における、標的対象物及び近接した器官を分節化できる。その後、セグメンテーションにより4Dモデルを構築して、患者の呼吸サイクルの間の変化を予想することができる;及び治療計画及び治療実施の間のこれらの変化を説明できる。
【0100】
更に他の例において、本発明を用いて、頭頚部における癌の放射線治療計画を改善できる。例えば、m−repを用いて、リンパシステム下位領域と共に、頭頚部の両側の15又はそれ以上の対象物が、臨床的に重要な解剖学的構造である領域である、頭頚部の腫瘍の放射線治療を計画することができる。
【0101】
他の可能な応用として、コンピューター支援のデザイン、重要な製作及び構造物部品のシミュレートされたストレス検査、及び漫画製作を含むが、これらに限られない。本明細書で述べたこれらの応用は、広い範囲の可能な製品分野を強調するだけである。前述した事柄は、幾つかの進行中の又は計画中の医学研究プロジェクトを含むが、本発明を、医学的画像における解剖学的対象を抽出するための方法として、統計的に調整した形態物指し、即ち、形態統計に基づいて測定し、識別する方法、例えば、(正常な)1クラス(部類)の形態を他の(疾病の)クラスから区別する方法として、あるいはその両者として、用いることができる。
【0102】
本発明の有利な効果
本発明は、可視標的を示すために、非超音波画像からの癌領域をTRUSバイオプシ画像にマッピングを行い、医師がより正確に彼/彼女の器具を向けることを可能にすることにより、公知技術の短所を克服できる。患者にとっての正味の恩恵は、バイオプシの繰り返し回数の減少;ネガティブバイオプシが偽りであるかどうか、又は低いGleasonスコアは偽りで低いかどうかの不確かさに関係する心理的ストレスの安楽化;治療法決定の基礎となるより良いデータ;及びクオリティオブライフ(生活の質)の全体としての改善であろう。更に、バイオプシの繰り返しに伴う医療費も減少させるべきである。
【0103】
本発明は、自動的に患者モデルを抽出することにより殆ど全ての人間の介入を取り除くことができる、またこれは、使用者の好ましくない変動性が無いやり方で行われる。
本発明は、イメージング研究、及びバイオプシ処置の際、直腸内プローブにより引き起こされた前立腺の変形を正確に形に表すことができる、またTRUS及びMR画像の間の異なる画像特性を扱うことができる。
【0104】
更に、本発明は、診断のための、手術のための、及び他の治療のための介入の全てに対して応用できることは評価される。
本発明の様々な詳細は、本発明の範囲を離れることなく、変更可能であることは、理解されるであろう。更に、前述の記載は本発明は別に述べたクレイムにより定義されたように、描写のみを目的としており、制限付けを目的にしたものではない。
【符号の説明】
【0105】
100 コンピューター
109 バス(母線)
111 遠隔のコンピューター
113 表示装置
114 マウス
116 キーボード
128、130 ソフトウェア
1700 超音波プローブ
1702 患者の直腸
1704 TRUS画像
1706 前立腺境界
1708 介入標的領域
1710 バイオプシ針
【特許請求の範囲】
【請求項1】
ある画像における解剖学的構造から成る対象物のモデルを、他の画像における対象物の画像データにマッピングする方法であって、
(a)対象物の少なくとも第1事例の画像データに基づく解剖学的構造から成る初期"内側表現対象物モデル(m−rep)"を作成する段階、
(b)この対象物の少なくとも第2事例は患者に関連し、この対象物の少なくとも第2事例の画像データのプラン(プランニング画像データ)に基づいて当該初期内側表現対象物モデル(m−rep)を変形することにより、この患者に特異的な内側表現対象物モデル(m−rep)を作成する段階、
(c)このプランニング画像データに記録された"介入標的領域"を特定する段階、及び
(d)この患者に特異的な内側表現対象物モデル(m−rep)及びこの介入標的領域を、上記対象物の少なくとも第2事例の"介入がガイドする画像データ"に関係づける段階、
から成る方法。
【請求項2】
(e)前記プランニング画像データにおけるm−repと前記"介入がガイドする画像データ"におけるm−repとの間の変換から導き出されたマッピングを用いて、"介入がガイドする画像データ"における"介入標的領域"を特定する段階を含む請求項1に記載の方法。
【請求項3】
前記プランニング画像データが、磁気共鳴イメージング(MRI)データ及び磁気共鳴分光イメージング(MRSI)データを含み、このMRSIデータが、介入標的領域を決定するための、このMRIデータに記録された画像を含む請求項1に記載の方法。
【請求項4】
前記"介入がガイドする画像データ"が、1又はそれ以上の超音波(US)画像データ及び経直腸的超音波(TRUS)画像データを含む請求項1に記載の方法。
【請求項5】
前記解剖学的構造が、膀胱、前立腺、心臓、脳構造、肝臓及び肺のなかの1つを含む請求項1に記載の方法。
【請求項6】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、前記対象物の形態可変性のモードを解剖学的に可能な可変性に制限することを含む請求項1に記載の方法。
【請求項7】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、主ジオデシック(測地学)解析(PGA)の使用して、前記対象物の形態可変性のモードをパラメーター化することを含む請求項1に記載の方法。
【請求項8】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、有限要素法(FEM)の使用して、前記対象物の可能な変形をシミュレートし形作ることを含む請求項1に記載の方法。
【請求項9】
前記初期m−repを作成する段階が、この対象物に対する調整データに基づいて初期m−repを変形することを含み、初期m−repを変形すること又は患者に特異的なm−repを変形することが、画像強度値に基づいてm−repを変形することを含み、この変形されるm−repを、プランニング画像又は介入がガイドする画像へ適合させることを調整するために、領域の強度変位値関数と主成分解析が用いられる請求項1に記載の方法。
【請求項10】
有限要素法(FEM)に基づいて複数の形態変化シナリオを事前コンパイルすること、及び、対象物が変形される介入処置の際、この対象物変形に形態変化シナリオを合わせるための検査を実行することを含む請求項1に記載の方法。
【請求項11】
バイオプシ処置の際、前記対象物の変形に基づいて、有限要素法(FEM)により形態変形シミュレーションを計算することを含む請求項1に記載の方法。
【請求項12】
前記患者特異的m−rep、前記介入標的領域、及び前記"介入がガイドする画像データ"を、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて、同時に表示することを含む請求項1に記載の方法。
【請求項13】
前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて同時に表示すること、及び、この重ね合わせた画像を、手術の間、手術機器をガイドするために用いることを含む請求項1に記載の方法。
【請求項14】
前記重ね合わせて同時に表示された患者特異的m−repを、大脳皮質及び皮質下脳構造の形態測定のために用いることを含む請求項13に記載の方法。
【請求項15】
前記重ね合わせて同時に表示された患者特異的m−repを、心拍モデルを作成して筋肉障害を評価するために用いることを含む請求項13に記載の方法。
【請求項16】
前記重ね合わせて同時に表示された患者特異的m−repを、慢性閉塞性呼吸器系疾患(COPD)の観察又は発見のために用いることを含む請求項13に記載の方法。
【請求項17】
前記重ね合わせて同時に表示された患者特異的m−repを、呼吸運動下で解剖学的構造の放射線治療を行うために用いることを含む請求項13に記載の方法。
【請求項18】
前記重ね合わせて同時に表示された患者特異的m−repを、画像でガイドされた前立腺バイオプシのために用いることを含む請求項13に記載の方法。
【請求項19】
前記重ね合わせて同時に表示された患者特異的m−repを、画像でガイドされた前立腺ブラキ療法を含む、画像でガイドされたブラキ療法のために用いることを含む請求項13に記載の方法。
【請求項20】
前記重ね合わせて同時に表示された患者特異的m−repを、頭頚部の癌の放射線治療計画のために用いることを含む請求項13に記載の方法。
【請求項21】
前記患者特異的m−repを作成する段階が、対象物形態及び内部の疑わしい領域の患者特異的アトラスを作成することを含む請求項1に記載の方法。
【請求項22】
ある解剖学的構造から成る対象物のプランニング画像モデルを、"介入がガイドする対象物の画像データ"にマッピングするためのシステムであって、
(i)ある解剖学的構造から成る対象物の"内側表現対象物モデル(m−rep)"を作成するため、及び、この対象物の少なくとも第1事例のプランニング画像データに基づいて、この対象物内の"介入標的領域"を特定するための、"対象物モデルジェネレーター"、及び
(ii)この"内側表現対象物モデル(m−rep)"及びこの"介入標的領域"を、プランニング画像から変形した、対象物の少なくとも第1事例の"介入がガイドする画像データ"に関係づけるための、"対象物モデルを変形してマッピングするモジュール"、
から成るシステム。
【請求項23】
前記"対象物モデルジェネレーター"が、1又は2以上の磁気共鳴イメージング(MRI)データ及びコンピューター断層撮影(CT)画像データに基づいて、m−repを生成するように構成されている請求項22に記載のシステム。
【請求項24】
前記"対象物モデルを変形してマッピングするモジュール"が、前記m−repを、1又は2以上の超音波(US)画像データ及び経直腸超音波(TRUS)画像データに関連付けるように構成されている請求項22に記載のシステム。
【請求項25】
前記"対象物モデルジェネレーター"が、膀胱、前立腺、心臓、脳構造、肝臓及び肺のうちの1つに基づいて、前記m−repを生成するように構成されている請求項22に記載のシステム。
【請求項26】
前記"対象物モデルジェネレーター"が、対象物モデルの形態変化のモードを、解剖学的に可能な変形に制限するように構成された請求項22に記載のシステム。
【請求項27】
前記"対象物モデルジェネレーター"が、主ジオデシック解析(PGA)を使用して、対象物の形態変化のモードをパラメーター化するように構成された請求項22に記載のシステム。
【請求項28】
前記"対象物モデルジェネレーター"が、有限要素法(FEM)を用いて、対象物の可能な変形をシミュレートし、形作るように構成された請求項22に記載のシステム。
【請求項29】
前記"対象物モデルを変形してマッピングするモジュール"が、画像強度値に基づいて、対象物モデルを変形するように構成された請求項22に記載のシステム。
【請求項30】
前記"対象物モデルを変形してマッピングするモジュール"が、有限要素法(FEM)に基づいて複数の形態変化シナリオを事前コンパイルするように構成され、かつ、対象物が変形される介入処置の際、この対象物変形に形態変化シナリオを合わせるための検査を実行するように構成された請求項22に記載のシステム。
【請求項31】
前記"対象物モデルを変形してマッピングするモジュール"が、バイオプシ処置の際、前記対象物の変形に基づいて、有限要素法(FEM)により形態変形シミュレーションを計算するように構成された請求項22に記載のシステム。
【請求項32】
前記"対象物モデルを変形してマッピングするモジュール"が、前記患者特異的m−rep、前記介入標的領域、及び前記"介入がガイドする画像データ"を、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて、同時に表示するように構成された請求項22に記載のシステム。
【請求項33】
前記"対象物モデルを変形してマッピングするモジュール"が、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて同時に表示するように構成され、この重ね合わせた画像が、手術の間、手術機器をガイドするために用られる請求項22に記載のシステム。
【請求項34】
前記重ね合わせて同時に表示されたm−repが、大脳皮質及び皮質下脳構造の形態測定のために用いられる請求項33に記載の方法。
【請求項35】
前記重ね合わせて同時に表示されたm−repが、関節炎の治療中に膝軟骨を観察するために用いられる請求項33に記載の方法。
【請求項36】
前記重ね合わせて同時に表示されたm−repが、心拍モデルを作成して筋肉障害を評価するために用いられる請求項33に記載の方法。
【請求項37】
前記重ね合わせて同時に表示されたm−repが、慢性閉塞性呼吸器系疾患(COPD)の観察又は発見のために用いられる請求項33に記載の方法。
【請求項38】
前記重ね合わせて同時に表示されたm−repが、呼吸運動下で解剖学的構造の放射線治療を行うために用いられる請求項33に記載の方法。
【請求項39】
前記重ね合わせて同時に表示されたm−repが、頭頚部の癌の放射線治療計画のために用いられる請求項33に記載の方法。
【請求項40】
前記重ね合わせて同時に表示されたm−repが、画像でガイドされた前立腺バイオプシのために用いられる請求項33に記載の方法。
【請求項41】
前記重ね合わせて同時に表示されたm−repが、画像でガイドされた前立腺ブラキ治療のために用いられる請求項33に記載の方法。
【請求項42】
前記"対象物モデルジェネレーター"が、患者特異的m−rep及び対象物形態の患者特異的アトラスを作成するように構成され、かつ、このm−rep内の対象物相対座標における内部の疑わしい領域を表示するように構成された請求項22に記載のシステム。
【請求項43】
コンピューターのプロセッサーにより処理されたときに以下の段階を実行するように、コンピューターが実行可能な指令が保存された、コンピューターで読み取り可能な媒体。
(a)対象物の少なくとも第1事例の画像データに基づく解剖学的構造から成る初期"内側表現対象物モデル(m−rep)"を作成する段階、
(b)この対象物の少なくとも第2事例は患者に関連し、この対象物の少なくとも第2事例の画像データのプラン(プランニング画像データ)に基づいて当該初期内側表現対象物モデル(m−rep)を変形することにより、この患者に特異的な内側表現対象物モデル(m−rep)を作成する段階、
(c)このプランニング画像データに記録された"介入標的領域"を特定する段階、及び
(d)この患者に特異的な内側表現対象物モデル(m−rep)及びこの介入標的領域を、上記対象物の少なくとも第2事例の"介入がガイドする画像データ"に関係づける段階
【請求項1】
ある画像における解剖学的構造から成る対象物のモデルを、他の画像における対象物の画像データにマッピングする方法であって、
(a)対象物の少なくとも第1事例の画像データに基づく解剖学的構造から成る初期"内側表現対象物モデル(m−rep)"を作成する段階、
(b)この対象物の少なくとも第2事例は患者に関連し、この対象物の少なくとも第2事例の画像データのプラン(プランニング画像データ)に基づいて当該初期内側表現対象物モデル(m−rep)を変形することにより、この患者に特異的な内側表現対象物モデル(m−rep)を作成する段階、
(c)このプランニング画像データに記録された"介入標的領域"を特定する段階、及び
(d)この患者に特異的な内側表現対象物モデル(m−rep)及びこの介入標的領域を、上記対象物の少なくとも第2事例の"介入がガイドする画像データ"に関係づける段階、
から成る方法。
【請求項2】
(e)前記プランニング画像データにおけるm−repと前記"介入がガイドする画像データ"におけるm−repとの間の変換から導き出されたマッピングを用いて、"介入がガイドする画像データ"における"介入標的領域"を特定する段階を含む請求項1に記載の方法。
【請求項3】
前記プランニング画像データが、磁気共鳴イメージング(MRI)データ及び磁気共鳴分光イメージング(MRSI)データを含み、このMRSIデータが、介入標的領域を決定するための、このMRIデータに記録された画像を含む請求項1に記載の方法。
【請求項4】
前記"介入がガイドする画像データ"が、1又はそれ以上の超音波(US)画像データ及び経直腸的超音波(TRUS)画像データを含む請求項1に記載の方法。
【請求項5】
前記解剖学的構造が、膀胱、前立腺、心臓、脳構造、肝臓及び肺のなかの1つを含む請求項1に記載の方法。
【請求項6】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、前記対象物の形態可変性のモードを解剖学的に可能な可変性に制限することを含む請求項1に記載の方法。
【請求項7】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、主ジオデシック(測地学)解析(PGA)の使用して、前記対象物の形態可変性のモードをパラメーター化することを含む請求項1に記載の方法。
【請求項8】
前記初期m−repを作成する段階又は患者に特異的なm−repを作成する段階が、有限要素法(FEM)の使用して、前記対象物の可能な変形をシミュレートし形作ることを含む請求項1に記載の方法。
【請求項9】
前記初期m−repを作成する段階が、この対象物に対する調整データに基づいて初期m−repを変形することを含み、初期m−repを変形すること又は患者に特異的なm−repを変形することが、画像強度値に基づいてm−repを変形することを含み、この変形されるm−repを、プランニング画像又は介入がガイドする画像へ適合させることを調整するために、領域の強度変位値関数と主成分解析が用いられる請求項1に記載の方法。
【請求項10】
有限要素法(FEM)に基づいて複数の形態変化シナリオを事前コンパイルすること、及び、対象物が変形される介入処置の際、この対象物変形に形態変化シナリオを合わせるための検査を実行することを含む請求項1に記載の方法。
【請求項11】
バイオプシ処置の際、前記対象物の変形に基づいて、有限要素法(FEM)により形態変形シミュレーションを計算することを含む請求項1に記載の方法。
【請求項12】
前記患者特異的m−rep、前記介入標的領域、及び前記"介入がガイドする画像データ"を、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて、同時に表示することを含む請求項1に記載の方法。
【請求項13】
前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて同時に表示すること、及び、この重ね合わせた画像を、手術の間、手術機器をガイドするために用いることを含む請求項1に記載の方法。
【請求項14】
前記重ね合わせて同時に表示された患者特異的m−repを、大脳皮質及び皮質下脳構造の形態測定のために用いることを含む請求項13に記載の方法。
【請求項15】
前記重ね合わせて同時に表示された患者特異的m−repを、心拍モデルを作成して筋肉障害を評価するために用いることを含む請求項13に記載の方法。
【請求項16】
前記重ね合わせて同時に表示された患者特異的m−repを、慢性閉塞性呼吸器系疾患(COPD)の観察又は発見のために用いることを含む請求項13に記載の方法。
【請求項17】
前記重ね合わせて同時に表示された患者特異的m−repを、呼吸運動下で解剖学的構造の放射線治療を行うために用いることを含む請求項13に記載の方法。
【請求項18】
前記重ね合わせて同時に表示された患者特異的m−repを、画像でガイドされた前立腺バイオプシのために用いることを含む請求項13に記載の方法。
【請求項19】
前記重ね合わせて同時に表示された患者特異的m−repを、画像でガイドされた前立腺ブラキ療法を含む、画像でガイドされたブラキ療法のために用いることを含む請求項13に記載の方法。
【請求項20】
前記重ね合わせて同時に表示された患者特異的m−repを、頭頚部の癌の放射線治療計画のために用いることを含む請求項13に記載の方法。
【請求項21】
前記患者特異的m−repを作成する段階が、対象物形態及び内部の疑わしい領域の患者特異的アトラスを作成することを含む請求項1に記載の方法。
【請求項22】
ある解剖学的構造から成る対象物のプランニング画像モデルを、"介入がガイドする対象物の画像データ"にマッピングするためのシステムであって、
(i)ある解剖学的構造から成る対象物の"内側表現対象物モデル(m−rep)"を作成するため、及び、この対象物の少なくとも第1事例のプランニング画像データに基づいて、この対象物内の"介入標的領域"を特定するための、"対象物モデルジェネレーター"、及び
(ii)この"内側表現対象物モデル(m−rep)"及びこの"介入標的領域"を、プランニング画像から変形した、対象物の少なくとも第1事例の"介入がガイドする画像データ"に関係づけるための、"対象物モデルを変形してマッピングするモジュール"、
から成るシステム。
【請求項23】
前記"対象物モデルジェネレーター"が、1又は2以上の磁気共鳴イメージング(MRI)データ及びコンピューター断層撮影(CT)画像データに基づいて、m−repを生成するように構成されている請求項22に記載のシステム。
【請求項24】
前記"対象物モデルを変形してマッピングするモジュール"が、前記m−repを、1又は2以上の超音波(US)画像データ及び経直腸超音波(TRUS)画像データに関連付けるように構成されている請求項22に記載のシステム。
【請求項25】
前記"対象物モデルジェネレーター"が、膀胱、前立腺、心臓、脳構造、肝臓及び肺のうちの1つに基づいて、前記m−repを生成するように構成されている請求項22に記載のシステム。
【請求項26】
前記"対象物モデルジェネレーター"が、対象物モデルの形態変化のモードを、解剖学的に可能な変形に制限するように構成された請求項22に記載のシステム。
【請求項27】
前記"対象物モデルジェネレーター"が、主ジオデシック解析(PGA)を使用して、対象物の形態変化のモードをパラメーター化するように構成された請求項22に記載のシステム。
【請求項28】
前記"対象物モデルジェネレーター"が、有限要素法(FEM)を用いて、対象物の可能な変形をシミュレートし、形作るように構成された請求項22に記載のシステム。
【請求項29】
前記"対象物モデルを変形してマッピングするモジュール"が、画像強度値に基づいて、対象物モデルを変形するように構成された請求項22に記載のシステム。
【請求項30】
前記"対象物モデルを変形してマッピングするモジュール"が、有限要素法(FEM)に基づいて複数の形態変化シナリオを事前コンパイルするように構成され、かつ、対象物が変形される介入処置の際、この対象物変形に形態変化シナリオを合わせるための検査を実行するように構成された請求項22に記載のシステム。
【請求項31】
前記"対象物モデルを変形してマッピングするモジュール"が、バイオプシ処置の際、前記対象物の変形に基づいて、有限要素法(FEM)により形態変形シミュレーションを計算するように構成された請求項22に記載のシステム。
【請求項32】
前記"対象物モデルを変形してマッピングするモジュール"が、前記患者特異的m−rep、前記介入標的領域、及び前記"介入がガイドする画像データ"を、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて、同時に表示するように構成された請求項22に記載のシステム。
【請求項33】
前記"対象物モデルを変形してマッピングするモジュール"が、前記患者特異的m−repと前記介入標的領域とを、前記"介入がガイドする画像データ"上に重ね合わせて同時に表示するように構成され、この重ね合わせた画像が、手術の間、手術機器をガイドするために用られる請求項22に記載のシステム。
【請求項34】
前記重ね合わせて同時に表示されたm−repが、大脳皮質及び皮質下脳構造の形態測定のために用いられる請求項33に記載の方法。
【請求項35】
前記重ね合わせて同時に表示されたm−repが、関節炎の治療中に膝軟骨を観察するために用いられる請求項33に記載の方法。
【請求項36】
前記重ね合わせて同時に表示されたm−repが、心拍モデルを作成して筋肉障害を評価するために用いられる請求項33に記載の方法。
【請求項37】
前記重ね合わせて同時に表示されたm−repが、慢性閉塞性呼吸器系疾患(COPD)の観察又は発見のために用いられる請求項33に記載の方法。
【請求項38】
前記重ね合わせて同時に表示されたm−repが、呼吸運動下で解剖学的構造の放射線治療を行うために用いられる請求項33に記載の方法。
【請求項39】
前記重ね合わせて同時に表示されたm−repが、頭頚部の癌の放射線治療計画のために用いられる請求項33に記載の方法。
【請求項40】
前記重ね合わせて同時に表示されたm−repが、画像でガイドされた前立腺バイオプシのために用いられる請求項33に記載の方法。
【請求項41】
前記重ね合わせて同時に表示されたm−repが、画像でガイドされた前立腺ブラキ治療のために用いられる請求項33に記載の方法。
【請求項42】
前記"対象物モデルジェネレーター"が、患者特異的m−rep及び対象物形態の患者特異的アトラスを作成するように構成され、かつ、このm−rep内の対象物相対座標における内部の疑わしい領域を表示するように構成された請求項22に記載のシステム。
【請求項43】
コンピューターのプロセッサーにより処理されたときに以下の段階を実行するように、コンピューターが実行可能な指令が保存された、コンピューターで読み取り可能な媒体。
(a)対象物の少なくとも第1事例の画像データに基づく解剖学的構造から成る初期"内側表現対象物モデル(m−rep)"を作成する段階、
(b)この対象物の少なくとも第2事例は患者に関連し、この対象物の少なくとも第2事例の画像データのプラン(プランニング画像データ)に基づいて当該初期内側表現対象物モデル(m−rep)を変形することにより、この患者に特異的な内側表現対象物モデル(m−rep)を作成する段階、
(c)このプランニング画像データに記録された"介入標的領域"を特定する段階、及び
(d)この患者に特異的な内側表現対象物モデル(m−rep)及びこの介入標的領域を、上記対象物の少なくとも第2事例の"介入がガイドする画像データ"に関係づける段階
【図1】


【図2】


【図3A】


【図3B】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9A】


【図9B】


【図10A】


【図10B】


【図10C】


【図11A】


【図11B】


【図12】


【図13】


【図14】


【図15A】


【図15B】


【図15C】


【図16】


【図17】




【図2】


【図3A】


【図3B】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9A】


【図9B】


【図10A】


【図10B】


【図10C】


【図11A】


【図11B】


【図12】


【図13】


【図14】


【図15A】


【図15B】


【図15C】


【図16】


【図17】


【公表番号】特表2011−504115(P2011−504115A)
【公表日】平成23年2月3日(2011.2.3)
【国際特許分類】
【出願番号】特願2010−530175(P2010−530175)
【出願日】平成20年10月20日(2008.10.20)
【国際出願番号】PCT/US2008/080504
【国際公開番号】WO2009/052497
【国際公開日】平成21年4月23日(2009.4.23)
【公序良俗違反の表示】
(特許庁注:以下のものは登録商標)
1.ETHERNET
【出願人】(501345323)ザ ユニバーシティ オブ ノース カロライナ アット チャペル ヒル (52)
【氏名又は名称原語表記】THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL
【住所又は居所原語表記】308 Bynum Hall,Campus Box 4105,Chapel Hill,North Carolina 27599−4105, United States of America
【Fターム(参考)】
【公表日】平成23年2月3日(2011.2.3)
【国際特許分類】
【出願日】平成20年10月20日(2008.10.20)
【国際出願番号】PCT/US2008/080504
【国際公開番号】WO2009/052497
【国際公開日】平成21年4月23日(2009.4.23)
【公序良俗違反の表示】
(特許庁注:以下のものは登録商標)
1.ETHERNET
【出願人】(501345323)ザ ユニバーシティ オブ ノース カロライナ アット チャペル ヒル (52)
【氏名又は名称原語表記】THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL
【住所又は居所原語表記】308 Bynum Hall,Campus Box 4105,Chapel Hill,North Carolina 27599−4105, United States of America
【Fターム(参考)】
[ Back to top ]

