2−アザ−ビシクロ[3.3.0]オクタン誘導体
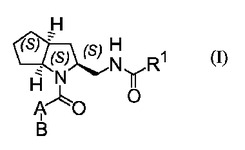
本発明は、式(I)の2−アザ−ビシクロ[3.3.0]オクタン誘導体、
【化1】

(式中、A,B及びR1は明細書中に記載の通りである。)、医薬、特にオレキシン受容体拮抗薬としての、そのような化合物又はその薬学的に許容される塩の使用に関する。
【化1】

(式中、A,B及びR1は明細書中に記載の通りである。)、医薬、特にオレキシン受容体拮抗薬としての、そのような化合物又はその薬学的に許容される塩の使用に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、式(I)の新規な2−アザ−ビシクロ[3.3.0]オクタン誘導体及び医薬としてのこれらの使用に関する。本発明はまた上記化合物の製造方法、式(I)の化合物を1又は2以上含有する医薬組成物、及び特にオレキシン受容体拮抗薬としてのそれらの使用を含む関連した側面に関する。
【背景技術】
【0002】
オレキシン類(オレキシンA又はOX−A及びオレキシンB又はOX−B)は、二つの研究グループによって1998年に発見された新規な神経ペプチド類であり、オレキシンAは、33個のアミノ酸ペプチドであり、オレキシンBは、28個のアミノ酸ペプチドである(Sakurai T.ら、Cell、1998、92、573−585)。オレキシン類は、外側視床下部の離散性神経細胞内で産生され、G蛋白質共役型受容体(OX1及びOX2受容体)に結合する。オレキシン−1受容体(OX1)はOX−Aに対して選択的であり、オレキシン−2受容体(OX2)はOX−Bと同様にOX−Aにも結合することができる。オレキシン類は、ラットにおいて食物消費を刺激し、食行動を調節する中枢フィードバック機構におけるこれらペプチド類のメディエーターとしての生理学的役割を示唆している(Sakurai T.ら、Cell、1998、92、573−585)。他方、オレキシン類は睡眠状態及び覚醒状態を調節しており、ナルコレプシー(睡眠発作)患者に対する潜在的な新規治療への道を開くものであるとも提唱されている(Chemelli R.M.ら、Cell、1999、98、437−451)。
【0003】
オレキシン受容体は哺乳動物の脳に見出され、文献から知られているように、病理学に多くの密接な関係をもっている可能性がある。
【0004】
本発明は、2−アザ−ビシクロ[3.3.0]オクタン化合物を提供し、これらはヒトオレキシン受容体の非ペプチド性拮抗薬である。これらの化合物は、特に、例えば摂食障害、摂水障害(drinking disorders)、睡眠障害又は精神及び神経障害における認知障害の治療における利用可能性を有している。
【0005】
これまでに、OX1か又はOX2のどちらか、あるいは同時に両方の受容体に拮抗する能力を有するいくつかの低分子量化合物が知られている。オレキシン受容体拮抗薬として有用なピペリジン誘導体が国際公開公報第01/96302号に開示されている。
【0006】
本発明は、オレキシン受容体拮抗薬としての2−アザ−ビシクロ[3.3.0]オクタン化合物を初めて記述するものである。
【発明の概要】
【0007】
i) 本発明の第1の側面は、立体中心が(1S,3S,5S)−配置である、式(I)の化合物から成る:
【0008】
【化1】

【0009】
式中
Aは、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン及び、未置換であるか若しくは(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択され;
Bは、アリール−又はヘテロシクリル−基を表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択され;
R1は、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択されるか;又は
R1は、2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表し、当該基は、未置換であるか、又は1若しくは2個の(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンにより独立に置換され;
R2は、水素又は(C1−4)アルキルを表し;
R3は、水素又は(C1−4)アルキルを表す。
【0010】
式(I)の化合物及びその薬学的に許容される塩もまた、本発明の一部である。
【0011】
「ハロゲン」という用語は、フッ素、塩素又は臭素、好ましくはフッ素又は塩素を意味する。
【0012】
「(C1−4)アルキル」という用語は、単独の場合も、組み合わせて用いる場合も、1ないし4個の炭素原子をもつ、直鎖又は分枝鎖アルキル基を意味する。(C1−4)アルキル基の例は、メチル、エチル、プロピル、イソプロピル、n−ブチル、イソ−ブチル、sec.−ブチル又はtert.−ブチルである。好ましくはメチル及びエチルである。最も好ましくは、メチルである。
【0013】
「(C2−6)アルキニル」という用語は、単独の場合も、組み合わせて用いる場合も、2ないし6個の炭素原子をもつ、直鎖又は分枝鎖アルキニル基を意味する。(C2−6)アルキニル基の例は、エチニル、1−プロピニル、1−ブチニル、3−メチル−1−ブチニル、1−ペンチニル、3,3−ジメチル−1−ブチニル、3−メチル−1−ペンチニル、4−メチル−1−ペンチニル又は1−ヘキシニルである。
【0014】
「(C3−6)シクロアルキル」という用語は、単独の場合も、組み合わせて用いる場合も、3ないし6個の炭素原子をもつ、シクロアルキル基を意味する。(C3−6)シクロアルキル基の例は、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである。好ましくはシクロプロピルである。
【0015】
「(C1−4)アルコキシ」という用語は、単独の場合も、組み合わせて用いる場合も、メトキシ、エトキシ、n−プロポキシ、イソプロポキシ、n−ブトキシ、イソブトキシ、sec.−ブトキシ又はtert.−ブトキシ等の、用語(C1−4)アルキルが前記の意味を有する、式(C1−4)アルキル−O−の基を意味する。好ましくはメトキシ及びエトキシである。最も好ましくは、メトキシである。
【0016】
「アリール」という用語は、単独の場合も、組み合わせて用いる場合も、フェニル又はナフチル基を意味する。アリール基は、未置換であっても、1、2又は3個の置換基により独立に置換されていてもよく、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3、ハロゲン及び、未置換であるか、若しくは、(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択される。
【0017】
「A」が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1若しくは2個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン、及び、未置換であるか又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基が(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される、上記の基を意味する。「A」が「アリール」を表す場合の好ましい例は、未置換であるか、又は1若しくは2個の置換基により独立に置換されたフェニル(好ましくは1置換フェニル)であり、当該置換基は、(C1−4)アルキル,(C3−6)シクロアルキル,(C1−4)アルコキシ及びNR2R3から成る群より独立に選択される。1つの例はフェニルである。上記の置換基に加えて、置換基「A」は置換基「B」によっても置換される。
【0018】
「B」が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2若しくは3個の置換基により置換され、当該置換基が(C1−4)アルキル,(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択される、上記の基を意味する。「B」が「アリール」を表す場合の好ましい例は、未置換であるか又は置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲン(好ましくは、(C1−4)アルキル,NHC(O)CH3、トリフルオロメチル及びハロゲン)から成る群より独立に選択される1、2若しくは3個の置換基により置換されたフェニル(好ましくは、1若しくは2置換フェニル)である。例は、フェニル、3−メチルフェニル、4−メチルフェニル、3,5−ジメチルフェニル、2,4−ジメチルフェニル、3,4−ジメチルフェニル、3−フルオロフェニル、4−フルオロフェニル、3−クロロフェニル、4−ブロモフェニル、3,4−ジフルオロフェニル、3,4−ジクロロフェニル、3−ブロモ−4−フルオロフェニル、3−アセチルアミノフェニル及び3−トリフルオロメチルフェニルである。上記の置換基に加えて、置換基「B」は置換基「A」に結合している。
【0019】
「A」及び「B」が共に「アリール」を表す場合には、組み合わせ「A−B」は、好ましくは、「A」が未置換であるか、又は1若しくは2個の置換基により独立に置換され、「B」が未置換であるか、又は1、2若しくは3個の置換基により置換され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択されるビフェニル基である。「A」及び「B」が共にアリールを表す場合の好ましい例は、「A」が未置換であるか、又は1若しくは2個の置換基により独立に置換され、「B」が未置換であるか、又は1、2若しくは3個の置換基により置換(好ましくは1若しくは2置換)され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル及びハロゲンから成る群より独立に選択されるビフェニル基である。
【0020】
R1が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2又は3個の置換基により置換され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3(好ましくは、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン及びトリフルオロメチル)から成る群より独立に選択される上記の基を意味する。
【0021】
「ヘテロシクリル」という用語は、単独の場合も、組み合わせて用いる場合も、酸素、窒素および硫黄から選択される、例えば1、2または3個の同じか又は異なっていてもよいヘテロ原子を含む5−から10−員の単環又は二環芳香環を意味する。そのようなヘテロシクリル基の例は、フラニル、オキサゾリル、イソオキサゾリル、オキサジアゾリル、チエニル、チアゾリル、イソチアゾリル、チアジアゾリル、ピロリル、イミダゾリル、ピラゾリル、トリアゾリル、ピリジル、ピリミジル、ピリダジニル、ピラジニル、インドリル、イソインドリル、ベンゾフラニル、イソベンゾフラニル、ベンゾチオフェニル、インダゾリル、ベンズイミダゾリル、ベンズオキサゾリル、ベンズイソオキサゾリル、ベンゾチアゾリル、ベンゾトリアゾリル、ベンズオキサジアゾリル、ベンゾチアジアゾリル、キノリニル、イソキノリニル、ナフチリジニル、シノリニル、キナゾリニル、キノキサリニル、フタラジニル、ピラゾロ[1,5−a]ピリジル、ピラゾロ[1,5−a]ピリミジル、イミダゾ[1,2−a]ピリジル又はイミダゾ[2,1−b]チアゾリルである。上記のヘテロシクリル基は、未置換であっても、又は1、2又は3個の置換基により独立に置換されていてもよく、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル、NR2R3、NHC(O)CH3、及び、未置換であるか、又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基は(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される。
【0022】
「A」が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は1若しくは2個の置換基により置換され(好ましくは、未置換若しくは1置換)、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン、及び、未置換であるか、又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基が(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される上記の基を意味する。
【0023】
「A」が「ヘテロシクリル」を表す場合におけるさらに好ましい態様において、この用語は、未置換であるか、又は1個の置換基により置換され、当該置換基が(C1−4)アルキル、(C3−6)シクロアルキル及びNR2R3から成る群より選択される上記の基を意味する。「A」が「ヘテロシクリル」を表す場合の好ましい例は、未置換であるか、又は1個の置換基により置換され、当該置換基が(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から選択される、チアゾリル、オキサゾリル、ピリミジル及びピラジニル(好ましくは、チアゾリル)である。上記の置換基に加えて、置換基「A」は置換基「B」によっても置換される。
【0024】
「A」が「ヘテロシクリル」を表し、置換基の1つが「B」により表される特定の例は:
【化2】

である。
【0025】
「B」が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2又は3個の置換基により置換され(好ましくは、1又は2置換)、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、−NR2R3及びハロゲン(好ましくは、(C1−4)アルキル、トリフルオロメチル及びハロゲン)から成る群より独立に選択される上記の基を意味する。上記の置換基に加えて、置換基「B」は置換基「A」に結合される。
【0026】
R1が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され(好ましくは、未置換であるか、又は1若しくは2個の置換基により独立に置換され)、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択される上記の基を意味する。さらなる好ましい態様において、R1が「ヘテロシクリル」を表す場合には、この用語は、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基が(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される上記の基を意味する。さらなる好ましい態様において、R1が「ヘテロシクリル」を表す場合には、この用語は、未置換であるか、又は独立に1若しくは2個の置換基により置換され、当該置換基がメチルである上記の基を意味する。
【0027】
R1が「ヘテロシクリル」を表す好ましい例は:
【化3】

である。
【0028】
R1が「ヘテロシクリル」を表すさらなる好ましい例は:
【化4】

である。
【0029】
「NR2R3」という用語は、例えばNH2及びN(CH3)2を意味する。
【0030】
「薬学的に許容される塩」という用語は、無毒性の無機若しくは有機酸及び/又は塩基付加塩を意味する。「Salt selection for basic drugs1、 Int. J. Pharm.(1986)、 33、 201−217」を参照してもよい。
【0031】
ii) 本発明のさらなる態様は、Aがヘテロシクリルを表し、当該ヘテロシクリルが未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から成る群より選択される、態様i)に従う式(I)の化合物を含む。
【0032】
iii) 本発明のさらなる態様は、Bがアリールを表し、当該アリールが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NHC(O)CH3及びハロゲンから成る群より独立に選択される、態様i)ないしii)のいずれか1つに従う式(I)の化合物を含む。
【0033】
iv) 本発明のさらなる態様は、R1がアリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルが未置換であるか、又は1若しく2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンから成る群より独立に選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表す、態様i)ないしiii)のいずれか1つに従う式(I)の化合物を含む。
【0034】
v) 本発明のさらなる態様は、Aがオキサゾリル、チアゾリル又はピリミジル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、態様i)ないしiv)のいずれか1つに従う式(I)の化合物を含む。
【0035】
vi) 本発明のさらなる態様は、Bがフェニルを表し、当該フェニルが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される、態様i)ないしv)のいずれか1つに従う式(I)の化合物を含む。
【0036】
vii) 本発明のさらなる態様は、R1がイミダゾ[2,1−b]チアゾリル又はベンゾイソキサゾリル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−基を表す、態様i)ないしvi)のいずれか1つに従う式(I)の化合物を含む。
【0037】
viii) 本発明のさらなる態様は、Aがチアゾリル基を表し、当該基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、態様i)ないしvii)のいずれか1つに従う式(I)の化合物を含む。
【0038】
ix) 本発明のさらなる態様は、R2及びR3が共に水素を表す、態様i)ないしviii)のいずれか1つに従う式(I)の化合物を含む。
【0039】
好ましい化合物の例は、以下の化合物から成る群より選択される:
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−アミノ−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−m−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;及び
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド。
【0040】
式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造のために使用されてもよく、そのような疾病の予防又は治療に好適である:
大うつ病性障害及び気分循環症を含む気分変調性障害、情動神経症、すべてのタイプの躁鬱病、譫妄、精神病性障害、精神分裂病、緊張型分裂病、妄想性偏執病、適応障害及びすべての群の人格障害;分裂感情障害;全般性不安障害、強迫性障害、心的外傷後ストレス障害、パニック発作、すべてのタイプの恐怖症性不安及び回避性障害を含む不安障害;分離不安;向精神薬の使用、乱用、探索及び再燃;すべてのタイプの心理的又は身体依存、多重人格症候群及び心因性健忘を含む解離性障害;性及び生殖機能障害、心理性的障害及び依存;麻薬耐性又は麻薬離脱症状;麻酔リスク、麻酔応答性の増大;視床下部・副腎機能不全;生物リズム及び概日リズム障害;神経障害性疼痛、下肢静止不能症候群を含む神経障害等の疾患に関連した睡眠障害;睡眠時無呼吸;ナルコレプシー;慢性疲労症候群;精神障害に関連する不眠症;すべてのタイプの突発性不眠症及び錯眠;時差ぼけを含む睡眠−覚醒スケジュール障害;健常者並びに精神及び神経障害におけるすべての痴呆及び認知機能障害;加齢に伴う精神機能障害;すべてのタイプの健忘;重度知的障害;ジスキネジア及び筋疾患;筋痙縮、振戦、運動障害;自発性及び薬剤誘発ジスキネジア;ハンチントン病、クロイツフェルト・ヤコブ病、アルツハイマー病及びトウレット症候群を含む神経変性障害;筋萎縮性側索硬化症;パーキンソン病;クッシング症候群;外傷性病変;脊髄外傷;頭部外傷;周産期低酸素症;難聴;耳鳴り;脱髄疾患;脊髄及び脳神経疾患;眼損傷;網膜症;癲癇;発作障害;欠神発作、複雑部分及び全般発作;レノックスガストー症候群;偏頭痛及び頭痛;疼痛性障害;感覚脱失及び痛覚脱失;痛覚過敏、灼熱痛、異痛症などの疼痛感受性増強又は過大;急性疼痛;熱傷痛;非定型顔面痛;神経障害性疼痛;背部痛;複合局所性疼痛症候群I及びII;関節炎性疼痛;スポーツ外傷痛;歯痛;感染、たとえばHIVに関連した疼痛、化学療法後の疼痛;発作後疼痛;術後痛;神経痛;骨関節炎;過敏腸管症候群などの内臓痛に関連した状態;摂食障害;糖尿病;無酸素脳症、糖尿病性神経障害及びアルコール依存症を含む中毒性及び代謝異常疾患;食欲、味覚障害、摂食又は摂水(Drinking)障害;心気症を含む身体表現性障害;嘔吐/悪心;嘔吐症;胃運動機能異常(ジスキネジア);胃潰瘍;カルマン症候群(嗅覚脱失);耐糖能障害;腸運動機能異常;視床下部疾患;下垂体疾患;高熱症候群、発熱、熱性痙攣、特発性発育不全;小人症;巨人症;先端巨大症;好塩基性細胞腺腫、プロラクチノーマ、高プロラクチン血症;脳腫瘍、腺腫;良性前立腺肥大、前立腺癌;子宮体癌、乳癌、大腸癌;すべてのタイプの精巣機能障害、避妊法;生殖ホルモン異常;閉経期一過性熱感;視床下部性生殖機能低下、機能性又は心因性無月経;膀胱尿失禁;喘息;アレルギー;すべてのタイプの皮膚炎、面皰及び嚢胞、皮脂腺機能障害;心臓血管疾患;心・肺疾患、急性・鬱血性心不全;低血圧;高血圧;脂質異常症、高脂血症、インスリン抵抗性;尿閉;骨粗鬆症;狭心症;心筋梗塞;不整脈、冠動脈疾患、左室肥大;虚血性又は出血性発作;クモ膜下出血;クモ膜下出血、虚血性及び出血性発作並びに血管性痴呆を含むすべてのタイプの脳血管障害;慢性腎不全及びその他の腎疾患;痛風;腎臓癌;尿失禁;並びに一般のオレキシン系機能障害に関連するその他の疾患。
【0041】
式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用、乱用、探索及び再燃、健常者並びに精神及び神経障害における認知機能障害並びに摂食又は摂水(Drinking)障害。
【0042】
摂食障害は代謝機能不全;食欲調節不全;強迫的肥満;嘔吐・過食又は神経性食欲不振症を含むものとして定義できる。この摂食の病理学的変形は、食欲障害(食物に対する誘惑又は嫌悪);エネルギーバランスの変調(摂取/消費)、食品品質についての知覚障害(高脂肪又は高炭水化物、良味覚);食物入手可能性障害(無制限節食又は遮断)又は水分平衡障害から生じるかもしれない。
【0043】
摂水障害(Drinking disorders)は、精神障害における多飲症及びすべての他のタイプの過剰液体摂取を含む。
【0044】
睡眠障害は、すべてのタイプの錯眠、不眠症、ナルコレプシー及び過眠症、睡眠関連失調症、下肢静止不能症候群、睡眠時無呼吸症、時差症候群、交代勤務睡眠障害、睡眠相遅延症候群、睡眠相前進症候群又は精神障害に関連する不眠症を含む。不眠症は、加齢と関係付けられる睡眠障害;慢性不眠の間歇治療;環境による一過性の不眠症(新しい環境、騒音)又はストレス;悲嘆;疼痛又は病気による短期間の不眠症を含むものとして定義される。不眠症は、全般性不安障害、強迫性障害、パニック発作並びにすべてのタイプの恐怖症性不安及び回避性障害等の他のタイプ及びサブタイプの不安障害のみならず心的外傷後ストレス障害を含むストレス関連症候群をも包含する;向精神薬の使用、乱用、探索及び再燃は、すべてのタイプの心理的又は身体依存並びにそれらに関連する耐性及び依存因子と定義される。認知機能障害は、正常な、健康な、若年の、成人の又は老齢の集団において一時的に又は慢性的に生じ、また精神、神経、心臓血管及び免疫疾患において一時的に又は慢性的に生じるすべてのタイプの注意、学習及び記憶機能における欠損を含む。
【0045】
本発明のさらに好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:すべてのタイプの不眠、ナルコレプシー及び過眠症、睡眠関連失調症、下肢静止不能症候群、睡眠時無呼吸症、時差症候群、交代勤務睡眠障害、睡眠相遅延症候群、睡眠相前進症候群又は精神障害に関連する不眠症の他の障害を含む睡眠障害。
【0046】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:正常な、健康な、若年の、成人の又は老齢の集団において一時的に又は慢性的に生じ、また精神、神経、心臓血管及び免疫疾患において一時的に又は慢性的に生じるすべてのタイプの注意、学習及び記憶機能における欠損を含む認知機能障害。
【0047】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:代謝機能不全;食欲調節不全;強迫的肥満;嘔吐・過食又は神経性食欲不振症を含む摂食障害。
【0048】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:すべてのタイプの心理的又は身体依存並びにそれらに関連する耐性及び依存因子を含む向精神薬の使用、乱用、探索及び再燃。
【0049】
医薬組成物の製造は、いずれの当業者によく知られた様式で(例えば、Remington、The Science and Practice of Pharmacy、21st Edition(2005)、Part 5、“Pharmaceutical Manufacturing” [Lippincott Williams & Wilkinsにより出版]を見よ。)、記述された式(I)の化合物又はこれらの薬学的に許容される塩を、任意にその他の治療的に有益な物質と組み合わせて、適切な無毒の不活性な治療上許容される固体又は液体の担体材料及び必要に応じて、通常の薬学的アジュバントと共に、製剤投与形態とすることにより遂行することができる。
【0050】
式(I)の化合物及びこれらの薬学的に許容される塩は、医薬として、たとえば経腸又は非経口投与のための医薬組成物の形態で使用することができる。
【0051】
本発明のさらなる側面は、式(I)の化合物の製造のための方法である。本発明の式(I)の化合物は、下記のスキームに概説した反応の包括的なシークエンスに従って製造することができ、該スキーム中、A、B及びR1は、式(I)の記述において定義した通りである。得られた化合物は、それ自体知られた方法により、それらの薬学的に許容される塩に変換してもよい。
【0052】
一般的に、すべての化学的変換は、文献に記載され、又は下記の手順に記載された、よく知られた標準的方法論に従って遂行することができる。
【0053】
式(I)の化合物の製造:
【化5】

【0054】
式(I)の2−アザ−ビシクロ[3.3.0]オクタン誘導体の合成における最初の工程は、(1S,3S,5S)−2−アザビシクロ[3.3.0]オクタン−3−カルボキシレートの窒素原子の、Boc2Oでの保護により、式(2)の化合物を得ることであった。式(2)の化合物は、低温でのDIBALによる処理により、アルコール(3)に還元された。アルコール(3)は、例えばデス−マーチンペルヨージナン等の酸化剤で、対応するアルデヒド(4)に酸化された。ナトリウムトリアセトキシボロヒドリドのような還元剤の存在下における、ベンジルアミンでの(4)の還元的アミノ化の後、中間体(5)のベンジル基は水素化分解により除去され、第一アミン(6)を生じた。TBTUのようなカップリング剤の存在下における、カルボン酸R1COOHでの(6)のアシル化により、アミド(7)の形成が起こり、アミド(7)は、Boc−基の除去後、アミドカップリング(例えばB−A−COOH、TBTU)により、式(I)の化合物に変換された。
【0055】
式B−A−COOHのチアゾール−4−カルボン酸誘導体は、例えばスキーム2に従って合成された。
【0056】
【化6】

【0057】
カリウムtert−ブトキシド等の塩基の存在下で、メチルジクロロアセテート(9;購入可能)をアルデヒドと反応させることにより、α−オキソ−エステル誘導体(10)が得られ、この化合物は、チオアミド[R=C1−4アルキル又は(C3−6)シクロアルキル]との反応において2−アルキル−又は2−シクロアルキル置換チアゾール誘導体(11)に、又はチオウレア(R=NR2R3)との反応において2−アミノ−置換チアゾール誘導体(11)に変換された。メタノール等の溶媒中での、例えば水酸化ナトリウム水溶液でのエステル官能基のけん化により、所望のカルボン酸(12、R=C1−4アルキル、(C3−6)シクロアルキル又はNR2R3)が生成した。2−ブロモ−チアゾール誘導体(13)は、例えば、臭化銅(II)の存在下における、それぞれの2−アミノ−チアゾール誘導体(11、R=NH2)の亜硝酸イソアミルとの反応により得られた。エステル誘導体(13)は、シクロプロピル−スズ誘導体(購入可能)による、パラジウム触媒反応において、化合物(14)に変換され、それをけん化することにより、それぞれのカルボン酸(15)が得られた。さらに、2−ブロモ−チアゾール誘導体(13)は、上記のように、対応するカルボン酸(16)にけん化され、又はナトリウムアルコキシドとの反応、それに続くNaOHでのけん化により、2−メトキシ置換アナログ(17)に変換される。加えて、2位が未置換の化合物(19)は、木炭上パラジウムの存在下での水素による(13)の水素化、それに続く中間体エステル(18)のけん化により合成される。(11)の合成における(C3−6)シクロアルキル−置換チオアミドは、購入可能であるか、又は、それぞれのカルボキサミドのLawessonの試薬との反応により得られた(実験の部のA.1.6も見よ。)。アルデヒドB−CHOは購入可能であるか、又は、例えばそれぞれのカルボン酸又はそれらの異なる誘導体の還元剤による還元のような文献から知られている手順により、それぞれのニトリルの還元により、又はベンジルアルコール及びそれらのヘテロシクリルアナログを酸化剤で酸化することにより合成してもよい(例えば:J. March、Advanced Organic Chemistry、4th edition、John Wiley & Sons、p. 447−449、919−920及び1167−1171)。
【0058】
式R1−COOHのイミダゾ[2,1−b]チアゾール−カルボン酸誘導体は、購入可能でない場合には、例えばスキーム3に示す異なった経路の一つに従って合成してもよい。
【0059】
【化7】

【0060】
【化8】

【0061】
【化9】

【0062】
経路Aに従い、イミダゾ[2,1−b]チアゾール−カルボン酸誘導体を、2−クロロ−3−オキソ−ブチル酸メチルエステル(20;購入可能)から、エタノール等の溶媒中での、高温におけるチオ尿素(購入可能)との反応により合成した。得られたアミノ−チアゾール(21)は、アルキル化、続く濃塩酸等の酸の存在下におけるブロモアセトアルデヒドジエチルアセタールでの環化により、イミダゾ[2,1−b]チアゾール誘導体(22)に変換された。THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによる(22)のけん化により、所望の酸(23)を得た。
【0063】
別のアプローチ(経路B)は、アセトン等の溶媒中での、2−ブロモ−3−オキソ−酪酸エステル(24;購入可能)の、2−アミノ−5−メチル−チアゾール(購入可能)との反応で始まり、得られたイミダゾ[2,1−b]チアゾール誘導体(25)は、THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによるけん化により、所望の酸(26)に変換された。
【0064】
木炭上パラジウムの存在下における、酸性条件下(例えば、EtOH中HCl)での、2−ヒドロキシイミノ−3−オキソ−酪酸エステル(27;購入可能)の水素化、及び、続くチオシアン酸カリウムとの反応により、イミダゾール誘導体(28)を得、それを、それぞれのα−ハロゲン化プロパノン(購入可能)又はブタノン誘導体(経路C;購入可能)との反応により、2つの可能な異性体(29)及び(30)の混合物に変換した。クロマトグラフィーにより異性体を分離した後、THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによるけん化により、所望のイミダゾ[2,1−b]チアゾール−カルボン酸誘導体(31)及び(32)を得た。
【0065】
イミダゾール誘導体(28)はまた、ナトリウムエトキシド等の塩基の存在下での、ブロモアセトアルデヒドジエチルアセタール(購入可能。)によるアルキル化により、アセタール(33)に変換してもよい(経路D)。酸性条件下(例えば塩酸)での環化及び例えば塩化ホスホリルでの中間体(34)の脱水によりエステル(35)が得られ、エステル(35)は、THF及びMeOH等の溶媒中における例えば水酸化ナトリウムでのけん化により、所望の酸(36)に変換された。
【0066】
さらに別の手順(経路E)においては、それぞれのアミノ−チアゾール(37;購入可能)は、(37)を、トルエン等の溶媒中でN,N−ジメチルホルムアミドジメチルアセタール(購入可能)とともに加熱することにより、ホルムアミジン誘導体(38)に変換された。エチルブロモアセテート(購入可能)でのアルキル化の後、それぞれの臭化チアゾリウム(39)はDBUで環化され、エステル(40)が得られた。エステル(40)は、THF及びMeOH等の溶媒中で、例えば水酸化ナトリウムでけん化され、所望の酸(41)が得られた。
【0067】
最後に、2−アミノ−チアゾール(購入可能)の3−ブロモ−1,1,1−トリフルオロアセトン(購入可能)でのアルキル化で始まる経路Fにより、トリフルオロメチル−置換イミダゾ[2,1−b]チアゾール誘導体(42)が得られ、この誘導体は、DMF等の溶媒中における塩化ホスホリルとの反応によりホルミル化され、アルデヒド(43)を与えた。亜塩素酸ナトリウムでのアルデヒド(43)の酸化により、所望のイミダゾ[2,1−b]チアゾール−カルボン酸(44、Y=CF3))が得られた。同様に、購入可能な塩素化アルデヒド(43、Y=Cl)は、酸(44、Y=Cl)に酸化された。
【0068】
実験の部
(この項において、及び本明細書のこれまでの部分において使用される)略語:
Ac OAcにおけるようにアセチル:アセテート
Boc tert−ブトキシカルボニル
BSA ウシ血清アルブミン
Bu n−ブチル
CHO チャイニーズハムスター卵巣
conc. 濃縮された
d 日
DBU 1,8−ジアザビシクロ−[5.4.0]−ウンデス−7−エン
DCM ジクロロメタン
DIBAL ジイソブチルアルミニウム水和物
DIPEA ジイソプロピルエチルアミン
DMAP 4−ジメチルアミノピリジン
DMF N,N−ジメチルホルムアミド
eq 当量
ES 電子スプレー
Et エチル
EtOH エタノール
EtOAc 酢酸エチル
エーテル ジエチルエーテル
FCS ウシ胎児血清
FLIPR 蛍光イメージングプレートリーダー
h 時間
HBSS ハンクス平衡塩溶液
HEPES 4−(2−ヒドロキシエチル)−ピペリジン−1−エタンスルホン酸
HPLC 高速液体クロマトグラフィー
KOt−Bu カリウムtertiary(tert.)ブトキシド
LC 液体クロマトグラフィー
M モル
Me メチル
MeCN アセトニトリル
MeOH メタノール
min 分
MS 質量分析
Ph フェニル
prep. 分取用
RT 室温
sat 飽和
tR 保持時間
TBTU O−ベンゾトリアゾール−1−イル−N,N,N’,N’−テトラメチル
ウロニウムテトラフルオロホウ酸塩
TFA トリフルオロ酢酸
THF テトラヒドロフラン
【0069】
I−化学
以下の実施例は、本発明の薬理学的に活性を有する化合物の製造を説明するが、本発明の範囲をまったく限定するものではない。
【0070】
温度はすべて℃で示す。
【0071】
化合物は、
1H−NMRによって:300MHz Varian Oxford又は400MHz Bruker Avance;化学シフトは、使用する溶媒と関連して、ppmで示される;多重度:s=一重項、d=二重項、t=三重項、m=多重項、b=広域、結合定数はHzで示される;
LC−MSによって:DAD及びMS検知を備えたAgilent 1100シリーズ(MS:Finnigan シングル 四重極);カラム(4.6x5mm、5m):Zorbax SB−AQ、Zorbax Extend C18又はWaters XBridge C18;条件:
塩基性:溶出液A:MeCN、溶出液B:濃NH3水溶液(1.0mL/L)、5%から95%CH3CN;
酸性:溶出液A:MeCN、溶出液B:TFA水溶液(0.4mL/L)、5%から95%CH3CN、tRは分で示される;
特徴付けられる。
【0072】
化合物は、シリカゲル上のカラム・クロマトグラフィーにより、又はMeCN/水勾配を用い、ギ酸又はアンモニアを添加した、RP−C18ベースのカラムを用いた分取用HPLCにより精製される。
【0073】
A. 前駆体及び中間体の製造:
A.1 チアゾール−4−カルボン酸誘導体の合成
A.1.1 3−クロロ−2−オキソ−プロピオンエステル誘導体の合成(一般的手順)
【0074】
【化10】

【0075】
それぞれのアルデヒド(338mmol、1.0eq)及びジクロロ酢酸メチル(338mmol、1.0eq)のTHF(100ml)中の溶液を、KOtBu(335mmol、1.0eq)のTHF(420ml)中の冷(−60℃)懸濁液に滴下する。4h後、混合物をRTにし、一晩攪拌し、真空濃縮する。DCM及び氷冷水を添加し、層を分離し、水層をDCMで2回抽出する。合わせた有機層を氷冷水及び塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のα−オキソ−エステルを得、それをさらに精製することなく使用する。
【0076】
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステル
4−メチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0077】
3−クロロ−3−(3−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0078】
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
4−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0079】
3−クロロ−3−(3−クロロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−クロロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0080】
3−クロロ−2−オキソ−3−m−トリル−プロピオン酸メチルエステル
3−メチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0081】
3−クロロ−2−オキソ−3−(3−トリフルオロメチル−フェニル)−プロピオン酸メチルエステル
3−トリフルオロメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0082】
3−(4−ブロモ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステル
4−ブロモ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0083】
3−クロロ−3−(3,5−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,5−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0084】
3−(3−ブロモ−4−フルオロ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステル
3−ブロモ−4−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0085】
3−クロロ−3−(3,4−ジフルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジフルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0086】
3−クロロ−3−(2,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
2,4−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0087】
3−クロロ−3−(3,4−ジクロロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジクロロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0088】
3−クロロ−3−(3,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0089】
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステル
ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0090】
3−クロロ−3−(3−ニトロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−ニトロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0091】
A.1.2 チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0092】
【化11】

【0093】
チオアセタミド(132mmol、1.0eq)のMeCN(250ml)中の溶液を、それぞれのα−オキソ−エステル(132mmol、1.0eq)及びモレキュラー・シーヴ(4Å、12g)のMeCN(60ml)中の混合物に添加する。5h撹拌した後、混合物を氷浴中で冷却し、得られた沈殿物をろ過する。残渣を冷MeCNで洗浄し、乾燥し、MeOH(280ml)中に溶解し、50℃で6h撹拌する。溶媒を真空除去して、所望のチアゾール誘導体を、白色の固体として得る。
【0094】
2−メチル−5−p−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.92min;[M+H]+=248.2。
【0095】
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.91min;[M+H]+=252.1。
【0096】
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。1H−NMR(CDCl3):δ=2.75(s、3H);3.84(s、3H);7.10(m、2H);7.47(m、2H)。
【0097】
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−クロロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=268.0。
【0098】
2−メチル−5−m−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−m−トリル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.98min;[M+H]+=248.5。
【0099】
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−(3−トリフルオロメチル−フェニル)−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.98min;[M+H]+=302.2。
【0100】
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−(4−ブロモ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=312.2。
【0101】
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,5−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.97min;[M+H]+=262.3。
【0102】
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−(3−ブロモ−4−フルオロ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=330.2。
【0103】
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジフルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.92min;[M+H]+=270.3。
【0104】
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(2,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.96min;[M+H]+=262.3。
【0105】
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジクロロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.99min;[M+H]+=302.2。
【0106】
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.96min;[M+H]+=262.3。
【0107】
2−メチル−5−フェニル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.89min;[M+H]+=234.0。
【0108】
2−メチル−5−(3−ニトロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−ニトロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.94min;[M+H]+=279.3。
【0109】
A.1.3 2−アミノ−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0110】
【化12】

【0111】
それぞれのα−オキソ−エステル(22.1mmol、1.0eq)のアセトン(25ml)中の溶液を、チオウレア(22.1mmol、1.0eq)のアセトン(45ml)中の懸濁液に添加する。混合物を57℃(温浴の温度)に加熱し、24h撹拌し、半分の体積になるまで濃縮する。得られた懸濁液をろ過し、残渣をアセトンで洗浄する。乾燥後、所望のアミノ−チアゾール誘導体を固体として得る。
【0112】
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.77min;[M+H]+=249.3。
【0113】
2−アミノ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.75min;[M+H]+=253.2。
【0114】
2−アミノ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−トリフルオロメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.86min;[M+H]+=303.3。
【0115】
A.1.4 2−ブロモ−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0116】
【化13】

【0117】
不活性雰囲気下、臭化銅(II)(69.6mmol、1.0eq)を、アセトニトリル(300ml)に懸濁し、そして5−10℃に冷却した後、亜硝酸3−メチルブチル(104mmol、1.45eq)を15minに渡って添加した。この反応混合物に、それぞれの2−アミノチアゾール誘導体(70.0mmol、1eq、遊離アミン)を、5−10℃にて、20min.に渡り、少しずつ添加した。次いで、反応混合物を注意深く65℃に加熱し、そして攪拌を2h継続した。揮発物を減圧下で除去し、そして残渣をカラムクロマトグラフィー(シリカゲル;ヘプタン/EtOAc又はDCM/メタノール、適宜な混合物として)で精製して、それぞれの生成物を得た。
【0118】
2−ブロモ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−アミノ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルの反応により製造。LC−MS:tR=0.97min;[M+H]+=316.1。
【0119】
2−ブロモ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−アミノ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルの反応により製造。LC−MS:tR=1.04min;[M+H]+=366.2。
【0120】
A.1.5 2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順I)
【0121】
【化14】

【0122】
不活性雰囲気において、それぞれの2−ブロモ−チアゾール誘導体(9.0mmol、1.0eq)及びトリブチル−シクロプロピル−スタナン(9.9mmol、1.1eq)の、1,2−ジクロロ−エタン(90mL)中の溶液を、5min攪拌し、そしてビス(トリフェニルホスフィン)−パラジウム(II)クロリド(0.45mmol、0.05eq)で処理する。混合物を80℃に加熱し、3d攪拌し、そしてRTに到達させる。DCMと水を添加し、層を分離し、そして水層をDCMで1回抽出する。合わせた有機層をMgSO4上で乾燥し、そして真空濃縮する。残渣をカラムクロマトグラフィー(シリカゲル;ヘプタン/EtOAc、適宜な混合物として)で精製して、所望の生成物を得る。
【0123】
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−ブロモ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルのシクロプロピル化により製造。LC−MS:tR=0.97min;[M+H]+=278.3。
【0124】
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−ブロモ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのシクロプロピル化により製造。LC−MS:tR=1.03min;[M+H]+=328.2。
【0125】
A.1.6 2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順II)
【0126】
【化15】

【0127】
シクロプロパンカルボチオ酸アミドの合成
2,4−ビス−(4−メトキシ−フェニル)−[1,3,2,4]ジチアジホスフェタン−2,4−ジスルフィド(Lawessonの試薬、115mmol)を、シクロプロパンカルボキサミド(115mmol)と炭酸ナトリウム(115mmol)の、THF(500mL)中の混合物に添加する。混合物を2h加熱還流し、溶媒を真空除去し、そして残渣をエーテル(500mL)と水(500mL)で希釈する。層を分離し、そして水層をエーテル(250mL)で抽出する。合わせた有機層を塩水(100mL)で洗浄し、MgSO4上で乾燥し、そして真空濃縮して、所望のチオアミドを得、それをさらに精製することなく使用する。LC−MS:tR=0.39min;[M+H+CH3CN]+=143.2。
【0128】
2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順II)
シクロプロパンカルボチオ酸アミド(44.5mmol、1.0eq)のMeCN(40ml)中の溶液を、それぞれのα−オキソ−エステル(44.5mmol、1.0eq)及びNaHCO3(134mmol、3.0eq)のMeCN(80ml)中の混合物に添加する。16h撹拌した後、混合物を真空濃縮し、残渣をEtOAc(200ml)及び水(200ml)で希釈する。層を分離し、水層をEtOAc(100ml)で抽出する。合わせた有機層を塩水(100ml)で洗浄し、MgSO4上で乾燥し、そして真空濃縮する。粗生成物をMeOH(90ml)中に溶解し、濃縮H2SO4(0.25ml)で処理する。混合物を60℃で16h撹拌し、真空濃縮して、それぞれのチアゾール誘導体を得る。
【0129】
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステルの、シクロプロパンカルボチオ酸アミドとの反応により製造。LC−MS:tR=0.99min;[M+H]+=260.5。
【0130】
A.1.7 5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルの合成
A.1.7.1 5−(3−アミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルの合成
2−メチル−5−(3−ニトロ−フェニル)−チアゾール−4−カルボン酸メチルエステル(44.1mmol)及び塩化アンモニウム(220mmol)の、EtOH(100ml)及び水(50ml)の混合物中の懸濁液を、鉄粉(53.0mmol)で処理し、そして80℃に加熱する。4h後、鉄粉(53.0mmol)をさらに添加し、混合物を80℃で3h加熱し、さらに鉄粉(26.5mmol)を添加し、そして混合物を再び80℃にて3.5h加熱する。混合物をRTに到達させ、DCMで希釈し、そしてセライトを通してろ過する。ろ液を真空濃縮し、そしてDCM及びsat.NaHCO3水溶液で希釈する。層を分離し、そして有機層を水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアニリン誘導体を得る粗生成物を得る。LC−MS:tR=0.67min;[M+H]+=249.4。
【0131】
A.1.7.2 5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸 メチルエステルの合成
トリエチルアミン(14.2mmol)及びDMAP(4.00mmol)を、5−(3−アミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル(4.00mmol)の無水酢酸(25ml)中の溶液に添加する。30min後、EtOAc及び水を添加し、層を分離し、水層をEtOAcで1回抽出する。合わせた有機層をsat.塩化アンモニウム水溶液で2回、sat.NaHCO3水溶液で1回そして水で1回洗浄し、そして溶媒を真空除去する。残渣をEtOAcで希釈し、そしてsat NaHCO3水溶液で3回抽出する。有機層をMgSO4上で乾燥し、真空濃縮して、粗製の固形物を得、それをエーテルで希釈する。得られた懸濁液をろ過し、そして残渣をエーテルで洗浄して、所望のアセタミドを得る。LC−MS:tR=0.81min;[M+H]+=291.3。
【0132】
A.1.8 チアゾール−4−カルボン酸誘導体の合成(一般的手順)
【0133】
【化16】

【0134】
それぞれのエステル(96.2mmol)の、THF(150ml)、及びMeOH(又はイソプロパノール、50ml)の混合物中の溶液を、NaOH水溶液(1.0M、192ml)で処理する。3h撹拌した後、白色の懸濁液が生成し、有機揮発物を真空除去する。残った混合物を水(100ml)で希釈し、氷浴中で冷却し、塩酸(1.0M)の添加により酸性(pH=3−4)にする。沈殿が生成した場合には、懸濁液をろ過し、残渣を冷水で洗浄し、そして真空乾燥して、所望の酸を得る。そうでない場合には、混合物をEtOAcで2回抽出し、そして有機層を合わせ、MgSO4上で乾燥し、真空濃縮して、それぞれの酸を得る。
【0135】
2−メチル−5−p−トリル−チアゾール−4−カルボン酸
2−メチル−5−p−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.83min;[M+H]+=234.0。
【0136】
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.82min;[M+H]+=238.1。
【0137】
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。1H−NMR(DMSO−d6):δ=2.67(s、3H);7.27(m、2H);7.53(m、2H);12.89(br.s、1H)。
【0138】
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.84min;[M+H]+=254.0。
【0139】
2−メチル−5−m−トリル−チアゾール−4−カルボン酸
2−メチル−5−m−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.87min;[M+H]+=234.4。
【0140】
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.88min;[M+H]+=288.0。
【0141】
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.85min;[M+H]+=298.2。
【0142】
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=248.3。
【0143】
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=316.2。
【0144】
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.82min;[M+H]+=256.3。
【0145】
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.85min;[M+H]+=248.3。
【0146】
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.88min;[M+H]+=288.2。
【0147】
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=248.3。
【0148】
2−メチル−5−フェニル−チアゾール−4−カルボン酸
2−メチル−5−フェニル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.77min;[M+H]+=220.0。
【0149】
5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.73min;[M+H]+=277.2。
【0150】
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.64min;[M+H]+=235.2。
【0151】
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.87min;[M+H]+=264.2。
【0152】
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.94min;[M+H]+=314.2。
【0153】
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸のけん化により製造。LC−MS:tR=0.91min;[M+H]+=246.4。
【0154】
A.2 2,3−ジヒドロ−ベンゾフラン−4−カルボン酸の合成
ベンゾフラン−4−カルボン酸(30.8mmol、M.A.Eissenstatら J.Med.Chem.1995、38,3094−3105)を、Pd/C(10%、2.00g)のEtOH(25ml)中の懸濁液に添加する。さらにEtOH(75ml)を添加し、混合物を水素雰囲気下(4bar)、16h、RTにて撹拌する。セライトを通してろ過し、溶媒を除いた後、所望の生成物を得、それをさらに精製することなく使用する。1H−NMR(DMSO−d6):δ=3.45(t、J=8.79Hz、2H);4.55(t、J=8.79Hz、2H);6.99(d、J=7.78Hz、1H);7.21(t、J=7.91Hz、1H);7.39(d、J=7.78Hz、1H);12.9(bs、1H)。
【0155】
A.3 (1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
A.3.1 (1S,3S,5S)−(2−tert−ブトキシ−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−カルボン酸 ベンジルエステルの合成
ベンジル(1S,3S,5S)−2−アザビシクロ[3.3.0]オクタン−3−カルボキシレート塩酸塩(17.3mmol、1.0eq)の、DCM(50mL)中の溶液に、DIPEA(22.5mmol、1.3eq)、二炭酸ジ−tert−ブチル(17.3mmol、1.0eq)及び追加のDCM(5mL)を添加する。混合物を1h攪拌し、そして真空濃縮する。EtOAc及びクエン酸水溶液(10%)を添加し、層を分離し、そして水層をEtOAcで1回抽出する。合わせた有機層を塩水で洗浄し、MgSO4上で乾燥し、そして真空濃縮する。残渣をカラムクロマトグラフィー(ヘプタン/EtOAc 3/1)で精製して、所望の生成物を得る。LC−MS:tR=1.08min;[M+H]+=346.3。
【0156】
A.3.2 (1S,3S,5S)−3−ヒドロキシメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
−78℃にて、DIBALのトルエン中の溶液(1.7M、22.5mmol)を、(1S,3S,5S)−(2−tert−ブトキシ−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−カルボン酸ベンジルエステル(9.0mmol)の、THF(50mL)中の溶液に滴下する。40min後、混合物をRTに到達させ、さらに45min攪拌し、そしてNaOH水溶液(1.0M、250mL)と氷の混合物に注ぐ。EtOAcを添加し、層を分離し、そして水層をEtOAcで抽出する。合わせた有機層を、NaOH水溶液(1.0M)と塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアルコールを得、それをフラッシュ・クロマトグラフィー(ヘプタン/EtOAc 3/1)で精製する。LC−MS:tR=0.91min;[M+H]+=242.4。
【0157】
A.3.3 (1S,3S,5S)−3−ホルミル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
デス−マーチン ペルヨージナン(4.14mmol、2.2eq)の、DCM(10ml)中の溶液を、(1S,3S,5S)−3−ヒドロキシメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(1.85mmol、1.0eq)のDCM(4mL)中の溶液及び数滴の水で処理する。5h後、エーテルとNaOH水溶液(1.0M)を添加し、そして層を分離する。有機層をクエン酸水溶液(10%)と塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアルデヒドを得、それをさらに精製することなく使用する。
【0158】
A.3.4 (1S,3S,5S)−3−(ベンジルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
ベンジルアミン(2.76mmol、2.3eq)を、(1S,3S,5S)−3−ホルミル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(1.2mmol、1.0eq)の、クロロホルム(10mL)中の溶液に添加する。混合物を5min攪拌し、ナトリウムトリアセトキシボロヒドリド(4.8mmol、4.0eq)及び酢酸(0.05mL)で処理し、そしてさらに14h攪拌し、sat.NaHCO3水溶液中に注ぐ。DCMを添加し、層を分離し、そして水層をDCMで抽出する。合わせた有機層を水(100mL)で洗浄し、そして真空濃縮する。残渣をエーテル中に溶解し、そして塩酸(0.1M)で3回抽出する。合わせた水層をエーテルで1回抽出し、NaOH溶液(1.0M)の添加により塩基性(pH9−10)にし、そしてエーテルで3回抽出する。合わせた有機層をMgSO4上で乾燥し、真空濃縮して、所望のベンジルアミンを得、それをさらに精製することなく使用する。LC−MS:tR=0.89min;[M+H]+=331.5。
【0159】
A.3.5 (1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
(1S,3S,5S)−3−(ベンジルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(9.0mmol)の、エタノール(10mL)中の溶液を、Pd/C(1.9g、10%)の、エタノール(40mL)中の懸濁液に添加し、そして水素雰囲気下(1bar)で16h攪拌する。セライトを通してろ過し、エタノールで洗浄し、そして溶媒を除去した後、所望のアミンを得、それをさらに精製することなく使用する。LC−MS:tR=0.73min;[M+H]+=241.4。
【0160】
A.4 (1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イルメチル)−アミド誘導体の合成
A.4.1 (1S,3S,5S)−3−(アロイルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成(一般的手順)
【0161】
【化17】

【0162】
それぞれのカルボン酸(4.6mmol、1.1eq)のDMF(15mL)中の溶液に、TBTU(5.0mmol、1.2eq)を添加する。30min後、DIPEA(12.5mmol、3.0eq)と(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(4.2mmol、1.0eq)のDMF(10mL)中の溶液を添加し、そして混合物を60min攪拌する。水とEtOAcを添加し、層を分離し、そして有機層を水で1回洗浄する。合わせた水層をEtOAcで1回抽出し、そして合わせた有機層をMgSO4上で乾燥する。溶媒を真空除去し、そして残渣をカラムクロマトグラフィー(DCM)で精製して、それぞれのアミドを得る。
【0163】
(1S,3S,5S)−3−{[(6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸(A.Andreaniら、Eur.J.Med.Chem 1982、17、271−274)の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=0.91min;[M+H]+=405.2。
【0164】
(1S,3S,5S)−3−{[(ベンゾ[d]イソキサゾール−3−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
ベンゾ[d]イソキサゾール−3−カルボン酸の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=1.11min;[M+H]+=386.6。
【0165】
(1S,3S,5S)−3−{[(2,3−ジヒドロ−ベンゾフラン−4−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=1.00min;[M+H]+=387.1。
【0166】
A.4.2 (1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イルメチル)−アミド誘導体の合成(一般的手順)
【0167】
【化18】

【0168】
HClのジオキサン(4.0M、20mL)中の溶液を、それぞれのBoc−保護2−アザビシクロ[3.3.0]オクタン誘導体(3.6mmol)の、ジオキサン(20mL)中の溶液に添加する。LC−MSが反応の完了を示した後(1−3h)、混合物を真空濃縮して、それぞれの脱保護生成物を得、それをさらに精製することなく使用する。
【0169】
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.56min;[M+H]+=305.3。
【0170】
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(ベンゾ[d]イソキサゾール−3−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.71min;[M+H]+=286.3。
【0171】
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(2,3−ジヒドロ−ベンゾフラン−4−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.70min;[M+H]+=287.4。
【0172】
B. 式(I)の化合物の製造:
B.1 カルボン酸アミド誘導体の合成(一般的手順)
【0173】
【化19】

【0174】
それぞれのカルボン酸(0.44mmol、1.1eq)の、アセトニトリル(1.0mL)中の混合物に、TBTU(0.48mmol、1.2eq)を添加し、そして30min後にDIPEA(1.2mmol、3.0eq)を添加する。15min後に、それぞれの2−アザビシクロ[3.3.0]オクタン誘導体(0.40mmol、1.0eq)のDCM(1.0mL)中の溶液を添加する。混合物を一晩攪拌し、そしてprep.HPLCで精製して、それぞれのアミド誘導体を得る。
【0175】
それぞれのカルボン酸の、6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0176】
【表1】

【0177】
それぞれのカルボン酸の、ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0178】
【表2】

【0179】
それぞれのカルボン酸の、2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0180】
【表3】

【0181】
【表4】

【0182】
II. 生物学的アッセイ
式(I)の化合物のオレキシン受容体拮抗活性は、以下の実験法に従って測定される。
【0183】
細胞内カルシウム濃度の測定:
ヒトオレキシン−1受容体及びヒトオレキシン−2受容体を発現しているチャイニーズハムスター卵巣(CHO)細胞をそれぞれ300μg/mlのG418、100U/mlのペニシリン、100μg/mlのストレプトマイシン及び10%熱不活性化牛胎児血清(FCS)を含む培地(L−グルタミン含有HAM F−12)で培養する。予め、ハンクス平衡塩溶液(HBSS)に溶解した1%ゼラチンで被覆した384穴の黒色の透明底の滅菌プレート(Greiner)に1穴当り20、000個の細胞を播種する。播種したプレートは、5%のCO2下、37℃で一晩インキュベートする。
【0184】
作働薬のヒトオレキシン−Aを、MeOH:水(1:1)中の1mM保存溶液として調製し、アッセイでの使用に際しては、0.1%牛血清アルブミン(BSA)、0.375g/lのNaHCO3及び20mMのHEPESを含むHBSSに、3nMの最終濃度に希釈する。
【0185】
拮抗薬はDMSOに10mMの保存溶液として調製したのち、384穴のプレート中で、DMSOを用いて希釈し、次いで、希釈液を、0.1%牛血清アルブミン(BSA)、0.375g/lのNaHCO3及び20mMのHEPESを含むHBSSに移す。
【0186】
アッセイの日に、染色バッファー50ml(1%のFCS、20mMのHEPES、0.375g/lのNaHCO3、5mMのプロベネシド(シグマ)及び3μMの蛍光カルシウム指示薬のfluo-4AM(10%のプルロン酸を含むDMSO中の1mM保存溶液)(モルキュラープローブス社製)を含むHBSS)を各ウェルに添加する。
【0187】
その384穴セルプレートを37℃で50分間、5%CO2下でインキュベートし、続いて、測定前に、30ないし120分間、rtにて平衡化する。
【0188】
蛍光イメージングプレートリーダー(FLIPR2又はFLIPR Tetra、Molecular Devices)内で、各ウェル10μlの容量の拮抗薬をプレートに添加し、10分間インキュベートし、最後に各ウェル10μlの作働薬を加える。各ウェルの蛍光を1秒間隔で測定し、各蛍光ピークの高さを、拮抗薬をビークルに代えた3nMのオレキシン−Aによって誘発される蛍光ピークの高さと比較する。各拮抗薬に対して、IC50値(作働薬による反応を50%抑制するために必要とされる化合物の濃度)を測定する。化合物の、算出されるIC50値は、各日の細胞アッセイ操作により変動する。この種の変動は、当業者に既知である。
【0189】
26個の例示化合物のIC50値は、OX1受容体に関して、4−2438nMの範囲内である。すべての例示化合物のIC50値は、OX2受容体に関して、11−1669nMの範囲内である。選択した化合物の拮抗活性を表1に示す。
【0190】
表1
【表5】

【技術分野】
【0001】
本発明は、式(I)の新規な2−アザ−ビシクロ[3.3.0]オクタン誘導体及び医薬としてのこれらの使用に関する。本発明はまた上記化合物の製造方法、式(I)の化合物を1又は2以上含有する医薬組成物、及び特にオレキシン受容体拮抗薬としてのそれらの使用を含む関連した側面に関する。
【背景技術】
【0002】
オレキシン類(オレキシンA又はOX−A及びオレキシンB又はOX−B)は、二つの研究グループによって1998年に発見された新規な神経ペプチド類であり、オレキシンAは、33個のアミノ酸ペプチドであり、オレキシンBは、28個のアミノ酸ペプチドである(Sakurai T.ら、Cell、1998、92、573−585)。オレキシン類は、外側視床下部の離散性神経細胞内で産生され、G蛋白質共役型受容体(OX1及びOX2受容体)に結合する。オレキシン−1受容体(OX1)はOX−Aに対して選択的であり、オレキシン−2受容体(OX2)はOX−Bと同様にOX−Aにも結合することができる。オレキシン類は、ラットにおいて食物消費を刺激し、食行動を調節する中枢フィードバック機構におけるこれらペプチド類のメディエーターとしての生理学的役割を示唆している(Sakurai T.ら、Cell、1998、92、573−585)。他方、オレキシン類は睡眠状態及び覚醒状態を調節しており、ナルコレプシー(睡眠発作)患者に対する潜在的な新規治療への道を開くものであるとも提唱されている(Chemelli R.M.ら、Cell、1999、98、437−451)。
【0003】
オレキシン受容体は哺乳動物の脳に見出され、文献から知られているように、病理学に多くの密接な関係をもっている可能性がある。
【0004】
本発明は、2−アザ−ビシクロ[3.3.0]オクタン化合物を提供し、これらはヒトオレキシン受容体の非ペプチド性拮抗薬である。これらの化合物は、特に、例えば摂食障害、摂水障害(drinking disorders)、睡眠障害又は精神及び神経障害における認知障害の治療における利用可能性を有している。
【0005】
これまでに、OX1か又はOX2のどちらか、あるいは同時に両方の受容体に拮抗する能力を有するいくつかの低分子量化合物が知られている。オレキシン受容体拮抗薬として有用なピペリジン誘導体が国際公開公報第01/96302号に開示されている。
【0006】
本発明は、オレキシン受容体拮抗薬としての2−アザ−ビシクロ[3.3.0]オクタン化合物を初めて記述するものである。
【発明の概要】
【0007】
i) 本発明の第1の側面は、立体中心が(1S,3S,5S)−配置である、式(I)の化合物から成る:
【0008】
【化1】

【0009】
式中
Aは、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン及び、未置換であるか若しくは(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択され;
Bは、アリール−又はヘテロシクリル−基を表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択され;
R1は、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択されるか;又は
R1は、2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表し、当該基は、未置換であるか、又は1若しくは2個の(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンにより独立に置換され;
R2は、水素又は(C1−4)アルキルを表し;
R3は、水素又は(C1−4)アルキルを表す。
【0010】
式(I)の化合物及びその薬学的に許容される塩もまた、本発明の一部である。
【0011】
「ハロゲン」という用語は、フッ素、塩素又は臭素、好ましくはフッ素又は塩素を意味する。
【0012】
「(C1−4)アルキル」という用語は、単独の場合も、組み合わせて用いる場合も、1ないし4個の炭素原子をもつ、直鎖又は分枝鎖アルキル基を意味する。(C1−4)アルキル基の例は、メチル、エチル、プロピル、イソプロピル、n−ブチル、イソ−ブチル、sec.−ブチル又はtert.−ブチルである。好ましくはメチル及びエチルである。最も好ましくは、メチルである。
【0013】
「(C2−6)アルキニル」という用語は、単独の場合も、組み合わせて用いる場合も、2ないし6個の炭素原子をもつ、直鎖又は分枝鎖アルキニル基を意味する。(C2−6)アルキニル基の例は、エチニル、1−プロピニル、1−ブチニル、3−メチル−1−ブチニル、1−ペンチニル、3,3−ジメチル−1−ブチニル、3−メチル−1−ペンチニル、4−メチル−1−ペンチニル又は1−ヘキシニルである。
【0014】
「(C3−6)シクロアルキル」という用語は、単独の場合も、組み合わせて用いる場合も、3ないし6個の炭素原子をもつ、シクロアルキル基を意味する。(C3−6)シクロアルキル基の例は、シクロプロピル、シクロブチル、シクロペンチル又はシクロヘキシルである。好ましくはシクロプロピルである。
【0015】
「(C1−4)アルコキシ」という用語は、単独の場合も、組み合わせて用いる場合も、メトキシ、エトキシ、n−プロポキシ、イソプロポキシ、n−ブトキシ、イソブトキシ、sec.−ブトキシ又はtert.−ブトキシ等の、用語(C1−4)アルキルが前記の意味を有する、式(C1−4)アルキル−O−の基を意味する。好ましくはメトキシ及びエトキシである。最も好ましくは、メトキシである。
【0016】
「アリール」という用語は、単独の場合も、組み合わせて用いる場合も、フェニル又はナフチル基を意味する。アリール基は、未置換であっても、1、2又は3個の置換基により独立に置換されていてもよく、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3、ハロゲン及び、未置換であるか、若しくは、(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択される。
【0017】
「A」が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1若しくは2個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン、及び、未置換であるか又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基が(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される、上記の基を意味する。「A」が「アリール」を表す場合の好ましい例は、未置換であるか、又は1若しくは2個の置換基により独立に置換されたフェニル(好ましくは1置換フェニル)であり、当該置換基は、(C1−4)アルキル,(C3−6)シクロアルキル,(C1−4)アルコキシ及びNR2R3から成る群より独立に選択される。1つの例はフェニルである。上記の置換基に加えて、置換基「A」は置換基「B」によっても置換される。
【0018】
「B」が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2若しくは3個の置換基により置換され、当該置換基が(C1−4)アルキル,(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択される、上記の基を意味する。「B」が「アリール」を表す場合の好ましい例は、未置換であるか又は置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲン(好ましくは、(C1−4)アルキル,NHC(O)CH3、トリフルオロメチル及びハロゲン)から成る群より独立に選択される1、2若しくは3個の置換基により置換されたフェニル(好ましくは、1若しくは2置換フェニル)である。例は、フェニル、3−メチルフェニル、4−メチルフェニル、3,5−ジメチルフェニル、2,4−ジメチルフェニル、3,4−ジメチルフェニル、3−フルオロフェニル、4−フルオロフェニル、3−クロロフェニル、4−ブロモフェニル、3,4−ジフルオロフェニル、3,4−ジクロロフェニル、3−ブロモ−4−フルオロフェニル、3−アセチルアミノフェニル及び3−トリフルオロメチルフェニルである。上記の置換基に加えて、置換基「B」は置換基「A」に結合している。
【0019】
「A」及び「B」が共に「アリール」を表す場合には、組み合わせ「A−B」は、好ましくは、「A」が未置換であるか、又は1若しくは2個の置換基により独立に置換され、「B」が未置換であるか、又は1、2若しくは3個の置換基により置換され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択されるビフェニル基である。「A」及び「B」が共にアリールを表す場合の好ましい例は、「A」が未置換であるか、又は1若しくは2個の置換基により独立に置換され、「B」が未置換であるか、又は1、2若しくは3個の置換基により置換(好ましくは1若しくは2置換)され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル及びハロゲンから成る群より独立に選択されるビフェニル基である。
【0020】
R1が「アリール」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2又は3個の置換基により置換され、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3(好ましくは、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン及びトリフルオロメチル)から成る群より独立に選択される上記の基を意味する。
【0021】
「ヘテロシクリル」という用語は、単独の場合も、組み合わせて用いる場合も、酸素、窒素および硫黄から選択される、例えば1、2または3個の同じか又は異なっていてもよいヘテロ原子を含む5−から10−員の単環又は二環芳香環を意味する。そのようなヘテロシクリル基の例は、フラニル、オキサゾリル、イソオキサゾリル、オキサジアゾリル、チエニル、チアゾリル、イソチアゾリル、チアジアゾリル、ピロリル、イミダゾリル、ピラゾリル、トリアゾリル、ピリジル、ピリミジル、ピリダジニル、ピラジニル、インドリル、イソインドリル、ベンゾフラニル、イソベンゾフラニル、ベンゾチオフェニル、インダゾリル、ベンズイミダゾリル、ベンズオキサゾリル、ベンズイソオキサゾリル、ベンゾチアゾリル、ベンゾトリアゾリル、ベンズオキサジアゾリル、ベンゾチアジアゾリル、キノリニル、イソキノリニル、ナフチリジニル、シノリニル、キナゾリニル、キノキサリニル、フタラジニル、ピラゾロ[1,5−a]ピリジル、ピラゾロ[1,5−a]ピリミジル、イミダゾ[1,2−a]ピリジル又はイミダゾ[2,1−b]チアゾリルである。上記のヘテロシクリル基は、未置換であっても、又は1、2又は3個の置換基により独立に置換されていてもよく、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル、NR2R3、NHC(O)CH3、及び、未置換であるか、又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基は(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される。
【0022】
「A」が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は1若しくは2個の置換基により置換され(好ましくは、未置換若しくは1置換)、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン、及び、未置換であるか、又は独立に1若しくは2個の置換基により置換されたフェニルから成る群より独立に選択され、当該フェニルの置換基が(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される上記の基を意味する。
【0023】
「A」が「ヘテロシクリル」を表す場合におけるさらに好ましい態様において、この用語は、未置換であるか、又は1個の置換基により置換され、当該置換基が(C1−4)アルキル、(C3−6)シクロアルキル及びNR2R3から成る群より選択される上記の基を意味する。「A」が「ヘテロシクリル」を表す場合の好ましい例は、未置換であるか、又は1個の置換基により置換され、当該置換基が(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から選択される、チアゾリル、オキサゾリル、ピリミジル及びピラジニル(好ましくは、チアゾリル)である。上記の置換基に加えて、置換基「A」は置換基「B」によっても置換される。
【0024】
「A」が「ヘテロシクリル」を表し、置換基の1つが「B」により表される特定の例は:
【化2】

である。
【0025】
「B」が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は独立に1、2又は3個の置換基により置換され(好ましくは、1又は2置換)、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、−NR2R3及びハロゲン(好ましくは、(C1−4)アルキル、トリフルオロメチル及びハロゲン)から成る群より独立に選択される上記の基を意味する。上記の置換基に加えて、置換基「B」は置換基「A」に結合される。
【0026】
R1が「ヘテロシクリル」を表す場合には、この用語は、好ましくは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され(好ましくは、未置換であるか、又は1若しくは2個の置換基により独立に置換され)、当該置換基が(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択される上記の基を意味する。さらなる好ましい態様において、R1が「ヘテロシクリル」を表す場合には、この用語は、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基が(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される上記の基を意味する。さらなる好ましい態様において、R1が「ヘテロシクリル」を表す場合には、この用語は、未置換であるか、又は独立に1若しくは2個の置換基により置換され、当該置換基がメチルである上記の基を意味する。
【0027】
R1が「ヘテロシクリル」を表す好ましい例は:
【化3】

である。
【0028】
R1が「ヘテロシクリル」を表すさらなる好ましい例は:
【化4】

である。
【0029】
「NR2R3」という用語は、例えばNH2及びN(CH3)2を意味する。
【0030】
「薬学的に許容される塩」という用語は、無毒性の無機若しくは有機酸及び/又は塩基付加塩を意味する。「Salt selection for basic drugs1、 Int. J. Pharm.(1986)、 33、 201−217」を参照してもよい。
【0031】
ii) 本発明のさらなる態様は、Aがヘテロシクリルを表し、当該ヘテロシクリルが未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から成る群より選択される、態様i)に従う式(I)の化合物を含む。
【0032】
iii) 本発明のさらなる態様は、Bがアリールを表し、当該アリールが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NHC(O)CH3及びハロゲンから成る群より独立に選択される、態様i)ないしii)のいずれか1つに従う式(I)の化合物を含む。
【0033】
iv) 本発明のさらなる態様は、R1がアリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルが未置換であるか、又は1若しく2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンから成る群より独立に選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表す、態様i)ないしiii)のいずれか1つに従う式(I)の化合物を含む。
【0034】
v) 本発明のさらなる態様は、Aがオキサゾリル、チアゾリル又はピリミジル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、態様i)ないしiv)のいずれか1つに従う式(I)の化合物を含む。
【0035】
vi) 本発明のさらなる態様は、Bがフェニルを表し、当該フェニルが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される、態様i)ないしv)のいずれか1つに従う式(I)の化合物を含む。
【0036】
vii) 本発明のさらなる態様は、R1がイミダゾ[2,1−b]チアゾリル又はベンゾイソキサゾリル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−基を表す、態様i)ないしvi)のいずれか1つに従う式(I)の化合物を含む。
【0037】
viii) 本発明のさらなる態様は、Aがチアゾリル基を表し、当該基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、態様i)ないしvii)のいずれか1つに従う式(I)の化合物を含む。
【0038】
ix) 本発明のさらなる態様は、R2及びR3が共に水素を表す、態様i)ないしviii)のいずれか1つに従う式(I)の化合物を含む。
【0039】
好ましい化合物の例は、以下の化合物から成る群より選択される:
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−アミノ−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−m−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;及び
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド。
【0040】
式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造のために使用されてもよく、そのような疾病の予防又は治療に好適である:
大うつ病性障害及び気分循環症を含む気分変調性障害、情動神経症、すべてのタイプの躁鬱病、譫妄、精神病性障害、精神分裂病、緊張型分裂病、妄想性偏執病、適応障害及びすべての群の人格障害;分裂感情障害;全般性不安障害、強迫性障害、心的外傷後ストレス障害、パニック発作、すべてのタイプの恐怖症性不安及び回避性障害を含む不安障害;分離不安;向精神薬の使用、乱用、探索及び再燃;すべてのタイプの心理的又は身体依存、多重人格症候群及び心因性健忘を含む解離性障害;性及び生殖機能障害、心理性的障害及び依存;麻薬耐性又は麻薬離脱症状;麻酔リスク、麻酔応答性の増大;視床下部・副腎機能不全;生物リズム及び概日リズム障害;神経障害性疼痛、下肢静止不能症候群を含む神経障害等の疾患に関連した睡眠障害;睡眠時無呼吸;ナルコレプシー;慢性疲労症候群;精神障害に関連する不眠症;すべてのタイプの突発性不眠症及び錯眠;時差ぼけを含む睡眠−覚醒スケジュール障害;健常者並びに精神及び神経障害におけるすべての痴呆及び認知機能障害;加齢に伴う精神機能障害;すべてのタイプの健忘;重度知的障害;ジスキネジア及び筋疾患;筋痙縮、振戦、運動障害;自発性及び薬剤誘発ジスキネジア;ハンチントン病、クロイツフェルト・ヤコブ病、アルツハイマー病及びトウレット症候群を含む神経変性障害;筋萎縮性側索硬化症;パーキンソン病;クッシング症候群;外傷性病変;脊髄外傷;頭部外傷;周産期低酸素症;難聴;耳鳴り;脱髄疾患;脊髄及び脳神経疾患;眼損傷;網膜症;癲癇;発作障害;欠神発作、複雑部分及び全般発作;レノックスガストー症候群;偏頭痛及び頭痛;疼痛性障害;感覚脱失及び痛覚脱失;痛覚過敏、灼熱痛、異痛症などの疼痛感受性増強又は過大;急性疼痛;熱傷痛;非定型顔面痛;神経障害性疼痛;背部痛;複合局所性疼痛症候群I及びII;関節炎性疼痛;スポーツ外傷痛;歯痛;感染、たとえばHIVに関連した疼痛、化学療法後の疼痛;発作後疼痛;術後痛;神経痛;骨関節炎;過敏腸管症候群などの内臓痛に関連した状態;摂食障害;糖尿病;無酸素脳症、糖尿病性神経障害及びアルコール依存症を含む中毒性及び代謝異常疾患;食欲、味覚障害、摂食又は摂水(Drinking)障害;心気症を含む身体表現性障害;嘔吐/悪心;嘔吐症;胃運動機能異常(ジスキネジア);胃潰瘍;カルマン症候群(嗅覚脱失);耐糖能障害;腸運動機能異常;視床下部疾患;下垂体疾患;高熱症候群、発熱、熱性痙攣、特発性発育不全;小人症;巨人症;先端巨大症;好塩基性細胞腺腫、プロラクチノーマ、高プロラクチン血症;脳腫瘍、腺腫;良性前立腺肥大、前立腺癌;子宮体癌、乳癌、大腸癌;すべてのタイプの精巣機能障害、避妊法;生殖ホルモン異常;閉経期一過性熱感;視床下部性生殖機能低下、機能性又は心因性無月経;膀胱尿失禁;喘息;アレルギー;すべてのタイプの皮膚炎、面皰及び嚢胞、皮脂腺機能障害;心臓血管疾患;心・肺疾患、急性・鬱血性心不全;低血圧;高血圧;脂質異常症、高脂血症、インスリン抵抗性;尿閉;骨粗鬆症;狭心症;心筋梗塞;不整脈、冠動脈疾患、左室肥大;虚血性又は出血性発作;クモ膜下出血;クモ膜下出血、虚血性及び出血性発作並びに血管性痴呆を含むすべてのタイプの脳血管障害;慢性腎不全及びその他の腎疾患;痛風;腎臓癌;尿失禁;並びに一般のオレキシン系機能障害に関連するその他の疾患。
【0041】
式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用、乱用、探索及び再燃、健常者並びに精神及び神経障害における認知機能障害並びに摂食又は摂水(Drinking)障害。
【0042】
摂食障害は代謝機能不全;食欲調節不全;強迫的肥満;嘔吐・過食又は神経性食欲不振症を含むものとして定義できる。この摂食の病理学的変形は、食欲障害(食物に対する誘惑又は嫌悪);エネルギーバランスの変調(摂取/消費)、食品品質についての知覚障害(高脂肪又は高炭水化物、良味覚);食物入手可能性障害(無制限節食又は遮断)又は水分平衡障害から生じるかもしれない。
【0043】
摂水障害(Drinking disorders)は、精神障害における多飲症及びすべての他のタイプの過剰液体摂取を含む。
【0044】
睡眠障害は、すべてのタイプの錯眠、不眠症、ナルコレプシー及び過眠症、睡眠関連失調症、下肢静止不能症候群、睡眠時無呼吸症、時差症候群、交代勤務睡眠障害、睡眠相遅延症候群、睡眠相前進症候群又は精神障害に関連する不眠症を含む。不眠症は、加齢と関係付けられる睡眠障害;慢性不眠の間歇治療;環境による一過性の不眠症(新しい環境、騒音)又はストレス;悲嘆;疼痛又は病気による短期間の不眠症を含むものとして定義される。不眠症は、全般性不安障害、強迫性障害、パニック発作並びにすべてのタイプの恐怖症性不安及び回避性障害等の他のタイプ及びサブタイプの不安障害のみならず心的外傷後ストレス障害を含むストレス関連症候群をも包含する;向精神薬の使用、乱用、探索及び再燃は、すべてのタイプの心理的又は身体依存並びにそれらに関連する耐性及び依存因子と定義される。認知機能障害は、正常な、健康な、若年の、成人の又は老齢の集団において一時的に又は慢性的に生じ、また精神、神経、心臓血管及び免疫疾患において一時的に又は慢性的に生じるすべてのタイプの注意、学習及び記憶機能における欠損を含む。
【0045】
本発明のさらに好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:すべてのタイプの不眠、ナルコレプシー及び過眠症、睡眠関連失調症、下肢静止不能症候群、睡眠時無呼吸症、時差症候群、交代勤務睡眠障害、睡眠相遅延症候群、睡眠相前進症候群又は精神障害に関連する不眠症の他の障害を含む睡眠障害。
【0046】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:正常な、健康な、若年の、成人の又は老齢の集団において一時的に又は慢性的に生じ、また精神、神経、心臓血管及び免疫疾患において一時的に又は慢性的に生じるすべてのタイプの注意、学習及び記憶機能における欠損を含む認知機能障害。
【0047】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:代謝機能不全;食欲調節不全;強迫的肥満;嘔吐・過食又は神経性食欲不振症を含む摂食障害。
【0048】
本発明の別の好ましい態様において、式(I)の化合物は、下記の群より選択される疾病の予防又は治療のための医薬の製造に使用されてもよく、そのような疾病の予防又は治療に好適である:すべてのタイプの心理的又は身体依存並びにそれらに関連する耐性及び依存因子を含む向精神薬の使用、乱用、探索及び再燃。
【0049】
医薬組成物の製造は、いずれの当業者によく知られた様式で(例えば、Remington、The Science and Practice of Pharmacy、21st Edition(2005)、Part 5、“Pharmaceutical Manufacturing” [Lippincott Williams & Wilkinsにより出版]を見よ。)、記述された式(I)の化合物又はこれらの薬学的に許容される塩を、任意にその他の治療的に有益な物質と組み合わせて、適切な無毒の不活性な治療上許容される固体又は液体の担体材料及び必要に応じて、通常の薬学的アジュバントと共に、製剤投与形態とすることにより遂行することができる。
【0050】
式(I)の化合物及びこれらの薬学的に許容される塩は、医薬として、たとえば経腸又は非経口投与のための医薬組成物の形態で使用することができる。
【0051】
本発明のさらなる側面は、式(I)の化合物の製造のための方法である。本発明の式(I)の化合物は、下記のスキームに概説した反応の包括的なシークエンスに従って製造することができ、該スキーム中、A、B及びR1は、式(I)の記述において定義した通りである。得られた化合物は、それ自体知られた方法により、それらの薬学的に許容される塩に変換してもよい。
【0052】
一般的に、すべての化学的変換は、文献に記載され、又は下記の手順に記載された、よく知られた標準的方法論に従って遂行することができる。
【0053】
式(I)の化合物の製造:
【化5】

【0054】
式(I)の2−アザ−ビシクロ[3.3.0]オクタン誘導体の合成における最初の工程は、(1S,3S,5S)−2−アザビシクロ[3.3.0]オクタン−3−カルボキシレートの窒素原子の、Boc2Oでの保護により、式(2)の化合物を得ることであった。式(2)の化合物は、低温でのDIBALによる処理により、アルコール(3)に還元された。アルコール(3)は、例えばデス−マーチンペルヨージナン等の酸化剤で、対応するアルデヒド(4)に酸化された。ナトリウムトリアセトキシボロヒドリドのような還元剤の存在下における、ベンジルアミンでの(4)の還元的アミノ化の後、中間体(5)のベンジル基は水素化分解により除去され、第一アミン(6)を生じた。TBTUのようなカップリング剤の存在下における、カルボン酸R1COOHでの(6)のアシル化により、アミド(7)の形成が起こり、アミド(7)は、Boc−基の除去後、アミドカップリング(例えばB−A−COOH、TBTU)により、式(I)の化合物に変換された。
【0055】
式B−A−COOHのチアゾール−4−カルボン酸誘導体は、例えばスキーム2に従って合成された。
【0056】
【化6】

【0057】
カリウムtert−ブトキシド等の塩基の存在下で、メチルジクロロアセテート(9;購入可能)をアルデヒドと反応させることにより、α−オキソ−エステル誘導体(10)が得られ、この化合物は、チオアミド[R=C1−4アルキル又は(C3−6)シクロアルキル]との反応において2−アルキル−又は2−シクロアルキル置換チアゾール誘導体(11)に、又はチオウレア(R=NR2R3)との反応において2−アミノ−置換チアゾール誘導体(11)に変換された。メタノール等の溶媒中での、例えば水酸化ナトリウム水溶液でのエステル官能基のけん化により、所望のカルボン酸(12、R=C1−4アルキル、(C3−6)シクロアルキル又はNR2R3)が生成した。2−ブロモ−チアゾール誘導体(13)は、例えば、臭化銅(II)の存在下における、それぞれの2−アミノ−チアゾール誘導体(11、R=NH2)の亜硝酸イソアミルとの反応により得られた。エステル誘導体(13)は、シクロプロピル−スズ誘導体(購入可能)による、パラジウム触媒反応において、化合物(14)に変換され、それをけん化することにより、それぞれのカルボン酸(15)が得られた。さらに、2−ブロモ−チアゾール誘導体(13)は、上記のように、対応するカルボン酸(16)にけん化され、又はナトリウムアルコキシドとの反応、それに続くNaOHでのけん化により、2−メトキシ置換アナログ(17)に変換される。加えて、2位が未置換の化合物(19)は、木炭上パラジウムの存在下での水素による(13)の水素化、それに続く中間体エステル(18)のけん化により合成される。(11)の合成における(C3−6)シクロアルキル−置換チオアミドは、購入可能であるか、又は、それぞれのカルボキサミドのLawessonの試薬との反応により得られた(実験の部のA.1.6も見よ。)。アルデヒドB−CHOは購入可能であるか、又は、例えばそれぞれのカルボン酸又はそれらの異なる誘導体の還元剤による還元のような文献から知られている手順により、それぞれのニトリルの還元により、又はベンジルアルコール及びそれらのヘテロシクリルアナログを酸化剤で酸化することにより合成してもよい(例えば:J. March、Advanced Organic Chemistry、4th edition、John Wiley & Sons、p. 447−449、919−920及び1167−1171)。
【0058】
式R1−COOHのイミダゾ[2,1−b]チアゾール−カルボン酸誘導体は、購入可能でない場合には、例えばスキーム3に示す異なった経路の一つに従って合成してもよい。
【0059】
【化7】

【0060】
【化8】

【0061】
【化9】

【0062】
経路Aに従い、イミダゾ[2,1−b]チアゾール−カルボン酸誘導体を、2−クロロ−3−オキソ−ブチル酸メチルエステル(20;購入可能)から、エタノール等の溶媒中での、高温におけるチオ尿素(購入可能)との反応により合成した。得られたアミノ−チアゾール(21)は、アルキル化、続く濃塩酸等の酸の存在下におけるブロモアセトアルデヒドジエチルアセタールでの環化により、イミダゾ[2,1−b]チアゾール誘導体(22)に変換された。THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによる(22)のけん化により、所望の酸(23)を得た。
【0063】
別のアプローチ(経路B)は、アセトン等の溶媒中での、2−ブロモ−3−オキソ−酪酸エステル(24;購入可能)の、2−アミノ−5−メチル−チアゾール(購入可能)との反応で始まり、得られたイミダゾ[2,1−b]チアゾール誘導体(25)は、THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによるけん化により、所望の酸(26)に変換された。
【0064】
木炭上パラジウムの存在下における、酸性条件下(例えば、EtOH中HCl)での、2−ヒドロキシイミノ−3−オキソ−酪酸エステル(27;購入可能)の水素化、及び、続くチオシアン酸カリウムとの反応により、イミダゾール誘導体(28)を得、それを、それぞれのα−ハロゲン化プロパノン(購入可能)又はブタノン誘導体(経路C;購入可能)との反応により、2つの可能な異性体(29)及び(30)の混合物に変換した。クロマトグラフィーにより異性体を分離した後、THF及びMeOH等の溶媒中での、例えば、水酸化ナトリウムによるけん化により、所望のイミダゾ[2,1−b]チアゾール−カルボン酸誘導体(31)及び(32)を得た。
【0065】
イミダゾール誘導体(28)はまた、ナトリウムエトキシド等の塩基の存在下での、ブロモアセトアルデヒドジエチルアセタール(購入可能。)によるアルキル化により、アセタール(33)に変換してもよい(経路D)。酸性条件下(例えば塩酸)での環化及び例えば塩化ホスホリルでの中間体(34)の脱水によりエステル(35)が得られ、エステル(35)は、THF及びMeOH等の溶媒中における例えば水酸化ナトリウムでのけん化により、所望の酸(36)に変換された。
【0066】
さらに別の手順(経路E)においては、それぞれのアミノ−チアゾール(37;購入可能)は、(37)を、トルエン等の溶媒中でN,N−ジメチルホルムアミドジメチルアセタール(購入可能)とともに加熱することにより、ホルムアミジン誘導体(38)に変換された。エチルブロモアセテート(購入可能)でのアルキル化の後、それぞれの臭化チアゾリウム(39)はDBUで環化され、エステル(40)が得られた。エステル(40)は、THF及びMeOH等の溶媒中で、例えば水酸化ナトリウムでけん化され、所望の酸(41)が得られた。
【0067】
最後に、2−アミノ−チアゾール(購入可能)の3−ブロモ−1,1,1−トリフルオロアセトン(購入可能)でのアルキル化で始まる経路Fにより、トリフルオロメチル−置換イミダゾ[2,1−b]チアゾール誘導体(42)が得られ、この誘導体は、DMF等の溶媒中における塩化ホスホリルとの反応によりホルミル化され、アルデヒド(43)を与えた。亜塩素酸ナトリウムでのアルデヒド(43)の酸化により、所望のイミダゾ[2,1−b]チアゾール−カルボン酸(44、Y=CF3))が得られた。同様に、購入可能な塩素化アルデヒド(43、Y=Cl)は、酸(44、Y=Cl)に酸化された。
【0068】
実験の部
(この項において、及び本明細書のこれまでの部分において使用される)略語:
Ac OAcにおけるようにアセチル:アセテート
Boc tert−ブトキシカルボニル
BSA ウシ血清アルブミン
Bu n−ブチル
CHO チャイニーズハムスター卵巣
conc. 濃縮された
d 日
DBU 1,8−ジアザビシクロ−[5.4.0]−ウンデス−7−エン
DCM ジクロロメタン
DIBAL ジイソブチルアルミニウム水和物
DIPEA ジイソプロピルエチルアミン
DMAP 4−ジメチルアミノピリジン
DMF N,N−ジメチルホルムアミド
eq 当量
ES 電子スプレー
Et エチル
EtOH エタノール
EtOAc 酢酸エチル
エーテル ジエチルエーテル
FCS ウシ胎児血清
FLIPR 蛍光イメージングプレートリーダー
h 時間
HBSS ハンクス平衡塩溶液
HEPES 4−(2−ヒドロキシエチル)−ピペリジン−1−エタンスルホン酸
HPLC 高速液体クロマトグラフィー
KOt−Bu カリウムtertiary(tert.)ブトキシド
LC 液体クロマトグラフィー
M モル
Me メチル
MeCN アセトニトリル
MeOH メタノール
min 分
MS 質量分析
Ph フェニル
prep. 分取用
RT 室温
sat 飽和
tR 保持時間
TBTU O−ベンゾトリアゾール−1−イル−N,N,N’,N’−テトラメチル
ウロニウムテトラフルオロホウ酸塩
TFA トリフルオロ酢酸
THF テトラヒドロフラン
【0069】
I−化学
以下の実施例は、本発明の薬理学的に活性を有する化合物の製造を説明するが、本発明の範囲をまったく限定するものではない。
【0070】
温度はすべて℃で示す。
【0071】
化合物は、
1H−NMRによって:300MHz Varian Oxford又は400MHz Bruker Avance;化学シフトは、使用する溶媒と関連して、ppmで示される;多重度:s=一重項、d=二重項、t=三重項、m=多重項、b=広域、結合定数はHzで示される;
LC−MSによって:DAD及びMS検知を備えたAgilent 1100シリーズ(MS:Finnigan シングル 四重極);カラム(4.6x5mm、5m):Zorbax SB−AQ、Zorbax Extend C18又はWaters XBridge C18;条件:
塩基性:溶出液A:MeCN、溶出液B:濃NH3水溶液(1.0mL/L)、5%から95%CH3CN;
酸性:溶出液A:MeCN、溶出液B:TFA水溶液(0.4mL/L)、5%から95%CH3CN、tRは分で示される;
特徴付けられる。
【0072】
化合物は、シリカゲル上のカラム・クロマトグラフィーにより、又はMeCN/水勾配を用い、ギ酸又はアンモニアを添加した、RP−C18ベースのカラムを用いた分取用HPLCにより精製される。
【0073】
A. 前駆体及び中間体の製造:
A.1 チアゾール−4−カルボン酸誘導体の合成
A.1.1 3−クロロ−2−オキソ−プロピオンエステル誘導体の合成(一般的手順)
【0074】
【化10】

【0075】
それぞれのアルデヒド(338mmol、1.0eq)及びジクロロ酢酸メチル(338mmol、1.0eq)のTHF(100ml)中の溶液を、KOtBu(335mmol、1.0eq)のTHF(420ml)中の冷(−60℃)懸濁液に滴下する。4h後、混合物をRTにし、一晩攪拌し、真空濃縮する。DCM及び氷冷水を添加し、層を分離し、水層をDCMで2回抽出する。合わせた有機層を氷冷水及び塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のα−オキソ−エステルを得、それをさらに精製することなく使用する。
【0076】
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステル
4−メチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0077】
3−クロロ−3−(3−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0078】
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
4−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0079】
3−クロロ−3−(3−クロロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−クロロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0080】
3−クロロ−2−オキソ−3−m−トリル−プロピオン酸メチルエステル
3−メチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0081】
3−クロロ−2−オキソ−3−(3−トリフルオロメチル−フェニル)−プロピオン酸メチルエステル
3−トリフルオロメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0082】
3−(4−ブロモ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステル
4−ブロモ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0083】
3−クロロ−3−(3,5−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,5−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0084】
3−(3−ブロモ−4−フルオロ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステル
3−ブロモ−4−フルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0085】
3−クロロ−3−(3,4−ジフルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジフルオロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0086】
3−クロロ−3−(2,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
2,4−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0087】
3−クロロ−3−(3,4−ジクロロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジクロロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0088】
3−クロロ−3−(3,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステル
3,4−ジメチル−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0089】
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステル
ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0090】
3−クロロ−3−(3−ニトロ−フェニル)−2−オキソ−プロピオン酸メチルエステル
3−ニトロ−ベンズアルデヒドの、ジクロロ酢酸メチルとの反応により製造。
【0091】
A.1.2 チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0092】
【化11】

【0093】
チオアセタミド(132mmol、1.0eq)のMeCN(250ml)中の溶液を、それぞれのα−オキソ−エステル(132mmol、1.0eq)及びモレキュラー・シーヴ(4Å、12g)のMeCN(60ml)中の混合物に添加する。5h撹拌した後、混合物を氷浴中で冷却し、得られた沈殿物をろ過する。残渣を冷MeCNで洗浄し、乾燥し、MeOH(280ml)中に溶解し、50℃で6h撹拌する。溶媒を真空除去して、所望のチアゾール誘導体を、白色の固体として得る。
【0094】
2−メチル−5−p−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.92min;[M+H]+=248.2。
【0095】
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.91min;[M+H]+=252.1。
【0096】
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。1H−NMR(CDCl3):δ=2.75(s、3H);3.84(s、3H);7.10(m、2H);7.47(m、2H)。
【0097】
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−クロロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=268.0。
【0098】
2−メチル−5−m−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−m−トリル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.98min;[M+H]+=248.5。
【0099】
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−(3−トリフルオロメチル−フェニル)−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.98min;[M+H]+=302.2。
【0100】
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−(4−ブロモ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=312.2。
【0101】
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,5−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.97min;[M+H]+=262.3。
【0102】
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−(3−ブロモ−4−フルオロ−フェニル)−3−クロロ−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.95min;[M+H]+=330.2。
【0103】
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジフルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.92min;[M+H]+=270.3。
【0104】
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(2,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.96min;[M+H]+=262.3。
【0105】
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジクロロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.99min;[M+H]+=302.2。
【0106】
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3,4−ジメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.96min;[M+H]+=262.3。
【0107】
2−メチル−5−フェニル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.89min;[M+H]+=234.0。
【0108】
2−メチル−5−(3−ニトロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−ニトロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオアセタミドとの反応により製造。LC−MS:tR=0.94min;[M+H]+=279.3。
【0109】
A.1.3 2−アミノ−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0110】
【化12】

【0111】
それぞれのα−オキソ−エステル(22.1mmol、1.0eq)のアセトン(25ml)中の溶液を、チオウレア(22.1mmol、1.0eq)のアセトン(45ml)中の懸濁液に添加する。混合物を57℃(温浴の温度)に加熱し、24h撹拌し、半分の体積になるまで濃縮する。得られた懸濁液をろ過し、残渣をアセトンで洗浄する。乾燥後、所望のアミノ−チアゾール誘導体を固体として得る。
【0112】
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−p−トリル−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.77min;[M+H]+=249.3。
【0113】
2−アミノ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(4−フルオロ−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.75min;[M+H]+=253.2。
【0114】
2−アミノ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
3−クロロ−3−(3−トリフルオロメチル−フェニル)−2−オキソ−プロピオン酸メチルエステルの、チオウレアとの反応により製造。LC−MS:tR=0.86min;[M+H]+=303.3。
【0115】
A.1.4 2−ブロモ−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順)
【0116】
【化13】

【0117】
不活性雰囲気下、臭化銅(II)(69.6mmol、1.0eq)を、アセトニトリル(300ml)に懸濁し、そして5−10℃に冷却した後、亜硝酸3−メチルブチル(104mmol、1.45eq)を15minに渡って添加した。この反応混合物に、それぞれの2−アミノチアゾール誘導体(70.0mmol、1eq、遊離アミン)を、5−10℃にて、20min.に渡り、少しずつ添加した。次いで、反応混合物を注意深く65℃に加熱し、そして攪拌を2h継続した。揮発物を減圧下で除去し、そして残渣をカラムクロマトグラフィー(シリカゲル;ヘプタン/EtOAc又はDCM/メタノール、適宜な混合物として)で精製して、それぞれの生成物を得た。
【0118】
2−ブロモ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−アミノ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルの反応により製造。LC−MS:tR=0.97min;[M+H]+=316.1。
【0119】
2−ブロモ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−アミノ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルの反応により製造。LC−MS:tR=1.04min;[M+H]+=366.2。
【0120】
A.1.5 2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順I)
【0121】
【化14】

【0122】
不活性雰囲気において、それぞれの2−ブロモ−チアゾール誘導体(9.0mmol、1.0eq)及びトリブチル−シクロプロピル−スタナン(9.9mmol、1.1eq)の、1,2−ジクロロ−エタン(90mL)中の溶液を、5min攪拌し、そしてビス(トリフェニルホスフィン)−パラジウム(II)クロリド(0.45mmol、0.05eq)で処理する。混合物を80℃に加熱し、3d攪拌し、そしてRTに到達させる。DCMと水を添加し、層を分離し、そして水層をDCMで1回抽出する。合わせた有機層をMgSO4上で乾燥し、そして真空濃縮する。残渣をカラムクロマトグラフィー(シリカゲル;ヘプタン/EtOAc、適宜な混合物として)で精製して、所望の生成物を得る。
【0123】
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−ブロモ−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルのシクロプロピル化により製造。LC−MS:tR=0.97min;[M+H]+=278.3。
【0124】
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステル
2−ブロモ−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのシクロプロピル化により製造。LC−MS:tR=1.03min;[M+H]+=328.2。
【0125】
A.1.6 2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順II)
【0126】
【化15】

【0127】
シクロプロパンカルボチオ酸アミドの合成
2,4−ビス−(4−メトキシ−フェニル)−[1,3,2,4]ジチアジホスフェタン−2,4−ジスルフィド(Lawessonの試薬、115mmol)を、シクロプロパンカルボキサミド(115mmol)と炭酸ナトリウム(115mmol)の、THF(500mL)中の混合物に添加する。混合物を2h加熱還流し、溶媒を真空除去し、そして残渣をエーテル(500mL)と水(500mL)で希釈する。層を分離し、そして水層をエーテル(250mL)で抽出する。合わせた有機層を塩水(100mL)で洗浄し、MgSO4上で乾燥し、そして真空濃縮して、所望のチオアミドを得、それをさらに精製することなく使用する。LC−MS:tR=0.39min;[M+H+CH3CN]+=143.2。
【0128】
2−シクロプロピル−チアゾール−4−カルボン酸メチルエステル誘導体の合成(一般的手順II)
シクロプロパンカルボチオ酸アミド(44.5mmol、1.0eq)のMeCN(40ml)中の溶液を、それぞれのα−オキソ−エステル(44.5mmol、1.0eq)及びNaHCO3(134mmol、3.0eq)のMeCN(80ml)中の混合物に添加する。16h撹拌した後、混合物を真空濃縮し、残渣をEtOAc(200ml)及び水(200ml)で希釈する。層を分離し、水層をEtOAc(100ml)で抽出する。合わせた有機層を塩水(100ml)で洗浄し、MgSO4上で乾燥し、そして真空濃縮する。粗生成物をMeOH(90ml)中に溶解し、濃縮H2SO4(0.25ml)で処理する。混合物を60℃で16h撹拌し、真空濃縮して、それぞれのチアゾール誘導体を得る。
【0129】
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸メチルエステル
3−クロロ−2−オキソ−3−フェニル−プロピオン酸メチルエステルの、シクロプロパンカルボチオ酸アミドとの反応により製造。LC−MS:tR=0.99min;[M+H]+=260.5。
【0130】
A.1.7 5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルの合成
A.1.7.1 5−(3−アミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルの合成
2−メチル−5−(3−ニトロ−フェニル)−チアゾール−4−カルボン酸メチルエステル(44.1mmol)及び塩化アンモニウム(220mmol)の、EtOH(100ml)及び水(50ml)の混合物中の懸濁液を、鉄粉(53.0mmol)で処理し、そして80℃に加熱する。4h後、鉄粉(53.0mmol)をさらに添加し、混合物を80℃で3h加熱し、さらに鉄粉(26.5mmol)を添加し、そして混合物を再び80℃にて3.5h加熱する。混合物をRTに到達させ、DCMで希釈し、そしてセライトを通してろ過する。ろ液を真空濃縮し、そしてDCM及びsat.NaHCO3水溶液で希釈する。層を分離し、そして有機層を水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアニリン誘導体を得る粗生成物を得る。LC−MS:tR=0.67min;[M+H]+=249.4。
【0131】
A.1.7.2 5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸 メチルエステルの合成
トリエチルアミン(14.2mmol)及びDMAP(4.00mmol)を、5−(3−アミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステル(4.00mmol)の無水酢酸(25ml)中の溶液に添加する。30min後、EtOAc及び水を添加し、層を分離し、水層をEtOAcで1回抽出する。合わせた有機層をsat.塩化アンモニウム水溶液で2回、sat.NaHCO3水溶液で1回そして水で1回洗浄し、そして溶媒を真空除去する。残渣をEtOAcで希釈し、そしてsat NaHCO3水溶液で3回抽出する。有機層をMgSO4上で乾燥し、真空濃縮して、粗製の固形物を得、それをエーテルで希釈する。得られた懸濁液をろ過し、そして残渣をエーテルで洗浄して、所望のアセタミドを得る。LC−MS:tR=0.81min;[M+H]+=291.3。
【0132】
A.1.8 チアゾール−4−カルボン酸誘導体の合成(一般的手順)
【0133】
【化16】

【0134】
それぞれのエステル(96.2mmol)の、THF(150ml)、及びMeOH(又はイソプロパノール、50ml)の混合物中の溶液を、NaOH水溶液(1.0M、192ml)で処理する。3h撹拌した後、白色の懸濁液が生成し、有機揮発物を真空除去する。残った混合物を水(100ml)で希釈し、氷浴中で冷却し、塩酸(1.0M)の添加により酸性(pH=3−4)にする。沈殿が生成した場合には、懸濁液をろ過し、残渣を冷水で洗浄し、そして真空乾燥して、所望の酸を得る。そうでない場合には、混合物をEtOAcで2回抽出し、そして有機層を合わせ、MgSO4上で乾燥し、真空濃縮して、それぞれの酸を得る。
【0135】
2−メチル−5−p−トリル−チアゾール−4−カルボン酸
2−メチル−5−p−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.83min;[M+H]+=234.0。
【0136】
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.82min;[M+H]+=238.1。
【0137】
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。1H−NMR(DMSO−d6):δ=2.67(s、3H);7.27(m、2H);7.53(m、2H);12.89(br.s、1H)。
【0138】
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.84min;[M+H]+=254.0。
【0139】
2−メチル−5−m−トリル−チアゾール−4−カルボン酸
2−メチル−5−m−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.87min;[M+H]+=234.4。
【0140】
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸
2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.88min;[M+H]+=288.0。
【0141】
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.85min;[M+H]+=298.2。
【0142】
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=248.3。
【0143】
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=316.2。
【0144】
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.82min;[M+H]+=256.3。
【0145】
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.85min;[M+H]+=248.3。
【0146】
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.88min;[M+H]+=288.2。
【0147】
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.86min;[M+H]+=248.3。
【0148】
2−メチル−5−フェニル−チアゾール−4−カルボン酸
2−メチル−5−フェニル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.77min;[M+H]+=220.0。
【0149】
5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸
5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.73min;[M+H]+=277.2。
【0150】
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸
2−アミノ−5−p−トリル−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.64min;[M+H]+=235.2。
【0151】
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸
2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.87min;[M+H]+=264.2。
【0152】
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸
2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボン酸メチルエステルのけん化により製造。LC−MS:tR=0.94min;[M+H]+=314.2。
【0153】
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸
2−シクロプロピル−5−フェニル−チアゾール−4−カルボン酸のけん化により製造。LC−MS:tR=0.91min;[M+H]+=246.4。
【0154】
A.2 2,3−ジヒドロ−ベンゾフラン−4−カルボン酸の合成
ベンゾフラン−4−カルボン酸(30.8mmol、M.A.Eissenstatら J.Med.Chem.1995、38,3094−3105)を、Pd/C(10%、2.00g)のEtOH(25ml)中の懸濁液に添加する。さらにEtOH(75ml)を添加し、混合物を水素雰囲気下(4bar)、16h、RTにて撹拌する。セライトを通してろ過し、溶媒を除いた後、所望の生成物を得、それをさらに精製することなく使用する。1H−NMR(DMSO−d6):δ=3.45(t、J=8.79Hz、2H);4.55(t、J=8.79Hz、2H);6.99(d、J=7.78Hz、1H);7.21(t、J=7.91Hz、1H);7.39(d、J=7.78Hz、1H);12.9(bs、1H)。
【0155】
A.3 (1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
A.3.1 (1S,3S,5S)−(2−tert−ブトキシ−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−カルボン酸 ベンジルエステルの合成
ベンジル(1S,3S,5S)−2−アザビシクロ[3.3.0]オクタン−3−カルボキシレート塩酸塩(17.3mmol、1.0eq)の、DCM(50mL)中の溶液に、DIPEA(22.5mmol、1.3eq)、二炭酸ジ−tert−ブチル(17.3mmol、1.0eq)及び追加のDCM(5mL)を添加する。混合物を1h攪拌し、そして真空濃縮する。EtOAc及びクエン酸水溶液(10%)を添加し、層を分離し、そして水層をEtOAcで1回抽出する。合わせた有機層を塩水で洗浄し、MgSO4上で乾燥し、そして真空濃縮する。残渣をカラムクロマトグラフィー(ヘプタン/EtOAc 3/1)で精製して、所望の生成物を得る。LC−MS:tR=1.08min;[M+H]+=346.3。
【0156】
A.3.2 (1S,3S,5S)−3−ヒドロキシメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
−78℃にて、DIBALのトルエン中の溶液(1.7M、22.5mmol)を、(1S,3S,5S)−(2−tert−ブトキシ−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−カルボン酸ベンジルエステル(9.0mmol)の、THF(50mL)中の溶液に滴下する。40min後、混合物をRTに到達させ、さらに45min攪拌し、そしてNaOH水溶液(1.0M、250mL)と氷の混合物に注ぐ。EtOAcを添加し、層を分離し、そして水層をEtOAcで抽出する。合わせた有機層を、NaOH水溶液(1.0M)と塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアルコールを得、それをフラッシュ・クロマトグラフィー(ヘプタン/EtOAc 3/1)で精製する。LC−MS:tR=0.91min;[M+H]+=242.4。
【0157】
A.3.3 (1S,3S,5S)−3−ホルミル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
デス−マーチン ペルヨージナン(4.14mmol、2.2eq)の、DCM(10ml)中の溶液を、(1S,3S,5S)−3−ヒドロキシメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(1.85mmol、1.0eq)のDCM(4mL)中の溶液及び数滴の水で処理する。5h後、エーテルとNaOH水溶液(1.0M)を添加し、そして層を分離する。有機層をクエン酸水溶液(10%)と塩水で洗浄し、MgSO4上で乾燥し、真空濃縮して、所望のアルデヒドを得、それをさらに精製することなく使用する。
【0158】
A.3.4 (1S,3S,5S)−3−(ベンジルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
ベンジルアミン(2.76mmol、2.3eq)を、(1S,3S,5S)−3−ホルミル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(1.2mmol、1.0eq)の、クロロホルム(10mL)中の溶液に添加する。混合物を5min攪拌し、ナトリウムトリアセトキシボロヒドリド(4.8mmol、4.0eq)及び酢酸(0.05mL)で処理し、そしてさらに14h攪拌し、sat.NaHCO3水溶液中に注ぐ。DCMを添加し、層を分離し、そして水層をDCMで抽出する。合わせた有機層を水(100mL)で洗浄し、そして真空濃縮する。残渣をエーテル中に溶解し、そして塩酸(0.1M)で3回抽出する。合わせた水層をエーテルで1回抽出し、NaOH溶液(1.0M)の添加により塩基性(pH9−10)にし、そしてエーテルで3回抽出する。合わせた有機層をMgSO4上で乾燥し、真空濃縮して、所望のベンジルアミンを得、それをさらに精製することなく使用する。LC−MS:tR=0.89min;[M+H]+=331.5。
【0159】
A.3.5 (1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成
(1S,3S,5S)−3−(ベンジルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(9.0mmol)の、エタノール(10mL)中の溶液を、Pd/C(1.9g、10%)の、エタノール(40mL)中の懸濁液に添加し、そして水素雰囲気下(1bar)で16h攪拌する。セライトを通してろ過し、エタノールで洗浄し、そして溶媒を除去した後、所望のアミンを得、それをさらに精製することなく使用する。LC−MS:tR=0.73min;[M+H]+=241.4。
【0160】
A.4 (1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イルメチル)−アミド誘導体の合成
A.4.1 (1S,3S,5S)−3−(アロイルアミノ−メチル)−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの合成(一般的手順)
【0161】
【化17】

【0162】
それぞれのカルボン酸(4.6mmol、1.1eq)のDMF(15mL)中の溶液に、TBTU(5.0mmol、1.2eq)を添加する。30min後、DIPEA(12.5mmol、3.0eq)と(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル(4.2mmol、1.0eq)のDMF(10mL)中の溶液を添加し、そして混合物を60min攪拌する。水とEtOAcを添加し、層を分離し、そして有機層を水で1回洗浄する。合わせた水層をEtOAcで1回抽出し、そして合わせた有機層をMgSO4上で乾燥する。溶媒を真空除去し、そして残渣をカラムクロマトグラフィー(DCM)で精製して、それぞれのアミドを得る。
【0163】
(1S,3S,5S)−3−{[(6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸(A.Andreaniら、Eur.J.Med.Chem 1982、17、271−274)の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=0.91min;[M+H]+=405.2。
【0164】
(1S,3S,5S)−3−{[(ベンゾ[d]イソキサゾール−3−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
ベンゾ[d]イソキサゾール−3−カルボン酸の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=1.11min;[M+H]+=386.6。
【0165】
(1S,3S,5S)−3−{[(2,3−ジヒドロ−ベンゾフラン−4−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステル
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸の、(1S,3S,5S)−3−アミノメチル−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルとの反応により製造。LC−MS:tR=1.00min;[M+H]+=387.1。
【0166】
A.4.2 (1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イルメチル)−アミド誘導体の合成(一般的手順)
【0167】
【化18】

【0168】
HClのジオキサン(4.0M、20mL)中の溶液を、それぞれのBoc−保護2−アザビシクロ[3.3.0]オクタン誘導体(3.6mmol)の、ジオキサン(20mL)中の溶液に添加する。LC−MSが反応の完了を示した後(1−3h)、混合物を真空濃縮して、それぞれの脱保護生成物を得、それをさらに精製することなく使用する。
【0169】
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.56min;[M+H]+=305.3。
【0170】
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(ベンゾ[d]イソキサゾール−3−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.71min;[M+H]+=286.3。
【0171】
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミド
(1S,3S,5S)−3−{[(2,3−ジヒドロ−ベンゾフラン−4−カルボニル)−アミノ]−メチル}−2−アザビシクロ[3.3.0]オクタン−2−カルボン酸tert−ブチルエステルの脱保護により製造。LC−MS:tR=0.70min;[M+H]+=287.4。
【0172】
B. 式(I)の化合物の製造:
B.1 カルボン酸アミド誘導体の合成(一般的手順)
【0173】
【化19】

【0174】
それぞれのカルボン酸(0.44mmol、1.1eq)の、アセトニトリル(1.0mL)中の混合物に、TBTU(0.48mmol、1.2eq)を添加し、そして30min後にDIPEA(1.2mmol、3.0eq)を添加する。15min後に、それぞれの2−アザビシクロ[3.3.0]オクタン誘導体(0.40mmol、1.0eq)のDCM(1.0mL)中の溶液を添加する。混合物を一晩攪拌し、そしてprep.HPLCで精製して、それぞれのアミド誘導体を得る。
【0175】
それぞれのカルボン酸の、6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0176】
【表1】

【0177】
それぞれのカルボン酸の、ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0178】
【表2】

【0179】
それぞれのカルボン酸の、2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−(2−アザビシクロ[3.3.0]オクタン−3−イル)メチル]−アミドとの反応による、カルボン酸アミド誘導体の合成:
【0180】
【表3】

【0181】
【表4】

【0182】
II. 生物学的アッセイ
式(I)の化合物のオレキシン受容体拮抗活性は、以下の実験法に従って測定される。
【0183】
細胞内カルシウム濃度の測定:
ヒトオレキシン−1受容体及びヒトオレキシン−2受容体を発現しているチャイニーズハムスター卵巣(CHO)細胞をそれぞれ300μg/mlのG418、100U/mlのペニシリン、100μg/mlのストレプトマイシン及び10%熱不活性化牛胎児血清(FCS)を含む培地(L−グルタミン含有HAM F−12)で培養する。予め、ハンクス平衡塩溶液(HBSS)に溶解した1%ゼラチンで被覆した384穴の黒色の透明底の滅菌プレート(Greiner)に1穴当り20、000個の細胞を播種する。播種したプレートは、5%のCO2下、37℃で一晩インキュベートする。
【0184】
作働薬のヒトオレキシン−Aを、MeOH:水(1:1)中の1mM保存溶液として調製し、アッセイでの使用に際しては、0.1%牛血清アルブミン(BSA)、0.375g/lのNaHCO3及び20mMのHEPESを含むHBSSに、3nMの最終濃度に希釈する。
【0185】
拮抗薬はDMSOに10mMの保存溶液として調製したのち、384穴のプレート中で、DMSOを用いて希釈し、次いで、希釈液を、0.1%牛血清アルブミン(BSA)、0.375g/lのNaHCO3及び20mMのHEPESを含むHBSSに移す。
【0186】
アッセイの日に、染色バッファー50ml(1%のFCS、20mMのHEPES、0.375g/lのNaHCO3、5mMのプロベネシド(シグマ)及び3μMの蛍光カルシウム指示薬のfluo-4AM(10%のプルロン酸を含むDMSO中の1mM保存溶液)(モルキュラープローブス社製)を含むHBSS)を各ウェルに添加する。
【0187】
その384穴セルプレートを37℃で50分間、5%CO2下でインキュベートし、続いて、測定前に、30ないし120分間、rtにて平衡化する。
【0188】
蛍光イメージングプレートリーダー(FLIPR2又はFLIPR Tetra、Molecular Devices)内で、各ウェル10μlの容量の拮抗薬をプレートに添加し、10分間インキュベートし、最後に各ウェル10μlの作働薬を加える。各ウェルの蛍光を1秒間隔で測定し、各蛍光ピークの高さを、拮抗薬をビークルに代えた3nMのオレキシン−Aによって誘発される蛍光ピークの高さと比較する。各拮抗薬に対して、IC50値(作働薬による反応を50%抑制するために必要とされる化合物の濃度)を測定する。化合物の、算出されるIC50値は、各日の細胞アッセイ操作により変動する。この種の変動は、当業者に既知である。
【0189】
26個の例示化合物のIC50値は、OX1受容体に関して、4−2438nMの範囲内である。すべての例示化合物のIC50値は、OX2受容体に関して、11−1669nMの範囲内である。選択した化合物の拮抗活性を表1に示す。
【0190】
表1
【表5】

【特許請求の範囲】
【請求項1】
立体中心が(1S,3S,5S)−配置である、式(I)の化合物、又はその薬学的に許容される塩:
【化1】

式(I)中、
Aは、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン及び、未置換であるか若しくは(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択され;
Bは、アリール−又はヘテロシクリル−基を表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択され;
R1は、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択されるか;又はR1は、2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表し、これらの基は、未置換であるか、又は1若しくは2個の(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンにより独立に置換され;
R2は、水素又は(C1−4)アルキルを表し;
R3は、水素又は(C1−4)アルキルを表す。
【請求項2】
Aがヘテロシクリルを表し、当該ヘテロシクリルが、未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から成る群より選択される、請求項1に記載の化合物;又はその薬学的に許容される塩。
【請求項3】
Bがアリールを表し、当該アリールが、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NHC(O)CH3及びハロゲンから成る群より独立に選択される、請求項1ないし2のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項4】
R1がアリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルが、未置換であるか、又は1若しく2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンから成る群より独立に選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表す、請求項1ないし3のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項5】
Aがオキサゾリル、チアゾリル又はピリミジル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、請求項1ないし4のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項6】
Bがフェニルを表し、当該フェニルが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される、請求項1ないし5のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項7】
R1がイミダゾ[2,1−b]チアゾリル又はベンゾイソキサゾリル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−基を表す、請求項1ないし6のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項8】
Aがチアゾリル基を表し、当該基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、請求項1ないし7のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項9】
R2及びR3が共に水素を表す、請求項1ないし8のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項10】
以下からなる群より選択される請求項1ないし9のいずれか1項に記載の化合物:
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−アミノ−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−m−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;及び
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
又はその薬学的に許容される塩。
【請求項11】
活性成分として、請求項1に記載の式(I)の化合物、又はその薬学的に許容される塩を、そして少なくとも一種の治療上不活性な賦型剤を含む医薬組成物。
【請求項12】
医薬として使用するための、請求項1ないし10のいずれか1項に記載の化合物、又はその薬学的に許容される塩。
【請求項13】
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用及び乱用、健常者並びに精神及び神経障害における認知機能障害、摂食又は摂水(Drinking)障害からなる群より選択される疾患の予防又は治療のための医薬を製造するための、請求項1ないし10のいずれかに記載の化合物、又はその薬学的に許容される塩の使用。
【請求項14】
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用及び乱用、健常者並びに精神及び神経障害における認知機能障害、摂食又は摂水(Drinking)障害からなる群より選択される疾患の予防又は治療のための、請求項1ないし10のいずれか1項の化合物、又はその薬学的に許容される塩。
【請求項1】
立体中心が(1S,3S,5S)−配置である、式(I)の化合物、又はその薬学的に許容される塩:
【化1】

式(I)中、
Aは、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C3−6)シクロアルキル、(C2−6)アルキニル、(C1−4)アルコキシ、NR2R3、ハロゲン及び、未置換であるか若しくは(C1−4)アルキル、(C1−4)アルコキシ、フッ素及び塩素から成る群より独立に選択される1若しくは2個の置換基により独立に置換されるフェニル、から成る群より独立に選択され;
Bは、アリール−又はヘテロシクリル−基を表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NR2R3、NHC(O)CH3及びハロゲンから成る群より独立に選択され;
R1は、アリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルは、未置換であるか、又は1、2若しくは3個の置換基により独立に置換され、当該置換基は、(C1−4)アルキル、(C1−4)アルコキシ、ハロゲン、トリフルオロメチル及びNR2R3から成る群より独立に選択されるか;又はR1は、2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表し、これらの基は、未置換であるか、又は1若しくは2個の(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンにより独立に置換され;
R2は、水素又は(C1−4)アルキルを表し;
R3は、水素又は(C1−4)アルキルを表す。
【請求項2】
Aがヘテロシクリルを表し、当該ヘテロシクリルが、未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNR2R3から成る群より選択される、請求項1に記載の化合物;又はその薬学的に許容される塩。
【請求項3】
Bがアリールを表し、当該アリールが、未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ、トリフルオロメチル、NHC(O)CH3及びハロゲンから成る群より独立に選択される、請求項1ないし2のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項4】
R1がアリール又はヘテロシクリルを表し、当該アリール又はヘテロシクリルが、未置換であるか、又は1若しく2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、(C1−4)アルコキシ及びハロゲンから成る群より独立に選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−又は2,3−ジヒドロ−ベンゾ[1,4]ジオキシニル−基を表す、請求項1ないし3のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項5】
Aがオキサゾリル、チアゾリル又はピリミジル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、請求項1ないし4のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項6】
Bがフェニルを表し、当該フェニルが未置換であるか、又は1若しくは2個の置換基により独立に置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より独立に選択される、請求項1ないし5のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項7】
R1がイミダゾ[2,1−b]チアゾリル又はベンゾイソキサゾリル基を表し、これらの基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、トリフルオロメチル及びハロゲンから成る群より選択されるか;又はR1が2,3−ジヒドロ−ベンゾフラニル−基を表す、請求項1ないし6のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項8】
Aがチアゾリル基を表し、当該基が未置換であるか、又は1個の置換基により置換され、当該置換基が、(C1−4)アルキル、(C3−6)シクロアルキル又はNH2から成る群より選択される、請求項1ないし7のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項9】
R2及びR3が共に水素を表す、請求項1ないし8のいずれか1項に記載の化合物;又はその薬学的に許容される塩。
【請求項10】
以下からなる群より選択される請求項1ないし9のいずれか1項に記載の化合物:
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸[(1S,3S,5S)−2−(2−アミノ−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(4−フルオロ−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
6−メチル−イミダゾ[2,1−b]チアゾール−5−カルボン酸{(1S,3S,5S)−2−[2−シクロプロピル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−p−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
ベンゾ[d]イソキサゾール−3−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−クロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−m−トリル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[2−メチル−5−(3−トリフルオロメチル−フェニル)−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(4−ブロモ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,5−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−ブロモ−4−フルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジフルオロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(2,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジクロロ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3,4−ジメチル−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸{(1S,3S,5S)−2−[5−(3−アセチルアミノ−フェニル)−2−メチル−チアゾール−4−カルボニル]−2−アザビシクロ[3.3.0]オクタン−3−イルメチル}−アミド;
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−メチル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;及び
2,3−ジヒドロ−ベンゾフラン−4−カルボン酸[(1S,3S,5S)−2−(2−シクロプロピル−5−フェニル−チアゾール−4−カルボニル)−2−アザビシクロ[3.3.0]オクタン−3−イルメチル]−アミド;
又はその薬学的に許容される塩。
【請求項11】
活性成分として、請求項1に記載の式(I)の化合物、又はその薬学的に許容される塩を、そして少なくとも一種の治療上不活性な賦型剤を含む医薬組成物。
【請求項12】
医薬として使用するための、請求項1ないし10のいずれか1項に記載の化合物、又はその薬学的に許容される塩。
【請求項13】
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用及び乱用、健常者並びに精神及び神経障害における認知機能障害、摂食又は摂水(Drinking)障害からなる群より選択される疾患の予防又は治療のための医薬を製造するための、請求項1ないし10のいずれかに記載の化合物、又はその薬学的に許容される塩の使用。
【請求項14】
すべてのタイプの睡眠障害、ストレス関連症候群、向精神薬の使用及び乱用、健常者並びに精神及び神経障害における認知機能障害、摂食又は摂水(Drinking)障害からなる群より選択される疾患の予防又は治療のための、請求項1ないし10のいずれか1項の化合物、又はその薬学的に許容される塩。
【公表番号】特表2010−534647(P2010−534647A)
【公表日】平成22年11月11日(2010.11.11)
【国際特許分類】
【出願番号】特願2010−517536(P2010−517536)
【出願日】平成20年7月25日(2008.7.25)
【国際出願番号】PCT/IB2008/052989
【国際公開番号】WO2009/016564
【国際公開日】平成21年2月5日(2009.2.5)
【出願人】(500226786)アクテリオン ファーマシューティカルズ リミテッド (151)
【氏名又は名称原語表記】Actelion Pharmaceuticals Ltd
【住所又は居所原語表記】Gewerbestrass 16,CH−4123 Allschwil,Switzerland
【Fターム(参考)】
【公表日】平成22年11月11日(2010.11.11)
【国際特許分類】
【出願日】平成20年7月25日(2008.7.25)
【国際出願番号】PCT/IB2008/052989
【国際公開番号】WO2009/016564
【国際公開日】平成21年2月5日(2009.2.5)
【出願人】(500226786)アクテリオン ファーマシューティカルズ リミテッド (151)
【氏名又は名称原語表記】Actelion Pharmaceuticals Ltd
【住所又は居所原語表記】Gewerbestrass 16,CH−4123 Allschwil,Switzerland
【Fターム(参考)】
[ Back to top ]

