2次電池用正極材料及びその製造方法
【課題】 リチウムとナトリウムを同時に含むマンガンフッ化リン酸化物LiXNa2−XMnPO4Fを電極材料として使用できる2次電池用正極材料及びその製造方法を提供する。
【解決手段】 化学的方法によりリチウムをナトリウムの位置に部分置換したLiXNa2−XMnPO4Fを製造し、電極素材として使用可能にした点、及びカーボンコーティングにより電気伝導度を向上させて電気化学的活性を有するリチウム電池の正極材料を提供できることを特徴とする。
【解決手段】 化学的方法によりリチウムをナトリウムの位置に部分置換したLiXNa2−XMnPO4Fを製造し、電極素材として使用可能にした点、及びカーボンコーティングにより電気伝導度を向上させて電気化学的活性を有するリチウム電池の正極材料を提供できることを特徴とする。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、2次電池用正極材料及びこの製造方法に係り、より詳しくは、リチウムあるいはナトリウムを含むマンガンフッ化リン酸化物を電極材料として使用できる2次電池用正極材料及びその製造方法に関する。
【背景技術】
【0002】
携帯可能な小型電機電子機器の普及が広がるにつれてニッケル水素電池やリチウム2次電池という新型の2次電池の開発が盛んである。この中、リチウム2次電池は、黒鉛などのカーボンを負極活物質とし、リチウムが含まれている酸化物を正極活物質とし、非水溶媒を電解液とする電池であり、リチウムはイオン化傾向が非常に大きい金属であるため、高電圧を発生でき、高エネルギー密度の電池開発に活用されている。
【0003】
前記正極活物質としてはリチウムを含有しているリチウム遷移金属酸化物が主に使われており、コバルト系、ニッケル系、及びコバルト、ニッケル、マンガンが共存する3成分系などの層状系リチウム遷移金属酸化物が90%以上使用されている。
【0004】
しかし、正極活物質として主に使用されている層状系リチウム遷移金属酸化物は、非理想状態(過充電及び高温状態)で格子にある酸素が脱離して反応に関与するため、電池の発火のような異常挙動の原因となり、このような層状系リチウム金属酸化物が有する短所を克服するために、スピネル型及びオリビン型の構造を有する正極活物質に対する研究が行われている。
【0005】
このような正極の劣化により安全性が悪くなったリチウム2次電池の問題点を解決するために、正極材料として層状系リチウム遷移金属酸化物ではなく、3次元的なリチウムの移動経路を有するスピネル型リチウムマンガン酸化物及びオリビン構造を含むポリアニオン系リチウム金属リン酸化物が提案されたが、スピネル型リチウムマンガン酸化物は充電/放電によるリチウムの溶出問題とヤーン・テラー歪みによる構造の不安定性により、その使用が制限されている。
【0006】
前記オリビン型リチウム金属リン酸化物のうち、鉄(Fe)系とマンガン(Mn)系は低電気伝導により正極材料としての使用が制限されたが、粒子のナノサイズ化及びカーボンコーティングなどによりその問題点が改善され、正極材料として使用が可能になった。
【0007】
最近、ポリアニオン系材料のうち、フッ素を含むフッ化リン酸化物(Fluorophosphates)が報告されており、フッ化リン酸化物は、フッ素を含むA2MPO4Fの化学式を持つもので、AはLi、Naであり、Mは電位金属Mn、Fe、Co、Ni、V、あるいはこれらの混合物である。理論的には2つのナトリウムを含むため、従来のリチウム金属リン酸化物に比して約2倍の理論容量が期待される。
【0008】
また、ナトリウムを含むNa2MPO4F(M=Mn、Fe、Co、Ni、Vあるいはこれらの混合物)は、リチウム2次電池の正極素材として使用する時、初期充電過程でナトリウムが脱離され、初期放電過程でリチウムが挿入され、その後のサイクルではリチウムの挿入脱離反応が充電/放電と共に行われ、また、ナトリウム電池の正極素材として使用する時、ナトリウムの挿入脱離が充電/放電と共に行われる。
【0009】
特許文献1ではナトリウムを含むNaVPO4F、Na2FePO4F、(Na,Li)2FePO4Fなどのフッ化リン酸化物をナトリウム電池(Sodium based battery)の正極材料として使用した例が開示されているが、リチウム電池ではなく、ナトリウム電池に限定している。
【0010】
従来技術の他の例では、ナトリウム鉄フッ化リン酸化物Na2FePO4Fとして、Na2FePO4Fの構造、リチウム2次電池の正極素材としての電気化学的な特性などが公開されているが、鉄系のNa2FePO4Fの場合、充電/放電電位が3.5V近くになって、鉄系オリビン素材のように低充電/放電電位を有する短所があり、また、鉄系と比較してマンガン系Na2MnPo4Fは、高電位(4V)を有するが、マンガンを含むポリアニオン系材料の低電気伝導度による電気化学的な不活性が問題である。
【0011】
フッ化リン酸化物に関する発明者の先行特許の特許文献2では、粒子の大きさを制御することにより電気化学的な特性が向上することを報告した。この時、優れた充電/放電特性を得るためには、粒子の大きさを100nm以下に制御しなければならないことを提示した。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】米国特許6,872,492
【特許文献2】大韓民国特許出願第10−2011−051912号
【発明の開示】
【発明が解決しようとする課題】
【0013】
本発明は前記のような点に鑑みてなされたものであって、本発明の目的は、粒子のナノサイズ化によりリチウムの拡散距離を短縮させて電池特性を向上させる以外に、化学的方法によりナトリウムを脱離し、リチウムを挿入する方法で正極素材にリチウムの拡散経路(diffusion path)を予め確保することで、電気化学特性を改善したリチウム2次電池用正極材料及びこの製造方法を提供することにある。
【課題を解決するための手段】
【0014】
上記のような目的を達成するための本発明の一実施形態は、Na2MnPO4Fに化学的な方法によりリチウムを挿入してLiXNa2−XMnPO4Fで表わされる化合物を含む2次電池用正極材料を提供することを特徴とする。
【0015】
前記目的を達成するための本発明の実施例は、(i)粒子の大きさが制御されたNa2MnPO4Fを合成する段階と、(ii)イオン交換法によりリチウム挿入/ナトリウム脱離する段階と、を含むことを特徴とする。
【発明の効果】
【0016】
本発明によれば、イオン交換法を用いて化学的にリチウムを挿入してリチウムが拡散可能なサイトを確保することで、リチウムを含んでいない同じ大きさの正極素材Na2MnPO4Fと比較して優れた充電/放電特性が得られる。したがって、電気化学特性に優れたリチウムを含むマンガンフッ化リン酸塩を正極材料として提供できる。
【0017】
本発明の正極材料を2次電池用正極に適用する場合、同じ大きさの1次粒子を有するNa2MnPOF4と比較して最大4倍以上の容量が得られる。
【図面の簡単な説明】
【0018】
【図1】MnO4F2が8面体、PO4が4面体を形成して骨格構造をなし、リチウムとナトリウムが挿入脱離可能なチャネルが存在するLiXNa2−XMnPO4Fの結晶構造を示す図。
【図2】本発明の実施例3により製造された正極材料の、(a)イオン交換前、(b)イオン交換後を示す電子顕微鏡イメージ。
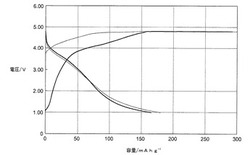
【図3】本発明の比較例1により製造された正極材料の室温における充電/放電曲線のグラフ。
【図4】本発明の実施例1により製造された正極材料の室温における充電/放電曲線のグラフ。
【図5】実施例1、実施例2、実施例3、及び比較例1により製造された正極材料の室温における、リチウムの挿入量に応じた放電曲線の変化を示すグラフ。
【発明を実施するための形態】
【0019】
本発明の一実施形態によれば、本発明は、下記一般式(1)で表されるマンガン系フッ化リン酸塩化合物を含むリチウム2次電池用正極材料を提供する。
[化1]
LiXNa2−XMnPO4F (1)
【0020】
本発明の好ましい実施例によれば、前記化学式を含む2次電池用正極材料は1次粒子の大きさが300nm以下であり、導電性を向上させるためにカーボンをコーティングし、3.7V〜4.0Vで放電による電位平坦面を示す。
【0021】
本発明の他の実施形態によれば、本発明は、(i)ナトリウム(Na)酸化物またはその前駆体、マンガン(Mn)酸化物またはその前駆体、リン(P)酸化物またはその前駆体、フッ化物(F)またはその前駆体をボールミルを用いて均一に混合して前処理した後、焼成することによりNa2MnPO4Fを合成する段階と、(ii)前記(i)段階で合成された正極材料にイオン交換法を用いてリチウムを挿入してLiXNa2−XMnPO4Fを合成する段階と、を含むことを特徴とするリチウム2次電池用正極材料の製造方法を提供する。
【0022】
本発明の好ましい実施例によれば、前記段階(i)は、前記ボールミルを用いて6時間均一に混合した混合物を300℃で2時間空気雰囲気で前処理する。
【0023】
本発明の好ましい実施例によれば、前記段階(ii)は、前記段階(i)から得られた前記正極材料にイオン交換法を用いてリチウム挿入/ナトリウム脱離によりリチウムイオンを正極材料内に挿入する過程を含む。
【0024】
本発明の好ましい実施例によれば、前記段階(ii)は、前記段階(i)により合成した前記正極材料に化学的にナトリウムを脱離した後、化学的にリチウムを挿入する過程を含む。
【0025】
本発明の好ましい実施例によれば、前記段階(ii)から得られた正極材料とカーボン導電材を60:40〜90:10の比率で均一に混合した後、ボールミルする過程でカーボン導電材を正極表面に均一にコーティングして電気伝導度を高める。
【0026】
本発明の好ましい実施例によれば、前記ナトリウム酸化物の前駆体は、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物から選択された何れか1つである。
【0027】
本発明の好ましい実施例によれば、前記マンガン酸化物の前駆体は、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物から選択された何れか1つである。
【0028】
本発明の好ましい実施例によれば、前記イン酸化物の前駆体は、リン酸アンモニウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物から選択された何れか1つである。
【0029】
本発明の好ましい実施例によれば、前記イオン交換法を用いてリチウムを挿入する場合、イオン交換を誘発する物質としてLiBrまたはLiIを用いる。
【0030】
本発明の好ましい実施例によれば、前記カーボン導電材は、クエン酸(Citric Acid)、スクロース(Sucrose)、スーパーP(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンである。
【0031】
以下、本発明について添付図面を参照して詳細に説明する。
本発明は、下記の一般式(1)で表される化合物を含む2次電池用正極材料を提供する。
[化1]
LiXNa2−XMnPO4F (1)
前記一般式(1)でxの範囲は、0<x<2である。
【0032】
特に、本発明の正極材料は、リチウムとナトリウムを同時に含んでおり、3.7V〜4.0Vで放電による電位平坦面を示し、導電性を向上させるためにカーボンによりコーティングされる。
【0033】
ここで、本発明による2次電池用正極材料の製造方法を説明すれば次の通りであり、具体的な製造方法は下記の実施例から容易に理解できる。
本発明の正極材料は、ナトリウム酸化物またはその前駆体、マンガン酸化物またはその前駆体、リン酸化物またはその前駆体、フッ化物またはその前駆体をボールミル(Ball mill)を用いて均一に混合して前処理段階が行われ、このように前処理段階から得られた混合物を焼成する熱処理段階により2次電池用正極材料Na2MnPO4Fが製造される。
【0034】
この時、製造されたNa2MnPO4Fは粒子の大きさが1μm以下で、300nmの平均粒子の大きさを有する。
【0035】
このように製造されたNa2MnPO4Fは、LiBrが溶解されたアセトニトリル溶液に投入してArガスを流しながら温度を上昇させてリチウムとナトリウムのイオン交換を起こす。イオン交換の結果物を洗浄及び乾燥する過程を経てマンガンフッ化リン酸塩LiXNa2−XMnPO4Fの正極材料が得られる。
【0036】
マンガンフッ化リン酸化物の低電気伝導度の問題を解決するために、得られたLiXNa2−XMnPO4Fの正極材にカーボンコーティングを施した。
【0037】
前記ナトリウム酸化物の前駆体は特に制限されることはないが、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物である。
【0038】
前記マンガン酸化物の前駆体は特に制限されることはないが、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物である。
【0039】
前記イン酸化物の前駆体は特に制限されることはないが、リン酸リチウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物である。
【0040】
前記フッ素の前駆体は特に制限されることはないが、金属フッ化物、フッ化物、またはこれらの混合物である。
【0041】
前記イオン交換に用いられるリチウムソースはLiBrに特に制限されることはなく、イオン交換を誘発するリチウム混合物である。
【0042】
前記イオン交換に用いられる溶媒はアセトニトリルに特に制限されることはなく、イオン交換を提供する溶媒である。
【0043】
前記カーボン導電材は特に制限されることはないが、クエン酸(Citric Acid)、シュクロス(Sucrose)、スーパーP(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンからなる物質が使用される。
【0044】
このように製造される本発明の正極材料はリチウム2次電池の製造に使用されるが、正極材料を異なる方式で適用したことを除き、既存のリチウム2次電池の製造方式と同一であり、その構成及び製造方法を簡略に説明すると次の通りである。
【0045】
先ず、本発明の正極材料を用いた正極極板の製作工程を説明すると、必要に応じて導電材、結着剤、フィラー、分散剤、イオン導電剤、圧力増強剤など、通常用いられる1種または2種以上の添加成分を添加し、適当な溶媒(有機溶媒)によりスラリーやペースト化し、得られたスラリーまたはペーストを電極支持基板にドクターブレード法などを用いて塗布した後、乾燥過程を経て圧延ロールなどでプレス(pressing)して最終的な正極極板を製造する。
【0046】
この時、前記導電材としては、黒鉛、カーボンブラック、アセチレンブラック、ケッチェンブラック(Ketchen Black)、炭素繊維、金属粉などがある。結着剤としては、PVdF、ポリエチレンなどが用いられ、電極支持基板(集電体)は、銅、ニッケル、ステンレス鋼鉄、アルミニウムなどの箔、シート、あるいは炭素繊維などで構成できる。
【0047】
このように製造された正極極板を用いてリチウム2次電池を製作するが、リチウム2次電池の形態は、コイン、ボタン、シート、円筒形、角形など何れも良く、リチウム2次電池の負極、電解質、分離膜などは従来のリチウム2次電池のものを使用する。
【0048】
また、前記負極活物質はリチウムを含んでいない黒鉛系材料を用いてもよい。勿論、リチウムを含む遷移金属の複合酸化物などの1種あるいは2種以上を用いてもよい。その他、シリコン、スズなども負極活物質として用いてもよい。
【0049】
また、前記電解液は、有機溶媒にリチウム塩を溶解させた非水系電解液、無機固体電解質、無機固体電解質の複合材などの何れもよく、非水系電解液の溶媒としてはエチレンカーボネート、プロピレンカーボネート、ジメチルカーボネート、ジエチルカーボネート、メチルエチルカーボネートなどのエステル類、ブチルラクトンなどのラクトン類、1,2−ジメトキシエタン、エトキシメトキシエタンなどのエーテル類、アセッツニトリルなどのニトリル類などの1種あるいは2種以上を使用でき、非水系電解液のリチウム塩の例としてはLiAsF6、LiBF4、LiPF6などを使用できる。
【0050】
また、前記分離膜としてはPP及び/またはPEなどのポリオレフィン(Polyolefin)から製造される多孔性フィルムや不織布などの多孔性材を使用できる。
以下、本発明を具体的な実施例を挙げて詳細に説明するが、本発明の権利範囲がこれら実施例に限定されることはない。
【0051】
実施例1
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0052】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0053】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0054】
実施例2
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0055】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを1.0MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0056】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0057】
実施例3
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0058】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを2.5MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0059】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0060】
比較例1
実施例1と同じ条件により得られたNa2MnPO4Fをイオン交換過程を経ることなく、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0061】
比較例2〜4
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0062】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、10時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例2)、1.0M(比較例3)、2.5M(比較例4)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0063】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0064】
比較例5〜7
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0065】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、550℃、3時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例5)、1.0M(比較例6)、2.5M(比較例7)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0066】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0067】
比較例8〜10
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0068】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、550℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例8)、1.0M(比較例9)、2.5M(比較例10)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0069】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0070】
実験例1:電極性能の評価
実施例1〜3と比較例1〜10により製造された正極材料の1次粒子の大きさと正極材料の金属組成分析をICP発光分光分析により測定し、下記表1に示した。
【0071】
【表1】

【0072】
粒子の大きさが減少するにつれて、同一のLiBrの濃度に対応してイオン交換によりLiXNa2−XMnPO4Fに挿入されるリチウムの量が増加することが確認できた。特に、1次粒子の大きさが700nm〜400nmである場合は、粒子の大きさの減少により挿入されるリチウムの量が少し増加したが、300nmで挿入されるリチウムの量が大きく増加することが確認できた。
【0073】
これは化学的な方法によるリチウムの挿入は1次粒子の大きさに大きく依存することを意味する。したがって、Na2MnPO4Fに、イオン交換などの化学的な方法によりリチウムを挿入させるためには、粒子の大きさの制御が重要であることが分かる。化学的方法による効果的なリチウムの挿入に求められる1次粒子の大きさは300nm以下である。したがって、出発物質のボールミリング条件及び熱処理条件が重要であることが分かる。
【0074】
本発明の粒子の大きさを制御することは、このようなボールミリング及び熱処理条件を調節することによりなされ、これは実験装備の条件に応じて多少変更することもある。重要な点は、1粒子の大きさが一定の大きさ以下に制御されることにより、化学的なリチウムの挿入が可能になり、結果的にリチウムとナトリウムを同時に含んだLiXNa2−XMnPO4Fが製造される。
【0075】
実施例1〜3と比較例1〜10の正極材料複合体の粉末を用いて正極材料複合体95wt%、結着剤PVdF 5wt%を混合し、N−メチルピロリドン(NMP)を溶媒としてスラリーを製造した。
【0076】
このスラリーを厚さ20μmのアルミニウム箔(Al foil)に塗布して乾燥した後、プレスで圧密化して真空上で120℃で16時間乾燥することにより、直径16mmのディスク電極を製造した。
【0077】
対極としては直径16mmにパンチングしたリチウム金属箔を、分離膜としてはポリプロピレン(PP)フィルムを使用し、電解液としては1MのLiPF6のエチレンカーボネート/ジメトキシエタン(EC/DME)1:1v/vの混合溶液を使用し、電解液を分離膜に含浸させた後、この分離膜を作用極と対極との間に入れた後、SUS製品のケースを電極評価用試験セルにして電池の電極性能を評価し、放電容量を含んだ測定結果を下記表2に記載した。
【0078】
【表2】

【0079】
図2は実施例3のイオン交換処理前後の試料の表面を電子顕微鏡イメージで示す図面であり、イオン交換後の試料の表面がナトリウムの脱離及びリチウムの挿入により荒くなったことを観測した。
【0080】
イオン交換による充電/放電特性の変化を実施例1と比較例1から確認した(図3及び図4)。イオン交換を施さなかったNa2MnPO4Fは55mAhg−1の放電容量を示し、これと比較してイオン交換を施してリチウムが0.3挿入されたLi0.3Na1.7Mn2PO4Fは140mAhg−1という2.5倍程度高い放電容量を示すことを確認した。
【0081】
0.3のリチウムが挿入されるだけで、純粋ナトリウムのみ含むNa2MnPO4Fと比較して高い放電容量が得られるため、リチウムの挿入がマンガン系フッ化リン酸化物の容量増加に大きい影響を及ぼすことが分かる。
【0082】
また、図5に示すように、リチウムの挿入量が0.3から1.9まで増加するにつれて(実施例1〜3)放電容量が140mAhg−1から197mAhg−1に増加することが確認できた。以上の結果から判断すると、マンガン系フッ化リン酸化物にリチウムを挿入することにより、顕著な容量増加の効果が得られ、これは挿入されたリチウムがリチウム拡散に起因する通路(pathway)を確保することにより、充電/放電によるリチウムの挿入/脱離、あるいはナトリウムの挿入/脱離に肯定的な効果を与えると判断される。
【産業上の利用可能性】
【0083】
本発明は、リチウムあるいはナトリウムを含むマンガンフッ化リン酸化物を電極材料として使用できる2次電池用正極材料及びこの製造方法の分野に適用できる。
【技術分野】
【0001】
本発明は、2次電池用正極材料及びこの製造方法に係り、より詳しくは、リチウムあるいはナトリウムを含むマンガンフッ化リン酸化物を電極材料として使用できる2次電池用正極材料及びその製造方法に関する。
【背景技術】
【0002】
携帯可能な小型電機電子機器の普及が広がるにつれてニッケル水素電池やリチウム2次電池という新型の2次電池の開発が盛んである。この中、リチウム2次電池は、黒鉛などのカーボンを負極活物質とし、リチウムが含まれている酸化物を正極活物質とし、非水溶媒を電解液とする電池であり、リチウムはイオン化傾向が非常に大きい金属であるため、高電圧を発生でき、高エネルギー密度の電池開発に活用されている。
【0003】
前記正極活物質としてはリチウムを含有しているリチウム遷移金属酸化物が主に使われており、コバルト系、ニッケル系、及びコバルト、ニッケル、マンガンが共存する3成分系などの層状系リチウム遷移金属酸化物が90%以上使用されている。
【0004】
しかし、正極活物質として主に使用されている層状系リチウム遷移金属酸化物は、非理想状態(過充電及び高温状態)で格子にある酸素が脱離して反応に関与するため、電池の発火のような異常挙動の原因となり、このような層状系リチウム金属酸化物が有する短所を克服するために、スピネル型及びオリビン型の構造を有する正極活物質に対する研究が行われている。
【0005】
このような正極の劣化により安全性が悪くなったリチウム2次電池の問題点を解決するために、正極材料として層状系リチウム遷移金属酸化物ではなく、3次元的なリチウムの移動経路を有するスピネル型リチウムマンガン酸化物及びオリビン構造を含むポリアニオン系リチウム金属リン酸化物が提案されたが、スピネル型リチウムマンガン酸化物は充電/放電によるリチウムの溶出問題とヤーン・テラー歪みによる構造の不安定性により、その使用が制限されている。
【0006】
前記オリビン型リチウム金属リン酸化物のうち、鉄(Fe)系とマンガン(Mn)系は低電気伝導により正極材料としての使用が制限されたが、粒子のナノサイズ化及びカーボンコーティングなどによりその問題点が改善され、正極材料として使用が可能になった。
【0007】
最近、ポリアニオン系材料のうち、フッ素を含むフッ化リン酸化物(Fluorophosphates)が報告されており、フッ化リン酸化物は、フッ素を含むA2MPO4Fの化学式を持つもので、AはLi、Naであり、Mは電位金属Mn、Fe、Co、Ni、V、あるいはこれらの混合物である。理論的には2つのナトリウムを含むため、従来のリチウム金属リン酸化物に比して約2倍の理論容量が期待される。
【0008】
また、ナトリウムを含むNa2MPO4F(M=Mn、Fe、Co、Ni、Vあるいはこれらの混合物)は、リチウム2次電池の正極素材として使用する時、初期充電過程でナトリウムが脱離され、初期放電過程でリチウムが挿入され、その後のサイクルではリチウムの挿入脱離反応が充電/放電と共に行われ、また、ナトリウム電池の正極素材として使用する時、ナトリウムの挿入脱離が充電/放電と共に行われる。
【0009】
特許文献1ではナトリウムを含むNaVPO4F、Na2FePO4F、(Na,Li)2FePO4Fなどのフッ化リン酸化物をナトリウム電池(Sodium based battery)の正極材料として使用した例が開示されているが、リチウム電池ではなく、ナトリウム電池に限定している。
【0010】
従来技術の他の例では、ナトリウム鉄フッ化リン酸化物Na2FePO4Fとして、Na2FePO4Fの構造、リチウム2次電池の正極素材としての電気化学的な特性などが公開されているが、鉄系のNa2FePO4Fの場合、充電/放電電位が3.5V近くになって、鉄系オリビン素材のように低充電/放電電位を有する短所があり、また、鉄系と比較してマンガン系Na2MnPo4Fは、高電位(4V)を有するが、マンガンを含むポリアニオン系材料の低電気伝導度による電気化学的な不活性が問題である。
【0011】
フッ化リン酸化物に関する発明者の先行特許の特許文献2では、粒子の大きさを制御することにより電気化学的な特性が向上することを報告した。この時、優れた充電/放電特性を得るためには、粒子の大きさを100nm以下に制御しなければならないことを提示した。
【先行技術文献】
【特許文献】
【0012】
【特許文献1】米国特許6,872,492
【特許文献2】大韓民国特許出願第10−2011−051912号
【発明の開示】
【発明が解決しようとする課題】
【0013】
本発明は前記のような点に鑑みてなされたものであって、本発明の目的は、粒子のナノサイズ化によりリチウムの拡散距離を短縮させて電池特性を向上させる以外に、化学的方法によりナトリウムを脱離し、リチウムを挿入する方法で正極素材にリチウムの拡散経路(diffusion path)を予め確保することで、電気化学特性を改善したリチウム2次電池用正極材料及びこの製造方法を提供することにある。
【課題を解決するための手段】
【0014】
上記のような目的を達成するための本発明の一実施形態は、Na2MnPO4Fに化学的な方法によりリチウムを挿入してLiXNa2−XMnPO4Fで表わされる化合物を含む2次電池用正極材料を提供することを特徴とする。
【0015】
前記目的を達成するための本発明の実施例は、(i)粒子の大きさが制御されたNa2MnPO4Fを合成する段階と、(ii)イオン交換法によりリチウム挿入/ナトリウム脱離する段階と、を含むことを特徴とする。
【発明の効果】
【0016】
本発明によれば、イオン交換法を用いて化学的にリチウムを挿入してリチウムが拡散可能なサイトを確保することで、リチウムを含んでいない同じ大きさの正極素材Na2MnPO4Fと比較して優れた充電/放電特性が得られる。したがって、電気化学特性に優れたリチウムを含むマンガンフッ化リン酸塩を正極材料として提供できる。
【0017】
本発明の正極材料を2次電池用正極に適用する場合、同じ大きさの1次粒子を有するNa2MnPOF4と比較して最大4倍以上の容量が得られる。
【図面の簡単な説明】
【0018】
【図1】MnO4F2が8面体、PO4が4面体を形成して骨格構造をなし、リチウムとナトリウムが挿入脱離可能なチャネルが存在するLiXNa2−XMnPO4Fの結晶構造を示す図。
【図2】本発明の実施例3により製造された正極材料の、(a)イオン交換前、(b)イオン交換後を示す電子顕微鏡イメージ。
【図3】本発明の比較例1により製造された正極材料の室温における充電/放電曲線のグラフ。
【図4】本発明の実施例1により製造された正極材料の室温における充電/放電曲線のグラフ。
【図5】実施例1、実施例2、実施例3、及び比較例1により製造された正極材料の室温における、リチウムの挿入量に応じた放電曲線の変化を示すグラフ。
【発明を実施するための形態】
【0019】
本発明の一実施形態によれば、本発明は、下記一般式(1)で表されるマンガン系フッ化リン酸塩化合物を含むリチウム2次電池用正極材料を提供する。
[化1]
LiXNa2−XMnPO4F (1)
【0020】
本発明の好ましい実施例によれば、前記化学式を含む2次電池用正極材料は1次粒子の大きさが300nm以下であり、導電性を向上させるためにカーボンをコーティングし、3.7V〜4.0Vで放電による電位平坦面を示す。
【0021】
本発明の他の実施形態によれば、本発明は、(i)ナトリウム(Na)酸化物またはその前駆体、マンガン(Mn)酸化物またはその前駆体、リン(P)酸化物またはその前駆体、フッ化物(F)またはその前駆体をボールミルを用いて均一に混合して前処理した後、焼成することによりNa2MnPO4Fを合成する段階と、(ii)前記(i)段階で合成された正極材料にイオン交換法を用いてリチウムを挿入してLiXNa2−XMnPO4Fを合成する段階と、を含むことを特徴とするリチウム2次電池用正極材料の製造方法を提供する。
【0022】
本発明の好ましい実施例によれば、前記段階(i)は、前記ボールミルを用いて6時間均一に混合した混合物を300℃で2時間空気雰囲気で前処理する。
【0023】
本発明の好ましい実施例によれば、前記段階(ii)は、前記段階(i)から得られた前記正極材料にイオン交換法を用いてリチウム挿入/ナトリウム脱離によりリチウムイオンを正極材料内に挿入する過程を含む。
【0024】
本発明の好ましい実施例によれば、前記段階(ii)は、前記段階(i)により合成した前記正極材料に化学的にナトリウムを脱離した後、化学的にリチウムを挿入する過程を含む。
【0025】
本発明の好ましい実施例によれば、前記段階(ii)から得られた正極材料とカーボン導電材を60:40〜90:10の比率で均一に混合した後、ボールミルする過程でカーボン導電材を正極表面に均一にコーティングして電気伝導度を高める。
【0026】
本発明の好ましい実施例によれば、前記ナトリウム酸化物の前駆体は、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物から選択された何れか1つである。
【0027】
本発明の好ましい実施例によれば、前記マンガン酸化物の前駆体は、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物から選択された何れか1つである。
【0028】
本発明の好ましい実施例によれば、前記イン酸化物の前駆体は、リン酸アンモニウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物から選択された何れか1つである。
【0029】
本発明の好ましい実施例によれば、前記イオン交換法を用いてリチウムを挿入する場合、イオン交換を誘発する物質としてLiBrまたはLiIを用いる。
【0030】
本発明の好ましい実施例によれば、前記カーボン導電材は、クエン酸(Citric Acid)、スクロース(Sucrose)、スーパーP(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンである。
【0031】
以下、本発明について添付図面を参照して詳細に説明する。
本発明は、下記の一般式(1)で表される化合物を含む2次電池用正極材料を提供する。
[化1]
LiXNa2−XMnPO4F (1)
前記一般式(1)でxの範囲は、0<x<2である。
【0032】
特に、本発明の正極材料は、リチウムとナトリウムを同時に含んでおり、3.7V〜4.0Vで放電による電位平坦面を示し、導電性を向上させるためにカーボンによりコーティングされる。
【0033】
ここで、本発明による2次電池用正極材料の製造方法を説明すれば次の通りであり、具体的な製造方法は下記の実施例から容易に理解できる。
本発明の正極材料は、ナトリウム酸化物またはその前駆体、マンガン酸化物またはその前駆体、リン酸化物またはその前駆体、フッ化物またはその前駆体をボールミル(Ball mill)を用いて均一に混合して前処理段階が行われ、このように前処理段階から得られた混合物を焼成する熱処理段階により2次電池用正極材料Na2MnPO4Fが製造される。
【0034】
この時、製造されたNa2MnPO4Fは粒子の大きさが1μm以下で、300nmの平均粒子の大きさを有する。
【0035】
このように製造されたNa2MnPO4Fは、LiBrが溶解されたアセトニトリル溶液に投入してArガスを流しながら温度を上昇させてリチウムとナトリウムのイオン交換を起こす。イオン交換の結果物を洗浄及び乾燥する過程を経てマンガンフッ化リン酸塩LiXNa2−XMnPO4Fの正極材料が得られる。
【0036】
マンガンフッ化リン酸化物の低電気伝導度の問題を解決するために、得られたLiXNa2−XMnPO4Fの正極材にカーボンコーティングを施した。
【0037】
前記ナトリウム酸化物の前駆体は特に制限されることはないが、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物である。
【0038】
前記マンガン酸化物の前駆体は特に制限されることはないが、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物である。
【0039】
前記イン酸化物の前駆体は特に制限されることはないが、リン酸リチウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物である。
【0040】
前記フッ素の前駆体は特に制限されることはないが、金属フッ化物、フッ化物、またはこれらの混合物である。
【0041】
前記イオン交換に用いられるリチウムソースはLiBrに特に制限されることはなく、イオン交換を誘発するリチウム混合物である。
【0042】
前記イオン交換に用いられる溶媒はアセトニトリルに特に制限されることはなく、イオン交換を提供する溶媒である。
【0043】
前記カーボン導電材は特に制限されることはないが、クエン酸(Citric Acid)、シュクロス(Sucrose)、スーパーP(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンからなる物質が使用される。
【0044】
このように製造される本発明の正極材料はリチウム2次電池の製造に使用されるが、正極材料を異なる方式で適用したことを除き、既存のリチウム2次電池の製造方式と同一であり、その構成及び製造方法を簡略に説明すると次の通りである。
【0045】
先ず、本発明の正極材料を用いた正極極板の製作工程を説明すると、必要に応じて導電材、結着剤、フィラー、分散剤、イオン導電剤、圧力増強剤など、通常用いられる1種または2種以上の添加成分を添加し、適当な溶媒(有機溶媒)によりスラリーやペースト化し、得られたスラリーまたはペーストを電極支持基板にドクターブレード法などを用いて塗布した後、乾燥過程を経て圧延ロールなどでプレス(pressing)して最終的な正極極板を製造する。
【0046】
この時、前記導電材としては、黒鉛、カーボンブラック、アセチレンブラック、ケッチェンブラック(Ketchen Black)、炭素繊維、金属粉などがある。結着剤としては、PVdF、ポリエチレンなどが用いられ、電極支持基板(集電体)は、銅、ニッケル、ステンレス鋼鉄、アルミニウムなどの箔、シート、あるいは炭素繊維などで構成できる。
【0047】
このように製造された正極極板を用いてリチウム2次電池を製作するが、リチウム2次電池の形態は、コイン、ボタン、シート、円筒形、角形など何れも良く、リチウム2次電池の負極、電解質、分離膜などは従来のリチウム2次電池のものを使用する。
【0048】
また、前記負極活物質はリチウムを含んでいない黒鉛系材料を用いてもよい。勿論、リチウムを含む遷移金属の複合酸化物などの1種あるいは2種以上を用いてもよい。その他、シリコン、スズなども負極活物質として用いてもよい。
【0049】
また、前記電解液は、有機溶媒にリチウム塩を溶解させた非水系電解液、無機固体電解質、無機固体電解質の複合材などの何れもよく、非水系電解液の溶媒としてはエチレンカーボネート、プロピレンカーボネート、ジメチルカーボネート、ジエチルカーボネート、メチルエチルカーボネートなどのエステル類、ブチルラクトンなどのラクトン類、1,2−ジメトキシエタン、エトキシメトキシエタンなどのエーテル類、アセッツニトリルなどのニトリル類などの1種あるいは2種以上を使用でき、非水系電解液のリチウム塩の例としてはLiAsF6、LiBF4、LiPF6などを使用できる。
【0050】
また、前記分離膜としてはPP及び/またはPEなどのポリオレフィン(Polyolefin)から製造される多孔性フィルムや不織布などの多孔性材を使用できる。
以下、本発明を具体的な実施例を挙げて詳細に説明するが、本発明の権利範囲がこれら実施例に限定されることはない。
【0051】
実施例1
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0052】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0053】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0054】
実施例2
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0055】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを1.0MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0056】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0057】
実施例3
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0058】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを2.5MのLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0059】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0060】
比較例1
実施例1と同じ条件により得られたNa2MnPO4Fをイオン交換過程を経ることなく、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0061】
比較例2〜4
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0062】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、500℃、10時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例2)、1.0M(比較例3)、2.5M(比較例4)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0063】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0064】
比較例5〜7
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0065】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、550℃、3時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例5)、1.0M(比較例6)、2.5M(比較例7)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0066】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0067】
比較例8〜10
定量の炭酸ナトリウム(Na2HCO3)、シュウ酸マンガン二水和物(MnC2O4・2H2O)、フッ化ナトリウム(NaF)、炭酸水素ナトリウム(NaHCO3)、リン酸アンモニウム(NH4H2PO4)を総量10g基準に投入して6時間ボールミル(ball mill)して均一に混合した。
【0068】
得られた混合物を300℃で2時間空気雰囲気で前処理した後、550℃、6時間、アルゴンガスの雰囲気で焼成し、このように製造されたNa2MnPO4Fを0.6M(比較例8)、1.0M(比較例9)、2.5M(比較例10)のLiBrが溶解されたアセトニトリルに沈殿させた後、アルゴンガスを流しながら反応させた。この時、反応温度は80℃であった。
【0069】
イオン交換済みの試料は、無水エタノールで洗浄する過程を介して残存NaBrを除去した後、乾燥させ、Super−Pと75:25の比率でボールミルを用いて均一に混合して正極材料複合体を製造した。
【0070】
実験例1:電極性能の評価
実施例1〜3と比較例1〜10により製造された正極材料の1次粒子の大きさと正極材料の金属組成分析をICP発光分光分析により測定し、下記表1に示した。
【0071】
【表1】

【0072】
粒子の大きさが減少するにつれて、同一のLiBrの濃度に対応してイオン交換によりLiXNa2−XMnPO4Fに挿入されるリチウムの量が増加することが確認できた。特に、1次粒子の大きさが700nm〜400nmである場合は、粒子の大きさの減少により挿入されるリチウムの量が少し増加したが、300nmで挿入されるリチウムの量が大きく増加することが確認できた。
【0073】
これは化学的な方法によるリチウムの挿入は1次粒子の大きさに大きく依存することを意味する。したがって、Na2MnPO4Fに、イオン交換などの化学的な方法によりリチウムを挿入させるためには、粒子の大きさの制御が重要であることが分かる。化学的方法による効果的なリチウムの挿入に求められる1次粒子の大きさは300nm以下である。したがって、出発物質のボールミリング条件及び熱処理条件が重要であることが分かる。
【0074】
本発明の粒子の大きさを制御することは、このようなボールミリング及び熱処理条件を調節することによりなされ、これは実験装備の条件に応じて多少変更することもある。重要な点は、1粒子の大きさが一定の大きさ以下に制御されることにより、化学的なリチウムの挿入が可能になり、結果的にリチウムとナトリウムを同時に含んだLiXNa2−XMnPO4Fが製造される。
【0075】
実施例1〜3と比較例1〜10の正極材料複合体の粉末を用いて正極材料複合体95wt%、結着剤PVdF 5wt%を混合し、N−メチルピロリドン(NMP)を溶媒としてスラリーを製造した。
【0076】
このスラリーを厚さ20μmのアルミニウム箔(Al foil)に塗布して乾燥した後、プレスで圧密化して真空上で120℃で16時間乾燥することにより、直径16mmのディスク電極を製造した。
【0077】
対極としては直径16mmにパンチングしたリチウム金属箔を、分離膜としてはポリプロピレン(PP)フィルムを使用し、電解液としては1MのLiPF6のエチレンカーボネート/ジメトキシエタン(EC/DME)1:1v/vの混合溶液を使用し、電解液を分離膜に含浸させた後、この分離膜を作用極と対極との間に入れた後、SUS製品のケースを電極評価用試験セルにして電池の電極性能を評価し、放電容量を含んだ測定結果を下記表2に記載した。
【0078】
【表2】

【0079】
図2は実施例3のイオン交換処理前後の試料の表面を電子顕微鏡イメージで示す図面であり、イオン交換後の試料の表面がナトリウムの脱離及びリチウムの挿入により荒くなったことを観測した。
【0080】
イオン交換による充電/放電特性の変化を実施例1と比較例1から確認した(図3及び図4)。イオン交換を施さなかったNa2MnPO4Fは55mAhg−1の放電容量を示し、これと比較してイオン交換を施してリチウムが0.3挿入されたLi0.3Na1.7Mn2PO4Fは140mAhg−1という2.5倍程度高い放電容量を示すことを確認した。
【0081】
0.3のリチウムが挿入されるだけで、純粋ナトリウムのみ含むNa2MnPO4Fと比較して高い放電容量が得られるため、リチウムの挿入がマンガン系フッ化リン酸化物の容量増加に大きい影響を及ぼすことが分かる。
【0082】
また、図5に示すように、リチウムの挿入量が0.3から1.9まで増加するにつれて(実施例1〜3)放電容量が140mAhg−1から197mAhg−1に増加することが確認できた。以上の結果から判断すると、マンガン系フッ化リン酸化物にリチウムを挿入することにより、顕著な容量増加の効果が得られ、これは挿入されたリチウムがリチウム拡散に起因する通路(pathway)を確保することにより、充電/放電によるリチウムの挿入/脱離、あるいはナトリウムの挿入/脱離に肯定的な効果を与えると判断される。
【産業上の利用可能性】
【0083】
本発明は、リチウムあるいはナトリウムを含むマンガンフッ化リン酸化物を電極材料として使用できる2次電池用正極材料及びこの製造方法の分野に適用できる。
【特許請求の範囲】
【請求項1】
下記一般式(1)で表されるマンガン系フッ化リン酸塩化合物を含むリチウム2次電池用正極材料。
[化1]
LiXNa2−XMnPO4F (1)
【請求項2】
前記一般式(1)を含む2次電池用正極材料は、1次粒子の大きさが300nm以下であり、導電性を向上させるためにカーボンをコーティングし、3.7V〜4.0Vで放電による電位平坦面を示すことを特徴とする請求項1に記載のリチウム2次電池用正極材料。
【請求項3】
(i)ナトリウム(Na)酸化物またはその前駆体、マンガン(Mn)酸化物またはその前駆体、リン(P)酸化物またはその前駆体、フッ化物(F)またはその前駆体をボールミルを用いて均一に混合して前処理した後、焼成することによりNa2MnPO4Fを合成する段階と、
(ii)前記(i)段階で合成された正極材料にイオン交換法を用いてリチウムを挿入してLiXNa2−XMnPO4Fを合成する段階と、
を含むことを特徴とするリチウム2次電池用正極材料の製造方法。
【請求項4】
前記段階(i)は、
前記ボールミルを用いて6時間均一に混合した混合物を300℃で2時間空気雰囲気で前処理することを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項5】
前記段階(ii)は、
前記段階(i)から得られた前記正極材料にイオン交換法を用いてリチウム挿入/ナトリウム脱離によりリチウムイオンを正極材料内に挿入する過程を含むことを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項6】
前記段階(ii)は、
前記段階(i)により合成した前記正極材料に化学的にナトリウムを脱離した後、化学的にリチウムを挿入する過程を含むことを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項7】
前記段階(ii)から得られた正極材料とカーボン導電材を60:40〜90:10の比率で均一に混合し、ボールミルする過程によりカーボン導電材を正極表面に均一にコーティングして電気伝導度を高めることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項8】
前記ナトリウム酸化物の前駆体は、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項9】
前記マンガン酸化物の前駆体は、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項10】
前記イン酸化物の前駆体は、リン酸アンモニウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項11】
前記イオン交換法を用いてリチウムを挿入する場合、イオン交換を誘発する物質としてLiBrまたはLiIを用いることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項12】
前記イオン交換法に用いられる物質のLiBrまたはLiIは、その濃度が0.5M以上でイオン交換することを特徴とする請求項11に記載のリチウム2次電池用正極材料の製造方法。
【請求項13】
前記カーボン導電材は、クエン酸(Citric Acid)、スクロース(Sucrose)、スーパー−P(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンであることを特徴とする請求項7に記載のリチウム2次電池用正極材料の製造方法。
【請求項1】
下記一般式(1)で表されるマンガン系フッ化リン酸塩化合物を含むリチウム2次電池用正極材料。
[化1]
LiXNa2−XMnPO4F (1)
【請求項2】
前記一般式(1)を含む2次電池用正極材料は、1次粒子の大きさが300nm以下であり、導電性を向上させるためにカーボンをコーティングし、3.7V〜4.0Vで放電による電位平坦面を示すことを特徴とする請求項1に記載のリチウム2次電池用正極材料。
【請求項3】
(i)ナトリウム(Na)酸化物またはその前駆体、マンガン(Mn)酸化物またはその前駆体、リン(P)酸化物またはその前駆体、フッ化物(F)またはその前駆体をボールミルを用いて均一に混合して前処理した後、焼成することによりNa2MnPO4Fを合成する段階と、
(ii)前記(i)段階で合成された正極材料にイオン交換法を用いてリチウムを挿入してLiXNa2−XMnPO4Fを合成する段階と、
を含むことを特徴とするリチウム2次電池用正極材料の製造方法。
【請求項4】
前記段階(i)は、
前記ボールミルを用いて6時間均一に混合した混合物を300℃で2時間空気雰囲気で前処理することを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項5】
前記段階(ii)は、
前記段階(i)から得られた前記正極材料にイオン交換法を用いてリチウム挿入/ナトリウム脱離によりリチウムイオンを正極材料内に挿入する過程を含むことを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項6】
前記段階(ii)は、
前記段階(i)により合成した前記正極材料に化学的にナトリウムを脱離した後、化学的にリチウムを挿入する過程を含むことを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項7】
前記段階(ii)から得られた正極材料とカーボン導電材を60:40〜90:10の比率で均一に混合し、ボールミルする過程によりカーボン導電材を正極表面に均一にコーティングして電気伝導度を高めることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項8】
前記ナトリウム酸化物の前駆体は、リン酸ナトリウム、炭酸ナトリウム、水酸化ナトリウム、酢酸ナトリウム、硫酸ナトリウム、亜硫酸ナトリウム、フッ化ナトリウム、塩化ナトリウム、臭化ナトリウム、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項9】
前記マンガン酸化物の前駆体は、マンガン金属、酸化マンガン、シュウ酸マンガン、酢酸マンガン、硝酸塩マンガン、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項10】
前記イン酸化物の前駆体は、リン酸アンモニウム、リン酸ナトリウム、リン酸カリウム、またはこれらの混合物から選択された何れか1つであることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項11】
前記イオン交換法を用いてリチウムを挿入する場合、イオン交換を誘発する物質としてLiBrまたはLiIを用いることを特徴とする請求項3に記載のリチウム2次電池用正極材料の製造方法。
【請求項12】
前記イオン交換法に用いられる物質のLiBrまたはLiIは、その濃度が0.5M以上でイオン交換することを特徴とする請求項11に記載のリチウム2次電池用正極材料の製造方法。
【請求項13】
前記カーボン導電材は、クエン酸(Citric Acid)、スクロース(Sucrose)、スーパー−P(Super−P)、アセチレンブラック、ケッチェンブラック(Ketchen Black)、またはカーボンであることを特徴とする請求項7に記載のリチウム2次電池用正極材料の製造方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2013−73931(P2013−73931A)
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願番号】特願2011−272492(P2011−272492)
【出願日】平成23年12月13日(2011.12.13)
【出願人】(591251636)現代自動車株式会社 (1,064)
【出願人】(599028364)電子部品研究院 (28)
【氏名又は名称原語表記】KOREA ELECTRONICS TECHNOLOGY INSTITUTE
【住所又は居所原語表記】68 Yatap−dong, Bundang−gu, Seongnam−si, Gyeonggi−do 463−816, Republic of Korea
【Fターム(参考)】
【公開日】平成25年4月22日(2013.4.22)
【国際特許分類】
【出願日】平成23年12月13日(2011.12.13)
【出願人】(591251636)現代自動車株式会社 (1,064)
【出願人】(599028364)電子部品研究院 (28)
【氏名又は名称原語表記】KOREA ELECTRONICS TECHNOLOGY INSTITUTE
【住所又は居所原語表記】68 Yatap−dong, Bundang−gu, Seongnam−si, Gyeonggi−do 463−816, Republic of Korea
【Fターム(参考)】
[ Back to top ]

