D−プシコース結晶を製造する方法
【課題】本発明は、D−プシコース結晶を製造する方法を提供することを目的とする。
【解決手段】本発明は、過飽和を利用することによってD−プシコース溶液からD−プシコース結晶を製造する方法に関する。
【解決手段】本発明は、過飽和を利用することによってD−プシコース溶液からD−プシコース結晶を製造する方法に関する。
【発明の詳細な説明】
【技術分野】
【0001】
本出願は、2010年3月26日に韓国特許庁に出願された大韓民国特許出願第10-2010-0027546号の恩典を主張し、その開示はその全体が参照により本明細書に組み入れられる。
【0002】
本発明は、過飽和を利用することによってD−プシコース溶液からD−プシコース結晶を製造する方法に関する。
【背景技術】
【0003】
D−プシコースは、糖蜜やブドウ糖の異性化反応中に極少量存在する天然糖であり、砂糖に比べて約70%の甘味を有する単糖類である。D−プシコースは、ヒトでは代謝されず、カロリーが実質的になく、体脂肪の形成を抑制することから、体重増加に影響が小さい甘味料であると報告されている(非特許文献1及び2)。
【0004】
最近になって、非齲蝕(non-carious)機能及び抗齲蝕(anti-carious)機能に対するD−プシコースの効果が発表され、したがってD−プシコースの、歯の健康の一助となる材料としての、及び砂糖を代替することができる甘味料としての開発が活発になされている。
【0005】
D−プシコースは、その特性及び機能性によって、体重増加を防ぐ甘味料として食品産業分野で関心を集めているが、高温でフルクトースから製造されるD−プシコースの量はわずかであり、したがって化学合成によりD−プシコースを製造することは困難である。フルクトースとD−タガトースエピメラーゼとを反応させる、またはフルクトースとD−プシコースエピメラーゼを反応させることにより大量生産する方法が報告されたが、D−プシコースの収率が非常に低いことから製造コストは高くなる。
【0006】
最近、本発明者らは、ブドウ糖をフルクトースに異性化させた後にフルクトースとD−プシコースエピメラーゼを生産する固定化細胞とを反応させることにより、D−プシコースを経済的に生産する方法を報告した(特許文献1)。
【0007】
酵素反応によって生産されたD−プシコースを含む反応液は、約20重量%〜約30重量%の量の固形のD−プシコースを含む低純度産物であるために、高純度にD−プシコースを分離することが要求される。高純度に分離するために多様な方法が産業的に生産される材料に適用されている。糖の場合、通常クロマトグラフィを使用して高純度液を作り、その後、結晶化させて高純度糖産物を得る。D−プシコースの場合、産業的に適用可能な製造方法はまだ開発されていない。
【0008】
D−プシコースの反応液中の未反応フルクトースを酵母で発酵させて除去する、及び大量のエタノールを使用することによって、粉末形態のD−プシコースを製造する方法が報告されている(非特許文献3)。しかし、大量のエタノール使用は、防爆及び産物回収のための高価な設備を必要とし、有機溶媒の使用による撹拌器の故障、及び回収産物中の異物の存在などの問題点が発生しうる。また、最終産物が微粉状であるために、脱水、洗浄、及び乾燥過程において多くが失われる。最終産物製造のためにD−プシコースを粉末化するあいだ粉末は互いに吸着し、これは粉末粒子中に不純物をもたらし、その結果最終産物の純度が低くなる。微粉状の産物は、重さの増加に比べて体積の増加が大きくなり、これは過大包装による製造コストの上昇、及び流通上の追加費用の発生をもたらす。さらに、このような精密化学製品は、流動性が低いことから食品製造工程において不利である。従って、エタノールなどの有機溶媒を使用することなく経済的にD−プシコースを製造し、かつ製造工程中の流動性及び生産物価値を改善するために、微粉状ではない結晶状の純粋なD−プシコースを製造する方法が依然として必要とされている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】大韓民国特許出願第10−2009−0118465号
【非特許文献】
【0010】
【非特許文献1】Matuo,T.et al.,Asia Pac.J.Clin.Nutr.,10,233-237,2001
【非特許文献2】Matsuo,T.and K.Izumori,Asia Pac.J.Clin.Nutr.,13,S127,2004
【非特許文献3】Kei T.et al.,J.Biosci.Bioeng.,90(4),453-455,2000
【発明の概要】
【発明が解決しようとする課題】
【0011】
本発明の目的は、D−プシコース結晶を製造する方法を提供することである。
【課題を解決するための手段】
【0012】
このために、本発明者らは、生物学的変換や酵素反応によって得られたD−プシコース溶液から有機溶媒を使用せずにD−プシコース結晶を製造する方法に関する研究を行った。この方法において、該D−プシコース結晶は、D−プシコース溶液を準安定域(metastable zone)の過飽和状態に維持することによって適切なサイズに製造され、これにより本発明は完成した。
【0013】
本発明は、D−プシコース溶液を、飽和曲線と過飽和曲線との間にある準安定域に維持することによってD−プシコース結晶を製造する方法を提供する。
【0014】
より具体的には、本発明は以下の通りである。
本発明(1)は、
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域(metastable zone)の過飽和状態で結晶化させる段階と
を含む、D−プシコース結晶を製造する方法である。
本発明(2)は、
前記精製されたD−プシコース溶液を得る段階が、
前記D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含む、
本発明(1)の方法である。
本発明(3)は、前記精製されたD−プシコース溶液を濃縮させる段階が、約60℃〜約70℃の温度で行われる、本発明(1)の方法である 。
本発明(4)は、前記結晶化させる段階で使用される前記濃縮されたD−プシコース溶液に、D−プシコース種晶が、前記濃縮されたD−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加される、本発明(1)の方法である。
本発明(5)は、前記結晶化させる段階で使用される濃縮されたD−プシコース溶液が、約70%(g/g)以上のD−プシコース溶液である、本発明(1)の方法である。
本発明(6)は、前記結晶化させる段階における結晶化の進行をモニタリングし、D−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に溶液の温度を低くすることによって、前記濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、本発明(1)の方法である。
本発明(7)は、前記結晶化させる段階における結晶化の進行をモニタリングし、前記溶液中のD−プシコースが過飽和レベル以上に濃縮された場合に前記濃縮されたD−プシコース溶液より低い濃度のD−プシコース溶液を添加することによって、該濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、本発明(1)の方法である。
本発明(8)は、前記結晶化させる段階における準安定域の過飽和状態が、飽和濃度から、該飽和濃度からさらに約6%(g/g溶液)高い濃度までの範囲に存在する、本発明(1)の方法である。
【発明の効果】
【0015】
本発明の態様による製造方法を利用して、D−プシコース溶液から、有機溶媒を使用しない経済的な結晶化工程を通して、純粋であって、かつ産業的適用に適した形態のD−プシコース結晶を製造できる。
【図面の簡単な説明】
【0016】
上記および他の本発明の特徴および利点は、添付の図面への参照と共にその例示的態様を詳細に説明することにより、より明らかになるであろう。
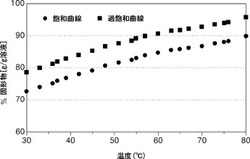
【図1】温度に関連した、純粋なD−プシコースの飽和曲線と過飽和曲線とを示すグラフである。
【図2】温度に関連した、80%(g/g溶液)濃度でのD−プシコースの残存量を示すグラフである。
【図3】顕微鏡で観察した、生成されたD−プシコース種晶を示す写真である。
【図4】顕微鏡使用して撮影された、本発明の例示的態様による温度調節によって生成されたD−プシコース結晶を示す写真である。
【図5】顕微鏡使用して撮影された、本発明の例示的態様による減圧濃縮によって生成されたD−プシコース結晶を示すイメージである。
【発明を実施するための形態】
【0017】
本発明の詳細な説明
本発明のある局面に従い、
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を収得する段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階と
を含む、精製されたD−プシコース結晶を製造する方法が提供される。
【0018】
本明細書で使われている「過飽和状態」とは、溶質が溶媒の溶解能を超えて溶解されている不安定な状態であり、溶質が固体に結晶化しうる状態を意味する。従って、結晶化によって溶液から溶質を分離するためには、溶液において過飽和状態に達することが必要である。一般的に、溶液の過飽和状態は、外部条件、不純物、温度、濃度、pHなどによって影響を受けうる。
【0019】
本明細書で使われている「準安定域」の過飽和状態は、溶液の濃度が平衡濃度、すなわち飽和濃度から、結晶が自発的に析出する最低過飽和濃度までの範囲を意味する。この範囲の濃度では結晶核形成(crystal nucleation)などの結晶化は起こらない。しかしながら、この範囲の濃度の溶液に外部から結晶を入れれば、溶液中の溶質の量が過飽和濃度であるので、自発的に結晶成長が起こって結晶サイズが大きくなる。すなわち、結晶を生成するために、飽和濃度以上である溶液に種晶(seed)が投入されれば、準安定域で種晶が成長して結晶を形成する。結晶化用溶液が過度に濃縮あるいは急激に冷却されると準安定域を超える過飽和状態に達し、従って結晶の成長ではなく結晶核形成が起こり、複数の微細結晶が形成される。従って、適切なサイズの結晶を得るために、結晶化用溶液を、準安定域の過飽和状態に維持させながら適切な速度で結晶化を行わなければならない。
【0020】
本発明のある態様において、出発物質であるD−プシコース溶液は、D−プシコースエピメラーゼを発現するコリネバクテリウム属由来の細菌、またはそれから単離されたD−プシコースエピメラーゼによって調製される。
【0021】
本発明のある態様において、D−プシコース溶液は、大韓民国特許出願第2009−0118465号に記載されているように、コリネバクテリウムグルタミクム(Corynebacterium glutamicum)KCTC13032を培養して得られた細胞またはそれから単離された酵素を固定化担体に固定化させること、および該固定化された細胞または酵素にフルクトースを基質として供給することにより、得られうる。
【0022】
D−プシコース溶液からD−プシコース結晶を得るために、D−プシコースの精製及び結晶化に影響を及ぼしうる他の物質を除去し、効率的な結晶化のために必要な状態を形成しなければならない。
【0023】
従って、本発明によるD−プシコース結晶を製造する方法は、D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階を含みうる。
【0024】
本発明のある態様において、前記精製されたD−プシコース溶液を得る段階は、
D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含みうる。
【0025】
本発明のある態様において、前記D−プシコース溶液を脱塩させる段階は、溶液が陽イオン交換樹脂が充填されたカラム、陰イオン交換樹脂が充填されたカラム、及び陽イオン交換樹脂と陰イオン交換樹脂との混合物が充填されたカラムを通過するクロマトグラフィによって遂行されうる。
【0026】
高純度のD−プシコースを得るために、一般的にクロマトグラフィによる分離が利用される。D−プシコース結晶を得るために、D−プシコース溶液中でのD−プシコースの量は、約70%〜約85%またはそれ以上でなければならない。従って、D−プシコースエピメラーゼ反応によって調製されたD−プシコース溶液中でのD−プシコースの純度は約22%でありこれは直接結晶化を行うには低すぎることから、結晶化段階前にD−プシコースを精製し、所望のレベルまで濃縮しなければならない。高純度のD−プシコース結晶を得るために、結晶化段階前に、溶液を脱色及び脱塩することによって不純物を除去してもよく、及び、クロマトグラフィ、例えば、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムでのクロマトグラフィによって、D−プシコースを精製してもよい。
【0027】
本発明によるD−プシコース結晶を製造する方法は、精製されたD−プシコース溶液を濃縮させる段階を含みうる。
【0028】
本発明のある態様において、前記精製されたD−プシコース溶液を濃縮させる段階は、約60℃〜約70℃で行われうる。濃縮液の温度が約70℃より高く上昇すると、D−プシコースの熱変性が起こることがある。温度が約60℃未満に下がると、溶液を所望レベルに濃縮することは困難である。濃縮が進むにつれて蒸発熱によって反応物の温度が急上昇するので、溶液の濃縮は、温度を約70℃以下に維持しながら速かに行わなければならない。
【0029】
本発明のある態様において、D−プシコース溶液の濃縮は、約65℃以下で行われうる。
【0030】
本発明によるD−プシコース結晶を製造する方法は、濃縮されたD−プシコース溶液の温度及び濃度を調節することによって、該溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階を含みうる。
【0031】
本発明のある態様において、結晶化段階で使用される濃縮されたD−プシコース溶液は、約70%〜約85%(g/g)またはそれ以上のD−プシコース溶液でありうる。
【0032】
本発明のある態様において、結晶化段階で使用される濃縮されたD−プシコース溶液に、D−プシコース種晶が、該D−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加されうる。
【0033】
本発明において、D−プシコース結晶は、D−プシコースが溶液中で溶媒と平衡状態をなす平衡濃度以上でD−プシコースが存在することから自発的に結晶成長が起こる準安定域の過飽和状態にD−プシコース溶液を維持することによって製造される。本発明において、結晶化に必要とされる過飽和状態は、D−プシコース溶液の温度を低くするか、またはD−プシコース溶液中のD−プシコースの濃度を変化させることによって維持されうる。
【0034】
本発明のある態様において、所定の間隔で試料を採取して該試料を肉眼もしくは顕微鏡を使用して観察すること、または試料の遠心分離から得られた上層中の糖濃度を分析することによって、結晶化段階における結晶化の進行をモニタリングしてもよい。その結果によって、温度またはD−プシコースの濃度を調節することができる。
【0035】
本発明のある態様において、D−プシコース種晶をD−プシコース溶液に添加した後、溶液中でのD−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に温度を低くすることによって、結晶化段階におけるD−プシコース溶液の準安定域の過飽和状態を維持してもよい。
【0036】
本発明のある態様において、D−プシコース溶液へのD−プシコース種晶の添加、および溶液の穏やかな撹拌、例えば約10rpmで撹拌しながらの結晶成長の後、D−プシコースが過飽和レベル以上に濃縮された場合に前記D−プシコース溶液よりも低濃度のD−プシコース溶液を添加することによって、結晶化段階におけるD−プシコース溶液の準安定域の過飽和状態を維持してもよい。
【0037】
本発明のある態様において、結晶化段階においてD−プシコース溶液を準安定域の過飽和状態に維持させるために添加されるD−プシコース溶液は、過飽和レベル以上に濃縮されたD−プシコース溶液よりも低濃度のD−プシコースを含む。例えば、添加されるD−プシコース溶液は約60%〜約70%のD−プシコース溶液でありうる。
【0038】
本発明のある態様において、結晶化段階における過飽和状態は、飽和濃度と該飽和濃度からさらに約6%(g/g溶液)高い濃度との間の範囲に存在しうる。
【0039】
過飽和濃度は、物質に固有の特性であり、飽和した溶液を冷却または濃縮することにより得られる。溶液の温度が溶液の飽和に達する温度から徐々に下がった場合に、高度に濃縮した溶液が不安定な状態に達して微細結晶が形成され始める濃度及び温度として、過飽和濃度及び過飽和温度をそれぞれ定義することができる。過飽和濃度の溶液に脱イオン水を添加し、該溶液を再加熱して微結晶を速やかに溶解させ、希釈された濃度で溶液の温度を飽和温度に調節し、この溶液を再度冷やすことにより、微結晶が生成される過飽和濃度を特定することができる。様々な飽和濃度で、物質の溶液の希釈、加熱、及び再冷却を繰り返すことによって、該物質の準安定域を特定することができる。D−プシコースも固有の準安定域の濃度範囲を有し、この範囲は飽和濃度またはそれ以上から該飽和濃度より約6%高いものまでであることが確認された。D−プシコースの準安定域にD−プシコース溶液を維持しながら結晶化を行って、形状が安定しておりかつサイズが大きい結晶を得ることができる。
【0040】
本発明のある態様において、本発明によるD−プシコース結晶を製造する方法は、
結晶化段階で得られたD−プシコース結晶を遠心分離によって回収する段階と、
前記結晶を脱イオン水で洗浄する段階と、
前記結晶を乾燥させる段階と
をさらに含むことができる。
【0041】
結晶の乾燥は、流動床乾燥器または真空乾燥器で行われうる。
【0042】
本発明のある態様において、前記精製されたD−プシコース結晶は、約0.1mm〜約0.2mmのサイズを有する。
【0043】
本発明のある態様において、精製されたD−プシコース結晶は、
酵素反応などによって生成されたD−プシコース溶液を約40%(g/g溶液)の濃度に濃縮し、得られた溶液を、粒状活性炭(GAC:granulated active carbon)脱色剤が充填されたカラムに、1時間当たり約4mの線速度で通して脱色する段階と、
脱色されたD−プシコース溶液を、陽イオン交換樹脂、陰イオン交換樹脂、及び陽イオン交換樹脂と陰イオン交換樹脂との混合物がそれぞれ充填されたカラムに、約40℃で、時間当りイオン交換樹脂体積の2倍の速度で注入して、脱色されたD−プシコース溶液を脱塩させる段階と、
脱色及び脱塩によって精製されたD−プシコース溶液を約60%(g/g溶液)の濃度に濃縮し、この溶液をカルシウム活性基が付着したイオン交換樹脂で充填された分離カラムに通過させて、フルクトースからプシコースを分離する段階と、
分離されたD−プシコース溶液を、約70℃以下で、濃縮器において、約85%(g/g)以上の濃度まで濃縮する段階と、
濃縮されたD−プシコース溶液に、D−プシコース種晶を、濃縮されたD−プシコース溶液に溶解されたD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で注入し、温度及び濃度を調節して、溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階と、
D−プシコース結晶を、結晶化に供された溶液から遠心分離によって分離し、該溶液及びD−プシコース結晶を洗浄し、結晶を流動床乾燥器または真空乾燥器において乾燥する段階と
を含む方法によって製造されうる。
【0044】
以下、本発明について、具体的な実施例を参照しながら詳細に説明する。しかしながら、それら実施例は、本発明の例示的説明を目的としたものであり、本発明の範囲は、それら実施例になんら限定されるものではない。
【実施例】
【0045】
実施例1:コリネバクテリウム属微生物を利用した低純度D−プシコース溶液の生成
大韓民国特許出願第10−2009−0118465号に開示されているように、コリネバクテリウムグルタミクムKCTC13032培養する段階、及び該微生物、またはそれから単離されたD−プシコースエピメラーゼが固定化された担体によってフルクトースをD−プシコースに転換する段階を含む、D−プシコースを連続生成する方法によって、D−プシコースを調製した。この方法によって調製されたD−プシコース溶液中のD−プシコースの量は約22%であり、それから直接結晶化させるには低すぎる濃度であった。
【0046】
実施例2:低純度D−プシコース溶液の精製
実施例1で生成されたD−プシコース溶液を約40%(g/g溶液)に濃縮した後、粒状活性炭素(granulated active carbon)が充填された脱色カラムを通して、濃縮液内の有色物質を除去した。
【0047】
実施例1で生成されたD−プシコース溶液のD−プシコース純度は、固形分含有量が約22%と非常に低く、結晶化するには適していなかった。結晶化のためには、結晶化対象物質の純度を約70%〜約90%またはそれ以上に高めねばならない。クロマトグラフィによるD−プシコースの効率的な分離のためには、D−プシコース溶液からイオンが除去されねばならない。分離対象溶液中にイオン成分が存在する場合、分離樹脂の活性基がイオン成分と置換されて樹脂の分離能が低下するので、分離樹脂を繰り返し使用することが不可能となる。従って、前記で調製された脱色されたD−プシコース溶液を、水素基で置換された陽イオン交換樹脂とヒドロキシル基で置換された陰イオン交換樹脂とが充填されたカラムに通した後、最終段階で、陽イオン交換樹脂及び陰イオン交換樹脂の混合物が充填されたイオン交換カラムに通し、前記溶液中のイオン成分を除去した。溶液中のイオン成分除去は、導電率を導電計で測定することによって確認した。精製溶液の導電率は、単位cm当たり約10マイクロジーメンス以下になるように調節した。
【0048】
実施例3:クロマトグラフィを利用した高純度D−プシコース溶液の調製
前記実施例2で脱色及び脱塩により有色物質及びイオン成分などの不純物を除去した、低純度D−プシコース溶液を、約60%(g/g溶液)まで濃縮し、その後カルシウム基で置換させたイオン交換樹脂(Purolite PCR 642K)に通過させて、精製されたD−プシコース溶液を得た。
【0049】
前記イオン交換樹脂カラム内に充填されたイオン交換樹脂の量は、約200Lであり、該カラムに通した試料、すなわち、実施例2で調製された精製されたD−プシコース溶液の量は、約20Lであり、運転温度は、約60℃であった。試料を注入し、時間当たり約260Lの脱イオン水で溶出させた後、採取した各分画において、HPLCシステム(HP、Agilent 1200シリーズ)を使用することによって、フルクトースおよびD−プシコースの濃度をそれぞれ測定した。純粋なD−プシコース分画を取り、D−プシコース及びフルクトースを含有する分画を濃縮し、分離対象試料として再度用いた。カルシウム基で置換されたカラム(Bio Rad社)をHPLC分析カラムに利用し、脱イオン水を分当たり約0.5mLの流量で適用した。
【0050】
実施例4:D−プシコース溶液の濃縮
結晶化のために必要なD−プシコース濃縮液を得るために、実施例3で精製されたD−プシコース溶液を、真空濃縮器(EYELA社、N−11)に入れて、約80%(g/g溶液)に濃縮した。濃縮された液をそれぞれチューブに分注し、それぞれ70℃,65℃、及び60℃のウォーターバス中に立てて放置した。試料を経時的に一定間隔で採取し、濃縮液のアリコートにおける残存量を測定した。その結果が図2に図示されている。濃縮液の温度が約70℃以上になると、3時間後にD−プシコースの熱変性が起こり、22時間後には、初期量に比べて約78%のみが残存することが確認された。濃縮過程中、蒸発熱によって内部の温度は約40℃以下に維持されるが、D−プシコースの量が約80%(g/g溶液)以上になると、温度は急上昇する。このような結果から、D−プシコースを約80%(g/g溶液)以上に濃縮する場合、濃縮液の内部温度を約70℃以下に迅速に低下させるか、または例えば約65℃以下で濃縮段階を遂行することが必要であるということが確認された。
【0051】
実施例5:D−プシコース種晶の生成
前記実施例3において精製分離されたD−プシコース溶液(D−プシコースを約1,000g含有)を、実施例4において説明されるように、約85%(g/g溶液)に濃縮した。純度95%の製品(Sigma社)1gを購入し、乳鉢に入れて粉砕した後、これをエタノール溶液と混合させた。二重の(double jacketed)2L反応槽を備える反応器システム(IKA(登録商標)、LR−2.ST)を晶析装置(crystallizer)として利用し、晶析装置内の濃縮液の初期温度を約50℃に調節し、調製した95%純度のD−プシコースのエタノール溶液を種晶として添加し、得られた溶液を約100rpmの速度で撹拌した。濃縮溶液と種晶との混合状態を確認した後、撹拌速度を約10rpmに再調節し、この混合物を時間当たり約1℃ずつ冷却した。顕微鏡を使用して、D−プシコースの結晶個数が急増する濃度を求めた。この状態を過飽和度と見なした。その後、顕微鏡観察及び検糖分析(saccharimetric analysis)が、結晶がそれ以上成長しないか、または上澄み液の糖濃度がそれ以上変化しないことを示すまで温度を維持して結晶を成長させ、その後、溶液の温度を約1℃ずつ冷却した。温度が約33℃まで冷却された後、最終結晶の状態が得られ、これは図3に図示されている。約33℃で冷却を中止し、遠心分離による脱水、洗浄、及び乾燥を実施して、D−プシコース種晶を得た。得られた最終種晶は、直径約0.04mm〜約0.10mmの範囲にあり、乾燥重量は、初期水溶液中に存在したD−プシコースの重さに比べて約40%であった。
【0052】
実施例6:D−プシコースの飽和濃度及び過飽和濃度の測定
前記実施例3から実施例5の手順を繰り返して、純粋なD−プシコースを得た。調製されたD−プシコースを溶解させて、温度による飽和曲線を得た。30℃で始め、D−プシコースを少量添加した場合にD−プシコースがそれ以上溶けない濃度を、対応する温度での飽和濃度と定義し、飽和濃度は、温度を80℃まで上昇させることによって求め、図1に図示されたD−プシコース飽和曲線を作成した。
【0053】
さらに、D−プシコースを溶解させ、約85%(g/g溶液)まで濃縮した。その後、D−プシコース溶液を晶析装置に入れて、微細結晶が急激に形成される温度まで徐々に冷却した。脱イオン水を添加して、飽和濃度を変化させた後、この冷却実験を繰り返して、それぞれの飽和温度の過飽和濃度を測定した。この結果に基づき、図1に図示されているD−プシコース過飽和曲線を作成した。
【0054】
実施例7:温度変化を利用したD−プシコース結晶化
前記実施例3に説明されるように精製されたD−プシコース溶液(D−プシコースを約2,780g含有)を得、これを約85%(g/g溶液)まで濃縮し、晶析装置に入れた。晶析装置は約50℃の温度を維持するように調節した。実施例5で得た種晶を乳鉢に入れ、エタノールと混合してD−プシコース溶液を調製した。結晶化のために、このD−プシコースエタノール溶液を、晶析装置中の濃縮されたD−プシコース溶液に、種晶が溶液中のD−プシコースと比較して0.3%(w/w)の量で存在するように、種晶として投入した。その後、得られた溶液を撹拌器によって約100rpmで撹拌させ、種晶を濃縮液に均一に分布させた。その後、撹拌器の速度を約10rpmに下げ、経時的に一定間隔で試料を採取して、結晶個数の増加及び結晶サイズの変化を顕微鏡で観察した。試料を、1.5mLマイクロチューブを利用して遠心分離し、上澄み液の濃度及び純度を、それぞれ検糖計(saccharimeter)及びHPLCで測定した。
【0055】
温度が、結晶サイズの変化、または上澄み液の濃度変化がそれ以上起こらない温度(飽和温度)に達した場合、晶析装置の温度を約1℃ずつ冷やして、D−プシコース溶液がその飽和濃度と過飽和濃度との間の領域に存在するように、すなわち、準安定域の過飽和状態が維持されるようにした。
【0056】
急冷によって、結晶化のためのD−プシコース溶液が過飽和領域に移行すると、微細結晶が形成され始め、これは種晶の量が多くなる結果となり、最終的に、結晶サイズの減少をもたらす。結晶サイズが小さいと、遠心分離による脱水が容易ではなく、そのためこの結晶を実際の工程に適用することが困難になる。
【0057】
最終上澄み液を、濃度が約74%(g/g溶液)に達するまで冷やし、このときの結晶状態を図4に図示する。結晶化が完了した溶液を高速遠心脱水器に入れ、約4,000rpmで約10分間遠心分離し、上澄み液をデカントし、結晶のみ回収した。その後、脱水中に脱イオン水を噴霧状で加えて、結晶の外部表面の上澄み液を洗い流した。脱水後に回収されたD−プシコースを、乾燥のために流動床乾燥器または真空乾燥器に移動させた。結果は、乾燥後のD−プシコース結晶の量が約1,408gと、最初に溶解されたD−プシコース約2,789gと比較して、50%の回収であったことを示した。結晶サイズは、約0.1mm〜約0.2mmの範囲にあり、市販されているフルクトースまたはショ糖の約1/2ほどのサイズに相当した。
【0058】
実施例8:濃度変化を利用したD−プシコースの結晶化
前記実施例3に説明されるように精製されたD−プシコース溶液から、固形分約5,000gを得た。このうち、約2/3は約60%(g/g溶液)に濃縮し、残りの1/3は約80%(g/g溶液)に濃縮した。80%(g/g溶液)の濃縮液を、10Lのフラスコを装着した濃縮器(EYELA社、N−11)に入れ、約10rpmで撹拌しながら濃縮させた。実施例5で種晶として調製されたD−プシコースエタノール溶液をフラスコに真空下で添加し、フラスコ中に温度計を装着して、内部温度の変化を測定した。濃縮が進められるにつれて結晶が成長した。経時的に一定間隔で試料を採取して、結晶個数の増加、及び結晶サイズの変化を顕微鏡で観察し、1.5mLマイクロチューブを利用して遠心分離した後、上澄み液の濃度を検糖計で測定し、上澄み液の純度を、HPLCで測定した。溶液はときには過飽和レベル以上に濃縮され、そのため微細結晶が形成された。結果として、結晶サイズは減少した。そのような場合には、あらかじめ調製した約60%(g/g溶液)の低濃度D−プシコース溶液を注入して、生成された微細結晶を溶解させ、結果として同時に、濃度が結晶の成長によって低くなっていた濃縮溶液の純度を高めた。
【0059】
試料を採取して遠心分離に供した。その後、それ以上結晶サイズに変化が認められなければ、真空を除去して、試料を約40℃で約12時間立てて放置した。このときの結晶状態を図4に図示する。結晶化が完了した溶液を高速遠心脱水器に入れ、約4,000rpmで約10分間遠心分離し、上澄み液をデカントして結晶のみ回収した。その後、脱イオン水を噴霧状で加え、結晶の外部表面の上澄み液を洗い流した。脱水後に回収されたD−プシコース結晶を、流動床乾燥器または真空乾燥器に移動させて乾燥させた。乾燥後の結晶量は約2,650gであり、溶解されていたD−プシコース約5,000gと比較して約53%が回収されたことが分かった。結晶サイズは約0.1mm〜約0.2mmの範囲であることが分かった。この結晶を、温度変化を利用して調製した結晶と比較した場合、このようにして得た結晶の長さは温度変化により得た結晶よりも長かった。
【0060】
本発明の例示的な実施例について説明したが、上記で説明された態様はあらゆる面において単に例示として提供され、本発明の変形および変化を限定するものではないということが理解されるべきである。本発明の範囲は、前記詳細な説明ではなく添付の特許請求の範囲により規定される。特許請求の範囲の精神及び範囲、ならびにその等価物から導き出されるあらゆる変形または変化は、本発明の範囲に含まれるものであると解釈されねばならない。
【技術分野】
【0001】
本出願は、2010年3月26日に韓国特許庁に出願された大韓民国特許出願第10-2010-0027546号の恩典を主張し、その開示はその全体が参照により本明細書に組み入れられる。
【0002】
本発明は、過飽和を利用することによってD−プシコース溶液からD−プシコース結晶を製造する方法に関する。
【背景技術】
【0003】
D−プシコースは、糖蜜やブドウ糖の異性化反応中に極少量存在する天然糖であり、砂糖に比べて約70%の甘味を有する単糖類である。D−プシコースは、ヒトでは代謝されず、カロリーが実質的になく、体脂肪の形成を抑制することから、体重増加に影響が小さい甘味料であると報告されている(非特許文献1及び2)。
【0004】
最近になって、非齲蝕(non-carious)機能及び抗齲蝕(anti-carious)機能に対するD−プシコースの効果が発表され、したがってD−プシコースの、歯の健康の一助となる材料としての、及び砂糖を代替することができる甘味料としての開発が活発になされている。
【0005】
D−プシコースは、その特性及び機能性によって、体重増加を防ぐ甘味料として食品産業分野で関心を集めているが、高温でフルクトースから製造されるD−プシコースの量はわずかであり、したがって化学合成によりD−プシコースを製造することは困難である。フルクトースとD−タガトースエピメラーゼとを反応させる、またはフルクトースとD−プシコースエピメラーゼを反応させることにより大量生産する方法が報告されたが、D−プシコースの収率が非常に低いことから製造コストは高くなる。
【0006】
最近、本発明者らは、ブドウ糖をフルクトースに異性化させた後にフルクトースとD−プシコースエピメラーゼを生産する固定化細胞とを反応させることにより、D−プシコースを経済的に生産する方法を報告した(特許文献1)。
【0007】
酵素反応によって生産されたD−プシコースを含む反応液は、約20重量%〜約30重量%の量の固形のD−プシコースを含む低純度産物であるために、高純度にD−プシコースを分離することが要求される。高純度に分離するために多様な方法が産業的に生産される材料に適用されている。糖の場合、通常クロマトグラフィを使用して高純度液を作り、その後、結晶化させて高純度糖産物を得る。D−プシコースの場合、産業的に適用可能な製造方法はまだ開発されていない。
【0008】
D−プシコースの反応液中の未反応フルクトースを酵母で発酵させて除去する、及び大量のエタノールを使用することによって、粉末形態のD−プシコースを製造する方法が報告されている(非特許文献3)。しかし、大量のエタノール使用は、防爆及び産物回収のための高価な設備を必要とし、有機溶媒の使用による撹拌器の故障、及び回収産物中の異物の存在などの問題点が発生しうる。また、最終産物が微粉状であるために、脱水、洗浄、及び乾燥過程において多くが失われる。最終産物製造のためにD−プシコースを粉末化するあいだ粉末は互いに吸着し、これは粉末粒子中に不純物をもたらし、その結果最終産物の純度が低くなる。微粉状の産物は、重さの増加に比べて体積の増加が大きくなり、これは過大包装による製造コストの上昇、及び流通上の追加費用の発生をもたらす。さらに、このような精密化学製品は、流動性が低いことから食品製造工程において不利である。従って、エタノールなどの有機溶媒を使用することなく経済的にD−プシコースを製造し、かつ製造工程中の流動性及び生産物価値を改善するために、微粉状ではない結晶状の純粋なD−プシコースを製造する方法が依然として必要とされている。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】大韓民国特許出願第10−2009−0118465号
【非特許文献】
【0010】
【非特許文献1】Matuo,T.et al.,Asia Pac.J.Clin.Nutr.,10,233-237,2001
【非特許文献2】Matsuo,T.and K.Izumori,Asia Pac.J.Clin.Nutr.,13,S127,2004
【非特許文献3】Kei T.et al.,J.Biosci.Bioeng.,90(4),453-455,2000
【発明の概要】
【発明が解決しようとする課題】
【0011】
本発明の目的は、D−プシコース結晶を製造する方法を提供することである。
【課題を解決するための手段】
【0012】
このために、本発明者らは、生物学的変換や酵素反応によって得られたD−プシコース溶液から有機溶媒を使用せずにD−プシコース結晶を製造する方法に関する研究を行った。この方法において、該D−プシコース結晶は、D−プシコース溶液を準安定域(metastable zone)の過飽和状態に維持することによって適切なサイズに製造され、これにより本発明は完成した。
【0013】
本発明は、D−プシコース溶液を、飽和曲線と過飽和曲線との間にある準安定域に維持することによってD−プシコース結晶を製造する方法を提供する。
【0014】
より具体的には、本発明は以下の通りである。
本発明(1)は、
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域(metastable zone)の過飽和状態で結晶化させる段階と
を含む、D−プシコース結晶を製造する方法である。
本発明(2)は、
前記精製されたD−プシコース溶液を得る段階が、
前記D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含む、
本発明(1)の方法である。
本発明(3)は、前記精製されたD−プシコース溶液を濃縮させる段階が、約60℃〜約70℃の温度で行われる、本発明(1)の方法である 。
本発明(4)は、前記結晶化させる段階で使用される前記濃縮されたD−プシコース溶液に、D−プシコース種晶が、前記濃縮されたD−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加される、本発明(1)の方法である。
本発明(5)は、前記結晶化させる段階で使用される濃縮されたD−プシコース溶液が、約70%(g/g)以上のD−プシコース溶液である、本発明(1)の方法である。
本発明(6)は、前記結晶化させる段階における結晶化の進行をモニタリングし、D−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に溶液の温度を低くすることによって、前記濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、本発明(1)の方法である。
本発明(7)は、前記結晶化させる段階における結晶化の進行をモニタリングし、前記溶液中のD−プシコースが過飽和レベル以上に濃縮された場合に前記濃縮されたD−プシコース溶液より低い濃度のD−プシコース溶液を添加することによって、該濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、本発明(1)の方法である。
本発明(8)は、前記結晶化させる段階における準安定域の過飽和状態が、飽和濃度から、該飽和濃度からさらに約6%(g/g溶液)高い濃度までの範囲に存在する、本発明(1)の方法である。
【発明の効果】
【0015】
本発明の態様による製造方法を利用して、D−プシコース溶液から、有機溶媒を使用しない経済的な結晶化工程を通して、純粋であって、かつ産業的適用に適した形態のD−プシコース結晶を製造できる。
【図面の簡単な説明】
【0016】
上記および他の本発明の特徴および利点は、添付の図面への参照と共にその例示的態様を詳細に説明することにより、より明らかになるであろう。
【図1】温度に関連した、純粋なD−プシコースの飽和曲線と過飽和曲線とを示すグラフである。
【図2】温度に関連した、80%(g/g溶液)濃度でのD−プシコースの残存量を示すグラフである。
【図3】顕微鏡で観察した、生成されたD−プシコース種晶を示す写真である。
【図4】顕微鏡使用して撮影された、本発明の例示的態様による温度調節によって生成されたD−プシコース結晶を示す写真である。
【図5】顕微鏡使用して撮影された、本発明の例示的態様による減圧濃縮によって生成されたD−プシコース結晶を示すイメージである。
【発明を実施するための形態】
【0017】
本発明の詳細な説明
本発明のある局面に従い、
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を収得する段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階と
を含む、精製されたD−プシコース結晶を製造する方法が提供される。
【0018】
本明細書で使われている「過飽和状態」とは、溶質が溶媒の溶解能を超えて溶解されている不安定な状態であり、溶質が固体に結晶化しうる状態を意味する。従って、結晶化によって溶液から溶質を分離するためには、溶液において過飽和状態に達することが必要である。一般的に、溶液の過飽和状態は、外部条件、不純物、温度、濃度、pHなどによって影響を受けうる。
【0019】
本明細書で使われている「準安定域」の過飽和状態は、溶液の濃度が平衡濃度、すなわち飽和濃度から、結晶が自発的に析出する最低過飽和濃度までの範囲を意味する。この範囲の濃度では結晶核形成(crystal nucleation)などの結晶化は起こらない。しかしながら、この範囲の濃度の溶液に外部から結晶を入れれば、溶液中の溶質の量が過飽和濃度であるので、自発的に結晶成長が起こって結晶サイズが大きくなる。すなわち、結晶を生成するために、飽和濃度以上である溶液に種晶(seed)が投入されれば、準安定域で種晶が成長して結晶を形成する。結晶化用溶液が過度に濃縮あるいは急激に冷却されると準安定域を超える過飽和状態に達し、従って結晶の成長ではなく結晶核形成が起こり、複数の微細結晶が形成される。従って、適切なサイズの結晶を得るために、結晶化用溶液を、準安定域の過飽和状態に維持させながら適切な速度で結晶化を行わなければならない。
【0020】
本発明のある態様において、出発物質であるD−プシコース溶液は、D−プシコースエピメラーゼを発現するコリネバクテリウム属由来の細菌、またはそれから単離されたD−プシコースエピメラーゼによって調製される。
【0021】
本発明のある態様において、D−プシコース溶液は、大韓民国特許出願第2009−0118465号に記載されているように、コリネバクテリウムグルタミクム(Corynebacterium glutamicum)KCTC13032を培養して得られた細胞またはそれから単離された酵素を固定化担体に固定化させること、および該固定化された細胞または酵素にフルクトースを基質として供給することにより、得られうる。
【0022】
D−プシコース溶液からD−プシコース結晶を得るために、D−プシコースの精製及び結晶化に影響を及ぼしうる他の物質を除去し、効率的な結晶化のために必要な状態を形成しなければならない。
【0023】
従って、本発明によるD−プシコース結晶を製造する方法は、D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階を含みうる。
【0024】
本発明のある態様において、前記精製されたD−プシコース溶液を得る段階は、
D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含みうる。
【0025】
本発明のある態様において、前記D−プシコース溶液を脱塩させる段階は、溶液が陽イオン交換樹脂が充填されたカラム、陰イオン交換樹脂が充填されたカラム、及び陽イオン交換樹脂と陰イオン交換樹脂との混合物が充填されたカラムを通過するクロマトグラフィによって遂行されうる。
【0026】
高純度のD−プシコースを得るために、一般的にクロマトグラフィによる分離が利用される。D−プシコース結晶を得るために、D−プシコース溶液中でのD−プシコースの量は、約70%〜約85%またはそれ以上でなければならない。従って、D−プシコースエピメラーゼ反応によって調製されたD−プシコース溶液中でのD−プシコースの純度は約22%でありこれは直接結晶化を行うには低すぎることから、結晶化段階前にD−プシコースを精製し、所望のレベルまで濃縮しなければならない。高純度のD−プシコース結晶を得るために、結晶化段階前に、溶液を脱色及び脱塩することによって不純物を除去してもよく、及び、クロマトグラフィ、例えば、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムでのクロマトグラフィによって、D−プシコースを精製してもよい。
【0027】
本発明によるD−プシコース結晶を製造する方法は、精製されたD−プシコース溶液を濃縮させる段階を含みうる。
【0028】
本発明のある態様において、前記精製されたD−プシコース溶液を濃縮させる段階は、約60℃〜約70℃で行われうる。濃縮液の温度が約70℃より高く上昇すると、D−プシコースの熱変性が起こることがある。温度が約60℃未満に下がると、溶液を所望レベルに濃縮することは困難である。濃縮が進むにつれて蒸発熱によって反応物の温度が急上昇するので、溶液の濃縮は、温度を約70℃以下に維持しながら速かに行わなければならない。
【0029】
本発明のある態様において、D−プシコース溶液の濃縮は、約65℃以下で行われうる。
【0030】
本発明によるD−プシコース結晶を製造する方法は、濃縮されたD−プシコース溶液の温度及び濃度を調節することによって、該溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階を含みうる。
【0031】
本発明のある態様において、結晶化段階で使用される濃縮されたD−プシコース溶液は、約70%〜約85%(g/g)またはそれ以上のD−プシコース溶液でありうる。
【0032】
本発明のある態様において、結晶化段階で使用される濃縮されたD−プシコース溶液に、D−プシコース種晶が、該D−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加されうる。
【0033】
本発明において、D−プシコース結晶は、D−プシコースが溶液中で溶媒と平衡状態をなす平衡濃度以上でD−プシコースが存在することから自発的に結晶成長が起こる準安定域の過飽和状態にD−プシコース溶液を維持することによって製造される。本発明において、結晶化に必要とされる過飽和状態は、D−プシコース溶液の温度を低くするか、またはD−プシコース溶液中のD−プシコースの濃度を変化させることによって維持されうる。
【0034】
本発明のある態様において、所定の間隔で試料を採取して該試料を肉眼もしくは顕微鏡を使用して観察すること、または試料の遠心分離から得られた上層中の糖濃度を分析することによって、結晶化段階における結晶化の進行をモニタリングしてもよい。その結果によって、温度またはD−プシコースの濃度を調節することができる。
【0035】
本発明のある態様において、D−プシコース種晶をD−プシコース溶液に添加した後、溶液中でのD−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に温度を低くすることによって、結晶化段階におけるD−プシコース溶液の準安定域の過飽和状態を維持してもよい。
【0036】
本発明のある態様において、D−プシコース溶液へのD−プシコース種晶の添加、および溶液の穏やかな撹拌、例えば約10rpmで撹拌しながらの結晶成長の後、D−プシコースが過飽和レベル以上に濃縮された場合に前記D−プシコース溶液よりも低濃度のD−プシコース溶液を添加することによって、結晶化段階におけるD−プシコース溶液の準安定域の過飽和状態を維持してもよい。
【0037】
本発明のある態様において、結晶化段階においてD−プシコース溶液を準安定域の過飽和状態に維持させるために添加されるD−プシコース溶液は、過飽和レベル以上に濃縮されたD−プシコース溶液よりも低濃度のD−プシコースを含む。例えば、添加されるD−プシコース溶液は約60%〜約70%のD−プシコース溶液でありうる。
【0038】
本発明のある態様において、結晶化段階における過飽和状態は、飽和濃度と該飽和濃度からさらに約6%(g/g溶液)高い濃度との間の範囲に存在しうる。
【0039】
過飽和濃度は、物質に固有の特性であり、飽和した溶液を冷却または濃縮することにより得られる。溶液の温度が溶液の飽和に達する温度から徐々に下がった場合に、高度に濃縮した溶液が不安定な状態に達して微細結晶が形成され始める濃度及び温度として、過飽和濃度及び過飽和温度をそれぞれ定義することができる。過飽和濃度の溶液に脱イオン水を添加し、該溶液を再加熱して微結晶を速やかに溶解させ、希釈された濃度で溶液の温度を飽和温度に調節し、この溶液を再度冷やすことにより、微結晶が生成される過飽和濃度を特定することができる。様々な飽和濃度で、物質の溶液の希釈、加熱、及び再冷却を繰り返すことによって、該物質の準安定域を特定することができる。D−プシコースも固有の準安定域の濃度範囲を有し、この範囲は飽和濃度またはそれ以上から該飽和濃度より約6%高いものまでであることが確認された。D−プシコースの準安定域にD−プシコース溶液を維持しながら結晶化を行って、形状が安定しておりかつサイズが大きい結晶を得ることができる。
【0040】
本発明のある態様において、本発明によるD−プシコース結晶を製造する方法は、
結晶化段階で得られたD−プシコース結晶を遠心分離によって回収する段階と、
前記結晶を脱イオン水で洗浄する段階と、
前記結晶を乾燥させる段階と
をさらに含むことができる。
【0041】
結晶の乾燥は、流動床乾燥器または真空乾燥器で行われうる。
【0042】
本発明のある態様において、前記精製されたD−プシコース結晶は、約0.1mm〜約0.2mmのサイズを有する。
【0043】
本発明のある態様において、精製されたD−プシコース結晶は、
酵素反応などによって生成されたD−プシコース溶液を約40%(g/g溶液)の濃度に濃縮し、得られた溶液を、粒状活性炭(GAC:granulated active carbon)脱色剤が充填されたカラムに、1時間当たり約4mの線速度で通して脱色する段階と、
脱色されたD−プシコース溶液を、陽イオン交換樹脂、陰イオン交換樹脂、及び陽イオン交換樹脂と陰イオン交換樹脂との混合物がそれぞれ充填されたカラムに、約40℃で、時間当りイオン交換樹脂体積の2倍の速度で注入して、脱色されたD−プシコース溶液を脱塩させる段階と、
脱色及び脱塩によって精製されたD−プシコース溶液を約60%(g/g溶液)の濃度に濃縮し、この溶液をカルシウム活性基が付着したイオン交換樹脂で充填された分離カラムに通過させて、フルクトースからプシコースを分離する段階と、
分離されたD−プシコース溶液を、約70℃以下で、濃縮器において、約85%(g/g)以上の濃度まで濃縮する段階と、
濃縮されたD−プシコース溶液に、D−プシコース種晶を、濃縮されたD−プシコース溶液に溶解されたD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で注入し、温度及び濃度を調節して、溶液からD−プシコースを準安定域の過飽和状態で結晶化させる段階と、
D−プシコース結晶を、結晶化に供された溶液から遠心分離によって分離し、該溶液及びD−プシコース結晶を洗浄し、結晶を流動床乾燥器または真空乾燥器において乾燥する段階と
を含む方法によって製造されうる。
【0044】
以下、本発明について、具体的な実施例を参照しながら詳細に説明する。しかしながら、それら実施例は、本発明の例示的説明を目的としたものであり、本発明の範囲は、それら実施例になんら限定されるものではない。
【実施例】
【0045】
実施例1:コリネバクテリウム属微生物を利用した低純度D−プシコース溶液の生成
大韓民国特許出願第10−2009−0118465号に開示されているように、コリネバクテリウムグルタミクムKCTC13032培養する段階、及び該微生物、またはそれから単離されたD−プシコースエピメラーゼが固定化された担体によってフルクトースをD−プシコースに転換する段階を含む、D−プシコースを連続生成する方法によって、D−プシコースを調製した。この方法によって調製されたD−プシコース溶液中のD−プシコースの量は約22%であり、それから直接結晶化させるには低すぎる濃度であった。
【0046】
実施例2:低純度D−プシコース溶液の精製
実施例1で生成されたD−プシコース溶液を約40%(g/g溶液)に濃縮した後、粒状活性炭素(granulated active carbon)が充填された脱色カラムを通して、濃縮液内の有色物質を除去した。
【0047】
実施例1で生成されたD−プシコース溶液のD−プシコース純度は、固形分含有量が約22%と非常に低く、結晶化するには適していなかった。結晶化のためには、結晶化対象物質の純度を約70%〜約90%またはそれ以上に高めねばならない。クロマトグラフィによるD−プシコースの効率的な分離のためには、D−プシコース溶液からイオンが除去されねばならない。分離対象溶液中にイオン成分が存在する場合、分離樹脂の活性基がイオン成分と置換されて樹脂の分離能が低下するので、分離樹脂を繰り返し使用することが不可能となる。従って、前記で調製された脱色されたD−プシコース溶液を、水素基で置換された陽イオン交換樹脂とヒドロキシル基で置換された陰イオン交換樹脂とが充填されたカラムに通した後、最終段階で、陽イオン交換樹脂及び陰イオン交換樹脂の混合物が充填されたイオン交換カラムに通し、前記溶液中のイオン成分を除去した。溶液中のイオン成分除去は、導電率を導電計で測定することによって確認した。精製溶液の導電率は、単位cm当たり約10マイクロジーメンス以下になるように調節した。
【0048】
実施例3:クロマトグラフィを利用した高純度D−プシコース溶液の調製
前記実施例2で脱色及び脱塩により有色物質及びイオン成分などの不純物を除去した、低純度D−プシコース溶液を、約60%(g/g溶液)まで濃縮し、その後カルシウム基で置換させたイオン交換樹脂(Purolite PCR 642K)に通過させて、精製されたD−プシコース溶液を得た。
【0049】
前記イオン交換樹脂カラム内に充填されたイオン交換樹脂の量は、約200Lであり、該カラムに通した試料、すなわち、実施例2で調製された精製されたD−プシコース溶液の量は、約20Lであり、運転温度は、約60℃であった。試料を注入し、時間当たり約260Lの脱イオン水で溶出させた後、採取した各分画において、HPLCシステム(HP、Agilent 1200シリーズ)を使用することによって、フルクトースおよびD−プシコースの濃度をそれぞれ測定した。純粋なD−プシコース分画を取り、D−プシコース及びフルクトースを含有する分画を濃縮し、分離対象試料として再度用いた。カルシウム基で置換されたカラム(Bio Rad社)をHPLC分析カラムに利用し、脱イオン水を分当たり約0.5mLの流量で適用した。
【0050】
実施例4:D−プシコース溶液の濃縮
結晶化のために必要なD−プシコース濃縮液を得るために、実施例3で精製されたD−プシコース溶液を、真空濃縮器(EYELA社、N−11)に入れて、約80%(g/g溶液)に濃縮した。濃縮された液をそれぞれチューブに分注し、それぞれ70℃,65℃、及び60℃のウォーターバス中に立てて放置した。試料を経時的に一定間隔で採取し、濃縮液のアリコートにおける残存量を測定した。その結果が図2に図示されている。濃縮液の温度が約70℃以上になると、3時間後にD−プシコースの熱変性が起こり、22時間後には、初期量に比べて約78%のみが残存することが確認された。濃縮過程中、蒸発熱によって内部の温度は約40℃以下に維持されるが、D−プシコースの量が約80%(g/g溶液)以上になると、温度は急上昇する。このような結果から、D−プシコースを約80%(g/g溶液)以上に濃縮する場合、濃縮液の内部温度を約70℃以下に迅速に低下させるか、または例えば約65℃以下で濃縮段階を遂行することが必要であるということが確認された。
【0051】
実施例5:D−プシコース種晶の生成
前記実施例3において精製分離されたD−プシコース溶液(D−プシコースを約1,000g含有)を、実施例4において説明されるように、約85%(g/g溶液)に濃縮した。純度95%の製品(Sigma社)1gを購入し、乳鉢に入れて粉砕した後、これをエタノール溶液と混合させた。二重の(double jacketed)2L反応槽を備える反応器システム(IKA(登録商標)、LR−2.ST)を晶析装置(crystallizer)として利用し、晶析装置内の濃縮液の初期温度を約50℃に調節し、調製した95%純度のD−プシコースのエタノール溶液を種晶として添加し、得られた溶液を約100rpmの速度で撹拌した。濃縮溶液と種晶との混合状態を確認した後、撹拌速度を約10rpmに再調節し、この混合物を時間当たり約1℃ずつ冷却した。顕微鏡を使用して、D−プシコースの結晶個数が急増する濃度を求めた。この状態を過飽和度と見なした。その後、顕微鏡観察及び検糖分析(saccharimetric analysis)が、結晶がそれ以上成長しないか、または上澄み液の糖濃度がそれ以上変化しないことを示すまで温度を維持して結晶を成長させ、その後、溶液の温度を約1℃ずつ冷却した。温度が約33℃まで冷却された後、最終結晶の状態が得られ、これは図3に図示されている。約33℃で冷却を中止し、遠心分離による脱水、洗浄、及び乾燥を実施して、D−プシコース種晶を得た。得られた最終種晶は、直径約0.04mm〜約0.10mmの範囲にあり、乾燥重量は、初期水溶液中に存在したD−プシコースの重さに比べて約40%であった。
【0052】
実施例6:D−プシコースの飽和濃度及び過飽和濃度の測定
前記実施例3から実施例5の手順を繰り返して、純粋なD−プシコースを得た。調製されたD−プシコースを溶解させて、温度による飽和曲線を得た。30℃で始め、D−プシコースを少量添加した場合にD−プシコースがそれ以上溶けない濃度を、対応する温度での飽和濃度と定義し、飽和濃度は、温度を80℃まで上昇させることによって求め、図1に図示されたD−プシコース飽和曲線を作成した。
【0053】
さらに、D−プシコースを溶解させ、約85%(g/g溶液)まで濃縮した。その後、D−プシコース溶液を晶析装置に入れて、微細結晶が急激に形成される温度まで徐々に冷却した。脱イオン水を添加して、飽和濃度を変化させた後、この冷却実験を繰り返して、それぞれの飽和温度の過飽和濃度を測定した。この結果に基づき、図1に図示されているD−プシコース過飽和曲線を作成した。
【0054】
実施例7:温度変化を利用したD−プシコース結晶化
前記実施例3に説明されるように精製されたD−プシコース溶液(D−プシコースを約2,780g含有)を得、これを約85%(g/g溶液)まで濃縮し、晶析装置に入れた。晶析装置は約50℃の温度を維持するように調節した。実施例5で得た種晶を乳鉢に入れ、エタノールと混合してD−プシコース溶液を調製した。結晶化のために、このD−プシコースエタノール溶液を、晶析装置中の濃縮されたD−プシコース溶液に、種晶が溶液中のD−プシコースと比較して0.3%(w/w)の量で存在するように、種晶として投入した。その後、得られた溶液を撹拌器によって約100rpmで撹拌させ、種晶を濃縮液に均一に分布させた。その後、撹拌器の速度を約10rpmに下げ、経時的に一定間隔で試料を採取して、結晶個数の増加及び結晶サイズの変化を顕微鏡で観察した。試料を、1.5mLマイクロチューブを利用して遠心分離し、上澄み液の濃度及び純度を、それぞれ検糖計(saccharimeter)及びHPLCで測定した。
【0055】
温度が、結晶サイズの変化、または上澄み液の濃度変化がそれ以上起こらない温度(飽和温度)に達した場合、晶析装置の温度を約1℃ずつ冷やして、D−プシコース溶液がその飽和濃度と過飽和濃度との間の領域に存在するように、すなわち、準安定域の過飽和状態が維持されるようにした。
【0056】
急冷によって、結晶化のためのD−プシコース溶液が過飽和領域に移行すると、微細結晶が形成され始め、これは種晶の量が多くなる結果となり、最終的に、結晶サイズの減少をもたらす。結晶サイズが小さいと、遠心分離による脱水が容易ではなく、そのためこの結晶を実際の工程に適用することが困難になる。
【0057】
最終上澄み液を、濃度が約74%(g/g溶液)に達するまで冷やし、このときの結晶状態を図4に図示する。結晶化が完了した溶液を高速遠心脱水器に入れ、約4,000rpmで約10分間遠心分離し、上澄み液をデカントし、結晶のみ回収した。その後、脱水中に脱イオン水を噴霧状で加えて、結晶の外部表面の上澄み液を洗い流した。脱水後に回収されたD−プシコースを、乾燥のために流動床乾燥器または真空乾燥器に移動させた。結果は、乾燥後のD−プシコース結晶の量が約1,408gと、最初に溶解されたD−プシコース約2,789gと比較して、50%の回収であったことを示した。結晶サイズは、約0.1mm〜約0.2mmの範囲にあり、市販されているフルクトースまたはショ糖の約1/2ほどのサイズに相当した。
【0058】
実施例8:濃度変化を利用したD−プシコースの結晶化
前記実施例3に説明されるように精製されたD−プシコース溶液から、固形分約5,000gを得た。このうち、約2/3は約60%(g/g溶液)に濃縮し、残りの1/3は約80%(g/g溶液)に濃縮した。80%(g/g溶液)の濃縮液を、10Lのフラスコを装着した濃縮器(EYELA社、N−11)に入れ、約10rpmで撹拌しながら濃縮させた。実施例5で種晶として調製されたD−プシコースエタノール溶液をフラスコに真空下で添加し、フラスコ中に温度計を装着して、内部温度の変化を測定した。濃縮が進められるにつれて結晶が成長した。経時的に一定間隔で試料を採取して、結晶個数の増加、及び結晶サイズの変化を顕微鏡で観察し、1.5mLマイクロチューブを利用して遠心分離した後、上澄み液の濃度を検糖計で測定し、上澄み液の純度を、HPLCで測定した。溶液はときには過飽和レベル以上に濃縮され、そのため微細結晶が形成された。結果として、結晶サイズは減少した。そのような場合には、あらかじめ調製した約60%(g/g溶液)の低濃度D−プシコース溶液を注入して、生成された微細結晶を溶解させ、結果として同時に、濃度が結晶の成長によって低くなっていた濃縮溶液の純度を高めた。
【0059】
試料を採取して遠心分離に供した。その後、それ以上結晶サイズに変化が認められなければ、真空を除去して、試料を約40℃で約12時間立てて放置した。このときの結晶状態を図4に図示する。結晶化が完了した溶液を高速遠心脱水器に入れ、約4,000rpmで約10分間遠心分離し、上澄み液をデカントして結晶のみ回収した。その後、脱イオン水を噴霧状で加え、結晶の外部表面の上澄み液を洗い流した。脱水後に回収されたD−プシコース結晶を、流動床乾燥器または真空乾燥器に移動させて乾燥させた。乾燥後の結晶量は約2,650gであり、溶解されていたD−プシコース約5,000gと比較して約53%が回収されたことが分かった。結晶サイズは約0.1mm〜約0.2mmの範囲であることが分かった。この結晶を、温度変化を利用して調製した結晶と比較した場合、このようにして得た結晶の長さは温度変化により得た結晶よりも長かった。
【0060】
本発明の例示的な実施例について説明したが、上記で説明された態様はあらゆる面において単に例示として提供され、本発明の変形および変化を限定するものではないということが理解されるべきである。本発明の範囲は、前記詳細な説明ではなく添付の特許請求の範囲により規定される。特許請求の範囲の精神及び範囲、ならびにその等価物から導き出されるあらゆる変形または変化は、本発明の範囲に含まれるものであると解釈されねばならない。
【特許請求の範囲】
【請求項1】
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域(metastable zone)の過飽和状態で結晶化させる段階と
を含む、D−プシコース結晶を製造する方法。
【請求項2】
前記精製されたD−プシコース溶液を得る段階が、
前記D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含む、
請求項1に記載の方法。
【請求項3】
前記精製されたD−プシコース溶液を濃縮させる段階が、約60℃〜約70℃の温度で行われる、請求項1に記載の方法 。
【請求項4】
前記結晶化させる段階で使用される前記濃縮されたD−プシコース溶液に、D−プシコース種晶が、前記濃縮されたD−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加される、請求項1に記載の方法。
【請求項5】
前記結晶化させる段階で使用される濃縮されたD−プシコース溶液が、約70%(g/g)以上のD−プシコース溶液である、請求項1に記載の方法。
【請求項6】
前記結晶化させる段階における結晶化の進行をモニタリングし、D−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に溶液の温度を低くすることによって、前記濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、請求項1に記載の方法。
【請求項7】
前記結晶化させる段階における結晶化の進行をモニタリングし、前記溶液中のD−プシコースが過飽和レベル以上に濃縮された場合に前記濃縮されたD−プシコース溶液より低い濃度のD−プシコース溶液を添加することによって、該濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、請求項1に記載の方法。
【請求項8】
前記結晶化させる段階における準安定域の過飽和状態が、飽和濃度から、該飽和濃度からさらに約6%(g/g溶液)高い濃度までの範囲に存在する、請求項1に記載の方法。
【請求項1】
D−プシコース溶液から不純物を除去して精製されたD−プシコース溶液を得る段階と、
前記精製されたD−プシコース溶液を濃縮させる段階と、
前記で濃縮されたD−プシコース溶液からD−プシコースを準安定域(metastable zone)の過飽和状態で結晶化させる段階と
を含む、D−プシコース結晶を製造する方法。
【請求項2】
前記精製されたD−プシコース溶液を得る段階が、
前記D−プシコース溶液を、脱色剤が充填されたカラムに通過させて、D−プシコース溶液を脱色させる段階と、
前記で脱色されたD−プシコース溶液を、イオン交換クロマトグラフィによって脱塩させる段階と、
前記で脱塩されたD−プシコース溶液を、カルシウム活性基が付着したイオン交換樹脂が充填されたカラムに通し、精製されたD−プシコース溶液を得る段階と
を含む、
請求項1に記載の方法。
【請求項3】
前記精製されたD−プシコース溶液を濃縮させる段階が、約60℃〜約70℃の温度で行われる、請求項1に記載の方法 。
【請求項4】
前記結晶化させる段階で使用される前記濃縮されたD−プシコース溶液に、D−プシコース種晶が、前記濃縮されたD−プシコース溶液中のD−プシコース総量に基づき約0.01%〜約1%(g/g)の量で添加される、請求項1に記載の方法。
【請求項5】
前記結晶化させる段階で使用される濃縮されたD−プシコース溶液が、約70%(g/g)以上のD−プシコース溶液である、請求項1に記載の方法。
【請求項6】
前記結晶化させる段階における結晶化の進行をモニタリングし、D−プシコースの結晶成長が止まるか、またはD−プシコース溶液の濃度がそれ以上変化しない場合に溶液の温度を低くすることによって、前記濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、請求項1に記載の方法。
【請求項7】
前記結晶化させる段階における結晶化の進行をモニタリングし、前記溶液中のD−プシコースが過飽和レベル以上に濃縮された場合に前記濃縮されたD−プシコース溶液より低い濃度のD−プシコース溶液を添加することによって、該濃縮されたD−プシコース溶液を準安定域の過飽和状態に維持する、請求項1に記載の方法。
【請求項8】
前記結晶化させる段階における準安定域の過飽和状態が、飽和濃度から、該飽和濃度からさらに約6%(g/g溶液)高い濃度までの範囲に存在する、請求項1に記載の方法。
【図1】


【図2】


【図3】


【図4】


【図5】




【図2】


【図3】


【図4】


【図5】


【公開番号】特開2011−206054(P2011−206054A)
【公開日】平成23年10月20日(2011.10.20)
【国際特許分類】
【外国語出願】
【出願番号】特願2011−66870(P2011−66870)
【出願日】平成23年3月25日(2011.3.25)
【出願人】(508139664)シージェイ チェイルジェダン コーポレーション (12)
【Fターム(参考)】
【公開日】平成23年10月20日(2011.10.20)
【国際特許分類】
【出願番号】特願2011−66870(P2011−66870)
【出願日】平成23年3月25日(2011.3.25)
【出願人】(508139664)シージェイ チェイルジェダン コーポレーション (12)
【Fターム(参考)】
[ Back to top ]

