HER−3関連疾患を治療または予防するための物質および方法
本明細書には、HER−3に結合する第1の薬剤を、HERファミリ−の別のメンバ−に結合するおよび/またはそれを阻害する第2の薬剤と併用して投与することによって、HER−3関連疾患を有する被験者を治療するための物質および方法が記載されている。第1および第2の薬剤は、例えば、抗原結合タンパク質などの生物学的薬剤、または小分子チロシンキナ−ゼ阻害剤とすることができる。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合するものであり、そして第2の薬剤がHERファミリ−の別のメンバ−に結合するおよび/またはその活性を阻害するものである、方法。
【請求項2】
第1の薬剤が、HER−3に結合する小分子化合物または抗原結合タンパク質である、請求項1記載の方法。
【請求項3】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、
配列番号236、251、252、および256からなる群より選択されるCDRH1;配列番号258、278、280、および282からなる群より選択されるCDRH2;および配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含む重鎖アミノ酸配列;および
配列番号320、334、337、および340からなる群より選択されるCDRL1;配列番号343、356、351、および344からなる群より選択されるCDRL2;および配列番号360、381、385、および387からなる群より選択されるCDRL3を含む軽鎖アミノ酸配列;
を含んでなる、請求項1記載の方法。
【請求項4】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(a)配列番号236、251、252、および256に示されるCDRH1;(b)配列番号258、278、280、および282に示されるCDRH2;および(c)配列番号283、285、309、313、および315に示されるCDRH3からなる群より選択されるCDRの少なくとも1つを含む重鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項5】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(d)配列番号320、334、337、および340に示されるCDRL1;(e)配列番号343、356、351、および344に示されるCDRL2;および(f)配列番号360、381、385、および387に示されるCDRL3からなる群より選択されるCDRの少なくとも1つを含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項6】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(a)配列番号236、251、252、および256に示されるCDRH1;(b)配列番号258、278、280、および282に示されるCDRH2;および(c)配列番号283、285、309、313、および315に示されるCDRH3からなる群より選択されるCDRの少なくとも1つを含む重鎖アミノ酸配列と、(d)配列番号320、334、337、および340に示されるCDRL1;(e)配列番号343、356、351、および344に示されるCDRL2;および(f)配列番号360、381、385、および387に示されるCDRL3からなる群より選択されるCDRの少なくとも1つを含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項7】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号236、251、252、および256からなる群より選択されるCDRH1、配列番号258、278、280、および282からなる群より選択されるCDRH2、および配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含む重鎖アミノ酸配列、または配列番号320、334、337、および340からなる群より選択されるCDRL1、配列番号343、356、351、および344からなる群より選択されるCDRL2、および配列番号360、381、385、および387からなる群より選択されるCDRL3を含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項8】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42、54、70、92、および96からなる群より選択される重鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項9】
前記抗原結合タンパク質が配列番号44、56、72、94、および98からなる群より選択される軽鎖アミノ酸配列を含んでなる、請求項8記載の方法。
【請求項10】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42、54、70、92、および96からなる群より選択される重鎖アミノ酸配列と、配列番号44、56、72、94、および98からなる群より選択される軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項11】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項12】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号54の重鎖アミノ酸配列および配列番号56の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項13】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号70の重鎖アミノ酸配列および配列番号72の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項14】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含んでなる、請求項1記載の方法。
【請求項15】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号360、381、385、および387からなる群より選択されるCDRL3を含んでなる、請求項1記載の方法。
【請求項16】
前記抗原結合タンパク質がHER−3の細胞外ドメインに対して向けられたものである、請求項3〜15のいずれか一項記載の方法。
【請求項17】
前記抗原結合タンパク質のHER−3への結合がHER−3介在シグナル伝達を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項18】
前記抗原結合タンパク質のHER−3への結合がHER−3リン酸化を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項19】
前記抗原結合タンパク質のHER−3への結合が細胞増殖を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項20】
前記抗原結合タンパク質のHER−3への結合が細胞移動を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項21】
前記抗原結合タンパク質のHER−3への結合がHER−3のダウンレギュレ−ションを増加させる、請求項3〜20のいずれか一項記載の方法。
【請求項22】
HER−3に結合する前記抗原結合タンパク質が抗体である、請求項3〜20のいずれか一項記載の方法。
【請求項23】
前記抗体がモノクロ−ナル抗体、ポリクロ−ナル抗体、組換え抗体、ヒト化抗体、ヒト抗体、キメラ抗体、多重特異性抗体、またはその抗体フラグメントである、請求項22記載の方法。
【請求項24】
前記抗体フラグメントがFabフラグメント、Fab’フラグメント、F(ab’)2フラグメント、Fvフラグメント、ダイアボディ、または一本鎖抗体分子である、請求項23記載の方法。
【請求項25】
前記抗体がIgG1−、IgG2−、IgG3−またはIgG4−タイプのものである、請求項22記載の方法。
【請求項26】
第1の薬剤がHER−3に結合する抗原結合タンパク質であり、その抗原結合タンパク質がエフェクタ−グル−プに結合されている、請求項1記載の方法。
【請求項27】
前記エフェクタ−グル−プが放射性同位元素もしくは放射性核種、毒素、または治療薬もしくは化学療法薬グル−プである、請求項26記載の方法。
【請求項28】
前記治療薬もしくは化学療法薬グル−プがカリケアマイシン、アウリスタチン−PE、ゲルダナマイシン、メイタンシンおよびそれらの誘導体からなる群より選択される、請求項27記載の方法。
【請求項29】
第2の薬剤が小分子化合物または抗原結合タンパク質である、請求項1〜15のいずれか一項記載の方法。
【請求項30】
第2の薬剤がトラスツズマブである、請求項29記載の方法。
【請求項31】
第2の薬剤がラパチニブおよびネラチニブからなる群より選択される、請求項29記載の方法。
【請求項32】
第2の薬剤がパニツムマブである、請求項29記載の方法。
【請求項33】
第2の薬剤がエルロチニブである、請求項29記載の方法。
【請求項34】
第2の薬剤がセツキシマブである、請求項29記載の方法。
【請求項35】
第2の薬剤がペルツズマブである、請求項29記載の方法。
【請求項36】
第2の薬剤がア−ビタックスである、請求項29記載の方法。
【請求項37】
第2の薬剤がT−DM1である、請求項29記載の方法。
【請求項38】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなり、そして第2の薬剤がエルロチニブ、ラパチニブ、ネラチニブおよびペルツズマブからなる群より選択される、方法。
【請求項39】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなり、そして第2の薬剤がトラスツズマブ、T−DM1、パニツムマブ、ア−ビタックス、およびセツキシマブからなる群より選択される、方法。
【請求項40】
場合により、さらなる治療薬および/または放射線療法を投与することを含む、請求項1記載の方法。
【請求項41】
さらなる治療薬が抗腫瘍薬である、請求項40記載の方法。
【請求項42】
抗腫瘍薬が抗腫瘍抗体または化学療法薬である、請求項40記載の方法。
【請求項43】
化学療法薬がカペシタビン、アントラサイクリン、ドキソルビシン、シクロホスファミド、パクリタキセル、ドセタキセル、シスプラチン、ゲムシタビン、およびカルボプラチンからなる群より選択される、請求項42記載の方法。
【請求項44】
第1の薬剤と第2の薬剤が静脈内、皮下、筋肉内または経口投与により投与される、請求項29記載の方法。
【請求項45】
前記疾患が過剰増殖性疾患である、請求項29記載の方法。
【請求項46】
前記疾患が乳癌、卵巣癌、前立腺癌、結腸癌、腎癌、肺癌、膵臓癌、類表皮癌、線維肉腫、黒色腫、上咽頭癌、および扁平上皮細胞癌からなる群より選択される、請求項29記載の方法。
【請求項47】
第1の薬剤を約1〜約20mg/kg体重の用量で6週間に少なくとも1回投与することを含む、請求項29記載の方法。
【請求項48】
第2の薬剤を約1〜約20mg/kg体重の用量で6週間に少なくとも1回投与することを含む、請求項29記載の方法。
【請求項49】
投与に先立って、HER−3と関連した疾患を有する被験者を選択するための予測マ−カ−の解析を含む方法を用いることをさらに含む、請求項29記載の方法。
【請求項50】
投与後、治療結果をモニタリングすることをさらに含む、請求項29記載の方法。
【請求項1】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合するものであり、そして第2の薬剤がHERファミリ−の別のメンバ−に結合するおよび/またはその活性を阻害するものである、方法。
【請求項2】
第1の薬剤が、HER−3に結合する小分子化合物または抗原結合タンパク質である、請求項1記載の方法。
【請求項3】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、
配列番号236、251、252、および256からなる群より選択されるCDRH1;配列番号258、278、280、および282からなる群より選択されるCDRH2;および配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含む重鎖アミノ酸配列;および
配列番号320、334、337、および340からなる群より選択されるCDRL1;配列番号343、356、351、および344からなる群より選択されるCDRL2;および配列番号360、381、385、および387からなる群より選択されるCDRL3を含む軽鎖アミノ酸配列;
を含んでなる、請求項1記載の方法。
【請求項4】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(a)配列番号236、251、252、および256に示されるCDRH1;(b)配列番号258、278、280、および282に示されるCDRH2;および(c)配列番号283、285、309、313、および315に示されるCDRH3からなる群より選択されるCDRの少なくとも1つを含む重鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項5】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(d)配列番号320、334、337、および340に示されるCDRL1;(e)配列番号343、356、351、および344に示されるCDRL2;および(f)配列番号360、381、385、および387に示されるCDRL3からなる群より選択されるCDRの少なくとも1つを含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項6】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ(a)配列番号236、251、252、および256に示されるCDRH1;(b)配列番号258、278、280、および282に示されるCDRH2;および(c)配列番号283、285、309、313、および315に示されるCDRH3からなる群より選択されるCDRの少なくとも1つを含む重鎖アミノ酸配列と、(d)配列番号320、334、337、および340に示されるCDRL1;(e)配列番号343、356、351、および344に示されるCDRL2;および(f)配列番号360、381、385、および387に示されるCDRL3からなる群より選択されるCDRの少なくとも1つを含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項7】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号236、251、252、および256からなる群より選択されるCDRH1、配列番号258、278、280、および282からなる群より選択されるCDRH2、および配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含む重鎖アミノ酸配列、または配列番号320、334、337、および340からなる群より選択されるCDRL1、配列番号343、356、351、および344からなる群より選択されるCDRL2、および配列番号360、381、385、および387からなる群より選択されるCDRL3を含む軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項8】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42、54、70、92、および96からなる群より選択される重鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項9】
前記抗原結合タンパク質が配列番号44、56、72、94、および98からなる群より選択される軽鎖アミノ酸配列を含んでなる、請求項8記載の方法。
【請求項10】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42、54、70、92、および96からなる群より選択される重鎖アミノ酸配列と、配列番号44、56、72、94、および98からなる群より選択される軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項11】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項12】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号54の重鎖アミノ酸配列および配列番号56の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項13】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号70の重鎖アミノ酸配列および配列番号72の軽鎖アミノ酸配列を含んでなる、請求項1記載の方法。
【請求項14】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号283、285、309、313、および315からなる群より選択されるCDRH3を含んでなる、請求項1記載の方法。
【請求項15】
第1の薬剤が、HER−3に結合する抗原結合タンパク質であり、かつ配列番号360、381、385、および387からなる群より選択されるCDRL3を含んでなる、請求項1記載の方法。
【請求項16】
前記抗原結合タンパク質がHER−3の細胞外ドメインに対して向けられたものである、請求項3〜15のいずれか一項記載の方法。
【請求項17】
前記抗原結合タンパク質のHER−3への結合がHER−3介在シグナル伝達を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項18】
前記抗原結合タンパク質のHER−3への結合がHER−3リン酸化を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項19】
前記抗原結合タンパク質のHER−3への結合が細胞増殖を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項20】
前記抗原結合タンパク質のHER−3への結合が細胞移動を減少させる、請求項3〜15のいずれか一項記載の方法。
【請求項21】
前記抗原結合タンパク質のHER−3への結合がHER−3のダウンレギュレ−ションを増加させる、請求項3〜20のいずれか一項記載の方法。
【請求項22】
HER−3に結合する前記抗原結合タンパク質が抗体である、請求項3〜20のいずれか一項記載の方法。
【請求項23】
前記抗体がモノクロ−ナル抗体、ポリクロ−ナル抗体、組換え抗体、ヒト化抗体、ヒト抗体、キメラ抗体、多重特異性抗体、またはその抗体フラグメントである、請求項22記載の方法。
【請求項24】
前記抗体フラグメントがFabフラグメント、Fab’フラグメント、F(ab’)2フラグメント、Fvフラグメント、ダイアボディ、または一本鎖抗体分子である、請求項23記載の方法。
【請求項25】
前記抗体がIgG1−、IgG2−、IgG3−またはIgG4−タイプのものである、請求項22記載の方法。
【請求項26】
第1の薬剤がHER−3に結合する抗原結合タンパク質であり、その抗原結合タンパク質がエフェクタ−グル−プに結合されている、請求項1記載の方法。
【請求項27】
前記エフェクタ−グル−プが放射性同位元素もしくは放射性核種、毒素、または治療薬もしくは化学療法薬グル−プである、請求項26記載の方法。
【請求項28】
前記治療薬もしくは化学療法薬グル−プがカリケアマイシン、アウリスタチン−PE、ゲルダナマイシン、メイタンシンおよびそれらの誘導体からなる群より選択される、請求項27記載の方法。
【請求項29】
第2の薬剤が小分子化合物または抗原結合タンパク質である、請求項1〜15のいずれか一項記載の方法。
【請求項30】
第2の薬剤がトラスツズマブである、請求項29記載の方法。
【請求項31】
第2の薬剤がラパチニブおよびネラチニブからなる群より選択される、請求項29記載の方法。
【請求項32】
第2の薬剤がパニツムマブである、請求項29記載の方法。
【請求項33】
第2の薬剤がエルロチニブである、請求項29記載の方法。
【請求項34】
第2の薬剤がセツキシマブである、請求項29記載の方法。
【請求項35】
第2の薬剤がペルツズマブである、請求項29記載の方法。
【請求項36】
第2の薬剤がア−ビタックスである、請求項29記載の方法。
【請求項37】
第2の薬剤がT−DM1である、請求項29記載の方法。
【請求項38】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなり、そして第2の薬剤がエルロチニブ、ラパチニブ、ネラチニブおよびペルツズマブからなる群より選択される、方法。
【請求項39】
第1の薬剤と第2の薬剤を被験者に投与することを含んでなる、被験者においてHER−3と関連した疾患を治療または予防する方法であって、第1の薬剤がHER−3に結合する抗原結合タンパク質であり、かつ配列番号42の重鎖アミノ酸配列および配列番号44の軽鎖アミノ酸配列を含んでなり、そして第2の薬剤がトラスツズマブ、T−DM1、パニツムマブ、ア−ビタックス、およびセツキシマブからなる群より選択される、方法。
【請求項40】
場合により、さらなる治療薬および/または放射線療法を投与することを含む、請求項1記載の方法。
【請求項41】
さらなる治療薬が抗腫瘍薬である、請求項40記載の方法。
【請求項42】
抗腫瘍薬が抗腫瘍抗体または化学療法薬である、請求項40記載の方法。
【請求項43】
化学療法薬がカペシタビン、アントラサイクリン、ドキソルビシン、シクロホスファミド、パクリタキセル、ドセタキセル、シスプラチン、ゲムシタビン、およびカルボプラチンからなる群より選択される、請求項42記載の方法。
【請求項44】
第1の薬剤と第2の薬剤が静脈内、皮下、筋肉内または経口投与により投与される、請求項29記載の方法。
【請求項45】
前記疾患が過剰増殖性疾患である、請求項29記載の方法。
【請求項46】
前記疾患が乳癌、卵巣癌、前立腺癌、結腸癌、腎癌、肺癌、膵臓癌、類表皮癌、線維肉腫、黒色腫、上咽頭癌、および扁平上皮細胞癌からなる群より選択される、請求項29記載の方法。
【請求項47】
第1の薬剤を約1〜約20mg/kg体重の用量で6週間に少なくとも1回投与することを含む、請求項29記載の方法。
【請求項48】
第2の薬剤を約1〜約20mg/kg体重の用量で6週間に少なくとも1回投与することを含む、請求項29記載の方法。
【請求項49】
投与に先立って、HER−3と関連した疾患を有する被験者を選択するための予測マ−カ−の解析を含む方法を用いることをさらに含む、請求項29記載の方法。
【請求項50】
投与後、治療結果をモニタリングすることをさらに含む、請求項29記載の方法。
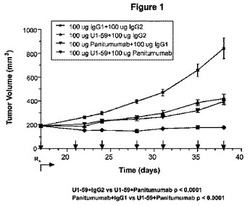
【図1】


【図2】


【図6A】


【図6B】


【図6C】


【図6D】


【図19】


【図3】


【図4】


【図5】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図20】




【図2】


【図6A】


【図6B】


【図6C】


【図6D】


【図19】


【図3】


【図4】


【図5】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図20】


【公表番号】特表2013−510868(P2013−510868A)
【公表日】平成25年3月28日(2013.3.28)
【国際特許分類】
【出願番号】特願2012−538994(P2012−538994)
【出願日】平成22年11月12日(2010.11.12)
【国際出願番号】PCT/US2010/056430
【国際公開番号】WO2011/060206
【国際公開日】平成23年5月19日(2011.5.19)
【出願人】(507107992)ウー3・フアルマ・ゲー・エム・ベー・ハー (5)
【氏名又は名称原語表記】U3 PHARMA
【出願人】(512121738)
【Fターム(参考)】
【公表日】平成25年3月28日(2013.3.28)
【国際特許分類】
【出願日】平成22年11月12日(2010.11.12)
【国際出願番号】PCT/US2010/056430
【国際公開番号】WO2011/060206
【国際公開日】平成23年5月19日(2011.5.19)
【出願人】(507107992)ウー3・フアルマ・ゲー・エム・ベー・ハー (5)
【氏名又は名称原語表記】U3 PHARMA
【出願人】(512121738)

【Fターム(参考)】
[ Back to top ]

