IKK−Bセリン・スレオニンプロテインキナーゼのチオフェン阻害剤
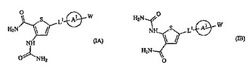
本発明は、(a)式(IA)もしくは(IB)

(式中、L1、A1およびWは、本明細書中で定義した通りである)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。該化合物は、IKKβ阻害剤として有用である。したがって、該化合物は、例えば自己免疫疾患および炎症性疾患の治療において、医薬として使用することができる。

(式中、L1、A1およびWは、本明細書中で定義した通りである)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。該化合物は、IKKβ阻害剤として有用である。したがって、該化合物は、例えば自己免疫疾患および炎症性疾患の治療において、医薬として使用することができる。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、一連のアミノ酸誘導体、それを含む組成物、その製造方法、およびIKK阻害剤としての医薬におけるその使用に関する。
【背景技術】
【0002】
(発明の背景)
多くの炎症性遺伝子の発現は、転写活性化因子である核因子(nuclear factor)κB(NF-κB)によって制御されている。こうした転写因子は、その発見以来、慢性および急性の炎症性疾患において、中枢的な役割を果たしているのではないかと思われている。現在では、NF-κBの異常な調節はまた、自己免疫疾患および種々の種類の癌の基礎にもなっていると見られている。
【0003】
その活性がNF-κBの活性化に依存する物質としては、腫瘍壊死因子TNF-α、インターロイキン(IL)-6、IL-8およびIL-1βなどのサイトカイン;接着分子E-セレクチン、細胞間接着分子(intercellular adhesion molecule)(ICAM)-1および血管細胞接着分子(vascular cell adhesion molecule)(VCAM)-1;ならびに酵素一酸化窒素シンターゼ(nitric oxide synthase)(NOS)およびシクロオキシゲナーゼ(cyclooxygenase)(COX)-2が挙げられる。NF-κBは、通常は、IκB阻害タンパク質ファミリーのメンバーとの不活性な複合体として、刺激されていない細胞の細胞質中に存在している。しかしながら、細胞活性化時には、IκBは、IκBキナーゼ(IκB kinase)(IKK)によってリン酸化され、その後に分解される。その後、遊離したNF-κBは、核に移行し、そこで炎症性遺伝子の発現を媒介する。
【0004】
IκBファミリーの3つの古典的なメンバーは、IκBα、IκBβおよびIκBεである。これらはすべて、分解され得る前に、2つの重要なセリン残基のリン酸化を必要とする。2つの主要な酵素IKK-αおよびIKK-βが、IκBのリン酸化の原因であるようである。これらの酵素のいずれのドミナントネガティブ(dominant-negative)(DN)型(重要なキナーゼドメイン残基の変異によって、ATPに結合することができない)も、TNF-α、IL-1βおよびLPSによるNF-κBの活性化を抑制することがわかっている。重要なことには、IKK-β DNは、IKK-α DNよりも、はるかに強力な阻害剤であることがわかっている(Zandi E, Cell, 1997, 91, 243)。さらに、IKK-αおよびIKK-βの欠損したマウスの作製により、炎症誘発性の刺激によるNF-κBの活性化が起こるためにはIKK-βが必要であることが確証され、IKK-βがこの経路において主要な役割を果たしていることを示唆する生化学的データが確証されている。実際に、IKK-αは、こうした刺激によるNF-κBの活性化に不要であることが実証されている(Tanaka M, Immunity 1999, 10, 421)。
【0005】
したがって、IKK-βの阻害は、免疫機能の調節のための、したがって自己免疫疾患の治療用薬物の開発のための、潜在的に魅力的な標的となる。例えば、II型糖尿病の治療に関しては、IKK-βの組織特異的欠失またはIKK-βに対する薬理学的ターゲティングなどの方法によってNF-κBシグナル伝達経路を破壊することで、インスリン抵抗性を弱めることができることが示されている(Shoelson Sら, Gastroenterology 2007, 132, 2169)。
【0006】
現在、IKKアイソフォーム、特にIKK-βの強力かつ選択的な阻害剤である一群の化合物が同定されている。したがって、これらの化合物は、例えば、IKKの活性亢進と関連する容態などの種々の増殖性疾患状態、およびNF-κBカスケードによって調節される疾患の治療において、医薬として有用であり得る。
【発明の概要】
【発明が解決しようとする課題】
【0007】
α-一置換グリシンエステルモチーフを細胞内酵素または細胞質受容体のモジュレーターに結合させて、カルボン酸の加水分解生成物の細胞内蓄積の利益を得るという一般概念が、WO 2006/117567に記述されている。しかしながら、この公報は、α,α-二置換グリシンエステルの結合体が、細胞内カルボキシルエステラーゼによって加水分解され得ることを示唆するものではない。細胞内カルボキシルエステラーゼ(carboxyl esterases)、主としてhCE-1、hCE-2およびhCE-3の、α,α-二置換グリシンエステルを加水分解する能力は、これまでは研究されてこなかったようである。
【課題を解決するための手段】
【0008】
(発明の簡単な説明)
本発明は、(a)式(IA)もしくは(IB):
【0009】
【化1】

【0010】
〔式中、
・L1は、C1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表すか、またはL1は、基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-もしくは-(CH2)mNR1(CH2)n-(式中、R1は、C1〜4アルキルであり、mおよびnは、同一であるか、もしくは異なっており、0、1、2、3もしくは4である)を表し;
・環A1は、さらなるC6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル(carbocyclyl)基または5〜10員のヘテロシクリル基に縮合していてもよい、C6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基であり;
・Wは、式:
【0011】
【化2】

【0012】
{式中、
・L2は、基-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、結合、またはC1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表し;
・Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し;
・A2は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基または5〜6員のヘテロアリール基を表し;
・Hetは、-O-、-S-または-NR’-(式中、R’は、水素もしくは非置換C1〜2アルキルを表す)を表し;
・xは、0または1であり;
・Alk1は、結合、またはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基、または基-A3-Alk4-(式中、A3は、縮合していないか、もしくはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基もしくは5〜6員のヘテロアリール基を表し、Alk4は、結合、もしくはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基を表す)を表し;
・Rは、式(X1)、(X2)、(Y1)または(Y2):
【0013】
【化3】

【0014】
[式中、
・R2は、基-COOH、または1種以上の細胞内カルボキシルエステラーゼ酵素によって-COOH基に加水分解され得るエステル基であり;
・R3は、水素原子またはC1〜4アルキル基を表し;
・R4、R7およびR8は、同一であるか、または異なっており、それぞれ天然α-アミノ酸または非天然α-アミノ酸のα-置換基を表すか、あるいはR7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和スピロシクロアルキル環またはヘテロシクリル環を形成し;
・R5は、水素原子、またはC1〜6アルキル基、C3〜7カルボシクリル基、C6〜10アリール基もしくは5〜6員のヘテロアリール基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくはC1〜6アルキル基である)を表し;
・環Dは、5〜6員のヘテロシクリル基であり、ここでR2は、示された環窒素に隣接する環炭素に結合しており;R7は、存在する場合、R2と同じ環炭素に結合しており;環Dは、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合していてもよい]
の基を表す(ただし、Rが式(Y2)の基を表し、かつ環Dがフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合している場合、波線によって横切られた示された結合は、環Dまたは前記第二の環の環原子からのものであってもよい)}
の基を表し;
式中、別段記載しない限り、
・R1、R2、R3、R4、R5、R6、R7、R8、L1、Alk1、Alk2、Alk3およびAlk4における、任意のアルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、同一であるか、または異なっており、それぞれ置換されていないか、または1個、2個もしくは3個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン原子ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、-SR’基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択され;
・A1、A2、A3、DおよびR5における、任意のアリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分は、同一であるか、または異なっており、それぞれ置換されていないか、またはハロゲン原子ならびにシアノ基、ニトロ基、C1〜4アルキル基、C1〜4アルコキシ基、C2〜4アルケニル基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、C1〜4ヒドロキシアルキル基、-SR’基および-NR’R’’基(式中、R’およびR’’は、それぞれ同一であるか、もしくは異なっており、水素もしくは非置換C1〜4アルキルを表す)から選択される1個、2個、3個もしくは4個の非置換置換基によって、もしくは式-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBもしくは-NRACONRARB(式中、RAおよびRBは、同一であるか、もしくは異なっており、非置換C1〜6アルキル、C3〜6シクロアルキル、非縮合フェニル、もしくは非縮合の5〜6員のヘテロアリールを表すか、もしくはRAおよびRBは、同一の窒素原子に結合している場合、非縮合の5員もしくは6員のヘテロシクリル基を形成する)の置換基から選択される1個、2個、3個もしくは4個の非置換置換基によって、置換されている〕
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0015】
本発明の化合物は、細胞内カルボキシルエステラーゼによって加水分解され得るアミノ酸モチーフまたはアミノ酸エステルモチーフを含む。該化合物はまた、最後がアミノ酸モチーフまたはアミノ酸エステルモチーフで終わる分子の側鎖に保持された環式基から分子のチオフェン環母核を分離するリンカー基も含む。驚くべきことに、この親油性のアミノ酸モチーフまたはアミノ酸エステルモチーフとリンカー基との組み合わせを有する本発明の化合物は、IKKアイソフォーム、特にIKK-βの強力かつ選択的な阻害剤である。
【0016】
本発明の好ましい化合物は、細胞内カルボキシルエステラーゼによって加水分解され得るアミノ酸エステルモチーフを含む化合物である。こうした化合物は、細胞膜を容易に通過することができ、その後細胞内カルボキシルエステラーゼによって、酸に加水分解され得る。極性の加水分解生成物は、細胞膜を同様に容易には通過しないため、細胞内に蓄積する。そのため、該化合物のIKK活性は、長期にわたり得、細胞内で高まり得る。したがって、この蓄積の効果は、本発明の化合物の細胞内IKK活性の、該化合物の細胞外活性に対する増大をもたらし得る。
【0017】
さらに、Rが式(X1)または(Y1)の基である本発明の化合物は、単球内に選択的に蓄積することがわかっている。したがって、こうした本発明の化合物は、全身投与が望まれる場合、有利に使用することができる。なぜならば、該化合物は、プレシステミック代謝(pre-systemic metabolism)に対してあまり感受性がなく、したがってインタクトで(in tact)標的組織に到達し得る(その後、標的細胞の内部で酸の生成物に変換される)からである。単球細胞株における優先的な蓄積は、他の隣接する細胞に優先して単球に集中した、患者に投与された1用量の化合物の、IKK阻害効果をもたらし得る。したがって、この選択性は、例えば癌および自己免疫疾患の治療において、単核球細胞を標的とするために使用された場合、本発明の化合物と関連する治療濃度域を向上させ得る。したがって、例えば、標的ではない非単核球細胞のIKK阻害と関連する副作用を減少させることができる。
【0018】
逆に、局所投与が望まれる場合、Rが式(X2)または(Y2)の基である本発明の化合物を使用することが有利であり得る。かかる本発明の化合物は、単球選択性を示さず、典型的にはエステル開裂がより急速に起こる。この急速なエステル開裂速度は、全身的な曝露、および結果としての望まれない副作用を減少させることに関して、有利であり得る。
【0019】
本発明の化合物は、式(IA)もしくは(IB)の化合物もしくはその互変異性体、またはその薬学的に許容される塩であることが好ましい。
【0020】
本発明はまた、ヒトまたは動物の身体の治療方法に使用するための、上に定義した化合物も提供する。
【0021】
本発明は、さらに、上に定義した化合物および薬学的に許容される担体または希釈剤を含む、医薬組成物を提供する。
【0022】
別の態様において、本発明は、IKK酵素によって媒介される障害の治療に使用するための、上に定義した化合物を供給する。本発明はまた、IKK酵素によって媒介される障害の治療または予防に使用するための医薬の製造における、上に定義した化合物の使用も提供する。これらの態様において、IKK酵素は、好ましくはIKK-βである。
【0023】
さらに、本発明は、患者におけるIKKによって媒介される障害の治療方法または予防方法を提供し、該方法は、有効量の上に定義した化合物を前記患者に投与することを含む。
【発明を実施するための形態】
【0024】
(発明の詳細な説明)
上記定義は分子量の高い分子を含む可能性があるが、医薬品化学のプラクティスの一般的な原則に従って、本発明が関係する化合物は、600以下の分子量を有するべきであることが好ましい。
【0025】
好ましくは、R1、R2、R3、R4、R5、R6、R7、R8、L1、L2、L3、Alk1、Alk2、Alk3およびAlk4における、アルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、置換されていないか、または1個、2個もしくは3個、好ましくは1個もしくは2個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン、C1〜4アルキル、C2〜4アルケニル、C1〜4アルコキシ、ヒドロキシル、C1〜4ハロアルキル、C2〜4ハロアルケニル、C1〜4ハロアルキルオキシおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)から選択される。より好ましい置換基は、ハロゲン、非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)である。例えば、特に好ましい置換基としては、非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)が挙げられる。
【0026】
上記のアルキル部分、アルキレン部分、アルケニレン部分およびアルキニレン部分が2個または3個の置換基によって置換されている場合、2個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることが好ましい。1個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることがより好ましい。
【0027】
本明細書中で使用される場合、C1〜6アルキル基またはC1〜6アルキル部分は、1〜6個の炭素原子を含む、直鎖状または分枝状のアルキル基またはアルキル部分、例えば1〜4個の炭素原子を含む、C1〜4アルキル基またはC1〜4アルキル部分である。C1〜4アルキル基の例としては、メチル、エチル、n-プロピル、i-プロピル、n-ブチル、i-ブチルおよびt-ブチルが挙げられる。誤解を避けるためであるが、1個の基に2個のアルキル部分が存在している場合、それらのアルキル部分は、同一であってもよく、異なっていてもよい。
【0028】
本明細書中で使用される場合、C2〜6アルケニル基またはC2〜6アルケニル部分は、適用可能である場合、EまたはZのいずれかの立体化学の少なくとも1つの二重結合を有し、2〜6個の炭素原子を含む、直鎖状または分枝状のアルケニル基またはアルケニル部分、例えば-CH=CH2または-CH2-CH=CH2、-CH2-CH2-CH=CH2、-CH2-CH=CH-CH3、-CH=C(CH3)-CH3および-CH2-C(CH3)=CH2などの2〜4個の炭素原子を含む、C2〜4アルケニル基またはC2〜4アルケニル部分である。誤解を避けるためであるが、1個の基に2個のアルケニル部分が存在している場合、それらのアルケニル部分は、同一であってもよく、異なっていてもよい。
【0029】
本明細書中で使用される場合、C2〜6アルキニル基またはC2〜6アルキニル部分は、2〜6個の炭素原子を含む、直鎖状または分枝状のアルキニル基またはアルキニル部分、例えば2〜4個の炭素原子を含む、C2〜4アルキニル基またはC2〜4アルキニル部分である。例示的なアルキニル基としては、-C≡CHまたは-CH2-C≡CH、ならびに1-ブチニルおよび2-ブチニル、2-メチル-2-プロピニル、2-ペンチニル、3-ペンチニル、4-ペンチニル、2-ヘキシニル、3-ヘキシニル、4-ヘキシニルおよび5-ヘキシニルが挙げられる。誤解を避けるためであるが、1個の基に2個のアルキニル部分が存在している場合、それらのアルキニル部分は、同一であってもよく、異なっていてもよい。
【0030】
本明細書中で使用される場合、C1〜6アルキレン基またはC1〜6アルキレン部分は、直鎖状または分枝状のアルキレン基またはアルキレン部分、例えばC1〜4アルキレン基またはC1〜4アルキレン部分である。例としては、メチレン基およびメチレン部分、n-エチレン基およびn-エチレン部分、n-プロピレン基およびn-プロピレン部分ならびに-C(CH3)2-基および-C(CH3)2-部分が挙げられる。
【0031】
本明細書中で使用される場合、C2〜6アルケニレン基またはC2〜6アルケニレン部分は、直鎖状または分枝状のアルケニレン基またはアルケニレン部分、例えばC2〜4アルケニレン基またはC2〜4アルケニレン部分である。例としては、-CH=CH-、-CH=CH-CH2-、-CH2-CH=CH-および-CH=CH-CH=CH-が挙げられる。
【0032】
本明細書中で使用される場合、C2〜6アルキニレン基またはC2〜6アルキニレン部分は、直鎖状または分枝状のアルキニレン基またはアルキニレン部分、例えばC2〜4アルキニレン基またはC2〜4アルキニレン部分である。例としては、-C≡C-、-C≡C-CH2-および-CH2-C≡C-が挙げられる。
【0033】
本明細書中で使用される場合、ハロゲン原子は、塩素、フッ素、臭素またはヨウ素である。
【0034】
本明細書中で使用される場合、C1〜6アルコキシ基またはC2〜6アルケニルオキシ基は、典型的には、それぞれ酸素原子に結合している前記C1〜6アルキル(例えばC1〜4アルキル)基または前記C2〜6アルケニル(例えばC2〜4アルケニル)基である。
【0035】
ハロアルキル基、ハロアルケニル基、ハロアルコキシ基またはハロアルケニルオキシ基は、典型的には、それぞれ、1個以上の前記ハロゲン原子によって置換されている前記アルキル基、アルケニル基、アルコキシ基またはアルケニルオキシ基である。典型的には、アルキル基、アルケニル基、アルコキシ基またはアルケニルオキシ基が、1個、2個または3個の前記ハロゲン原子によって置換されている。好ましいハロアルキル基およびハロアルコキシ基としては、-CX3および-OCX3(式中、Xは、前記ハロゲン原子、例えば塩素およびフッ素である)などのペルハロアルキル基およびペルハロアルコキシ基が挙げられる。
【0036】
本明細書中で使用される場合、C1〜4アルキルチオ基またはC2〜4アルケニルチオ基は、典型的には、それぞれ、硫黄原子に結合している前記C1〜4アルキル基またはC2〜4アルケニル基、例えば-S-CH3である。
【0037】
本明細書中で使用される場合、C1〜4ヒドロキシアルキル基は、1個以上のヒドロキシ基によって置換されたC1〜4アルキル基である。典型的には、C1〜4アルキル基が、1個、2個または3個のヒドロキシ基によって置換されている。好ましくは、C1〜4アルキル基が、単一のヒドロキシ基によって置換されている。
【0038】
本明細書中で使用される場合、C6〜10アリール基またはC6〜10アリール部分は、6〜10個の炭素原子を有する単環式6〜10員の芳香族炭化水素環である。フェニルが好ましい。
【0039】
本明細書中で使用される場合、C6〜10アリール基またはC6〜10アリール部分は、縮合していないことが好ましい。しかしながら、C6〜10アリール基またはC6〜10アリール部分がさらなるC6〜10アリール基、5〜10員のヘテロシクリル基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合している場合、該基または部分は、さらなるフェニル基、5〜6員のヘテロシクリル基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基に縮合していることが好ましく、5〜6員のヘテロアリール基または5〜6員のヘテロシクリル基に縮合していることがより好ましい。該基または部分は、5〜6員のヘテロシクリル基に縮合していることが最も好ましい。この場合、好ましい5〜6員のヘテロシクリル基としては、テトラヒドロフラニル、テトラヒドロチエニル、ピロリジニル、ジチオラニル、ジオキソラニル、オキサゾリジニル、イミダゾリル、イソオキサゾリジニル、イミダゾリジニル、ピラゾリジニル、チオキソラニル、チアゾリジニルおよびイソチアゾリジニルが挙げられ、より好ましくはオキサゾリジニル、イミダゾリジニル、チアゾリジニル、チオキソラニル、ジオキソラニルおよびジチオラニルが挙げられ、最も好ましくはジオキソラニルが挙げられる。
【0040】
本明細書中で使用される場合、5〜10員のヘテロアリール基またはヘテロアリール部分は、O、SおよびNから選択される少なくとも1個のヘテロ原子、例えば1個、2個、3個または4個のヘテロ原子を含む、5員環または6員環などの単環式5〜10員の芳香環である。環が4個のヘテロ原子を含む場合、これらのヘテロ原子はすべて窒素原子であることが好ましい。例としては、チエニル基、フリル基、ピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、チアジアゾリル基、オキサジアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基、ピラジニル基、トリアジニル基およびテトラゾリル基が挙げられる。チエニル基、ピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基およびピラジニル基、例えばピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基およびピラジニル基が好ましい。より好ましい基は、チエニル、ピリジニル、ピリダジニル、ピリミジニル、ピラジニル、ピロリルおよびトリアジニル、例えばピリジニル、ピリダジニル、ピリミジニル、ピラジニル、ピロリルおよびトリアジニルであり、最も好ましくはピリジニルである。
【0041】
本明細書中で使用される場合、ヘテロアリール基またはヘテロアリール部分は、縮合していないことが好ましい。しかしながら、ヘテロアリール基またはヘテロアリール部分が別の基に縮合している場合、該基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合がある。好ましくは、該基または部分は、フェニル環、5〜6員のヘテロアリール環または5〜6員のヘテロシクリル環に縮合していることが好ましく、フェニル基に縮合していることがより好ましい。例としては、ベンゾチエニル基、ベンゾフリル基、ベンゾイミダゾリル基、ベンゾチアゾリル基、ベンゾイソチアゾリル基、ベンゾオキサゾリル基、ベンゾイソオキサゾリル基、ベンゾトリアゾリル基、インドリル基、イソインドリル基およびインダゾリル基が挙げられる。好ましい基としては、インドリル基、イソインドリル基、ベンゾイミダゾリル基、インダゾリル基、ベンゾフリル基、ベンゾチエニル基、ベンゾオキサゾリル基、ベンゾイソオキサゾリル基、ベンゾチアゾリル基およびベンゾイソチアゾリル基が挙げられ、より好ましくはベンゾイミダゾリル、ベンゾオキサゾリルおよびベンゾチアゾリルが挙げられ、最も好ましくはベンゾチアゾリルが挙げられる。
【0042】
本明細書中で使用される場合、5〜10員のヘテロシクリル基またはヘテロシクリル部分は、1個以上、例えば1個、2個、3個または4個の炭素原子が、N、O、S、S(O)およびS(O)2から選択される部分で置換された、非芳香族の飽和または不飽和のC5〜10炭素環であり、ここで1個以上の残りの炭素原子は、任意選択で基-C(O)-または-C(S)-によって置換されている。1個以上の残りの炭素原子が基-C(O)-または-C(S)-によって置換されている場合、好ましくは、1個だけまたは2個(より好ましくは2個)のかかる炭素原子が置換されている。典型的には、5〜10員のヘテロシクリル環は、5〜6員の環である。
【0043】
適切なヘテロシクリル基およびヘテロシクリル部分としては、アゼチジニル基およびアゼチジニル部分、オキセタニル基およびオキセタニル部分、チエタニル基およびチエタニル部分、ピロリジニル基およびピロリジニル部分、イミダゾリジニル基およびイミダゾリジニル部分、オキサゾリジニル基およびオキサゾリジニル部分、イソオキサゾリジニル基およびイソオキサゾリジニル部分、チアゾリジニル基およびチアゾリジニル部分、イソチアゾリジニル基およびイソチアゾリジニル部分、テトラヒドロフラニル基およびテトラヒドロフラニル部分、テトラヒドロチエニル基およびテトラヒドロチエニル部分、テトラヒドロピラニル基およびテトラヒドロピラニル部分、テトラヒドロチオピラニル基およびテトラヒドロチオピラニル部分、ジチオラニル基およびジチオラニル部分、ジオキソラニル基およびジオキソラニル部分、ピラゾリジニル基およびピラゾリジニル部分、ピペリジニル基およびピペリジニル部分、ピペラジニル基およびピペラジニル部分、ヘキサヒドロピリミジニル基およびヘキサヒドロピリミジニル部分、メチレンジオキシフェニル基およびメチレンジオキシフェニル部分、エチレンジオキシフェニル基およびエチレンジオキシフェニル部分、チオモルホリニル基およびチオモルホリニル部分、S-オキソ-チオモルホリニル基およびS-オキソ-チオモルホリニル部分、S,S-ジオキソ-チオモルホリニル基およびS,S-ジオキソ-チオモルホリニル部分、モルホリニル基およびモルホリニル部分、1,3-ジオキソラニル基および1,3-ジオキソラニル部分、1,4-ジオキソラニル基および1,4-ジオキソラニル部分、トリオキソラニル基およびトリオキソラニル部分、トリチアニル基およびトリチアニル部分、イミダゾリニル基およびイミダゾリニル部分、ピラニル基およびピラニル部分、ピラゾリニル基およびピラゾリニル部分、チオキソラニル基およびチオキソラニル部分、チオキソチアゾリジニル基およびチオキソチアゾリジニル部分、1H-ピラゾール-5-(4H)-オンイル(1H-pyrazol-5-(4H)-onyl)基および1H-ピラゾール-5-(4H)-オンイル部分、1,3,4-チアジアゾール-2(3H)-チオニル基および1,3,4-チアジアゾール-2(3H)-チオニル部分、オキソピロリジニル基およびオキソピロリジニル部分、オキソチアゾリジニル基およびオキソチアゾリジニル部分、オキソピラゾリジニル基およびオキソピラゾリジニル部分、スクシンイミド基およびスクシンイミド部分、ならびにマレイミド基およびマレイミド部分が挙げられる。好ましいヘテロシクリル基は、ピロリジニル基およびピロリジニル部分、イミダゾリジニル基およびイミダゾリジニル部分、オキサゾリジニル基およびオキサゾリジニル部分、イソオキサゾリジニル基およびイソオキサゾリジニル部分、チアゾリジニル基およびチアゾリジニル部分、イソチアゾリジニル基およびイソチアゾリジニル部分、テトラヒドロフラニル基およびテトラヒドロフラニル部分、テトラヒドロチエニル基およびテトラヒドロチエニル部分、テトラヒドロピラニル基およびテトラヒドロピラニル部分、テトラヒドロチオピラニル基およびテトラヒドロチオピラニル部分、ジチオラニル基およびジチオラニル部分、ジオキソラニル基およびジオキソラニル部分、ピラゾリジニル基およびピラゾリジニル部分、ピペリジニル基およびピペリジニル部分、ピペラジニル基およびピペラジニル部分、ヘキサヒドロピリミジニル基およびヘキサヒドロピリミジニル部分、チオモルホリニル基およびチオモルホリニル部分、ならびにモルホリニル基およびモルホリニル部分である。より好ましいヘテロシクリル基は、テトラヒドロピラニル基、テトラヒドロチオピラニル基、チオモルホリニル基、テトラヒドロフラニル基、テトラヒドロチエニル基、ピペリジニル基、モルホリニル基およびピロリジニル基、ならびに1個または2個の環炭素原子が-C(O)-基で置換されているバリアントである。特に好ましい基としては、テトラヒドロフラニルおよびピロリル-2,5-ジオンが挙げられる。
【0044】
ヘテロシクリル基またはヘテロシクリル部分が別の基に縮合している場合、この基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合があり、より好ましくはさらなるフェニル基、5〜6員のヘテロアリール基または5〜6員のヘテロシクリル基に縮合している場合がある。この基または部分は、単環式である(すなわちその基または部分は縮合していない)ことが好ましい。
【0045】
誤解を避けるためであるが、ヘテロアリール基およびヘテロシクリル基の上記定義は、環に存在し得る「N」部分について言及するものであるが、当業者に明らかなように、N原子は、単結合を介して隣接する環原子のそれぞれに結合している場合、プロトン化されることになる(または以下に定義する置換基を有することになる)。
【0046】
本明細書中で使用される場合、C3〜7炭素環式基またはC3〜7炭素環式部分は、3〜7個の炭素原子を有する、非芳香族の、飽和または不飽和の炭化水素環である。好ましくは、該基または部分は、3〜7個の炭素原子、より好ましくは3〜6個の炭素原子を有する、飽和炭化水素環または一不飽和炭化水素環(すなわちシクロアルキル部分またはシクロアルケニル部分)である。例としては、シクロプロピル、シクロブチル、シクロペンチルおよびシクロヘキシル、ならびにこれらの一不飽和のバリアント、より具体的にはシクロペンチルおよびシクロヘキシルが挙げられる。C3〜7カルボシクリル基またはC3〜7カルボシクリル部分にはまた、上記のC3〜7カルボシクリル基またはC3〜7カルボシクリル部分であるが、1個以上の環炭素原子が基-C(O)-によって置換されているC3〜7カルボシクリル基またはC3〜7カルボシクリル部分も含まれる。より好ましくは、0個、1個または2個の環炭素原子(最も好ましくは0個または2個)が-C(O)-によって置換されている。好ましいかかる基は、ベンゾキノンである。
【0047】
カルボシクリル基またはカルボシクリル部分が別の基に縮合している場合、この基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合があり、より好ましくはさらなるフェニル環、5〜6員のヘテロアリール環または5〜6員のヘテロシクリル環に縮合している場合がある。例えば、この基または部分は、さらなるフェニル環に縮合している場合がある。例示的な縮合したカルボシクリル基は、インダニルである。カルボシクリル基は、単環式である(すなわち縮合していない)ことがより好ましい。
【0048】
A1、A2、A3、B、DおよびR5におけるアリール部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分が2個、3個または4個の置換基によって置換される場合、2個以下の置換基がヒドロキシル、シアノおよびニトロから選択されることが好ましい。1個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることがより好ましい。さらに、アリール部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分が2個または3個の置換基によって置換される場合、1個以下の置換基が、-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBまたは-NRACONRARBから選択されることが好ましい。
【0049】
典型的には、A1、A2、A3、B、DおよびR5における、アリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分における、フェニル部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分は、置換されていないか、または1個、2個、3個もしくは4個の置換基によって、例えば1個、2個もしくは3個の置換基によって、置換されている。好ましい置換基としては、ハロゲン原子、ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、メルカプト基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基、C2〜4ヒドロキシアルケニル基、C1〜4アルキルチオ基、C2〜4アルケニルチオ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)が挙げられる。置換基は、非置換の置換基であることが好ましい。より好ましい置換基としては、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)が挙げられる。より好ましい置換基としては、ハロゲン原子、ならびにC1〜2アルキル基およびC1〜2アルコキシ基が挙げられる。
【0050】
本明細書中で使用される場合、用語「塩」は、塩基付加塩、酸付加塩および第四級塩を含む。酸性である本発明の化合物は、アルカリ金属水酸化物、例えば水酸化ナトリウムおよび水酸化カリウムなどの塩基;アルカリ土類金属水酸化物、例えば水酸化カルシウム、水酸化バリウムおよび水酸化マグネシウムなどの塩基;有機塩基、例えばN-メチル-D-グルカミン、コリン、トリス(ヒドロキシメチル)アミノ-メタン、L-アルギニン、L-リジン、N-エチルピペリジン、ジベンジルアミンなどと、薬学的に許容される塩を含む塩を形成することができる。塩基性である化合物(IA)または(IB)は、無機酸、例えば塩酸もしくは臭化水素酸などのハロゲン化水素酸、硫酸、硝酸またはリン酸など、ならびに有機酸、例えば酢酸、酒石酸、コハク酸、フマル酸、マレイン酸、リンゴ酸、サリチル酸、クエン酸、メタンスルホン酸、p-トルエンスルホン酸、安息香酸、ベンゼンスルホン酸、グルタミン酸、乳酸およびマンデル酸などと、薬学的に許容される塩を含む塩を形成することができる。
【0051】
1つ以上の実際のまたは潜在的なキラル中心を含む本発明の化合物は、不斉炭素原子が存在するために、各キラル中心でRまたはSの立体化学を有するいくつかのジアステレオ異性体として存在し得る。本発明は、すべてのかかるジアステレオ異性体およびそれらの混合物を含む。
【0052】
誤解を避けるためであるが、L1が基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-または-(CH2)mNR1(CH2)n-を表す場合、記載された基の左側は、本発明の化合物のチオフェン環部分に結合しており、したがってその基の右側は、本発明の化合物の環A1に結合している。好ましくは、整数nおよびmの和は、6以下である。より好ましくは、整数nおよびmの和は、4以下である。最も好ましくは、整数nおよびmの和は、3以下である。好ましくは、mおよびnの少なくとも一方は、ゼロに等しい。より好ましくは、少なくともmは、ゼロに等しい。
【0053】
本発明の好ましい実施態様において、L1は、C2〜4アルキニレン基ではない。
【0054】
好ましくは、L1は、-O-、-S-、-NR1-またはC1〜4アルキレンを表し、該C1〜4アルキレンは、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、式中、R1は、非置換のC1〜4アルキルを表す。
【0055】
より好ましくは、L1は、-O-またはC1〜4アルキレンを表し、該C1〜4アルキレン部分は、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、L1は、C1〜4アルキレンを表し、該C1〜4アルキレンは、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択される。
【0056】
最も好ましくは、L1は、非置換のC1〜4アルキレン、例えばメチル、エチル、n-プロピルまたはi-プロピルを表す。特に好ましい実施態様において、L1は、メチルを表す。
【0057】
好ましくは、A1は、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を表し、このそれぞれの基は、縮合していないか、またはさらなるフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基もしくは5〜6員のヘテロシクリル基に縮合している。
【0058】
より好ましくは、A1は、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロシクリル基に縮合している。A1が、縮合していないかまたは5〜6員のヘテロシクリル基に縮合している、フェニル基または5〜6員のヘテロアリール基を表す場合、そのヘテロシクリル基は、好ましくはジオキソール基である。例えば、A1が、縮合していないかまたは5〜6員のヘテロシクリル基に縮合している、フェニル基または5〜6員のヘテロアリール基を表す場合、好ましいA1基は、ベンゾジオキソールである。
【0059】
より好ましくは、A1は、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、縮合していないか、またはさらなるフェニル基に縮合している。より好ましくは、A1は、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、より好ましくは1,4-フェニレン基または1,3-フェニレン基などの非縮合のフェニル基を表す。1つの好ましい実施態様において、A1は、1,3-フェニレン基を表す。
【0060】
好ましくは、A1基は、置換されていないか、または1個、2個もしくは3個の置換基を有する。1個よりも多くの置換基が存在している場合、それらの置換基は、同一であってもよく、異なっていてもよい。1個よりも多くの置換基が存在している場合、1個の置換基だけがヒドロキシル基、シアノ基またはニトロ基であることが好ましい。
【0061】
A1上の好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択される。
【0062】
A1上のより好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0063】
より好ましくは、A1上の置換基は、ハロゲン原子、ならびに非置換のC1〜2アルキル基およびC1〜2アルコキシ基から選択される。
【0064】
最も好ましくは、A1基は、置換されていない。
【0065】
好ましくは、Alk2は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表す。より好ましくは、Alk2は、C1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表す。
【0066】
好ましくは、Alk2基は、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されている。より好ましくは、Alk2基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個、より好ましくは1個もしくは2個の非置換の置換基で置換されている。最も好ましくは、Alk2基は、置換されていない。
【0067】
より好ましくは、Alk2は、非置換のメチレン基、エチレン(-CH2CH2-)基、ビニレン(-CH=CH-)基またはエチニレン(-C≡C-)基を表す。最も好ましくは、Alk2は、メチレンなどのC1〜2アルキレン基を表す。
【0068】
L2が-Alk2-A2-を表す場合、好ましくは、A2は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表す。より好ましくは、A2は、非縮合のフェニル基を表す。Alk2基およびHet基またはAlk1基は、任意の位置でフェニル基に結合していてよいが、Alk2基およびHet基またはAlk1基は、互いにメタまたはパラの関係で結合していること、より好ましくはパラの関係で結合していることが好ましい。
【0069】
好ましくは、A2基は、0個、1個、2個または3個の置換基、より好ましくは、0個、1個または2個の置換基を有する。1個よりも多くの置換基が存在している場合、それらの置換基は、同一であってもよく、異なっていてもよい。1個よりも多くの置換基が存在している場合、1個の置換基だけがヒドロキシル基、シアノ基またはニトロ基であることが好ましい。
【0070】
A2上の好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0071】
A2上のより好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0072】
より好ましくは、A2上の置換基は、ハロゲン原子、ならびに非置換のC1〜2アルキル基およびC1〜2アルコキシ基から選択される。最も好ましくは、A2基は、置換されていない。
【0073】
L2が-Alk2-Alk3を表す場合、好ましくは、Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、Alk3は、非置換のC1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表す。最も好ましくは、Alk3は、非置換のC1〜4アルキレン、例えばC3〜4アルキレン基、より好ましくは基-CH2-CH2-CH2-を表す。
【0074】
L2は、-Alk2-であることが好ましい。
【0075】
Het基は、存在する場合、好ましくは、-O-、-NR’または-S-(式中、R’は、水素または非置換のメチルを表す)を表す。より好ましくは、Het基は、-O-、-NHまたは-S-を表す。最も好ましくは、Het基は、-O-である。
【0076】
L2が-Alk2-である場合、好ましくは、xは0である。別の好ましい実施態様において、xは0である。
【0077】
好ましくは、Alk1は、結合またはC1〜6アルキレン基または基-A3-Alk4-を表す。より好ましくは、Alk1は、結合またはC1〜6アルキレン基を表す。最も好ましくは、Alk1は、結合を表す。
【0078】
Alk1がC1〜6アルキレン基を表す場合、該アルキレン基は、好ましくはC1〜4アルキレン基であり、より好ましくはC1〜3アルキレン基であり、好ましくはメチレン基またはプロピレン基である。
【0079】
Alk1がC1〜6アルキレン基を表す場合、好ましくはAlk1基は、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されている。より好ましくは、Alk1基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個、より好ましくは1個の非置換の置換基で置換されている。最も好ましくは、Alk1は、置換されていない。
【0080】
Alk1が基-A3-Alk4-を表す場合、A3は、好ましくは、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0081】
Alk1が基-A3-Alk4-を表す場合、好ましくは、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、またはハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の置換基で置換されている。より好ましくは、A3は、非縮合のフェニルを表し、該フェニルは、置換されていないか、またはハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の置換基で置換されている。最も好ましくは、A3は、非置換の、非縮合のフェニル基を表す。
【0082】
Alk1が基-A3-Alk4-を表す場合、Alk4は、好ましくは非置換のC1〜6アルキレン基を表し、より好ましくは非置換のC1〜3アルキレン基を表し、より好ましくは非置換のC1〜2アルキレン基を表し、具体的にはメチレン基-CH2-またはエチレン基-CH2-CH2-を表す。
【0083】
A2およびA3の一方のみが存在していることが好ましい。すなわち、Alk1が-A3-Alk4-である場合、L2は-Alk2-A2-ではないことが好ましく、逆もまた同様である。
【0084】
xが1である場合、好ましくは、Alk1は、C3アルキレン基である。L2が-Alk2-である場合、好ましくは、xは0であり、Alk1は、結合またはC3アルキレン基、例えばC3アルキレン基である。L2が-Alk2-A2-である場合、好ましくは、xは1であり、Alk1はC1アルキレン基である。
【0085】
好ましい基(Y1)および(Y2)としては、環Dが非縮合の5〜6員のヘテロアリール基またはヘテロシクリル基であり、R2が環D中に示された窒素原子に隣接する炭素原子に結合している、基が挙げられる。より好ましくは、環Dは、非縮合の5〜6員のヘテロシクリル基、例えば、ピロリジニル基、オキサゾリジニル基、イソオキサゾリジニル基、イミダゾリジニル基、ピラゾリジニル基、チアゾリジニル基、イソチアゾリジニル基、ピペリジニル基、ヘキサヒドロピリミジニル基、ピペラジニル基、モルホリニル基またはチオモルホリニル基である。環Dは、より好ましくは、ピロリジニル基、ピペラジニル基またはピペリジニル基であり、より好ましくは、ピペリジル基またはピペラジニル基である。
【0086】
基Rが式(Y1)のものである場合、好ましくは、環Dは、有している基R2およびR7に加えて、置換されていないか、またはハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルコキシ基およびヒドロキシル基から選択される1個もしくは2個の基によって置換されている。より好ましくは、環Dは、基R2およびR7を有していることは別として、置換されていない。
【0087】
基Rが式(Y2)のものである場合、好ましくは、環Dは、基R2を有していることに加えて、置換されていないか、またはハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルコキシ基およびヒドロキシル基から選択される1個もしくは2個の基によって、置換されている。より好ましくは、環Dは、基R2を有していることは別として、置換されていない。
【0088】
Rが式(Y2)の基である場合、特に好ましい環D基は、
【0089】
【化4】

【0090】
である。
【0091】
Rが式(X1)の基を表す場合、R3は、好ましくは、水素原子または非置換のC1〜2アルキルを表す。より好ましくは、R3は、水素原子または非置換のメチルを表す。最も好ましくは、R3は、水素原子を表す。
【0092】
Rが式(X2)の基を表す場合、好ましくは、R5は、水素原子、または非置換のC1〜4アルキル基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR12の基(式中、R6は、水素原子もしくは非置換のC1〜4アルキル基である)を表す。より好ましくは、R5は、水素原子または非置換のC1〜2アルキル基を表す。最も好ましくは、R5は、水素原子を表す。
【0093】
誤解を避けるためであるが、Rが式(X1)の基を表す場合、基R7およびR8は、同一であってもよく、異なっていてもよい。
【0094】
置換基R7およびR8が、これらが結合する炭素と一緒になって、3〜6員の飽和のスピロシクロアルキル環またはスピロヘテロシクリル環を形成する場合、適切なスピロシクロアルキル環としては、シクロプロピル環、シクロペンチル環およびシクロヘキシル環が挙げられ、一方、適切なスピロヘテロシクリル環としては、ピペリジン-4-イル環が挙げられる。
【0095】
誤解を避けるためであるが、「天然α-アミノ酸または非天然α-アミノ酸のα-置換基」としての基R4、R7およびR8の定義において、「α-アミノ酸」は、式H2NCHRαCOOHの化合物を意味し、「α-置換基」は、前記α-アミノ酸の基Rαを意味する。
【0096】
天然α-アミノ酸または非天然α-アミノ酸のα-置換基上の(すなわち、基R4、R7およびR8上の)どの官能基も、保護されていてよい。用語「保護された(protected)」は、α-アミノ酸の側鎖における官能性置換基との関連で使用される場合、実質的に非官能性である、かかる置換基の誘導体を意味することが、当業者にはわかる。例えば、カルボキシ基は、エステル化されていてもよく(例えばC1〜C6アルキルエステルとして)、アミノ基は、アミド(例えばNHCOC1〜C6アルキルアミドとして)またはカルバミン酸エステル(例えばNHC(=O)OC1〜C6アルキルカルバミン酸エステルもしくはNHC(=O)OCH2Phカルバミン酸エステルとして)に転換されていてもよく、ヒドロキシル基は、エーテル(例えばOC1〜C6アルキルエーテルもしくはO(C1〜C6アルキル)フェニルエーテル)またはエステル(例えばOC(=O)C1〜C6アルキルエステル)に転換されていてもよく、チオール基は、チオエーテル(例えばtert-ブチルチオエーテルもしくはベンジルチオエーテル)またはチオエステル(例えばSC(=O)C1〜C6アルキルチオエステル)に転換されていてもよい。
【0097】
好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合またはC1〜6アルキレン基を表し、Bは、C6〜10アリール基または5〜10員のヘテロアリール基を表す);
(iv)式-CRpRqRrの基{式中、
(a)Rp、RqおよびRrが、同一であるか、もしくは異なっており、
・水素原子、
・-OH基、-SH基、ハロゲン基、-CN基、-CO2H基、CONH2基もしくは(C1〜4)ペルフルオロアルキル基、もしくは
・C1〜6アルキル基、C2〜6アルケニル基、C2〜6アルキニル基、フェニル基、5〜6員のヘテロアリール基、フェニル(C1〜6)アルキル基、C3〜8シクロアルキル基、-O(C1〜6)アルキル基、-O(C2〜6)アルケニル基、-S(C1〜6)アルキル基、-SO(C1〜6)アルキル基、-SO2(C1〜6)アルキル基、-S(C2〜6)アルケニル基、-SO(C2〜6)アルケニル基もしくは-SO2(C2〜6)アルケニル基[このそれぞれの基は、ヒドロキシル、-O(C1〜6)アルキル、フェニルオキシ、ベンジルオキシ、-SH、-S(C1〜6)アルキル、フェニルチオ、ベンジルチオ、-COOH、-CONH2、-NHC(NH)NH2もしくは
【0098】
【化5】

【0099】
によって、置換されていてもよい]を表すか;
(b)Rp、RqおよびRrのうちの2つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他のものが、基-Q-W[式中、Qは、結合、もしくは-O-、-S-、-SO-もしくは-SO2-を表し、Wは、すべてさらなるフェニル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環に縮合していてもよい、フェニル基、フェニル(C1〜6)アルキル基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基、C4〜8シクロアルケニル基、C4〜8シクロアルケニル(C1〜6)アルキル基、5員もしくは6員のヘテロアリール基もしくは5員もしくは6員のヘテロアリール(C1〜6)アルキル基を表し、該基Wは、置換されていないか、もしくは1個以上の置換基によって置換されており、該置換基は、同一であるか、もしくは異なっており、ヒドロキシル、ハロゲン、-CN、-CONH2、-CONH(C1〜6)アルキル、-CONH(C1〜6アルキル)2、-CHO、-CH2OH、(C1〜4)ペルフルオロアルキル、-O(C1〜6)アルキル、-S(C1〜6)アルキル、-SO(C1〜6)アルキル、-SO2(C1〜6)アルキル、-NO2、-NH2、-NH(C1〜6)アルキル、-N((C1〜6)アルキル)2、-NHCO(C1〜6)アルキル、(C1〜6)アルキル、(C2〜6)アルケニル、(C2〜6)アルキニル、(C3〜8)シクロアルキル、(C4〜8)シクロアルケニル、フェニルもしくはベンジルを表す]を表すか;または
(c)Rp、RqおよびRrのうちの1つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他の2つが、これらが結合する炭素原子と一緒になって、3〜8員のカルボシクリル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環を形成するか、もしくはRp、RqおよびRrが、これらが結合する炭素原子と一緒になって、三環系を形成する(ただし、式-CRpRqRrの基は、(i)、(ii)および(iii)で定義された基とは異なっている)};
を表すか;
あるいは、R7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和のスピロシクロアルキル環またはスピロヘテロシクリル環を形成する。
【0100】
この好ましい実施態様において、式-CRpRqRrの基は、より好ましくは、式-CRpRqRrの基{式中、
(a)Rp、RqおよびRrが、同一であるか、もしくは異なっており、
・水素原子、
・-OH基、-SH基、-CO2H基もしくはCONH2基、もしくは
・C1〜6アルキル基、フェニル基、5〜6員のヘテロアリール基、フェニル(C1〜6)アルキル基、C3〜8シクロアルキル基、-O(C1〜6)アルキル基もしくは-S(C1〜6)アルキル基[このそれぞれの基は、ヒドロキシル、-O(C1〜6)アルキル、フェニルオキシ、ベンジルオキシ、-SH、-S(C1〜6)アルキル、フェニルチオ、ベンジルチオ、-COOH、-CONH2もしくは-NHC(NH)NH2によって、置換されていてもよい]を表すか;または
(b)Rp、RqおよびRrのうちの2つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他のものが、基-W[式中、Wは、すべてさらなるフェニル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環に縮合していてもよい、フェニル基、フェニル(C1〜6)アルキル基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基、5員もしくは6員のヘテロアリール基もしくは5員もしくは6員のヘテロアリール(C1〜6)アルキル基を表し、該基Wは、置換されていないか、もしくはヒドロキシル、ハロゲン、-O(C1〜6)アルキル、-NH2、-NH(C1〜6)アルキル、-N((C1〜6)アルキル)2もしくは(C1〜6)アルキルによって、置換されている]を表す}
である。
【0101】
本発明のより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合もしくはC1〜6アルキレン基を表し、Bは、C6〜10アリール基もしくは5〜10員のヘテロアリール基を表す);または
(iv)インドール-3-イルメチル、-CH2COOH、-CH2CH2COOH、-CH2CONH2、-CH2CH2CONH2、-CH2CH2CH2NHC(NH)NH2、シクロヘキシル、シクロヘキシルメチルおよび1-ベンジルチオ-1-メチルエチルから選択される基
を表す。
【0102】
このより好ましい実施態様の1つの例示的な実施態様において、R4、R7およびR8は、同一であるか、または異なっており、天然のタンパク新生α-アミノ酸、またはシクロヘキシルグリシン、t-ブチルセリン、t-ブチルシステイン、tert-ブチルグリシンおよびフェニルグリシンから選択されるα-アミノ酸のα-置換基から選択される。誤解を避けるためであるが、前記天然のタンパク新生α-アミノ酸は、アラニン、アルギニン、アスパラギン、アスパラギン酸、システイン、グルタミン酸、グルタミン、グリシン、ヒスチジン、イソロイシン、ロイシン、リジン、メチオニン、フェニルアラニン、セリン、トレオニン、トリプトファン、チロシンおよびバリンから選択される。したがって、この例示的な実施態様において、R4、R7およびR8は、同一であるか、または異なっており、メチル、-CH2CH2CH2NHC(NH)NH2、-CH2CONH2、-CH2COOH、-CH2SH、-CH2CH2COOH、-CH2CH2CONH2、水素、イミダゾール-5-イルメチル、sec-ブチル、イソブチル、-CH2CH2CH2CH2NH3、-CH2CH2SCH3、ベンジル、ヒドロキシメチル、-CHOHCH3、インドール-3-イルメチル、4-ヒドロキシフェニルメチル、プロパ-2-イル、シクロヘキシル、t-ブトキシメチル、-CH2SC(CH3)3、t-ブチルおよびフェニルから選択される。これらの基のうち、この場合好ましい基としては、水素、フェニル、ベンジル、イソブチル、シクロヘキシルおよびt-ブトキシメチルが挙げられる。
【0103】
本発明のさらにより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;または
(iii)基-L3-B(式中、L3は、結合もしくはC1〜4アルキレン基を表し、Bは、フェニル基もしくは5〜10員のヘテロアリール基を表す)
を表す。
【0104】
基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、該アルキル基は、好ましくはC1〜4アルキル基であり、より好ましくはC1〜2アルキル基であり、最も好ましくはメチル基である。
【0105】
基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、L3は、好ましくは結合またはC1〜4アルキレン基であり、より好ましくはC1〜2アルキレン基であり、最も好ましくはメチレン基である。基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、Bは、好ましくは、フェニル基または5〜10員のヘテロアリール基を表す。Bが、5〜10員のヘテロアリール基を表す場合、好ましいヘテロアリール基としては、イミダゾリルおよびインドリルが挙げられる。基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、好ましくは、Bは、フェニル基を表す。
【0106】
基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、該アルキル基は、好ましくは、置換されていないか、またはハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくはC1〜2アルキルを表す)から選択される1個もしくは2個、好ましくは1個の非置換の置換基で置換されている。基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、最も好ましくは、該アルキル基は、置換されていない。
【0107】
基R中に存在する任意の基R4、R7またはR8が、L3がC1〜6アルキレン基を表す式-L3-Bの基を表す場合、前記C1〜6アルキレン基は、好ましくは、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、前記C1〜6アルキレン基は、置換されていない。
【0108】
基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、好ましくは、Bは、置換されていないか、または1個、2個もしくは3個、より好ましくは1個もしくは2個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、Bは、置換されていないか、またはハロゲン原子、もしくはC1〜4アルキル基、C1〜2アルコキシ基、C1〜2アルキルチオ基もしくはヒドロキシ基から選択される1個の置換基で置換されている。最も好ましくは、Bは、置換されていない。
【0109】
さらにより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、水素原子、非置換のC1〜6アルキル基、または基-L3-B(式中、L3は、結合または非置換のC1〜2アルキレン基を表し、Bは、非置換のフェニル基、またはハロゲン原子、もしくはC1〜2アルキル基、C1〜2アルコキシ基、C1〜2アルキルチオ基もしくはヒドロキシ基から選択される1個の置換基で置換されたフェニル基を表す)を表す。
【0110】
特に好ましいR4基、R7基およびR8基は、水素原子および非置換のC1〜6アルキル基である。最も好ましいR4基、R7基およびR8基としては、水素原子、ならびに非置換のメチル基、エチル基、n-プロピル基、i-プロピル基、n-ブチル基、i-ブチル基、sec-ブチル基およびt-ブチル基が挙げられる。
【0111】
好ましくは、Rが式(X1)の基である場合、置換基R7およびR8の少なくとも1つは、C1〜6アルキル基、例えばメチル、エチル、n-プロピルもしくはイソプロピル、またはn-ブチル、イソブチル、sec-ブチルもしくはt-ブチルである。
【0112】
好ましくは、(X1)において、R7およびR8の少なくとも1つは、水素原子である。
【0113】
最も好ましくは、Rが式(X1)の基である場合、R7およびR8は、同一であるか、または異なっており、水素原子、または非置換のC1〜6アルキル基、フェニル基、5〜6員のヘテロアリール基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基もしくはフェニル(C1〜6)アルキル基を表す。R7またはR8の1つが水素である場合、好ましくは、R7およびR8の他のものは、水素以外のものである。より好ましくは、R7およびR8は、同一であるか、または異なっており、水素または非置換のC1〜6アルキルを表す。R7およびR8がいずれも水素ではない場合、好ましくは、R7およびR8は、同一であるか、または異なっており、非置換のC1〜2アルキル基を表す。より好ましくは、R7およびR8がいずれも水素ではない場合、R7およびR8は、どちらも非置換のメチル基である。
【0114】
Rが、(i)R7およびR8の1つが水素であり、R7およびR8の他のものが水素以外の基である式(X1)の基、または(ii)R7が水素である式(Y1)の基、のいずれかを表す場合、好ましくは、基Rは、L-異性を有する。誤解を避けるためであるが、基R2に直接結合している炭素原子が、天然のタンパク新生アミノ酸がそのα-炭素原子について有するL-異性と一致するL-異性を有するキラル中心を表す場合、基Rは、L-異性を有する。したがって、この実施態様においては、立体化学は、以下に図示した通りである。
【0115】
【化6】

【0116】
好ましくは、Rは、式(X1)または(Y1)の基である。最も好ましくは、Rは、式(X1)の基である。Rが式(X1)または(Y1)の基である化合物は、全身投与レジメンに特によく適している。
【0117】
好ましい実施態様において、基Rは、その基の中の明示的に書き表された窒素部分が直接カルボニル(-C(=O)-)に結合していない、式(X1)または(Y1)の基である。より好ましくは、基Rは、その基の中の明示的に書き表された窒素部分が直接カルボニル(-C(=O)-)に結合していない、式(X1)の基である。
【0118】
別の実施態様において、基Rは、式(X2)または(Y2)の基である。かかる化合物は、局所(local)投与療法または局所(topical)投与療法に特によく適している。
【0119】
A1が非縮合の1,3-フェニレン基を表す、好ましい実施態様において、基R中に存在する任意の基R4、R7またはR8は、水素以外の基である。A1が非縮合の1,3-フェニレン基を表す、特に好ましい実施態様において、基R中に存在する任意の基R4、R7またはR8は、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す。A1が非縮合の1,3-フェニレン基を表す、最も好ましい実施態様において、Rは、式(X1)の基であり、R7およびR8は、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す。
【0120】
R2は、カルボン酸基-COOHまたはエステル基-COOR9のいずれかである。上記の置換基R2との関連における用語「エステル」または「エステル化カルボキシル基」は、基-(C=O)OR9(式中、R9は、理論上アルコールR9-OHに由来する、エステルを特徴付ける基である)を意味する。1つの実施態様において、好ましくは、R2は、エステル基-COOR9である。すなわち、好ましくは、R2は、1種以上の細胞のカルボキシルエステラーゼ(caboxylesterase)酵素によって-COOH基に加水分解され得るエステル基である。
【0121】
R2がエステル基である場合、該エステル基は、本発明の化合物において、1種以上の細胞内カルボキシルエステラーゼ酵素によって、カルボン酸基に加水分解され得るエステル基でなければならない。本発明の化合物のエステル基を対応する酸に加水分解することができる細胞内カルボキシルエステラーゼ酵素としては、3種の公知のヒト酵素アイソタイプhCE-1、hCE-2およびhCE-3が挙げられる。これらのアイソタイプが主要な酵素であると考えられているが、ビフェニルヒドロラーゼ(biphenylhydrolase)(BPH)などの他の酵素もまた、結合体の加水分解において役割を有し得る。一般に、カルボキシルエステラーゼが、遊離したアミノ酸エステルを親の酸に加水分解するのであれば、カルボキシルエステラーゼは、エステルモチーフを、IKK阻害剤に共有結合しているときにも加水分解することになる。そのため、後述の破壊細胞アッセイにより、所要の加水分解プロフィールを有するエステルの直接的、迅速かつ簡便な最初のスクリーニングが提供される。この方法で選定したエステルモチーフは、その後、選択した結合化学によってIKK阻害剤に結合させて同じカルボキシルエステラーゼアッセイで再度アッセイして、その基礎環境において依然としてカルボキシルエステラーゼの基質であることを確認することができる。
【0122】
エステルモチーフが、細胞内カルボキシルエステラーゼ酵素によって加水分解され得るという必要条件に従えば、特定のエステル基R2の例としては、式-(C=O)OR9〔式中、R9は、-CR14R15R16{式中、
(i)R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基[式中、aおよびbは、同一であるか、または異なっており、0または1を表し、Z1は、-O-、-S-または-NR17-(式中、R17は、水素またはC1〜4アルキルである)を表す]を表し、R16が、水素またはC1〜4アルキルを表し、R14が、水素またはC1〜4アルキルを表すか;
(ii)R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表し、R16が、水素またはC1〜4アルキルを表し、R14が、水素を表すか;
(iii)R15が、式-(Alk5)-NR18R19の基(式中、Alk5は、C1〜4アルキレン基を表し、(a)R18およびR19は、同一であるか、もしくは異なっており、水素もしくはC1〜4アルキルを表すか、または(b)R18およびR19は、これらが結合している窒素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基もしくは5〜10員のヘテロシクリル基に縮合していてもよい、5〜10員のヘテロアリール基もしくは5〜10員のヘテロシクリル基を形成するか、のいずれかである)を表し;R16が、水素またはC1〜4アルキルを表し、R14が、水素を表すか;または
(iv)R15およびR16が、これらが結合している炭素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基を形成し、R14が、水素を表す}
である〕のエステル基が挙げられる。
【0123】
R14基、R15基、R16基、R17基、R18基、R19基およびAlk5基における、アルキル基、アルキレン基およびアルケニル基上の好ましい置換基としては、同一であるか、または異なっており、ハロゲン、C1〜4アルキル、C2〜4アルケニル、C1〜4アルコキシ、ヒドロキシルおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)から選択される、1個または2個の置換基が挙げられる。より好ましい置換基は、ハロゲン、C1〜2アルコキシ、ヒドロキシルおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)である。最も好ましくは、R15、R16およびAlk5における、アルキル基、アルキレン基およびアルケニル基は、置換されていない。
【0124】
R15基、R16基、R18基およびR19基における、またはこれらの基によって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基上の好ましい置換基としては、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルキレン基、C1〜4アルコキシ基、C1〜4ハロアルキル基、ヒドロキシル基、シアノ基、ニトロ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)から、より好ましくは、ハロゲン原子、ならびにC1〜2アルキル基、C1〜2アルキレン基、C1〜2アルコキシ基およびヒドロキシル基から選択される、1個または2個の置換基が挙げられる。より好ましくは、R15、R16、R18およびR19における、またはこれらによって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、またはC1〜2アルキレン基、特にメチレン基によって置換されている。最も好ましくは、R15、R16、R18およびR19における、またはこれらによって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていない。
【0125】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表す場合、好ましくは、aまたはbのいずれかは、ゼロであり、例えば、aおよびbは、いずれもゼロである。[C1〜4アルキレン]が存在している場合、それは、好ましくは、C1〜3アルキレンであり、より好ましくは、基-CH2-CH2-などのC1〜2アルキレンである。
【0126】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表す場合、好ましくは、C1〜4アルキルは、メチル、エチルまたはn-プロピルなどのC1〜3アルキル基であり、最も好ましくはメチルである。
【0127】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表し、aが1である場合、Z1は、好ましくは、-O-または-NR17-(式中、R17は、水素またはC1〜2アルキルである)であり、より好ましくは、Z1は、-O-である。
【0128】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、aまたはbのいずれかは、ゼロであり、より好ましくは、aおよびbは、いずれもゼロである。[C1〜4アルキレン]が存在している場合、それは、好ましくは、C1〜3アルキレンであり、より好ましくは、C1〜2アルキレンである。
【0129】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、C2〜4アルケニルは、C2〜3アルケニル基、特に-CH=CH2である。
【0130】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルケニル]の基を表し、aが1である場合、Z1は、好ましくは、-O-または-NR17-(式中、R17は、水素またはC1〜2アルキルである)であり、より好ましくは、Z1は、-O-である。最も好ましくは、Z1は存在しない(すなわちaはゼロである)。
【0131】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、R15は、水素、またはC1〜4アルキル基もしくはC2〜4アルケニル基、または基-(C1〜4アルキル)-O-(C1〜4アルキル)を表す。R15は、より好ましくは、水素、メチル、エチル、n-プロピル、-CH=CH2または-CH2-CH2-O-CH3を表し、最も好ましくは、メチルを表す。
【0132】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、R16は、好ましくは、水素またはC1〜2アルキルを表し、より好ましくは、水素またはメチルを表す。
【0133】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、R14は、水素またはC1〜2アルキルを表し、より好ましくは、R14は、水素またはメチルを表す。
【0134】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、R15およびR16の双方における、アルキル基、アルキレン基およびアルケニル基は、置換されていないことが好ましい。
【0135】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、好ましくは、該フェニル基またはヘテロアリール基は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表す。好ましいヘテロアリール基としては、ピリジル、ピロリル、イソチアゾリル、ピラゾリルおよびイソオキサゾリルが挙げられ、最も好ましくは、ピリジルが挙げられる。
【0136】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、R9における、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないことが好ましい。
【0137】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、R16は、好ましくは、水素またはC1〜4アルキルを表し、より好ましくは、水素またはC1〜2アルキルを表し、最も好ましくは、水素を表す。R16のC1〜4アルキル基は、置換されていないことが好ましい。
【0138】
R15が、式-(Alk5)-NR18R19の基を表す場合、Alk5は、好ましくは、C1〜2アルキレン基を表し、好ましくは、-CH2-または-CH2CH2-のいずれかを表す。
【0139】
R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、同一であるか、または異なっており、水素またはC1〜4アルキルを表す場合、好ましくは、R18は、水素またはC1〜2アルキルを表し、より好ましくは、R18は、メチル基を表す。R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、同一であるか、または異なっており、水素またはC1〜4アルキルを表す場合、好ましくは、R19は、水素またはC1〜2アルキルを表し、より好ましくは、R19は、メチル基を表す。
【0140】
R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、これらが結合している窒素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、5〜10員のヘテロアリール基または5〜10員のヘテロシクリル基を形成する場合、R18およびR19は、非縮合の5〜6員のヘテロアリール基または非縮合の5〜6員のヘテロシクリル基を形成することが好ましい。R18およびR19が、5〜6員のヘテロシクリル基を形成することがより好ましい。好ましいヘテロシクリル基としては、ピペリジニル、ピペラジニル、モルホリニルおよびピロリジニルが挙げられ、最も好ましくはモルホリニルが挙げられる。
【0141】
R15が式-(Alk5)-NR18R19の基を表す場合、Alk5は、好ましくは、C1〜2アルキレン基を表し、より好ましくは、基-CH2CH2-を表す。
【0142】
R15が式-(Alk5)-NR18R19の基を表す場合、R16は、好ましくは、水素またはC1〜2アルキルを表し、最も好ましくは、水素を表す。
【0143】
R15が式-(Alk5)-NR18R19の基を表す場合、Alk5、R18およびR19における、アルキル基およびアルキレン基は、置換されていないことが好ましい。R15が、式-(Alk5)-NR18R19の基を表す場合、R18およびR19における、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないことが好ましい。
【0144】
R15が式-(Alk5)-NR18R19の基を表す場合、好ましい基としては、-CH2-CH2-NMe2および-CH2-CH2-モルホリニルが挙げられる。
【0145】
R15およびR16が、これらが結合している炭素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基を形成する場合、好ましい基としては、非縮合のフェニル、非縮合の5〜6員のヘテロアリール、非縮合の5〜6員のヘテロシクリル、非縮合のC3〜7カルボシクリル、およびフェニル環に縮合したC3〜7カルボシクリルが挙げられ、より好ましくは、非縮合のフェニル、非縮合の5〜6員のヘテロシクリル、非縮合のC3〜7カルボシクリル、およびフェニル環に縮合したC3〜7カルボシクリルが挙げられる。
【0146】
R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましい非縮合の5〜6員のヘテロシクリル基としては、ピペリジニル基、テトラヒドロフラニル基、ピペラジニル基、モルホリニル基およびピロリジニル基が挙げられ、より好ましくは、ピペリジニル基およびテトラヒドロフラニル基が挙げられる。R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましい非縮合のC3〜7カルボシクリル基としては、シクロペンチルおよびシクロヘキシルが挙げられ、より好ましくは、シクロペンチルが挙げられる。R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましいフェニル環に縮合したC3〜7カルボシクリル基としては、インダニルが挙げられる。
【0147】
R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましくは、形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、または1個もしくは2個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルキレン基、C1〜4アルコキシ基、C1〜4ハロアルキル基、ヒドロキシル基、シアノ基、ニトロ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)から選択され、より好ましくは、ハロゲン原子、またはC1〜2アルキル基、C1〜2アルキレン基、C1〜2アルコキシ基およびヒドロキシル基から選択される。最も好ましくは、形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、またはC1〜2アルキル基(例えばメチル基など)によって、もしくはC1〜2アルキレン基によって(例えばメチレン基などによって)、置換されている。さらにより好ましくは、そのようにして形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていない。
【0148】
好ましいR2基は、-COOHおよび-COOR9[式中、R9は、C1〜4アルキル基(例えばメチル、エチル、n-プロピルまたはイソプロピル、ならびにn-ブチル、sec-ブチルおよびtert-ブチルなど)、C3〜7カルボシクリル基(例えばシクロペンチルおよびシクロヘキシルなど)、C2〜4アルケニル基(例えばアリルなど)、さらにフェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基およびモルホリノエチル基を表す]である。より好ましくは、R9は、C1〜4アルキルまたはC3〜7カルボシクリルを表す。
【0149】
好ましくは、前記好ましいR9基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、前記好ましいR9基は、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択される。最も好ましくは、前記好ましいR9基は、置換されていない。前記好ましいR9基が置換されている場合、好ましくは、最大で1個の置換基がヒドロキシル基である。
【0150】
R2が-COOR9である場合、より好ましくは、R9は、非置換のC1〜4アルキル、非置換のC3〜7カルボシクリルまたは非置換のC2〜4アルケニルを表す。より好ましくは、R9は、シクロペンチルまたはt-ブチルであり;最も好ましくは、R9は、シクロペンチルである。
【0151】
R2が、-COOHまたは-COOR9(式中、R9は、C1〜4アルキルまたはC3〜7カルボシクリルである)を表す化合物は、R2が-COOR10であり、R10が水素、C1〜4アルキルまたはC3〜7カルボシクリルである基によって、記述することができる。好ましくは、R2は、-COOR10(式中、R10は、水素またはC3〜7カルボシクリルであり、より好ましくは、式中、R10は、水素またはシクロペンチルである)である。1つの実施態様において、R10は、水素以外のものである。すなわち、R10は、上記のC1〜4アルキルまたはC3〜7カルボシクリルから選択される。
【0152】
マクロファージは、サイトカイン、特にTNF-αおよびIL-1の放出を通じて、炎症性疾患において、重要な役割を果たしていることが知られている。関節リウマチにおいて、マクロファージは、関節炎症および関節破壊の維持に対する主要な寄与体である。マクロファージはまた、腫瘍増殖および腫瘍発達にもかかわっている。したがって、マクロファージ細胞の増殖を選択的に標的とする薬剤は、癌および自己免疫疾患の治療において、価値のあるものであり得る。特定の細胞型を標的とすることで、副作用の減少がもたらされると期待される。本発明者らは、マクロファージならびに単球、破骨細胞および樹状細胞などの骨髄単球性系列に由来する他の細胞に対して阻害剤を標的化する方法を発見した。これは、エステラーゼモチーフが阻害剤に結合する方法により、阻害剤が加水分解されるかどうか、したがって異なる細胞型に蓄積されるか否かが決まるという知見に基づく。具体的に言えば、マクロファージおよび骨髄単球性系列に由来する他の細胞がヒトカルボキシルエステラーゼhCE-1を含むのに対して、他の細胞型は含まないことが見出されている。基Rが、窒素部分が直接カルボニル(-C(=O)-)に結合していない式(X1)または(Y1)の基である場合の一般式(IA)および(IB)では、エステルは、hCE-1によって加水分解されるだけであり、したがって阻害剤は、マクロファージ類縁細胞中に選択的に蓄積することになる。誤解を避けるためであるが、ここで言及した窒素部分は、基(X1)および(Y1)において、明示的に記載されたN原子である。本明細書においては、「単球(monocyte)」または「単球(monocytes)」と明示しない限り、用語「マクロファージ(macrophage)」または「マクロファージ(macrophages)」は、マクロファージ(macrophages)(腫瘍関連マクロファージを含む)および/または単球(monocytes)を示すために使用する。
【0153】
本発明の好ましい実施態様(1)において、
・L1が、C1〜4アルキレンを表し、該アルキレンが、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択され;
・A1が、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2が、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3が、非置換のC1〜4アルキレン基を表し;
・A2が、非縮合のフェニルを表し、該フェニルが、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Hetが、-O-、-NH-または-S-を表し;
・Alk1が、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、非置換のC1〜3アルキレン基を表す]を表し;
・Rが、式(X1)または(Y1)の基:
【0154】
【化7】

【0155】
{式中、
・R2は、-COOHまたは-COOR9[式中、R9は、C1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表すか、またはR9は、フェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基またはモルホリノエチル基を表し、前記R9は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表し;
・環Dは、非縮合の非置換の5〜6員のヘテロシクリル基を表す}
を表す、
本発明の化合物が提供される。
【0156】
より好ましい実施態様(2)において、本発明は、(a)式(IA’)もしくは(IB’):
【0157】
【化8】

【0158】
[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・L2は、-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3は、非置換のC1〜4アルキレン基を表し;
・A2は、非縮合のフェニルを表し、該フェニルは、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・xは、0または1であり;
・Alk1は、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されており;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0159】
特に好ましい実施態様(3)において、本発明は、(a)式(IC)もしくは(ID):
【0160】
【化9】

【0161】
[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0162】
本発明の好ましい化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸である。
【0163】
特に好ましい本発明の化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
である。
【0164】
本発明で最も好ましい本発明の化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
である。
【0165】
本発明が関係する化合物は、IKK、特にIKKβのキナーゼ活性の阻害剤であり、したがって、IKK活性およびNF-κBカスケードによって調節される疾患の治療に有用である。かかる疾患としては、腫瘍性/増殖性疾患、免疫疾患および炎症性疾患が挙げられる。具体的には、該化合物の用途としては、肝細胞癌または黒色腫などであるが、さらに腸癌、卵巣癌、頭頸部扁平上皮癌および子宮頸部扁平上皮癌、胃癌もしくは肺癌、退形成乏突起膠腫、多形神経膠芽腫または髄芽細胞腫も含めた癌の治療;ならびに関節リウマチ、乾癬、炎症性腸疾患、クローン病、潰瘍性大腸炎、慢性閉塞性肺疾患、喘息、多発性硬化症、II型糖尿病などの糖尿病、アトピー性皮膚炎、移植片対宿主病または全身性エリテマトーデスの治療が挙げられる。
【0166】
任意の特定の患者に対する具体的な用量レベルは、用いられる特定の化合物の活性、年齢、体重、全体的な健康、性別、食事、投与時間、投与経路、排泄速度、薬物の組み合わせ、および治療を受けている特定の疾患の重症度を含む種々の要因に依存するであろうことは、理解されるであろう。最適な用量レベルおよび投与頻度は、臨床試験によって決定されることになるが、例示的な投薬量は、1日あたり0.1〜1000 mgである。
【0167】
本発明が関係する化合物は、その薬物動態学的性質と合致する任意の経路により投与するために、調製することができる。経口投与可能な組成物は、錠剤、カプセル剤、散剤、顆粒剤、ロゼンジ、液体製剤またはゲル製剤、例えば経口液剤もしくは経口懸濁液、局所用溶液もしくは局所用懸濁液、または無菌の非経口溶液もしくは無菌の非経口懸濁液などの形態とすることができる。経口投与用の錠剤およびカプセル剤は、単位用量の提示形態とすることができ、慣用の賦形剤、例えば結合剤、例えばシロップ、アラビアゴム、ゼラチン、ソルビトール、トラガントもしくはポリビニル-ピロリドン;充填剤、例えばラクトース、糖、トウモロコシデンプン、リン酸カルシウム、ソルビトールもしくはグリシン;錠剤化滑沢剤(tabletting lubricant)、例えばステアリン酸マグネシウム、タルク、ポリエチレングリコールもしくはシリカ;崩壊剤、例えばジャガイモデンプン、または許容される湿潤剤、例えばラウリル硫酸ナトリウムなどを含んでいてもよい。錠剤は、通常の製薬プラクティスにおいて周知の方法に従ってコーティングしてもよい。経口液体製剤は、例えば、水性もしくは油性の懸濁液、溶液、エマルション、シロップ剤もしくはエリキシル剤の形態とすることができ、または使用前に水もしくは他の適切な媒体で再構成するための乾燥製品として提示することができる。かかる液体製剤は、慣用の添加剤、例えば懸濁剤、例えばソルビトール、シロップ、メチルセルロース、グルコースシロップ、ゼラチン、水素化食用脂;乳化剤、例えばレシチン、ソルビタンモノオレアートまたはアラビアゴム;非水性媒体(食用油を含み得る)、例えばアーモンドオイル、分留されたヤシ油、グリセリンなどの油性エステル、プロピレングリコールまたはエチルアルコール;保存剤、例えばp-ヒドロキシ安息香酸メチルもしくはp-ヒドロキシ安息香酸プロピルまたはソルビン酸、および所望される場合は慣用の香味剤または着色剤を含んでいてもよい。
【0168】
皮膚への局所的な適用については、薬物を、クリーム、ローションまたは軟膏になるように調合することができる。薬物に使用することができるクリーム製剤または軟膏製剤は、例えば英国薬局方などの薬剤学の標準的な教科書に記述されている、当該技術分野で周知の慣用の製剤である。
【0169】
吸入による局所適用については、例えば、圧力駆動のジェット式噴霧器もしくは超音波噴霧器によって、または好ましくは、微粒子化した粉末、例えば吸入用カプセル剤または他の「乾燥粉末」送達系の、噴射剤で駆動される計量されたエアロゾルの投与または噴射剤なしの投与によって、エアロゾルを送達するために、薬物を製剤化することができる。かかる吸入される製剤中には、賦形剤、例えば、噴射剤(例えば計量されたエアロゾルの場合にはフリゲン(Frigen))、界面活性物質、乳化剤、安定剤、保存剤、香味料および充填剤(例えば粉末吸入器の場合にはラクトース)などを存在させることができる。吸入のためには、患者に適した吸入技術を用いて、最適な粒径のエアロゾルを発生させ、投与することができる、多くの装置(apparata)を利用できる。特に粉末吸入器の場合、計量されたエアロゾルについては、アダプター(スペーサー、エキスパンダ)およびセイヨウナシ形の容器(例えばNebulator(登録商標)、Volumatic(登録商標))およびパッファスプレー(puffer spray)を放出する自動装置(Autohaler(登録商標))の使用に加えて、いくつかの技術的解決策が利用できる(例えばDiskhaler(登録商標)、Rotadisk(登録商標)、Turbohaler(登録商標)または例えばヨーロッパ特許出願第EP 0 505 321号に記載された吸入器)。
【0170】
眼への局所的な適用については、薬物を、適切な無菌の水性または非水性の媒体中の溶液または懸濁液になるように調合することができる。添加剤、例えばメタ重亜硫酸ナトリウムまたはエデト酸二ナトリウム(disodium edeate)などの緩衝剤;殺菌剤および殺真菌剤を含む保存剤、例えば酢酸フェニル水銀もしくは硝酸フェニル水銀、塩化ベンザルコニウムまたはクロルヘキシジンなど、ならびに増粘剤、例えばヒプロメロースなど、も含めることができる。
【0171】
活性成分はまた、無菌の媒体に入れて非経口的に投与することもできる。使用する媒体および濃度に応じて、薬物を、媒体中に懸濁させるか、または溶解させることができる。有利には、局所麻酔薬、保存剤および緩衝剤などの補助剤を媒体中に溶解させることができる。
【0172】
本発明の化合物は、いくつかの公知の薬学的に活性な物質とともに使用することができる。例えば、本発明の化合物は、細胞毒、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤およびモノクローナル抗体(例えば成長因子受容体に対するもの)とともに使用することができる。好ましい細胞毒としては、例えば、タキサン類(taxanes)、プラチン類(platins)、代謝拮抗剤、例えば5-フルオロウラシル(5-fluoracil)、トポイソメラーゼ阻害剤など、が挙げられる。したがって、式(IA)もしくは(IB)のアミノ酸誘導体、その互変異性体、またはその薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物を含む、本発明の医薬は、典型的には、細胞毒、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体をさらに含む。
【0173】
さらに、本発明は、
(a)(i)式(IA)もしくは(IB)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(ii)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物;
(b)細胞毒性薬、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体;ならびに
(c)薬学的に許容される担体または希釈剤
を含む、医薬組成物を提供する。
【0174】
さらに、ヒトまたは動物の身体の治療に、別々に、同時に、または連続的に使用するための、
(a)(i)式(IA)もしくは(IB)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(ii)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物;ならびに
(b)細胞毒性薬、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体
を含む、製品も提供する。
【0175】
合成
本発明が関係する式(IA)または(IB)の化合物の合成については、複数の合成戦略が存在するが、すべてのものが、合成有機化学者に知られた公知の化学に依存している。したがって、式(IA)または(IB)に従う化合物は、標準的な文献に記載された、当業者に周知の手順に従って、合成することができる。典型的な文献の出所は、「Advanced organic chemistry」, 第4版 (Wiley), J March、「Comprehensive Organic Transformation」, 第2版 (Wiley), R.C. Larock、「Handbook of Heterocyclic Chemistry」, 第2版 (Pergamon), A.R. Katritzky、総説記事、例えば「Synthesis」、「Acc. Chem. Res.」、「Chem. Rev」に見出されるものなど、もしくはオンラインでの標準的な文献探索によって特定される一次的な文献の出所であるか、または「Chemical Abstracts」もしくは「Beilstein」などの二次的な出所からのものである。
【0176】
本発明の化合物は、以下に一般的に記載され、本明細書中で以下の実施例においてより具体的に記載される、いくつかの方法によって調製することができる。以下に記載される反応においては、反応性官能基、例えば、ヒドロキシル基、アミノ基およびカルボキシ基が最終生成物に望まれる場合、これらの官能基が反応に不必要に関与することを避けるために、該官能基を保護することが必要な場合がある[例えばGreene, T.W., 「Protecting Groups in Organic Synthesis」, John Wiley and Sons, 1999を参照]。標準的なプラクティスと組み合わせて、慣用の保護基を使用することができる。場合によっては、脱保護が、一般式(IA)または(IB)の化合物の合成の最終工程となることがあり、本明細書中で以下に記載される本発明に従う方法は、かかる保護基の除去に及ぶことを理解されたい。
【0177】
アミノ酸エステル構成要素は、いくつかの方法で調製することができる。スキーム1は、本願のために該構成要素の調製に用いた主な経路を示している。当業者には、やはりこれらの中間体の調製を達成する他の方法があることは、明らかであろう。
【0178】
スキーム1 アミノ酸エステル構成要素の調製の一般的スキーム(R7、R8およびR9は、本明細書中で定義した通りであり、Pは、適切な保護基である)
【0179】
【化10】

【0180】
スキーム2 チオフェンカルボキサミド構成要素Cの調製のスキーム
【0181】
【化11】

【0182】
当業者には、スキーム2に示した一般的経路は、利用可能ないくつかの経路の1つであることは、明らかであろう。例えば、適切なチオフェンカルボキサミド母核の調製方法は、WO 03/104218に詳細に記載されており、その内容は、その全体が参照によって本明細書中に援用される。
【0183】
スキーム3 L1がアルキルであり、A1がフェニルであり、L2が結合であり、x=0であり、Alk1がメチルであり、R7、R8およびR9が本明細書中で定義した通りである化合物の調製の一般的スキーム)
【0184】
【化12】

【0185】
スキーム3は、対応するベンズアルデヒドによるアミノ酸エステルの還元的アミノ化を含み、その後にN-保護およびヘック(Heck)反応が続き、重要なアルデヒド中間体を生じさせる、方法を示している。この中間体は、2-シアノアセトアミドを用いて、チオフェン環に転換される。基L1の性質が合成経路の選択に影響することになるのは、当業者には明らかであろう。当業者は、かかる化合物の合成の合成可能性を容易に認識する。
【0186】
スキーム4 酸の、その対応するエステルからの調製の一般的スキーム(L1、A1、L2、x、Alk1、R7、R8およびR9は、本明細書中で定義した通りである)
【0187】
【化13】

【0188】
本明細書中に記載したエステルのカルボン酸誘導体は、その親のエステルから、加水分解によって、容易に調製することができる。当業者には、除去するエステル基に応じて、塩基性条件または酸性条件のいずれを用いることができるかは、明らかであろう。
【実施例】
【0189】
以下の実施例は、いくつかの特定の本発明の化合物の調製および性質を説明するものである。次の略語が使用される。
MeOH=メタノール
EtOH=エタノール
EtOAc=酢酸エチル
Boc=tert-ブトキシカルボニル
DCE=ジクロロエタン
DCM=ジクロロメタン
DMA=N,N-ジメチルアセトアミド
DME=1,2-ジメトキシエタン
DMF=ジメチルホルムアミド
DMSO=ジメチルスルホキシド
Bu4NBr=テトラブチルアンモニウムブロミド
MeCN=アセトニトリル
TFA=トリフルオロ酢酸
THF=テトラヒドロフラン
Na2CO3=炭酸ナトリウム
HCl=塩酸
NaH=水素化ナトリウム
NaHCO3=炭酸水素ナトリウム
Pd/C=パラジウム炭素
N2=窒素
Na2SO4=硫酸ナトリウム
Et3N=トリエチルアミン
STAB=ナトリウムトリアセトキシボロヒドリド
MgSO4=硫酸マグネシウム
EDCI=N-(3-ジメチルアミノプロピル)-N′-エチルカルボジイミド塩酸塩
Et2O=ジエチルエーテル
LiOH=水酸化リチウム
ELS=蒸発光散乱
TLC=薄層クロマトグラフィー
mL=ミリリットル
g=グラム
mg=ミリグラム
mol=モル
mmol=ミリモル
LCMS=高速液体クロマトグラフィー/質量分析法
NMR=核磁気共鳴
RT=室温
sat.=飽和水溶液
【0190】
市販の試薬および溶媒(HPLCグレード)は、さらに精製することなく使用した。溶媒は、BuchiロータリーエバポレーターまたはVirTis Benchtop SLC凍結乾燥機を用いて除去した。マイクロ波照射は、Biotage InitiatorTM Eightマイクロ波シンセサイザーを用いて行なった。特定の水素化は、Thales Technology H-Cube HC-2連続水素化装置を用いて行った。フラッシュクロマトグラフィーカラムによる化合物の精製は、Fluorochemから入手した、粒径40〜63 μm(230〜400メッシュ)のシリカゲルを用いて行った。分取HPLCによる化合物の精製は、逆相AxiaTM分取用(prep)Luna C18カラム(10 μm、100×21.2 mm)、10分間にわたる0%B〜100%B(A=水+0.05%TFA、B=アセトニトリル)のグラジエント、流速=25 mL/min、254 nmでのUV検出を用いて、Gilsonシステムで行った。
【0191】
1H NMRスペクトルは、重水素化溶媒中で、Bruker 300 MHz AV分光計で記録した。化学シフトδは、百万分率単位のものである。薄層クロマトグラフィー(TLC)分析は、Kieselgel 60 F254(Merck)プレートを用いて行い、UV光を用いて可視化した。
【0192】
分析用HPLC/MSは、逆相Luna C18カラム(3 μm、50×4.6 mm)、2.25分間にわたる5%B〜95%B(A=水+0.1%のギ酸、B=アセトニトリル+0.1%のギ酸)のグラジエント、流速=2.25 mL/minを用いて、Agilent HP1100 LCシステムで行った。UVスペクトルは、G1315B DAD検出器を用いて、220 nmおよび254 nmで記録した。質量スペクトルは、LC/MSD SL G1956B検出器で、150〜800のm/z範囲にわたって得た。データは、ChemStationおよびChemStation Data Browserソフトウェアを用いて、積分し、報告した。
【0193】
図1 本明細書中に記載した実施例の合成において、次の構成要素を使用した。
【0194】
【化14】

【0195】
構成要素A スキーム1、経路3で概説した方法を用いて、シクロペンチルL-ロイシナートを調製した。
L-ロイシン(5 g、30.5 mmol)を含むシクロヘキサン(150 mL)のスラリーに、シクロペンタノール(27.5 mL、305 mmol)およびp-トルエンスルホン酸(6.33 g、33.3 mmol)を加えた。反応には、ディーン・スターク(Dean-Stark)受け器を取り付け、完全に溶解させるために135℃に加熱した。この温度を12時間の間維持し、その時間の後、反応を完結させた。反応をRTまで冷却すると、白色固体が沈殿した。この固体をろ過し、EtOAcで洗浄してから、減圧下で乾燥させた。所要の生成物をトシル酸塩として単離した(10.88 g、85 %)。m/z = 200 [M+H]+; 1H NMR (300 MHz, CD3OD) δ: 1.01 (6H, t, J=5.8 Hz), 1.54-2.03 (11H, m), 2.39 (3H, s), 3.96 (1H, t, J=6.5 Hz), 5.26-5.36 (1H, m), 7.25 (2H, d, J=7.9 Hz), 7.72 (2H, d, J=8.3 Hz)。
【0196】
構成要素B tert-ブチルL-ロイシナートは、市販されている(Novabiochem、カタログ番号:04-12-5108)。
【0197】
構成要素C WO 03/104218に記載された方法を用いて、5-ブロモ-2-(カルバモイルアミノ)チオフェン-3-カルボキサミドを調製した。
【0198】
(実施例)
実施例1 シクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナート
【0199】
【化15】

【0200】
スキーム5 構成要素Aからの実施例1の調製方法
【0201】
【化16】

【0202】
中間体1a 以下のように、シクロペンチルN-(tert-ブトキシカルボニル)-L-ロイシナートを調製した。
構成要素A(5 g、13.5 mmol)を含むDCM(100 mL)に、Et3N(3.76 mL、26.9 mmol)およびジ-tert-ブチルジカルボナート(3.24 g、14.8 mmol)を加えた。この反応混合物を室温で18時間攪拌し、次いでDCM(100 mL)で希釈し、1M HCl、NaHCO3 sat.で、次いでブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮して所望の生成物を無色の油状物として得、これをさらなる精製も特徴付けもせずに先に進めた(4 g、収率100%)。
【0203】
中間体1b 以下のように、中間体1aからシクロペンチルN-(tert-ブトキシカルボニル)-N-(4-ヨードベンジル)-L-ロイシナートを調製した。
中間体1a(1.8 g、6 mmol))およびBu4NI(476 mg、1.2 mmol)を含むDMF(50 mL)に、0℃で、NaH(480 mg、12 mmol)を含むDMF(3 mL)を加えた。反応を5分間攪拌してから、4-ヨード-ベンジルブロミド(3.56g、12 mmol)を加えた。この反応混合物を室温まで温まらせ、反応を完結させるために4時間攪拌した。EtOAcを加え(200 mL)、有機層を水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(10%EtOAc/ヘプタン)により精製することにより、所要の生成物が固体として得られ(2.56 g、収率82%)、m/zは516 [M+H]+であった。
【0204】
中間体1c 以下のように、中間体1bからシクロペンチルN-(tert-ブトキシカルボニル)-N-[4-(3-オキソプロピル)ベンジル]-L-ロイシナートを調製した。
【0205】
中間体1b(2.56 g、4.9 mmol)を含むDMF(17 mL)に、Pd(OAc)2(34 mg、0.15 mmol)、アリルアルコール(0.51 mL、7.5 mmol)、NaHCO3(1.04 g、12.4 mmol)、Bu4NBr(1.6 g、4.9 mmol)および4Åモレキュラーシーブ(965 mg)を加えた。この反応混合物を、80℃で2時間加熱した。室温まで冷却し、混合物をセライトを通してろ過し、DMFおよび水で洗浄した。母液をジエチルエーテル(2×50 mL)で抽出し、有機層を水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(30%EtOAc/ヘプタン)により精製することにより、所要の生成物が固体として得られ(1.66 g、収率75%)、m/zは446 [M+H]+であった。
【0206】
中間体1d 以下のように、中間体1cからシクロペンチルN-{4-[(5-アミノ-4-カルバモイル-2-チエニル)メチル]ベンジル}-N-(tert-ブトキシカルボニル)-L-ロイシナートを調製した。
2-シアノ-アセトアミド(306 mg、3.61 mmol)、硫黄(116 mg、3.61 mmol)および中間体1c(1.61 g、3.61 mmol)の混合物を含むDMF(12 mL)に、トリエチルアミン(0.5 mL、3.61 mmol)を滴下した。生じた混合物を室温で18時間攪拌し、次いで水中に注ぎ、EtOAc(2×100 mL)で抽出した。合わせた有機層をブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(50%EtOAc/ヘプタン)による精製により、所要の生成物(710 mg、収率36%)が得られ、m/zは544 [M+H]+であった。
【0207】
中間体1e 以下のように、中間体1dからシクロペンチルN-(tert-ブトキシカルボニル)-N-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体1d(300 mg、0.55 mmol)の無水DCM(6 mL)溶液に、0℃で、窒素下で、クロロスルホニルイソシアナート(58 μL、0.67 mmol)を滴下した。反応混合物を室温まで温まらせ、反応を完結させるために3時間攪拌した。反応を水(2 mL)でクエンチし、10分間攪拌し、EtOAcとNaHCO3satとの間で分配した。有機層をブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(5%MeOH/DCM)により精製することにより、所要の生成物(100 mg、収率31%)が得られ、m/zは587 [M+H]+であった。
【0208】
実施例1 以下のように、中間体1eからシクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体1e(100 mg)をDCM(2 mL)およびTFA(2 mL)に溶解し、室温で18時間攪拌した。この反応混合物を真空中で濃縮し、メタノールに溶解し、SCX陽イオン交換樹脂によって精製した。これに続くGilson分取HPLCによる精製により、所要の生成物が淡褐色の固体として得られた(60 mg、収率72%)。
【0209】
LCMSによる純度 = 95 %; m/z = 487 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.28-7.18 (4H, q, J=8.1Hz), 6.91 (1H, s), 5.16-5.07 (1H, m), 3.98 (2H, s), 3.73 (1H, d, J=12.9Hz), 3.63 (1H, d, J=12.9Hz), 3.24 (1H, t, J=7.3Hz), 1.94-1.56 (9H, m), 1.51-1.43 (1H, m), 0.91 (3H, d, J=6.6Hz), 0.85 (3H, d, J=6.6Hz)。
【0210】
実施例2 tert-ブチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナート
【0211】
【化17】

【0212】
スキーム6 構成要素Bからの実施例2の調製方法
【0213】
【化18】

【0214】
中間体2a 以下のように、tert-ブチルN-(4-ヨードベンジル)-L-ロイシナートを調製した。
構成要素B(2.89 g、12.9 mmol)を含むDCM(40 mL)に、4-ヨードベンズアルデヒド(2 g、8.63 mmol)を加えた。反応を2時間攪拌してから0℃まで冷却し、STAB(5.47 g、25.86 mmol)を少しずつ加えた。反応を室温まで温まらせ、18時間攪拌した。この反応混合物をDCM(100 mL)で希釈し、1M HCl、NaHCO3sat.およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(20%EtOAc/ヘプタン)により精製することにより所要の生成物(2.81 g、収率80%)が得られ、m/zは404 [M+H]+であった。
【0215】
中間体2b 以下のように、中間体2aからtert-ブチルN-(tert-ブトキシカルボニル)-N-(4-ヨードベンジル)-L-ロイシナートを調製した。
中間体2a(2.8 g 7 mmol)を含むアセトニトリル(30 mL)に、ジ-tert-ブチルジカルボナート(3.08 g、14.1 mmol)を加えた。反応を室温で18時間攪拌させておいてから、減圧下で濃縮した。粗製の残渣をEtOAcに溶解し、水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(3%EtOAc/ヘプタン)により精製することにより、所要の生成物(3.5 g、収率100%)が得られ、これをさらなる精製も特徴付けもせずに先に進めた。
【0216】
中間体2c〜2eを、実施例1について記載した方法と同じ方法を用いて調製した。
【0217】
実施例2 以下のように、中間体2eからtert-ブチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体2e(20 mg)を含むジオキサン(2 mL)に、0℃で、窒素下で、4M HCL/ジオキサン(0.5 mL)を加えた。反応を0℃で2時間攪拌してからNaHCO3 satでクエンチし、減圧下で濃縮した。残渣をメタノールに溶解し、SCX陽イオン交換樹脂によって精製して、所要の生成物(8 mg)を得た。
LCMSによる純度 = 85 %; m/z = 475 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.35 (2H, d, J=8.1Hz), 7.30 (2H, d, J=8.1Hz), 6.96 (1H, s), 4.03 (2H, s), 3.95-3.80 (2H, m), 2.25-2.16 (1H, m), 1.85-1.65 (2H, m), 1.51 (9H, s), 1.17-1.11 (1H, m), 0.96 (3H, d, J=6.6Hz), 0.92 (3H, d, J=6.6Hz)。
【0218】
実施例3 シクロペンチルN-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシナート
【0219】
【化19】

【0220】
スキーム7 構成要素Aおよび構成要素Cからの実施例3の調製方法
【0221】
【化20】

【0222】
中間体3a 以下のように、4-[(E)-2-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)ビニル]ベンズアルデヒドを調製した。
4-ブロモベンズアルデヒド(1.818 g、9.83 mmol)、酢酸パラジウム(0.110 g、0.491 mmol)および1,10-フェナントロリン(0.089 g、0.491 mmol)をバイアルに仕込み、その後、バイアルをN2でパージした。無水アセトニトリル(15 mL)を加え、室温で攪拌した。トリエチルアミン(2.74 ml、19.65 mmol)およびビニルボロン酸ピナコールエステル(2.0 ml、11.79 mmol)を加え、この反応混合物を60℃に18時間加熱した。17時間後のLCMS分析では、わずか15%の生成物および75%の4-ブロモベンズアルデヒド出発物質が示された。さらなる酢酸パラジウム(55 mg)および1,10-フェナントロリン(45 mg)をMeCN溶液として加え、反応をさらに24時間、60℃で加熱した。反応を冷却し、2M HClを加え、ジエチルエーテルで抽出した。有機層を2M HClおよびブラインで洗浄し、乾燥させ(MgSO4)、真空中で濃縮した。カラムクロマトグラフィー(50〜100%DCM/ヘキサンにより精製することにより、所要の生成物が淡黄色の固体として得られ(0.54 g、収率22%)、m/zは259 [M+H]+であった。
【0223】
中間体3b 以下のように、中間体3aから2-(カルバモイルアミノ)-5-[(E)-2-(4-ホルミルフェニル)ビニル]チオフェン-3-カルボキサミドを調製した。
構成要素C(453 mg、1.714 mmol)およびテトラキスパラジウム(198 mg、0.171 mmol)に、中間体3a(531 mg、2.057 mmol)を加え、N2でパージした。重炭酸ナトリウム飽和水溶液1 mLとともに、DME(7 mL)を加えた。この混合物を、反応を完結させるために80℃で20時間加熱した。反応混合物を冷却し、1M HCl(200 mL)の中に注ぎ、EtOAc(300 mL)中へ抽出した。合わせた有機層を乾燥させ(MgSO4)、真空中で濃縮して、生成物が黄色固体として得られ(342 mg、収率60.7%)、m/zは314 [M-H]+であった。
【0224】
中間体3c 以下のように、中間体3bからシクロペンチルN-(4-{(E)-2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]ビニル}ベンジル)-L-ロイシナートを調製した。
中間体3b(249 mg、0.790 mmol)および構成要素A(157 mg、0.790 mmol)をTHF(15 mL)および酢酸(15 mL)に溶解し、室温で30分間攪拌した。STAB(502 mg、2.369 mmol)を少しずつ加え、反応を48時間攪拌した。2M HClを加え、生成物をEtOAc中へ抽出した。合わせた有機物抽出液を水で洗浄し、乾燥させ(MgSO4)、真空中で濃縮して、オレンジ色の油状固体477 mgを得た。カラムクロマトグラフィー(2〜4%MeOH/DCM)およびそれに続くSCX陽イオン交換樹脂により精製することにより、所要の生成物が得られ(40 mg、収率10%)、m/zは499 [M+H]+であった。
【0225】
実施例3 以下のように、中間体3cからシクロペンチルN-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシナートを調製した。
中間体3c(40 mg、0.080 mmol)をメタノール(6 mL)に溶解し、Pd/CaCO3(Pbを触媒毒とする)を用いて、1 barの圧力で、3 mL/minでH-Cube水素化装置を通るようにポンピングした。減圧下でメタノールを除去し、カラムクロマトグラフィー(3〜5%MeOH/DCM)によって粗製の残渣を精製し、標題の化合物を得た(15 mg、収率38%)。
LCMSによる純度 = 96 %; m/z = 501 [M+H]+; 1H NMR (300 MHz, DMSO-d6) 10.85 (1H, s), 7.50 (1H, br s), 7.20 (4H, m), 7.15 (1H, br s), 7.01 (1H, s), 6.78 (2H, br s), 5.1 (1H, m), 3.70 (1H, d, J=6.5Hz), 3.50 (1H, d, J=6.3Hz), 3.05 (1H,s), 2.23 (1H, m), 1.8 (2H, m), 1.70-1.50 (7H, bm), 1.35 (2H, m), 0.82 (3H, d, J=6.8Hz), 0.79 (3H, d, J=6.4Hz)。
【0226】
実施例4 シクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチニル}ベンジル)-L-ロイシナート
【0227】
【化21】

【0228】
スキーム8 構成要素Aおよび構成要素Cからの実施例4の調製方法
【0229】
【化22】

【0230】
中間体4a シクロペンチルN-(4-エチニルベンジル)-L-ロイシナート
構成要素A(918 mg、4.6 mmol)のDCM(60 mL)溶液に、4-エチニルベンズアルデヒド(500 mg、3.84 mmol)を加えた。反応を3時間攪拌してから、0℃に冷却した。次いで、STAB(2.44 g、11.5 mmol)を少しずつ加え、室温で18時間攪拌を続けた。反応をDCM(50 mL)で希釈し、1M HCL(100 mL)、NaHCO3 sat(100 mL)、ブライン(50 mL)で洗浄し、乾燥させ(MgSO4)、真空中で濃縮した。カラムクロマトグラフィー(25%EtOAc/ヘプタン)により精製することにより所要の生成物(0.878 g、収率73%)が得られ、m/zは314 [M+H]+であった。
【0231】
実施例4 以下のように、中間体4aからシクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチニル}ベンジル)-L-ロイシナートを調製した。
DMA(2.5 mL)およびEtOH(2.5 mL)の中で、中間体4a(200 mg、0.64 mmol)を構成要素C(91 mg、0.34 mmol)と混合した。次いで、ジ-イソプロピルエチルアミン(0.184 mL、1.0 mmol)およびヨウ化銅(20 mg、0.10 mmol)を加え、溶液を窒素を用いて15分間脱気した。次いで、(1,1-ビス(ジフェニルホスフィノ)--フェロセンジクロロパラジウム(8 mg、8wt%)を加え、反応を65℃に18時間加熱した。反応混合物を冷却し、セライトを通してろ過し、Gilson分取HPLCによって精製した。所要の生成物を白色固体として単離した(17 mg、収率10%)。
LCMSによる純度 = 90 %; m/z = 497 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.61 (2H, d, J=6.5Hz), 7.55 (2H, d, J=6.8Hz), 7.45 (1H, s), 5.31 (1H, m), 4.25 (2H, m), 4.05 (1H, m), 2.05-1.65 (11H, bm), 1.00 (6H, m)。
【0232】
実施例5 N-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシン
【0233】
【化23】

【0234】
スキーム9 実施例1からの実施例5の調製方法
【0235】
【化24】

【0236】
実施例5 以下のように、実施例1からN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシンを調製した。
実施例1(50 mg、0.1 mmol)のTHF(2 mL)および水(2 mL)の溶液に、水酸化リチウム(25 mg、1 mmol)を加えた。この反応混合物を、反応を完結させるために40℃で18時間加熱した。反応を室温まで冷却し、THFを減圧下で除去してから、水で希釈し、酢酸でpHを4に調節した。沈殿をろ過し、水およびジエチルエーテルで洗浄してから、Gilson分取HPLCによって精製した。所要の生成物を白色固体として単離した(11 mg、収率26%)。
LCMSによる純度 = 94 %; m/z = 419 [M+H]+; 1H NMR (300 MHz, DMSO-d6) 10.88 (1H, s), 7.58 (1H, br s), 7.33 (2H, d, J=7.8Hz), 7.23 (2H, d, J=7.8Hz), 7.16 (1H, br s), 7.06 (1H, s), 6.83 (2H, br s),3.94 (2H, s), 3.90 (1H, d,J=13.2Hz), 3.75 (1H, d, J=13.2Hz), 3.13 (1H, t, J=7.1Hz), 1.90-1.70 (1H, m), 1.52-1.40 (2H, m),0.85 (3H, d, J=6.6Hz), 0.79 (3H, d, J=6.6Hz)。
【0237】
実施例6 N-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシン
【0238】
【化25】

【0239】
スキーム10 実施例3からの実施例6の調製方法
【0240】
【化26】

【0241】
実施例6を、実施例5について記載した方法と同じ方法を用いて調製した。
LCMSによる純度 = 97 %; m/z = 431 [M-H]+; 1H NMR (300 MHz, DMSO-d6) 10.85 (1H, s), 7.49 (1H, br s), 7.22 (2H, d, J=7.8Hz), 7.15 (2H, d, J=7.8Hz), 7.10 (1H, br s), 6.99 (1H, s), 6.75 (2H, br s), 3.75 (1H, d, J=13.2Hz), 3.50 (1H, d, J=13.2Hz), 3.13 (1H, m), 1.75 (1H, m), 1.40-1.20 (3H, bm), 0.83 (3H, d, J=6.6Hz), 0.73 (3H, d, J=6.6Hz)。
【0242】
生物学的アッセイ
IKKβ酵素アッセイ
化合物がIKKβキナーゼ活性を阻害する能力を、Invitrogen(Paisley,UK)が実施するアッセイで測定した。Z’−LYTETM生化学アッセイは、蛍光ベースの共役酵素形式を用い、タンパク質分解性の切断に対する、リン酸化ペプチド及び非リン酸化ペプチドの感受性の差に基づく。ペプチド基質は、2つのフルオロフォア(各末端に1つずつ)で標識され、これらはFRETペアを構成する。一次反応において、キナーゼは、ATPのγ−リン酸を合成FRETペプチド中の単一のセリン又はスレオニン残基に転移させる。二次反応では、部位特異的プロテアーゼが非リン酸化FRETペプチドを認識し、切断する。FRETペプチドのリン酸化は、発色試薬(Development Reagent)による切断を抑制する。切断は、FRETペプチド上のドナーフルオロフォア(即ち、クマリン)とアクセプターフルオロフォア(即ち、フルオレセイン)との間のFRETを破壊するが、未切断のリン酸化FRETペプチドはFRETを維持する。400nmでのドナーフルオロフォアの励起後のドナー発光対アクセプター発光の比率(発光比(Emission Ratio))を計算する放射測定法を使用して、反応の進行を定量する。
【0243】
最終的な10μLのキナーゼ反応(Kinase Reaction)は、50mM HEPES(pH7.5)、0.01% BRIJ−35、10mM MgCl2、1mM EGTA中0.9〜8.0ngのIKBKB(IKKβ)、2μM Ser/Thr 05 Peptide及びATPからなる。このアッセイは、Km又はその近傍のATP濃度で実施される。室温で60分のキナーゼ反応インキュベーション後、1:128希釈の発色試薬を5μL添加する。アッセイプレートを室温でさらに60分間インキュベートし、蛍光プレートリーダーで読み取る。
【0244】
二連のデータポイントを、試験化合物のDMSO中ストック溶液の1/3 log希釈系列から生成する。9回の希釈工程を10μMの最高濃度から行い、「化合物なし」のブランクを含める。IDBSのXlfitソフトウェアを使用して、データを収集し分析する。用量反応曲線は、モデル番号205(シグモイダル用量反応モデル)にフィットさせた曲線である。得られた曲線から、50%阻害を与える濃度を決定し、報告する。
【0245】
THP−1細胞のLPS刺激
THP−1細胞を、V底96ウェルの組織培養物処理したプレート中、4×104細胞/ウェルの密度で100μlプレートし、5% CO2中37℃で16時間インキュベートした。100μlの組織培養培地中の阻害剤を添加して2時間後、細胞を1μg/mlの最終濃度のLPS(E coli株005:B5、Sigma)で刺激し、5% CO2中37℃で6時間インキュベートした。TNF−αレベルを、サンドイッチELISA(R&D Systems #QTA00B)によって無細胞上清から測定した。
【0246】
ヒト全血のLPS刺激
ヘパリン処理バキュテナー(Becton Dickinson)を使用した静脈穿刺によって全血を採取し、等体積のRPMI1640組織培養培地(Sigma)中に希釈した。V底96ウェルの組織培養物処理したプレートに100μlをプレートした。100μlのRPMI1640培地中の阻害剤を添加して2時間後、血液を100ng/mlの最終濃度のLPS(E coli株005:B5、Sigma)で刺激し、5% CO2中37℃で6時間インキュベートした。TNF−αレベルを、サンドイッチELISA(R&D Systems #QTA00B)によって無細胞上清から測定した。
【0247】
破壊細胞アッセイ
特定の基R2を含む化合物が1種以上の細胞内カルボキシルエステラーゼ酵素によって−COOH基に加水分解され得るか否かを決定するために、化合物を以下のアッセイで試験することもできる:
【0248】
細胞抽出物の調製
U937又はHUT78腫瘍細胞(約109)を、4体積のDulbeccos PBS(約1リットル)で洗浄し、4℃で10分間525gでペレット化する。これを2回繰り返し、最終的な細胞ペレットを35mlの冷ホモジナイジングバッファー(Trizma 10mM、NaCl 130mM、CaCl2 0.5mM、pH7.0、25℃)中に再縣濁する。ホモジネートを窒素キャビテーション(4℃で50分間700psi)によって調製する。このホモジネートを氷上に維持し、Leupeptin 1μM、Aprotinin 0.1μM、E64 8μM,Pepstatin 1.5μM、Bestatin 162μM、Chymostatin 33μMの最終濃度の阻害剤カクテルを添加する。1500rpmで10分間遠心分離して細胞ホモジネートを清澄化した後、得られた上清をエステラーゼ活性の供給源として使用し、必要になるまで−80℃で保存する。
【0249】
エステル開裂の測定
対応するカルボン酸へのエステルの加水分解は、上のように調製した細胞抽出物を使用して測定することができる。この趣旨で、細胞抽出物(総アッセイ体積0.5ml中約30μg)を、Tris−HCl 25mM、125mM NaClバッファー、pH7.5、25℃中で、37℃でインキュベートする。次いで、ゼロ時点で2.5mMの最終濃度のエステル(基質)を添加し、サンプルを適切な時間(通常0分間又は80分間)にわたり37℃でインキュベートした。2×体積のアセトニトリルを添加して反応を停止させる。ゼロ時点のサンプルについては、エステル化合物の前にアセトニトリルを添加する。12000gで5分間の遠心分離後、サンプルを、エステル及びその対応するカルボン酸について、LCMS(Sciex API 3000、HP1100バイナリポンプ、CTC PAL)によって室温にて分析する。クロマトグラフィーは、MeCN(75×2.1mm)カラム及び水/0.1%ギ酸中5〜95%のアセトニトリルの移動相に基づいた。加水分解速度はpg/mL/minで表す。
【0250】
インタクト細胞蓄積アッセイ
細胞(4×104/mL)を、5%(v/v)CO2−加湿雰囲気中で、6μmol/Lの化合物を含む培養倍地中37℃でインキュベートした。インキュベーションは、6時間後に、細胞懸濁物の25mLアリコートを4℃で1500rpmで5分間遠心分離することによって終了させた。培養培地上清の0.2mLサンプルを、4体積のアセトニトリルに添加した。上清をデカントした後、残った細胞ペレット(106細胞)を1mLのアセトニトリル中に抽出した。次いで、LC/MS/MS(Sciex API3000)で室温にて、サンプルをエステル及び酸代謝産物について分析した。クロマトグラフィーは、MeCN(75×21mm)カラムと5%〜95%(v/v)のアセトニトリル/水、0.1%(v/v)ギ酸移動相とに基づいた。ゼロ時点のサンプルについては、細胞懸濁物を冷却し、エステルを添加して直ぐに遠心分離し、次いで記載されたようにアセトニトリル中に抽出した。細胞中のレベルはng/mLで表す。
【0251】
結果:
本発明の例示的な化合物について生物学的アッセイで得られたIC50値を表1中に示す。IC50値は、以下の3つの範囲のうち1つに割り当てられる:
範囲A:IC50<500nM
範囲B:500nM<IC50<5000nM
範囲C:IC50>5000nM
【0252】
【表1】

【0253】
NT=試験せず。
NR=不適当。実施例5−6は、細胞の内側で開裂されるアミノ酸エステルの結果物カルボン酸のアナログである。これらのカルボン酸は、細胞と接触しても細胞中へ浸透せず、従って、これらのアッセイではTNF−α産生を阻害しない。
【0254】
0時間又は6時間のインキュベーション時間後の、U937(単球細胞株)細胞及びHUT78(非単球細胞株)細胞と関連した実施例1及び5の化合物の濃度を、表2に示す。
【0255】
【表2】

【0256】
表2は、実施例1の化合物(エステル誘導体)が、0時間の時点で、それぞれ420ng/106細胞及び466ng/106細胞の濃度で、U937細胞株及びHUT78細胞株の両方に蓄積できることを示している。6時間のインキュベーション後、実施例5の化合物(酸誘導体)は、U937単球細胞株中に選択的に蓄積し(268ng/106細胞)、対応するHUT78非単球細胞株には蓄積しないことが明らかになった。実施例1の化合物は、ヒトカルボキシルエステラーゼhCE−1(U937などのマクロファージ関連細胞株中にのみ存在する)によって加水分解されるので、実施例4の化合物は、マクロファージ関連細胞中に選択的に蓄積するであろう。6時間の時点でのHUT78中の実施例1の化合物の濃度は、0時間の時点から変化していない(466対465ng/106細胞)。0時間の時点でU937細胞と関連している少量の実施例5は、細胞と培地との分離の間に細胞内で形成された酸を反映している。
【0257】
実施例1の化合物とその親分子(化合物1)との間のin vitro生物学的データの比較を表3に示す。
【0258】
【表3】

【0259】
表3は、実施例1の化合物の酸が、酵素アッセイにおいてその親化合物(化合物1)と類似のIC50を有することを示し、これは、酵素への結合が、エステラーゼモチーフの結合によって破壊されなかったことを示している。実施例1の化合物などのメチレン架橋された化合物(即ち、L1がメチレン基である)は、hCE−1によって加水分解され、結果として酸が細胞中に蓄積する。この酸の蓄積は、実施例1の化合物が、特にヒト全血アッセイにおいて、親化合物よりもかなり強力であるという結果をもたらす。これらのデータは、エステラーゼモチーフの結合と、それにより生じる対応する酸の細胞蓄積によって達成され得る強力な利益を強調する。
【技術分野】
【0001】
本発明は、一連のアミノ酸誘導体、それを含む組成物、その製造方法、およびIKK阻害剤としての医薬におけるその使用に関する。
【背景技術】
【0002】
(発明の背景)
多くの炎症性遺伝子の発現は、転写活性化因子である核因子(nuclear factor)κB(NF-κB)によって制御されている。こうした転写因子は、その発見以来、慢性および急性の炎症性疾患において、中枢的な役割を果たしているのではないかと思われている。現在では、NF-κBの異常な調節はまた、自己免疫疾患および種々の種類の癌の基礎にもなっていると見られている。
【0003】
その活性がNF-κBの活性化に依存する物質としては、腫瘍壊死因子TNF-α、インターロイキン(IL)-6、IL-8およびIL-1βなどのサイトカイン;接着分子E-セレクチン、細胞間接着分子(intercellular adhesion molecule)(ICAM)-1および血管細胞接着分子(vascular cell adhesion molecule)(VCAM)-1;ならびに酵素一酸化窒素シンターゼ(nitric oxide synthase)(NOS)およびシクロオキシゲナーゼ(cyclooxygenase)(COX)-2が挙げられる。NF-κBは、通常は、IκB阻害タンパク質ファミリーのメンバーとの不活性な複合体として、刺激されていない細胞の細胞質中に存在している。しかしながら、細胞活性化時には、IκBは、IκBキナーゼ(IκB kinase)(IKK)によってリン酸化され、その後に分解される。その後、遊離したNF-κBは、核に移行し、そこで炎症性遺伝子の発現を媒介する。
【0004】
IκBファミリーの3つの古典的なメンバーは、IκBα、IκBβおよびIκBεである。これらはすべて、分解され得る前に、2つの重要なセリン残基のリン酸化を必要とする。2つの主要な酵素IKK-αおよびIKK-βが、IκBのリン酸化の原因であるようである。これらの酵素のいずれのドミナントネガティブ(dominant-negative)(DN)型(重要なキナーゼドメイン残基の変異によって、ATPに結合することができない)も、TNF-α、IL-1βおよびLPSによるNF-κBの活性化を抑制することがわかっている。重要なことには、IKK-β DNは、IKK-α DNよりも、はるかに強力な阻害剤であることがわかっている(Zandi E, Cell, 1997, 91, 243)。さらに、IKK-αおよびIKK-βの欠損したマウスの作製により、炎症誘発性の刺激によるNF-κBの活性化が起こるためにはIKK-βが必要であることが確証され、IKK-βがこの経路において主要な役割を果たしていることを示唆する生化学的データが確証されている。実際に、IKK-αは、こうした刺激によるNF-κBの活性化に不要であることが実証されている(Tanaka M, Immunity 1999, 10, 421)。
【0005】
したがって、IKK-βの阻害は、免疫機能の調節のための、したがって自己免疫疾患の治療用薬物の開発のための、潜在的に魅力的な標的となる。例えば、II型糖尿病の治療に関しては、IKK-βの組織特異的欠失またはIKK-βに対する薬理学的ターゲティングなどの方法によってNF-κBシグナル伝達経路を破壊することで、インスリン抵抗性を弱めることができることが示されている(Shoelson Sら, Gastroenterology 2007, 132, 2169)。
【0006】
現在、IKKアイソフォーム、特にIKK-βの強力かつ選択的な阻害剤である一群の化合物が同定されている。したがって、これらの化合物は、例えば、IKKの活性亢進と関連する容態などの種々の増殖性疾患状態、およびNF-κBカスケードによって調節される疾患の治療において、医薬として有用であり得る。
【発明の概要】
【発明が解決しようとする課題】
【0007】
α-一置換グリシンエステルモチーフを細胞内酵素または細胞質受容体のモジュレーターに結合させて、カルボン酸の加水分解生成物の細胞内蓄積の利益を得るという一般概念が、WO 2006/117567に記述されている。しかしながら、この公報は、α,α-二置換グリシンエステルの結合体が、細胞内カルボキシルエステラーゼによって加水分解され得ることを示唆するものではない。細胞内カルボキシルエステラーゼ(carboxyl esterases)、主としてhCE-1、hCE-2およびhCE-3の、α,α-二置換グリシンエステルを加水分解する能力は、これまでは研究されてこなかったようである。
【課題を解決するための手段】
【0008】
(発明の簡単な説明)
本発明は、(a)式(IA)もしくは(IB):
【0009】
【化1】

【0010】
〔式中、
・L1は、C1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表すか、またはL1は、基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-もしくは-(CH2)mNR1(CH2)n-(式中、R1は、C1〜4アルキルであり、mおよびnは、同一であるか、もしくは異なっており、0、1、2、3もしくは4である)を表し;
・環A1は、さらなるC6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル(carbocyclyl)基または5〜10員のヘテロシクリル基に縮合していてもよい、C6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基であり;
・Wは、式:
【0011】
【化2】

【0012】
{式中、
・L2は、基-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、結合、またはC1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表し;
・Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し;
・A2は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基または5〜6員のヘテロアリール基を表し;
・Hetは、-O-、-S-または-NR’-(式中、R’は、水素もしくは非置換C1〜2アルキルを表す)を表し;
・xは、0または1であり;
・Alk1は、結合、またはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基、または基-A3-Alk4-(式中、A3は、縮合していないか、もしくはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基もしくは5〜6員のヘテロアリール基を表し、Alk4は、結合、もしくはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基を表す)を表し;
・Rは、式(X1)、(X2)、(Y1)または(Y2):
【0013】
【化3】

【0014】
[式中、
・R2は、基-COOH、または1種以上の細胞内カルボキシルエステラーゼ酵素によって-COOH基に加水分解され得るエステル基であり;
・R3は、水素原子またはC1〜4アルキル基を表し;
・R4、R7およびR8は、同一であるか、または異なっており、それぞれ天然α-アミノ酸または非天然α-アミノ酸のα-置換基を表すか、あるいはR7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和スピロシクロアルキル環またはヘテロシクリル環を形成し;
・R5は、水素原子、またはC1〜6アルキル基、C3〜7カルボシクリル基、C6〜10アリール基もしくは5〜6員のヘテロアリール基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくはC1〜6アルキル基である)を表し;
・環Dは、5〜6員のヘテロシクリル基であり、ここでR2は、示された環窒素に隣接する環炭素に結合しており;R7は、存在する場合、R2と同じ環炭素に結合しており;環Dは、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合していてもよい]
の基を表す(ただし、Rが式(Y2)の基を表し、かつ環Dがフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合している場合、波線によって横切られた示された結合は、環Dまたは前記第二の環の環原子からのものであってもよい)}
の基を表し;
式中、別段記載しない限り、
・R1、R2、R3、R4、R5、R6、R7、R8、L1、Alk1、Alk2、Alk3およびAlk4における、任意のアルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、同一であるか、または異なっており、それぞれ置換されていないか、または1個、2個もしくは3個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン原子ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、-SR’基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択され;
・A1、A2、A3、DおよびR5における、任意のアリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分は、同一であるか、または異なっており、それぞれ置換されていないか、またはハロゲン原子ならびにシアノ基、ニトロ基、C1〜4アルキル基、C1〜4アルコキシ基、C2〜4アルケニル基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、C1〜4ヒドロキシアルキル基、-SR’基および-NR’R’’基(式中、R’およびR’’は、それぞれ同一であるか、もしくは異なっており、水素もしくは非置換C1〜4アルキルを表す)から選択される1個、2個、3個もしくは4個の非置換置換基によって、もしくは式-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBもしくは-NRACONRARB(式中、RAおよびRBは、同一であるか、もしくは異なっており、非置換C1〜6アルキル、C3〜6シクロアルキル、非縮合フェニル、もしくは非縮合の5〜6員のヘテロアリールを表すか、もしくはRAおよびRBは、同一の窒素原子に結合している場合、非縮合の5員もしくは6員のヘテロシクリル基を形成する)の置換基から選択される1個、2個、3個もしくは4個の非置換置換基によって、置換されている〕
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0015】
本発明の化合物は、細胞内カルボキシルエステラーゼによって加水分解され得るアミノ酸モチーフまたはアミノ酸エステルモチーフを含む。該化合物はまた、最後がアミノ酸モチーフまたはアミノ酸エステルモチーフで終わる分子の側鎖に保持された環式基から分子のチオフェン環母核を分離するリンカー基も含む。驚くべきことに、この親油性のアミノ酸モチーフまたはアミノ酸エステルモチーフとリンカー基との組み合わせを有する本発明の化合物は、IKKアイソフォーム、特にIKK-βの強力かつ選択的な阻害剤である。
【0016】
本発明の好ましい化合物は、細胞内カルボキシルエステラーゼによって加水分解され得るアミノ酸エステルモチーフを含む化合物である。こうした化合物は、細胞膜を容易に通過することができ、その後細胞内カルボキシルエステラーゼによって、酸に加水分解され得る。極性の加水分解生成物は、細胞膜を同様に容易には通過しないため、細胞内に蓄積する。そのため、該化合物のIKK活性は、長期にわたり得、細胞内で高まり得る。したがって、この蓄積の効果は、本発明の化合物の細胞内IKK活性の、該化合物の細胞外活性に対する増大をもたらし得る。
【0017】
さらに、Rが式(X1)または(Y1)の基である本発明の化合物は、単球内に選択的に蓄積することがわかっている。したがって、こうした本発明の化合物は、全身投与が望まれる場合、有利に使用することができる。なぜならば、該化合物は、プレシステミック代謝(pre-systemic metabolism)に対してあまり感受性がなく、したがってインタクトで(in tact)標的組織に到達し得る(その後、標的細胞の内部で酸の生成物に変換される)からである。単球細胞株における優先的な蓄積は、他の隣接する細胞に優先して単球に集中した、患者に投与された1用量の化合物の、IKK阻害効果をもたらし得る。したがって、この選択性は、例えば癌および自己免疫疾患の治療において、単核球細胞を標的とするために使用された場合、本発明の化合物と関連する治療濃度域を向上させ得る。したがって、例えば、標的ではない非単核球細胞のIKK阻害と関連する副作用を減少させることができる。
【0018】
逆に、局所投与が望まれる場合、Rが式(X2)または(Y2)の基である本発明の化合物を使用することが有利であり得る。かかる本発明の化合物は、単球選択性を示さず、典型的にはエステル開裂がより急速に起こる。この急速なエステル開裂速度は、全身的な曝露、および結果としての望まれない副作用を減少させることに関して、有利であり得る。
【0019】
本発明の化合物は、式(IA)もしくは(IB)の化合物もしくはその互変異性体、またはその薬学的に許容される塩であることが好ましい。
【0020】
本発明はまた、ヒトまたは動物の身体の治療方法に使用するための、上に定義した化合物も提供する。
【0021】
本発明は、さらに、上に定義した化合物および薬学的に許容される担体または希釈剤を含む、医薬組成物を提供する。
【0022】
別の態様において、本発明は、IKK酵素によって媒介される障害の治療に使用するための、上に定義した化合物を供給する。本発明はまた、IKK酵素によって媒介される障害の治療または予防に使用するための医薬の製造における、上に定義した化合物の使用も提供する。これらの態様において、IKK酵素は、好ましくはIKK-βである。
【0023】
さらに、本発明は、患者におけるIKKによって媒介される障害の治療方法または予防方法を提供し、該方法は、有効量の上に定義した化合物を前記患者に投与することを含む。
【発明を実施するための形態】
【0024】
(発明の詳細な説明)
上記定義は分子量の高い分子を含む可能性があるが、医薬品化学のプラクティスの一般的な原則に従って、本発明が関係する化合物は、600以下の分子量を有するべきであることが好ましい。
【0025】
好ましくは、R1、R2、R3、R4、R5、R6、R7、R8、L1、L2、L3、Alk1、Alk2、Alk3およびAlk4における、アルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、置換されていないか、または1個、2個もしくは3個、好ましくは1個もしくは2個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン、C1〜4アルキル、C2〜4アルケニル、C1〜4アルコキシ、ヒドロキシル、C1〜4ハロアルキル、C2〜4ハロアルケニル、C1〜4ハロアルキルオキシおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)から選択される。より好ましい置換基は、ハロゲン、非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)である。例えば、特に好ましい置換基としては、非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)が挙げられる。
【0026】
上記のアルキル部分、アルキレン部分、アルケニレン部分およびアルキニレン部分が2個または3個の置換基によって置換されている場合、2個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることが好ましい。1個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることがより好ましい。
【0027】
本明細書中で使用される場合、C1〜6アルキル基またはC1〜6アルキル部分は、1〜6個の炭素原子を含む、直鎖状または分枝状のアルキル基またはアルキル部分、例えば1〜4個の炭素原子を含む、C1〜4アルキル基またはC1〜4アルキル部分である。C1〜4アルキル基の例としては、メチル、エチル、n-プロピル、i-プロピル、n-ブチル、i-ブチルおよびt-ブチルが挙げられる。誤解を避けるためであるが、1個の基に2個のアルキル部分が存在している場合、それらのアルキル部分は、同一であってもよく、異なっていてもよい。
【0028】
本明細書中で使用される場合、C2〜6アルケニル基またはC2〜6アルケニル部分は、適用可能である場合、EまたはZのいずれかの立体化学の少なくとも1つの二重結合を有し、2〜6個の炭素原子を含む、直鎖状または分枝状のアルケニル基またはアルケニル部分、例えば-CH=CH2または-CH2-CH=CH2、-CH2-CH2-CH=CH2、-CH2-CH=CH-CH3、-CH=C(CH3)-CH3および-CH2-C(CH3)=CH2などの2〜4個の炭素原子を含む、C2〜4アルケニル基またはC2〜4アルケニル部分である。誤解を避けるためであるが、1個の基に2個のアルケニル部分が存在している場合、それらのアルケニル部分は、同一であってもよく、異なっていてもよい。
【0029】
本明細書中で使用される場合、C2〜6アルキニル基またはC2〜6アルキニル部分は、2〜6個の炭素原子を含む、直鎖状または分枝状のアルキニル基またはアルキニル部分、例えば2〜4個の炭素原子を含む、C2〜4アルキニル基またはC2〜4アルキニル部分である。例示的なアルキニル基としては、-C≡CHまたは-CH2-C≡CH、ならびに1-ブチニルおよび2-ブチニル、2-メチル-2-プロピニル、2-ペンチニル、3-ペンチニル、4-ペンチニル、2-ヘキシニル、3-ヘキシニル、4-ヘキシニルおよび5-ヘキシニルが挙げられる。誤解を避けるためであるが、1個の基に2個のアルキニル部分が存在している場合、それらのアルキニル部分は、同一であってもよく、異なっていてもよい。
【0030】
本明細書中で使用される場合、C1〜6アルキレン基またはC1〜6アルキレン部分は、直鎖状または分枝状のアルキレン基またはアルキレン部分、例えばC1〜4アルキレン基またはC1〜4アルキレン部分である。例としては、メチレン基およびメチレン部分、n-エチレン基およびn-エチレン部分、n-プロピレン基およびn-プロピレン部分ならびに-C(CH3)2-基および-C(CH3)2-部分が挙げられる。
【0031】
本明細書中で使用される場合、C2〜6アルケニレン基またはC2〜6アルケニレン部分は、直鎖状または分枝状のアルケニレン基またはアルケニレン部分、例えばC2〜4アルケニレン基またはC2〜4アルケニレン部分である。例としては、-CH=CH-、-CH=CH-CH2-、-CH2-CH=CH-および-CH=CH-CH=CH-が挙げられる。
【0032】
本明細書中で使用される場合、C2〜6アルキニレン基またはC2〜6アルキニレン部分は、直鎖状または分枝状のアルキニレン基またはアルキニレン部分、例えばC2〜4アルキニレン基またはC2〜4アルキニレン部分である。例としては、-C≡C-、-C≡C-CH2-および-CH2-C≡C-が挙げられる。
【0033】
本明細書中で使用される場合、ハロゲン原子は、塩素、フッ素、臭素またはヨウ素である。
【0034】
本明細書中で使用される場合、C1〜6アルコキシ基またはC2〜6アルケニルオキシ基は、典型的には、それぞれ酸素原子に結合している前記C1〜6アルキル(例えばC1〜4アルキル)基または前記C2〜6アルケニル(例えばC2〜4アルケニル)基である。
【0035】
ハロアルキル基、ハロアルケニル基、ハロアルコキシ基またはハロアルケニルオキシ基は、典型的には、それぞれ、1個以上の前記ハロゲン原子によって置換されている前記アルキル基、アルケニル基、アルコキシ基またはアルケニルオキシ基である。典型的には、アルキル基、アルケニル基、アルコキシ基またはアルケニルオキシ基が、1個、2個または3個の前記ハロゲン原子によって置換されている。好ましいハロアルキル基およびハロアルコキシ基としては、-CX3および-OCX3(式中、Xは、前記ハロゲン原子、例えば塩素およびフッ素である)などのペルハロアルキル基およびペルハロアルコキシ基が挙げられる。
【0036】
本明細書中で使用される場合、C1〜4アルキルチオ基またはC2〜4アルケニルチオ基は、典型的には、それぞれ、硫黄原子に結合している前記C1〜4アルキル基またはC2〜4アルケニル基、例えば-S-CH3である。
【0037】
本明細書中で使用される場合、C1〜4ヒドロキシアルキル基は、1個以上のヒドロキシ基によって置換されたC1〜4アルキル基である。典型的には、C1〜4アルキル基が、1個、2個または3個のヒドロキシ基によって置換されている。好ましくは、C1〜4アルキル基が、単一のヒドロキシ基によって置換されている。
【0038】
本明細書中で使用される場合、C6〜10アリール基またはC6〜10アリール部分は、6〜10個の炭素原子を有する単環式6〜10員の芳香族炭化水素環である。フェニルが好ましい。
【0039】
本明細書中で使用される場合、C6〜10アリール基またはC6〜10アリール部分は、縮合していないことが好ましい。しかしながら、C6〜10アリール基またはC6〜10アリール部分がさらなるC6〜10アリール基、5〜10員のヘテロシクリル基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合している場合、該基または部分は、さらなるフェニル基、5〜6員のヘテロシクリル基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基に縮合していることが好ましく、5〜6員のヘテロアリール基または5〜6員のヘテロシクリル基に縮合していることがより好ましい。該基または部分は、5〜6員のヘテロシクリル基に縮合していることが最も好ましい。この場合、好ましい5〜6員のヘテロシクリル基としては、テトラヒドロフラニル、テトラヒドロチエニル、ピロリジニル、ジチオラニル、ジオキソラニル、オキサゾリジニル、イミダゾリル、イソオキサゾリジニル、イミダゾリジニル、ピラゾリジニル、チオキソラニル、チアゾリジニルおよびイソチアゾリジニルが挙げられ、より好ましくはオキサゾリジニル、イミダゾリジニル、チアゾリジニル、チオキソラニル、ジオキソラニルおよびジチオラニルが挙げられ、最も好ましくはジオキソラニルが挙げられる。
【0040】
本明細書中で使用される場合、5〜10員のヘテロアリール基またはヘテロアリール部分は、O、SおよびNから選択される少なくとも1個のヘテロ原子、例えば1個、2個、3個または4個のヘテロ原子を含む、5員環または6員環などの単環式5〜10員の芳香環である。環が4個のヘテロ原子を含む場合、これらのヘテロ原子はすべて窒素原子であることが好ましい。例としては、チエニル基、フリル基、ピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、チアジアゾリル基、オキサジアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基、ピラジニル基、トリアジニル基およびテトラゾリル基が挙げられる。チエニル基、ピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基およびピラジニル基、例えばピロリル基、イミダゾリル基、チアゾリル基、イソチアゾリル基、ピラゾリル基、オキサゾリル基、イソオキサゾリル基、トリアゾリル基、ピリジニル基、ピリダジニル基、ピリミジニル基およびピラジニル基が好ましい。より好ましい基は、チエニル、ピリジニル、ピリダジニル、ピリミジニル、ピラジニル、ピロリルおよびトリアジニル、例えばピリジニル、ピリダジニル、ピリミジニル、ピラジニル、ピロリルおよびトリアジニルであり、最も好ましくはピリジニルである。
【0041】
本明細書中で使用される場合、ヘテロアリール基またはヘテロアリール部分は、縮合していないことが好ましい。しかしながら、ヘテロアリール基またはヘテロアリール部分が別の基に縮合している場合、該基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合がある。好ましくは、該基または部分は、フェニル環、5〜6員のヘテロアリール環または5〜6員のヘテロシクリル環に縮合していることが好ましく、フェニル基に縮合していることがより好ましい。例としては、ベンゾチエニル基、ベンゾフリル基、ベンゾイミダゾリル基、ベンゾチアゾリル基、ベンゾイソチアゾリル基、ベンゾオキサゾリル基、ベンゾイソオキサゾリル基、ベンゾトリアゾリル基、インドリル基、イソインドリル基およびインダゾリル基が挙げられる。好ましい基としては、インドリル基、イソインドリル基、ベンゾイミダゾリル基、インダゾリル基、ベンゾフリル基、ベンゾチエニル基、ベンゾオキサゾリル基、ベンゾイソオキサゾリル基、ベンゾチアゾリル基およびベンゾイソチアゾリル基が挙げられ、より好ましくはベンゾイミダゾリル、ベンゾオキサゾリルおよびベンゾチアゾリルが挙げられ、最も好ましくはベンゾチアゾリルが挙げられる。
【0042】
本明細書中で使用される場合、5〜10員のヘテロシクリル基またはヘテロシクリル部分は、1個以上、例えば1個、2個、3個または4個の炭素原子が、N、O、S、S(O)およびS(O)2から選択される部分で置換された、非芳香族の飽和または不飽和のC5〜10炭素環であり、ここで1個以上の残りの炭素原子は、任意選択で基-C(O)-または-C(S)-によって置換されている。1個以上の残りの炭素原子が基-C(O)-または-C(S)-によって置換されている場合、好ましくは、1個だけまたは2個(より好ましくは2個)のかかる炭素原子が置換されている。典型的には、5〜10員のヘテロシクリル環は、5〜6員の環である。
【0043】
適切なヘテロシクリル基およびヘテロシクリル部分としては、アゼチジニル基およびアゼチジニル部分、オキセタニル基およびオキセタニル部分、チエタニル基およびチエタニル部分、ピロリジニル基およびピロリジニル部分、イミダゾリジニル基およびイミダゾリジニル部分、オキサゾリジニル基およびオキサゾリジニル部分、イソオキサゾリジニル基およびイソオキサゾリジニル部分、チアゾリジニル基およびチアゾリジニル部分、イソチアゾリジニル基およびイソチアゾリジニル部分、テトラヒドロフラニル基およびテトラヒドロフラニル部分、テトラヒドロチエニル基およびテトラヒドロチエニル部分、テトラヒドロピラニル基およびテトラヒドロピラニル部分、テトラヒドロチオピラニル基およびテトラヒドロチオピラニル部分、ジチオラニル基およびジチオラニル部分、ジオキソラニル基およびジオキソラニル部分、ピラゾリジニル基およびピラゾリジニル部分、ピペリジニル基およびピペリジニル部分、ピペラジニル基およびピペラジニル部分、ヘキサヒドロピリミジニル基およびヘキサヒドロピリミジニル部分、メチレンジオキシフェニル基およびメチレンジオキシフェニル部分、エチレンジオキシフェニル基およびエチレンジオキシフェニル部分、チオモルホリニル基およびチオモルホリニル部分、S-オキソ-チオモルホリニル基およびS-オキソ-チオモルホリニル部分、S,S-ジオキソ-チオモルホリニル基およびS,S-ジオキソ-チオモルホリニル部分、モルホリニル基およびモルホリニル部分、1,3-ジオキソラニル基および1,3-ジオキソラニル部分、1,4-ジオキソラニル基および1,4-ジオキソラニル部分、トリオキソラニル基およびトリオキソラニル部分、トリチアニル基およびトリチアニル部分、イミダゾリニル基およびイミダゾリニル部分、ピラニル基およびピラニル部分、ピラゾリニル基およびピラゾリニル部分、チオキソラニル基およびチオキソラニル部分、チオキソチアゾリジニル基およびチオキソチアゾリジニル部分、1H-ピラゾール-5-(4H)-オンイル(1H-pyrazol-5-(4H)-onyl)基および1H-ピラゾール-5-(4H)-オンイル部分、1,3,4-チアジアゾール-2(3H)-チオニル基および1,3,4-チアジアゾール-2(3H)-チオニル部分、オキソピロリジニル基およびオキソピロリジニル部分、オキソチアゾリジニル基およびオキソチアゾリジニル部分、オキソピラゾリジニル基およびオキソピラゾリジニル部分、スクシンイミド基およびスクシンイミド部分、ならびにマレイミド基およびマレイミド部分が挙げられる。好ましいヘテロシクリル基は、ピロリジニル基およびピロリジニル部分、イミダゾリジニル基およびイミダゾリジニル部分、オキサゾリジニル基およびオキサゾリジニル部分、イソオキサゾリジニル基およびイソオキサゾリジニル部分、チアゾリジニル基およびチアゾリジニル部分、イソチアゾリジニル基およびイソチアゾリジニル部分、テトラヒドロフラニル基およびテトラヒドロフラニル部分、テトラヒドロチエニル基およびテトラヒドロチエニル部分、テトラヒドロピラニル基およびテトラヒドロピラニル部分、テトラヒドロチオピラニル基およびテトラヒドロチオピラニル部分、ジチオラニル基およびジチオラニル部分、ジオキソラニル基およびジオキソラニル部分、ピラゾリジニル基およびピラゾリジニル部分、ピペリジニル基およびピペリジニル部分、ピペラジニル基およびピペラジニル部分、ヘキサヒドロピリミジニル基およびヘキサヒドロピリミジニル部分、チオモルホリニル基およびチオモルホリニル部分、ならびにモルホリニル基およびモルホリニル部分である。より好ましいヘテロシクリル基は、テトラヒドロピラニル基、テトラヒドロチオピラニル基、チオモルホリニル基、テトラヒドロフラニル基、テトラヒドロチエニル基、ピペリジニル基、モルホリニル基およびピロリジニル基、ならびに1個または2個の環炭素原子が-C(O)-基で置換されているバリアントである。特に好ましい基としては、テトラヒドロフラニルおよびピロリル-2,5-ジオンが挙げられる。
【0044】
ヘテロシクリル基またはヘテロシクリル部分が別の基に縮合している場合、この基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合があり、より好ましくはさらなるフェニル基、5〜6員のヘテロアリール基または5〜6員のヘテロシクリル基に縮合している場合がある。この基または部分は、単環式である(すなわちその基または部分は縮合していない)ことが好ましい。
【0045】
誤解を避けるためであるが、ヘテロアリール基およびヘテロシクリル基の上記定義は、環に存在し得る「N」部分について言及するものであるが、当業者に明らかなように、N原子は、単結合を介して隣接する環原子のそれぞれに結合している場合、プロトン化されることになる(または以下に定義する置換基を有することになる)。
【0046】
本明細書中で使用される場合、C3〜7炭素環式基またはC3〜7炭素環式部分は、3〜7個の炭素原子を有する、非芳香族の、飽和または不飽和の炭化水素環である。好ましくは、該基または部分は、3〜7個の炭素原子、より好ましくは3〜6個の炭素原子を有する、飽和炭化水素環または一不飽和炭化水素環(すなわちシクロアルキル部分またはシクロアルケニル部分)である。例としては、シクロプロピル、シクロブチル、シクロペンチルおよびシクロヘキシル、ならびにこれらの一不飽和のバリアント、より具体的にはシクロペンチルおよびシクロヘキシルが挙げられる。C3〜7カルボシクリル基またはC3〜7カルボシクリル部分にはまた、上記のC3〜7カルボシクリル基またはC3〜7カルボシクリル部分であるが、1個以上の環炭素原子が基-C(O)-によって置換されているC3〜7カルボシクリル基またはC3〜7カルボシクリル部分も含まれる。より好ましくは、0個、1個または2個の環炭素原子(最も好ましくは0個または2個)が-C(O)-によって置換されている。好ましいかかる基は、ベンゾキノンである。
【0047】
カルボシクリル基またはカルボシクリル部分が別の基に縮合している場合、この基または部分は、さらなるフェニル基、5〜10員のヘテロアリール基、5〜10員のヘテロシクリル基またはC3〜7カルボシクリル基に縮合している場合があり、より好ましくはさらなるフェニル環、5〜6員のヘテロアリール環または5〜6員のヘテロシクリル環に縮合している場合がある。例えば、この基または部分は、さらなるフェニル環に縮合している場合がある。例示的な縮合したカルボシクリル基は、インダニルである。カルボシクリル基は、単環式である(すなわち縮合していない)ことがより好ましい。
【0048】
A1、A2、A3、B、DおよびR5におけるアリール部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分が2個、3個または4個の置換基によって置換される場合、2個以下の置換基がヒドロキシル、シアノおよびニトロから選択されることが好ましい。1個以下の置換基が、ヒドロキシル、シアノおよびニトロから選択されることがより好ましい。さらに、アリール部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分が2個または3個の置換基によって置換される場合、1個以下の置換基が、-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBまたは-NRACONRARBから選択されることが好ましい。
【0049】
典型的には、A1、A2、A3、B、DおよびR5における、アリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分における、フェニル部分、ヘテロアリール部分、ヘテロシクリル部分およびカルボシクリル部分は、置換されていないか、または1個、2個、3個もしくは4個の置換基によって、例えば1個、2個もしくは3個の置換基によって、置換されている。好ましい置換基としては、ハロゲン原子、ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、メルカプト基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基、C2〜4ヒドロキシアルケニル基、C1〜4アルキルチオ基、C2〜4アルケニルチオ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)が挙げられる。置換基は、非置換の置換基であることが好ましい。より好ましい置換基としては、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)が挙げられる。より好ましい置換基としては、ハロゲン原子、ならびにC1〜2アルキル基およびC1〜2アルコキシ基が挙げられる。
【0050】
本明細書中で使用される場合、用語「塩」は、塩基付加塩、酸付加塩および第四級塩を含む。酸性である本発明の化合物は、アルカリ金属水酸化物、例えば水酸化ナトリウムおよび水酸化カリウムなどの塩基;アルカリ土類金属水酸化物、例えば水酸化カルシウム、水酸化バリウムおよび水酸化マグネシウムなどの塩基;有機塩基、例えばN-メチル-D-グルカミン、コリン、トリス(ヒドロキシメチル)アミノ-メタン、L-アルギニン、L-リジン、N-エチルピペリジン、ジベンジルアミンなどと、薬学的に許容される塩を含む塩を形成することができる。塩基性である化合物(IA)または(IB)は、無機酸、例えば塩酸もしくは臭化水素酸などのハロゲン化水素酸、硫酸、硝酸またはリン酸など、ならびに有機酸、例えば酢酸、酒石酸、コハク酸、フマル酸、マレイン酸、リンゴ酸、サリチル酸、クエン酸、メタンスルホン酸、p-トルエンスルホン酸、安息香酸、ベンゼンスルホン酸、グルタミン酸、乳酸およびマンデル酸などと、薬学的に許容される塩を含む塩を形成することができる。
【0051】
1つ以上の実際のまたは潜在的なキラル中心を含む本発明の化合物は、不斉炭素原子が存在するために、各キラル中心でRまたはSの立体化学を有するいくつかのジアステレオ異性体として存在し得る。本発明は、すべてのかかるジアステレオ異性体およびそれらの混合物を含む。
【0052】
誤解を避けるためであるが、L1が基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-または-(CH2)mNR1(CH2)n-を表す場合、記載された基の左側は、本発明の化合物のチオフェン環部分に結合しており、したがってその基の右側は、本発明の化合物の環A1に結合している。好ましくは、整数nおよびmの和は、6以下である。より好ましくは、整数nおよびmの和は、4以下である。最も好ましくは、整数nおよびmの和は、3以下である。好ましくは、mおよびnの少なくとも一方は、ゼロに等しい。より好ましくは、少なくともmは、ゼロに等しい。
【0053】
本発明の好ましい実施態様において、L1は、C2〜4アルキニレン基ではない。
【0054】
好ましくは、L1は、-O-、-S-、-NR1-またはC1〜4アルキレンを表し、該C1〜4アルキレンは、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、式中、R1は、非置換のC1〜4アルキルを表す。
【0055】
より好ましくは、L1は、-O-またはC1〜4アルキレンを表し、該C1〜4アルキレン部分は、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、L1は、C1〜4アルキレンを表し、該C1〜4アルキレンは、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択される。
【0056】
最も好ましくは、L1は、非置換のC1〜4アルキレン、例えばメチル、エチル、n-プロピルまたはi-プロピルを表す。特に好ましい実施態様において、L1は、メチルを表す。
【0057】
好ましくは、A1は、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を表し、このそれぞれの基は、縮合していないか、またはさらなるフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基もしくは5〜6員のヘテロシクリル基に縮合している。
【0058】
より好ましくは、A1は、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロシクリル基に縮合している。A1が、縮合していないかまたは5〜6員のヘテロシクリル基に縮合している、フェニル基または5〜6員のヘテロアリール基を表す場合、そのヘテロシクリル基は、好ましくはジオキソール基である。例えば、A1が、縮合していないかまたは5〜6員のヘテロシクリル基に縮合している、フェニル基または5〜6員のヘテロアリール基を表す場合、好ましいA1基は、ベンゾジオキソールである。
【0059】
より好ましくは、A1は、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、縮合していないか、またはさらなるフェニル基に縮合している。より好ましくは、A1は、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、より好ましくは1,4-フェニレン基または1,3-フェニレン基などの非縮合のフェニル基を表す。1つの好ましい実施態様において、A1は、1,3-フェニレン基を表す。
【0060】
好ましくは、A1基は、置換されていないか、または1個、2個もしくは3個の置換基を有する。1個よりも多くの置換基が存在している場合、それらの置換基は、同一であってもよく、異なっていてもよい。1個よりも多くの置換基が存在している場合、1個の置換基だけがヒドロキシル基、シアノ基またはニトロ基であることが好ましい。
【0061】
A1上の好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択される。
【0062】
A1上のより好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0063】
より好ましくは、A1上の置換基は、ハロゲン原子、ならびに非置換のC1〜2アルキル基およびC1〜2アルコキシ基から選択される。
【0064】
最も好ましくは、A1基は、置換されていない。
【0065】
好ましくは、Alk2は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表す。より好ましくは、Alk2は、C1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表す。
【0066】
好ましくは、Alk2基は、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されている。より好ましくは、Alk2基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個、より好ましくは1個もしくは2個の非置換の置換基で置換されている。最も好ましくは、Alk2基は、置換されていない。
【0067】
より好ましくは、Alk2は、非置換のメチレン基、エチレン(-CH2CH2-)基、ビニレン(-CH=CH-)基またはエチニレン(-C≡C-)基を表す。最も好ましくは、Alk2は、メチレンなどのC1〜2アルキレン基を表す。
【0068】
L2が-Alk2-A2-を表す場合、好ましくは、A2は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表す。より好ましくは、A2は、非縮合のフェニル基を表す。Alk2基およびHet基またはAlk1基は、任意の位置でフェニル基に結合していてよいが、Alk2基およびHet基またはAlk1基は、互いにメタまたはパラの関係で結合していること、より好ましくはパラの関係で結合していることが好ましい。
【0069】
好ましくは、A2基は、0個、1個、2個または3個の置換基、より好ましくは、0個、1個または2個の置換基を有する。1個よりも多くの置換基が存在している場合、それらの置換基は、同一であってもよく、異なっていてもよい。1個よりも多くの置換基が存在している場合、1個の置換基だけがヒドロキシル基、シアノ基またはニトロ基であることが好ましい。
【0070】
A2上の好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0071】
A2上のより好ましい置換基は、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0072】
より好ましくは、A2上の置換基は、ハロゲン原子、ならびに非置換のC1〜2アルキル基およびC1〜2アルコキシ基から選択される。最も好ましくは、A2基は、置換されていない。
【0073】
L2が-Alk2-Alk3を表す場合、好ましくは、Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、Alk3は、非置換のC1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表す。最も好ましくは、Alk3は、非置換のC1〜4アルキレン、例えばC3〜4アルキレン基、より好ましくは基-CH2-CH2-CH2-を表す。
【0074】
L2は、-Alk2-であることが好ましい。
【0075】
Het基は、存在する場合、好ましくは、-O-、-NR’または-S-(式中、R’は、水素または非置換のメチルを表す)を表す。より好ましくは、Het基は、-O-、-NHまたは-S-を表す。最も好ましくは、Het基は、-O-である。
【0076】
L2が-Alk2-である場合、好ましくは、xは0である。別の好ましい実施態様において、xは0である。
【0077】
好ましくは、Alk1は、結合またはC1〜6アルキレン基または基-A3-Alk4-を表す。より好ましくは、Alk1は、結合またはC1〜6アルキレン基を表す。最も好ましくは、Alk1は、結合を表す。
【0078】
Alk1がC1〜6アルキレン基を表す場合、該アルキレン基は、好ましくはC1〜4アルキレン基であり、より好ましくはC1〜3アルキレン基であり、好ましくはメチレン基またはプロピレン基である。
【0079】
Alk1がC1〜6アルキレン基を表す場合、好ましくはAlk1基は、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されている。より好ましくは、Alk1基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個、より好ましくは1個の非置換の置換基で置換されている。最も好ましくは、Alk1は、置換されていない。
【0080】
Alk1が基-A3-Alk4-を表す場合、A3は、好ましくは、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該非置換の置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。
【0081】
Alk1が基-A3-Alk4-を表す場合、好ましくは、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、またはハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の置換基で置換されている。より好ましくは、A3は、非縮合のフェニルを表し、該フェニルは、置換されていないか、またはハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の置換基で置換されている。最も好ましくは、A3は、非置換の、非縮合のフェニル基を表す。
【0082】
Alk1が基-A3-Alk4-を表す場合、Alk4は、好ましくは非置換のC1〜6アルキレン基を表し、より好ましくは非置換のC1〜3アルキレン基を表し、より好ましくは非置換のC1〜2アルキレン基を表し、具体的にはメチレン基-CH2-またはエチレン基-CH2-CH2-を表す。
【0083】
A2およびA3の一方のみが存在していることが好ましい。すなわち、Alk1が-A3-Alk4-である場合、L2は-Alk2-A2-ではないことが好ましく、逆もまた同様である。
【0084】
xが1である場合、好ましくは、Alk1は、C3アルキレン基である。L2が-Alk2-である場合、好ましくは、xは0であり、Alk1は、結合またはC3アルキレン基、例えばC3アルキレン基である。L2が-Alk2-A2-である場合、好ましくは、xは1であり、Alk1はC1アルキレン基である。
【0085】
好ましい基(Y1)および(Y2)としては、環Dが非縮合の5〜6員のヘテロアリール基またはヘテロシクリル基であり、R2が環D中に示された窒素原子に隣接する炭素原子に結合している、基が挙げられる。より好ましくは、環Dは、非縮合の5〜6員のヘテロシクリル基、例えば、ピロリジニル基、オキサゾリジニル基、イソオキサゾリジニル基、イミダゾリジニル基、ピラゾリジニル基、チアゾリジニル基、イソチアゾリジニル基、ピペリジニル基、ヘキサヒドロピリミジニル基、ピペラジニル基、モルホリニル基またはチオモルホリニル基である。環Dは、より好ましくは、ピロリジニル基、ピペラジニル基またはピペリジニル基であり、より好ましくは、ピペリジル基またはピペラジニル基である。
【0086】
基Rが式(Y1)のものである場合、好ましくは、環Dは、有している基R2およびR7に加えて、置換されていないか、またはハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルコキシ基およびヒドロキシル基から選択される1個もしくは2個の基によって置換されている。より好ましくは、環Dは、基R2およびR7を有していることは別として、置換されていない。
【0087】
基Rが式(Y2)のものである場合、好ましくは、環Dは、基R2を有していることに加えて、置換されていないか、またはハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルコキシ基およびヒドロキシル基から選択される1個もしくは2個の基によって、置換されている。より好ましくは、環Dは、基R2を有していることは別として、置換されていない。
【0088】
Rが式(Y2)の基である場合、特に好ましい環D基は、
【0089】
【化4】

【0090】
である。
【0091】
Rが式(X1)の基を表す場合、R3は、好ましくは、水素原子または非置換のC1〜2アルキルを表す。より好ましくは、R3は、水素原子または非置換のメチルを表す。最も好ましくは、R3は、水素原子を表す。
【0092】
Rが式(X2)の基を表す場合、好ましくは、R5は、水素原子、または非置換のC1〜4アルキル基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR12の基(式中、R6は、水素原子もしくは非置換のC1〜4アルキル基である)を表す。より好ましくは、R5は、水素原子または非置換のC1〜2アルキル基を表す。最も好ましくは、R5は、水素原子を表す。
【0093】
誤解を避けるためであるが、Rが式(X1)の基を表す場合、基R7およびR8は、同一であってもよく、異なっていてもよい。
【0094】
置換基R7およびR8が、これらが結合する炭素と一緒になって、3〜6員の飽和のスピロシクロアルキル環またはスピロヘテロシクリル環を形成する場合、適切なスピロシクロアルキル環としては、シクロプロピル環、シクロペンチル環およびシクロヘキシル環が挙げられ、一方、適切なスピロヘテロシクリル環としては、ピペリジン-4-イル環が挙げられる。
【0095】
誤解を避けるためであるが、「天然α-アミノ酸または非天然α-アミノ酸のα-置換基」としての基R4、R7およびR8の定義において、「α-アミノ酸」は、式H2NCHRαCOOHの化合物を意味し、「α-置換基」は、前記α-アミノ酸の基Rαを意味する。
【0096】
天然α-アミノ酸または非天然α-アミノ酸のα-置換基上の(すなわち、基R4、R7およびR8上の)どの官能基も、保護されていてよい。用語「保護された(protected)」は、α-アミノ酸の側鎖における官能性置換基との関連で使用される場合、実質的に非官能性である、かかる置換基の誘導体を意味することが、当業者にはわかる。例えば、カルボキシ基は、エステル化されていてもよく(例えばC1〜C6アルキルエステルとして)、アミノ基は、アミド(例えばNHCOC1〜C6アルキルアミドとして)またはカルバミン酸エステル(例えばNHC(=O)OC1〜C6アルキルカルバミン酸エステルもしくはNHC(=O)OCH2Phカルバミン酸エステルとして)に転換されていてもよく、ヒドロキシル基は、エーテル(例えばOC1〜C6アルキルエーテルもしくはO(C1〜C6アルキル)フェニルエーテル)またはエステル(例えばOC(=O)C1〜C6アルキルエステル)に転換されていてもよく、チオール基は、チオエーテル(例えばtert-ブチルチオエーテルもしくはベンジルチオエーテル)またはチオエステル(例えばSC(=O)C1〜C6アルキルチオエステル)に転換されていてもよい。
【0097】
好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合またはC1〜6アルキレン基を表し、Bは、C6〜10アリール基または5〜10員のヘテロアリール基を表す);
(iv)式-CRpRqRrの基{式中、
(a)Rp、RqおよびRrが、同一であるか、もしくは異なっており、
・水素原子、
・-OH基、-SH基、ハロゲン基、-CN基、-CO2H基、CONH2基もしくは(C1〜4)ペルフルオロアルキル基、もしくは
・C1〜6アルキル基、C2〜6アルケニル基、C2〜6アルキニル基、フェニル基、5〜6員のヘテロアリール基、フェニル(C1〜6)アルキル基、C3〜8シクロアルキル基、-O(C1〜6)アルキル基、-O(C2〜6)アルケニル基、-S(C1〜6)アルキル基、-SO(C1〜6)アルキル基、-SO2(C1〜6)アルキル基、-S(C2〜6)アルケニル基、-SO(C2〜6)アルケニル基もしくは-SO2(C2〜6)アルケニル基[このそれぞれの基は、ヒドロキシル、-O(C1〜6)アルキル、フェニルオキシ、ベンジルオキシ、-SH、-S(C1〜6)アルキル、フェニルチオ、ベンジルチオ、-COOH、-CONH2、-NHC(NH)NH2もしくは
【0098】
【化5】

【0099】
によって、置換されていてもよい]を表すか;
(b)Rp、RqおよびRrのうちの2つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他のものが、基-Q-W[式中、Qは、結合、もしくは-O-、-S-、-SO-もしくは-SO2-を表し、Wは、すべてさらなるフェニル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環に縮合していてもよい、フェニル基、フェニル(C1〜6)アルキル基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基、C4〜8シクロアルケニル基、C4〜8シクロアルケニル(C1〜6)アルキル基、5員もしくは6員のヘテロアリール基もしくは5員もしくは6員のヘテロアリール(C1〜6)アルキル基を表し、該基Wは、置換されていないか、もしくは1個以上の置換基によって置換されており、該置換基は、同一であるか、もしくは異なっており、ヒドロキシル、ハロゲン、-CN、-CONH2、-CONH(C1〜6)アルキル、-CONH(C1〜6アルキル)2、-CHO、-CH2OH、(C1〜4)ペルフルオロアルキル、-O(C1〜6)アルキル、-S(C1〜6)アルキル、-SO(C1〜6)アルキル、-SO2(C1〜6)アルキル、-NO2、-NH2、-NH(C1〜6)アルキル、-N((C1〜6)アルキル)2、-NHCO(C1〜6)アルキル、(C1〜6)アルキル、(C2〜6)アルケニル、(C2〜6)アルキニル、(C3〜8)シクロアルキル、(C4〜8)シクロアルケニル、フェニルもしくはベンジルを表す]を表すか;または
(c)Rp、RqおよびRrのうちの1つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他の2つが、これらが結合する炭素原子と一緒になって、3〜8員のカルボシクリル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環を形成するか、もしくはRp、RqおよびRrが、これらが結合する炭素原子と一緒になって、三環系を形成する(ただし、式-CRpRqRrの基は、(i)、(ii)および(iii)で定義された基とは異なっている)};
を表すか;
あるいは、R7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和のスピロシクロアルキル環またはスピロヘテロシクリル環を形成する。
【0100】
この好ましい実施態様において、式-CRpRqRrの基は、より好ましくは、式-CRpRqRrの基{式中、
(a)Rp、RqおよびRrが、同一であるか、もしくは異なっており、
・水素原子、
・-OH基、-SH基、-CO2H基もしくはCONH2基、もしくは
・C1〜6アルキル基、フェニル基、5〜6員のヘテロアリール基、フェニル(C1〜6)アルキル基、C3〜8シクロアルキル基、-O(C1〜6)アルキル基もしくは-S(C1〜6)アルキル基[このそれぞれの基は、ヒドロキシル、-O(C1〜6)アルキル、フェニルオキシ、ベンジルオキシ、-SH、-S(C1〜6)アルキル、フェニルチオ、ベンジルチオ、-COOH、-CONH2もしくは-NHC(NH)NH2によって、置換されていてもよい]を表すか;または
(b)Rp、RqおよびRrのうちの2つが、上記の(a)で述べた基を表し、Rp、RqおよびRrのうちの他のものが、基-W[式中、Wは、すべてさらなるフェニル環、5〜6員のヘテロアリール環もしくは5〜6員のヘテロシクリル環に縮合していてもよい、フェニル基、フェニル(C1〜6)アルキル基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基、5員もしくは6員のヘテロアリール基もしくは5員もしくは6員のヘテロアリール(C1〜6)アルキル基を表し、該基Wは、置換されていないか、もしくはヒドロキシル、ハロゲン、-O(C1〜6)アルキル、-NH2、-NH(C1〜6)アルキル、-N((C1〜6)アルキル)2もしくは(C1〜6)アルキルによって、置換されている]を表す}
である。
【0101】
本発明のより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合もしくはC1〜6アルキレン基を表し、Bは、C6〜10アリール基もしくは5〜10員のヘテロアリール基を表す);または
(iv)インドール-3-イルメチル、-CH2COOH、-CH2CH2COOH、-CH2CONH2、-CH2CH2CONH2、-CH2CH2CH2NHC(NH)NH2、シクロヘキシル、シクロヘキシルメチルおよび1-ベンジルチオ-1-メチルエチルから選択される基
を表す。
【0102】
このより好ましい実施態様の1つの例示的な実施態様において、R4、R7およびR8は、同一であるか、または異なっており、天然のタンパク新生α-アミノ酸、またはシクロヘキシルグリシン、t-ブチルセリン、t-ブチルシステイン、tert-ブチルグリシンおよびフェニルグリシンから選択されるα-アミノ酸のα-置換基から選択される。誤解を避けるためであるが、前記天然のタンパク新生α-アミノ酸は、アラニン、アルギニン、アスパラギン、アスパラギン酸、システイン、グルタミン酸、グルタミン、グリシン、ヒスチジン、イソロイシン、ロイシン、リジン、メチオニン、フェニルアラニン、セリン、トレオニン、トリプトファン、チロシンおよびバリンから選択される。したがって、この例示的な実施態様において、R4、R7およびR8は、同一であるか、または異なっており、メチル、-CH2CH2CH2NHC(NH)NH2、-CH2CONH2、-CH2COOH、-CH2SH、-CH2CH2COOH、-CH2CH2CONH2、水素、イミダゾール-5-イルメチル、sec-ブチル、イソブチル、-CH2CH2CH2CH2NH3、-CH2CH2SCH3、ベンジル、ヒドロキシメチル、-CHOHCH3、インドール-3-イルメチル、4-ヒドロキシフェニルメチル、プロパ-2-イル、シクロヘキシル、t-ブトキシメチル、-CH2SC(CH3)3、t-ブチルおよびフェニルから選択される。これらの基のうち、この場合好ましい基としては、水素、フェニル、ベンジル、イソブチル、シクロヘキシルおよびt-ブトキシメチルが挙げられる。
【0103】
本発明のさらにより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;または
(iii)基-L3-B(式中、L3は、結合もしくはC1〜4アルキレン基を表し、Bは、フェニル基もしくは5〜10員のヘテロアリール基を表す)
を表す。
【0104】
基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、該アルキル基は、好ましくはC1〜4アルキル基であり、より好ましくはC1〜2アルキル基であり、最も好ましくはメチル基である。
【0105】
基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、L3は、好ましくは結合またはC1〜4アルキレン基であり、より好ましくはC1〜2アルキレン基であり、最も好ましくはメチレン基である。基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、Bは、好ましくは、フェニル基または5〜10員のヘテロアリール基を表す。Bが、5〜10員のヘテロアリール基を表す場合、好ましいヘテロアリール基としては、イミダゾリルおよびインドリルが挙げられる。基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、好ましくは、Bは、フェニル基を表す。
【0106】
基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、該アルキル基は、好ましくは、置換されていないか、またはハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくはC1〜2アルキルを表す)から選択される1個もしくは2個、好ましくは1個の非置換の置換基で置換されている。基R中に存在する任意の基R4、R7またはR8がC1〜6アルキル基である場合、最も好ましくは、該アルキル基は、置換されていない。
【0107】
基R中に存在する任意の基R4、R7またはR8が、L3がC1〜6アルキレン基を表す式-L3-Bの基を表す場合、前記C1〜6アルキレン基は、好ましくは、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、前記C1〜6アルキレン基は、置換されていない。
【0108】
基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、好ましくは、Bは、置換されていないか、または1個、2個もしくは3個、より好ましくは1個もしくは2個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、基R中に存在する任意の基R4、R7またはR8が式-L3-Bの基を表す場合、Bは、置換されていないか、またはハロゲン原子、もしくはC1〜4アルキル基、C1〜2アルコキシ基、C1〜2アルキルチオ基もしくはヒドロキシ基から選択される1個の置換基で置換されている。最も好ましくは、Bは、置換されていない。
【0109】
さらにより好ましい実施態様において、R4、R7およびR8は、同一であるか、または異なっており、それぞれ、水素原子、非置換のC1〜6アルキル基、または基-L3-B(式中、L3は、結合または非置換のC1〜2アルキレン基を表し、Bは、非置換のフェニル基、またはハロゲン原子、もしくはC1〜2アルキル基、C1〜2アルコキシ基、C1〜2アルキルチオ基もしくはヒドロキシ基から選択される1個の置換基で置換されたフェニル基を表す)を表す。
【0110】
特に好ましいR4基、R7基およびR8基は、水素原子および非置換のC1〜6アルキル基である。最も好ましいR4基、R7基およびR8基としては、水素原子、ならびに非置換のメチル基、エチル基、n-プロピル基、i-プロピル基、n-ブチル基、i-ブチル基、sec-ブチル基およびt-ブチル基が挙げられる。
【0111】
好ましくは、Rが式(X1)の基である場合、置換基R7およびR8の少なくとも1つは、C1〜6アルキル基、例えばメチル、エチル、n-プロピルもしくはイソプロピル、またはn-ブチル、イソブチル、sec-ブチルもしくはt-ブチルである。
【0112】
好ましくは、(X1)において、R7およびR8の少なくとも1つは、水素原子である。
【0113】
最も好ましくは、Rが式(X1)の基である場合、R7およびR8は、同一であるか、または異なっており、水素原子、または非置換のC1〜6アルキル基、フェニル基、5〜6員のヘテロアリール基、C3〜8カルボシクリル基、C3〜8シクロアルキル(C1〜6)アルキル基もしくはフェニル(C1〜6)アルキル基を表す。R7またはR8の1つが水素である場合、好ましくは、R7およびR8の他のものは、水素以外のものである。より好ましくは、R7およびR8は、同一であるか、または異なっており、水素または非置換のC1〜6アルキルを表す。R7およびR8がいずれも水素ではない場合、好ましくは、R7およびR8は、同一であるか、または異なっており、非置換のC1〜2アルキル基を表す。より好ましくは、R7およびR8がいずれも水素ではない場合、R7およびR8は、どちらも非置換のメチル基である。
【0114】
Rが、(i)R7およびR8の1つが水素であり、R7およびR8の他のものが水素以外の基である式(X1)の基、または(ii)R7が水素である式(Y1)の基、のいずれかを表す場合、好ましくは、基Rは、L-異性を有する。誤解を避けるためであるが、基R2に直接結合している炭素原子が、天然のタンパク新生アミノ酸がそのα-炭素原子について有するL-異性と一致するL-異性を有するキラル中心を表す場合、基Rは、L-異性を有する。したがって、この実施態様においては、立体化学は、以下に図示した通りである。
【0115】
【化6】

【0116】
好ましくは、Rは、式(X1)または(Y1)の基である。最も好ましくは、Rは、式(X1)の基である。Rが式(X1)または(Y1)の基である化合物は、全身投与レジメンに特によく適している。
【0117】
好ましい実施態様において、基Rは、その基の中の明示的に書き表された窒素部分が直接カルボニル(-C(=O)-)に結合していない、式(X1)または(Y1)の基である。より好ましくは、基Rは、その基の中の明示的に書き表された窒素部分が直接カルボニル(-C(=O)-)に結合していない、式(X1)の基である。
【0118】
別の実施態様において、基Rは、式(X2)または(Y2)の基である。かかる化合物は、局所(local)投与療法または局所(topical)投与療法に特によく適している。
【0119】
A1が非縮合の1,3-フェニレン基を表す、好ましい実施態様において、基R中に存在する任意の基R4、R7またはR8は、水素以外の基である。A1が非縮合の1,3-フェニレン基を表す、特に好ましい実施態様において、基R中に存在する任意の基R4、R7またはR8は、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す。A1が非縮合の1,3-フェニレン基を表す、最も好ましい実施態様において、Rは、式(X1)の基であり、R7およびR8は、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す。
【0120】
R2は、カルボン酸基-COOHまたはエステル基-COOR9のいずれかである。上記の置換基R2との関連における用語「エステル」または「エステル化カルボキシル基」は、基-(C=O)OR9(式中、R9は、理論上アルコールR9-OHに由来する、エステルを特徴付ける基である)を意味する。1つの実施態様において、好ましくは、R2は、エステル基-COOR9である。すなわち、好ましくは、R2は、1種以上の細胞のカルボキシルエステラーゼ(caboxylesterase)酵素によって-COOH基に加水分解され得るエステル基である。
【0121】
R2がエステル基である場合、該エステル基は、本発明の化合物において、1種以上の細胞内カルボキシルエステラーゼ酵素によって、カルボン酸基に加水分解され得るエステル基でなければならない。本発明の化合物のエステル基を対応する酸に加水分解することができる細胞内カルボキシルエステラーゼ酵素としては、3種の公知のヒト酵素アイソタイプhCE-1、hCE-2およびhCE-3が挙げられる。これらのアイソタイプが主要な酵素であると考えられているが、ビフェニルヒドロラーゼ(biphenylhydrolase)(BPH)などの他の酵素もまた、結合体の加水分解において役割を有し得る。一般に、カルボキシルエステラーゼが、遊離したアミノ酸エステルを親の酸に加水分解するのであれば、カルボキシルエステラーゼは、エステルモチーフを、IKK阻害剤に共有結合しているときにも加水分解することになる。そのため、後述の破壊細胞アッセイにより、所要の加水分解プロフィールを有するエステルの直接的、迅速かつ簡便な最初のスクリーニングが提供される。この方法で選定したエステルモチーフは、その後、選択した結合化学によってIKK阻害剤に結合させて同じカルボキシルエステラーゼアッセイで再度アッセイして、その基礎環境において依然としてカルボキシルエステラーゼの基質であることを確認することができる。
【0122】
エステルモチーフが、細胞内カルボキシルエステラーゼ酵素によって加水分解され得るという必要条件に従えば、特定のエステル基R2の例としては、式-(C=O)OR9〔式中、R9は、-CR14R15R16{式中、
(i)R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基[式中、aおよびbは、同一であるか、または異なっており、0または1を表し、Z1は、-O-、-S-または-NR17-(式中、R17は、水素またはC1〜4アルキルである)を表す]を表し、R16が、水素またはC1〜4アルキルを表し、R14が、水素またはC1〜4アルキルを表すか;
(ii)R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表し、R16が、水素またはC1〜4アルキルを表し、R14が、水素を表すか;
(iii)R15が、式-(Alk5)-NR18R19の基(式中、Alk5は、C1〜4アルキレン基を表し、(a)R18およびR19は、同一であるか、もしくは異なっており、水素もしくはC1〜4アルキルを表すか、または(b)R18およびR19は、これらが結合している窒素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基もしくは5〜10員のヘテロシクリル基に縮合していてもよい、5〜10員のヘテロアリール基もしくは5〜10員のヘテロシクリル基を形成するか、のいずれかである)を表し;R16が、水素またはC1〜4アルキルを表し、R14が、水素を表すか;または
(iv)R15およびR16が、これらが結合している炭素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基を形成し、R14が、水素を表す}
である〕のエステル基が挙げられる。
【0123】
R14基、R15基、R16基、R17基、R18基、R19基およびAlk5基における、アルキル基、アルキレン基およびアルケニル基上の好ましい置換基としては、同一であるか、または異なっており、ハロゲン、C1〜4アルキル、C2〜4アルケニル、C1〜4アルコキシ、ヒドロキシルおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)から選択される、1個または2個の置換基が挙げられる。より好ましい置換基は、ハロゲン、C1〜2アルコキシ、ヒドロキシルおよび-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)である。最も好ましくは、R15、R16およびAlk5における、アルキル基、アルキレン基およびアルケニル基は、置換されていない。
【0124】
R15基、R16基、R18基およびR19基における、またはこれらの基によって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基上の好ましい置換基としては、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルキレン基、C1〜4アルコキシ基、C1〜4ハロアルキル基、ヒドロキシル基、シアノ基、ニトロ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)から、より好ましくは、ハロゲン原子、ならびにC1〜2アルキル基、C1〜2アルキレン基、C1〜2アルコキシ基およびヒドロキシル基から選択される、1個または2個の置換基が挙げられる。より好ましくは、R15、R16、R18およびR19における、またはこれらによって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、またはC1〜2アルキレン基、特にメチレン基によって置換されている。最も好ましくは、R15、R16、R18およびR19における、またはこれらによって形成された、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていない。
【0125】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表す場合、好ましくは、aまたはbのいずれかは、ゼロであり、例えば、aおよびbは、いずれもゼロである。[C1〜4アルキレン]が存在している場合、それは、好ましくは、C1〜3アルキレンであり、より好ましくは、基-CH2-CH2-などのC1〜2アルキレンである。
【0126】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表す場合、好ましくは、C1〜4アルキルは、メチル、エチルまたはn-プロピルなどのC1〜3アルキル基であり、最も好ましくはメチルである。
【0127】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]の基を表し、aが1である場合、Z1は、好ましくは、-O-または-NR17-(式中、R17は、水素またはC1〜2アルキルである)であり、より好ましくは、Z1は、-O-である。
【0128】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、aまたはbのいずれかは、ゼロであり、より好ましくは、aおよびbは、いずれもゼロである。[C1〜4アルキレン]が存在している場合、それは、好ましくは、C1〜3アルキレンであり、より好ましくは、C1〜2アルキレンである。
【0129】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、C2〜4アルケニルは、C2〜3アルケニル基、特に-CH=CH2である。
【0130】
R15が、式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルケニル]の基を表し、aが1である場合、Z1は、好ましくは、-O-または-NR17-(式中、R17は、水素またはC1〜2アルキルである)であり、より好ましくは、Z1は、-O-である。最も好ましくは、Z1は存在しない(すなわちaはゼロである)。
【0131】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、R15は、水素、またはC1〜4アルキル基もしくはC2〜4アルケニル基、または基-(C1〜4アルキル)-O-(C1〜4アルキル)を表す。R15は、より好ましくは、水素、メチル、エチル、n-プロピル、-CH=CH2または-CH2-CH2-O-CH3を表し、最も好ましくは、メチルを表す。
【0132】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、R16は、好ましくは、水素またはC1〜2アルキルを表し、より好ましくは、水素またはメチルを表す。
【0133】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、好ましくは、R14は、水素またはC1〜2アルキルを表し、より好ましくは、R14は、水素またはメチルを表す。
【0134】
R15が、水素または式-[C1〜4アルキレン]b-(Z1)a-[C1〜4アルキル]もしくは-[C1〜4アルキレン]b-(Z1)a-[C2〜4アルケニル]の基を表す場合、R15およびR16の双方における、アルキル基、アルキレン基およびアルケニル基は、置換されていないことが好ましい。
【0135】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、好ましくは、該フェニル基またはヘテロアリール基は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表す。好ましいヘテロアリール基としては、ピリジル、ピロリル、イソチアゾリル、ピラゾリルおよびイソオキサゾリルが挙げられ、最も好ましくは、ピリジルが挙げられる。
【0136】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、R9における、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないことが好ましい。
【0137】
R15が、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基または5〜10員のヘテロアリール基を表す場合、R16は、好ましくは、水素またはC1〜4アルキルを表し、より好ましくは、水素またはC1〜2アルキルを表し、最も好ましくは、水素を表す。R16のC1〜4アルキル基は、置換されていないことが好ましい。
【0138】
R15が、式-(Alk5)-NR18R19の基を表す場合、Alk5は、好ましくは、C1〜2アルキレン基を表し、好ましくは、-CH2-または-CH2CH2-のいずれかを表す。
【0139】
R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、同一であるか、または異なっており、水素またはC1〜4アルキルを表す場合、好ましくは、R18は、水素またはC1〜2アルキルを表し、より好ましくは、R18は、メチル基を表す。R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、同一であるか、または異なっており、水素またはC1〜4アルキルを表す場合、好ましくは、R19は、水素またはC1〜2アルキルを表し、より好ましくは、R19は、メチル基を表す。
【0140】
R15が、式-(Alk5)-NR18R19の基を表し、R18およびR19が、これらが結合している窒素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、5〜10員のヘテロアリール基または5〜10員のヘテロシクリル基を形成する場合、R18およびR19は、非縮合の5〜6員のヘテロアリール基または非縮合の5〜6員のヘテロシクリル基を形成することが好ましい。R18およびR19が、5〜6員のヘテロシクリル基を形成することがより好ましい。好ましいヘテロシクリル基としては、ピペリジニル、ピペラジニル、モルホリニルおよびピロリジニルが挙げられ、最も好ましくはモルホリニルが挙げられる。
【0141】
R15が式-(Alk5)-NR18R19の基を表す場合、Alk5は、好ましくは、C1〜2アルキレン基を表し、より好ましくは、基-CH2CH2-を表す。
【0142】
R15が式-(Alk5)-NR18R19の基を表す場合、R16は、好ましくは、水素またはC1〜2アルキルを表し、最も好ましくは、水素を表す。
【0143】
R15が式-(Alk5)-NR18R19の基を表す場合、Alk5、R18およびR19における、アルキル基およびアルキレン基は、置換されていないことが好ましい。R15が、式-(Alk5)-NR18R19の基を表す場合、R18およびR19における、フェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないことが好ましい。
【0144】
R15が式-(Alk5)-NR18R19の基を表す場合、好ましい基としては、-CH2-CH2-NMe2および-CH2-CH2-モルホリニルが挙げられる。
【0145】
R15およびR16が、これらが結合している炭素原子と一緒になって、さらなるフェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、フェニル基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基を形成する場合、好ましい基としては、非縮合のフェニル、非縮合の5〜6員のヘテロアリール、非縮合の5〜6員のヘテロシクリル、非縮合のC3〜7カルボシクリル、およびフェニル環に縮合したC3〜7カルボシクリルが挙げられ、より好ましくは、非縮合のフェニル、非縮合の5〜6員のヘテロシクリル、非縮合のC3〜7カルボシクリル、およびフェニル環に縮合したC3〜7カルボシクリルが挙げられる。
【0146】
R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましい非縮合の5〜6員のヘテロシクリル基としては、ピペリジニル基、テトラヒドロフラニル基、ピペラジニル基、モルホリニル基およびピロリジニル基が挙げられ、より好ましくは、ピペリジニル基およびテトラヒドロフラニル基が挙げられる。R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましい非縮合のC3〜7カルボシクリル基としては、シクロペンチルおよびシクロヘキシルが挙げられ、より好ましくは、シクロペンチルが挙げられる。R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましいフェニル環に縮合したC3〜7カルボシクリル基としては、インダニルが挙げられる。
【0147】
R15およびR16が、これらが結合している炭素原子と一緒になって環式基を形成する場合、好ましくは、形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、または1個もしくは2個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜4アルキル基、C1〜4アルキレン基、C1〜4アルコキシ基、C1〜4ハロアルキル基、ヒドロキシル基、シアノ基、ニトロ基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、または異なっており、水素またはC1〜4アルキルを表す)から選択され、より好ましくは、ハロゲン原子、またはC1〜2アルキル基、C1〜2アルキレン基、C1〜2アルコキシ基およびヒドロキシル基から選択される。最も好ましくは、形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていないか、またはC1〜2アルキル基(例えばメチル基など)によって、もしくはC1〜2アルキレン基によって(例えばメチレン基などによって)、置換されている。さらにより好ましくは、そのようにして形成されたフェニル基、ヘテロアリール基、カルボシクリル基およびヘテロシクリル基は、置換されていない。
【0148】
好ましいR2基は、-COOHおよび-COOR9[式中、R9は、C1〜4アルキル基(例えばメチル、エチル、n-プロピルまたはイソプロピル、ならびにn-ブチル、sec-ブチルおよびtert-ブチルなど)、C3〜7カルボシクリル基(例えばシクロペンチルおよびシクロヘキシルなど)、C2〜4アルケニル基(例えばアリルなど)、さらにフェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基およびモルホリノエチル基を表す]である。より好ましくは、R9は、C1〜4アルキルまたはC3〜7カルボシクリルを表す。
【0149】
好ましくは、前記好ましいR9基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される。より好ましくは、前記好ましいR9基は、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択される。最も好ましくは、前記好ましいR9基は、置換されていない。前記好ましいR9基が置換されている場合、好ましくは、最大で1個の置換基がヒドロキシル基である。
【0150】
R2が-COOR9である場合、より好ましくは、R9は、非置換のC1〜4アルキル、非置換のC3〜7カルボシクリルまたは非置換のC2〜4アルケニルを表す。より好ましくは、R9は、シクロペンチルまたはt-ブチルであり;最も好ましくは、R9は、シクロペンチルである。
【0151】
R2が、-COOHまたは-COOR9(式中、R9は、C1〜4アルキルまたはC3〜7カルボシクリルである)を表す化合物は、R2が-COOR10であり、R10が水素、C1〜4アルキルまたはC3〜7カルボシクリルである基によって、記述することができる。好ましくは、R2は、-COOR10(式中、R10は、水素またはC3〜7カルボシクリルであり、より好ましくは、式中、R10は、水素またはシクロペンチルである)である。1つの実施態様において、R10は、水素以外のものである。すなわち、R10は、上記のC1〜4アルキルまたはC3〜7カルボシクリルから選択される。
【0152】
マクロファージは、サイトカイン、特にTNF-αおよびIL-1の放出を通じて、炎症性疾患において、重要な役割を果たしていることが知られている。関節リウマチにおいて、マクロファージは、関節炎症および関節破壊の維持に対する主要な寄与体である。マクロファージはまた、腫瘍増殖および腫瘍発達にもかかわっている。したがって、マクロファージ細胞の増殖を選択的に標的とする薬剤は、癌および自己免疫疾患の治療において、価値のあるものであり得る。特定の細胞型を標的とすることで、副作用の減少がもたらされると期待される。本発明者らは、マクロファージならびに単球、破骨細胞および樹状細胞などの骨髄単球性系列に由来する他の細胞に対して阻害剤を標的化する方法を発見した。これは、エステラーゼモチーフが阻害剤に結合する方法により、阻害剤が加水分解されるかどうか、したがって異なる細胞型に蓄積されるか否かが決まるという知見に基づく。具体的に言えば、マクロファージおよび骨髄単球性系列に由来する他の細胞がヒトカルボキシルエステラーゼhCE-1を含むのに対して、他の細胞型は含まないことが見出されている。基Rが、窒素部分が直接カルボニル(-C(=O)-)に結合していない式(X1)または(Y1)の基である場合の一般式(IA)および(IB)では、エステルは、hCE-1によって加水分解されるだけであり、したがって阻害剤は、マクロファージ類縁細胞中に選択的に蓄積することになる。誤解を避けるためであるが、ここで言及した窒素部分は、基(X1)および(Y1)において、明示的に記載されたN原子である。本明細書においては、「単球(monocyte)」または「単球(monocytes)」と明示しない限り、用語「マクロファージ(macrophage)」または「マクロファージ(macrophages)」は、マクロファージ(macrophages)(腫瘍関連マクロファージを含む)および/または単球(monocytes)を示すために使用する。
【0153】
本発明の好ましい実施態様(1)において、
・L1が、C1〜4アルキレンを表し、該アルキレンが、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択され;
・A1が、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2が、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3が、非置換のC1〜4アルキレン基を表し;
・A2が、非縮合のフェニルを表し、該フェニルが、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Hetが、-O-、-NH-または-S-を表し;
・Alk1が、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、非置換のC1〜3アルキレン基を表す]を表し;
・Rが、式(X1)または(Y1)の基:
【0154】
【化7】

【0155】
{式中、
・R2は、-COOHまたは-COOR9[式中、R9は、C1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表すか、またはR9は、フェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基またはモルホリノエチル基を表し、前記R9は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表し;
・環Dは、非縮合の非置換の5〜6員のヘテロシクリル基を表す}
を表す、
本発明の化合物が提供される。
【0156】
より好ましい実施態様(2)において、本発明は、(a)式(IA’)もしくは(IB’):
【0157】
【化8】

【0158】
[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・L2は、-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3は、非置換のC1〜4アルキレン基を表し;
・A2は、非縮合のフェニルを表し、該フェニルは、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・xは、0または1であり;
・Alk1は、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基は、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されており;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0159】
特に好ましい実施態様(3)において、本発明は、(a)式(IC)もしくは(ID):
【0160】
【化9】

【0161】
[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物を提供する。
【0162】
本発明の好ましい化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸である。
【0163】
特に好ましい本発明の化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチニル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
である。
【0164】
本発明で最も好ましい本発明の化合物は、
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
である。
【0165】
本発明が関係する化合物は、IKK、特にIKKβのキナーゼ活性の阻害剤であり、したがって、IKK活性およびNF-κBカスケードによって調節される疾患の治療に有用である。かかる疾患としては、腫瘍性/増殖性疾患、免疫疾患および炎症性疾患が挙げられる。具体的には、該化合物の用途としては、肝細胞癌または黒色腫などであるが、さらに腸癌、卵巣癌、頭頸部扁平上皮癌および子宮頸部扁平上皮癌、胃癌もしくは肺癌、退形成乏突起膠腫、多形神経膠芽腫または髄芽細胞腫も含めた癌の治療;ならびに関節リウマチ、乾癬、炎症性腸疾患、クローン病、潰瘍性大腸炎、慢性閉塞性肺疾患、喘息、多発性硬化症、II型糖尿病などの糖尿病、アトピー性皮膚炎、移植片対宿主病または全身性エリテマトーデスの治療が挙げられる。
【0166】
任意の特定の患者に対する具体的な用量レベルは、用いられる特定の化合物の活性、年齢、体重、全体的な健康、性別、食事、投与時間、投与経路、排泄速度、薬物の組み合わせ、および治療を受けている特定の疾患の重症度を含む種々の要因に依存するであろうことは、理解されるであろう。最適な用量レベルおよび投与頻度は、臨床試験によって決定されることになるが、例示的な投薬量は、1日あたり0.1〜1000 mgである。
【0167】
本発明が関係する化合物は、その薬物動態学的性質と合致する任意の経路により投与するために、調製することができる。経口投与可能な組成物は、錠剤、カプセル剤、散剤、顆粒剤、ロゼンジ、液体製剤またはゲル製剤、例えば経口液剤もしくは経口懸濁液、局所用溶液もしくは局所用懸濁液、または無菌の非経口溶液もしくは無菌の非経口懸濁液などの形態とすることができる。経口投与用の錠剤およびカプセル剤は、単位用量の提示形態とすることができ、慣用の賦形剤、例えば結合剤、例えばシロップ、アラビアゴム、ゼラチン、ソルビトール、トラガントもしくはポリビニル-ピロリドン;充填剤、例えばラクトース、糖、トウモロコシデンプン、リン酸カルシウム、ソルビトールもしくはグリシン;錠剤化滑沢剤(tabletting lubricant)、例えばステアリン酸マグネシウム、タルク、ポリエチレングリコールもしくはシリカ;崩壊剤、例えばジャガイモデンプン、または許容される湿潤剤、例えばラウリル硫酸ナトリウムなどを含んでいてもよい。錠剤は、通常の製薬プラクティスにおいて周知の方法に従ってコーティングしてもよい。経口液体製剤は、例えば、水性もしくは油性の懸濁液、溶液、エマルション、シロップ剤もしくはエリキシル剤の形態とすることができ、または使用前に水もしくは他の適切な媒体で再構成するための乾燥製品として提示することができる。かかる液体製剤は、慣用の添加剤、例えば懸濁剤、例えばソルビトール、シロップ、メチルセルロース、グルコースシロップ、ゼラチン、水素化食用脂;乳化剤、例えばレシチン、ソルビタンモノオレアートまたはアラビアゴム;非水性媒体(食用油を含み得る)、例えばアーモンドオイル、分留されたヤシ油、グリセリンなどの油性エステル、プロピレングリコールまたはエチルアルコール;保存剤、例えばp-ヒドロキシ安息香酸メチルもしくはp-ヒドロキシ安息香酸プロピルまたはソルビン酸、および所望される場合は慣用の香味剤または着色剤を含んでいてもよい。
【0168】
皮膚への局所的な適用については、薬物を、クリーム、ローションまたは軟膏になるように調合することができる。薬物に使用することができるクリーム製剤または軟膏製剤は、例えば英国薬局方などの薬剤学の標準的な教科書に記述されている、当該技術分野で周知の慣用の製剤である。
【0169】
吸入による局所適用については、例えば、圧力駆動のジェット式噴霧器もしくは超音波噴霧器によって、または好ましくは、微粒子化した粉末、例えば吸入用カプセル剤または他の「乾燥粉末」送達系の、噴射剤で駆動される計量されたエアロゾルの投与または噴射剤なしの投与によって、エアロゾルを送達するために、薬物を製剤化することができる。かかる吸入される製剤中には、賦形剤、例えば、噴射剤(例えば計量されたエアロゾルの場合にはフリゲン(Frigen))、界面活性物質、乳化剤、安定剤、保存剤、香味料および充填剤(例えば粉末吸入器の場合にはラクトース)などを存在させることができる。吸入のためには、患者に適した吸入技術を用いて、最適な粒径のエアロゾルを発生させ、投与することができる、多くの装置(apparata)を利用できる。特に粉末吸入器の場合、計量されたエアロゾルについては、アダプター(スペーサー、エキスパンダ)およびセイヨウナシ形の容器(例えばNebulator(登録商標)、Volumatic(登録商標))およびパッファスプレー(puffer spray)を放出する自動装置(Autohaler(登録商標))の使用に加えて、いくつかの技術的解決策が利用できる(例えばDiskhaler(登録商標)、Rotadisk(登録商標)、Turbohaler(登録商標)または例えばヨーロッパ特許出願第EP 0 505 321号に記載された吸入器)。
【0170】
眼への局所的な適用については、薬物を、適切な無菌の水性または非水性の媒体中の溶液または懸濁液になるように調合することができる。添加剤、例えばメタ重亜硫酸ナトリウムまたはエデト酸二ナトリウム(disodium edeate)などの緩衝剤;殺菌剤および殺真菌剤を含む保存剤、例えば酢酸フェニル水銀もしくは硝酸フェニル水銀、塩化ベンザルコニウムまたはクロルヘキシジンなど、ならびに増粘剤、例えばヒプロメロースなど、も含めることができる。
【0171】
活性成分はまた、無菌の媒体に入れて非経口的に投与することもできる。使用する媒体および濃度に応じて、薬物を、媒体中に懸濁させるか、または溶解させることができる。有利には、局所麻酔薬、保存剤および緩衝剤などの補助剤を媒体中に溶解させることができる。
【0172】
本発明の化合物は、いくつかの公知の薬学的に活性な物質とともに使用することができる。例えば、本発明の化合物は、細胞毒、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤およびモノクローナル抗体(例えば成長因子受容体に対するもの)とともに使用することができる。好ましい細胞毒としては、例えば、タキサン類(taxanes)、プラチン類(platins)、代謝拮抗剤、例えば5-フルオロウラシル(5-fluoracil)、トポイソメラーゼ阻害剤など、が挙げられる。したがって、式(IA)もしくは(IB)のアミノ酸誘導体、その互変異性体、またはその薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物を含む、本発明の医薬は、典型的には、細胞毒、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体をさらに含む。
【0173】
さらに、本発明は、
(a)(i)式(IA)もしくは(IB)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(ii)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物;
(b)細胞毒性薬、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体;ならびに
(c)薬学的に許容される担体または希釈剤
を含む、医薬組成物を提供する。
【0174】
さらに、ヒトまたは動物の身体の治療に、別々に、同時に、または連続的に使用するための、
(a)(i)式(IA)もしくは(IB)のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(ii)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物;ならびに
(b)細胞毒性薬、HDAC阻害剤、キナーゼ阻害剤、アミノペプチダーゼ阻害剤および/またはモノクローナル抗体
を含む、製品も提供する。
【0175】
合成
本発明が関係する式(IA)または(IB)の化合物の合成については、複数の合成戦略が存在するが、すべてのものが、合成有機化学者に知られた公知の化学に依存している。したがって、式(IA)または(IB)に従う化合物は、標準的な文献に記載された、当業者に周知の手順に従って、合成することができる。典型的な文献の出所は、「Advanced organic chemistry」, 第4版 (Wiley), J March、「Comprehensive Organic Transformation」, 第2版 (Wiley), R.C. Larock、「Handbook of Heterocyclic Chemistry」, 第2版 (Pergamon), A.R. Katritzky、総説記事、例えば「Synthesis」、「Acc. Chem. Res.」、「Chem. Rev」に見出されるものなど、もしくはオンラインでの標準的な文献探索によって特定される一次的な文献の出所であるか、または「Chemical Abstracts」もしくは「Beilstein」などの二次的な出所からのものである。
【0176】
本発明の化合物は、以下に一般的に記載され、本明細書中で以下の実施例においてより具体的に記載される、いくつかの方法によって調製することができる。以下に記載される反応においては、反応性官能基、例えば、ヒドロキシル基、アミノ基およびカルボキシ基が最終生成物に望まれる場合、これらの官能基が反応に不必要に関与することを避けるために、該官能基を保護することが必要な場合がある[例えばGreene, T.W., 「Protecting Groups in Organic Synthesis」, John Wiley and Sons, 1999を参照]。標準的なプラクティスと組み合わせて、慣用の保護基を使用することができる。場合によっては、脱保護が、一般式(IA)または(IB)の化合物の合成の最終工程となることがあり、本明細書中で以下に記載される本発明に従う方法は、かかる保護基の除去に及ぶことを理解されたい。
【0177】
アミノ酸エステル構成要素は、いくつかの方法で調製することができる。スキーム1は、本願のために該構成要素の調製に用いた主な経路を示している。当業者には、やはりこれらの中間体の調製を達成する他の方法があることは、明らかであろう。
【0178】
スキーム1 アミノ酸エステル構成要素の調製の一般的スキーム(R7、R8およびR9は、本明細書中で定義した通りであり、Pは、適切な保護基である)
【0179】
【化10】

【0180】
スキーム2 チオフェンカルボキサミド構成要素Cの調製のスキーム
【0181】
【化11】

【0182】
当業者には、スキーム2に示した一般的経路は、利用可能ないくつかの経路の1つであることは、明らかであろう。例えば、適切なチオフェンカルボキサミド母核の調製方法は、WO 03/104218に詳細に記載されており、その内容は、その全体が参照によって本明細書中に援用される。
【0183】
スキーム3 L1がアルキルであり、A1がフェニルであり、L2が結合であり、x=0であり、Alk1がメチルであり、R7、R8およびR9が本明細書中で定義した通りである化合物の調製の一般的スキーム)
【0184】
【化12】

【0185】
スキーム3は、対応するベンズアルデヒドによるアミノ酸エステルの還元的アミノ化を含み、その後にN-保護およびヘック(Heck)反応が続き、重要なアルデヒド中間体を生じさせる、方法を示している。この中間体は、2-シアノアセトアミドを用いて、チオフェン環に転換される。基L1の性質が合成経路の選択に影響することになるのは、当業者には明らかであろう。当業者は、かかる化合物の合成の合成可能性を容易に認識する。
【0186】
スキーム4 酸の、その対応するエステルからの調製の一般的スキーム(L1、A1、L2、x、Alk1、R7、R8およびR9は、本明細書中で定義した通りである)
【0187】
【化13】

【0188】
本明細書中に記載したエステルのカルボン酸誘導体は、その親のエステルから、加水分解によって、容易に調製することができる。当業者には、除去するエステル基に応じて、塩基性条件または酸性条件のいずれを用いることができるかは、明らかであろう。
【実施例】
【0189】
以下の実施例は、いくつかの特定の本発明の化合物の調製および性質を説明するものである。次の略語が使用される。
MeOH=メタノール
EtOH=エタノール
EtOAc=酢酸エチル
Boc=tert-ブトキシカルボニル
DCE=ジクロロエタン
DCM=ジクロロメタン
DMA=N,N-ジメチルアセトアミド
DME=1,2-ジメトキシエタン
DMF=ジメチルホルムアミド
DMSO=ジメチルスルホキシド
Bu4NBr=テトラブチルアンモニウムブロミド
MeCN=アセトニトリル
TFA=トリフルオロ酢酸
THF=テトラヒドロフラン
Na2CO3=炭酸ナトリウム
HCl=塩酸
NaH=水素化ナトリウム
NaHCO3=炭酸水素ナトリウム
Pd/C=パラジウム炭素
N2=窒素
Na2SO4=硫酸ナトリウム
Et3N=トリエチルアミン
STAB=ナトリウムトリアセトキシボロヒドリド
MgSO4=硫酸マグネシウム
EDCI=N-(3-ジメチルアミノプロピル)-N′-エチルカルボジイミド塩酸塩
Et2O=ジエチルエーテル
LiOH=水酸化リチウム
ELS=蒸発光散乱
TLC=薄層クロマトグラフィー
mL=ミリリットル
g=グラム
mg=ミリグラム
mol=モル
mmol=ミリモル
LCMS=高速液体クロマトグラフィー/質量分析法
NMR=核磁気共鳴
RT=室温
sat.=飽和水溶液
【0190】
市販の試薬および溶媒(HPLCグレード)は、さらに精製することなく使用した。溶媒は、BuchiロータリーエバポレーターまたはVirTis Benchtop SLC凍結乾燥機を用いて除去した。マイクロ波照射は、Biotage InitiatorTM Eightマイクロ波シンセサイザーを用いて行なった。特定の水素化は、Thales Technology H-Cube HC-2連続水素化装置を用いて行った。フラッシュクロマトグラフィーカラムによる化合物の精製は、Fluorochemから入手した、粒径40〜63 μm(230〜400メッシュ)のシリカゲルを用いて行った。分取HPLCによる化合物の精製は、逆相AxiaTM分取用(prep)Luna C18カラム(10 μm、100×21.2 mm)、10分間にわたる0%B〜100%B(A=水+0.05%TFA、B=アセトニトリル)のグラジエント、流速=25 mL/min、254 nmでのUV検出を用いて、Gilsonシステムで行った。
【0191】
1H NMRスペクトルは、重水素化溶媒中で、Bruker 300 MHz AV分光計で記録した。化学シフトδは、百万分率単位のものである。薄層クロマトグラフィー(TLC)分析は、Kieselgel 60 F254(Merck)プレートを用いて行い、UV光を用いて可視化した。
【0192】
分析用HPLC/MSは、逆相Luna C18カラム(3 μm、50×4.6 mm)、2.25分間にわたる5%B〜95%B(A=水+0.1%のギ酸、B=アセトニトリル+0.1%のギ酸)のグラジエント、流速=2.25 mL/minを用いて、Agilent HP1100 LCシステムで行った。UVスペクトルは、G1315B DAD検出器を用いて、220 nmおよび254 nmで記録した。質量スペクトルは、LC/MSD SL G1956B検出器で、150〜800のm/z範囲にわたって得た。データは、ChemStationおよびChemStation Data Browserソフトウェアを用いて、積分し、報告した。
【0193】
図1 本明細書中に記載した実施例の合成において、次の構成要素を使用した。
【0194】
【化14】

【0195】
構成要素A スキーム1、経路3で概説した方法を用いて、シクロペンチルL-ロイシナートを調製した。
L-ロイシン(5 g、30.5 mmol)を含むシクロヘキサン(150 mL)のスラリーに、シクロペンタノール(27.5 mL、305 mmol)およびp-トルエンスルホン酸(6.33 g、33.3 mmol)を加えた。反応には、ディーン・スターク(Dean-Stark)受け器を取り付け、完全に溶解させるために135℃に加熱した。この温度を12時間の間維持し、その時間の後、反応を完結させた。反応をRTまで冷却すると、白色固体が沈殿した。この固体をろ過し、EtOAcで洗浄してから、減圧下で乾燥させた。所要の生成物をトシル酸塩として単離した(10.88 g、85 %)。m/z = 200 [M+H]+; 1H NMR (300 MHz, CD3OD) δ: 1.01 (6H, t, J=5.8 Hz), 1.54-2.03 (11H, m), 2.39 (3H, s), 3.96 (1H, t, J=6.5 Hz), 5.26-5.36 (1H, m), 7.25 (2H, d, J=7.9 Hz), 7.72 (2H, d, J=8.3 Hz)。
【0196】
構成要素B tert-ブチルL-ロイシナートは、市販されている(Novabiochem、カタログ番号:04-12-5108)。
【0197】
構成要素C WO 03/104218に記載された方法を用いて、5-ブロモ-2-(カルバモイルアミノ)チオフェン-3-カルボキサミドを調製した。
【0198】
(実施例)
実施例1 シクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナート
【0199】
【化15】

【0200】
スキーム5 構成要素Aからの実施例1の調製方法
【0201】
【化16】

【0202】
中間体1a 以下のように、シクロペンチルN-(tert-ブトキシカルボニル)-L-ロイシナートを調製した。
構成要素A(5 g、13.5 mmol)を含むDCM(100 mL)に、Et3N(3.76 mL、26.9 mmol)およびジ-tert-ブチルジカルボナート(3.24 g、14.8 mmol)を加えた。この反応混合物を室温で18時間攪拌し、次いでDCM(100 mL)で希釈し、1M HCl、NaHCO3 sat.で、次いでブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮して所望の生成物を無色の油状物として得、これをさらなる精製も特徴付けもせずに先に進めた(4 g、収率100%)。
【0203】
中間体1b 以下のように、中間体1aからシクロペンチルN-(tert-ブトキシカルボニル)-N-(4-ヨードベンジル)-L-ロイシナートを調製した。
中間体1a(1.8 g、6 mmol))およびBu4NI(476 mg、1.2 mmol)を含むDMF(50 mL)に、0℃で、NaH(480 mg、12 mmol)を含むDMF(3 mL)を加えた。反応を5分間攪拌してから、4-ヨード-ベンジルブロミド(3.56g、12 mmol)を加えた。この反応混合物を室温まで温まらせ、反応を完結させるために4時間攪拌した。EtOAcを加え(200 mL)、有機層を水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(10%EtOAc/ヘプタン)により精製することにより、所要の生成物が固体として得られ(2.56 g、収率82%)、m/zは516 [M+H]+であった。
【0204】
中間体1c 以下のように、中間体1bからシクロペンチルN-(tert-ブトキシカルボニル)-N-[4-(3-オキソプロピル)ベンジル]-L-ロイシナートを調製した。
【0205】
中間体1b(2.56 g、4.9 mmol)を含むDMF(17 mL)に、Pd(OAc)2(34 mg、0.15 mmol)、アリルアルコール(0.51 mL、7.5 mmol)、NaHCO3(1.04 g、12.4 mmol)、Bu4NBr(1.6 g、4.9 mmol)および4Åモレキュラーシーブ(965 mg)を加えた。この反応混合物を、80℃で2時間加熱した。室温まで冷却し、混合物をセライトを通してろ過し、DMFおよび水で洗浄した。母液をジエチルエーテル(2×50 mL)で抽出し、有機層を水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(30%EtOAc/ヘプタン)により精製することにより、所要の生成物が固体として得られ(1.66 g、収率75%)、m/zは446 [M+H]+であった。
【0206】
中間体1d 以下のように、中間体1cからシクロペンチルN-{4-[(5-アミノ-4-カルバモイル-2-チエニル)メチル]ベンジル}-N-(tert-ブトキシカルボニル)-L-ロイシナートを調製した。
2-シアノ-アセトアミド(306 mg、3.61 mmol)、硫黄(116 mg、3.61 mmol)および中間体1c(1.61 g、3.61 mmol)の混合物を含むDMF(12 mL)に、トリエチルアミン(0.5 mL、3.61 mmol)を滴下した。生じた混合物を室温で18時間攪拌し、次いで水中に注ぎ、EtOAc(2×100 mL)で抽出した。合わせた有機層をブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(50%EtOAc/ヘプタン)による精製により、所要の生成物(710 mg、収率36%)が得られ、m/zは544 [M+H]+であった。
【0207】
中間体1e 以下のように、中間体1dからシクロペンチルN-(tert-ブトキシカルボニル)-N-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体1d(300 mg、0.55 mmol)の無水DCM(6 mL)溶液に、0℃で、窒素下で、クロロスルホニルイソシアナート(58 μL、0.67 mmol)を滴下した。反応混合物を室温まで温まらせ、反応を完結させるために3時間攪拌した。反応を水(2 mL)でクエンチし、10分間攪拌し、EtOAcとNaHCO3satとの間で分配した。有機層をブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(5%MeOH/DCM)により精製することにより、所要の生成物(100 mg、収率31%)が得られ、m/zは587 [M+H]+であった。
【0208】
実施例1 以下のように、中間体1eからシクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体1e(100 mg)をDCM(2 mL)およびTFA(2 mL)に溶解し、室温で18時間攪拌した。この反応混合物を真空中で濃縮し、メタノールに溶解し、SCX陽イオン交換樹脂によって精製した。これに続くGilson分取HPLCによる精製により、所要の生成物が淡褐色の固体として得られた(60 mg、収率72%)。
【0209】
LCMSによる純度 = 95 %; m/z = 487 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.28-7.18 (4H, q, J=8.1Hz), 6.91 (1H, s), 5.16-5.07 (1H, m), 3.98 (2H, s), 3.73 (1H, d, J=12.9Hz), 3.63 (1H, d, J=12.9Hz), 3.24 (1H, t, J=7.3Hz), 1.94-1.56 (9H, m), 1.51-1.43 (1H, m), 0.91 (3H, d, J=6.6Hz), 0.85 (3H, d, J=6.6Hz)。
【0210】
実施例2 tert-ブチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナート
【0211】
【化17】

【0212】
スキーム6 構成要素Bからの実施例2の調製方法
【0213】
【化18】

【0214】
中間体2a 以下のように、tert-ブチルN-(4-ヨードベンジル)-L-ロイシナートを調製した。
構成要素B(2.89 g、12.9 mmol)を含むDCM(40 mL)に、4-ヨードベンズアルデヒド(2 g、8.63 mmol)を加えた。反応を2時間攪拌してから0℃まで冷却し、STAB(5.47 g、25.86 mmol)を少しずつ加えた。反応を室温まで温まらせ、18時間攪拌した。この反応混合物をDCM(100 mL)で希釈し、1M HCl、NaHCO3sat.およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(20%EtOAc/ヘプタン)により精製することにより所要の生成物(2.81 g、収率80%)が得られ、m/zは404 [M+H]+であった。
【0215】
中間体2b 以下のように、中間体2aからtert-ブチルN-(tert-ブトキシカルボニル)-N-(4-ヨードベンジル)-L-ロイシナートを調製した。
中間体2a(2.8 g 7 mmol)を含むアセトニトリル(30 mL)に、ジ-tert-ブチルジカルボナート(3.08 g、14.1 mmol)を加えた。反応を室温で18時間攪拌させておいてから、減圧下で濃縮した。粗製の残渣をEtOAcに溶解し、水およびブラインで洗浄し、乾燥させ(MgSO4)、減圧下で濃縮した。カラムクロマトグラフィー(3%EtOAc/ヘプタン)により精製することにより、所要の生成物(3.5 g、収率100%)が得られ、これをさらなる精製も特徴付けもせずに先に進めた。
【0216】
中間体2c〜2eを、実施例1について記載した方法と同じ方法を用いて調製した。
【0217】
実施例2 以下のように、中間体2eからtert-ブチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシナートを調製した。
中間体2e(20 mg)を含むジオキサン(2 mL)に、0℃で、窒素下で、4M HCL/ジオキサン(0.5 mL)を加えた。反応を0℃で2時間攪拌してからNaHCO3 satでクエンチし、減圧下で濃縮した。残渣をメタノールに溶解し、SCX陽イオン交換樹脂によって精製して、所要の生成物(8 mg)を得た。
LCMSによる純度 = 85 %; m/z = 475 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.35 (2H, d, J=8.1Hz), 7.30 (2H, d, J=8.1Hz), 6.96 (1H, s), 4.03 (2H, s), 3.95-3.80 (2H, m), 2.25-2.16 (1H, m), 1.85-1.65 (2H, m), 1.51 (9H, s), 1.17-1.11 (1H, m), 0.96 (3H, d, J=6.6Hz), 0.92 (3H, d, J=6.6Hz)。
【0218】
実施例3 シクロペンチルN-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシナート
【0219】
【化19】

【0220】
スキーム7 構成要素Aおよび構成要素Cからの実施例3の調製方法
【0221】
【化20】

【0222】
中間体3a 以下のように、4-[(E)-2-(4,4,5,5-テトラメチル-1,3,2-ジオキサボロラン-2-イル)ビニル]ベンズアルデヒドを調製した。
4-ブロモベンズアルデヒド(1.818 g、9.83 mmol)、酢酸パラジウム(0.110 g、0.491 mmol)および1,10-フェナントロリン(0.089 g、0.491 mmol)をバイアルに仕込み、その後、バイアルをN2でパージした。無水アセトニトリル(15 mL)を加え、室温で攪拌した。トリエチルアミン(2.74 ml、19.65 mmol)およびビニルボロン酸ピナコールエステル(2.0 ml、11.79 mmol)を加え、この反応混合物を60℃に18時間加熱した。17時間後のLCMS分析では、わずか15%の生成物および75%の4-ブロモベンズアルデヒド出発物質が示された。さらなる酢酸パラジウム(55 mg)および1,10-フェナントロリン(45 mg)をMeCN溶液として加え、反応をさらに24時間、60℃で加熱した。反応を冷却し、2M HClを加え、ジエチルエーテルで抽出した。有機層を2M HClおよびブラインで洗浄し、乾燥させ(MgSO4)、真空中で濃縮した。カラムクロマトグラフィー(50〜100%DCM/ヘキサンにより精製することにより、所要の生成物が淡黄色の固体として得られ(0.54 g、収率22%)、m/zは259 [M+H]+であった。
【0223】
中間体3b 以下のように、中間体3aから2-(カルバモイルアミノ)-5-[(E)-2-(4-ホルミルフェニル)ビニル]チオフェン-3-カルボキサミドを調製した。
構成要素C(453 mg、1.714 mmol)およびテトラキスパラジウム(198 mg、0.171 mmol)に、中間体3a(531 mg、2.057 mmol)を加え、N2でパージした。重炭酸ナトリウム飽和水溶液1 mLとともに、DME(7 mL)を加えた。この混合物を、反応を完結させるために80℃で20時間加熱した。反応混合物を冷却し、1M HCl(200 mL)の中に注ぎ、EtOAc(300 mL)中へ抽出した。合わせた有機層を乾燥させ(MgSO4)、真空中で濃縮して、生成物が黄色固体として得られ(342 mg、収率60.7%)、m/zは314 [M-H]+であった。
【0224】
中間体3c 以下のように、中間体3bからシクロペンチルN-(4-{(E)-2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]ビニル}ベンジル)-L-ロイシナートを調製した。
中間体3b(249 mg、0.790 mmol)および構成要素A(157 mg、0.790 mmol)をTHF(15 mL)および酢酸(15 mL)に溶解し、室温で30分間攪拌した。STAB(502 mg、2.369 mmol)を少しずつ加え、反応を48時間攪拌した。2M HClを加え、生成物をEtOAc中へ抽出した。合わせた有機物抽出液を水で洗浄し、乾燥させ(MgSO4)、真空中で濃縮して、オレンジ色の油状固体477 mgを得た。カラムクロマトグラフィー(2〜4%MeOH/DCM)およびそれに続くSCX陽イオン交換樹脂により精製することにより、所要の生成物が得られ(40 mg、収率10%)、m/zは499 [M+H]+であった。
【0225】
実施例3 以下のように、中間体3cからシクロペンチルN-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシナートを調製した。
中間体3c(40 mg、0.080 mmol)をメタノール(6 mL)に溶解し、Pd/CaCO3(Pbを触媒毒とする)を用いて、1 barの圧力で、3 mL/minでH-Cube水素化装置を通るようにポンピングした。減圧下でメタノールを除去し、カラムクロマトグラフィー(3〜5%MeOH/DCM)によって粗製の残渣を精製し、標題の化合物を得た(15 mg、収率38%)。
LCMSによる純度 = 96 %; m/z = 501 [M+H]+; 1H NMR (300 MHz, DMSO-d6) 10.85 (1H, s), 7.50 (1H, br s), 7.20 (4H, m), 7.15 (1H, br s), 7.01 (1H, s), 6.78 (2H, br s), 5.1 (1H, m), 3.70 (1H, d, J=6.5Hz), 3.50 (1H, d, J=6.3Hz), 3.05 (1H,s), 2.23 (1H, m), 1.8 (2H, m), 1.70-1.50 (7H, bm), 1.35 (2H, m), 0.82 (3H, d, J=6.8Hz), 0.79 (3H, d, J=6.4Hz)。
【0226】
実施例4 シクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチニル}ベンジル)-L-ロイシナート
【0227】
【化21】

【0228】
スキーム8 構成要素Aおよび構成要素Cからの実施例4の調製方法
【0229】
【化22】

【0230】
中間体4a シクロペンチルN-(4-エチニルベンジル)-L-ロイシナート
構成要素A(918 mg、4.6 mmol)のDCM(60 mL)溶液に、4-エチニルベンズアルデヒド(500 mg、3.84 mmol)を加えた。反応を3時間攪拌してから、0℃に冷却した。次いで、STAB(2.44 g、11.5 mmol)を少しずつ加え、室温で18時間攪拌を続けた。反応をDCM(50 mL)で希釈し、1M HCL(100 mL)、NaHCO3 sat(100 mL)、ブライン(50 mL)で洗浄し、乾燥させ(MgSO4)、真空中で濃縮した。カラムクロマトグラフィー(25%EtOAc/ヘプタン)により精製することにより所要の生成物(0.878 g、収率73%)が得られ、m/zは314 [M+H]+であった。
【0231】
実施例4 以下のように、中間体4aからシクロペンチルN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチニル}ベンジル)-L-ロイシナートを調製した。
DMA(2.5 mL)およびEtOH(2.5 mL)の中で、中間体4a(200 mg、0.64 mmol)を構成要素C(91 mg、0.34 mmol)と混合した。次いで、ジ-イソプロピルエチルアミン(0.184 mL、1.0 mmol)およびヨウ化銅(20 mg、0.10 mmol)を加え、溶液を窒素を用いて15分間脱気した。次いで、(1,1-ビス(ジフェニルホスフィノ)--フェロセンジクロロパラジウム(8 mg、8wt%)を加え、反応を65℃に18時間加熱した。反応混合物を冷却し、セライトを通してろ過し、Gilson分取HPLCによって精製した。所要の生成物を白色固体として単離した(17 mg、収率10%)。
LCMSによる純度 = 90 %; m/z = 497 [M+H]+; 1H NMR (300 MHz, CD3OD) 7.61 (2H, d, J=6.5Hz), 7.55 (2H, d, J=6.8Hz), 7.45 (1H, s), 5.31 (1H, m), 4.25 (2H, m), 4.05 (1H, m), 2.05-1.65 (11H, bm), 1.00 (6H, m)。
【0232】
実施例5 N-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシン
【0233】
【化23】

【0234】
スキーム9 実施例1からの実施例5の調製方法
【0235】
【化24】

【0236】
実施例5 以下のように、実施例1からN-(4-{[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]メチル}ベンジル)-L-ロイシンを調製した。
実施例1(50 mg、0.1 mmol)のTHF(2 mL)および水(2 mL)の溶液に、水酸化リチウム(25 mg、1 mmol)を加えた。この反応混合物を、反応を完結させるために40℃で18時間加熱した。反応を室温まで冷却し、THFを減圧下で除去してから、水で希釈し、酢酸でpHを4に調節した。沈殿をろ過し、水およびジエチルエーテルで洗浄してから、Gilson分取HPLCによって精製した。所要の生成物を白色固体として単離した(11 mg、収率26%)。
LCMSによる純度 = 94 %; m/z = 419 [M+H]+; 1H NMR (300 MHz, DMSO-d6) 10.88 (1H, s), 7.58 (1H, br s), 7.33 (2H, d, J=7.8Hz), 7.23 (2H, d, J=7.8Hz), 7.16 (1H, br s), 7.06 (1H, s), 6.83 (2H, br s),3.94 (2H, s), 3.90 (1H, d,J=13.2Hz), 3.75 (1H, d, J=13.2Hz), 3.13 (1H, t, J=7.1Hz), 1.90-1.70 (1H, m), 1.52-1.40 (2H, m),0.85 (3H, d, J=6.6Hz), 0.79 (3H, d, J=6.6Hz)。
【0237】
実施例6 N-(4-{2-[4-カルバモイル-5-(カルバモイルアミノ)-2-チエニル]エチル}ベンジル)-L-ロイシン
【0238】
【化25】

【0239】
スキーム10 実施例3からの実施例6の調製方法
【0240】
【化26】

【0241】
実施例6を、実施例5について記載した方法と同じ方法を用いて調製した。
LCMSによる純度 = 97 %; m/z = 431 [M-H]+; 1H NMR (300 MHz, DMSO-d6) 10.85 (1H, s), 7.49 (1H, br s), 7.22 (2H, d, J=7.8Hz), 7.15 (2H, d, J=7.8Hz), 7.10 (1H, br s), 6.99 (1H, s), 6.75 (2H, br s), 3.75 (1H, d, J=13.2Hz), 3.50 (1H, d, J=13.2Hz), 3.13 (1H, m), 1.75 (1H, m), 1.40-1.20 (3H, bm), 0.83 (3H, d, J=6.6Hz), 0.73 (3H, d, J=6.6Hz)。
【0242】
生物学的アッセイ
IKKβ酵素アッセイ
化合物がIKKβキナーゼ活性を阻害する能力を、Invitrogen(Paisley,UK)が実施するアッセイで測定した。Z’−LYTETM生化学アッセイは、蛍光ベースの共役酵素形式を用い、タンパク質分解性の切断に対する、リン酸化ペプチド及び非リン酸化ペプチドの感受性の差に基づく。ペプチド基質は、2つのフルオロフォア(各末端に1つずつ)で標識され、これらはFRETペアを構成する。一次反応において、キナーゼは、ATPのγ−リン酸を合成FRETペプチド中の単一のセリン又はスレオニン残基に転移させる。二次反応では、部位特異的プロテアーゼが非リン酸化FRETペプチドを認識し、切断する。FRETペプチドのリン酸化は、発色試薬(Development Reagent)による切断を抑制する。切断は、FRETペプチド上のドナーフルオロフォア(即ち、クマリン)とアクセプターフルオロフォア(即ち、フルオレセイン)との間のFRETを破壊するが、未切断のリン酸化FRETペプチドはFRETを維持する。400nmでのドナーフルオロフォアの励起後のドナー発光対アクセプター発光の比率(発光比(Emission Ratio))を計算する放射測定法を使用して、反応の進行を定量する。
【0243】
最終的な10μLのキナーゼ反応(Kinase Reaction)は、50mM HEPES(pH7.5)、0.01% BRIJ−35、10mM MgCl2、1mM EGTA中0.9〜8.0ngのIKBKB(IKKβ)、2μM Ser/Thr 05 Peptide及びATPからなる。このアッセイは、Km又はその近傍のATP濃度で実施される。室温で60分のキナーゼ反応インキュベーション後、1:128希釈の発色試薬を5μL添加する。アッセイプレートを室温でさらに60分間インキュベートし、蛍光プレートリーダーで読み取る。
【0244】
二連のデータポイントを、試験化合物のDMSO中ストック溶液の1/3 log希釈系列から生成する。9回の希釈工程を10μMの最高濃度から行い、「化合物なし」のブランクを含める。IDBSのXlfitソフトウェアを使用して、データを収集し分析する。用量反応曲線は、モデル番号205(シグモイダル用量反応モデル)にフィットさせた曲線である。得られた曲線から、50%阻害を与える濃度を決定し、報告する。
【0245】
THP−1細胞のLPS刺激
THP−1細胞を、V底96ウェルの組織培養物処理したプレート中、4×104細胞/ウェルの密度で100μlプレートし、5% CO2中37℃で16時間インキュベートした。100μlの組織培養培地中の阻害剤を添加して2時間後、細胞を1μg/mlの最終濃度のLPS(E coli株005:B5、Sigma)で刺激し、5% CO2中37℃で6時間インキュベートした。TNF−αレベルを、サンドイッチELISA(R&D Systems #QTA00B)によって無細胞上清から測定した。
【0246】
ヒト全血のLPS刺激
ヘパリン処理バキュテナー(Becton Dickinson)を使用した静脈穿刺によって全血を採取し、等体積のRPMI1640組織培養培地(Sigma)中に希釈した。V底96ウェルの組織培養物処理したプレートに100μlをプレートした。100μlのRPMI1640培地中の阻害剤を添加して2時間後、血液を100ng/mlの最終濃度のLPS(E coli株005:B5、Sigma)で刺激し、5% CO2中37℃で6時間インキュベートした。TNF−αレベルを、サンドイッチELISA(R&D Systems #QTA00B)によって無細胞上清から測定した。
【0247】
破壊細胞アッセイ
特定の基R2を含む化合物が1種以上の細胞内カルボキシルエステラーゼ酵素によって−COOH基に加水分解され得るか否かを決定するために、化合物を以下のアッセイで試験することもできる:
【0248】
細胞抽出物の調製
U937又はHUT78腫瘍細胞(約109)を、4体積のDulbeccos PBS(約1リットル)で洗浄し、4℃で10分間525gでペレット化する。これを2回繰り返し、最終的な細胞ペレットを35mlの冷ホモジナイジングバッファー(Trizma 10mM、NaCl 130mM、CaCl2 0.5mM、pH7.0、25℃)中に再縣濁する。ホモジネートを窒素キャビテーション(4℃で50分間700psi)によって調製する。このホモジネートを氷上に維持し、Leupeptin 1μM、Aprotinin 0.1μM、E64 8μM,Pepstatin 1.5μM、Bestatin 162μM、Chymostatin 33μMの最終濃度の阻害剤カクテルを添加する。1500rpmで10分間遠心分離して細胞ホモジネートを清澄化した後、得られた上清をエステラーゼ活性の供給源として使用し、必要になるまで−80℃で保存する。
【0249】
エステル開裂の測定
対応するカルボン酸へのエステルの加水分解は、上のように調製した細胞抽出物を使用して測定することができる。この趣旨で、細胞抽出物(総アッセイ体積0.5ml中約30μg)を、Tris−HCl 25mM、125mM NaClバッファー、pH7.5、25℃中で、37℃でインキュベートする。次いで、ゼロ時点で2.5mMの最終濃度のエステル(基質)を添加し、サンプルを適切な時間(通常0分間又は80分間)にわたり37℃でインキュベートした。2×体積のアセトニトリルを添加して反応を停止させる。ゼロ時点のサンプルについては、エステル化合物の前にアセトニトリルを添加する。12000gで5分間の遠心分離後、サンプルを、エステル及びその対応するカルボン酸について、LCMS(Sciex API 3000、HP1100バイナリポンプ、CTC PAL)によって室温にて分析する。クロマトグラフィーは、MeCN(75×2.1mm)カラム及び水/0.1%ギ酸中5〜95%のアセトニトリルの移動相に基づいた。加水分解速度はpg/mL/minで表す。
【0250】
インタクト細胞蓄積アッセイ
細胞(4×104/mL)を、5%(v/v)CO2−加湿雰囲気中で、6μmol/Lの化合物を含む培養倍地中37℃でインキュベートした。インキュベーションは、6時間後に、細胞懸濁物の25mLアリコートを4℃で1500rpmで5分間遠心分離することによって終了させた。培養培地上清の0.2mLサンプルを、4体積のアセトニトリルに添加した。上清をデカントした後、残った細胞ペレット(106細胞)を1mLのアセトニトリル中に抽出した。次いで、LC/MS/MS(Sciex API3000)で室温にて、サンプルをエステル及び酸代謝産物について分析した。クロマトグラフィーは、MeCN(75×21mm)カラムと5%〜95%(v/v)のアセトニトリル/水、0.1%(v/v)ギ酸移動相とに基づいた。ゼロ時点のサンプルについては、細胞懸濁物を冷却し、エステルを添加して直ぐに遠心分離し、次いで記載されたようにアセトニトリル中に抽出した。細胞中のレベルはng/mLで表す。
【0251】
結果:
本発明の例示的な化合物について生物学的アッセイで得られたIC50値を表1中に示す。IC50値は、以下の3つの範囲のうち1つに割り当てられる:
範囲A:IC50<500nM
範囲B:500nM<IC50<5000nM
範囲C:IC50>5000nM
【0252】
【表1】

【0253】
NT=試験せず。
NR=不適当。実施例5−6は、細胞の内側で開裂されるアミノ酸エステルの結果物カルボン酸のアナログである。これらのカルボン酸は、細胞と接触しても細胞中へ浸透せず、従って、これらのアッセイではTNF−α産生を阻害しない。
【0254】
0時間又は6時間のインキュベーション時間後の、U937(単球細胞株)細胞及びHUT78(非単球細胞株)細胞と関連した実施例1及び5の化合物の濃度を、表2に示す。
【0255】
【表2】

【0256】
表2は、実施例1の化合物(エステル誘導体)が、0時間の時点で、それぞれ420ng/106細胞及び466ng/106細胞の濃度で、U937細胞株及びHUT78細胞株の両方に蓄積できることを示している。6時間のインキュベーション後、実施例5の化合物(酸誘導体)は、U937単球細胞株中に選択的に蓄積し(268ng/106細胞)、対応するHUT78非単球細胞株には蓄積しないことが明らかになった。実施例1の化合物は、ヒトカルボキシルエステラーゼhCE−1(U937などのマクロファージ関連細胞株中にのみ存在する)によって加水分解されるので、実施例4の化合物は、マクロファージ関連細胞中に選択的に蓄積するであろう。6時間の時点でのHUT78中の実施例1の化合物の濃度は、0時間の時点から変化していない(466対465ng/106細胞)。0時間の時点でU937細胞と関連している少量の実施例5は、細胞と培地との分離の間に細胞内で形成された酸を反映している。
【0257】
実施例1の化合物とその親分子(化合物1)との間のin vitro生物学的データの比較を表3に示す。
【0258】
【表3】

【0259】
表3は、実施例1の化合物の酸が、酵素アッセイにおいてその親化合物(化合物1)と類似のIC50を有することを示し、これは、酵素への結合が、エステラーゼモチーフの結合によって破壊されなかったことを示している。実施例1の化合物などのメチレン架橋された化合物(即ち、L1がメチレン基である)は、hCE−1によって加水分解され、結果として酸が細胞中に蓄積する。この酸の蓄積は、実施例1の化合物が、特にヒト全血アッセイにおいて、親化合物よりもかなり強力であるという結果をもたらす。これらのデータは、エステラーゼモチーフの結合と、それにより生じる対応する酸の細胞蓄積によって達成され得る強力な利益を強調する。
【特許請求の範囲】
【請求項1】
(a)式(IA)もしくは(IB):
【化1】

〔式中、
・L1は、C1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表すか、またはL1は、基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-もしくは-(CH2)mNR1(CH2)n-(式中、R1は、C1〜4アルキルであり、mおよびnは、同一であるか、もしくは異なっており、0、1、2、3もしくは4である)を表し;
・環A1は、さらなるC6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、C6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基であり;
・Wは、式:
【化2】

{式中、
・L2は、基-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、結合、またはC1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表し;
・Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し;
・A2は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基または5〜6員のヘテロアリール基を表し;
・Hetは、-O-、-S-または-NR’-(式中、R’は、水素もしくは非置換C1〜2アルキルを表す)を表し;
・xは、0または1であり;
・Alk1は、結合、またはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基、または基-A3-Alk4-(式中、A3は、縮合していないか、もしくはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基もしくは5〜6員のヘテロアリール基を表し、Alk4は、結合、もしくはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基を表す)を表し;
・Rは、式(X1)、(X2)、(Y1)または(Y2):
【化3】

[式中、
・R2は、基-COOH、または1種以上の細胞内カルボキシルエステラーゼ酵素によって-COOH基に加水分解され得るエステル基であり;
・R3は、水素原子またはC1〜4アルキル基を表し;
・R4、R7およびR8は、同一であるか、または異なっており、それぞれ天然α-アミノ酸または非天然α-アミノ酸のα-置換基を表すか、あるいはR7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和スピロシクロアルキル環またはヘテロシクリル環を形成し;
・R5は、水素原子、またはC1〜6アルキル基、C3〜7カルボシクリル基、C6〜10アリール基もしくは5〜6員のヘテロアリール基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくはC1〜6アルキル基である)を表し;
・環Dは、5〜6員のヘテロシクリル基であり、ここでR2は、示された環窒素に隣接する環炭素に結合しており;R7は、存在する場合、R2と同じ環炭素に結合しており;環Dは、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合していてもよい]
の基を表す(ただし、Rが式(Y2)の基を表し、かつ環Dがフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合している場合、波線によって横切られた示された結合は、環Dまたは前記第二の環の環原子からのものであってもよい)}
の基を表し;
式中、別段記載しない限り、
・R1、R2、R3、R4、R5、R6、R7、R8、L1、Alk1、Alk2、Alk3およびAlk4における、任意のアルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、同一であるか、または異なっており、それぞれ置換されていないか、または1個、2個もしくは3個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン原子ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、-SR’基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択され;
・A1、A2、A3、DおよびR5における、任意のアリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分は、同一であるか、または異なっており、それぞれ置換されていないか、またはハロゲン原子ならびにシアノ基、ニトロ基、C1〜4アルキル基、C1〜4アルコキシ基、C2〜4アルケニル基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、C1〜4ヒドロキシアルキル基、-SR’基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、もしくは異なっており、水素もしくは非置換C1〜4アルキルを表す)から選択される1個、2個、3個もしくは4個の非置換置換基によって、もしくは式-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBもしくは-NRACONRARB(式中、RAおよびRBは、同一であるか、もしくは異なっており、非置換C1〜6アルキル、C3〜6シクロアルキル、非縮合フェニル、もしくは非縮合の5〜6員のヘテロアリールを表すか、もしくはRAおよびRBは、同一の窒素原子に結合している場合、非縮合の5員もしくは6員のヘテロシクリル基を形成する)の置換基から選択される1個、2個、3個もしくは4個の非置換置換基によって、置換されている〕
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物。
【請求項2】
・R4、R7およびR8が、同一であるか、または異なっており、それぞれ異なるものを示し、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合もしくはC1〜6アルキレン基を表し、Bは、C6〜10アリール基もしくは5〜10員のヘテロアリール基を表す);または
(iv)インドール-3-イルメチル、-CH2COOH、-CH2CH2COOH、-CH2CONH2、-CH2CH2CONH2、-CH2CH2CH2NHC(NH)NH2、シクロヘキシル、シクロヘキシルメチルおよび1-ベンジルチオ-1-メチルエチルから選択される基
を表し(represents different and each represents represents)、
・前記(ii)におけるC1〜6アルキル基が、置換されていないか、または1個もしくは2個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)を表し;
・前記(iii)におけるC1〜6アルキレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・前記(iii)におけるC6〜10アリール基または5〜10員のヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1に記載の化合物。
【請求項3】
・L1が、-O-、-S-、-NR1-またはC1〜4アルキレン[式中、R1は、非置換のC1〜4アルキルを表し、C1〜4アルキレン部分は、置換されていないか、もしくは1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、もしくは異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される]を表す、
請求項1または2に記載の化合物。
【請求項4】
・L1が、-O-またはC1〜4アルキレン[式中、C1〜4アルキレン部分は、置換されていないか、もしくは1個もしくは2個の非置換の置換基で置換されており、該置換基は、同一であるか、もしくは異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される]を表す、
請求項1〜3のいずれか1項に記載の化合物。
【請求項5】
・A1が、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロシクリル基に縮合しており、前記A1基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1〜4のいずれか1項に記載の化合物。
【請求項6】
・Alk2が、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk3が、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・A2が、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1〜5のいずれか1項に記載の化合物。
【請求項7】
・Hetが、-O-、-NR’または-S-(式中、R’は、水素もしくは非置換のメチルを表す)を表し;
・Alk1が、結合、またはC1〜6アルキレン基を表し、該アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3が、水素原子または非置換のC1〜2アルキル基を表し;
・R4、R7およびR8が、同一であるか、または異なっており、水素原子;C1〜6アルキル基[該アルキル基は、置換されていないか、または1個もしくは2個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)を表す];または式-L3-Bの基(式中、L3は、結合または非置換のC1〜4アルキレン基であり、Bは、フェニル基または5〜10員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、C1〜4アルキル、C1〜2アルコキシ、C1〜2アルキルチオおよびヒドロキシを表す)を表し;
・R5が、水素原子、または非置換のC1〜4アルキル基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくは非置換のC1〜4アルキル基である)を表し;
・環Dが、非縮合の5〜6員のヘテロシクリル基を表す、
請求項1〜6のいずれか1項に記載の化合物。
【請求項8】
・L1が、C1〜4アルキレンを表し、該アルキレンが、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択され;
・A1が、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2が、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3が、非置換のC1〜4アルキレン基を表し;
・A2が、非縮合のフェニルを表し、該フェニルが、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Hetが、-O-、-NH-または-S-を表し;
・Alk1が、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、非置換のC1〜3アルキレン基を表す]を表し;
・Rが、式(X1)または(Y1)の基:
【化4】

{式中、
・R2は、-COOHまたは-COOR9[式中、R9は、C1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表すか、またはR9は、フェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基またはモルホリノエチル基を表し、前記R9は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表し;
・環Dは、非縮合の非置換の5〜6員のヘテロシクリル基を表す}
を表す、
請求項1〜7のいずれか1項に記載の化合物。
【請求項9】
・L1が、非置換のC1〜4アルキレンを表す、
請求項8に記載の化合物。
【請求項10】
・A1が、1,4-フェニレン基または1,3-フェニレン基を表し、該1,4-フェニレン基または1,3-フェニレン基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項8または9に記載の化合物。
【請求項11】
・xが、0であり;
・L2が、基-Alk2-を表し;
・Alk1が、結合を表す、
請求項8〜10のいずれか1項に記載の化合物。
【請求項12】
Rが、式(X1)の基を表す、請求項8〜11のいずれか1項に記載の化合物。
【請求項13】
・R2が、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表す、
請求項8〜12のいずれか1項に記載の化合物。
【請求項14】
(a)式(IC)もしくは(ID):
【化5】

[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、請求項1〜13のいずれか1項に記載の化合物。
【請求項15】
R8が、水素原子を表す、請求項14に記載の化合物であって、式(IC’)または(ID’):
【化6】

を有する、化合物。
【請求項16】
・A1が、1,3-フェニレンを表し、該1,3-フェニレンが、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・R7およびR8が、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す、
請求項14に記載の化合物。
【請求項17】
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
から選択される、
請求項1〜16のいずれか1項に記載の化合物。
【請求項18】
ヒトまたは動物の身体の治療方法に使用するための、請求項1〜17のいずれか1項に記載の化合物。
【請求項19】
請求項1〜17のいずれか1項に記載の化合物および薬学的に許容される担体または希釈剤を含む、医薬組成物。
【請求項20】
IKK酵素によって媒介される障害の治療に使用するための、請求項1〜17のいずれか1項に記載の化合物であって、IKK酵素が好ましくはIKK-βである、化合物。
【請求項21】
前記障害が、腫瘍性/増殖性疾患、免疫疾患および炎症性疾患から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項22】
前記障害が癌である、請求項20に記載の障害の治療に使用するための化合物。
【請求項23】
前記障害が、腸癌;卵巣癌;頭頸部扁平上皮癌もしくは子宮頸部扁平上皮癌;胃癌もしくは肺癌;退形成乏突起膠腫;多形神経膠芽腫;または髄芽細胞腫から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項24】
前記障害が、関節リウマチ、乾癬、炎症性腸疾患、クローン病、潰瘍性大腸炎、慢性閉塞性肺疾患、喘息、多発性硬化症、糖尿病、アトピー性皮膚炎、移植片対宿主病、全身性エリテマトーデス、II型糖尿病またはアルツハイマー病から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項25】
患者におけるIKKによって媒介される障害の治療方法または予防方法であって、有効量の請求項1〜17のいずれか1項に記載の化合物を患者に投与することを含む、方法。
【請求項26】
IKK酵素によって媒介される障害の治療または予防に使用するための医薬の製造における、請求項1〜17のいずれか1項に記載の化合物の使用であって、IKK酵素が好ましくはIKK-βである、使用。
【請求項1】
(a)式(IA)もしくは(IB):
【化1】

〔式中、
・L1は、C1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表すか、またはL1は、基-(CH2)m(C=O)NR1(CH2)n-、-(CH2)mNR1(C=O)(CH2)n-、-(CH2)mO(CH2)n-、-(CH2)mS(CH2)n-、-(CH2)m(C=O)(CH2)n-もしくは-(CH2)mNR1(CH2)n-(式中、R1は、C1〜4アルキルであり、mおよびnは、同一であるか、もしくは異なっており、0、1、2、3もしくは4である)を表し;
・環A1は、さらなるC6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基に縮合していてもよい、C6〜10アリール基、5〜10員のヘテロアリール基、C3〜7カルボシクリル基または5〜10員のヘテロシクリル基であり;
・Wは、式:
【化2】

{式中、
・L2は、基-Alk2-、-Alk2-A2-または-Alk2-Alk3-を表し;
・Alk2は、結合、またはC1〜4アルキレン基、C2〜4アルケニレン基もしくはC2〜4アルキニレン基を表し;
・Alk3は、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し;
・A2は、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基または5〜6員のヘテロアリール基を表し;
・Hetは、-O-、-S-または-NR’-(式中、R’は、水素もしくは非置換C1〜2アルキルを表す)を表し;
・xは、0または1であり;
・Alk1は、結合、またはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基、または基-A3-Alk4-(式中、A3は、縮合していないか、もしくはさらなるフェニル基もしくは5〜6員のヘテロアリール基に縮合している、フェニル基もしくは5〜6員のヘテロアリール基を表し、Alk4は、結合、もしくはC1〜6アルキレン基、C2〜6アルケニレン基もしくはC2〜6アルキニレン基を表す)を表し;
・Rは、式(X1)、(X2)、(Y1)または(Y2):
【化3】

[式中、
・R2は、基-COOH、または1種以上の細胞内カルボキシルエステラーゼ酵素によって-COOH基に加水分解され得るエステル基であり;
・R3は、水素原子またはC1〜4アルキル基を表し;
・R4、R7およびR8は、同一であるか、または異なっており、それぞれ天然α-アミノ酸または非天然α-アミノ酸のα-置換基を表すか、あるいはR7およびR8は、これらが結合する炭素と一緒になって、3〜6員の飽和スピロシクロアルキル環またはヘテロシクリル環を形成し;
・R5は、水素原子、またはC1〜6アルキル基、C3〜7カルボシクリル基、C6〜10アリール基もしくは5〜6員のヘテロアリール基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくはC1〜6アルキル基である)を表し;
・環Dは、5〜6員のヘテロシクリル基であり、ここでR2は、示された環窒素に隣接する環炭素に結合しており;R7は、存在する場合、R2と同じ環炭素に結合しており;環Dは、フェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合していてもよい]
の基を表す(ただし、Rが式(Y2)の基を表し、かつ環Dがフェニル基、5〜6員のヘテロアリール基、C3〜7カルボシクリル基または5〜6員のヘテロシクリル基を含む第二の環に縮合している場合、波線によって横切られた示された結合は、環Dまたは前記第二の環の環原子からのものであってもよい)}
の基を表し;
式中、別段記載しない限り、
・R1、R2、R3、R4、R5、R6、R7、R8、L1、Alk1、Alk2、Alk3およびAlk4における、任意のアルキル基およびアルキル部分、アルケニル基およびアルケニル部分ならびにアルキニル基およびアルキニル部分は、同一であるか、または異なっており、それぞれ置換されていないか、または1個、2個もしくは3個の非置換置換基で置換されており、該非置換置換基は、同一であるか、または異なっており、ハロゲン原子ならびにC1〜4アルキル基、C2〜4アルケニル基、C1〜4アルコキシ基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、-SR’基、シアノ基、ニトロ基、C1〜4ヒドロキシアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換C1〜2アルキルを表す)から選択され;
・A1、A2、A3、DおよびR5における、任意のアリール基およびアリール部分、ヘテロアリール基およびヘテロアリール部分、カルボシクリル基およびカルボシクリル部分ならびにヘテロシクリル基およびヘテロシクリル部分は、同一であるか、または異なっており、それぞれ置換されていないか、またはハロゲン原子ならびにシアノ基、ニトロ基、C1〜4アルキル基、C1〜4アルコキシ基、C2〜4アルケニル基、C2〜4アルケニルオキシ基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基、C2〜4ハロアルケニルオキシ基、ヒドロキシル基、C1〜4ヒドロキシアルキル基、-SR’基および-NR’R’’基(式中、R’およびR’’は、それぞれ、同一であるか、もしくは異なっており、水素もしくは非置換C1〜4アルキルを表す)から選択される1個、2個、3個もしくは4個の非置換置換基によって、もしくは式-COOH、-COORA、-CORA、-SO2RA、-CONH2、-SO2NH2、-CONHRA、-SO2NHRA、-CONRARB、-SO2NRARB、-OCONH2、-OCONHRA、-OCONRARB、-NHCORA、-NRBCORA、-NHCOORA、-NRBCOORA、-NRBCOOH、-NHCOOH、-NHSO2RA、-NRBSO2RA、-NHSO2ORA、-NRBSO2OH、-NHSO2H、-NRBSO2ORA、-NHCONH2、-NRACONH2、-NHCONHRB、-NRACONHRB、-NHCONRARBもしくは-NRACONRARB(式中、RAおよびRBは、同一であるか、もしくは異なっており、非置換C1〜6アルキル、C3〜6シクロアルキル、非縮合フェニル、もしくは非縮合の5〜6員のヘテロアリールを表すか、もしくはRAおよびRBは、同一の窒素原子に結合している場合、非縮合の5員もしくは6員のヘテロシクリル基を形成する)の置換基から選択される1個、2個、3個もしくは4個の非置換置換基によって、置換されている〕
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、化合物。
【請求項2】
・R4、R7およびR8が、同一であるか、または異なっており、それぞれ異なるものを示し、それぞれ、
(i)水素原子;
(ii)C1〜6アルキル基;
(iii)基-L3-B(式中、L3は、結合もしくはC1〜6アルキレン基を表し、Bは、C6〜10アリール基もしくは5〜10員のヘテロアリール基を表す);または
(iv)インドール-3-イルメチル、-CH2COOH、-CH2CH2COOH、-CH2CONH2、-CH2CH2CONH2、-CH2CH2CH2NHC(NH)NH2、シクロヘキシル、シクロヘキシルメチルおよび1-ベンジルチオ-1-メチルエチルから選択される基
を表し(represents different and each represents represents)、
・前記(ii)におけるC1〜6アルキル基が、置換されていないか、または1個もしくは2個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)を表し;
・前記(iii)におけるC1〜6アルキレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・前記(iii)におけるC6〜10アリール基または5〜10員のヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1に記載の化合物。
【請求項3】
・L1が、-O-、-S-、-NR1-またはC1〜4アルキレン[式中、R1は、非置換のC1〜4アルキルを表し、C1〜4アルキレン部分は、置換されていないか、もしくは1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、もしくは異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される]を表す、
請求項1または2に記載の化合物。
【請求項4】
・L1が、-O-またはC1〜4アルキレン[式中、C1〜4アルキレン部分は、置換されていないか、もしくは1個もしくは2個の非置換の置換基で置換されており、該置換基は、同一であるか、もしくは異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される]を表す、
請求項1〜3のいずれか1項に記載の化合物。
【請求項5】
・A1が、フェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、縮合していないか、またはさらなるフェニル基もしくは5〜6員のヘテロシクリル基に縮合しており、前記A1基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1〜4のいずれか1項に記載の化合物。
【請求項6】
・Alk2が、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk3が、C1〜4アルキレン基、C2〜4アルケニレン基またはC2〜4アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基が、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・A2が、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項1〜5のいずれか1項に記載の化合物。
【請求項7】
・Hetが、-O-、-NR’または-S-(式中、R’は、水素もしくは非置換のメチルを表す)を表し;
・Alk1が、結合、またはC1〜6アルキレン基を表し、該アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C2〜4ハロアルケニル基、C1〜4ハロアルコキシ基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個、2個もしくは3個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、結合、またはC1〜3アルキレン基、C2〜3アルケニレン基もしくはC2〜3アルキニレン基を表し、該アルキレン基、アルケニレン基またはアルキニレン基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3が、水素原子または非置換のC1〜2アルキル基を表し;
・R4、R7およびR8が、同一であるか、または異なっており、水素原子;C1〜6アルキル基[該アルキル基は、置換されていないか、または1個もしくは2個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン、C1〜2アルコキシ、C1〜2ハロアルキル、ヒドロキシル、-COOR’、-COONR’R’’、-SR’および-NR’R’’(式中、R’およびR’’は、同一であるか、または異なっており、水素またはC1〜2アルキルを表す)を表す];または式-L3-Bの基(式中、L3は、結合または非置換のC1〜4アルキレン基であり、Bは、フェニル基または5〜10員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、C1〜4アルキル、C1〜2アルコキシ、C1〜2アルキルチオおよびヒドロキシを表す)を表し;
・R5が、水素原子、または非置換のC1〜4アルキル基、または式-(C=O)R6、-(C=O)OR6もしくは-(C=O)NR6の基(式中、R6は、水素原子もしくは非置換のC1〜4アルキル基である)を表し;
・環Dが、非縮合の5〜6員のヘテロシクリル基を表す、
請求項1〜6のいずれか1項に記載の化合物。
【請求項8】
・L1が、C1〜4アルキレンを表し、該アルキレンが、置換されていないか、または1個もしくは2個の非置換の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基およびC1〜2ハロアルキル基から選択され;
・A1が、非縮合のフェニル基または5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基、C1〜4ハロアルキル基、C1〜4ハロアルコキシ基、C1〜4ヒドロキシアルキル基、シアノ基、ニトロ基、-SR’基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2が、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・Alk3が、非置換のC1〜4アルキレン基を表し;
・A2が、非縮合のフェニルを表し、該フェニルが、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Hetが、-O-、-NH-または-S-を表し;
・Alk1が、結合またはC1〜4アルキレン基を表し、該C1〜4アルキレン基が、置換されていないか、またはハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、もしくは異なっており、水素もしくは非置換のC1〜2アルキルを表す)から選択される1個もしくは2個の非置換の置換基で置換されているか、あるいはAlk1が、基-A3-Alk4-[式中、A3は、非縮合のフェニル基または非縮合の5〜6員のヘテロアリール基を表し、該フェニル基またはヘテロアリール基は、置換されていないか、または1個、2個もしくは3個の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され、Alk4は、非置換のC1〜3アルキレン基を表す]を表し;
・Rが、式(X1)または(Y1)の基:
【化4】

{式中、
・R2は、-COOHまたは-COOR9[式中、R9は、C1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表すか、またはR9は、フェニル基、ベンジル基、2-ピリジルメチル基、3-ピリジルメチル基、4-ピリジルメチル基、N-メチルピペリジン-4-イル基、テトラヒドロフラン-3-イル基、メトキシエチル基、インダニル基、ノルボルニル(norbonyl)基、ジメチルアミノエチル基またはモルホリノエチル基を表し、前記R9は、置換されていないか、または1個、2個もしくは3個の非置換の置換基で置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびにC1〜2アルコキシ基、ヒドロキシル基、C1〜2ハロアルキル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される]を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表し;
・環Dは、非縮合の非置換の5〜6員のヘテロシクリル基を表す}
を表す、
請求項1〜7のいずれか1項に記載の化合物。
【請求項9】
・L1が、非置換のC1〜4アルキレンを表す、
請求項8に記載の化合物。
【請求項10】
・A1が、1,4-フェニレン基または1,3-フェニレン基を表し、該1,4-フェニレン基または1,3-フェニレン基が、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択される、
請求項8または9に記載の化合物。
【請求項11】
・xが、0であり;
・L2が、基-Alk2-を表し;
・Alk1が、結合を表す、
請求項8〜10のいずれか1項に記載の化合物。
【請求項12】
Rが、式(X1)の基を表す、請求項8〜11のいずれか1項に記載の化合物。
【請求項13】
・R2が、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表す、
請求項8〜12のいずれか1項に記載の化合物。
【請求項14】
(a)式(IC)もしくは(ID):
【化5】

[式中、
・L1は、非置換のC1〜4アルキレンを表し;
・A1は、1,4-フェニレンまたは1,3-フェニレンを表し、該1,4-フェニレンまたは1,3-フェニレンは、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基は、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・Alk2は、非置換のC1〜3アルキレン基、C2〜3アルケニレン基またはC2〜3アルキニレン基を表し;
・R2は、-COOR9(式中、R9は、非置換のC1〜4アルキル基、C3〜7カルボシクリル基またはC2〜4アルケニル基を表す)を表し;
・R3は、水素原子または非置換のメチル基を表し;
・R7およびR8は、同一であるか、または異なっており、水素原子または非置換のC1〜6アルキル基を表す]
のチオフェンカルボキサミド誘導体もしくはその互変異性体;または(b)その薬学的に許容される塩、N-オキシド、水和物もしくは溶媒和物である、請求項1〜13のいずれか1項に記載の化合物。
【請求項15】
R8が、水素原子を表す、請求項14に記載の化合物であって、式(IC’)または(ID’):
【化6】

を有する、化合物。
【請求項16】
・A1が、1,3-フェニレンを表し、該1,3-フェニレンが、置換されていないか、または1個、2個もしくは3個の置換基によって置換されており、該置換基が、同一であるか、または異なっており、ハロゲン原子、ならびに非置換のC1〜4アルキル基、C1〜4アルコキシ基、ヒドロキシル基および-NR’R’’基(式中、R’およびR’’は、同一であるか、または異なっており、水素または非置換のC1〜2アルキルを表す)から選択され;
・R7およびR8が、同一であるか、または異なっており、非置換のC1〜6アルキル基を表す、
請求項14に記載の化合物。
【請求項17】
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)メチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル;
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸シクロペンチル;および
・2-(4-((4-カルバモイル-5-ウレイドチオフェン-2-イル)エチル)ベンジルアミノ)-4-メチルペンタン酸tert-ブチル
から選択される、
請求項1〜16のいずれか1項に記載の化合物。
【請求項18】
ヒトまたは動物の身体の治療方法に使用するための、請求項1〜17のいずれか1項に記載の化合物。
【請求項19】
請求項1〜17のいずれか1項に記載の化合物および薬学的に許容される担体または希釈剤を含む、医薬組成物。
【請求項20】
IKK酵素によって媒介される障害の治療に使用するための、請求項1〜17のいずれか1項に記載の化合物であって、IKK酵素が好ましくはIKK-βである、化合物。
【請求項21】
前記障害が、腫瘍性/増殖性疾患、免疫疾患および炎症性疾患から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項22】
前記障害が癌である、請求項20に記載の障害の治療に使用するための化合物。
【請求項23】
前記障害が、腸癌;卵巣癌;頭頸部扁平上皮癌もしくは子宮頸部扁平上皮癌;胃癌もしくは肺癌;退形成乏突起膠腫;多形神経膠芽腫;または髄芽細胞腫から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項24】
前記障害が、関節リウマチ、乾癬、炎症性腸疾患、クローン病、潰瘍性大腸炎、慢性閉塞性肺疾患、喘息、多発性硬化症、糖尿病、アトピー性皮膚炎、移植片対宿主病、全身性エリテマトーデス、II型糖尿病またはアルツハイマー病から選択される、請求項20に記載の障害の治療に使用するための化合物。
【請求項25】
患者におけるIKKによって媒介される障害の治療方法または予防方法であって、有効量の請求項1〜17のいずれか1項に記載の化合物を患者に投与することを含む、方法。
【請求項26】
IKK酵素によって媒介される障害の治療または予防に使用するための医薬の製造における、請求項1〜17のいずれか1項に記載の化合物の使用であって、IKK酵素が好ましくはIKK-βである、使用。
【公表番号】特表2012−524767(P2012−524767A)
【公表日】平成24年10月18日(2012.10.18)
【国際特許分類】
【出願番号】特願2012−506561(P2012−506561)
【出願日】平成22年4月20日(2010.4.20)
【国際出願番号】PCT/GB2010/000790
【国際公開番号】WO2010/122294
【国際公開日】平成22年10月28日(2010.10.28)
【出願人】(507288718)クロマ セラピューティクス リミテッド (18)
【氏名又は名称原語表記】CHROMA THERAPEUTICS LTD
【住所又は居所原語表記】93 Milton Park,Abingdon,Oxfordshire OX14 4RY,UNITED KINGDOM
【Fターム(参考)】
【公表日】平成24年10月18日(2012.10.18)
【国際特許分類】
【出願日】平成22年4月20日(2010.4.20)
【国際出願番号】PCT/GB2010/000790
【国際公開番号】WO2010/122294
【国際公開日】平成22年10月28日(2010.10.28)
【出願人】(507288718)クロマ セラピューティクス リミテッド (18)
【氏名又は名称原語表記】CHROMA THERAPEUTICS LTD
【住所又は居所原語表記】93 Milton Park,Abingdon,Oxfordshire OX14 4RY,UNITED KINGDOM
【Fターム(参考)】
[ Back to top ]

