RANKL抗体−PTH/PTHrPキメラ分子
【課題】NF−κB受容体アクチベーターリガンド(RANKL)抗体−副甲状腺ホルモン/副甲状腺ホルモン関連蛋白(PTH/PTHrP)キメラ分子を提供する。
【解決手段】RANKL抗体−PTH/PTHrPキメラ分子はRANKLと結合する抗体と、PTH/PTHrPペプチドを含む。抗体は1個以上のヒト相補性決定領域(CDR)と、ヒト以外の種に由来する1個以上のフレームワーク領域及び/又は定常領域を含む。骨疾患の治療用組成物及び方法についても記載する。
【解決手段】RANKL抗体−PTH/PTHrPキメラ分子はRANKLと結合する抗体と、PTH/PTHrPペプチドを含む。抗体は1個以上のヒト相補性決定領域(CDR)と、ヒト以外の種に由来する1個以上のフレームワーク領域及び/又は定常領域を含む。骨疾患の治療用組成物及び方法についても記載する。
Notice: Undefined index: DEJ in /mnt/www/gzt_disp.php on line 298
【特許請求の範囲】
【請求項1】
(a)RANKLと結合する抗体;及び
(b)PTH/PTHrPペプチドを含み;
PTH/PTHrPペプチドが前記抗体と機能的に連結しているNF−κB受容体アクチベーターリガンド(RANKL)抗体−副甲状腺ホルモン/副甲状腺ホルモン関連蛋白(PTH/PTHrP)キメラ分子。
【請求項2】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項3】
PTH/PTHrPペプチドが重鎖と機能的に連結している請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項4】
PTH/PTHrPペプチドが軽鎖と機能的に連結している請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項5】
PTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項3のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項6】
PTH/PTHrPペプチドが軽鎖のN末端と機能的に連結している請求項4のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項7】
PTH/PTHrPペプチドが重鎖のN末端と融合している請求項5のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項8】
PTH/PTHrPペプチドが軽鎖のN末端と融合している請求項6のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項9】
抗体が配列番号2に記載のアミノ酸配列又はそのフラグメントをもつ重鎖を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項10】
抗体が配列番号4に記載のアミノ酸配列又はそのフラグメントをもつ軽鎖を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項11】
抗体が重鎖と軽鎖を含み、ならびに重鎖が配列番号2に記載のアミノ酸配列又はそのフラグメントを含み、及び軽鎖が配列番号4に記載のアミノ酸配列又はそのフラグメントを含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項12】
抗体が単鎖Fv抗体(scFv)、Fab抗体、Fab’抗体、(Fab’)2抗体、ドメイン抗体、ナノボディ、ミニボディ、マキシボディ及び二重特異性抗体から選択される請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項13】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号2に記載のアミノ酸配列又はそのフラグメントを含み、及び軽鎖が配列番号4に記載のアミノ酸配列又はそのフラグメントを含み、ならびにRANKLと結合する、抗体;
(b)第1のPTH/PTHrPペプチド;及び
(c)第2のPTH/PTHrPペプチド;
を含み、第1のPTH/PTHrPペプチドが軽鎖と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖と機能的に連結しており、ならびに第1のPTH/PTHrPペプチドと第2のPTH/PTHrPペプチドが同一又は異なるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項14】
第1のPTH/PTHrPペプチドが軽鎖のN末端と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項13のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項15】
第1のPTH/PTHrPペプチドが軽鎖のN末端と融合しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と融合している請求項13のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項16】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号11に記載のアミノ酸配列又はそのフラグメントを含む第1の可変領域を含み、及び軽鎖が配列番号12に記載のアミノ酸配列又はそのフラグメントを含む第2の可変領域を含み、ならびにRANKLと結合する抗体;及び
(b)PTH/PTHrPペプチドを含み;
PTH/PTHrPペプチドが重鎖又は軽鎖と機能的に連結しているRANKL抗体−PTH/PTHrPキメラ分子。
【請求項17】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項18】
PTH/PTHrPペプチドが重鎖と機能的に連結している請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項19】
PTH/PTHrPペプチドが軽鎖と機能的に連結している請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項20】
PTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項18のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項21】
PTH/PTHrPペプチドが軽鎖のN末端と機能的に連結している請求項19のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項22】
PTH/PTHrPペプチドが重鎖のN末端と融合している請求項20のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項23】
PTH/PTHrPペプチドが軽鎖のN末端と融合している請求項21のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項24】
重鎖と軽鎖がフレキシブルリンカーにより結合され、単鎖抗体を形成する請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項25】
単鎖抗体が単鎖Fv抗体である請求項24のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項26】
抗体がFab抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項27】
抗体がFab’抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項28】
抗体が(Fab’)2抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項29】
抗体が完全ヒト型である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項30】
RANKL抗体−PTH/PTHrPキメラ分子がRANKLとNF−κB受容体アクチベーター(RANK)の結合を阻害する請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項31】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号11に記載のアミノ酸配列又はそのフラグメントを含む可変領域を含み、及び軽鎖が配列番号12に記載のアミノ酸配列又はそのフラグメントを含む可変領域を含み、ならびにRANKLと結合する、抗体;
(b)第1のPTH/PTHrPペプチド;及び
(c)第2のPTH/PTHrPペプチド;
を含み、第1のPTH/PTHrPペプチドが軽鎖と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖と機能的に連結しており、ならびに第1のPTH/PTHrPペプチドと第2のPTH/PTHrPペプチドが同一又は異なるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項32】
第1のPTH/PTHrPペプチドが軽鎖のN末端と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項31のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項33】
第1のPTH/PTHrPペプチドが軽鎖のN末端と融合しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と融合している請求項32のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項34】
(a)重鎖と軽鎖を含む抗体であって、
(i)重鎖が第1の可変領域を含み、第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも92%の一致度をもつ配列を含み、及び
(ii)軽鎖が第2の可変領域を含み、第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも90%の一致度をもつ配列を含み、
NF−κB受容体アクチベーターリガンド(RANKL)と相互作用する、抗体;ならびに
(b)PTH/PTHrPペプチド;
を含み、PTH/PTHrPペプチドが重鎖又は軽鎖と機能的に連結しているRANKL抗体−PTH/PTHrPキメラ分子。
【請求項35】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項36】
第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも95%の一致度をもつ配列を含み、及び第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも95%の一致度をもつ配列を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項37】
第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも99%の一致度をもつ配列を含み、及び第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも99%の一致度をもつ配列を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項38】
PTH/PTHrPペプチドが式I:
XNHX10X11X12KX14X15X16X17X18X19RX21X22X23X24X25X26X27X28XC(式I;配列番号13)
(式中、
XNは不在であるか又はX3X4X5X6X7、X2X3X4X5X6X7、X1X2X3X4X5X6X7もしくはYX1X2X3X4X5X6X7であり;
X1からX7、X10、X11、X12、X14からX28は各々独立して選択されたアミノ酸残基であり;
XCは不在であるか又はX29、X29X30、X29X30X31、X29X30X31X32、X29X30X31X32X33、X29X30X31X32X33X34、X29X30X31X32X33X34X35もしくはX29X30X31X32X33X34X35X36であり;
X29からX36は各々独立して選択されたアミノ酸残基であり;
但し、X14からX36の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;及び
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項39】
XNがX1X2X3X4X5X6X7であり;
X1が親水性又は非機能的残基であり;
X2がVであり;
X3がSであり;
X4がEであり;
X5が非機能的又は塩基性残基であり;
X6がQであり;
X7がLであり;
X10が酸性又は親水性残基であり;
X11が非機能的又は塩基性残基であり;
X12が非機能的残基であり;
X14が塩基性又は親水性残基であり;
X15が非機能的残基であり;
X16が非機能的又は親水性残基であり;
X17が酸性、親水性又は非機能的残基であり;
X18が非機能的残基であり;
X19が酸性又は塩基性残基であり;
X21が非機能的又は塩基性残基であり;
X22が親水性、酸性又は芳香族残基であり;
X23が芳香族又は親油性残基であり;
X24が親油性残基であり;
X25が親水性又は塩基性残基であり;
X26が親水性又は塩基性残基であり;
X27が親油性、塩基性又は非機能的残基であり;及び
X28が親油性又は非機能的残基である
請求項38のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項40】
XCがX29X30X31X32X33X34であり;
X29が親水性又は非機能的残基であり;
X30が親水性又は酸性残基であり;
X31が親油性又は非機能的残基であり;
X32がHであり;
X33がシステイン又は親水性残基であり;及び
X34が非機能的又は芳香族残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項41】
XCがX29X30X31であり;
X29が親水性又は非機能的残基であり;
X30が親水性又は酸性残基であり;及び
X31が親油性又は非機能的残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項42】
XCがX29X30であり;
X29が親水性又は非機能的残基であり;及び
X30が親水性又は酸性残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項43】
XCがX29であり;及び
X29が親水性又は非機能的残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項44】
X27及びX33の少なくとも一方がシステインである請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項45】
XCが不在である請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項46】
X1がA、S又はYであり;
X5がH又はIであり;
X10がN又はDであり;
X11がL、R又はKであり;
X12がG、F又はWであり;
X14がH又はSであり;
X15がL又はIであり;
X16がQ、N、S又はAであり;
X17がS、D又はLであり;
X18がM、L、V又はNleであり;
X19がE又はRであり;
X21がV、M、R又はNleであり;
X22がE又はFであり;
X23がW又はFであり;
X25がR又はHであり;
X26がK又はHであり;
X27がCであり;及び
X28がL又はIである
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項47】
XCがX29X30X31X32X33X34であり;
X29がQ又はAであり;
X30がD又はEであり;
X31がV又はIであり;
X33がCであり;
X34がN又はTであり;及び
X35がA、F又はYである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項48】
XCがX29X30X31であり;
X29がQ又はAであり;
X30がD又はEであり;及び
X31がV又はIである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項49】
XCがX29X30であり;
X29がQ又はAであり;及び
X30がD又はEである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項50】
XCがX29であり;及び
X29がQ又はAである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項51】
XCが不在である請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項52】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項38のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項53】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項52のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項54】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項53のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項55】
PTH/PTHrPペプチドが式II:
JNJ7J8HNJ11J12KHLJ16SJ18J19RJ21EWLRKKLJC(式II;配列番号14)
(式中、
JNは不在であるか又はJ1J2J3J4J5J6、J2J3J4J5J6もしくはJ3J4J5J6であり;
J1からJ8、J12、J16、J18及びJ21は各々独立して選択されたアミノ酸残基であり;
J11は非機能的又は塩基性残基であり;
J19は酸性又は塩基性残基であり;
JCは不在であるか又はJ29、J29J30、J29J30J31、J29J30J31J32、J29J30J31J32J33もしくはJ29J30J31J32J33J34であり;
J29からJ34は各々独立して選択されたアミノ酸残基であり;
但し、PTH/PTHrP調節領域のJ14からC末端残基の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項56】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30J31J32J33J34であり;
J29が親水性又は非機能的残基であり;
J30が親水性又は酸性残基であり;
J31が親油性又は非機能的残基であり;
J32が塩基性残基であり;
J33が酸性残基であり;及び
J34が芳香族残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項57】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;
J30がD又はEであり;
J31がV又はIであり;
J31がHであり;
J33がNであり;及び
J34がF又はYである
請求項56のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項58】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30J31であり;
J29が親水性又は非機能的残基であり;
J30が親水性又は酸性残基であり;及び
J31が親油性又は非機能的残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項59】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18かM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;
J30がD又はEであり;及び
J31がV又はIである
請求項58のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項60】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30であり;
J29が親水性又は非機能的残基であり;及び
J30が親水性又は酸性残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項61】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;及び
J30がD又はEである
請求項60のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項62】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29であり;及び
J29が親水性又は非機能的残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項63】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;及び
J29がQ又はAである
請求項62のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項64】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;及び
JCが不在である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項65】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;及び
J21がV、M又はNleである
請求項64のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項66】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項67】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項66のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項68】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項67のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項69】
PTH/PTHrPペプチドが式III:
ONLHO10O11O12KSIO15O16O17LRRRFO23LHHLIOC(式III;配列番号15)
(式中、
ONは不在であるか又はYO1O2O3O4O5O6O7、O1O2O3O4O5O6O7、O2O3O4O5O6O7、O3O4O5O6O7、O4O5O6O7、O5O6O7、O6O7もしくはO7であり;
O1からO7、O10からO12、O15からO17及びO23は各々独立して選択されたアミノ酸残基であり;
OCは不在であるか又はO29、O29O30、O29O30O31、O29O30O31O32、O29O30O31O32O33、O29O30O31O32O33O34、O29O30O31O32O33O34O35もしくはO29O30O31O32O33O34O35O36であり;
O29からO36は各々独立してアミノ酸残基であり;
但し、PTH/PTHrP調節領域のO14からC末端残基の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;ならびに
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項70】
ONがO7であり;
O7が非機能的残基であり;
O10が酸性又は親水性残基であり;
O11が塩基性又は非機能的残基であり;
O12が芳香族又は非機能的残基であり;
O15が親水性又は非機能的残基であり;
O16が親水性残基であり;
O17が酸性又は非機能的残基であり;
O23が芳香族残基であり;及び
OCが不在である
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項71】
ONがO1O2O3O4O5O6O7であり;
O1が非機能的アミノ酸残基であり;
O2が非機能的アミノ酸残基であり;
O3が親水性アミノ酸残基であり;
O4が酸性アミノ酸残基であり;
O5が塩基性又は非機能的アミノ酸残基であり;
O6が親水性アミノ酸残基であり;
O7が非機能的残基であり;
O10が酸性又は親水性残基であり;
O11が塩基性又は非機能的残基であり;
O12が芳香族又は非機能的残基であり;
O15が親水性又は非機能的残基であり;
O16が親水性残基であり;
O17が酸性又は非機能的残基であり;及び
O23が芳香族残基である
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項72】
O1がAであり;
O2がVであり;
O3がSであり;
O4がEであり;
O5がH又はIであり;
O6がQであり;
O7がLであり;
O10がN又はDであり;
O11がK又はLであり;
O12がG、F又はWであり;
O15がI又はSであり;
O16がQ又はNであり;
O17がD又はLであり;及び
O23がF又はWである
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項73】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項74】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項73のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項75】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項74のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項76】
PTH/PTHrPペプチドが配列番号16から67から選択される配列を含むPTH/PTHrP調節領域を含む請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項77】
PTH/PTHrP調節領域が配列番号22のアミノ酸配列を含む請求項76のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項78】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項76のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項79】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項78のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項80】
プレプロ領域が配列番号188のアミノ酸配列を含み、及びPTH/PTHrP調節領域が配列番号22のアミノ酸配列を含む請求項79のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項81】
PTH/PTHrPペプチドが配列番号8のアミノ酸配列を含む請求項78のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項82】
(a)配列番号2のアミノ酸配列をもつ第1のポリペプチドと、配列番号8のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子;
(b)配列番号10のアミノ酸配列をもつ第1のポリペプチドと、配列番号4のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子;及び
(c)配列番号10のアミノ酸配列をもつ第1のポリペプチドと、配列番号8のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子
から選択されるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項83】
PTH/PTHrPペプチドが配列番号68から89から選択される配列を含むPTH/PTHrP調節領域を含む請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項84】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項83のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項85】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項84のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項86】
PTH/PTHrPペプチドが配列番号90から107から選択される配列を含むPTH/PTHrP調節領域を含み、但し、PTH/PTHrP調節領域の14位からC末端の1個以上の残基はシステイン残基で置換されている請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項87】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項86のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項88】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項87のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項89】
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子を含む医薬組成物。
【請求項90】
骨吸収抑制剤、骨同化剤、抗炎症剤、免疫抑制剤及び癌治療剤から選択される少なくとも1種の治療剤を更に含む請求項89の医薬組成物。
【請求項91】
少なくとも1種の治療剤がアナキンラ、エタネルセプト、インフリキシマブ、アダリムマブ及びメトトレキセートから選択される請求項90の医薬組成物。
【請求項92】
更に少なくとも1種の癌治療剤を含有する請求項89の医薬組成物。
【請求項93】
少なくとも1種の癌治療剤が放射線療法と化学療法から選択される請求項92の医薬組成物。
【請求項94】
少なくとも1種の癌治療剤が上皮成長因子受容体(EGFR)阻害剤、HER2阻害剤、vegF阻害剤、vegF受容体阻害剤、肝細胞増殖因子(HGF)/分散因子(SF)阻害剤、c−Met阻害剤、アンギオポエチン阻害剤、Tie2阻害剤、血小板由来増殖因子受容体(PDGFR)阻害剤、インスリン様成長因子受容体(IGFR)阻害剤、ムチン様糖蛋白阻害剤、CDC20阻害剤及びCDC33阻害剤から選択される請求項92の医薬組成物。
【請求項95】
更に少なくとも1種の治療用抗体を含有する請求項89の医薬組成物。
【請求項96】
少なくとも1種の治療用抗体がHer2抗体、CDC20抗体、EGFR抗体、vegF抗体、vegF受容体抗体、肝細胞増殖因子(HGF)/分散因子(SF)抗体、インスリン様成長因子受容体(IFGR)抗体及びCDC33抗体から選択される請求項95の医薬組成物。
【請求項97】
請求項89の医薬組成物を投与することを含む、患者における骨減少の治療方法。
【請求項98】
請求項89の医薬組成物と、骨吸収抑制剤、骨同化剤、抗炎症剤、免疫抑制剤及び癌治療剤から選択される少なくとも1種の薬剤を投与することを含む、患者における骨減少の治療方法。
【請求項99】
骨形態形成因子、トランスフォーミング増殖因子β(TGF−β)、インターロイキン−1(IL−1)阻害剤、IL−1ra、アナキンラ、TNFα阻害剤、可溶性TNFα受容体、エタネルセプト、抗TNFα抗体、インフリキシマブ、アダリムマブ、プロスタグランジン、ビスホスホネート、アレンドロネート、フッ化物、カルシウム、非ステロイド性抗炎症薬(NSAID)、COX−2阻害剤、セレコキシブ、ロフェコキシブ、免疫抑制剤、メトトレキセート、レフルノミド、セリンプロテアーゼ阻害剤、分泌型白血球プロテアーゼ阻害剤(SLPI)、IL−6阻害剤、IL−6抗体、IL−8阻害剤、IL−8抗体、IL−18阻害剤、IL−18結合蛋白、IL−18抗体、インターロイキン−1変換酵素(ICE)モジュレーター、線維芽細胞増殖因子(FGF)、FGFモジュレーター、PAFアンタゴニスト、ケラチノサイト増殖因子(KGF)、KGF関連分子、KGFモジュレーター、マトリックスメタロプロテイナーゼ(MMP)モジュレーター、一酸化窒素シンターゼ(NOS)モジュレーター、グルココルチコイド受容体のモジュレーター、グルタミン酸受容体のモジュレーター、リポ多糖(LPS)濃度のモジュレーター、ノルアドレナリン、ノルアドレナリンミメティック及びノルアドレナリンモジュレーターから選択される少なくとも1種の治療剤を投与することを更に含む請求項97の方法。
【請求項100】
請求項90の医薬組成物を投与することを含む、患者における骨減少を伴う炎症症状の治療方法。
【請求項101】
請求項90の医薬組成物を投与することを含む、患者における骨減少を伴う自己免疫症状の治療方法。
【請求項102】
請求項90の医薬組成物を投与することを含む、患者における関節リウマチの治療方法。
【請求項103】
請求項89の医薬組成物を投与することを含む、癌に伴う骨減少の治療方法。
【請求項104】
請求項89の医薬組成物と、上皮成長因子受容体(EGFR)阻害剤、HER2阻害剤、vegF阻害剤、vegF受容体阻害剤、肝細胞増殖因子(HGF)/分散因子(SF)阻害剤、c−Met阻害剤、アンギオポエチン阻害剤、Tie2阻害剤、血小板由来増殖因子受容体(PDGFR)阻害剤、インスリン様成長因子受容体(IGFR)阻害剤、ムチン様糖蛋白阻害剤、CDC20阻害剤及びCDC33阻害剤から選択される少なくとも1種の治療剤を投与することを含む、癌に伴う骨減少の治療方法。
【請求項105】
請求項89の医薬組成物と、Her2抗体、CDC20抗体、EGFR抗体、vegF抗体、vegF受容体抗体、肝細胞増殖因子(HGF)/分散因子(SF)抗体、インスリン様成長因子受容体(IFGR)抗体及びCDC33抗体から選択される少なくとも1種の抗体を投与することを含む、癌に伴う骨減少の治療方法。
【請求項1】
(a)RANKLと結合する抗体;及び
(b)PTH/PTHrPペプチドを含み;
PTH/PTHrPペプチドが前記抗体と機能的に連結しているNF−κB受容体アクチベーターリガンド(RANKL)抗体−副甲状腺ホルモン/副甲状腺ホルモン関連蛋白(PTH/PTHrP)キメラ分子。
【請求項2】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項3】
PTH/PTHrPペプチドが重鎖と機能的に連結している請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項4】
PTH/PTHrPペプチドが軽鎖と機能的に連結している請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項5】
PTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項3のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項6】
PTH/PTHrPペプチドが軽鎖のN末端と機能的に連結している請求項4のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項7】
PTH/PTHrPペプチドが重鎖のN末端と融合している請求項5のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項8】
PTH/PTHrPペプチドが軽鎖のN末端と融合している請求項6のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項9】
抗体が配列番号2に記載のアミノ酸配列又はそのフラグメントをもつ重鎖を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項10】
抗体が配列番号4に記載のアミノ酸配列又はそのフラグメントをもつ軽鎖を含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項11】
抗体が重鎖と軽鎖を含み、ならびに重鎖が配列番号2に記載のアミノ酸配列又はそのフラグメントを含み、及び軽鎖が配列番号4に記載のアミノ酸配列又はそのフラグメントを含む請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項12】
抗体が単鎖Fv抗体(scFv)、Fab抗体、Fab’抗体、(Fab’)2抗体、ドメイン抗体、ナノボディ、ミニボディ、マキシボディ及び二重特異性抗体から選択される請求項1のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項13】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号2に記載のアミノ酸配列又はそのフラグメントを含み、及び軽鎖が配列番号4に記載のアミノ酸配列又はそのフラグメントを含み、ならびにRANKLと結合する、抗体;
(b)第1のPTH/PTHrPペプチド;及び
(c)第2のPTH/PTHrPペプチド;
を含み、第1のPTH/PTHrPペプチドが軽鎖と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖と機能的に連結しており、ならびに第1のPTH/PTHrPペプチドと第2のPTH/PTHrPペプチドが同一又は異なるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項14】
第1のPTH/PTHrPペプチドが軽鎖のN末端と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項13のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項15】
第1のPTH/PTHrPペプチドが軽鎖のN末端と融合しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と融合している請求項13のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項16】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号11に記載のアミノ酸配列又はそのフラグメントを含む第1の可変領域を含み、及び軽鎖が配列番号12に記載のアミノ酸配列又はそのフラグメントを含む第2の可変領域を含み、ならびにRANKLと結合する抗体;及び
(b)PTH/PTHrPペプチドを含み;
PTH/PTHrPペプチドが重鎖又は軽鎖と機能的に連結しているRANKL抗体−PTH/PTHrPキメラ分子。
【請求項17】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項18】
PTH/PTHrPペプチドが重鎖と機能的に連結している請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項19】
PTH/PTHrPペプチドが軽鎖と機能的に連結している請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項20】
PTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項18のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項21】
PTH/PTHrPペプチドが軽鎖のN末端と機能的に連結している請求項19のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項22】
PTH/PTHrPペプチドが重鎖のN末端と融合している請求項20のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項23】
PTH/PTHrPペプチドが軽鎖のN末端と融合している請求項21のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項24】
重鎖と軽鎖がフレキシブルリンカーにより結合され、単鎖抗体を形成する請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項25】
単鎖抗体が単鎖Fv抗体である請求項24のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項26】
抗体がFab抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項27】
抗体がFab’抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項28】
抗体が(Fab’)2抗体である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項29】
抗体が完全ヒト型である請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項30】
RANKL抗体−PTH/PTHrPキメラ分子がRANKLとNF−κB受容体アクチベーター(RANK)の結合を阻害する請求項16のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項31】
(a)重鎖と軽鎖を含む抗体であって、重鎖が配列番号11に記載のアミノ酸配列又はそのフラグメントを含む可変領域を含み、及び軽鎖が配列番号12に記載のアミノ酸配列又はそのフラグメントを含む可変領域を含み、ならびにRANKLと結合する、抗体;
(b)第1のPTH/PTHrPペプチド;及び
(c)第2のPTH/PTHrPペプチド;
を含み、第1のPTH/PTHrPペプチドが軽鎖と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖と機能的に連結しており、ならびに第1のPTH/PTHrPペプチドと第2のPTH/PTHrPペプチドが同一又は異なるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項32】
第1のPTH/PTHrPペプチドが軽鎖のN末端と機能的に連結しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と機能的に連結している請求項31のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項33】
第1のPTH/PTHrPペプチドが軽鎖のN末端と融合しており、及び第2のPTH/PTHrPペプチドが重鎖のN末端と融合している請求項32のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項34】
(a)重鎖と軽鎖を含む抗体であって、
(i)重鎖が第1の可変領域を含み、第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも92%の一致度をもつ配列を含み、及び
(ii)軽鎖が第2の可変領域を含み、第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも90%の一致度をもつ配列を含み、
NF−κB受容体アクチベーターリガンド(RANKL)と相互作用する、抗体;ならびに
(b)PTH/PTHrPペプチド;
を含み、PTH/PTHrPペプチドが重鎖又は軽鎖と機能的に連結しているRANKL抗体−PTH/PTHrPキメラ分子。
【請求項35】
PTH/PTHrPペプチドがプレプロ領域とPTH/PTHrP調節領域を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項36】
第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも95%の一致度をもつ配列を含み、及び第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも95%の一致度をもつ配列を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項37】
第1の可変領域が配列番号11に記載のアミノ酸配列に対して少なくとも99%の一致度をもつ配列を含み、及び第2の可変領域が配列番号12に記載のアミノ酸配列に対して少なくとも99%の一致度をもつ配列を含む請求項34のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項38】
PTH/PTHrPペプチドが式I:
XNHX10X11X12KX14X15X16X17X18X19RX21X22X23X24X25X26X27X28XC(式I;配列番号13)
(式中、
XNは不在であるか又はX3X4X5X6X7、X2X3X4X5X6X7、X1X2X3X4X5X6X7もしくはYX1X2X3X4X5X6X7であり;
X1からX7、X10、X11、X12、X14からX28は各々独立して選択されたアミノ酸残基であり;
XCは不在であるか又はX29、X29X30、X29X30X31、X29X30X31X32、X29X30X31X32X33、X29X30X31X32X33X34、X29X30X31X32X33X34X35もしくはX29X30X31X32X33X34X35X36であり;
X29からX36は各々独立して選択されたアミノ酸残基であり;
但し、X14からX36の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;及び
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項39】
XNがX1X2X3X4X5X6X7であり;
X1が親水性又は非機能的残基であり;
X2がVであり;
X3がSであり;
X4がEであり;
X5が非機能的又は塩基性残基であり;
X6がQであり;
X7がLであり;
X10が酸性又は親水性残基であり;
X11が非機能的又は塩基性残基であり;
X12が非機能的残基であり;
X14が塩基性又は親水性残基であり;
X15が非機能的残基であり;
X16が非機能的又は親水性残基であり;
X17が酸性、親水性又は非機能的残基であり;
X18が非機能的残基であり;
X19が酸性又は塩基性残基であり;
X21が非機能的又は塩基性残基であり;
X22が親水性、酸性又は芳香族残基であり;
X23が芳香族又は親油性残基であり;
X24が親油性残基であり;
X25が親水性又は塩基性残基であり;
X26が親水性又は塩基性残基であり;
X27が親油性、塩基性又は非機能的残基であり;及び
X28が親油性又は非機能的残基である
請求項38のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項40】
XCがX29X30X31X32X33X34であり;
X29が親水性又は非機能的残基であり;
X30が親水性又は酸性残基であり;
X31が親油性又は非機能的残基であり;
X32がHであり;
X33がシステイン又は親水性残基であり;及び
X34が非機能的又は芳香族残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項41】
XCがX29X30X31であり;
X29が親水性又は非機能的残基であり;
X30が親水性又は酸性残基であり;及び
X31が親油性又は非機能的残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項42】
XCがX29X30であり;
X29が親水性又は非機能的残基であり;及び
X30が親水性又は酸性残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項43】
XCがX29であり;及び
X29が親水性又は非機能的残基である
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項44】
X27及びX33の少なくとも一方がシステインである請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項45】
XCが不在である請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項46】
X1がA、S又はYであり;
X5がH又はIであり;
X10がN又はDであり;
X11がL、R又はKであり;
X12がG、F又はWであり;
X14がH又はSであり;
X15がL又はIであり;
X16がQ、N、S又はAであり;
X17がS、D又はLであり;
X18がM、L、V又はNleであり;
X19がE又はRであり;
X21がV、M、R又はNleであり;
X22がE又はFであり;
X23がW又はFであり;
X25がR又はHであり;
X26がK又はHであり;
X27がCであり;及び
X28がL又はIである
請求項39のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項47】
XCがX29X30X31X32X33X34であり;
X29がQ又はAであり;
X30がD又はEであり;
X31がV又はIであり;
X33がCであり;
X34がN又はTであり;及び
X35がA、F又はYである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項48】
XCがX29X30X31であり;
X29がQ又はAであり;
X30がD又はEであり;及び
X31がV又はIである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項49】
XCがX29X30であり;
X29がQ又はAであり;及び
X30がD又はEである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項50】
XCがX29であり;及び
X29がQ又はAである
請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項51】
XCが不在である請求項46のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項52】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項38のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項53】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項52のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項54】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項53のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項55】
PTH/PTHrPペプチドが式II:
JNJ7J8HNJ11J12KHLJ16SJ18J19RJ21EWLRKKLJC(式II;配列番号14)
(式中、
JNは不在であるか又はJ1J2J3J4J5J6、J2J3J4J5J6もしくはJ3J4J5J6であり;
J1からJ8、J12、J16、J18及びJ21は各々独立して選択されたアミノ酸残基であり;
J11は非機能的又は塩基性残基であり;
J19は酸性又は塩基性残基であり;
JCは不在であるか又はJ29、J29J30、J29J30J31、J29J30J31J32、J29J30J31J32J33もしくはJ29J30J31J32J33J34であり;
J29からJ34は各々独立して選択されたアミノ酸残基であり;
但し、PTH/PTHrP調節領域のJ14からC末端残基の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項56】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30J31J32J33J34であり;
J29が親水性又は非機能的残基であり;
J30が親水性又は酸性残基であり;
J31が親油性又は非機能的残基であり;
J32が塩基性残基であり;
J33が酸性残基であり;及び
J34が芳香族残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項57】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;
J30がD又はEであり;
J31がV又はIであり;
J31がHであり;
J33がNであり;及び
J34がF又はYである
請求項56のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項58】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30J31であり;
J29が親水性又は非機能的残基であり;
J30が親水性又は酸性残基であり;及び
J31が親油性又は非機能的残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項59】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18かM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;
J30がD又はEであり;及び
J31がV又はIである
請求項58のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項60】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29J30であり;
J29が親水性又は非機能的残基であり;及び
J30が親水性又は酸性残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項61】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;
J29がQ又はAであり;及び
J30がD又はEである
請求項60のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項62】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;
JCがJ29であり;及び
J29が親水性又は非機能的残基である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項63】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;
J21がV、M又はNleであり;及び
J29がQ又はAである
請求項62のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項64】
JNがJ1J2J3J4J5J6であり;
J1が非機能的又は芳香族残基であり;
J2が非機能的残基であり;
J3が親水性残基であり;
J4が酸性残基であり;
J5が非機能的残基であり;
J6が塩基性残基であり;
J7が非機能的又は芳香族残基であり;
J8が非機能的残基であり;
J12が非機能的又は芳香族残基であり;
J16が非機能的又は親水性残基であり;
J18が非機能的残基であり;
J21が非機能的残基であり;及び
JCが不在である
請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項65】
J1がA、S又はYであり;
J2がVであり;
J3がSであり;
J4がEであり;
J5がIであり;
J6がQであり;
J7がL又はFであり;
J8がM又はNleであり;
J11がL、R又はKであり;
J12がG又はWであり;
J16がN、S又はAであり;
J18がM、Nle、L又はVであり;
J19がE又はRであり;及び
J21がV、M又はNleである
請求項64のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項66】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項55のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項67】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項66のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項68】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項67のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項69】
PTH/PTHrPペプチドが式III:
ONLHO10O11O12KSIO15O16O17LRRRFO23LHHLIOC(式III;配列番号15)
(式中、
ONは不在であるか又はYO1O2O3O4O5O6O7、O1O2O3O4O5O6O7、O2O3O4O5O6O7、O3O4O5O6O7、O4O5O6O7、O5O6O7、O6O7もしくはO7であり;
O1からO7、O10からO12、O15からO17及びO23は各々独立して選択されたアミノ酸残基であり;
OCは不在であるか又はO29、O29O30、O29O30O31、O29O30O31O32、O29O30O31O32O33、O29O30O31O32O33O34、O29O30O31O32O33O34O35もしくはO29O30O31O32O33O34O35O36であり;
O29からO36は各々独立してアミノ酸残基であり;
但し、PTH/PTHrP調節領域のO14からC末端残基の1個以上はシステイン残基である。)
のポリペプチドから選択されるPTH/PTHrP調節領域を含み;ならびに
PTH/PTHrPペプチドがPTH−1受容体又はPTH−2受容体と結合する
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項70】
ONがO7であり;
O7が非機能的残基であり;
O10が酸性又は親水性残基であり;
O11が塩基性又は非機能的残基であり;
O12が芳香族又は非機能的残基であり;
O15が親水性又は非機能的残基であり;
O16が親水性残基であり;
O17が酸性又は非機能的残基であり;
O23が芳香族残基であり;及び
OCが不在である
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項71】
ONがO1O2O3O4O5O6O7であり;
O1が非機能的アミノ酸残基であり;
O2が非機能的アミノ酸残基であり;
O3が親水性アミノ酸残基であり;
O4が酸性アミノ酸残基であり;
O5が塩基性又は非機能的アミノ酸残基であり;
O6が親水性アミノ酸残基であり;
O7が非機能的残基であり;
O10が酸性又は親水性残基であり;
O11が塩基性又は非機能的残基であり;
O12が芳香族又は非機能的残基であり;
O15が親水性又は非機能的残基であり;
O16が親水性残基であり;
O17が酸性又は非機能的残基であり;及び
O23が芳香族残基である
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項72】
O1がAであり;
O2がVであり;
O3がSであり;
O4がEであり;
O5がH又はIであり;
O6がQであり;
O7がLであり;
O10がN又はDであり;
O11がK又はLであり;
O12がG、F又はWであり;
O15がI又はSであり;
O16がQ又はNであり;
O17がD又はLであり;及び
O23がF又はWである
請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項73】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項69のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項74】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項73のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項75】
プレプロ領域が配列番号188のアミノ酸配列を含む請求項74のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項76】
PTH/PTHrPペプチドが配列番号16から67から選択される配列を含むPTH/PTHrP調節領域を含む請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項77】
PTH/PTHrP調節領域が配列番号22のアミノ酸配列を含む請求項76のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項78】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項76のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項79】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項78のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項80】
プレプロ領域が配列番号188のアミノ酸配列を含み、及びPTH/PTHrP調節領域が配列番号22のアミノ酸配列を含む請求項79のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項81】
PTH/PTHrPペプチドが配列番号8のアミノ酸配列を含む請求項78のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項82】
(a)配列番号2のアミノ酸配列をもつ第1のポリペプチドと、配列番号8のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子;
(b)配列番号10のアミノ酸配列をもつ第1のポリペプチドと、配列番号4のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子;及び
(c)配列番号10のアミノ酸配列をもつ第1のポリペプチドと、配列番号8のアミノ酸配列をもつ第2のポリペプチドを含むRANKL抗体−PTH/PTHrPキメラ分子
から選択されるRANKL抗体−PTH/PTHrPキメラ分子。
【請求項83】
PTH/PTHrPペプチドが配列番号68から89から選択される配列を含むPTH/PTHrP調節領域を含む請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項84】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項83のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項85】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項84のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項86】
PTH/PTHrPペプチドが配列番号90から107から選択される配列を含むPTH/PTHrP調節領域を含み、但し、PTH/PTHrP調節領域の14位からC末端の1個以上の残基はシステイン残基で置換されている請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項87】
PTH/PTHrPペプチドが更にプレプロ領域を含む請求項86のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項88】
プレプロ領域が配列番号188から207から選択されるアミノ酸配列を含む請求項87のRANKL抗体−PTH/PTHrPキメラ分子。
【請求項89】
請求項1、16及び34のいずれか一項のRANKL抗体−PTH/PTHrPキメラ分子を含む医薬組成物。
【請求項90】
骨吸収抑制剤、骨同化剤、抗炎症剤、免疫抑制剤及び癌治療剤から選択される少なくとも1種の治療剤を更に含む請求項89の医薬組成物。
【請求項91】
少なくとも1種の治療剤がアナキンラ、エタネルセプト、インフリキシマブ、アダリムマブ及びメトトレキセートから選択される請求項90の医薬組成物。
【請求項92】
更に少なくとも1種の癌治療剤を含有する請求項89の医薬組成物。
【請求項93】
少なくとも1種の癌治療剤が放射線療法と化学療法から選択される請求項92の医薬組成物。
【請求項94】
少なくとも1種の癌治療剤が上皮成長因子受容体(EGFR)阻害剤、HER2阻害剤、vegF阻害剤、vegF受容体阻害剤、肝細胞増殖因子(HGF)/分散因子(SF)阻害剤、c−Met阻害剤、アンギオポエチン阻害剤、Tie2阻害剤、血小板由来増殖因子受容体(PDGFR)阻害剤、インスリン様成長因子受容体(IGFR)阻害剤、ムチン様糖蛋白阻害剤、CDC20阻害剤及びCDC33阻害剤から選択される請求項92の医薬組成物。
【請求項95】
更に少なくとも1種の治療用抗体を含有する請求項89の医薬組成物。
【請求項96】
少なくとも1種の治療用抗体がHer2抗体、CDC20抗体、EGFR抗体、vegF抗体、vegF受容体抗体、肝細胞増殖因子(HGF)/分散因子(SF)抗体、インスリン様成長因子受容体(IFGR)抗体及びCDC33抗体から選択される請求項95の医薬組成物。
【請求項97】
請求項89の医薬組成物を投与することを含む、患者における骨減少の治療方法。
【請求項98】
請求項89の医薬組成物と、骨吸収抑制剤、骨同化剤、抗炎症剤、免疫抑制剤及び癌治療剤から選択される少なくとも1種の薬剤を投与することを含む、患者における骨減少の治療方法。
【請求項99】
骨形態形成因子、トランスフォーミング増殖因子β(TGF−β)、インターロイキン−1(IL−1)阻害剤、IL−1ra、アナキンラ、TNFα阻害剤、可溶性TNFα受容体、エタネルセプト、抗TNFα抗体、インフリキシマブ、アダリムマブ、プロスタグランジン、ビスホスホネート、アレンドロネート、フッ化物、カルシウム、非ステロイド性抗炎症薬(NSAID)、COX−2阻害剤、セレコキシブ、ロフェコキシブ、免疫抑制剤、メトトレキセート、レフルノミド、セリンプロテアーゼ阻害剤、分泌型白血球プロテアーゼ阻害剤(SLPI)、IL−6阻害剤、IL−6抗体、IL−8阻害剤、IL−8抗体、IL−18阻害剤、IL−18結合蛋白、IL−18抗体、インターロイキン−1変換酵素(ICE)モジュレーター、線維芽細胞増殖因子(FGF)、FGFモジュレーター、PAFアンタゴニスト、ケラチノサイト増殖因子(KGF)、KGF関連分子、KGFモジュレーター、マトリックスメタロプロテイナーゼ(MMP)モジュレーター、一酸化窒素シンターゼ(NOS)モジュレーター、グルココルチコイド受容体のモジュレーター、グルタミン酸受容体のモジュレーター、リポ多糖(LPS)濃度のモジュレーター、ノルアドレナリン、ノルアドレナリンミメティック及びノルアドレナリンモジュレーターから選択される少なくとも1種の治療剤を投与することを更に含む請求項97の方法。
【請求項100】
請求項90の医薬組成物を投与することを含む、患者における骨減少を伴う炎症症状の治療方法。
【請求項101】
請求項90の医薬組成物を投与することを含む、患者における骨減少を伴う自己免疫症状の治療方法。
【請求項102】
請求項90の医薬組成物を投与することを含む、患者における関節リウマチの治療方法。
【請求項103】
請求項89の医薬組成物を投与することを含む、癌に伴う骨減少の治療方法。
【請求項104】
請求項89の医薬組成物と、上皮成長因子受容体(EGFR)阻害剤、HER2阻害剤、vegF阻害剤、vegF受容体阻害剤、肝細胞増殖因子(HGF)/分散因子(SF)阻害剤、c−Met阻害剤、アンギオポエチン阻害剤、Tie2阻害剤、血小板由来増殖因子受容体(PDGFR)阻害剤、インスリン様成長因子受容体(IGFR)阻害剤、ムチン様糖蛋白阻害剤、CDC20阻害剤及びCDC33阻害剤から選択される少なくとも1種の治療剤を投与することを含む、癌に伴う骨減少の治療方法。
【請求項105】
請求項89の医薬組成物と、Her2抗体、CDC20抗体、EGFR抗体、vegF抗体、vegF受容体抗体、肝細胞増殖因子(HGF)/分散因子(SF)抗体、インスリン様成長因子受容体(IFGR)抗体及びCDC33抗体から選択される少なくとも1種の抗体を投与することを含む、癌に伴う骨減少の治療方法。
【図1】


【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


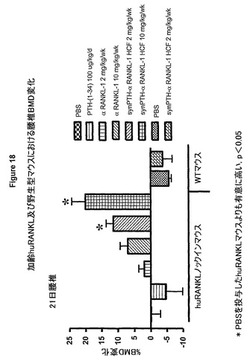
【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】




【図2】


【図3】


【図4】


【図5】


【図6】


【図7】


【図8】


【図9】


【図10】


【図11】


【図12】


【図13】


【図14】


【図15】


【図16】


【図17】


【図18】


【図19】


【図20】


【図21】


【図22】


【図23】


【図24】


【図25】


【図26】


【図27】


【図28】


【図29】


【公開番号】特開2013−55942(P2013−55942A)
【公開日】平成25年3月28日(2013.3.28)
【国際特許分類】
【外国語出願】
【出願番号】特願2012−229099(P2012−229099)
【出願日】平成24年10月16日(2012.10.16)
【分割の表示】特願2008−540279(P2008−540279)の分割
【原出願日】平成18年11月13日(2006.11.13)
【出願人】(500049716)アムジエン・インコーポレーテツド (242)
【Fターム(参考)】
【公開日】平成25年3月28日(2013.3.28)
【国際特許分類】
【出願番号】特願2012−229099(P2012−229099)
【出願日】平成24年10月16日(2012.10.16)
【分割の表示】特願2008−540279(P2008−540279)の分割
【原出願日】平成18年11月13日(2006.11.13)
【出願人】(500049716)アムジエン・インコーポレーテツド (242)
【Fターム(参考)】
[ Back to top ]

