Tie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物
【課題】優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有する安全性の高いTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物の提供。
【解決手段】サンザシの抽出物を有効成分として含有するTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物である。
【解決手段】サンザシの抽出物を有効成分として含有するTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物である。
【発明の詳細な説明】
【技術分野】
【0001】
本発明は、Tie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物に関する。
【背景技術】
【0002】
血管は、血管内皮細胞と血管壁細胞(血管平滑筋細胞やペリサイト)とが、細胞外マトリックスを介して間接的に、又は直接的に接着する構造を有しており、酸素及び栄養素を生体組織に供給し、生体組織から老廃物を除去する機能を有している。
【0003】
一般に、血管の形成は、新たに血管が形成される血管発生(vasculogenesis)と、形成された既存の血管が伸長し、分岐することにより、新たな血管のネットワークが形成される血管新生(angiogenesis)との2段階に分けられる。前者は、血管内皮増殖因子(VEGF)が作用し、脈管形成とよばれる血管の初期発生からその後の血管新生に至るまで非常に広い範囲の血管形成に関与するものであり、後者は、アンジオポエチン(Ang)が作用し、血管内皮細胞と血管壁細胞との接着の制御、血管の構造的安定化に関与するものである。
【0004】
血管は通常の酸素状況においては、血管内皮細胞とその周囲を裏打ちする血管壁細胞とが強固に接着しており、血管構造が安定に保たれているが、組織で低酸素が生じると血管壁細胞が血管内皮細胞から脱離し、無秩序な血管が増生することがある。このような現象(血管新生)は、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患において、しばしば観察されている。
【0005】
これらの血管新生は、血管内皮細胞に発現する受容体型チロシンキナーゼTie2(Tyrosine kinase with Ig and EGF homology domain2)を活性化させることにより、抑制されることが知られている(例えば、特許文献1参照)。血管狭小化あるいは血管拡大化の抑制が原因となって生じる虚血性疾患においては、Tie2の活性化により、血管腔が拡大化されることが報告されている(例えば、非特許文献1参照)。また、Tie2の活性化により、血管内皮細胞の細胞死を抑制することも報告されている(例えば、非特許文献2参照)。
【0006】
このように、Tie2の活性化により、血管新生が抑制されることが知られているだけでなく、血管を成熟化、正常化、及び安定化させることも知られている。
例えば、血管再生医療においては、Tie2の活性化により、血管における血管内皮細胞と血管壁細胞との接着を誘導して、血管を成熟化させることが知られている。
例えば、腫瘍や糖尿病性網膜症などで観察される血管壁細胞が血管内皮細胞に接着しないことによる無秩序な血管が増生するような疾患においては、Tie2の活性化により、血管壁細胞を内皮細胞に接着させ、血管を正常化させることが知られている。
例えば、種々の細胞内外の血管構造を破たんさせる環境因子に対しては、Tie2の活性化により、血管の不安定化を抑制し、血管を安定化させることが知られている。
【0007】
このようなTie2の活性化により血管新生を抑制する天然由来の物質としては、桂皮の抽出物が知られているが(例えば、特許文献1参照)、活性が不十分であるという問題がある。また、血管新生を抑制する物質としては、スラミンが知られているが(例えば、特許文献2参照)、安全性に優れないという問題がある。
【0008】
一方、サンザシの抽出物は、これまでにヒスタミン遊離抑制等の医薬品として用いられてきたが(例えば、特許文献3参照)、サンザシの抽出物が、Tie2活性化作用、VEGF阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有することについては知られておらず、優れたTie2活性化作用、VEGF阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有する安全性の高い物質について、速やかな開発が強く求められているのが現状である。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2009−263358号公報
【特許文献2】特表平9−503488号公報
【特許文献3】特開平6−183991号公報
【非特許文献】
【0010】
【非特許文献1】Science.1999 Dec 24;286(5449):2511−4.
【非特許文献2】P.N.A.S.2004 Apr 13;101(15):5553−8.
【発明の概要】
【発明が解決しようとする課題】
【0011】
本発明は、前記従来における諸問題を解決し、以下の目的を達成することを課題とする。即ち、本発明は、優れたTie2活性化作用を有し、安全性の高いTie2活性化剤を提供することを目的とする。また、本発明は、優れた血管内皮増殖因子(VEGF)阻害作用を有し、安全性の高い血管内皮増殖因子(VEGF)阻害剤を提供することを目的とする。また、本発明は、優れた血管新生抑制作用を有し、安全性の高い血管新生抑制剤を提供することを目的とする。また、本発明は、優れた血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い血管の成熟化剤、血管の正常化剤、及び血管の安定化剤を提供することを目的とする。また、本発明は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い医薬品組成物を提供することを目的とする。
【課題を解決するための手段】
【0012】
前記課題を解決するため本発明者らが鋭意検討を重ねた結果、サンザシの抽出物が優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有することを知見し、本発明を完成したものである。
【0013】
本発明は、本発明者らによる前記知見に基づくものであり、前記課題を解決するための手段としては、以下の通りである。即ち、
<1> サンザシの抽出物を有効成分として含有することを特徴とするTie2活性化剤である。
<2> サンザシの抽出物を有効成分として含有することを特徴とする血管内皮増殖因子(VEGF)阻害剤である。
<3> サンザシの抽出物を有効成分として含有することを特徴とする血管新生抑制剤である。
<4> サンザシの抽出物を有効成分として含有することを特徴とする血管の成熟化剤、血管の正常化剤又は血管の安定化剤である。
<5> 前記<1>に記載のTie2活性化剤、前記<2>に記載の血管内皮増殖因子(VEGF)阻害剤、前記<3>に記載の血管新生抑制剤、及び前記<4>に記載の血管の成熟化剤、血管の正常化剤又は血管の安定化剤の少なくともいずれかを含有することを特徴とする医薬品組成物である。
【発明の効果】
【0014】
本発明のTie2活性化剤によると、従来における前記諸問題を解決し、優れたTie2活性化作用を有し、安全性の高いTie2活性化剤を提供することができる。
本発明の血管内皮増殖因子(VEGF)阻害剤によると、従来における前記諸問題を解決し、優れた血管内皮増殖因子(VEGF)阻害作用を有し、安全性の高い血管内皮増殖因子(VEGF)阻害剤を提供することができる。
本発明の血管新生抑制剤によると、従来における前記諸問題を解決し、優れた血管新生抑制作用を有し、安全性の高い血管新生抑制剤を提供することができる。
本発明の血管の成熟化剤、血管の正常化剤、及び血管の安定化剤によると、従来における前記諸問題を解決し、優れた血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い血管の成熟化剤、血管の正常化剤、及び血管の安定化剤を提供することができる。
本発明の医薬品組成物によると、従来における前記諸問題を解決し、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い医薬品組成物を提供することができる。
【図面の簡単な説明】
【0015】
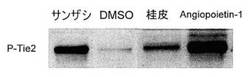
【図1】図1は、HUVECの各試料におけるTie2リン酸化をウエスタンブロットにより検出した結果を示す図である。
【図2】図2は、HUVECの各試料における血管分岐数を測定した結果を示す図である。
【発明を実施するための形態】
【0016】
(Tie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物)
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、サンザシの抽出物を有効成分として含有し、更に必要に応じてその他の成分を含有してなる。
【0017】
前記Tie2活性化剤は、Tie2をリン酸化することで、その活性体(リン酸化Tie2)に変換するTie2活性化作用を有する。前記Tie2が活性化されると、細胞内チロシンキナーゼドメインの自己リン酸化を惹起し、血管内皮細胞と血管壁細胞との接着が誘導される。血管狭小化あるいは血管拡大化の抑制が原因となって生じる虚血性疾患においては、Tie2の活性化により、血管腔が拡大化される。また、Tie2の活性化により、血管内皮細胞の細胞死が抑制される。
【0018】
前記血管内皮増殖因子(VEGF)阻害剤は、VEGFの働きを阻害するVEGF阻害作用を有する。前記VEGFは、分子量34kDa〜46kDaの糖タンパク質であり、血管内皮細胞に働き、細胞の増殖及び遊走の促進作用、並びに血管新生の促進作用を有する。
【0019】
前記血管新生抑制剤は、既存の血管から形成される新たな血管のネットワークを抑制する血管新生抑制作用を有する。低酸素状態では、Tie2の活性化が一時的に抑制され、血管内皮細胞と血管壁細胞との接着が乖離し、接着が乖離された血管内皮細胞から新しい血管のネットワークが形成される。血管新生抑制剤は、このような血管壁細胞が内皮細胞に接着しないことによる無秩序な血管の増生を抑制することができる。
【0020】
前記血管の成熟化剤は、血管内皮細胞と血管壁細胞との接着を誘導して、血管内環境因子(細胞及び液性因子)が容易には血管外に漏出しないような血管内皮細胞間の接着斑を形成する成熟化作用を有する。また、血管再生医療においては、Tie2の活性化により、血管における血管内皮細胞と血管壁細胞との接着を誘導して、血管を成熟化させることが可能である。
【0021】
前記血管の正常化剤は、血管内皮細胞同士の接着を高め、血管壁細胞の血管内皮細胞への裏打ちを促進することにより、血管透過性の破綻した血管や血管の無秩序な増生を招くような異常な血管を、正常な状態にする正常化作用を有する。また、腫瘍や糖尿病性網膜症などで観察される血管壁細胞が血管内皮細胞に接着しないことによる無秩序な血管が増生するような疾患においては、Tie2の活性化により、血管壁細胞を内皮細胞に接着させ、血管を正常化させることが可能である。
【0022】
前記血管の安定化剤は、既存の血管に対する障害、血管内皮細胞同士の解離、及び血管内皮細胞と血管壁細胞の解離を抑制する作用、及び血管内皮細胞の細胞死を抑制する安定化作用を有する。また、種々の細胞内外の血管構造を破たんさせる環境因子に対しては、Tie2の活性化により、血管の不安定化を抑制し、血管を安定化させることが可能である。
【0023】
前記医薬品組成物は、前記Tie2活性化剤、前記血管内皮増殖因子(VEGF)阻害剤、前記血管の成熟化剤、前記血管の正常化剤、前記血管の安定化剤、及び前記血管新生抑制剤のいずれかを含む組成物であり、Tie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有する。
【0024】
<サンザシの抽出物>
前記サンザシは、バラ科サンザシ属の落葉低木であり、学名はCrataegus cuneataである。前記サンザシは、中国中南部の地域から容易に入手可能である。前記サンザシの茎の高さは、30cm〜90cmであり、8月〜9月に紫又は白色の花が咲く。前記サンザシの薬用部位は果実であり、健胃消化薬として広く用いられている。
【0025】
前記サンザシの抽出物は、植物の抽出に一般に用いられている方法により容易に得ることができる。前記サンザシの抽出物としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、抽出液の希釈液、濃縮液、抽出液の乾燥物などが挙げられる。
【0026】
前記サンザシの抽出方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、抽出溶媒を満たした処理槽に抽出原料である前記サンザシを投入し、必要に応じて適宜攪拌しながら可溶性成分を溶出した後、濾過して抽出残渣を除くことにより抽出液を得る方法などが挙げられる。
【0027】
前記サンザシの抽出部位としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、葉部、枝部、幹部、樹皮部、花部、果実部などが挙げられるが、これらの中でも、果実部、葉部が好ましい。
前記サンザシの抽出部位の調製方法としては、各部位を乾燥した後、そのまま又は粗砕機を用い粉砕して溶媒抽出に供することにより得ることができる。前記乾燥は、天日で行ってもよいし、通常使用されている乾燥機を用いて行ってもよい。
【0028】
前記サンザシの抽出条件としては、特に制限はなく、目的に応じて適宜選択することができるが、抽出時間は1時間〜3時間が好ましく、抽出温度は常温〜95℃が好ましい。
【0029】
前記サンザシの抽出溶媒としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、水、親水性溶媒、又はこれらの混合溶媒が挙げられる。前記水としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、純水、水道水、井戸水、鉱泉水、鉱水、温泉水、湧水、淡水、精製水、熱水、イオン交換水、生理食塩水、リン酸緩衝液、リン酸緩衝生理食塩水などが挙げられる。前記親水性溶媒としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、メタノール、エタノール、プロピルアルコール、イソプロピルアルコール等の炭素数1〜5の低級アルコール;アセトン、メチルエチルケトン等の低級脂肪族ケトン;1,3−ブチレングリコール、プロピレングリコール、グリセリン等の炭素数2〜5の多価アルコールなどが挙げられる。前記混合溶媒としては、特に制限はなく、目的に応じて適宜選択することができるが、低級アルコールを使用する場合は、水10質量部に対して1質量部〜90質量部、低級脂肪族ケトンを使用する場合は、水10質量部に対して1質量部〜40質量部、多価アルコールを使用する場合は、水10質量部に対して1質量部〜90質量部、添加することが好ましい。なお、前記サンザシの抽出溶媒は、室温乃至溶媒の沸点以下の温度で用いることが好ましい。
これらの中でも、熱水を用いて抽出することが、好ましい。
【0030】
前記サンザシの抽出溶媒の使用量としては、特に制限はなく、目的に応じて適宜選択することができるが、抽出原料としてのサンザシに対して、5倍量〜15倍量(質量比)であることが好ましい。
【0031】
前記サンザシの抽出物の精製方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、液−液分配抽出、各種クロマトグラフィー、膜分離などの精製方法が挙げられる。
【0032】
<その他の成分>
前記その他の成分としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、賦形剤、防湿剤、防腐剤、強化剤、増粘剤、乳化剤、酸化防止剤、甘味料、酸味料、調味料、着色料、香料等、美白剤、保湿剤、油性成分、紫外線吸収剤、界面活性剤、増粘剤、アルコール類、粉末成分、色剤、水性成分、水、皮膚栄養剤などが挙げられる。
【0033】
<用途>
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有するため、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患、アトピー性皮膚炎、及び花粉症などのアレルギー性疾患に関する医薬品、並びにこれらの疾患に関する安全な予防薬として好適に用いることができ、その配合量、用法、及び剤型としては、その使用目的に応じて適宜選択することができる。また、本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤は、消化管で消化されるようなものではないことが確認されているので、美容用飲食品、健康用飲食品などの飲食品として好適に用いることができ、その配合量、用法、及び剤型としては、その使用目的に応じて適宜選択することができる。
【0034】
前記配合量としては、抽出物の生理活性等によって適宜調整することができるが、前記サンザシの精製物に換算して、0.0001質量%〜20質量%が好ましく、0.0001質量%〜10質量%がより好ましい。
【0035】
前記用法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、経口、非経口、外用などの投与形態が挙げられる。
【0036】
前記剤型としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、錠剤、粉剤、カプセル剤、顆粒剤、エキス剤、及びシロップ剤等の経口投与剤、注射剤、点滴剤、及び坐剤等の非経口投与剤、軟膏、クリーム、乳液、ローション、パック、及び浴用剤等の外用剤などが挙げられる。
【実施例】
【0037】
以下、本発明の実施例を説明するが、本発明は、これらの実施例に何ら限定されるものではない。
【0038】
(製造例1)
<サンザシの抽出物の製造>
サンザシの抽出物として、実施例1及び3では、サンザシエキスパウダーMF(果実部)(丸善製薬株式会社製)、実施例2では、山査葉エキスパウダー(葉部)(丸善製薬株式会社製)を用いた。
【0039】
(実施例1)
<Tie2リン酸化作用>
前記サンザシの抽出物の薬理効果について、リン酸化されたTie2のタンパク質量を検出することにより、評価を行った。前記リン酸化されたTie2のタンパク質量については、SDS−PAGE及びウエスタンブロットを用いた免疫化学的手法により検出した。以下に手順を示す。
まず、6well culture plateに2×105のヒト臍帯静脈内皮細胞(HUVEC)を播種し、Humedia EG2培地(Kurabo社製)にて、37℃、CO2インキュベーターで12時間培養した。培養液を除き、細胞をPBSで洗浄し、RPMI-1640培地(SIGMA社製、R−8755)中で2時間培養した。サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)をDMSOを用いて最終濃度が100μg/mLとなるよう溶解し、前記培地に添加した。10分間インキュベーション後、細胞を氷上で冷却し、冷PBSで洗浄した。タンパク質分解酵素阻害剤(Leupeptin,Aprotinin,Pepstatin,PMSF,Na3VO4)を含んだRIPA buffer中、細胞を超音波粉砕した。sample buffer(0.2M Tris−HCl(pH6.8)、4質量%SDS、20質量%glycerol、5mM EDTA,0.01質量%BPB)を加えて試料1とした。得られた試料1を用い、SDS−PAGE(7.5質量%ポリアクリルアミドゲル,12ウェル,NPU−7.5L,アトー株式会社製)を以下の条件にて行った。
・ ゲル:7.5質量%アクリルアミドゲル(NPU−7.5L,アトー株式会社製)
・ 泳動条件:40mA(75分、ゲル2枚)
・ Phospho−Tie2抗体:#4221(Cell Sigma製)
次に、Western blotting(20V,4℃,終夜)によりPVDF膜へ転写した。5質量%スキムミルク/TBSTによりブロッキング(1時間)を行い、その後、リン酸化Tie2(Cell Signaling,♯4221)を加え、室温で1時間放置した。次いでヤギ-抗ウサギIg’s HRP(BIOSOURCE ALI3404)を加え、室温で1時間放置した。化学発光検出(ECL)により、タンパク質のバンドを検出した。結果を図1に示す。
【0040】
(比較例1)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)に変更した以外は実施例1と同様にして、比較例1とした。なお、前記桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)はDMSOを用いて最終濃度が100μg/mLとなるように調製した。結果を図1に示す。
【0041】
(参考例1)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、陽性コントロールとしてAngiopoietin−1(R&D system社製)に変更した以外は実施例1と同様にして、参考例1とした。なお、前記Angiopoietin−1(R&D system社製)はDMSOを用いて最終濃度が300ng/mLとなるように調製した。結果を図1に示す。
【0042】
(参考例2)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、陰性コントロールとしてDMSOに変更した以外は実施例1と同様にして、参考例2とした。結果を図1に示す。
【0043】
実施例1、比較例1、並びに参考例1及び2におけるTie2リン酸化作用の結果について説明する。図1は、ウエスタンブロットにより検出した各試料におけるリン酸化されたTie2タンパク質のバンドを示している。検出されたバンドの濃さは、リン酸化されたTie2のタンパク質量に比例している。バンドが濃い程、リン酸化されたTie2のタンパク質量が多いことを示している。図1より、前記サンザシ抽出物(果実部)は、Angiopoietin−1と同様、Tie2の顕著なリン酸化をもたらすことが認められた。以前、Tie2をリン酸化すると報告のある桂皮についても、Tie2リン酸化誘導が確認されたが、サンザシの方がより強く活性化を誘導することがわかった。なお、陰性コントロールであるDMSOを添加した系では、Tie2のリン酸化は事実上認められなかった。また、Tie2抗体(Santa Cruz,sc−324)を用いたウエスタンブロットでは、Tie2の発現量そのものは全試料とも同量であった。
【0044】
(実施例2)
<Tie2リン酸化作用>
コンフルエントまで培養した正常ヒト臍帯静脈内皮細胞(HUVEC)を、96ウェルプレートへ2.0×104細胞/0.1mL/ウェルとなるように播種し、Humedia−EG2(低血清血管内皮細胞増殖用培地)を用いて一晩培養した。次に、一晩培養後の前記HUVECを、細胞刺激(被験試料添加)の3時間前に0.1mLのHumedia−EB2(血管内皮細胞基礎培地)に置換し、再度培養を行った。その後、前記ウェル内に、被験試料として前記Humedia−EB2で各濃度に調製したサンザシ抽出部(葉部)(丸善製薬株式会社製、山査葉エキスパウダー)を0.1mL添加し、10分間のインキュベーションを行った。インキュベーション後、イムノアッセイキット(R&D Systems社製、Human Phospho−Tie2(Y992)Immunoassay)を用いてプロトコールに従い、細胞内のリン酸化型Tie2量及び総Tie2量を測定し、総Tie2に対するリン酸化型Tie2の比率を計算し、下記式(1)に従いTie2リン酸化作用を評価した。
また、陰性コントロールとして被験試料の溶解に用いたDMSOについても同様に評価した。結果を表1に示す。
Tie2活性化率(%)=
[{(被験試料添加時のリン酸化型Tie2の測定値)/(被験試料添加時の総Tie2の測定値)}/{(陰性コントロールでのリン酸化型Tie2の測定値)/(陰性コントロールでの総Tie2の測定値)}]×100 ・・・式(1)
【0045】
(参考例3)
<Tie2リン酸化作用>
実施例2において、前記サンザシ抽出物(葉部)を、陽性コントロールとしてAngiopoietin−1(R&D system社製)に変更し、表1に記載の濃度を用いた以外は、実施例2と同様にして、参考例3とした。結果を表1に示す。
【0046】
【表1】

【0047】
実施例2及び参考例3におけるTie2リン酸化作用の結果について説明する。前記イムノアッセイキットによりTie2リン酸化作用の評価を実施したところ、実施例2の前記サンザシ抽出物(葉部)には、Tie2がリン酸化し、Tie2が活性化されることが認められた。なお、陰性コントロールであるDMSOを添加した系では、Tie2の顕著なリン酸化は認められなかった。また、参考例3の陽性コントロールであるAngiopoietin−1を添加した系では、Tie2がリン酸化し、Tie2が活性化されることが認められた。したがって、実施例2の前記サンザシ抽出物(葉部)によりTie2がリン酸化して活性化され、血管成熟化、血管正常化、血管安定化がもたらされ、血管新生が抑制されることが示唆された。
【0048】
(実施例3)
<血管新生抑制作用>
次に、前記サンザシの抽出物(果実部)により、どの程度、血管分岐数が低減されているのかを画像解析することで、血管新生抑制作用の評価を行った。以下に手順を示す。
まず、血管新生キット(倉敷紡績株式会社製)を用い、ヒト正常臍帯静脈血管内皮細胞とヒト正常真皮繊維芽細胞を一定の比率で共培養させ、管腔形成初期段階の増殖状態に調製した。血管内皮細胞増殖因子−A(VEGF−A)(倉敷紡績株式会社製)10ng/mLの共存下、被験試料として、サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)を用い、表2に記載の各濃度を含有した培地に添加後、37℃、5%CO2条件にて、インキュベーションした。培養開始から4日後、7日後、9日後の各々の時点で、VEGF−A共存下、サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)を表2に示す所定濃度含有した培地と交換した。その後、各ウェルの細胞層を70容積%エタノールで固定化し、管腔染色キット(倉敷紡績株式会社製、CD31)を用いてHUVEC細胞のCD31(PECAM−1)を染色した。各ウェルから得られた染色像を撮影し、管腔形成について、管腔の分岐数をもとに、血管新生抑制作用を評価した。結果を表2及び図2に示す。
【0049】
(比較例2)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を、桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)に変更し、表2に記載の濃度を用いた以外は実施例3と同様にして、比較例2とした。結果を表2及び図2に示す。
【0050】
(参考例4)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を用いずに、VEGF−A(+)をVEGF−A(−)に変更して、陰性コントロールとしたこと以外は実施例3と同様にして、参考例4とした。結果を表2及び図2に示す。
(参考例5)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を用いずに陽性コントロールとしたこと以外は実施例3と同様にして、参考例5とした。結果を表2及び図2に示す。
(参考例6)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を、血管新生阻害剤として知られるSuramin(倉敷紡績株式会社製(血管新生キットに付属))(50μM)に変更した以外は実施例3と同様にして、参考例6とした。結果を表2及び図2に示す。
【0051】
【表2】

【0052】
実施例3、比較例2、並びに参考例4〜6において、血管分岐数を基にした血管新生抑制作用の評価を実施したところ、実施例3のサンザシ抽出物(果実部)には、VEGF−A(+)によって増加する血管分岐数を濃度依存で抑制する作用が認められた(抑制率約20%)。一方、比較例2の桂皮抽出物には、今回実施した試験濃度において、作用を確認することができなかった。これらの結果から、今回実施した試験条件でサンザシ抽出物(果実部)には、VEGFの働きを阻害するVEGF阻害作用を有し、有効な血管新生抑制作用を有することがわかった。
【0053】
以上より、サンザシの抽出物が、Tie2リン酸化効果を有することにより、血管内皮増殖因子の阻害、及び血管新生の抑制が起こり、血管の成熟化、血管の正常化、及び血管の安定化を誘導できることが示唆された。
【産業上の利用可能性】
【0054】
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有するため、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患に関する医薬品、及びこれらの疾患に関する安全な予防薬として、幅広く用いることができる。また、本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤は、消化管で消化されるようなものではないことが確認されているので、美容用飲食品、健康用飲食品などの飲食品として、幅広く用いることができる。
【技術分野】
【0001】
本発明は、Tie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物に関する。
【背景技術】
【0002】
血管は、血管内皮細胞と血管壁細胞(血管平滑筋細胞やペリサイト)とが、細胞外マトリックスを介して間接的に、又は直接的に接着する構造を有しており、酸素及び栄養素を生体組織に供給し、生体組織から老廃物を除去する機能を有している。
【0003】
一般に、血管の形成は、新たに血管が形成される血管発生(vasculogenesis)と、形成された既存の血管が伸長し、分岐することにより、新たな血管のネットワークが形成される血管新生(angiogenesis)との2段階に分けられる。前者は、血管内皮増殖因子(VEGF)が作用し、脈管形成とよばれる血管の初期発生からその後の血管新生に至るまで非常に広い範囲の血管形成に関与するものであり、後者は、アンジオポエチン(Ang)が作用し、血管内皮細胞と血管壁細胞との接着の制御、血管の構造的安定化に関与するものである。
【0004】
血管は通常の酸素状況においては、血管内皮細胞とその周囲を裏打ちする血管壁細胞とが強固に接着しており、血管構造が安定に保たれているが、組織で低酸素が生じると血管壁細胞が血管内皮細胞から脱離し、無秩序な血管が増生することがある。このような現象(血管新生)は、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患において、しばしば観察されている。
【0005】
これらの血管新生は、血管内皮細胞に発現する受容体型チロシンキナーゼTie2(Tyrosine kinase with Ig and EGF homology domain2)を活性化させることにより、抑制されることが知られている(例えば、特許文献1参照)。血管狭小化あるいは血管拡大化の抑制が原因となって生じる虚血性疾患においては、Tie2の活性化により、血管腔が拡大化されることが報告されている(例えば、非特許文献1参照)。また、Tie2の活性化により、血管内皮細胞の細胞死を抑制することも報告されている(例えば、非特許文献2参照)。
【0006】
このように、Tie2の活性化により、血管新生が抑制されることが知られているだけでなく、血管を成熟化、正常化、及び安定化させることも知られている。
例えば、血管再生医療においては、Tie2の活性化により、血管における血管内皮細胞と血管壁細胞との接着を誘導して、血管を成熟化させることが知られている。
例えば、腫瘍や糖尿病性網膜症などで観察される血管壁細胞が血管内皮細胞に接着しないことによる無秩序な血管が増生するような疾患においては、Tie2の活性化により、血管壁細胞を内皮細胞に接着させ、血管を正常化させることが知られている。
例えば、種々の細胞内外の血管構造を破たんさせる環境因子に対しては、Tie2の活性化により、血管の不安定化を抑制し、血管を安定化させることが知られている。
【0007】
このようなTie2の活性化により血管新生を抑制する天然由来の物質としては、桂皮の抽出物が知られているが(例えば、特許文献1参照)、活性が不十分であるという問題がある。また、血管新生を抑制する物質としては、スラミンが知られているが(例えば、特許文献2参照)、安全性に優れないという問題がある。
【0008】
一方、サンザシの抽出物は、これまでにヒスタミン遊離抑制等の医薬品として用いられてきたが(例えば、特許文献3参照)、サンザシの抽出物が、Tie2活性化作用、VEGF阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有することについては知られておらず、優れたTie2活性化作用、VEGF阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有する安全性の高い物質について、速やかな開発が強く求められているのが現状である。
【先行技術文献】
【特許文献】
【0009】
【特許文献1】特開2009−263358号公報
【特許文献2】特表平9−503488号公報
【特許文献3】特開平6−183991号公報
【非特許文献】
【0010】
【非特許文献1】Science.1999 Dec 24;286(5449):2511−4.
【非特許文献2】P.N.A.S.2004 Apr 13;101(15):5553−8.
【発明の概要】
【発明が解決しようとする課題】
【0011】
本発明は、前記従来における諸問題を解決し、以下の目的を達成することを課題とする。即ち、本発明は、優れたTie2活性化作用を有し、安全性の高いTie2活性化剤を提供することを目的とする。また、本発明は、優れた血管内皮増殖因子(VEGF)阻害作用を有し、安全性の高い血管内皮増殖因子(VEGF)阻害剤を提供することを目的とする。また、本発明は、優れた血管新生抑制作用を有し、安全性の高い血管新生抑制剤を提供することを目的とする。また、本発明は、優れた血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い血管の成熟化剤、血管の正常化剤、及び血管の安定化剤を提供することを目的とする。また、本発明は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い医薬品組成物を提供することを目的とする。
【課題を解決するための手段】
【0012】
前記課題を解決するため本発明者らが鋭意検討を重ねた結果、サンザシの抽出物が優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有することを知見し、本発明を完成したものである。
【0013】
本発明は、本発明者らによる前記知見に基づくものであり、前記課題を解決するための手段としては、以下の通りである。即ち、
<1> サンザシの抽出物を有効成分として含有することを特徴とするTie2活性化剤である。
<2> サンザシの抽出物を有効成分として含有することを特徴とする血管内皮増殖因子(VEGF)阻害剤である。
<3> サンザシの抽出物を有効成分として含有することを特徴とする血管新生抑制剤である。
<4> サンザシの抽出物を有効成分として含有することを特徴とする血管の成熟化剤、血管の正常化剤又は血管の安定化剤である。
<5> 前記<1>に記載のTie2活性化剤、前記<2>に記載の血管内皮増殖因子(VEGF)阻害剤、前記<3>に記載の血管新生抑制剤、及び前記<4>に記載の血管の成熟化剤、血管の正常化剤又は血管の安定化剤の少なくともいずれかを含有することを特徴とする医薬品組成物である。
【発明の効果】
【0014】
本発明のTie2活性化剤によると、従来における前記諸問題を解決し、優れたTie2活性化作用を有し、安全性の高いTie2活性化剤を提供することができる。
本発明の血管内皮増殖因子(VEGF)阻害剤によると、従来における前記諸問題を解決し、優れた血管内皮増殖因子(VEGF)阻害作用を有し、安全性の高い血管内皮増殖因子(VEGF)阻害剤を提供することができる。
本発明の血管新生抑制剤によると、従来における前記諸問題を解決し、優れた血管新生抑制作用を有し、安全性の高い血管新生抑制剤を提供することができる。
本発明の血管の成熟化剤、血管の正常化剤、及び血管の安定化剤によると、従来における前記諸問題を解決し、優れた血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い血管の成熟化剤、血管の正常化剤、及び血管の安定化剤を提供することができる。
本発明の医薬品組成物によると、従来における前記諸問題を解決し、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有し、安全性の高い医薬品組成物を提供することができる。
【図面の簡単な説明】
【0015】
【図1】図1は、HUVECの各試料におけるTie2リン酸化をウエスタンブロットにより検出した結果を示す図である。
【図2】図2は、HUVECの各試料における血管分岐数を測定した結果を示す図である。
【発明を実施するための形態】
【0016】
(Tie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管新生抑制剤、血管の成熟化剤、血管の正常化剤、及び血管の安定化剤、並びに医薬品組成物)
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、サンザシの抽出物を有効成分として含有し、更に必要に応じてその他の成分を含有してなる。
【0017】
前記Tie2活性化剤は、Tie2をリン酸化することで、その活性体(リン酸化Tie2)に変換するTie2活性化作用を有する。前記Tie2が活性化されると、細胞内チロシンキナーゼドメインの自己リン酸化を惹起し、血管内皮細胞と血管壁細胞との接着が誘導される。血管狭小化あるいは血管拡大化の抑制が原因となって生じる虚血性疾患においては、Tie2の活性化により、血管腔が拡大化される。また、Tie2の活性化により、血管内皮細胞の細胞死が抑制される。
【0018】
前記血管内皮増殖因子(VEGF)阻害剤は、VEGFの働きを阻害するVEGF阻害作用を有する。前記VEGFは、分子量34kDa〜46kDaの糖タンパク質であり、血管内皮細胞に働き、細胞の増殖及び遊走の促進作用、並びに血管新生の促進作用を有する。
【0019】
前記血管新生抑制剤は、既存の血管から形成される新たな血管のネットワークを抑制する血管新生抑制作用を有する。低酸素状態では、Tie2の活性化が一時的に抑制され、血管内皮細胞と血管壁細胞との接着が乖離し、接着が乖離された血管内皮細胞から新しい血管のネットワークが形成される。血管新生抑制剤は、このような血管壁細胞が内皮細胞に接着しないことによる無秩序な血管の増生を抑制することができる。
【0020】
前記血管の成熟化剤は、血管内皮細胞と血管壁細胞との接着を誘導して、血管内環境因子(細胞及び液性因子)が容易には血管外に漏出しないような血管内皮細胞間の接着斑を形成する成熟化作用を有する。また、血管再生医療においては、Tie2の活性化により、血管における血管内皮細胞と血管壁細胞との接着を誘導して、血管を成熟化させることが可能である。
【0021】
前記血管の正常化剤は、血管内皮細胞同士の接着を高め、血管壁細胞の血管内皮細胞への裏打ちを促進することにより、血管透過性の破綻した血管や血管の無秩序な増生を招くような異常な血管を、正常な状態にする正常化作用を有する。また、腫瘍や糖尿病性網膜症などで観察される血管壁細胞が血管内皮細胞に接着しないことによる無秩序な血管が増生するような疾患においては、Tie2の活性化により、血管壁細胞を内皮細胞に接着させ、血管を正常化させることが可能である。
【0022】
前記血管の安定化剤は、既存の血管に対する障害、血管内皮細胞同士の解離、及び血管内皮細胞と血管壁細胞の解離を抑制する作用、及び血管内皮細胞の細胞死を抑制する安定化作用を有する。また、種々の細胞内外の血管構造を破たんさせる環境因子に対しては、Tie2の活性化により、血管の不安定化を抑制し、血管を安定化させることが可能である。
【0023】
前記医薬品組成物は、前記Tie2活性化剤、前記血管内皮増殖因子(VEGF)阻害剤、前記血管の成熟化剤、前記血管の正常化剤、前記血管の安定化剤、及び前記血管新生抑制剤のいずれかを含む組成物であり、Tie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有する。
【0024】
<サンザシの抽出物>
前記サンザシは、バラ科サンザシ属の落葉低木であり、学名はCrataegus cuneataである。前記サンザシは、中国中南部の地域から容易に入手可能である。前記サンザシの茎の高さは、30cm〜90cmであり、8月〜9月に紫又は白色の花が咲く。前記サンザシの薬用部位は果実であり、健胃消化薬として広く用いられている。
【0025】
前記サンザシの抽出物は、植物の抽出に一般に用いられている方法により容易に得ることができる。前記サンザシの抽出物としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、抽出液の希釈液、濃縮液、抽出液の乾燥物などが挙げられる。
【0026】
前記サンザシの抽出方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、抽出溶媒を満たした処理槽に抽出原料である前記サンザシを投入し、必要に応じて適宜攪拌しながら可溶性成分を溶出した後、濾過して抽出残渣を除くことにより抽出液を得る方法などが挙げられる。
【0027】
前記サンザシの抽出部位としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、葉部、枝部、幹部、樹皮部、花部、果実部などが挙げられるが、これらの中でも、果実部、葉部が好ましい。
前記サンザシの抽出部位の調製方法としては、各部位を乾燥した後、そのまま又は粗砕機を用い粉砕して溶媒抽出に供することにより得ることができる。前記乾燥は、天日で行ってもよいし、通常使用されている乾燥機を用いて行ってもよい。
【0028】
前記サンザシの抽出条件としては、特に制限はなく、目的に応じて適宜選択することができるが、抽出時間は1時間〜3時間が好ましく、抽出温度は常温〜95℃が好ましい。
【0029】
前記サンザシの抽出溶媒としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、水、親水性溶媒、又はこれらの混合溶媒が挙げられる。前記水としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、純水、水道水、井戸水、鉱泉水、鉱水、温泉水、湧水、淡水、精製水、熱水、イオン交換水、生理食塩水、リン酸緩衝液、リン酸緩衝生理食塩水などが挙げられる。前記親水性溶媒としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、メタノール、エタノール、プロピルアルコール、イソプロピルアルコール等の炭素数1〜5の低級アルコール;アセトン、メチルエチルケトン等の低級脂肪族ケトン;1,3−ブチレングリコール、プロピレングリコール、グリセリン等の炭素数2〜5の多価アルコールなどが挙げられる。前記混合溶媒としては、特に制限はなく、目的に応じて適宜選択することができるが、低級アルコールを使用する場合は、水10質量部に対して1質量部〜90質量部、低級脂肪族ケトンを使用する場合は、水10質量部に対して1質量部〜40質量部、多価アルコールを使用する場合は、水10質量部に対して1質量部〜90質量部、添加することが好ましい。なお、前記サンザシの抽出溶媒は、室温乃至溶媒の沸点以下の温度で用いることが好ましい。
これらの中でも、熱水を用いて抽出することが、好ましい。
【0030】
前記サンザシの抽出溶媒の使用量としては、特に制限はなく、目的に応じて適宜選択することができるが、抽出原料としてのサンザシに対して、5倍量〜15倍量(質量比)であることが好ましい。
【0031】
前記サンザシの抽出物の精製方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、液−液分配抽出、各種クロマトグラフィー、膜分離などの精製方法が挙げられる。
【0032】
<その他の成分>
前記その他の成分としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、賦形剤、防湿剤、防腐剤、強化剤、増粘剤、乳化剤、酸化防止剤、甘味料、酸味料、調味料、着色料、香料等、美白剤、保湿剤、油性成分、紫外線吸収剤、界面活性剤、増粘剤、アルコール類、粉末成分、色剤、水性成分、水、皮膚栄養剤などが挙げられる。
【0033】
<用途>
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有するため、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患、アトピー性皮膚炎、及び花粉症などのアレルギー性疾患に関する医薬品、並びにこれらの疾患に関する安全な予防薬として好適に用いることができ、その配合量、用法、及び剤型としては、その使用目的に応じて適宜選択することができる。また、本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤は、消化管で消化されるようなものではないことが確認されているので、美容用飲食品、健康用飲食品などの飲食品として好適に用いることができ、その配合量、用法、及び剤型としては、その使用目的に応じて適宜選択することができる。
【0034】
前記配合量としては、抽出物の生理活性等によって適宜調整することができるが、前記サンザシの精製物に換算して、0.0001質量%〜20質量%が好ましく、0.0001質量%〜10質量%がより好ましい。
【0035】
前記用法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、経口、非経口、外用などの投与形態が挙げられる。
【0036】
前記剤型としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、錠剤、粉剤、カプセル剤、顆粒剤、エキス剤、及びシロップ剤等の経口投与剤、注射剤、点滴剤、及び坐剤等の非経口投与剤、軟膏、クリーム、乳液、ローション、パック、及び浴用剤等の外用剤などが挙げられる。
【実施例】
【0037】
以下、本発明の実施例を説明するが、本発明は、これらの実施例に何ら限定されるものではない。
【0038】
(製造例1)
<サンザシの抽出物の製造>
サンザシの抽出物として、実施例1及び3では、サンザシエキスパウダーMF(果実部)(丸善製薬株式会社製)、実施例2では、山査葉エキスパウダー(葉部)(丸善製薬株式会社製)を用いた。
【0039】
(実施例1)
<Tie2リン酸化作用>
前記サンザシの抽出物の薬理効果について、リン酸化されたTie2のタンパク質量を検出することにより、評価を行った。前記リン酸化されたTie2のタンパク質量については、SDS−PAGE及びウエスタンブロットを用いた免疫化学的手法により検出した。以下に手順を示す。
まず、6well culture plateに2×105のヒト臍帯静脈内皮細胞(HUVEC)を播種し、Humedia EG2培地(Kurabo社製)にて、37℃、CO2インキュベーターで12時間培養した。培養液を除き、細胞をPBSで洗浄し、RPMI-1640培地(SIGMA社製、R−8755)中で2時間培養した。サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)をDMSOを用いて最終濃度が100μg/mLとなるよう溶解し、前記培地に添加した。10分間インキュベーション後、細胞を氷上で冷却し、冷PBSで洗浄した。タンパク質分解酵素阻害剤(Leupeptin,Aprotinin,Pepstatin,PMSF,Na3VO4)を含んだRIPA buffer中、細胞を超音波粉砕した。sample buffer(0.2M Tris−HCl(pH6.8)、4質量%SDS、20質量%glycerol、5mM EDTA,0.01質量%BPB)を加えて試料1とした。得られた試料1を用い、SDS−PAGE(7.5質量%ポリアクリルアミドゲル,12ウェル,NPU−7.5L,アトー株式会社製)を以下の条件にて行った。
・ ゲル:7.5質量%アクリルアミドゲル(NPU−7.5L,アトー株式会社製)
・ 泳動条件:40mA(75分、ゲル2枚)
・ Phospho−Tie2抗体:#4221(Cell Sigma製)
次に、Western blotting(20V,4℃,終夜)によりPVDF膜へ転写した。5質量%スキムミルク/TBSTによりブロッキング(1時間)を行い、その後、リン酸化Tie2(Cell Signaling,♯4221)を加え、室温で1時間放置した。次いでヤギ-抗ウサギIg’s HRP(BIOSOURCE ALI3404)を加え、室温で1時間放置した。化学発光検出(ECL)により、タンパク質のバンドを検出した。結果を図1に示す。
【0040】
(比較例1)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)に変更した以外は実施例1と同様にして、比較例1とした。なお、前記桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)はDMSOを用いて最終濃度が100μg/mLとなるように調製した。結果を図1に示す。
【0041】
(参考例1)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、陽性コントロールとしてAngiopoietin−1(R&D system社製)に変更した以外は実施例1と同様にして、参考例1とした。なお、前記Angiopoietin−1(R&D system社製)はDMSOを用いて最終濃度が300ng/mLとなるように調製した。結果を図1に示す。
【0042】
(参考例2)
<Tie2リン酸化作用>
実施例1において、前記サンザシ抽出物(果実部)を、陰性コントロールとしてDMSOに変更した以外は実施例1と同様にして、参考例2とした。結果を図1に示す。
【0043】
実施例1、比較例1、並びに参考例1及び2におけるTie2リン酸化作用の結果について説明する。図1は、ウエスタンブロットにより検出した各試料におけるリン酸化されたTie2タンパク質のバンドを示している。検出されたバンドの濃さは、リン酸化されたTie2のタンパク質量に比例している。バンドが濃い程、リン酸化されたTie2のタンパク質量が多いことを示している。図1より、前記サンザシ抽出物(果実部)は、Angiopoietin−1と同様、Tie2の顕著なリン酸化をもたらすことが認められた。以前、Tie2をリン酸化すると報告のある桂皮についても、Tie2リン酸化誘導が確認されたが、サンザシの方がより強く活性化を誘導することがわかった。なお、陰性コントロールであるDMSOを添加した系では、Tie2のリン酸化は事実上認められなかった。また、Tie2抗体(Santa Cruz,sc−324)を用いたウエスタンブロットでは、Tie2の発現量そのものは全試料とも同量であった。
【0044】
(実施例2)
<Tie2リン酸化作用>
コンフルエントまで培養した正常ヒト臍帯静脈内皮細胞(HUVEC)を、96ウェルプレートへ2.0×104細胞/0.1mL/ウェルとなるように播種し、Humedia−EG2(低血清血管内皮細胞増殖用培地)を用いて一晩培養した。次に、一晩培養後の前記HUVECを、細胞刺激(被験試料添加)の3時間前に0.1mLのHumedia−EB2(血管内皮細胞基礎培地)に置換し、再度培養を行った。その後、前記ウェル内に、被験試料として前記Humedia−EB2で各濃度に調製したサンザシ抽出部(葉部)(丸善製薬株式会社製、山査葉エキスパウダー)を0.1mL添加し、10分間のインキュベーションを行った。インキュベーション後、イムノアッセイキット(R&D Systems社製、Human Phospho−Tie2(Y992)Immunoassay)を用いてプロトコールに従い、細胞内のリン酸化型Tie2量及び総Tie2量を測定し、総Tie2に対するリン酸化型Tie2の比率を計算し、下記式(1)に従いTie2リン酸化作用を評価した。
また、陰性コントロールとして被験試料の溶解に用いたDMSOについても同様に評価した。結果を表1に示す。
Tie2活性化率(%)=
[{(被験試料添加時のリン酸化型Tie2の測定値)/(被験試料添加時の総Tie2の測定値)}/{(陰性コントロールでのリン酸化型Tie2の測定値)/(陰性コントロールでの総Tie2の測定値)}]×100 ・・・式(1)
【0045】
(参考例3)
<Tie2リン酸化作用>
実施例2において、前記サンザシ抽出物(葉部)を、陽性コントロールとしてAngiopoietin−1(R&D system社製)に変更し、表1に記載の濃度を用いた以外は、実施例2と同様にして、参考例3とした。結果を表1に示す。
【0046】
【表1】

【0047】
実施例2及び参考例3におけるTie2リン酸化作用の結果について説明する。前記イムノアッセイキットによりTie2リン酸化作用の評価を実施したところ、実施例2の前記サンザシ抽出物(葉部)には、Tie2がリン酸化し、Tie2が活性化されることが認められた。なお、陰性コントロールであるDMSOを添加した系では、Tie2の顕著なリン酸化は認められなかった。また、参考例3の陽性コントロールであるAngiopoietin−1を添加した系では、Tie2がリン酸化し、Tie2が活性化されることが認められた。したがって、実施例2の前記サンザシ抽出物(葉部)によりTie2がリン酸化して活性化され、血管成熟化、血管正常化、血管安定化がもたらされ、血管新生が抑制されることが示唆された。
【0048】
(実施例3)
<血管新生抑制作用>
次に、前記サンザシの抽出物(果実部)により、どの程度、血管分岐数が低減されているのかを画像解析することで、血管新生抑制作用の評価を行った。以下に手順を示す。
まず、血管新生キット(倉敷紡績株式会社製)を用い、ヒト正常臍帯静脈血管内皮細胞とヒト正常真皮繊維芽細胞を一定の比率で共培養させ、管腔形成初期段階の増殖状態に調製した。血管内皮細胞増殖因子−A(VEGF−A)(倉敷紡績株式会社製)10ng/mLの共存下、被験試料として、サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)を用い、表2に記載の各濃度を含有した培地に添加後、37℃、5%CO2条件にて、インキュベーションした。培養開始から4日後、7日後、9日後の各々の時点で、VEGF−A共存下、サンザシ抽出物(果実部)(丸善製薬株式会社製、サンザシエキスパウダーMF)を表2に示す所定濃度含有した培地と交換した。その後、各ウェルの細胞層を70容積%エタノールで固定化し、管腔染色キット(倉敷紡績株式会社製、CD31)を用いてHUVEC細胞のCD31(PECAM−1)を染色した。各ウェルから得られた染色像を撮影し、管腔形成について、管腔の分岐数をもとに、血管新生抑制作用を評価した。結果を表2及び図2に示す。
【0049】
(比較例2)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を、桂皮抽出物(丸善製薬株式会社製、ケイヒエキスパウダーMF)に変更し、表2に記載の濃度を用いた以外は実施例3と同様にして、比較例2とした。結果を表2及び図2に示す。
【0050】
(参考例4)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を用いずに、VEGF−A(+)をVEGF−A(−)に変更して、陰性コントロールとしたこと以外は実施例3と同様にして、参考例4とした。結果を表2及び図2に示す。
(参考例5)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を用いずに陽性コントロールとしたこと以外は実施例3と同様にして、参考例5とした。結果を表2及び図2に示す。
(参考例6)
<血管新生抑制作用>
実施例3において、前記サンザシ抽出物(果実部)を、血管新生阻害剤として知られるSuramin(倉敷紡績株式会社製(血管新生キットに付属))(50μM)に変更した以外は実施例3と同様にして、参考例6とした。結果を表2及び図2に示す。
【0051】
【表2】

【0052】
実施例3、比較例2、並びに参考例4〜6において、血管分岐数を基にした血管新生抑制作用の評価を実施したところ、実施例3のサンザシ抽出物(果実部)には、VEGF−A(+)によって増加する血管分岐数を濃度依存で抑制する作用が認められた(抑制率約20%)。一方、比較例2の桂皮抽出物には、今回実施した試験濃度において、作用を確認することができなかった。これらの結果から、今回実施した試験条件でサンザシ抽出物(果実部)には、VEGFの働きを阻害するVEGF阻害作用を有し、有効な血管新生抑制作用を有することがわかった。
【0053】
以上より、サンザシの抽出物が、Tie2リン酸化効果を有することにより、血管内皮増殖因子の阻害、及び血管新生の抑制が起こり、血管の成熟化、血管の正常化、及び血管の安定化を誘導できることが示唆された。
【産業上の利用可能性】
【0054】
本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤、並びに医薬品組成物は、優れたTie2活性化作用、血管内皮増殖因子(VEGF)阻害作用、血管新生抑制作用、血管の成熟化作用、血管の正常化作用、及び血管の安定化作用を有するため、腫瘍、慢性関節リウマチ、糖尿病網膜症、高脂血症、高血圧などの血管病変を主体とした疾患に関する医薬品、及びこれらの疾患に関する安全な予防薬として、幅広く用いることができる。また、本発明のTie2活性化剤、血管内皮増殖因子(VEGF)阻害剤、血管の成熟化剤、血管の正常化剤、血管の安定化剤、及び血管新生抑制剤は、消化管で消化されるようなものではないことが確認されているので、美容用飲食品、健康用飲食品などの飲食品として、幅広く用いることができる。
【特許請求の範囲】
【請求項1】
サンザシの抽出物を有効成分として含有することを特徴とするTie2活性化剤。
【請求項2】
サンザシの抽出物を有効成分として含有することを特徴とする血管内皮増殖因子(VEGF)阻害剤。
【請求項3】
サンザシの抽出物を有効成分として含有することを特徴とする血管新生抑制剤。
【請求項4】
サンザシの抽出物を有効成分として含有することを特徴とする血管の成熟化剤、血管の正常化剤又は血管の安定化剤。
【請求項5】
請求項1に記載のTie2活性化剤、請求項2に記載の血管内皮増殖因子(VEGF)阻害剤、請求項3に記載の血管新生抑制剤、及び請求項4に記載の血管の成熟化剤、血管の正常化剤又は血管の安定化剤の少なくともいずれかを含有することを特徴とする医薬品組成物。
【請求項1】
サンザシの抽出物を有効成分として含有することを特徴とするTie2活性化剤。
【請求項2】
サンザシの抽出物を有効成分として含有することを特徴とする血管内皮増殖因子(VEGF)阻害剤。
【請求項3】
サンザシの抽出物を有効成分として含有することを特徴とする血管新生抑制剤。
【請求項4】
サンザシの抽出物を有効成分として含有することを特徴とする血管の成熟化剤、血管の正常化剤又は血管の安定化剤。
【請求項5】
請求項1に記載のTie2活性化剤、請求項2に記載の血管内皮増殖因子(VEGF)阻害剤、請求項3に記載の血管新生抑制剤、及び請求項4に記載の血管の成熟化剤、血管の正常化剤又は血管の安定化剤の少なくともいずれかを含有することを特徴とする医薬品組成物。
【図1】


【図2】




【図2】


【公開番号】特開2012−131766(P2012−131766A)
【公開日】平成24年7月12日(2012.7.12)
【国際特許分類】
【出願番号】特願2011−105696(P2011−105696)
【出願日】平成23年5月10日(2011.5.10)
【出願人】(591082421)丸善製薬株式会社 (239)
【Fターム(参考)】
【公開日】平成24年7月12日(2012.7.12)
【国際特許分類】
【出願日】平成23年5月10日(2011.5.10)
【出願人】(591082421)丸善製薬株式会社 (239)
【Fターム(参考)】
[ Back to top ]

