サノフイにより出願された特許
31 - 40 / 433
2,5−置換されたオキサゾロピリミジン誘導体
本発明は、式(I)
【化1】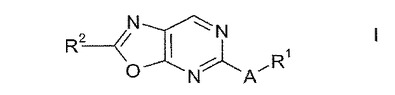
(式中、A、R1及びR2は、特許請求の範囲に記載された通り定義される)のオキサゾロピリミジン化合物に関する。式Iの化合物は、例えば創傷治癒に適している。 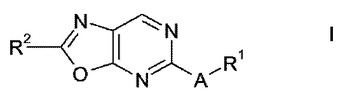 (もっと読む)
(もっと読む)
2,5−置換されたオキサゾロピリミジン環を有するカルボン酸誘導体
本発明は、式(I)
【化1】
(式中、A、R1、R2、R3及びXは、特許請求の範囲に記載された通り定義される)のオキサゾロピリミジン化合物に関する。式(I)の化合物は、例えば創傷治癒に適している。 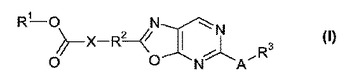 (もっと読む)
(もっと読む)
2,5,7−置換されたオキサゾロピリミジン環を有するカルボン酸誘導体
本発明は、式(I)
【化1】
(式中、A、R1、R2、R3、R4及びXは、特許請求の範囲に記載された通り定義される)のオキサゾロピリミジン化合物に関する。式(I)の化合物は、例えば創傷治癒に適している。 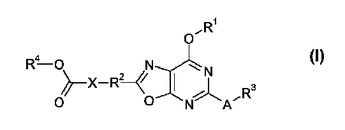 (もっと読む)
(もっと読む)
2,5−置換されたオキサゾロピリミジン環を有する複素環式カルボン酸誘導体
本発明は、式(I)
【化1】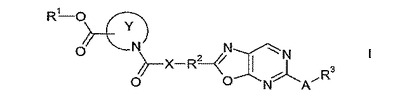
(式中、A、R1、R2、R3、X及びYは、特許請求の範囲に記載された通り定義される)のオキサゾロピリミジン化合物に関する。式(I)の化合物は、例えば創傷治癒に適している。 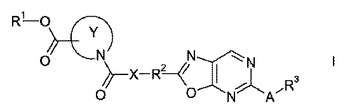 (もっと読む)
(もっと読む)
トランスジェニック非ヒト動物およびその使用
本発明は一般的には導入遺伝子構築物、導入遺伝子構築物を含むトランスジェニック非ヒト動物、該導入遺伝子構築物を含むトランスジェニック非ヒト動物の作製方法およびそれを用いる方法に関する。本発明の実施態様は、リガンドをGPCRレセプターに結合した後に経路変更に応答する生物発光導入遺伝子レポーターシステムを含むトランスジェニックモデルを用いて、全身の動物、組織片、またはネイティブ細胞中で非侵襲的にGPCRリガンドを試験する方法に関する。 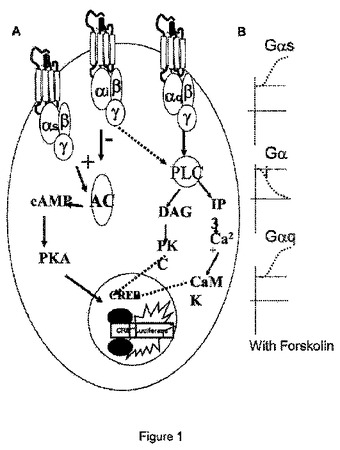 (もっと読む)
(もっと読む)
ドロネダロンの新規製造方法
本発明の主題は、式(I)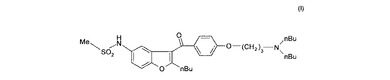
のN−[2−n−ブチル−3−{4−[(3−ジブチルアミノ)プロポキシ]ベンゾイル}−1−ベンゾフラン−5−イル]メタンスルホンアミドの新規製造方法及び前記製造方法の新規中間体である。 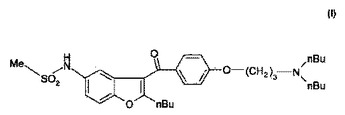 (もっと読む)
(もっと読む)
ミエリン塩基性タンパク質プロモーターの制御下でルシフェラーゼを発現する動物モデル(MBP−LUCI)、及び生物発光インビボ画像化のためのモデルの使用
CNSにおける脱髄及び再髄鞘化事象を転写レベルでインビボで可視化及び定量するための、ミエリン塩基性タンパク質−ルシフェラーゼバイオイメージング非侵襲的モデルが提供される。ルシフェラーゼを発現するトランスジェニック動物を、ホタルルシフェラーゼレポーターにカップリングされたミエリン塩基性タンパク質(MBP)プロモーターを用いて生成した。MBP−luciバイオイメージングモデルは、髄鞘形成の状態及び再髄鞘化を調節する試験化合物の有効性をモニタリングするための手段を提供する。バイオイメージングの利点は、長期間の研究において被験体がそれ自身のコントロールとして役立ち得るということである。同じ被験体が、脱髄及び再髄鞘化プロセスの間、少なくとも10週の期間にわたって連続して追跡され得る。このモデルは、個々の動物画像化応答の正規化を可能にし、そしてかなり分散が減少した良質のデータを提供する。さらに、動物のコホートを異なる時点で屠殺する必要がないので、化合物有効性研究に必要な数を減らすことが可能である。 (もっと読む)
アリールスルホンアミドピリジン−ピリジノン誘導体、該誘導体の調製、および該誘導体の治療用途
本発明は、一般式(I)のピリジン−ピリジノン誘導体:(式中、R1、R2、R3、R4、n、n’、V、W、Y、Z、Arは本明細書中で定義するとおりである。)、ならびに該誘導体の調製方法および該誘導体の治療応用に関する。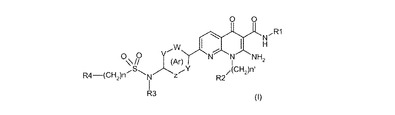
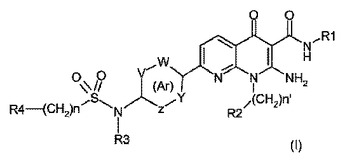 (もっと読む)
(もっと読む)
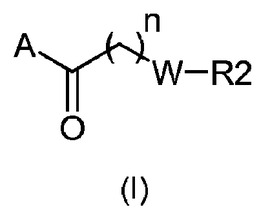
新規(複素環/縮合ピペリジン)−(ピペラジニル)−1−アルカノンまたは(複素環/縮合ピロリジン)−(ピペラジニル)−1−アルカノン誘導体およびp75阻害剤としてのこれらの使用
本発明は一般式(I)の(複素環/縮合ピペリジン)−(ピペラジニル)−1−アルカノンまたは(複素環/縮合ピロリジン)−(ピペラジニル)−1−アルカノン誘導体に関し、式中、A、W、nおよびR2は請求項1において定義される通りである。本発明は、さらに、該誘導体の調製方法および該誘導体の治療的使用に関する。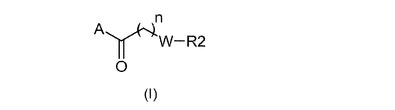
 (もっと読む)
(もっと読む)
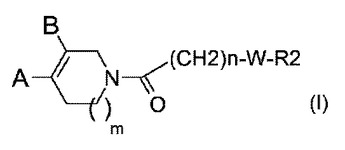
新規(複素環/テトラヒドロピリジン)−(ピペラジニル)−1−アルカノンおよび(複素環/ジヒドロピロリジン)−(ピペラジニル)−1−アルカノン誘導体、並びにp75阻害剤としてのこれらの使用
本発明は、一般式(I)の(複素環/テトラヒドロピリジン)−(ピペラジニル)−1−アルカノンおよび(複素環/ジヒドロピロリジン)−(ピペラジニル)−1−アルカノン誘導体(式中、A、W、nおよびR2は請求項1に定義される通りである。)に関する。本発明は、さらに、前記誘導体の調製並びに前記誘導体の治療上の使用に関する。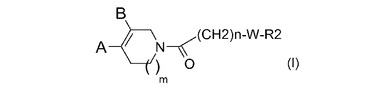
 (もっと読む)
(もっと読む)
31 - 40 / 433
[ Back to top ]

