Fターム[2G041DA04]の内容
その他の電気的手段による材料の調査、分析 (22,023) | イオン源 (4,018) | 光イオン化 (1,305) | レーザイオン化 (1,161) | MALDI (799)
Fターム[2G041DA04]に分類される特許
81 - 100 / 799
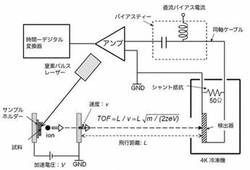
イオン価数弁別高速粒子検出器
【課題】粒子の衝突に対してナノ秒の高速パルスを生成する超伝導細線型検出器(SSLD)でイオンの価数弁別を可能にする。
【解決手段】SSLDに流すバイアス電流の変えることにより、SSLDで検出可能な粒子の運動エネルギー下限を変えることができ、1価以上の全てのイオン、2価以上の全てのイオンというように、複数の質量スペクトルのセットを得て、例えば、1価以上の全てのイオンからなるデータから、2価以上の全てのイオンのデータを差し引くことにより、1価イオンのみのデータを得ることができる。同様に2価のみのデータ、3価のみのデータ(順次多価イオンについても同様)を得ることができる。すなわち、価数弁別が可能になる。
(もっと読む)
飛行時間型質量分析方法及び装置
【課題】イオンの垂直方向の収束性を向上させ、感度向上のため直交加速イオン源との接続を可能にすることができる飛行時間型質量分析装置を提供する。
【解決手段】複数のイオンをパルス的に出射できるイオン源10と、らせん型軌道を実現する分析計と、イオンを検出する検出器15とを備えた飛行時間型質量分析装置であって、らせん軌道を実現するために分析計を複数の積層トロイダル電場で構成させる。
(もっと読む)
飛行時間型質量分析方法及び装置
【課題】イオンの垂直方向の収束性を向上させ、感度向上のため直交加速イオン源との接続を可能にすることができる飛行時間型質量分析装置を提供する。
【解決手段】複数のイオンをパルス的に出射できるイオン源10と、直進軌道とらせん型軌道を実現する分析計と、イオンを検出する検出器15とを備えた飛行時間型質量分析装置であって、らせん軌道を実現するために分析計を複数の積層トロイダル電場で構成させる。
(もっと読む)
糖鎖分析方法
【課題】糖鎖と夾雑物が混在する試料において、マススペクトルの中から糖鎖由来のピークを特異的に抽出することのできる糖鎖分析方法を提供する。
【解決手段】糖鎖を含む試料にアミノキノリンを添加し、上記試料をマトリックス支援レーザー脱離イオン化質量分析装置で分析する。糖鎖を含む試料をアミノキノリンの存在下で質量分析すると、プロトン付加分子イオンや金属イオン付加分子イオン等の通常の分子イオンに代えて又は加えて、これらのピークから高質量側にm/z=126離れた位置にピーク(126Da付加分子イオンピーク)が出現する。この126Da付加分子イオンピークは糖鎖特異的に出現するため、このピークを探索することにより、糖鎖と夾雑物が混在する試料のマススペクトルから糖鎖由来のピークのみを容易に抽出することができる。
(もっと読む)
一回の分析における多数の分析物の認識および定量のための方法
MALDI質量分析におけるマトリックスとしてのシアノケイ皮酸のハロゲン化誘導体の使用
発明は検体のMALDI質量分析のためのマトリックスにおける、一般式:
を有するハロゲン化シアノケイ皮酸誘導体、及び/または4-ブロモ-α-シアノケイ皮酸及び/またはα-シアノ-2,4-ジクロロケイ皮酸の使用に関する。ここで、RはF,Cl及びBrの中から独立に選ばれ、n=3,4または5である。R’はCOOH,CONH2,SO3H及びCOOR”の中から選ばれ、R”=C1-C5アルキル基である。  (もっと読む)
(もっと読む)
飛行時間型質量分析装置
【課題】従来の遅延引出し法ではイオンを加速する際にm/zの相違が考慮されないため、適切なエネルギ収束が達成されるm/z範囲が狭く、分解能が改善されるm/z範囲も狭い。
【解決手段】試料2にレーザ光を照射してイオンを発生させる時点で、試料プレート1から引出し電極3に向けて緩やかに下がる電位勾配をもつ電場を形成しておく(b)。試料2表面付近で発生したイオンはm/zに依存しない初速を持つが、そのほか電場の作用によりm/zに応じた速度を持つ。そのため、m/zが大きなイオンほど試料2近傍に残ることになり、遅延時間t経過後に試料プレート1への印加電圧がステップ状に上げられたとき(c)、m/zの大きなイオンはm/zが小さなイオンに比べて相対的に大きな加速エネルギを受ける。これにより、m/z毎に適切なポテンシャルエネルギ変化をイオンに与えることができ、幅広いm/zに亘ってエネルギ収束を適切に行い分解能を改善することができる。
(もっと読む)
MALDI−MS用試料調製方法
【課題】均一性及びイオン化持続性の高い試料/マトリックス混合物をサンプルプレート上に形成する。
【解決手段】液体マトリックスであるCHCA_Bと分析対象物質を含む試料液とをサンプルプレート10上に滴下して混合し、その上にメタノール又はアセトニトリルを含む液滴統一用液体を滴下する。これにより、サンプルプレート10上で複数の小液滴に分散した試料/マトリックス混合液を一つの液滴に纏めることができ分析対象物質を巨視的に均一な状態とすることができる。また、マトリックスとして液体マトリックスを用いることにより、固体マトリックスを用いた従来法に比べて高いイオン化持続性を達成することができる。以上の結果、数点のみのレーザー照射で十分な分析精度を達成することが可能となり、MALDI−MSにおける分析時間を大幅に短縮することができる。
(もっと読む)
質量分析装置
【課題】短い測定時間で広い質量電荷比範囲のマススペクトルを取得可能な分析と、複雑な分子構造の解析に有用なMSnスペクトルを取得可能な分析とを、1台の質量分析装置で切り替えて実施できるようにする。
【解決手段】MALDIイオン源、イオンを加速する引出し電極13、イオンを収束させるイオン光学系14などを含むイオン導入部10と、イオンを直線的に飛行させる飛行空間を内部に形成するフライトチューブ34との間に、イオントラップを含むイオン捕捉部20と第2検出部31とを配置する。通常分析の際には、イオン導入穴24及びイオン導出穴25を通過するようにイオン光学系14でイオン流を絞り、フライトチューブ34内空間のほかイオントラップ内空間や第2検出部31内の空間も自由飛行領域として飛行時間を計測する。MSn分析の際にはイオントラップに一旦イオンを捕捉し、イオントラップで質量分離して吐き出したイオンを第2検出部31で検出する。
(もっと読む)
生体分子及びその相互作用特性の検出方法
【解決手段】
生体分子を化学的不活性材料のシートの微視的孔の中に濃縮する工程と、当該開口部を制限する工程と、当該孔を通る電流又は当該孔開口部付近の蛍光を測定する工程とを含む、生体分子の検出方法。前記電流又は蛍光は分子が孔から拡散するにつれて変化し、拡散速度の尺度を与え、それによって分子の存在及び特性を検出する。相互作用する分子の場合、相互作用しない分子よりも拡散速度が遅くなると予想され、分子相互作用が測定される。孔の集団にキャップをし、質量分析計に挿入することで分子の同定が可能である。
(もっと読む)
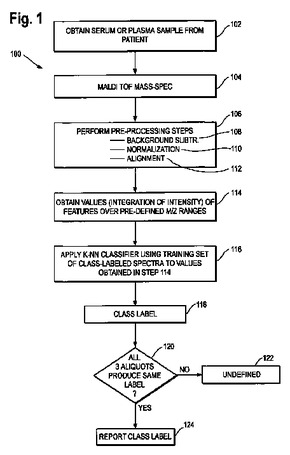
質量スペクトル分析を用いた、治療薬投与のための癌患者のセレクション
質量分析データおよび分類アルゴリズムにより、EGFRおよび/またはHER2を標的とした治療薬のような、AktまたはERK/JNK/p38またはPKCでの、またはそれらの上流でのMAPK(マイトジェン活性化プロテインキナーゼ)経路またはPKC(プロテインキナーゼC)経路に関わる受容体のアゴニスト、受容体もしくはタンパク質を標的にする治療薬または治療薬の組み合わせによる治療が固形上皮腫瘍癌患者に有効である可能性が高いかどうかを決定することが可能となる。該方法により、EGFRを標的とした治療薬およびCOX2を標的とした治療薬の組み合わせが該癌患者に有用である可能性が高いかどうか;あるいはNF−κB阻害剤による治療が該癌患者に有用である可能性が高いかどうかを決定することも可能となる。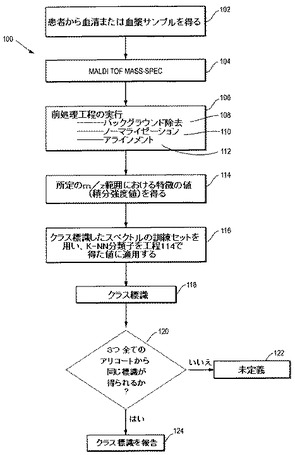
 (もっと読む)
(もっと読む)
質量分析装置
【課題】特別に加工された試料プレートを用いることなく、マトリクス付着後の試料プレートをステージに載置した際の位置ずれを精度良く検出し、その位置ずれを補正して分析者により指定された領域に対する正確な質量分析を実施する。
【解決手段】試料プレート3が試料ステージ2上に載置されると、照射痕形成制御部22が試料ステージ2を適宜移動させ高パワーのレーザ光を短時間させることにより、試料プレート3上の所定位置に照射痕を形成する。照射痕は固有の形状を有するから、照射痕の顕微観察画像を取得しこれを画像保存部32に保存しておく。一旦ステージ2上から取り出された試料プレート3が再びステージ2上に置かれたあと、その時点で得られる画像上の照射痕の位置と保存部32に保存されている画像上の照射痕の位置との相違から位置ずれ量を算出し、分析位置補正部24は求まったずれ量に応じて分析者により指定された領域の位置情報を修正する。
(もっと読む)
質量分析装置
【課題】高いイオン輸送効率を示すファンネル構造の電極部にイオンを導入する効率を高めることで、総合的な輸送効率一層高める。
【解決手段】大気圧下で試料のイオン化を行うイオン化室1から、直管状のキャピラリ管3を通してイオンを、第1中間真空室4内に配置されたファンネル構造の電極部10の内部空間に導入する。複数のリング電極の一部を、周方向に一部を切り欠いた略C形状の電極に置き換えることでキャピラリ管3を配設する空間を確保し、イオンの導入方向をイオン輸送方向と略直交させる。導入されたイオンは衝突冷却によりエネルギーを減じ、高周波電場の閉じ込め作用によりイオン光軸C近傍に収束し、直流電場の電位勾配に従って出口開口に向かって効率良く移動する。ガス流はリング電極間の空隙を抜けるのでリング電極内空間の出口付近のガス圧が高くならず、後段の真空を損なうことも防止できる。
(もっと読む)
リン脂質プロファイリング及びガン
一般に本発明は、リン脂質プロファイリングを利用することにより、患者における腫瘍の脂質生成性を決定するための予後的及び予測的方法ならびにキットを提供し、ここでポリ−不飽和リン脂質種における相対的な減少と組み合わされたモノ−不飽和リン脂質種における相対的な増加は、より耐性且つ侵略的な脂質生成性ガン表現型に関する指標である。 (もっと読む)
変形性関節症の進行し易さの検出方法
【課題】簡便に調製できるサンプルを用いて、変形性関節症の進行し易さを検出する方法、及び該方法に用いるキットを提供すること。
【解決手段】工程A:被検者由来の血液、血清及び血漿からなる群より選択される少なくとも1つの生体試料において、クラスタリン(Clusterin)、アファミン(Afamin)、ヘモペキシン(Hemopexin)、肝細胞成長因子様タンパク質(Hepatocyte growth factor-like protein)、及びアルファ1−酸性糖タンパク質2(α1-acid glycoprotein 2)からなる群より選択される、少なくとも1種類のタンパク質量を測定する工程、ならびに、工程B:工程Aで得られた被検者由来の生体試料における前記タンパク質量を基準値と対比することにより、被検者の変形性関節症の進行し易さを検出する工程、を含む変形性関節症の病態の進行し易さを検出するための方法。
(もっと読む)
水素−重水素交換が組み込まれた質量分析計
【解決手段】水素−重水素交換セルを備える質量分析計を開示する。イオンが水素−重水素交換を受けることにより、立体配座が異なる一方でイオン移動度がほぼ等しい異性体イオンを識別することが可能になる。水素−重水素交換の相対的な度合いを求めることにより、イオン移動度がほぼ等しい2つのイオンが異なる表面立体配座を持つ場合には、これら2つのイオンをより効果的に識別することができる。 (もっと読む)
有機高分子の分析方法
【課題】有機高分子に化学修飾剤を反応させて化学修飾することにより、有機高分子中の官能基数を決定する方法であって、有機高分子と化学修飾剤との反応効率が高く、また、共存する他の官能基含有低分子化合物類の影響を受けることなく、容易かつ的確に有機高分子の官能基数を決定することができる、利便性の高い有機高分子の分析方法を提供する。
【解決手段】水酸基、アミノ基、又はチオール基からなる群より選ばれるいずれか一種以上の官能基を有する有機高分子中の該官能基数を決定するに当たり、該有機高分子を、フッ素原子で置換されていても良い脂肪酸無水物で化学修飾し、得られた化学修飾体の質量分析を行って、化学修飾前の有機高分子の質量との差から該官能基数を決定する。
(もっと読む)
放射性元素検出用化合物及びこれを利用する放射性元素検出用器具並びに放射性元素検出方法
【課題】廃液の発生量を大幅に抑制できるようにする。
【解決手段】下記の一般式(1)で表される放射性元素検出用化合物を表面に反応させて結合させた保持部12を有する金属の基板11からなる放射性元素検出用器具10に試料を滴下した後、赤外光を照射して反射した赤外光を計測することにより、UやPuを検出する。ただし、式(1)において、A1〜A3のうちの少なくとも一つは、−SH,−PH2,−NH2のうちのいずれかの連結基であり、残りは、−Hであり、R1〜R4は、連結基が結合しているとき、炭素数4〜18のアルキレンであり、連結基が結合していないとき、炭素数0〜18のアルキレンである。
【化1】 (もっと読む)
(もっと読む)
質量分析方法及び質量分析装置
【課題】シアル酸等、脱離し易い修飾物が結合した糖鎖、ペプチドをMSn分析する際に、得られるマス(MSn)スペクトルの感度を高めることで構造解析の精度を向上させる。
【解決手段】分析対象の化合物Aから生成された各種イオンをイオントラップ内に捕捉した後に、質量選別を行うことなく(シアル酸が脱離したイオンを捕捉したまま)[M+H]+に対するCIDを実行する。これにより、1個のシアル酸が脱離した[M−Sia+2H]+が増加するから、次に質量選別を行うことなく[M−Sia+2H]+に対するCIDを実行する。このようにして全てのシアル酸が脱離した[M−3Sia+4H]+を増量した後に、該イオンに対する質量選別及びCIDを実行し、該イオンに由来する各種プロダクトイオンを生成させてそれを質量分析・イオン検出する。従来手法では分析に使用されていないイオンがマススペクトルに反映されるため高感度となる。
(もっと読む)
インスリン様増殖因子1受容体(IGF−1R)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にIGF−1Rタンパク質を定量するための特に好都合な、インスリン様増殖因子1受容体(IGF−1R)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、IGF−1Rタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。IGF−1Rペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
81 - 100 / 799
[ Back to top ]