Fターム[2G041EA04]の内容
その他の電気的手段による材料の調査、分析 (22,023) | 試料形態 (2,319) | 液体、流動体 (1,103) | 液体クロマト溶出液 (749)
Fターム[2G041EA04]に分類される特許
101 - 120 / 749
質量分析装置
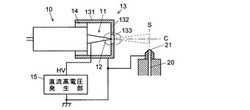
【課題】ESIイオン源において噴霧口近傍での電場強度を高めるとともに、生成された微細帯電液滴やイオンをイオン取り込み口まで移動させる効率を高めることで検出感度の向上を図る。
【解決手段】イオン化プローブ10のノズル11の先端に設けられた電極12の周囲を包囲するように、円筒部131と円板部132が一体化されたカバー電極13を設け、円板部132にあって中心軸Cと同軸の開口133を通して液体試料を噴霧する。カバー電極13の電位をイオン取り込み口と同じ接地電位とすることで、カバー電極13とイオン取り込み口21との間の空間をほぼ一様にゼロ電位とし、カバー電極13で囲まれる空間と噴霧口113付近に強い電場を形成する。これにより、帯電液滴の生成効率が上がるとともに、帯電液滴やイオンの移動に対する電場の悪影響がなくなるので、効率よく微細帯電液滴やイオンがイオン取り込み口まで輸送される。
(もっと読む)
多重タンデム質量分析法
本発明は、少なくとも2つの前駆体を含む被分析試料の多重タンデム質量分析方法に関する。少なくとも2つの単純化された多重MS-MSスペクトルの各々は、前記試料の少なくとも2つの選ばれた前駆体から得られる。当該方法は:各選ばれた前駆体について、前記単純化された多重MS-MSスペクトルのフラグメントイオンを選ぶことによって、前記単純化された多重MS-MSスペクトルから個々のMS-MSスペクトルを生成する手順であって、前記フラグメントイオンは前記前駆体から得られる可能性のあるフラグメントイオンである、MS-MSスペクトル生成手順;前記MS-MSスペクトル生成手順の個々のMS-MSスペクトルを、スコア閾値条件又は低スコア閾値条件が存在しないスコアリング処理を用いることにより現実のデータベース及び囮のデータベース検索へ提出することで、候補となる前駆体及び該前駆体のフラグメントイオンを同定するデータベース検索提出手順;前記データベース検索提出手順の現実のデータベース検索の結果同定された候補となる前駆体から現実の個々のMS-MSスペクトルを生成する現実のMS-MSスペクトル生成手順;前記データベース検索提出手順の囮のデータベース検索の結果同定された候補となる前駆体から囮の個々のMS-MSスペクトルを生成する囮のMS-MSスペクトル生成手順;並びに、前記現実の個々のMS-MSスペクトル及び囮の個々のMS-MSスペクトルを、スコア閾値条件が存在する他のスコアリング処理へ提出することで、現実の個々のMS-MSスペクトル及び囮の個々のMS-MSスペクトルについてのスコアを決定する手順を有する。 (もっと読む)
フルオラス化シアル酸誘導体およびその分析方法
【課題】LC-MS/MS法で検出するフルオラス化シアル酸誘導体の検出方法を提供する。
【解決手段】一般式[I]: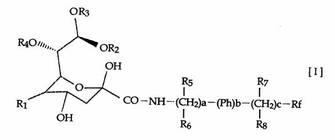
{式中、R1は、グリコリル基など、R2、R3及びR4は、水素原子など、aは1〜3の整数、bは0または1の整数、cは1〜3の整数、Rfは一般式[II]:
(式中、R9およびR10は、水素原子またはフッ素原子、dは4〜10の整数を意味する。)で表されるフルオロアルキル基を意味する。}で表されるフルオラス化シアル酸誘導体は、LC-MS/MS法で検出することができる。
(もっと読む)
心疾患マーカーとしての尿中トリアオシルセラミド(GB3)
本発明は、非ファブリー病の心疾患患者の尿中グロボトリアオシルセラミド(Gb3)レベルを判定する方法について記載する。Gb3レベルの判定により、心臓疾患のリスクを判定するスクリーニング方法を提供し、薬学的シャペロン又は他の薬剤を使用してGb3レベルを低減させることによって、心疾患の管理又は心疾患のリスクの軽減に対する代替的な治療の選択肢を提供することができるかもしれない。 (もっと読む)
四重極質量分析装置におけるスペクトル信号補正方法
【課題】四重極質量分析装置におけるスペクトル信号補正方法に関し、スキャンサイクル中に適宜ノイズを測定し、データ処理に反映させることを目的としている。
【解決手段】分子、原子等の粒子をイオン化し、イオン化した粒子を4重極マスフィルタを通したものを検出器で検出し、検出した信号をコンピュータで演算処理し、MSスペクトルを得るようにした四重極質量分析装置において、MSスペクトル採取におけるサイクル中に、ノイズを検出する工程を設け、MSスペクトル採取におけるイオン検出信号と、前記検出されたノイズとを比較してスペクトル補正を行なうように構成する。
(もっと読む)
胆道がんの新規バイオマーカー
【課題】胆道がんと関連する新規バイオマーカーの検出に、質量分析を使用する方法を提供する。
【解決手段】被験体における胆道がんと関連する異常量のバイオマーカーを検出する方法であって、a)質量分析を使用して該被験体由来の生物学的試料における約4204m/zのm/z値を有するプロトロンビンの断片の量を定量化すること、及びb)(a)において取得した定量化した値を閾値と比較することを含み、ここで該定量化した値が該閾値を上回る場合異常量の該バイオマーカーが該生物学的試料中に存在する、方法。
(もっと読む)
液体クロマトグラフィーを用いたビタミンUの精製および分析法
【課題】試料中に含まれるVUを精製および分析する方法の提供。
【解決手段】植物由来の試料中に含まれるビタミンU(VU)を液体クロマトグラフィーにより精製する方法であって、該液体クロマトグラフィーが親水性相互作用クロマトグラフィー用カラムを用いることを特徴とする。該親水性相互作用クロマトグラフィー用カラムが、エチレン架橋型親水性相互作用クロマトグラフィー用カラムであって、好ましい該親水性相互作用クロマトグラフィー用カラムは、XBridgeTMHILICカラムである。
(もっと読む)
感染症の疾患マーカー
【課題】感染症、特に敗血症を迅速且つ早期に診断することのできるツールを提供すること。
【解決手段】本発明は、ペントラキシン3及びアズロシジンを含んでなる、感染症の疾患マーカーを提供する。また、被験動物より採取した試料におけるペントラキシン3及びアズロシジンの有無又はその量を調べる工程を含む、感染症の罹患の有無の検出方法及び感染症の罹患の有無と感染症の病原菌との同時検出方法を提供する。さらに、抗ペントラキシン3抗体が結合した磁性粒子、並びにペントラキシン3及びアズロシジンを検出し得る物質を含有してなる、感染症の診断用キットを提供する。
(もっと読む)
肝実質細胞中のP450タンパク質のアイソフォームの質量分析による定量
チトクロームP450(CYP)誘導について薬物をスクリーニングする方法を提供する。この方法は、薬物を、ミクロソームを含む生物学的サンプルとインキュベートし、次いで少なくとも1つのチトクロームP450アイソフォームを定量することを含んでもよい。アイソフォームは、2B6アイソフォーム、3A4アイソフォーム、1A2アイソフォームおよび3A5アイソフォームから選択することができる。いくつかの実施形態では、この方法は、液体クロマトグラフィー/タンデム質量分析法(LC−MSMS)を使用する。定量された値は、閾値と比較してもよく、定量された値が閾値を超えない場合、薬物を許容可能なCYP誘導能を示すものと決定することができる。また、単離されたペプチドも提供する。  (もっと読む)
(もっと読む)
質量分析によって少なくとも一つの微生物を特徴づける方法
本発明は、少なくとも一つの微生物を同定して、タイピング、少なくとも一つの抗菌物質に対する潜在的耐性および毒性因子の特性を決定することを含む、試料から少なくとも一つの微生物を特徴づける方法であって、前記少なくとも一つの微生物についてタイピング、少なくとも一つの抗菌物質に対する耐性、および毒性因子の特性を決定することが、タイピング、少なくとも一つの抗菌物質に対する耐性および毒性因子の前記特性のマーカーとして、タンパク質、ペプチドおよび/または代謝産物を使用する質量分析によって実施することを特徴とする、方法に関する。 (もっと読む)
イオン源および電子源のためのアセンブリならびに使用方法
本明細書中に記載の特定の実施形態は、源アセンブリの構成要素を源ハウジング内に整列させる際に利用することが可能なデバイスに関する。いくつかの例において、各整列フィーチャを通じて前記ハウジングに接続するように構成された終端レンズを用いて、前記源ハウジング内の源構成要素を保持して、源アセンブリを提供することができる。 (もっと読む)
署名ペプチドおよび質量分析による混合物中の個々の組換えタンパク質の多重定量化
本発明は、複雑なマトリックス中の選択された複数の組換えタンパク質、例えば血清中の組換えポリクローナル抗体または培養上清中に発現される組換えポリクローナル抗体の定量化のための分析方法に関する。 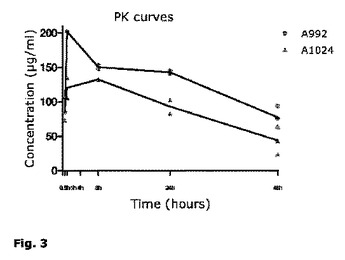 (もっと読む)
(もっと読む)
薬物誘導性の心毒性の代謝バイオマーカー
本発明は、医薬品、環境要因、化合物および生物療法に対する心臓代謝応答を評価するための方法およびバイオマーカーを提供する。本発明は、心毒性である医薬品、環境要因、化合物および生物療法への露出に応答して、初代心筋細胞、心筋細胞前駆細胞、成人の心臓に由来するクローン心筋細胞、不死化心筋細胞、ヒト胚性幹細胞(hESC)由来の心筋細胞、ヒト誘導多能性幹細胞(iPS)由来の心筋細胞、または心筋細胞特異的マーカーを示すあらゆる細胞によって分泌される細胞代謝産物を同定するための方法を提供する。心筋細胞によって分泌される細胞代謝産物は心毒性の代謝サインを提供し、医薬品、鉛化合物および候補薬物化合物、生物製剤、ならびにその他の治療法の心毒性の影響をスクリーニングするために使用され得る。 (もっと読む)
膵臓癌の血清ベースのバイオマーカー並びに疾患検出及び診断のためのその使用
膵臓癌のバイオマーカー並びにこれらの化合物を使用して膵臓癌を検出するための方法が記載される。本方法を使用して、患者の健康状態若しくは健康状態の変化を診断するか、又は膵臓癌を発症するリスク若しくはその存在を診断することができる。本方法は、患者由来の試料を分析して、1種又は2種以上の代謝産物マーカーの定量化データを得ることと、かかる定量化データを、1種又は2種以上の参照試料について得られた対応するデータと比較して、試料中の代謝産物マーカー(単数又は複数)のレベルの異常を同定することと、異常が観察される場合には診断を行うこととを含む。本方法を実施するための標準物質及びキットも記載される。 (もっと読む)
複雑な混合物における小分子成分分析のための装置及び関連する方法
方法、装置、及びコンピュータ可読記憶媒体を、成分分離/質量分析計(CS−MS)からのデータを分析するために提供し、各二次元データセットにおける統合手順を使用して決定されたその領域を用いて、強度ピークを決定する。強度ピークは、サンプル成分、及び前記サンプル成分の相対量を示す、その領域を示す。統合手順は、第1のサンプル成分に関する二次元データセットの第1の部分の選択されたピークの領域を決定し、第1の部分のサンプルにおける第1のサンプル成分の相対量に対して相対的な、第2のサンプルにおける前記第1のサンプル成分の相対量を調整するために、その統合手順によって決定されないその領域を有する第2の部分の強度ピークへ適用される。再統合はまた、第2のサンプル成分が、前記強度ピークによって示されたかどうかを決定することも、含み得る。 (もっと読む)
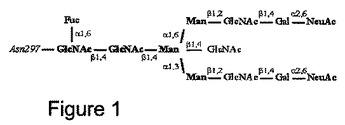
抗体における非フコシル化の検出法
本発明は、抗体調製物内のFcあたりのフコースの量および分布を決定するための新規の分析方法を記載する。
 (もっと読む)
(もっと読む)
質量標識体
質量分析によって検出するために生体分子を標識するための反応性質量標識体であって、チオール基又はカルボニル基を標識するための反応性官能基を含む反応性質量標識体。また、質量分析によって検出するために生体分子を標識するための反応性質量標識体であって、以下の構造を含む質量標識体を提供する。
X−L−M−S−Re
(式中、Xは、質量マーカー部分であり、Lは、開裂可能リンカーであり、Mは、質量正規化部分であり、Sは、以下の基:式(I)を含む質量系列修飾基であり、Reは、前記質量標識体を前記生体分子に結合させるための反応性官能基である
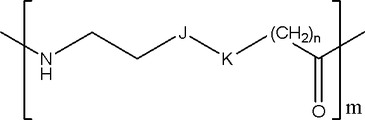
式(I)
(式中、JはC=Oであり、KはNHであり、且つnは2であるか、又はJ及びKは両方ともCH2であり、且つnは1であり;mは、少なくとも1である))
(もっと読む)
質量分析による分子の検出方法
【課題】質量分析による分子の検出方法の提供。
【解決手段】本発明は、サンプル中の少なくとも1種の標的分子を質量分析によって検出するための方法であって、
a)上記サンプルの上記分子をイオン化する工程と、
b)以下の工程(i)及び(ii):
(i)上記工程で得られたイオンを少なくとも1種、上記標的分子に基づいて質量分析計において選択する工程、及び、
(ii)こうして選択されたイオンを断片化セルにおいて断片化する工程
をn回(nは0、1、2、3又は4)行う工程と、
c)nが0の場合には工程a)で、又は、nが0でない場合には工程b)で得られた少なくとも2種類の異なるイオンであって、上記標的分子に特有の質量電荷比m/zを有する少なくとも2種類のイオンを質量分析計において捕捉する工程と、
d)こうして捕捉された特有のイオンを上記質量分析計から放出する工程と、
e)こうして放出された特有のイオンを検出器で検出する工程と
を含む方法に関する。本発明の方法は、上記特有のイオンが、工程d)において同時に放出され、工程e)において同時に検出されることを特徴とする。
(もっと読む)
分析装置制御システム及び該システム用プログラム
【課題】参照用クロマトグラムを基準として一又は複数の測定を実行するような、クロマトグラフと接続された分析装置において、分かりやすく且つ簡潔に測定条件を設定することができる分析装置制御システムを提供する。
【解決手段】予め用意されている参照用クロマトグラムを表示部14に表示するクロマトグラム表示部31と、表示されている参照用クロマトグラムに対し、測定を実行する一又は複数の時間範囲をそれぞれ範囲バーとして視覚的に重畳して表示する時間範囲表示部32と、ユーザによる指示に基づき、範囲バーの時間的位置や長さを変更する範囲変更部33と、範囲変更部33による範囲バーの時間的位置や長さの変更に基づき、範囲バーに対応する測定の時間範囲を再設定する測定時間再設定部34と、を備えたシステムとする。
(もっと読む)
クロマトグラフ用データ処理装置
【課題】多成分のスクリーニングを行う場合に、各ピークのSN比を計算するために用いるノイズ値を計算する区間の面倒な設定作業を自動化し、スループットの向上を図るとともに判断のばらつきを回避する。
【解決手段】オペレータはノイズ算出区間を探索する探索時間範囲とノイズ時間幅とを化合物毎に設定しておく。化合物のピークSN比を計算する際には、探索時間範囲内でノイズ時間幅をもつノイズ算出区間を1測定点ずつずらしつつ該区間に含まれるデータからノイズ値を計算し、探索時間範囲内で最小のノイズ値を与える区間を探索してノイズ値を取得する(S11〜S18)。化合物毎にピークの信号値とノイズ値を求め、それからSN比を計算してSN比を用いてその化合物の含有の有無を判断する。
(もっと読む)
101 - 120 / 749
[ Back to top ]