Fターム[2G041GA09]の内容
その他の電気的手段による材料の調査、分析 (22,023) | 装置部品 (5,630) | 質量分析部 (4,146) | タンデム、MS/MS (789)
Fターム[2G041GA09]の下位に属するFターム
MSn(n>2) (179)
Fターム[2G041GA09]に分類される特許
81 - 100 / 610
ビタミンD3、ビタミンD2、およびこれらの代謝体の定量分析
ビタミンD2、ビタミンD3、ならびにビタミンD2およびビタミンD3のモノヒドロキシおよびジヒドロキシ代謝体の定量は、分析物をマススペクトロメトリー(MS)タグ化試薬で標識し、かつ標識分析物のLC−MSMS分析を行なうことを含むことができる。標識分析物は、標識標準を含むことができ、かつ逆相カラムでの異なる保持時間、および異なる質量を有することができる。高エネルギー衝突下で、レポーター基を発生させることができる。各々のレポーター基について検出される強度またはピーク面積を定量に用いることができる。いくつかの実施形態では、ジエノフィルを含有する標識ディールス・アルダー試薬である1段階タグ化試薬を用いる。 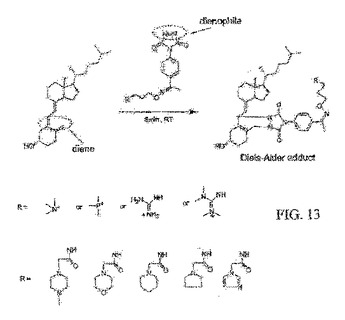 (もっと読む)
(もっと読む)
小分子の同時的な定量および同定のための質量タグ試薬
質量タグを分析物にコンジュゲートし、タンデムマススペクトロメトリーフラグメンテーション(MS−MSまたはMS2)後に、質量タグのシグナチャーイオンが分析物に付着したまま残る、分子の同定方法および定量方法を提供する。シグナチャーイオンを失うのではなく、構造物の質量バランス部分を、タンデムマススペクトロメトリーフラグメンテーションの下で、電荷中性基として失わせることができる。このシグナチャーイオンを定量に用いることができ、さらなるフラグメンテーションによって、分析物の特徴を示し、かつ分析物の同定に有用なイオンシグナルを提供することもできる。いくつかの実施形態では、3回目のマススペクトロメトリーフラグメンテーション(MS3)から生成されたイオンシグナルを、例えば、検索表、ライブラリー、またはデータベースからの既知のマススペクトルと比較して、分析物の一義的な同定を提供することができる。 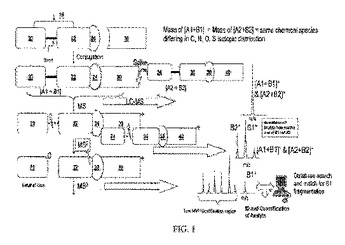 (もっと読む)
(もっと読む)
インスリン様増殖因子1受容体(IGF−1R)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にIGF−1Rタンパク質を定量するための特に好都合な、インスリン様増殖因子1受容体(IGF−1R)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、IGF−1Rタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。IGF−1Rペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
インスリン受容体基質1(IRS1)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にIRS1タンパク質を定量するための特に好都合な、インスリン受容体基質1(IRS1)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、IRS1タンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。IRS1ペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
酸性およびシステインに富む分泌(SPARC)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にSPARCタンパク質を定量するための特に好都合な、酸性およびシステインに富む分泌(SPARC)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、SPARCタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。SPARCペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
上皮成長因子受容体(EGFREGFR)タンパク質SRM/MRMアッセイ
本開示は、選択反応モニタリング(SRM)質量分析、または多重反応モニタリング(MRM)質量分析とも名付けられてもいる方法により、ホルマリン中で固定された生物検体中で直接的にEGFRタンパク質を定量するための特に好都合な、上皮成長因子受容体(EGFR)タンパク質由来の特異的ペプチド、および生成されるペプチドのイオン化特性を提供する。このような生物検体は、化学的に保存および固定され、前記生物検体は、ホルマリン固定組織/細胞、ホルマリン固定/パラフィン包埋(FFPE)組織/細胞、FFPE組織ブロックおよびこれらのブロック由来の細胞、ならびにホルマリン固定および/またはパラフィン包埋されている組織培養細胞を含む試薬/固定液を含むホルムアルデヒドで処理した組織および細胞から選択される。タンパク質検体は、前記生物検体からLiquid Tissue(登録商標)試薬およびプロトコルを使って調製され、EGFRタンパク質が、SRM/MRM質量分析法を使って、Liquid Tissue(登録商標)検体中でタンパク質検体中の少なくとも1つ以上の記載ペプチドを定量することにより定量化される。これらのペプチドが修飾または非修飾型で存在する場合は、定量化可能である。EGFRペプチドの修飾型の一例は、ペプチド配列内のチロシン、トレオニン、セリン、および/または他のアミノ酸残基のリン酸化である。 (もっと読む)
前立腺癌の代謝学的プロファイリング
本発明は、癌マーカーに関するものである。特に本発明は、癌(例えば、前立腺癌または乳癌)において特異的に存在する代謝物および代謝物パネルを提供する。 (もっと読む)
質量分析装置及び質量分析方法
【課題】 従来技術に比べ、小型・簡便な構成で耐久性と分解能を両立する。
【解決手段】 電子又はイオンを通過させる細孔を有するロッド電極を含む多重極ロッド電極を有するリニアイオントラップ部と、前記リニアイオントラップ部内のイオンを前記多重極ロッド電極の軸方向に移動させる機構と、前記リニアイオントラップ部から質量選択的に排出されるイオンを検出する検出器とを有することを特徴とする質量分析装置。
(もっと読む)
プラズマローゲンの分析方法
【課題】本発明の目的は、プラズマローゲン分析における内部標準として用いることのできる新規化合物、及び前記化合物を用いる精確なプラズマローゲン分析方法を提供することである。
【解決手段】前記課題は、一般式(1)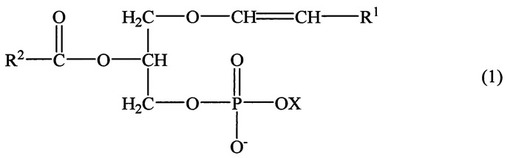
(式中、R1は、炭素数7、9、11、13、15、17、19、又は21のアルキル基であり、R2は、炭素数8〜21のアルキル基又はアルケニル基であり、Xは、CH2CH2N(CH3)3、又はCH2CH2NH2である)で表される化合物を、内部標準化合物として用いるプラズマローゲン分析方法によって解決することができる。
(もっと読む)
タグ付け試薬およびLC−MSワークフローを用いた、アミノ酸およびアミン含有化合物の分析
複数の質量差タグ付け試薬を使用して、アミン含有化合物中のアミン官能基を標識する。標識された分析物は、逆相カラム上の明確な保持時間、及び明確な質量を有する。高エネルギー衝突下では、レポーター基を生成することができ、各レポーター基に対して検出された強度又はピーク面積を定量化に使用することができる。試薬の例示的な1セットは、それぞれ(113、117及び121)原子質量単位のレポーター基を有する、それぞれ(140)原子質量単位、(144)原子質量単位及び(148)原子質量単位のタグ付け重量を有する、3種類の質量差試薬からなる1セットを含む。質量差試薬の各々を含むパッケージも提供され、パッケージは、個別の容器、例えば、異なる試薬の各々に対する容器を含むことができる。パッケージは、それぞれ既知濃度のそれぞれ既知のアミン含有化合物を各々含む、1種類以上の標準物質を含むこともできる。 (もっと読む)
イオンを処理する方法
高エネルギー、中エネルギー、低エネルギーの生成物イオンの混合物を含む生成物イオンスペクトルをもつフラグメントイオンを得る方法。この方法は、(a)イオン封込場の上流にあるイオン光学素子に、選択したRF場を提供することと;(b)選択したRF場が、イオン封込場内にあるイオンの選択した運動エネルギープロファイルを少なくとも部分的に決定するように、このイオン光学素子を通ってイオン封込場へとイオンを移動させ、この選択した運動エネルギープロファイルが、イオンをフラグメント化するとともに複数の生成物イオン群を与えるように選択されることと;(c)この複数の生成物イオン群のそれぞれの生成物イオン群を検出することとを含む。  (もっと読む)
(もっと読む)
非誘導体化非代謝化ビタミンDの質量分析法による決定
本発明は、非代謝化ビタミンDの検出に関する。特定の態様では、本発明は、非誘導体化非代謝化ビタミンDを質量分析法により検出するための方法に関する。 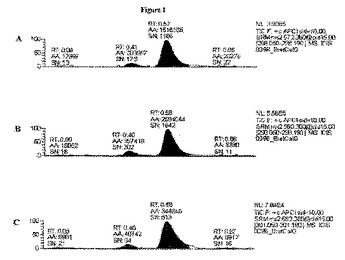 (もっと読む)
(もっと読む)
複合試料中のステロイド化合物の質量分析
本発明は、質量分析によるステロイド化合物の定量的測定に関する。特定の態様において、本発明は、質量分析による複数の試料からのステロイド化合物の定量的測定の方法に関する。 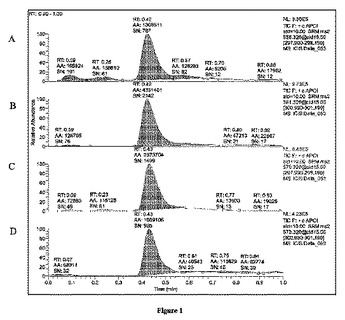 (もっと読む)
(もっと読む)
質量分析装置およびこれを用いる計測システム
【課題】実用的なプロテオーム解析用質量分析装置を提供する。
【解決手段】直交加速型イオントラップ結合飛行時間型質量分析計において、イオントラップから射出されたイオンの速度分布を縮小する手段を設けることにより、一度に分析できる質量対電荷比範囲を拡大する。
【効果】プロテオーム解析におけるタンパク同定の効率が向上される。
(もっと読む)
界面活性剤分析法
【課題】界面活性剤中の無機物イオン、とりわけ有機スルホン酸イオンの硫酸イオンの定量分析を高感度および高精度で行う手法を提供する。
【解決手段】有機スルホン酸塩などの界面活性剤中の無機物イオン、例えば、硫酸イオンの定量分析において、ESI(Electrospray Ionization)-MS(Mass Spectrometry)分析法を用い、メタノール・水混合溶液に試料を溶解し、内部標準添加法による所定濃度調製により無機物イオンを高感度および高精度分析法が可能となる。
(もっと読む)
ペプチド末端の同定方法
【課題】蛋白質のアミノ末端およびカルボキシ末端を、網羅的かつ簡便に決定する方法の提供。
【解決手段】(a)対象ポリペプチド中の1種のアミノ酸残基のアミノ末端側又はカルボキシ末端側の一方で切断したペプチド断片群の取得工程;(b)対象ポリペプチドと同一のポリペプチド中に含まれるアミノ酸残基と同一のアミノ酸残基について、工程(a)で切断した末端と逆側の末端で切断したペプチド断片群の取得工程;(c)工程(a、b)で得た二つのペプチド断片群の質量分析スペクトルの取得工程;(d)工程(c)の質量分析スペクトルから、質量差のあるピークの組を抽出する工程;(e)工程(d)で抽出されたピークの組について、各ピークの質量差、又は、各ピークのフラグメントの質量分析結果から、ピークの組が、対象ポリペプチドのアミノ末端、又は、カルボキシ末端を含むポリペプチドであると判断する工程;により、ポリペプチド末端を同定する。
(もっと読む)
多重タンデム質量分析法
本発明は、少なくとも2つの前駆体を含む被分析試料の多重タンデム質量分析方法に関する。少なくとも2つの単純化された多重MS-MSスペクトルの各々は、前記試料の少なくとも2つの選ばれた前駆体から得られる。当該方法は:各選ばれた前駆体について、前記単純化された多重MS-MSスペクトルのフラグメントイオンを選ぶことによって、前記単純化された多重MS-MSスペクトルから個々のMS-MSスペクトルを生成する手順であって、前記フラグメントイオンは前記前駆体から得られる可能性のあるフラグメントイオンである、MS-MSスペクトル生成手順;前記MS-MSスペクトル生成手順の個々のMS-MSスペクトルを、スコア閾値条件又は低スコア閾値条件が存在しないスコアリング処理を用いることにより現実のデータベース及び囮のデータベース検索へ提出することで、候補となる前駆体及び該前駆体のフラグメントイオンを同定するデータベース検索提出手順;前記データベース検索提出手順の現実のデータベース検索の結果同定された候補となる前駆体から現実の個々のMS-MSスペクトルを生成する現実のMS-MSスペクトル生成手順;前記データベース検索提出手順の囮のデータベース検索の結果同定された候補となる前駆体から囮の個々のMS-MSスペクトルを生成する囮のMS-MSスペクトル生成手順;並びに、前記現実の個々のMS-MSスペクトル及び囮の個々のMS-MSスペクトルを、スコア閾値条件が存在する他のスコアリング処理へ提出することで、現実の個々のMS-MSスペクトル及び囮の個々のMS-MSスペクトルについてのスコアを決定する手順を有する。 (もっと読む)
フルオラス化シアル酸誘導体およびその分析方法
【課題】LC-MS/MS法で検出するフルオラス化シアル酸誘導体の検出方法を提供する。
【解決手段】一般式[I]: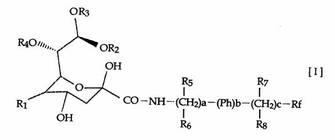
{式中、R1は、グリコリル基など、R2、R3及びR4は、水素原子など、aは1〜3の整数、bは0または1の整数、cは1〜3の整数、Rfは一般式[II]:
(式中、R9およびR10は、水素原子またはフッ素原子、dは4〜10の整数を意味する。)で表されるフルオロアルキル基を意味する。}で表されるフルオラス化シアル酸誘導体は、LC-MS/MS法で検出することができる。
(もっと読む)
イオントラップ質量分析装置
【課題】イオン捕捉用の高周波電場をイオントラップ内に形成するためにリング電極に矩形波電圧を印加するデジタルイオントラップを用いた質量分析装置において、MSn分析の際に生成される低質量のプロダクトイオンを的確に捕捉し検出可能とする。
【解決手段】MSn分析において、低質量のプロダクトイオンが生成される開裂操作(S16)の前にリング電極に印加されるイオン捕捉用の矩形波電圧の振幅を下げる(S10)。矩形波電圧の振幅を下げることにより安定捕捉条件を満たす最小質量が下がり、低質量のプロダクトイオンも捕捉可能となる。一方、イオントラップに捕捉されるイオンのm/zが比較的高い状態のとき(S1〜S7)には、矩形波電圧の振幅は大きいので擬電位ポテンシャルは深く、高い効率でイオンを捕捉することが可能である。
(もっと読む)
心疾患マーカーとしての尿中トリアオシルセラミド(GB3)
本発明は、非ファブリー病の心疾患患者の尿中グロボトリアオシルセラミド(Gb3)レベルを判定する方法について記載する。Gb3レベルの判定により、心臓疾患のリスクを判定するスクリーニング方法を提供し、薬学的シャペロン又は他の薬剤を使用してGb3レベルを低減させることによって、心疾患の管理又は心疾患のリスクの軽減に対する代替的な治療の選択肢を提供することができるかもしれない。 (もっと読む)
81 - 100 / 610
[ Back to top ]