Fターム[2G045FA40]の内容
生物学的材料の調査、分析 (60,403) | 測定の操作、検知手段(物理的) (4,180) | その他 (100)
Fターム[2G045FA40]に分類される特許
21 - 40 / 100
リガンド発見のための方法
【課題】結合技術を使用してリガンドを発見すること。
【解決手段】本発明は、リガンド発見のための新規の方法を開示する。本発明の方法は、「結合(tethering)」と称されるプロセスに依存し、ここで、潜在的なリガンドが、標的に共有結合されるか、または「結合」され、引き続き同定される。ほ1つの実施形態において、本発明は、標的−化合物結合体を提供する。1つの実施形態において、この標的は、酵素、レセプター、転写因子、レセプターに対するリガンド、増殖因子、サイトカイン、免疫グロブリン、核タンパク質、シグナル伝達成分、およびアロステリック酵素調節因子からなる群より選択される。
(もっと読む)
サンゴの光合成活性評価装置
【課題】電場が形成された環境において、サンゴの光合成活性を評価すること。
【解決手段】サンゴの光合成活性評価装置1は、海水W及びサンゴCを内部に閉じ込める試験容器2の内部に、陽極5と陰極6とが突出する。陽極5と陰極6とは、電源3に接続される。陽極5は、海水Wが満たされた電極格納容器20内に格納される。また、電極格納容器20の陽極5が配置される側の海水Wと、試験容器2の内部においてサンゴCが配置される部分の海水Wとは、導電性を有する電極隔離体21で仕切られている。
(もっと読む)
呼気判定装置
【課題】呼気の替わりに、呼気以外のガスが吹きかけられる場合であっても、判定対象の気体中に呼気が含まれるか否かを精度よく判定することができるようにする。
【解決手段】気体中の二酸化炭素の濃度及び酸素の濃度を算出し(350、352)、算出された二酸化炭素の濃度が、所定の濃度範囲外であるか、又は、算出された算出された酸素の濃度が、所定の濃度範囲外である場合には、気体中に呼気が含まれていないと判断する(104、354)。そして、二酸化炭素の濃度及び酸素の濃度が、所定の濃度範囲内である場合には、二酸化炭素の濃度及び酸素の濃度の各々に基づいて、呼気希釈率を各々算出し(356)、算出された2つの呼気希釈率の比が、1を含む許容範囲内である場合には、呼気希釈率がほぼ一致し、気体中に呼気が含まれていると判断する(358)。
(もっと読む)
マイクロサンプルの液相の自動抽出のためのシステムおよび方法、ならびにマイクロサンプルを採取し、抽出を実行し、測定を行うための自動設備
本発明は、特に、空間および時間の両方において不連続なパケットとして事前に採取されて保管された一連の液体マイクロサンプルの少なくとも1つの液相を物理的に抽出するための連続自動抽出システムおよび方法に関する。本発明による抽出システム(10)は、複数のマイクロホルダ(12)を有する遠心分離器(13)を備えており、前記マイクロホルダの少なくとも1つが、該当のマイクロサンプルで満たされるとともに、分離用の下部(12b)によって延長された注入用の上部(12a)を備え、前記下部(12b)の断面は前記上部(12a)の断面よりも小さい。本発明によれば、このように満たされたホルダまたは各ホルダは、所与の瞬間に、1つのマイクロホルダに収容されたただ1つのマイクロサンプル又はマイクロホルダの一部あるいは全てに収容された複数のマイクロサンプルを、マイクロホルダが満たされるにつれて徐々に遠心分離によって抽出できるという方法によって、マイクロサンプルの質量の10倍を超える質量を有している。 (もっと読む)
試料分析システム
毛髪試料分析システムであって、該システムは、容器内に位置する複数の試料列と、上記容器から個々の列を取出し、上記試料列の毛髪試料を第1概略位置に付勢する自動駆動機構と、該駆動機構を調節して前記試料をX線回折ビームと略一致させるよう配置するモニタリング及び制御システムと、を備え、上記試料を、上記X線回折ビームと略一致させるよう配置し、上記試料に上記ビームを所定時間照射し、上記毛髪試料を照射する上記ステップから得たデータを、分析するために受信し、保存し、上記試料列を、上記容器の元の位置に戻し、上記試料容器から別の列を取出し、上記ステップを連続する列に対して繰り返すこと、を特徴とする毛髪試料分析システム。 (もっと読む)
液体マトリックスを用いたMALDI質量分析による糖タンパク質又は糖ペプチドの構造解析手法
【課題】MALDI質量分析における糖タンパク質又は糖ペプチドの構造解析において、比較的均質な試料−マトリックス混合物の調製が可能で、且つ、糖ペプチドイオンのような糖−アミノ酸結合が維持されたイオンを優先的に検出することが可能な方法を提供する。
【解決手段】構造解析すべき糖タンパク質又は糖ペプチドと、マトリックスとしてのイオン性液体とを少なくとも含む混合物を、MALDI質量分析測定に供し、前記混合物中から前記構造解析すべき糖タンパク質又は糖ペプチドに由来し且つ糖−アミノ酸結合が維持されたイオンを検出することを含む、液体マトリックスを用いたMALDI質量分析による糖タンパク質又は糖ペプチドの構造解析手法。
(もっと読む)
蛍光強度解析法
【課題】蛍光基を蛋白質から除去することなく、蛋白質に存在する複数個の蛍光基Dが蛋白質の蛍光強度にそれぞれ寄与する割合を解析する方法を提供する。
【解決手段】アクセプター蛍光体Aを蛋白質に導入した変異型蛋白質M個を用いて得られる、蛍光基Dに由来するj番目(j = 1 〜 M)の変異型蛋白質の蛍光強度FDAのデータ、および、アクセプター蛍光体Aが存在しない場合の蛍光基Dに由来する蛋白質の蛍光強度FDのデータを用いて、j番目の変異型蛋白質の全蛍光基Dからアクセプター蛍光体Aへの有効蛍光共鳴エネルギー移動効率Eeff,jを求め、得られたEeff,j及び下記のデータを用いて次の式(9a)という連立一次方程式を解くことにより、fiを求める。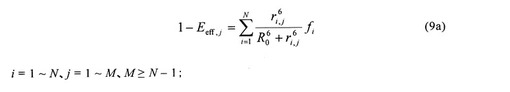
R0は蛍光基Dとそのアクセプター蛍光体Aのフェルスター距離;ri,jはi番目の蛍光基Dとj番目のアクセプター蛍光体A導入部位との距離である。
(もっと読む)
インターフェロン療法の有効性判定方法及び判定用キット
【課題】 C型肝炎患者におけるインターフェロン療法の有効性を事前に判定する。
【解決手段】 C型肝炎患者の体液中におけるマーカー物質の濃度を指標として、前記C型肝炎患者に対してインターフェロン療法が有効であるか否かを判定する。マーカー物質の濃度を測定する方法としては、イオン交換体や金属キレート体を固定化した基板等の担体にマーカー物質を捕捉し、質量分析により行なうことができる。前記マーカー物質に対する親和性を有する物質を固定化した担体を含むインターフェロン療法の有効性判定用キットによれば、より簡便かつ迅速に、C型肝炎患者に対してインターフェロン療法が有効であるか否かを判定することができる。
(もっと読む)
濾紙上のサンプル吸着を用いたスクリーニング方法
本発明は、血液又は他の生体液サンプルを試験化合物と混合し、血液又は生体液に対する試験化合物の効果を後に分析するために、該血液又は生体液を濾紙上にスポットすることを含む診断試験及び方法を開示する。生体液は、脳脊髄液、腹水、嚢胞液、羊水、唾液、細胞抽出物又は組織抽出物であってもよい。試験化合物は、血液又は生体液にその組成が変化を起こす影響を与える、アミノ酸、ペプチド、タンパク質、炭水化物、オリゴ糖、多糖、糖タンパク質、脂質、リポタンパク質、グリコサミノグリカン、ホルモン、ステロイド、ビタミン、低分子量合成又は天然化合物、例えば毒素、アレルゲン、自己抗原、細菌タンパク質若しくは多糖、ウイルスタンパク質、真菌タンパク質若しくは多糖、寄生虫タンパク質若しくは多糖、細菌リポ多糖、又は疾病に関連した任意の他の化合物の中から選択される。 (もっと読む)
扁平上皮癌危険群の呼気による簡易判定方法と装置及びそのための13Cアセトアルデヒド分別分離用チューブ
【課題】扁平上皮癌の発生危険度を判定し診断するための簡便で精度の高い検査方法とその装置を提供する。
【解決手段】一定濃度のアルコールを一定量摂取した後、呼気中のアセトアルデヒド濃度の経時変化を測定し、アセトアルデヒド濃度の急激な上昇が見られた場合や、時間経過によるアセトアルデヒド濃度の減少度が小さい場合に、扁平上皮癌発生の危険度が高いと判定する扁平上皮癌発生危険度の簡易判定方法であって、摂取するアルコールが炭素の安定同位体である13Cでラベル化されたアルコールであり、呼気中の13Cアセトアルデヒド濃度を測定する。
(もっと読む)
質量分光によるタンパク質分解処理の分析
本発明は、N末端ペプチドの同位体ラベリングに基づいて特異なタンパク質分解処理を決定するためのサンプルの同時分析に関し、同位体ラベリングが、酵素タンパク質分解の間の18Oの組込みによって達成される。例えば本発明は、同位体ラベリングを用いて2つのタンパク質サンプルを分析するための装置であって、2つのサンプルソース、修飾試剤のソースを備えたタンパク質修飾ユニット、ラベリング及びタンパク質切断ユニット及び対応するラベルソース、N末端ペプチド単離ユニット、分離ユニット、質量分光器ユニット、並びにデータ分析ユニットを有する装置である。 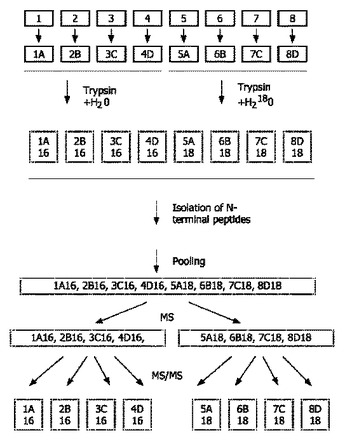 (もっと読む)
(もっと読む)
皮膚における創傷被覆材の環境模擬測定装置およびその測定方法
【課題】ヒト皮膚と創傷被覆材との間の微小空間の環境を模擬的に測定する装置およびその測定方法を提供する。
【解決手段】環境模擬測定装置は、外部環境を調節する恒温恒湿槽14、その中に設置された熱交換器12、これに温水を供給する恒温水槽10とポンプ11および熱交換器12に設置される簡単に着脱可能な容器1からなる。容器1は、保水性部材2を収容しており、その上部開口が水蒸気拡散調整部材4で覆われている。水蒸気拡散調整部材4とその上に置いた創傷被覆材5との間に生じる微小空間6は、人体と創傷被覆材5との間の空間を模擬的に再現したものである。この微小空間6内に薄型温湿度センサ7を設置して、経時的に温湿度を測定する。複数の容器1を用いれば、複数種類の創傷被覆材5を用いた測定を同時に行うことができる。
(もっと読む)
タンパク質構造解析方法、タンパク質構造解析装置、プログラム、および、記録媒体
【課題】立体構造予測結果の評価や、構造予測に有用な構造情報の提供が可能であり、高感度かつ迅速な立体構造情報の実測技術を提供することを目的としている。
【解決手段】本発明は、立体構造を予測する対象タンパク質について断片化して断片化スペクトルを測定し、測定された断片化スペクトルに基づいて、対象タンパク質のアミノ酸配列に対する断片化イオンの帰属情報を決定し、測定された断片化スペクトルおよび決定された断片化イオンの帰属情報に従って、対象タンパク質のアミノ酸配列において溶媒に接触している箇所を特定し、当該箇所に従って対象タンパク質のアミノ酸配列における溶媒接触残基情報を決定し、対象タンパク質について立体構造を予測し、対象タンパク質について基準振動計算を行い、予測された立体構造予測データと決定された溶媒接触残基情報と基準振動計算による計算結果とを対応させて出力する。
(もっと読む)
新規ダニアレルゲンおよびその利用
【課題】ダニアレルギー性疾患に関するDer fまたは、Der pファミリー以外の新規アレルゲンタンパク質、およびそれを用いた診断薬、予防薬および治療薬等を提供する。
【解決手段】本発明のタンパク質はダニ虫体抽出物に含まれ、SDS−ポリアクリルアミドゲル電気泳動法により測定すると分子量約15kDaを示し、等電点電気泳動法により測定すると約5.5付近に等電点を示し、IgEと交差反応を示す特徴を有している。上記タンパク質をESI Q−TOF MSによって解析したところグループ2のダニアレルゲンと相同性を示す新規アレルゲンであった。本発明から、新規ダニアレルゲンタンパク質、当該タンパク質をコードするポリヌクレオチド、当該タンパク質を認識する抗体が得られ、それらを用いることでダニアレルギー性疾患の診断薬、予防薬および治療薬等を提供することができる。
(もっと読む)
リポソームをリガンドとして用いた体液タンパク質の解析方法及び体液タンパク質の調製方法
【課題】体液に含有されるタンパク質を選択的に抽出し、調製できる方法を提供する。
【解決手段】体液とリポソームとをカルシウムイオン等の金属イオンの存在下に混合しタンパク質−リポソーム結合体を形成させ、該結合体以外の体液成分から分離した後、該結合体からタンパク質を遊離させ、分画し分画したタンパク質の少なくとも一つの画分を分析する、リポソーム結合性体液タンパク質の解析方法。前記と同様の方法で、タンパク質を遊離した後、遊離したタンパク質を回収するリポソーム結合性体液タンパク質の調製方法。前記と同様の方法で、タンパク質を分画した後、分画した結果を、同様の段階を経て得られた健常者から採取した体液についての分画結果と対比し、被検体液と健常者由来の体液において量の変化の認められるタンパク質を識別し、識別したタンパク質の少なくとも一つの画分を分析する、リポソーム結合性体液タンパク質を解析する。
(もっと読む)
貝類由来ADPリボシル化タンパク質、およびその利用
【課題】本発明は、ADPリボシル化活性を有する新規貝類由来タンパク質、および該タンパク質の用途の提供を課題とする。より詳しくは本発明は、ADPリボシル化活性を有する新規貝類由来タンパク質、および該タンパク質を成分とする抗癌剤もしくはアポトーシス誘導剤、並びに、該タンパク質を用いてDNAをADPリボシル化する方法、および、細胞に対してアポトーシス誘導する方法等の提供を課題とする。
【解決手段】貝類からDNAを基質としてADPリボシル化する活性を有する新規タンパク質が同定された。該タンパク質を電気穿孔法により癌細胞株であるHeLa細胞、TMK-1細胞内へ導入することにより、HeLa細胞、TMK-1細胞のアポトーシスが誘導され、細胞死に至ることが判明した。貝類から見出されたADPリボシル化活性を有するタンパク質は、アポトーシス誘導剤もしくは抗癌剤として有用である。
(もっと読む)
脂質代謝異常症の予測方法
【課題】被験物質が薬剤誘発性リン脂質症などの脂質代謝異常症を誘発する可能性があるか否かを簡便かつ確実に予測又は診断する方法を提供する。
【解決手段】被験物質の脂質代謝異常症誘発可能性を予測又は診断する方法であって、下記の工程:(1)被験物質を哺乳類動物に投与した後、該哺乳類動物から生体試料を採取する工程;及び(2)該生体試料中に含まれる特定生体内物質を測定し、得られた測定結果を被験物質非投与の測定結果と比較し、これらの測定結果に有意差が認められた場合には該被験物質が脂質代謝異常症を誘発する可能性があると判定する工程を含み、かつ該特定生体内物質がアミオダロン及びフェノキシプロピルアミン化合物のそれぞれの投与により有意に変動する1種又は2種以上の物質である方法。
(もっと読む)
ZAP−70相互作用分子の同定およびZAP−70の精製のための方法
本発明は、第一の局面において、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を所与の化合物とともにインキュベーションする段階、および(d) 化合物が固定化アミノピリド-ピリミジンリガンド24からリン酸化ZAP-70を分離できるかどうかを判定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第二の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物を提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(c) 段階(b)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体を検出する段階を含む、ZAP-70相互作用化合物の同定法に関する。第三の局面において、本発明は、(a) リン酸化ZAP-70を含有するタンパク質調製物の二つのアリコートを提供する段階、(b) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24と一方のアリコートを接触させる段階、(c) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、所与の化合物および固体支持体に固定化されたアミノピリド-ピリミジンリガンド24ともう一方のアリコートを接触させる段階、ならびに(d) 段階(b)および(c)において形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法を提供する。第四の局面において、本発明は、(a) リン酸化ZAP-70を含有する少なくとも一つの細胞をそれぞれ含む二つのアリコートを提供する段階、(b) 一方のアリコートを所与の化合物とともにインキュベーションする段階、(c) それぞれのアリコートの細胞を収集する段階、(d) タンパク質調製物を得るために細胞を溶解させる段階、(e) アミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の形成を可能にする条件の下で、固体支持体に固定化されたアミノピリド-ピリミジンリガンド24とタンパク質調製物を接触させる段階、ならびに(f) 段階(e)においてそれぞれのアリコートで形成されたアミノピリド-ピリミジンリガンド24-リン酸化ZAP-70複合体の量を測定する段階を含む、ZAP-70相互作用化合物の同定法に関する。
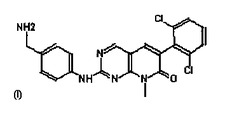 (もっと読む)
(もっと読む)
タンパク質結合部位同定技術
【課題】抗原抗体反応のようなタンパク質間相互作用においてその結合部位を効率的に同定する手法を提供すること。
【解決手段】相互作用する第1のタンパク質と第2のタンパク質について、前記第1のタンパク質を支持体上に固定化し、前記第2のタンパク質を断片化して、前記第1のタンパク質に添加し、前記第1のタンパク質に捕捉された前記第2のタンパク質断片を分離し、分離された前記第2のタンパク質断片のアミノ酸配列を質量分析により解析して、前記第1のタンパク質に対する前記第2のタンパク質の結合部位を同定する。
(もっと読む)
医薬品開発方法及び医薬品開発支援情報提供サービスシステム
【課題】新薬候補化合物の新薬としての不適格要素を早期に発見できるようにする。
【解決手段】非臨床試験と、臨床試験とからなる医薬品開発方法において、新薬候補化合物の少なくとも一部が、AMSやPET検査によって観測可能な放射性同位元素でラベルされ、そのラベルされた新薬候補化合物の血中濃度や体内動態が、AMSやPET検査によって検査され、その血中濃度や体内動態と標的部位との関係から新薬候補化合物の有効性を試験し、特に、健常人に対し、ラベルされた新薬候補化合物を投与し、広く健常人に対する新薬候補化合物の血中濃度や体内動態を検査し、そのデータを臨床試験の評価及び判定の基礎データとして活用する。
(もっと読む)
21 - 40 / 100
[ Back to top ]