Fターム[4B024DA02]の内容
突然変異又は遺伝子工学 (218,933) | 宿主 (25,064) | 動物細胞 (10,788)
Fターム[4B024DA02]の下位に属するFターム
ヒト細胞 (2,034)
Fターム[4B024DA02]に分類される特許
2,201 - 2,220 / 8,754
ヒト抗PD−1、PD−L1、及びPD−L2抗体とその用途
本発明は、部分的には、新規なヒト抗PD−1、PD−L1、及びPD−L2抗体の同定に基づく。従って、本発明は、ここに記載の新規なヒト抗PD−1、PD−L1、及びPD−L2抗体を使用して、PD−1、PD−L1、及び/又はPD−L2活性の調節から利点を得る症状(例えば、持続感染疾患、自己免疫疾患、喘息、移植片拒絶、炎症性疾患及び腫瘍)を診断し、予後診断し、及び治療するための組成物及び方法に関する。 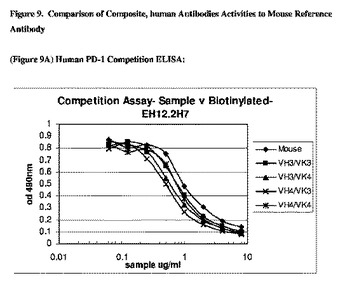 (もっと読む)
(もっと読む)
ヒトFGFR4ARG388多形のための齧歯類癌モデル
本発明は、制御されていない細胞成長、例えば癌及び改変したFGFR4に関連した分子機構及び生理学的プロセスを研究するための齧歯類動物を提供する。 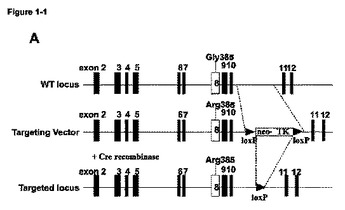 (もっと読む)
(もっと読む)
非複製性ベクターワクチンの粘膜投与による鳥類の免疫処置
本発明は概して、免疫学およびワクチン接種技術の分野に関する。より具体的には、本発明は、鳥インフルエンザウイルスをコードする遺伝子などの、鳥類免疫原または抗原をコードする遺伝子を送達するための、組換えヒトアデノウイルスベクターを含む組成物を含めた、免疫原性およびワクチン組成物の鳥類へのエアゾールスプレーによる粘膜投与に関する。本発明はさらに、このような投与において使用するための方法および装置を提供する。 (もっと読む)
組換えベクター
この開示は、改変シトシンデアミナーゼ(CD)を提供する。本開示は、そのような改変CDを発現するか又は含む細胞及びベクター、並びに疾患及び障害の治療でそのような改変CDを用いる方法にさらに関する。 (もっと読む)
ヒトIL17に対する抗体およびその使用
モノクローナル抗体3C1が結合するのと同じIL−17エピトープに結合し、そしてCH1とCH2との間のヒンジ領域のアミノ酸216位〜240位、好ましくはアミノ酸220位〜240位において、および/またはCH2とCH3との間の第2のドメイン間領域のアミノ酸327位〜331位において、改変されたヒトIgG1アイソタイプであることによって特徴付けられる、IL−17に結合する抗体は、炎症疾病の処置のための有利な特性を有する。 (もっと読む)
サイズが減少した自己送達用RNAi化合物
本発明は、最短の二本鎖領域を有するRNAiコンストラクト、および遺伝子サイレンシングにおけるそれらの使用に関する。本発明に関連するRNAiコンストラクトは、8〜14ヌクレオチドの二本鎖領域および多様な化学修飾を含み、遺伝子サイレンシングにおいて高度に有効である。 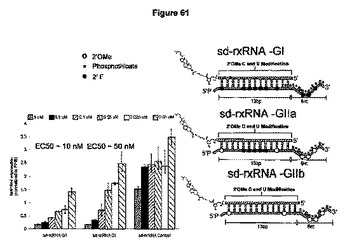 (もっと読む)
(もっと読む)
SNORF25受容体をコードするDNA
【課題】レチノイン酸受容体の提供。
【解決手段】ほ乳類SNORF25受容体をコードする単離された核酸、精製されたほ乳類SNORF25受容体、ほ乳類SNORF25をコードする核酸を含むベクター、そのようなベクターを含む細胞、ほ乳類SNORF25に対する抗体、ほ乳類SNORF25受容体をコードする核酸を検出するために有用な核酸プローブ、ほ乳類SNORF25受容体をコードする核酸に固有の配列に相補的なアンチセンスオリゴヌクレオチド、正常または変異哺乳物SNORF25受容体をコードするDNAを発現するトランスジェニック、非ヒト動物、ほ乳類SNORF25受容体を単離する方法。
(もっと読む)
ヘマグルチニンに対する抗体、保存インフルエンザ抗原および免疫賦活性担体結合ドメインとを含む多機能性リンカータンパク質
本発明は、免疫学およびワクチンの分野に関する。特に、本発明は、タンパク質様物質、および呼吸器系病原体を原因とする感染に対するワクチンにおけるその使用に関する。 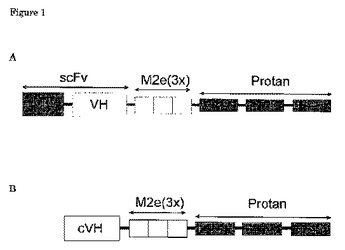 (もっと読む)
(もっと読む)
無細胞タンパク質合成系−バキュロウイルス発現系両用ベクター
【課題】無細胞タンパク質合成系とバキュロウイルス発現系とにおいて共用することができるベクターを提供する。
【解決手段】 上流側から下流側へ、バキュロウイルス後期遺伝子プロモーター配列(a)、バキュロウイルス後期遺伝子5’非翻訳領域配列(b)、及び所望の構造遺伝子を挿入するための配列(c)を含むバキュロウイルストランスファーベクターであって、
前記配列(a)の上流側、又は、前記配列(a)の下流側且つ前記配列(b)の上流側に、ファージ由来RNAポリメラーゼ認識配列(d)を含む、バキュロウイルストランスファーベクター。当該バキュロウイルストランスファーベクターに所望の構造遺伝子を挿入した組み換えバキュロウイルストランスファーベクターから、バキュロウイルス発現系及び/又は無細胞タンパク質合成系によりタンパク質を調製する方法。
(もっと読む)
LRRKのタンパク質基質及びその使用方法
(1)被験化合物が基質ポリペプチドにおけるLRRK2ポリペプチドのタンパク質キナーゼ活性を調節、例えば阻害するかどうかを決定すること;および(2)該LRRK2ポリペプチドタンパク質キナーゼ活性を調節、例えば阻害する化合物を選別すること;の工程を含んでなり、基質ポリペプチドは配列(W/F/R/K)(W/F/R/K)(R/K)(F/W/H/R)(Y/W/R)(S/T)(L/V/I)(R/K)(R/K)(A/Y)または(W/R)(X)(X)(F/Y/H/T)(Y/W/R)(T)(X)(R/T)(R)(X)(ここでXは任意のアミノ酸を表す)を含んでなるLRRK2タンパク質キナーゼ活性を調節、例えば阻害するのに有用であると予期される化合物を同定する方法。そのような化合物はパーキンソン病またはパーキンソン症を処置するのに有用であり得る。 (もっと読む)
臨床サンプル中のインターフェロン応答(IRIS)
本発明は、多発性硬化症(MS)に対する処置の有効性を決定するために有用な特定の遺伝子セットに関するものである。また、本発明は、MS処置の有効性を評価するために有用なこれらの遺伝子のアレイを提供する。また、MS処置効果を評価するための方法と、MSのインターフェロンβ-1Bの処置に対する患者応答における中和抗体を検出するための方法を提供する。 (もっと読む)
樹状細胞調節分子
本発明は、哺乳動物樹状細胞の分化および成熟化を調節(好ましくは阻害)する樹状細胞調節分子を提供する。本発明はまた、樹状細胞調節分子およびそのホモログおよび活性フラグメントを含有する医薬組成物、それに対する抗体、およびそれらの分子を利用する治療法およびスクリーニング法を提供する。 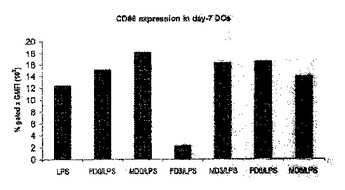 (もっと読む)
(もっと読む)
癌の治療のためのモノクローナル抗体
本発明は、腫瘍関連疾患、例えば乳癌、肺癌、胃癌、卵巣癌、肝細胞癌、結腸癌、膵臓癌、食道癌、頭頸部癌、腎癌、特に腎細胞癌、前立腺癌、肝臓癌、黒色腫、肉腫、骨髄腫、神経芽細胞腫、胎盤性絨毛癌、子宮頸癌及び甲状腺癌、並びにそれらの転移形態を含む、GT468を発現する細胞に関連する疾患を治療する及び/又は予防するための治療薬として有用な抗体を提供する。1つの実施形態において、腫瘍疾患は肺の転移性癌である。 (もっと読む)
細胞のNF−κB活性化を調節するための組成物および方法
【課題】ユビキチン経路を経由するIκB分解のさらなる理解を提供すること。
【解決手段】核因子κB(NF−κB)の活性化を調節する組成物および方法が提供される。この組成物は、リン酸化IκBαおよび/またはIκBβのユビキチン化を調節する1つ以上の因子を含む。このような組成物は、NF−κB活性化に関連する疾患を処置するために用いられ得る。調節因子は、E3ユビキチンリガーゼの認識ドメインを含むペプチドを含む。
(もっと読む)
チャイニーズハムスター卵巣細胞系
本発明者らは、野生型チャイニーズハムスター卵巣細胞と比較して、例えば機能的GnT1の存在下においてタンパク質を高度にシアル化できるチャイニーズハムスター卵巣(CHO)細胞であって、前記CHO細胞はRicinus communisアグルチニンI(RCA−I)を用いた選択によって入手できるCHO細胞を提供する。 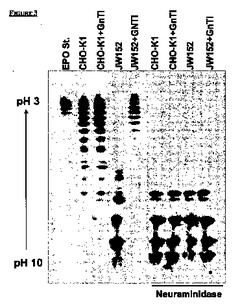 (もっと読む)
(もっと読む)
細胞培養用基材
【課題】細胞を、その特性を損なうことなく、かつ細胞同士が重なり合うことなく分散した状態で3次元培養できる細胞培養用基材を提供する。
【解決手段】平均繊維径が0.05〜5μmである高分子化合物より形成された繊維構造体の繊維表面上に、疎水性材料結合部位および細胞接着部位を有するキメラタンパク質が固定化された細胞培養用基材、かかる基材に幹細胞を播種して培養することにより得られる幹細胞培養複合体、ならびに該基材を含む細胞培養増殖装置。
(もっと読む)
修飾を有するdsRNAによる遺伝子発現の特異的な阻害のための組成物および方法
本発明は、真核細胞において特定された遺伝子の発現または活性を減少させるために有用である組成物および方法を特徴とする。 (もっと読む)
腸の治療
Y1レセプター及びY2レセプターよりもY4レセプターに選択的であるY4レセプターアゴニストは、放射線療法、放射線曝露、細胞毒性化学療法、炎症又は腸粘膜の虚血‐再潅流に起因する腸機能損傷の予防及び/又は治療に有用である。 (もっと読む)
DLL4に対する抗体およびその使用
本発明は、DLL4に対する標的結合剤およびかかる薬剤の使用に関する。さらに具体的には、本発明は、DLL4を指向する完全ヒトモノクローナル抗体に関する。記載したこれらの標的結合剤は、DLL4の活性および/または過剰生産と関連する疾患の治療において、ならびに診断として有用である。 (もっと読む)
CD40およびパターン認識受容体アダプターを誘発することによる免疫応答を生成するための方法および組成物
誘発性パターン認識受容体アダプターまたはアダプター断片およびCD40の活性を誘発することによって抗原提示細胞を活性化し、免疫応答を誘導するための方法が提供される。誘発性CD40ペプチドおよび誘発性パターン認識受容体アダプターまたはアダプター断片を含むキメラタンパク質をコードする配列を含む核酸組成物もまた提供される。例示的な一実施形態において、上記方法は、抗原提示細胞に、キメラタンパク質をコードするヌクレオチド配列を有する核酸を形質導入するステップを含み、前記キメラタンパク質は、(i)膜ターゲティング領域、(ii)リガンド結合領域、(iii)細胞質CD40ポリペプチド領域、ならびに(iv)TIRドメインを欠く切断型MyD88ペプチドおよびTRIFペプチドからなる群より選択されるペプチドを含む。 (もっと読む)
2,201 - 2,220 / 8,754
[ Back to top ]