Fターム[4B029CC03]の内容
微生物・酵素関連装置 (40,912) | 生物材料の存在状態 (7,687) | 固定 (1,880)
Fターム[4B029CC03]の下位に属するFターム
Fターム[4B029CC03]に分類される特許
1,701 - 1,720 / 1,741
細胞の培養及び増殖方法
本発明は、実質的に重ね合わされ、互いに連結されており、それらの層の間にフロースルー可能な空間が形成される、少なくとも2つの多孔性材料層、又は材料層の少なくとも2つの重ね合わされた断面の間にフロースルー可能な空間が形成されるように、その形状を維持しながら、それ自体の上に配置された又は折りたたまれた少なくとも1つの多孔性材料層から成る、層状構造を有する炭素ベースの基質を製造する工程を含む、細胞培養方法に関する。前記方法は、さらに、前記基質に生存及び/又は増殖している生物材料を負荷すること及び前記負荷した基質を液体培地と接触させることを含む。 (もっと読む)
埋設可能な装置に用いる酸素増大膜システム
本発明は埋設可能な装置における酸素の効率を高めるシステム及び方法に広く係るものである。好ましい実施形態は装置を生物学的な環境から保護し、及び/または酵素反応の触媒を提供する膜システムであって、前記膜システムは高い酸素溶解性材料から形成されるポリマーを含む。前記高い酸素溶解性を有するポリマー材料は、酸素欠乏下でも酸素利用源での酸素の効率が動的に高く保持されるように、埋設可能な装置上の酸素利用源近傍に配置される。前記膜システム(18)は細胞破壊ドメイン(40)、細胞不浸透性ドメイン(42)、抵抗ドメイン(44)、酵素ドメイン(46)、妨害ドメイン(48)、及び電気化学反応表面に近接した電解質ドメイン(50)を備えていてもよい。好ましい実施形態における膜システムは、酵素ベースの電気化学センサー等酸素利用源を備えた埋設可能な装置に有効であり、及び/または低酸素の状況でも機能する。 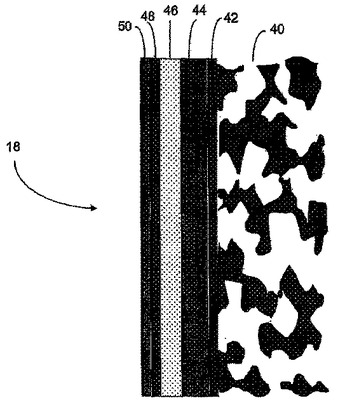 (もっと読む)
(もっと読む)
生理活性分子間の結合を決定するための磁性粒子の使用
ビーズのような少なくとも第1の粒子又はマイクロキャリアと、例えば第2のビーズのようなマイクロキャリアでありうる第2の粒子とを使用して、生理活性分子のような微生物学的エンティティの間の相互作用を決定するためのアッセイ、ツール及び装置が開示される。少なくとも第1のマイクロキャリアは磁性である。2つのビーズが使用され、両方のビーズが磁性であるとき、ビーズは、好適には、それらの磁気モーメントの大きさが異なる。それぞれ異なる強度の結合を区別するために生理活性分子間の結合を機械的応力下におく手段が設けられる。1つの見地において、(より大きい磁気モーメントを有する)第2のビーズが、(それ自体概して移動可能な又は移動可能でない表面に結合される)捕捉分子に弱く結合されるより小さい磁気モーメントを有するビーズにリンクされるターゲット分子を磁気的に除去するために使用される。代替例として、流体摩擦力が、弱い結合を崩壊させるために、粒子の一方に与えられることができる。実施例に依存して、第1のビーズ及び/又は第2の粒子が、検出目的のために使用されることができる。 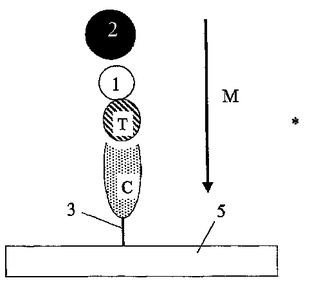 (もっと読む)
(もっと読む)
化学的結合を検出するための方法及び装置
導管を通じてサイズ排除フィルタにサイズ排除フィルタを通過するには大きすぎる対象バインダの溶液(好適には水溶液)を送ることと、次に対象バインダがフィルタ上に集まった後に同一の導管を通じてサイズ排除フィルタに一以上の潜在的な薬剤化学物質の溶液(好適には水溶液)を送ることを包含する、対象バインダと潜在的な薬剤化学物質の間の結合をスクリーニングするための方法である。潜在的な薬剤化学物質は、サイズ排除フィルタを通過するために十分に小さい。その後、X線がX線源からサイズ排除フィルタに送られ、潜在的な薬剤化学物質が対象バインダと共に化合物を形成する場合、化合物は、化合物が形成されたことを示す強度を有するX線蛍光信号を生成する。  (もっと読む)
(もっと読む)
CNS試料において非中枢神経系(CNS)疾病を診断するための方法およびシステム
本発明は、CNS、例えば、脳脊髄液、脳もしくは脊髄組織試料または他の生体液試料における遺伝子発現の変化を検出することによって非中枢神経系(非CNS)疾患を診断する方法、システムおよび組成物を特徴とする。 (もっと読む)
機能性DNAエレメントおよび細胞性タンパク質のゲノムマッピング
本発明は、タンパク質とゲノム上のDNA(例えば全ゲノムまたはその一部であって、1以上の染色体または染色体領域など)との結合を試験する方法を提供する。特に、本発明は、対象のタンパク質が結合するゲノムDNAの調節領域(例えば、プロモーターまたはエンハンサー領域)を同定する方法に関する。ある態様では、本発明は、組織に関連した調節に関する。別の態様では、本発明は、発生に関連した調節に関する。さらなる態様では、本発明は、特定の疾病状態または障害における発現の調節に関する。 (もっと読む)
ポリヌクレオチド増幅反応の測定
ポリヌクレオチド増幅反応の進行の定量的測定は、(i)標的ポリヌクレオチドの増幅のための反応を実行し、(ii)増幅反応の間または後に、増幅産物をポリヌクレオチドに結合する分子(空間的に規定された位置に存在するか、または非線形または非蛍光性の方法により判定される分子)に接触させ、(iii)印加された照射の変化を測定することによって、上記増幅産物および上記分子の間の相互作用を検出することにより行うことが出来る。 (もっと読む)
統合失調症の診断および治療のための標的としてのEGR遺伝子
本発明は、統合失調症および関連症状の診断および治療のための標的、方法、および試薬を提供する。本発明は、EGR分子もしくはEGR相互作用分子をコードする遺伝子発現における多型、変異、変動、変更などまたはこのような遺伝子に関連する多型の検出による統合失調症および統合失調症に対する感受性の診断方法を提供する。本発明は、多型および変異型の検出のためのオリゴヌクレオチド、アレイ、および抗体を提供する。本発明は、このような遺伝子が変化したトランスジェニックマウスを提供する。本発明はまた、これらの遺伝子をターゲティングする化合物の投与による統合失調症の治療方法を提供する。本発明は、さらに、このような化合物を同定するためのスクリーニング方法およびスクリーニングの実施によって得られた化合物を提供する。 (もっと読む)
バイオリアクタ
大きな比表面積を有する多孔担体からなる充填体が収容された濾過器を含むバイオリアクタを開示する。濾過器には、好ましくは光合成活性を有する微生物と発光微生物とを含む微生物混合物が導入されており、有機物の光動的分解が発生する。本発明では、微生物混合物は光触媒活性を有するナノ粒子を含む。 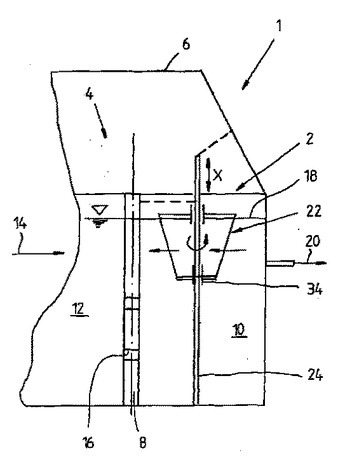 (もっと読む)
(もっと読む)
SARSウイルスおよび他の感染因子を検出するための方法および組成物
本発明は、一般に、ウイルス検出の分野に関する。特に本発明は、SARS−CoVヌクレオチド配列を増幅および検出するためのチップ、プローブ、プライマー、キットおよび方法を提供する。本発明のチップ、プローブ、プライマー、キットおよび方法の臨床的使用および他の使用もまた企図される。患者の症状のみに基づくSARSの診断には問題がある。本発明の目的の1つは、SARSウイルスおよびSARS様症状を引き起こす他の病原体の同時検出のためのバイオチップを提供することである。本発明の他の目的は、SARSウイルスおよびSARSの症状を悪化させる他の病原体を同時に検出するための核酸マイクロアレイを提供することである。 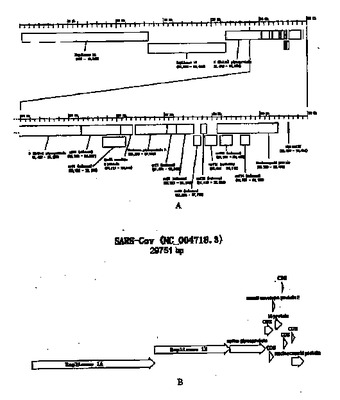 (もっと読む)
(もっと読む)
試料中に含有される物質の直接定量的invitro決定の装置および方法
本発明は、試料中に含有される物質の直接定量的in vitro 決定の装置および方法に関する。本発明による装置は、表面上に固定化された物質検出因子、遊離物質-放出体複合体、および表面上に固定化された放出体検出因子を含んでなる。使用する装置の放出体は、放出体検出因子との相互作用において放出特性の変化と反応する部分を含んでなる。本発明による装置により、抗原、例えば、タンパク質、ペプチド、核酸、オリゴヌクレオチド、血液成分、血清成分、脂質、薬剤および低分子量化合物または、他の設計において、抗体および抗体フラグメントから選択される物質を、例えば、全血試料において、直接定量的に決定することができる。 (もっと読む)
ロタキサン化合物、ロタキサン化合物が結合した固体基板及びこれを利用したバイオチップ
化学式2のククルビツリルまたはその誘導体の内部空洞に化学式3の化合物が垂直に貫通した化学式1の化合物を提供する。さらに、前記化合物が結合した固体基板および前記固体基板を含むバイオチップを提供する。 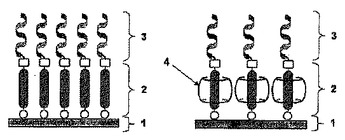 (もっと読む)
(もっと読む)
核酸を増幅および配列決定する方法
ゲノム配列決定のような迅速DNA配列決定を行うための装置および方法が本明細書中に提供される。本方法は、ゲノム配列決定用のサンプルDNAを調製する工程、調製されたDNAを典型的方法で増幅する工程、および、一つのプライマーハイブリダイゼーション工程しか用いずに増幅されたDNA上で多重配列決定反応を行う工程を含む。 (もっと読む)
マイクロRNA配列や小さな干渉RNA配列の標識と検出のための分析方法
短いRNA断片を保護する方法は、短いRNA断片を検出可能な白金化合物で標識して標識した小さなRNA断片を形成すること含んでいる。得られた標識した短いRNA断片を捕捉オリゴヌクレオチドにさらす。捕捉オリゴヌクレオチドは、短いRNA断片ヌクレオチド配列に相補的なヌクレオチド配列の少なくとも2つの複製物を含んでいる。標識した短いRNA断片と捕捉オリゴヌクレオチド配列は、ハイブリダイゼーション条件下で接触させる。ハイブリダイゼーションにおいて、ハイブリダイズし標識した小さなRNA断片-捕捉オリゴヌクレオチド結合体上にマーカー部分が検出される。短いRNA断片の検出アレイは、複数のスポットを有する基質を含み、第1スポットは第1の短いRNA断片に相補的なヌクレオチド配列の少なくとも2つの複製物を含む第1捕捉オリゴヌクレオチドを共通なコントローラ又はスペーサとして機能する追加のヌクレオチド配列と共に含んでいる。アレイ上の他のスポットは、第2の短いRNA断片に相補的な配列の少なくとも2つの複製物を有する第2捕捉オリゴヌクレオチドを共通なコントローラ又はスペーサとして機能する追加の配列と共に含んでいる。溶離と任意の白金化合物のそれからの除去によって配列を移動させた後に証明された小さなRNA断片も得られる。 (もっと読む)
ルックスルー突然変異誘発
予定アミノ酸が、ポリペプチド類似体のライブラリーを生成するためにポリペプチドの予備選定領域(またはいくつかの異なる領域)中の選定組の位置の各々および全ての位置に導入される突然変異誘発方法。当該方法は、ある旬補アミノ酸がタンパク質の構造および機能に重要な役割を演じる、という前提に基づく。所望のポリペプチド類似体のみを含有するそしてスクリーニングのための合理的サイズを有するライブラリーが生成され得る。ライブラリーを用いて、ポリペプチド構造および機能における特定アミノ酸の役割を試験し、そして新規のまたは改良されたポリペプチド、例えば抗体、抗体断片、一本鎖抗体、酵素およびリガンドを開発し得る。 (もっと読む)
グルカナーゼ、それらをコードする核酸並びにそれらを製造及び使用する方法
本発明は、グルカナーゼ(例えばエンドグルカナーゼ)、マンナナーゼ、キシラナーゼ活性またはこれら活性の組合せを有するポリペプチド、およびそれらをコードするポリヌクレオチドに関する。ある特徴では、前記グルカナーゼ活性はエンドグルカナーゼ活性(例えばエンド-1,4-ベータ-D-グルカン4-グルカノヒドロラーゼ活性)であり、さらに前記活性は、セルロース、セルロース誘導体(例えばカルボキシメチルセルロース及びヒドロキシエチルセルロース)、リケニン中の1,4-及び/又はβ-1,3-ベータ-D-グリコシド結合の加水分解、混合ベータ-1,3-グルカン(例えば穀類のベータ-D-グルカン又はキシログルカン)およびセルロース部分を含有する他の植物材料中のベータ-1,4-結合の加水分解を含む。さらに、新規な酵素を設計する方法およびそれらを使用する方法もまた提供される。別の特徴では、前記新規なグルカナーゼ(例えばエンドグルカナーゼ)、マンナナーゼ、キシラナーゼはより高いpHおよび温度で増進された活性および安定性を有する。 (もっと読む)
COPDキナーゼ(RCキナーゼ)において制御される、キナーゼの制御
【課題】なし
【解決手段】ヒトRCキナーゼ活性を制御する試薬、及びヒトRCキナーゼ遺伝子産物と結合する試薬を用いて、治療効果を得るためにこのタンパク質を制御することができる。そのような制御は、慢性閉塞性肺疾患、喘息、癌、及び細胞のシグナル伝達に欠陥がある疾患の治療に特に有用である。
(もっと読む)
空間選択的堆積によるミクロスケール及びナノスケールの加工及び製造
基板(10)上に固相アレイを形成するように、化学物質を空間選択的に堆積することによってマイクロメートル規模及びナノメートル規模で製作又は製造する方法であって、静電気的潜像の形成のように、基板上の少なくとも一つの領域に基板の他の領域の電荷とは異なる静電荷を形成することによって、少なくとも一つの領域(15)を定義する工程と、基板にエマルジョンを塗布する工程とを含む方法。エマルジョン(16)は、帯電した不連続相及び該不連続相の中に担持された、又は該不連続相を含んでなる選択的に堆積されるべき成分を有している。このエマルジョンの不連続層は、当該領域上の静電荷により引寄せられることによって予め選択された領域に引寄せられ、反応を伴って又は伴わずに堆積が得られる。光導電体の使用によって、静電画像を形成することができる。形成されるアレイは、フラットスクリーンディスプレーパネルのためのものであってよく、DNAチップ、印刷回路、半導体チップ、ナノテクノロジー、ミクロ電気機械的システム、可撓性印刷回路等を製造するためのものであってよい。 (もっと読む)
空間的に選択的なマイクロ及びナノメートルスケールの付着用の基体及びコンビナトリアル修正及び成形加工
空間的に選択的なマイクロ及びナノメートルスケールの付着及び/又は反応のための基体(1)であって、上記基体は、支持体(3)、上記支持体上の導電層(5)、静電荷パターンを保持する誘電層(7)、例えば上に入射光を受けた時に静電荷を分散させる材料の光導電層、及び化学的官能層(9)を有し、静電荷パターンが、上記基体上に予め決められた方法で形成され、上記基体上のエマルジョン(15)内の荷電した液滴の運動に影響することを特徴とする基体である。上記化学的官能層は、上記基体の化学的官能化のための表面を提供するか、又は上記誘電又は光導電層への接近又は反応を妨げる。 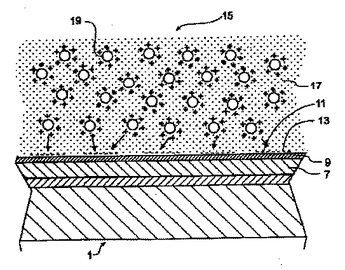 (もっと読む)
(もっと読む)
バクテリオファージを使用した微生物を検出するための装置および方法
原試料中の1つ以上の標的細菌を検出する方法であり、各標的細菌に特異的なバクテリオファージを原試料に添加し、この試験試料をインキュベートし、試験試料を、当該バクテリオファージまたは該バクテリオファージに関連する生物物質が存在すると色が変化する基板に塗布する。基板は各ファージに特異的に結合する抗体を含む。試験試料中の細菌は、バクテリオファージに曝露されたサンプルに微生物リゾチームを加えることによって溶菌してもよい。親ファージを、検出プロセスに先立って子孫ファージから分離できるような様式で標識する。ファージは、インキュベーションプロセス後に解離させて、試料に対して、個々のカプシドタンパク質またはファージ核酸の存在について調べることもできる。本発明は、兵家器細菌の抗生物質耐性を調べるために用いることもができる。 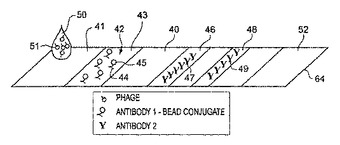 (もっと読む)
(もっと読む)
1,701 - 1,720 / 1,741
[ Back to top ]