Fターム[4B063QR06]の内容
酵素、微生物を含む測定、試験 (178,766) | 試薬 (61,469) | 試薬としての酵素 (8,175) | 転移酵素 (4,888)
Fターム[4B063QR06]の下位に属するFターム
リン酸転移酵素(←キナーゼ) (4,652)
Fターム[4B063QR06]に分類される特許
101 - 120 / 236
リコンビナーゼポリメラーゼ増幅
【課題】改善されたリコンビナーゼ依存性DNA増幅方法を提供すること。
【解決手段】RPAと称するDNAの増幅方法であって、以下の工程を含む。第1に、リコンビナーゼ因子を第1および第2の核酸プライマーと接触させ、第1および第2の核タンパク質プライマーを形成する。第2に、第1および第2の核タンパク質プライマーを二本鎖標的配列に接触させて、前記第1の鎖の第1の部分に第1の二本鎖構造を形成させ、そして前記第2の鎖の第2の部分に二本鎖構造を形成させ、前記第1の核酸プライマーおよび前記第2の核酸プライマーの3’末端が、所与の鋳型DNA分子で互いに向かって配向される。第3に、前記第1および第2の核タンパク質プライマーの3’末端はDNAポリメラーゼによって伸長され、第1および第2の二本鎖核酸ならびに核酸の第1および第2の被置換鎖を生成させる。最後に、第2および第3の工程を所望の増幅度に達するまで反復する。
(もっと読む)
新規の特異的細胞結合剤
本発明は幹細胞のグリカン構造に対する特異的結合剤のための試薬および方法を記載する。さらに本発明は、幹細胞の表面上の特異的グリカンエピトープに対するさらなる結合試薬のスクリーニングに関する。グリカン構造の好ましい結合剤としては酵素、レクチンおよび抗体等のタンパク質などが挙げられる。 (もっと読む)
ヒト細胞からの新規の炭水化物、ならびにその分析および修飾のための方法
本発明は幹細胞のグリカン構造に対する特異的結合剤のための試薬および方法を記載するものである。さらに本発明は、幹細胞表面の特定のグリカンエピトープに対するさらなる結合試薬のスクリーニングに関する。グリカン構造の好ましい結合剤としては、酵素、レクチン、および抗体等のタンパク質が挙げられる。 (もっと読む)
アセチル化及び脱アセチル化の蛍光可視化検出方法
【課題】 本発明はタンパク質のアセチル化状態をリアルタイムで測定可能な蛍光プローブの提供を目的とする。また、本発明は該蛍光プローブを用いて生細胞内のタンパク質のアセチル化状態をリアルタイムで測定する方法の提供を目的とする。
【解決手段】 本発明は、アセチル化基質ドメインと、アセチル化基質結合ドメインを、リンカーペプチドで連結し、該アセチル化基質ドメインと該アセチル化基質結合ドメインに、異なる蛍光特性を持つ蛍光タンパク質を、各々、連結した蛍光プローブを提供する。また、本発明は、該蛍光プローブを生細胞内に導入して、蛍光プローブからのFRET変化を検出することで、生細胞内のタンパク質のアセチル化状態を測定する方法を提供する。
(もっと読む)
O6−アルキルグアニン−DNAアルキルトランスフェラーゼ(AGT)の使用方法
【課題】O6−アルキルグアニン−DNAアルキルトランスフェラーゼ(AGT)を用いた、標識を基質からAGTを含む融合タンパク質に移転する方法の提供。
【解決手段】新たな物理学的または化学的特性を融合タンパク質に導入する分子を融合タンパク質に結合させることによって、インビトロとインビボとの双方での融合タンパク質の検出および/または操作を可能にする。そのような分子の例は、とりわけ、分光学的プローブもしくはリポーター分子、親和性タグ、反応性ラジカルを発生できる分子、架橋結合剤、タンパク質−タンパク質相互作用を仲介するリガンド、または融合タンパク質の固定化に適した分子である。
(もっと読む)
新規タンパク質およびそのDNA
【解決手段】レシチン:コレステロールアシルトランスフェラーゼ(LCAT)様活性を有する新規タンパク質,その部分ペプチドまたはそれらの塩、該タンパク質をコードするDNA、該DNAを含有する組換えベクター、形質転換体、該タンパク質の製造法、該タンパク質もしくはDNA含有してなる医薬、該タンパク質に対する抗体、該タンパク質のLCAT活性を促進または阻害する化合物またはその塩のスクリーニング方法/スクリーニング用キットなど。
【効果】該DNAは、動脈硬化症、高脂血症、高カロリー症、肥満、高トリグリセリド症などの種々の疾病の治療・予防剤として使用することができる。本発明のタンパク質は、本発明のタンパク質のLCAT様活性を促進または阻害する化合物をスクリーニングするための試薬として有用である。
(もっと読む)
精巣に発現する糖鎖関連酵素調節因子O−16
【課題】精巣に特異的に発現するタンパク質であって、糖鎖関連酵素に会合し、該糖鎖関連酵素の活性を調節するタンパク質またはその遺伝子を含む組成物を提供することを目的とする。さらに、該タンパク質やその変異体の遺伝子工学的な生産、該タンパク質に会合する糖鎖関連酵素の同定や、該タンパク質またはそれをコードする遺伝子を含む組成物を用いた精子形成異常または受精困難による不妊症の予防、診断、または予防のための方法を提供する。
【解決手段】本発明の組成物は、配列番号2に示されるアミノ酸配列または該アミノ酸配列において1若しくは複数個のアミノ酸が置換し若しくは欠失し、若しくは該アミノ酸配列に1若しくは複数個のアミノ酸が挿入され若しくは付加されたアミノ酸配列を有する、精巣に特異的に発現し、糖鎖関連酵素に会合するタンパク質を含む、糖鎖関連酵素の活性を調節するための組成物である。
(もっと読む)
分子毒性学モデリング
【課題】多細胞生物に対する、化合物、薬剤または毒素の毒性を評価する方法を提供する。
【解決手段】既知の毒素にさらされた組織もしくは細胞における、さらされない組織もしくは細胞と比較してのタンパク質の活性、遺伝子発現の全体的な変化の解明、ならびに毒素にさらすことにより示差的に発現された個々の遺伝子の同定に基づき、マイクロアレイおよびその他の固相プローブと共に使用するように設計された、毒素誘発性の示差的な発現によって特徴づけられる遺伝子のデータベースを含むことからなる。
(もっと読む)
エバネッセント光を用いた化学物質の濃度分布測定法及び装置
【課題】細胞が放出した化学物質の二次元的濃度分布を測定するための光学的方法及びその装置を提供すること。
【解決手段】エバネッセント光を発生しうる界面領域に酵素を固定しておき、前記酵素の作用下で、前記化学物質と蛍光元物質とを前記酵素の作用下で反応させさせることにより蛍光物質を生成させ、前記エバネッセント光によって励起された前記蛍光物質由来の蛍光を検出することにより、前記細胞が放出した当該化学物質の二次元的濃度分布を測定する光学装置。
(もっと読む)
選択マーカー遺伝子
本発明は、本明細書においてDSM-2と呼ばれる新規の遺伝子に関する。この遺伝子は、ストレプトマイセス・セリカラーA3において同定された。DSM-2タンパク質は、PATおよびBARと遠縁である。本発明はまた、DSM-2タンパク質をコードする植物に最適化された遺伝子を提供し、DSM-2は、除草剤グルホシネートおよびビアロホスに対する耐性を植物および植物細胞に賦与するためのトランスジェニック形質として使用され得る。本発明の遺伝子の1つの好ましい使用は、選択マーカーとしての使用である。細菌系における選択マーカーとしてのこの遺伝子の使用は、植物の形質転換の効率を上昇させることができる。唯一の選択マーカーとしてのDSM-2の使用により、クローニング中のさらなる(アンピシリン耐性などの)医療用抗生物質マーカーが不要となる。本発明によれば、様々なその他の使用も可能である。 (もっと読む)
ペプチジル転移反応中心のターゲッティングに関与するタンパク、および対応する治療薬剤並びに治療方法
【課題】ペプチジル転移反応中心のターゲッティングに関与するタンパク、および対応する治療薬剤並びに治療方法を提供すること。
【解決手段】酵母中のmof対立遺伝子のサブセットがナンセンス介在性mRNA崩壊経路に影響する。mmof4-1対立遺伝子を有する細胞はM1ウイルスを失うが、ナンセンス介在性mRNA崩壊に関与するその他のf対立遺伝子、upf1、upf2及びupf3はM1を維持する。乳癌ウイルスからの-1リボソームフレームシフトシグナルでフレームシフティングを増進する突然変異として既に同定されたifs1対立遺伝子及びifs2対立遺伝子は夫々UPF2遺伝子及びUPF1遺伝子の対立遺伝子であり、両方のifs株がM1を維持した。mof4-1株はupf1S8(D)株よりもアミノグリコシドパロモマイシンに感受性である。
(もっと読む)
デプシペプチドおよびその治療的使用
一般式(I)または(I’)のスピルコスタチン類似体である化合物、そのアイソスターおよびその医薬的に許容される塩は、HDACを阻害することが見出され、ここでR1、R2、R3およびR4は同一であっても異なっていてもよく、アミノ酸側鎖部分を表し、各R6は同一であっても異なっていてもよく、水素または炭素数1〜4のアルキルを表す。
【化1】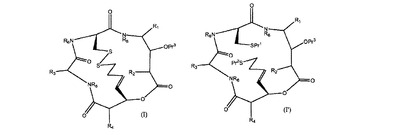
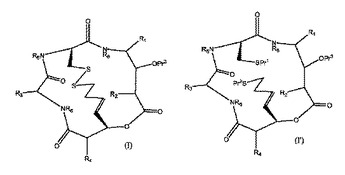 (もっと読む)
(もっと読む)
デプシペプチドおよびその治療的使用
一般構造(VII)または(VIII)の化合物またはそのアイソスターもしくは医薬的に許容される塩であって、式中、R1、R2(X=−CONR6−の場合)、R3およびR7は同一であっても異なっていてもよく、それぞれアミノ酸側鎖部分を表し;R2(X=−CHZ−の場合)、R4およびR6は同一であっても異なっていてもよく、それぞれ水素、炭素数1〜6のアルキル、炭素数2〜6のアルケニルまたは炭素数2〜6のアルキニルを表し;Kは炭素原子の直鎖または分岐鎖を表し、1〜10個の原子を有しており;Lはヒストン脱アセチル化酵素(HDAC)の活性部位において亜鉛をキレート化し得る部分、またはこのような部分にin vivoで(例えば、加水分解または還元により)変換され得る部分を表し;Mは炭素またはその他の原子の直鎖または分岐鎖であって、1〜10個の原子を有し、in vivoでの開裂により構造(VII)を生ずることが出来;そして、Zは単結合または二重結合により大員環に結合するヘテロ原子であって、Zに結合する他の基はいずれもHまたは保護基、である化合物。 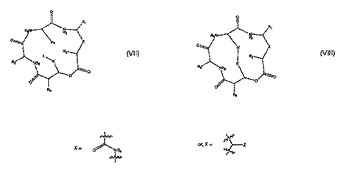 (もっと読む)
(もっと読む)
アルツハイマー病の診断方法及び遺伝子マーカー
治療効力がより高く副作用がより低いCNS薬剤で治療することができる(アルツハイマー病、挙動障害などを含む)CNS障害に罹患している個体を特定する方法、及びそのような治療に有用な化合物が開示される。CNS障害の治療のための薬剤候補の効力を予測する方法も開示される。本技術は、神経変性疾患の動物モデルで使用するための新薬発見にも適用できる。 (もっと読む)
ピロリ菌感染を治療するための新規の方法
本発明は、アミノ酸配列を含むポリペプチドであって、ポリペプチドのアミノ酸配列が、配列番号1に対応するアミノ酸配列を含むHPGGTの領域の一続きの連続アミノ酸配列と少なくとも80%同一であり、そのような領域が、(a)配列番号1に従ったアミノ酸配列のアミノ酸位置150〜200、又は(b)配列番号1に従ったアミノ酸配列のアミノ酸位置410〜480によって規定され、及びポリペプチドが、HPGGTの触媒活性を阻害することができる免疫応答を惹起するのに適する、前記ポリペプチドに関する。 (もっと読む)
機能改変フェニルアラニン脱水素酵素を用いた生体試料中のL−メチオニンの分析方法
【課題】L-メチオニンに対して基質特異性を有する改変型フェニルアラニン脱水素酵素を用いた、被検試料に含まれるL-メチオニンの高感度かつ簡便な分析方法、及び血液試料に存在するL-メチオニン以外のアミノ酸による測定誤差を抑制できる方法を提供する。
【解決手段】被検試料を、分岐鎖アミノ酸の少なくとも一部をオキソ酸に変換し得る処理に供する工程、処理後の被検試料を、改変型フェニルアラニン脱水素酵素と、レサズリン、ジアホラーゼ、および酸化型ニコチンアミドアデニンジヌクレオチド(NAD+)を含む反応液とともにインキュベーションする工程、及びインキュベーション後の反応液の発色を検出する工程を含む、被検試料に含まれるL-メチオニンの分析方法。L-メチオニンを分析するための被検試料に含まれる可能性がある分岐鎖アミノ酸の少なくとも一部をオキソ酸に変換することを含む、分岐鎖アミノ酸の被検試料中の量を低減する方法。
(もっと読む)
被験物の測定方法
【課題】B/F分離操作が不要であり、簡便かつ短時間での測定が可能であり、また酵素反応により検出シグナルを増幅することができることにより高感度の測定が可能である、被験物の測定方法を提供すること。
【解決手段】(1)(a)被験物、(b)該被験物と特異的に結合する反応部位及び酵素の補助因子を有する部位を有する第1反応体、並びに(c)該被験物と特異的に結合する反応部位及び前記酵素のアポ酵素部位を有する第2反応体、を反応させて、第1反応体と被験物と第2反応体との結合物を得る工程;及び(2)上記工程(1)で生成した第1反応体と被験物と第2反応体との結合物に、前記酵素の基質を接触させる工程を含む、被験物の測定方法。
(もっと読む)
グルタミニルシクラーゼに関連した新規遺伝子
本発明は、グルタミニルシクラーゼ(QC、EC 2.3.2.5)のアイソザイムである新規グルタミニル-ペプチドシクロトランスフェラーゼ様タンパク質(QPCTL)に、及びこれらのアイソザイムをコードする単離された核酸に関し、これらの全ては、新たな治療薬の発見のために、シクラーゼ活性を測定するために、及びこれらのグルタミニルシクラーゼアイソザイムに対する化合物の阻害活性を決定するために有用である。 (もっと読む)
肺癌に対する予後マーカーおよび治療標的
本発明は、肺癌の検出のための診断マーカーを提供する。特に本発明は、肺癌マーカー遺伝子、すなわちKIF4A、MAPJD、NPTX、またはFGFR1OPを提供する。本発明はさらに、肺癌を治療する化合物を同定するための方法およびキット、ならびに肺癌の予後または診断を予測するための方法を提供する。特に本発明は、肺癌の治療および予防において有用性が認められるKIF4A/ZNF549、KIF4A/ZNF553、MAPJD/MYC、またはFGFR1OP/WRNIP1の間の相互作用の阻害物質を同定するための方法およびキットを提供する。あるいは本発明は、治療標的としてのHAT複合体に結合したMAPJDを提供する。 (もっと読む)
HTLV−I特異的T細胞応答検定方法
【課題】ヒトでのHTLV−I特異的T細胞応答を追跡したり、種々の病態を示す患者のT細胞応答を調べるための、検査室レベルで簡便に測定できるHTLV−I特異的T細胞応答検定方法やそのための試薬を提供すること。
【解決手段】グルタチオン−S−トランスフェラーゼ(GST)−Tax融合タンパク質を用いる簡便なHTLV−I特異的T細胞応答の検出系を試作した。Taxはそれ自身が細胞増殖やアポトーシス抑制活性を持つためTaxタンパク質を3分割するようデザインした。HTLV−I感染者の末梢血単核球にGST−Tax融合タンパク質を添加して培養し、培養上清中のIFNγを測定することにより、HTLV−I特異的細胞性免疫応答を主要エピトープの部位に応じて感度良く測定する。
(もっと読む)
101 - 120 / 236
[ Back to top ]