Fターム[4B065AA87]の内容
微生物、その培養処理 (127,014) | 微生物の種類 (32,496) | 動植物細胞又は組織 (14,879)
Fターム[4B065AA87]の下位に属するFターム
植物細胞 (849)
植物組織、未分化細胞集団(カルス) (415)
動物細胞又は組織 (12,202)
Fターム[4B065AA87]に分類される特許
121 - 140 / 1,413
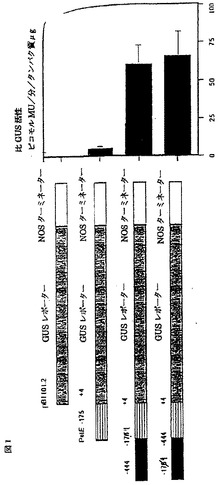
エンハンサーによって増大した植物における遺伝子の発現
【課題】1以上の遺伝子プロモーターに対するエンハンサーの提供。
【解決手段】エンハンサーはA及びT塩基に富むヌクレオチド配列であり、その含有するA及びT塩基の総量はこのヌクレオチド配列の50%を上回る。特定の配列はエンドウマメ・プラストシアニンプロモーターから同定され、該配列はA/Tのみのヌクレオチド配列と同様にエンハンサーとして活性である。
(もっと読む)
改変された糖タンパク質を生成するための方法
【課題】動物細胞(特に、ヒト細胞)により産生される糖タンパク質と同様のグリコシル化タンパク質(糖タンパク質)を産生させる方法および組成物の提供。
【解決手段】単細胞および多細胞の真菌を含む、N−グリカン含有の高マンノースを通常生成する下等真核生物は、Man5GlcAc2のようなN−グリカンまたはヒトグリコシル化経路に沿った他の構造を生成するために改変される。真菌糖タンパク質の所望でない複合体構造の特徴を生成する特定の酵素を発現しない系統、活性が所望される場合に真菌中に存在する条件下で最適な活性を有するかまたは最適な活性が達成される場合に細胞小器官を標的化するかであるように選択される外因性酵素を発現する系統。
(もっと読む)
ウシアデノウイルスタイプ3ゲノム
【課題】新規ウシアデノウイルス発現ベクター系を提供すること。
【解決手段】1つの実施態様において、本発明は、ウシアデノウイルスゲノムの以下の領域を利用する新規ウシアデノウイルス発現ベクター系に関する:ヌクレオチド4,092〜5,234、ヌクレオチド5,892〜17,735、ヌクレオチド21,198〜26,033およびヌクレオチド31,133〜34,445。これらの領域は、とりわけ、外来配列の挿入のため、転写調節配列および翻訳調節配列を含むDNA制御配列の提供のため、または被験体または生物学的サンプルにおいて、これらの領域によってコードされるウイルス核酸またはタンパク質の存在を検出する診断目的のために使用され得る。別の実施態様において、本発明は、E3領域において欠失(および必要に応じて異種配列の挿入を)含む組換えウシアデノウイルス(BAV)の構築、単離、および増殖のための新規の方法に関する。病原体の防御決定因子をコードする遺伝子の挿入物を含む組換えBAVは、全身および粘膜の免疫応答の増強を刺激し、そして病原体によるチャレンジから宿主動物を防御する。
(もっと読む)
プロテアーゼ
【課題】新規なプロテアーゼの提供。
【解決手段】ノカルジオプシス・ダソンビレイ亜種ダソンビレイDSM43235、ノカルジオプシス・プラシナDSM15649、ノカルジオプシス・プラシナ(以前はアルバ)DSM14010、ノカレジオプシスsp. DSM16424、ノカルジオプシス・アルカリフィラDSM44657及びノカルジオプシス・ルセンテンシスDSM44048由来のプロテアーゼ、及び相同プロテアーゼ;トランスジェニック植物及び非ヒト動物を包含する種々の宿主におけるそれらの組換え生成、及び動物飼料及び洗剤へのそれらの使用に関する。前記プロテアーゼは、酸安定性、アルカリ安定性及び/又は熱安定性である。
(もっと読む)
イネいもち病罹病性遺伝子Pi21および抵抗性遺伝子pi21ならびにそれらの利用
【課題】新規な植物の病斑進展制御遺伝子の提供ならびに該遺伝子を利用した植物の耐病性の改変方法を提供する。
【解決手段】連鎖解析によりイネの圃場抵抗性遺伝子pi21を単離することに成功し、該遺伝子の導入や発現制御により植物のいもち病圃場抵抗性を改変し得る可能性を見出した。これにより、植物に圃場抵抗性を効率的に付与することが可能となった。また、いもち病圃場抵抗性であるイネを早期に選抜することが可能となった。さらには圃場抵抗性に関与する遺伝子の組織発現特異性や発現レベルを変更することにより、抵抗性と実用性の高い特性を兼ね備えた品種を育成することからなる。
(もっと読む)
A型インフルエンザのヘマグルチニンに対する抗体およびその利用
【課題】A型インフルエンザウイルスのヘマグルチニンの各サブタイプを網羅的に認識する抗体を提供する。
【解決手段】A型インフルエンザウイルスのヘマグルチニンに対する抗体であって、A型インフルエンザウイルスのH1、H3、およびH5型のヘマグルチニンを何れも認識する抗体、抗体断片、当該抗体または抗体断片を利用するA型インフルエンザウイルスの検出試薬、検出キット、検出器具、および検出方法、当該抗体または抗体断片をコードする遺伝子。
(もっと読む)
修飾ヒトIGF−1/Eペプチドに対する抗体
【課題】本発明は、修飾ヒトインシュリン様増殖因子1タンパク質に免疫特異的に結合する抗体の製造および使用を提供すること。
【解決手段】本発明の高特異性抗体により上記課題を解決する。当該抗体は、修飾(例えば、hIGF−1/Ea 3mut)と内因性ヒトIGF−1タンパク質を区別できる。これらの抗体はhIGF−1またはhIGF−2とわずかしか、または全く交差反応しない。それらはまた齧歯類IGF−1またはIGF−2とわずかしか、または全く交差反応しない。本抗体はヒトまたは動物に投与されているIGF−1/Eペプチドの薬物動態学的(PK)/薬力学(PD)評価に使用できる。本発明の抗体を捕捉抗体として使用するサンドイッチELISAアッセイは、サンプル中の変異IGF−1/Eタンパク質を定量できる。
(もっと読む)
CD20抗体およびその使用
CD20は、B細胞の表面上で発現されるテトラスパニンファミリーの膜貫通タンパク質であり、末梢血ならびにリンパ系組織由来のB細胞上で見いだされる。CD20発現は、初期プレB細胞段階から形質細胞分化段階まで持続する。一方、造血幹細胞、プロB細胞、分化型形質細胞または非リンパ系組織上では見られない。正常なB細胞における発現に加えて、CD20は、非ホジキン(商標)リンパ腫(NHL)およびB細胞慢性リンパ性白血病(CLL)などのB細胞由来の悪性腫瘍で発現される。CD20発現細胞は、炎症をはじめとする他の疾患および障害に関与することが知られている。本発明は、優れた物理的および機能的特性を有する抗CD20抗体、形態および断片;免疫複合体、組成物、診断試薬、成長を阻害する方法、治療法、改善された抗体および細胞系;ならびにこれをコード化するポリヌクレオチド、ベクターおよび遺伝子構築物を含む。 (もっと読む)
癌の処置および検出において有用な109P1D4と称される、核酸および対応タンパク質
【課題】癌の治療、あるいは診断のための新規遺伝子109P1D4およびそのコードタンパク質、ならびにこれらの改変体の提供。
【解決手段】109P1D4は、正常な成人組織中で組織特異的な発現を示し、特定の癌において異常に発現される。109P1D4タンパク質をコードする単離されたポリヌクレオチド。該コードタンパク質。ポリヌクレオチドを含む、組換え発現ベクター。該発現ベクターを含む、宿主細胞。109P1D4と反応性である抗体。
(もっと読む)
FGF23融合ポリペプチドを使用する方法および組成物
本明細書は、加齢関連状態または代謝障害の予防または処置するための方法、キットおよび組成物に関する。本明細書の融合ポリペプチドは、FGF23またはその活性なフラグメントを含む。1つの態様において、融合ポリペプチドは、(a)線維芽細胞増殖因子23(FGF23)またはその機能的に活性な変異体もしくは誘導体を含むポリペプチドであって、FGF23が、Q156、C206およびC244の1つ以上の位置で変異を有するポリペプチド、および(b)減少したFc−ガンマ−受容体に対する親和性および/もしくは増加した血清半減期を有する修飾されたFcフラグメント、またはクロトータンパク質の少なくとも1つの細胞外サブドメインを含むポリペプチドのいずれか、またはそれらの機能的に活性な変異体もしくは誘導体、および、所望により(c)リンカーを含む。クロトー融合タンパク質は、種々の加齢関連状態および代謝障害の処置および予防において有用である。別の態様において、融合ポリペプチドは、FGF(例えば、FGF23)またはその機能的に活性な変異体もしくは誘導体、および修飾されたFcフラグメントまたはその機能的に活性な変異体もしくは誘導体を含む。融合ポリペプチドの種々の態様において、FGF23は、凝集およびプロテアーゼ介在開裂を減少させる変異を有する。 (もっと読む)
ヒトGタンパク質共役型受容体の内因性および非内因性型
【課題】受容体アゴニスト、逆アゴニストまたは部分アゴニストとしての候補化合物の直
接同定のために使用され得る受容体を提供すること。
【解決手段】本発明の特許明細書の中で開示される本発明は、膜貫通受容体に関し、さら
に具体的には内因性リガンドが未知であるヒトGタンパク質共役型受容体(「オーファン
GPCR受容体」)に関し、そして最も具体的には、構成的活性の証拠のためのヒトGP
CRの変異(非内因性)型に関する。
(もっと読む)
p−トルイル酸およびテレフタル酸を生合成するための方法および微生物
本発明は、(2−ヒドロキシ−3−メチル−4−オキソブトキシ)ホスホネート経路、p−トルイル酸経路および/またはテレフタル酸経路を有する非天然の微生物を提供する。本発明はさらに、(2−ヒドロキシ−3−メチル−4−オキソブトキシ)ホスホネート経路、p−トルイル酸経路またはテレフタル酸経路を生成するために上記生物を使用する方法を提供する。 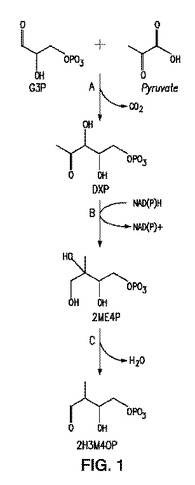 (もっと読む)
(もっと読む)
ワクチンにおいて使用するための組換えタンパク質、前記タンパク質に対する抗体、ならびに該タンパク質を含む診断法および療法
本発明は、タンパク質および/またはその断片および誘導体、ならびにワクチンとしての、およびバイオテクノロジー法におけるその使用に関する。ワクチンには、特に、ウシにおける趾皮膚炎から単離されるトレポネーマ属(Treponema)種における免疫原性タンパク質が含まれる。本発明はさらに、前記タンパク質またはその断片に対して作製される抗体、ならびに抗体がウシにおける趾皮膚炎の徴候として検出される診断法における前記タンパク質の使用にも関する。
なし
(もっと読む)
アミド化生成物の調製に有用な酵素を発現させるための細胞株
【課題】ペプチジルグリシンα−アミド化モノオキシゲナーゼ(PAM)、またはその2つの触媒ドメインの一方を発現させるための細胞株を提供する。
【解決手段】非動物供給源の低タンパク質組織培養培地を用いつつ、高レベルの酵素発現が達成される。ロバストな2工程の下流精製により高い酵素純度がもたらされる。得られるPAMまたはそのPHM触媒ドメインは、X−α−ヒドロキシ−GlyまたはX−NH2(Xは、グリシン基が共有結合し得るカルボニル基を有するペプチドまたは任意の化学的化合物である)へのX−Glyの変換の酵素的変換を触媒するために使用される。また、好ましい細胞株の調製方法も示す。
(もっと読む)
癌抗原NYESO−1由来の新規MHCクラスII拘束T細胞エピトープ
【課題】癌抗原NY−ESO−1由来の新規MHCクラスIIエピトープの同定及び単離方法の提供。
【解決手段】NY−EsO−1由来の新規癌ペプチドであるMHCクラスIIエピトープは、HLAクラスII拘束様式で、特にHLA−DR又はHLA−DP拘束様式でCD4+Tリンパ球によって認識される。少なくとも1つの単離されたNY−ESO−1 HLA−クラスI拘束T細胞癌ペプチドをコードする核酸配列遺伝子産物は、癌患者の予防、治療及び診断のための免疫治療的戦略の有望な候補である。
(もっと読む)
JCウイルス遺伝子の発現を抑制するための組成物および方法
【課題】細胞自身のRNAi機構を使用してJCウイルス中の遺伝子を選択的かつ効果的にサイレンシングする薬剤であって、高い生物活性と生体内安定性の両方を有し、JCウイルス感染によって媒介される病理過程の治療に使用されるJCウイルスの複製を効果的に阻害できる薬剤を提供する。
【解決手段】本発明は、JCウイルス遺伝子(JCウイルスゲノム)の発現を抑制するための二本鎖構造のリボ核酸(dsRNA)に関し、該dsRNAは、長さが30ヌクレオチド未満、通常は長さが19〜25ヌクレオチドでJCウイルス遺伝子の少なくとも一部にほぼ相補的なヌクレオチド配列を有するアンチセンス鎖を含む。本発明はまた、該dsRNAを医薬として許容可能な担体とともに含む医薬組成物;該医薬組成物を用いてJCウイルス発現を原因とする疾患を治療する方法;ならびに細胞内におけるJCウイルス遺伝子の発現を抑制する方法にも関する。
(もっと読む)
抗HCV抗体についてのイムノアッセイ
【課題】抗HCV抗体についてのイムノアッセイを提供すること。
【解決手段】本発明は、複数エピトープ融合抗原との組み合わせでのNS3/4aコンフォメーションエピトープの使用が、初期のHCVセロコンバージョンを検出するための高感度かつ確実な方法を提供するという知見に一部基づいている。本明細書中で記載されるアッセイはまた、6つの公知のHCV遺伝子型のいずれかによって引き起こされるHCVを検出し得る。複数エピトープ融合タンパク質の使用はまた、マスキングの問題を低減し、基質単位面積当たりのより多数のエピトープを可能にすることによって、抗体の検出における感度を改善し、そして選択性を改善するというさらなる利点を有する。
(もっと読む)
成長因子複合体ならびに細胞の移動および増殖の調節
【課題】成長因子受容体に結合し活性化することができる、成長因子、例えばIGF−I、IGF−II、VEGFまたはPDGF、あるいは少なくとも該成長因子のドメインと、ビトロネクチンまたはフィブロネクチンのインテグリン受容体結合ドメインとを含んでなる単離タンパク質複合体が提供される。
【解決手段】 これらのタンパク質複合体は、オリゴタンパク質複合体の形態でも、単一の合成タンパク質の形態でもよく、単一の合成タンパク質の場合、成長因子およびビトロネクチン配列またはフィブロネクチン配列はリンカー配列により連結される。特定の形態においては、ビトロネクチン配列またはフィブロネクチン配列はヘパリン結合ドメインおよびポリ陰イオン性ドメインのうち少なくともいずれかを含まない。細胞の移動および増殖のうち少なくともいずれかを刺激または誘導するためのこれらのタンパク質複合体の使用も提供され、創傷治癒、組織工学、美容的および治療的処置、例えば皮膚置換および皮膚補充、ならびに上皮細胞の移動が必要とされる熱傷の治療における用途を有し得る。その他の実施形態では、本発明は、特に乳がんに関するがん細胞転移の抑制を提供する。
(もっと読む)
変異ガウシアルシフェラーゼ
【課題】リフォールディング効率が良くかつ発光の減衰時間が長い変異ガウシアルシフェラーゼの提供。
【解決手段】ガウシアルシフェラーゼに含まれる、特定な配列からなるアミノ酸配列において59番目のシステインが他のアミノ酸と置換したアミノ酸配列からなる変異ガウシアルシフェラーゼ。
(もっと読む)
細胞の選択的溶解
本発明は、細菌などの微生物を含んでなるサンプル中で細胞を選択的に溶解するための方法および装置を開示する。選択的溶解は、アルカリ性条件下で、非イオン性界面活性剤中でサンプルをインキュベートすることにより得られる。 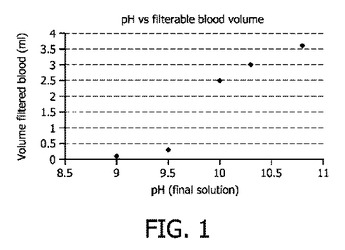 (もっと読む)
(もっと読む)
121 - 140 / 1,413
[ Back to top ]