Fターム[4C057LL43]の内容
糖類化合物 (12,552) | 1個の異項原子を糖類基と共有する複素環 (1,626) | Nを共有 (1,610) | 異項原子としてNのみを含有する複素環 (1,586) | プリン (738) | 糖がアラビノシル (10)
Fターム[4C057LL43]に分類される特許
1 - 10 / 10
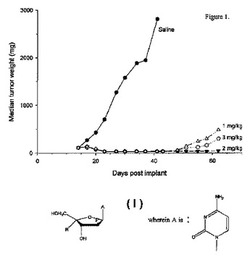
2’−フルオロアラビノヌクレオシド及びその使用
【課題】2’−フルオロアラビノヌクレオシド及びその使用。
【解決手段】ある特定の2’−フルオロアラビノヌクレオシド類を用いて癌を治療する方法を提供する。さらに、下記式:
[化1]
(式中、Aは
[化2]
であり、Rはアルキルである)で表される化合物、及びその薬学的に許容される塩、及びその化合物を含有する医薬組成物を提供する。
(もっと読む)
抗ウィルス薬
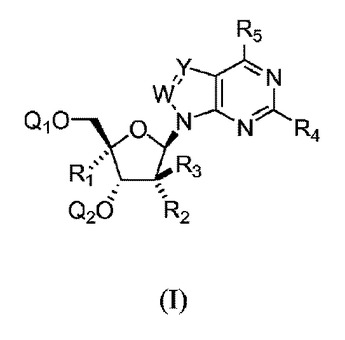
本明細書で定義の構造式(I)の化合物およびそれの製薬上許容される塩が、HCV感染の予防および/または治療での使用について説明される。式(I)の新規化合物およびそれを含む医薬製剤についても記載されている。
【化1】
 (もっと読む)
(もっと読む)
1−リン酸化糖誘導体のアノマーの選択的な製造法並びにヌクレオシドの製造法
【課題】フラノースやピラノースといった糖の骨格の違い、デオキシ糖といった置換基の有無、あるいは天然型や非天然型といった糖の種類に影響されることの無い、汎用性の高い、アノマー選択的な1−リン酸化糖誘導体ならびにヌクレオシドの製造方法を得ること。
【解決手段】1−リン酸化糖誘導体のアノマー混合物を加リン酸分解および異性化し、一方を結晶化することで平衡を傾け、選択的に望む異性体のみを製造する。さらに、ヌクレオシドホスホリラーゼの作用により、得られた1−リン酸化糖誘導体と塩基より、高い立体選択性と収率でヌクレオシドを製造する。
(もっと読む)
マークされたプリン誘導体の製造方法、該プリン誘導体、およびその使用
【課題】本発明は、2−ニトロプリン誘導体のフッ素化工程を含む、放射性同位体18Fでマークされた2−フルオロプリンの製造方法に関する。本発明は、本発明またはそのさまなざまな使用による方法により得られる、放射性同位体18Fでマークされた2−フルオロプリン誘導体を含む。
【解決手段】本発明の18F放射性同位体でマークされた2−フルオロプリン誘導体の製造方法は、任意に保護された2−ニトロプリン誘導体を、[18F]でマークされたフッ化物イオン源と反応させることを含むフッ素化工程と、任意に続く、脱保護工程とを含む。
(もっと読む)
蛍光標識としてのスルホン化ジアリールローダミン色素
【課題】スルホン化ジアリールローダミン化合物として、ヌクレオシド、ヌクレオチド、ポリヌクレオチド、およびポリペプチドの蛍光標識として有用であるものを提供すること。
【解決手段】本発明の化合物は、蛍光核酸分析(例えば、自動化DNA配列決定)およびフラグメント分析、ハイブリダイゼーションアレイにおけるプローブハイブリダイゼーションの検出、核酸増幅産物の検出などの分野における特定の用途を見出している。本発明の別の局面は、エネルギー移動色素化合物を包含し、この化合物は、第一の波長において光を吸収し、かつそれに応答して励起エネルギーを放射し得る、ドナー色素;このドナー色素によって放射された励起エネルギーを吸収し、かつそれに応答して第二の波長において蛍光を発し得る、アクセプター色素;ならびに、このドナー色素およびアクセプター色素を連結するためのリンカー、を含有する。
(もっと読む)
N2−キノリン又はイソキノリン置換のプリン誘導体及びその製造方法並びにその用途
本発明は、N2−キノリン又はイソキノリン置換のプリン誘導体、及び前述化合物を含む医薬組成物を開示する。本発明の化合物は、毒性が低く、抗癌スペクトルが広く、抗癌活性が高く、かつ安定性に優れている。本発明はまた、同化合物の製造方法を開示する。 (もっと読む)
抗菌活性および抗癌活性を有するヌクレオチド
本発明は、R1〜R6およびXが記載される値のいずれかを有する式(I)の化合物、ならびにかかる化合物を含む医薬組成物、ならびにかかる化合物を投与することを含む治療方法を提供する。本発明はまた、有効量の式Iの化合物そのまたは薬学的に受容可能な塩を、かかる治療を必要とする動物(例えば哺乳動物)に投与することを含む、動物におけるウイルス感染を治療するための方法を提供する。本発明はまた、有効量の式Iの化合物そのまたは薬学的に受容可能な塩を、かかる治療を必要とする動物に投与することを含む、動物におけるHCVを治療するための方法を提供する。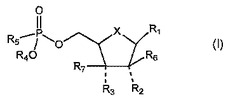
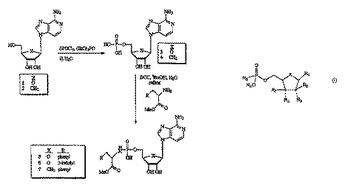 (もっと読む)
(もっと読む)
1,3−プロパン−1−アリールジオールの新規環状リン酸ジエステルおよびそのプロドラッグへの使用
式(I)の化合物、
【化1】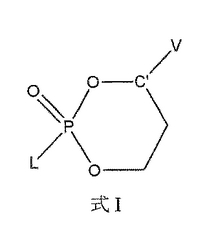
〔式中、VおよびLは相互にトランスであり;Vは炭素環式アリール、置換炭素環式アリール、ヘテロアリール、および置換ヘテロアリールよりなる群から選択され;Lは、ハロゲン、スルホン酸アルキル、1個から2個の置換基で任意に置換されてもよいアリールオキシ、含窒素ヘテロアリール、およびN-ヒドロキシ化窒素を含むヘテロアリールよりなる群から選択される脱離基を表す。〕
およびその塩、その調製および合成用中間体、およびプロドラッグの合成におけるそれらの使用。 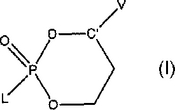 (もっと読む)
(もっと読む)
9−β−アノマー性ヌクレオシド類似体の調製方法
9−β−アノマー性ヌクレオシド類似体の位置選択的及び立体選択的合成を十分に増進させるための方法を説明する。6−置換プリン塩基への糖部分の導入は、9−β−D−又はL−プリンヌクレオシド類似体のみが得られるように実施された。糖部分のこの位置選択的及び立体選択的導入により、実質上7位―位置異性体の形成なしに高収率でヌクレオシド類似体、特に2’−デオキシ、3’−デオキシ、2’−デオキシ2’−β−フルオロ及び2’,3’−ジデオキシ−2’−β−フルオロプリンヌクレオシド類似体を合成できるようになる。該化合物は薬剤又は薬剤に対する中間体である。 (もっと読む)
α−1−リン酸化2−デオキシ−2−フルオロアラビノシド及び2’−デオキシ−2’−フルオロ−β−D−アラビノヌクレオシドの製造法
式(I):
【化1】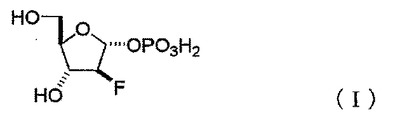
で表されるα−1−リン酸化2−デオキシ−2−フルオロアラビノシド又は式(V’):
【化2】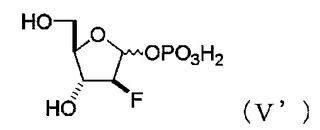
で表される1−リン酸化2−デオキシ−2−フルオロアラビノシドのαβ体混合物、及び塩基に、ヌクレオシドホスホリラーゼを作用させることを特徴とする、式(II):
【化3】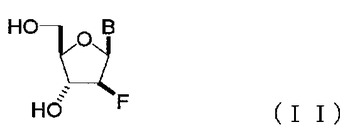
(式中、Bは塩基を示す。)
で表される2’−デオキシ−2’−フルオロ−β−D−アラビノヌクレオシド、特に2’−デオキシ−2’−フルオロ−β−D−アラビノプリンヌクレオシドを簡便、かつ高立体選択的に高収率で製造できる。
(もっと読む)
1 - 10 / 10
[ Back to top ]