Fターム[4C063EE05]の内容
Fターム[4C063EE05]に分類される特許
141 - 160 / 645
有機半導体材料、有機半導体薄膜および有機薄膜トランジスタ
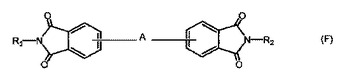
有機半導体材料は、下記一般式(F)で表される。
式中のAは1個またはそれ以上の芳香族環からなる環状共役系骨格構造を、R1、R2は各々独立に、置換基を有してもよいアルキル基を表す。
この有機半導体材料は、高い電子移動度および高いオン/オフ比を有すると共に、その溶液を用いた溶液塗布法により有機半導体薄膜を形成することができる。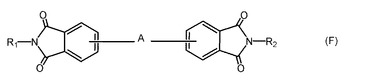
 (もっと読む)
(もっと読む)
バルサルタンの製造方法
【課題】本発明は、バルサルタンの新規製造法を提供することを目的とする。
【解決手段】(i)酸性条件下で、式(iva)で示される化合物またはその塩を、式(ivb)で示される化合物と反応させること;(ii)遷移金属触媒の存在下で、得られた式(ivc)で示される化合物を、式(ivd)で示される化合物と反応させること;(iii)酸で処理することにより、得られた式(ive)で示される化合物から連続してもしくは単一の工程で保護基を除去すること;および(iv)得られた式(IIa')で示される化合物またはその塩を単離することを含む製造法を提供することにより、上記課題を解決する。
(もっと読む)
反応性複素環置換7−ヒドロキシクマリンおよびその複合体
【解決手段】化学反応性の水溶性複素環置換7−ヒドロキシクマリン色素、その生体複合体、およびその使用方法を提供する。
【効果】反応性複素環置換7−ヒドロキシクマリン色素から得られた複合体は、405nmでのその強力な吸収と高い蛍光量子収率とに起因して、励起源として紫色レーザーを備えたフローサイトメーターを用いた生物学的化合物を分析に使用され、抗体や核酸プローブなどのバイオポリマー検出試薬用蛍光標識として特に有用である。
(もっと読む)
アルファへリックスミメティック及び関連の方法
アルファヘリックスミメティック構造体及び式(I)(一般式及び各記号の定義は明細書中で定義された通りである)で表される化合物、それらに関連する化学ライブラリー、並びにそれらに関連する方法、が開示される。医学的状態(例、癌疾患、線維症)の治療におけるこれらの化合物の適用、及び当該ミメティックを含む医薬組成物が更に開示される。 (もっと読む)
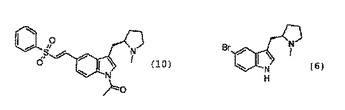
3−{[(2R)−1−メチルピロリジン−2−イル]メチル}−5−[2−(フェニルスルホニル)エチル]1H−インドールの合成
本発明は、エレトリプタンの名前で知られる薬物である、3−{[(2R)−1−メチルピロリジン−2−イル]メチル}−5−[2−(フェニルスルホニル)エチル]−1H−インドール、またはその塩の合成に関する。特に本発明は、エレトリプタン又はその塩を合成する方法に関し、以下のステップを含む:a)ジカルボン酸を用いて化学式(6)の中間体を塩化し、誘導体塩を得るステップと、b)任意で、ステップa)に従って得られた前記粗塩を、溶媒結晶化により精製して、化学式(6)の中間体の精製した塩を得るステップと、c)ステップa)に従った化学式(6)の中間体の前記塩、又はステップb)に従った前記精製した塩を、化学式(10)の中間体に転換するステップと、d)化学式(10)の中間体をエレトリプタン又はその塩に転換するステップ。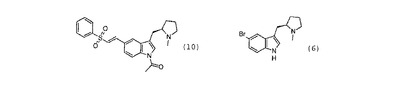
 (もっと読む)
(もっと読む)
ヘテロ芳香環を有するカルバゾール誘導体およびヘテロ芳香環を有するカルバゾール誘導体を用いた発光素子、発光装置、および電子機器
【課題】励起エネルギーの大きな物質、特に、可視光を発する燐光性化合物の励起三重項エネルギーより広いエネルギーギャップを有する化合物を提供することを課題とする。また、バイポーラ性を有する化合物を提供することを課題とする。また、発光素子の素子特性を向上させることを課題とする。さらに、消費電力が少なく、駆動電圧の低い発光装置および電子機器を提供することを課題とする。
【解決手段】電子輸送性を有するヘテロ芳香環であるオキサジアゾール骨格またはキノキサリン骨格と、正孔輸送性を有するカルバゾール骨格を同一分子に有するヘテロ芳香環を有するカルバゾール誘導体を提供する。また、発光層やキャリア輸送層に前記ヘテロ芳香環を有するカルバゾール誘導体を用いた発光素子を提供する。また、前記発光素子を適用した発光装置、および電子機器を提供する。
(もっと読む)
アルキル化されたインドール類の製造方法
【課題】特殊な装置が不要で、幅広い原料を使用でき、高収率で2位又は3位がアルキル化されたインドール類を製造できる方法の提供。
【解決手段】下記一般式(1)で表されるインドール類と、下記一般式(2)で表される化合物と、ヒドリド供与体とを反応させることを特徴とする下記一般式(3)で表される化合物の製造方法(式中、R1及びR2はそれぞれ独立に水素原子、脂肪族基、アリール基、ヘテロアリール基、アリールアルキル基、アルキルアリール基又はトリアルキルシリル基であり;R3は水素原子以外の一価の基であり;R4及びR5はそれぞれ独立に水素原子、又は置換基を有していても良いアルキル基、アリール基若しくはヘテロアリール基であり、相互に結合して環を形成していても良く;mは0〜4の整数であり;mが2〜4である場合には、複数のR3は互いに同一でも異なっていても良い。)。
[化1] (もっと読む)
(もっと読む)
ピリジル置換ピラゾールを調製するための方法
本発明は、アセチレンケトンをピリジルヒドラジン誘導体と反応させて1−ピリジル置換ジヒドロ−1H−ピラゾールを形成させる段階、続いて前記ピラゾールを反応させて脱水によって1−ピリジル置換トリハロゲンメチルピラゾールを形成させる段階、および続いて前記ピラゾールを加工する段階を含む、1−ピリジル置換ピラゾールを製造するための方法に関する。 (もっと読む)
アミノインダゾール誘導体を合成するための中間体化合物
【課題】キナーゼ阻害剤であるアミノインダゾール誘導体を合成するための中間体化合物を提供する。
【解決手段】下記式(I)で表されるアミノインダゾール誘導体、その製薬上許容される塩等を合成するためのインダゾール中間体化合物。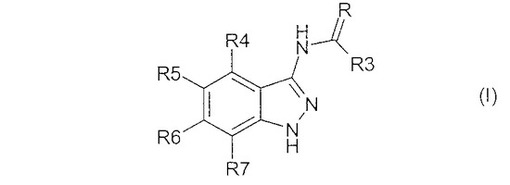
[式中、RはO,SまたはNHのいずれかであり、R3〜R7は相互に独立して(1〜6C)アルキル基、アリール基、等である。]
(もっと読む)
ドキサゾシン及びその塩の製造方法
本発明は、ドキサゾシン又はその塩の製造方法に関する。 (もっと読む)
縮合三環式スルホンアミドの製造プロセス
本発明は、融合した三環式スルホンアミド類似体、例えば、置換または非置換5−(アリール−スルホニル)−4,5−ジヒドロ−1H−ピラゾロ[4,3−c]キノリンおよび5−(ヘテロアリール−スルホニル)−4,5−ジヒドロ−1H−ピラゾロ[4,3−c]キノリンの生産のための方法、すなわち、拡張可能または大規模プロセスを提供する。本発明の典型的な方法は、炭素−窒素結合が形成され、少なくとも1つの有機リガンド、例えば、DMEDAを含有する銅系触媒を用いる、分子内環化ステップを含む。本発明は、本発明の方法において、中間体として有用な化合物をさらに提供する。 (もっと読む)
新規有機電界発光化合物およびこれを使用する有機電界発光素子
新規の有機電界発光化合物およびこれを含む有機電界発光素子が開示される。有機電界発光素子の正孔注入層もしくは正孔輸送層に含まれる場合に、開示された有機電界発光化合物はその素子の駆動電圧を低減させると共に、発光効率を向上させることができる。
【代表図】なし
(もっと読む)
4−(3’−クロロ−4’−フルオロアニリノ)−7−メトキシ−6−(3−モルホリノプロポキシ)キナゾリンの製造方法
【課題】薬理学的に有効なキナゾリン誘導体の製造に有用な手段を提供する。
【解決手段】式II及び式IIIの化合物の中間体はそれぞれ、キナゾリン誘導体、4−(3’−クロロ−4’−フルオロアニリノ)−7−メトキシ−6−(3−モルホリノプロポキシ)キナゾリンのような薬理学的に有効なキナゾリン誘導体の製造方法に有用である。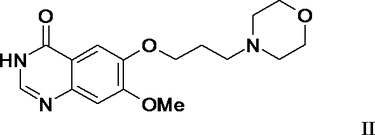
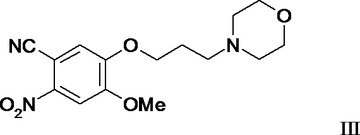 (もっと読む)
(もっと読む)
有機発光デバイス
【課題】 本発明は、少なくとも2色以上の有機電界発光素子を有する有機EL表示装置において、いずれの発光色についても高効率及び長寿命の有機発光デバイスを提供することを課題とする。
【解決手段】 少なくとも2色以上の有機電界発光素子を有する有機EL表示装置において、当該2色以上の有機電界発光素子の正孔阻止層が、いずれも同一の正孔阻止材料を含有し、該正孔阻止材料が当該2色以上の有機電界発光素子の発光層に含まれる、いずれか一つの化合物が有する縮合多環炭化水素及び/又は芳香族複素環と同じ環構造を、部分構造として有する化合物であることを特徴とする、有機発光デバイス。
(もっと読む)
ヒスタミンH3受容体モジュレーターの調製プロセス
本発明は、処置(例えば認知障害、睡眠障害及び/又は精神障害の処置)において、ヒスタミンH3受容体モジュレーターを調製するための新規プロセスを目的とする。式(I)。
【化1】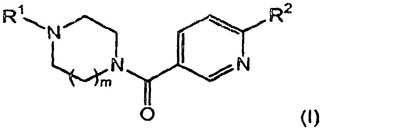
 (もっと読む)
(もっと読む)
ピラゾール誘導体の調製方法
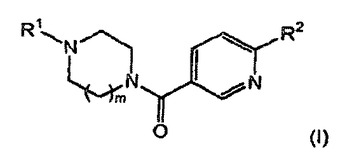
【化1】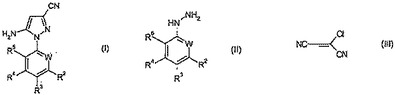
本発明は、式(I)〔式中、Wは、窒素又はCR1であり;R1、R2、R4及びR5は、それぞれ独立して、水素、ハロゲン、C1-C6-アルキル、C1-C6-ハロアルキル、C1-C6-アルコキシ、C1-C6-ハロアルコキシ、R7S(O)n、ニトロ、シアノ及びペンタフルオロチオから選択され;R3は、水素、ハロゲン、C1-C6-アルキル、C1-C6-ハロアルキル、C1-C6-アルコキシ、C1-C6-ハロアルコキシ、R7S(O)n、ニトロ、シアノ、ペンタフルオロチオ又はフェニル(ここで、該フェニルは、置換されていないか、又は、ハロゲン、C1-C6-アルキル、C1-C6-ハロアルキル、C1-C6-アルコキシ、C1-C6-ハロアルコキシ、R7S(O)n、ニトロ、シアノ及びペンタフルオロチオからなる群の同一であるか若しくは異なっている1〜5のメンバーでで置換されている)であり;R7は、C1-C6-アルキル又はC1-C6-ハロアルキルであり;及び、nは、0、1又は2である〕で表されるピラゾール誘導体を調製する方法に関し、ここで、該方法は、式(II)〔式中、W、R2、R3、R4及びR5は、式(I)で表されるピラゾール誘導体に関して定義されているとおりである〕で表されるヒドラジンを式(III)で表される化合物と反応させることを特徴とする。
(もっと読む)
スルホニルキノリンの製造方法
式(I)の化合物の非常に収束的な製造方法が開示され、これらの化合物は、C型肝炎ウイルス(HCV)感染症の治療に効能のある活性剤の製造における中間体として有用である。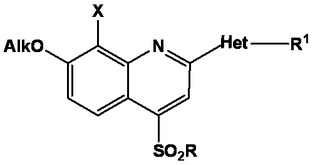
(I) 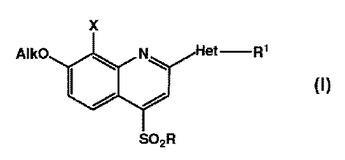 (もっと読む)
(もっと読む)
エナミノカルボニル化合物の新規な製造方法
本発明はエナミノカルボニル化合物の製造方法に関する。該方法において、式(II)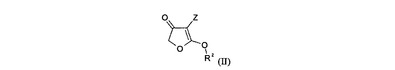
の化合物はブレンステッド酸の存在下で式(III)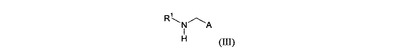
の化合物と反応し、式中、A、R1、R2、およびZの基は本記載で言及される通りに定義
される。 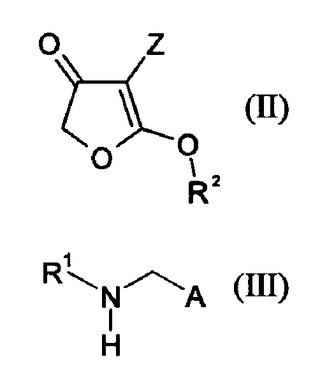 (もっと読む)
(もっと読む)
医薬を合成するための中間体化合物およびその製造方法
医薬を合成するための中間体として有用である光学活性2−{4−(5−置換オキサジアゾリル)フェニル}モルホリンの製造方法が提供される。上記方法は、以下の工程1)から4)を含む:
1)ブロモフェニルモルホリンとヘキサシアノ鉄(II)酸塩またはその水和物とを、110℃から140℃の温度で、極性非プロトン性溶媒単独または極性非プロトン性溶媒と他の極性非プロトン性溶媒もしくは炭化水素溶媒との組合せ中においてNa2CO3、有機リン化合物、およびパラジウム触媒を含む反応混合物中で反応させて、シアノフェニルモルホリンを得る工程;2)シアノフェニルモルホリンと、ヒドロキシルアミンまたはヒドロキシルアミン塩酸塩とを、10℃から40℃の温度で、非プロトン性極性溶媒中で反応させて、ヒドロキシルアミン誘導体を得る工程;3)ヒドロキシルアミン誘導体と、ハロゲン化脂肪族アシル、ハロゲン化芳香族アシル、脂肪族アシル無水物および芳香族アシル無水物からなる群から選択されるアシル化試薬とを反応させる工程、ならびに4)工程3)の後に得られた混合物を60℃から140℃の温度に保ち、2−{4−(5−置換オキサジアゾリル)フェニル}モルホリンを得る工程。
(もっと読む)
3環式化合物のエナンチオ選択的アルキル化
【課題】ファルネシルタンパク質トランスフェラーゼのインヒビターである化合物を調製するのに有用な中間体である式(I)の化合物を調製するためのプロセスを提供する。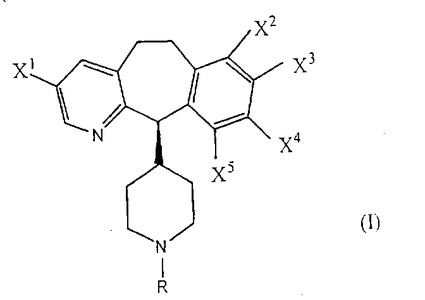
【解決手段】ベンゾ[5,6]シクロヘプタ[1.2−b]ピリジン誘導体が以下(a)〜(c)で任意の順序で処理される:(a)非求核性強塩基;(b)キラルアミノアルコール;および(c)4位に脱離基を有するピペリジン誘導体を有する化合物。
(もっと読む)
141 - 160 / 645
[ Back to top ]