Fターム[4C069BB02]の内容
ピロール系化合物 (8,574) | 置換炭化水素 (2,780) | 複素環と置換基を結ぶ炭化水素部分 (1,066) | 脂肪族鎖 (588)
Fターム[4C069BB02]の下位に属するFターム
不飽和脂肪族鎖 (53)
Fターム[4C069BB02]に分類される特許
201 - 220 / 535
非晶質アトルバスタチン・カルシウムの形成方法
【課題】非晶質アトルバスタチンの現在の製造方法は、毒性又は環境の観点から最適ではない溶媒を含み、さらに、現在の方法は、製造能力の点で最適ではなく、そして大規模合成に好適ではない。以上の課題を解決するための非晶質アトルバスタチン・カルシウムの改良された製造方法の提供。
【解決手段】以下のステップ:(a)溶媒中にアトルバスタチンを溶解して溶液を形成し;そして(b)上記溶液を、非溶媒とヒドロキシル溶媒を含む混合物に添加して、溶液からアトルバスタチンを沈澱させることによって非晶質アトルバスタチンを得る、を含む方法により形成される、非晶質アトルバスタチン・ヘミ−カルシウム塩トリヒドレート。
(もっと読む)
電位依存性ナトリウムチャネルのモジュレーターとしてのプロリンアミド誘導体
本発明は、電位依存性ナトリウムチャネルの変調によって媒介される疾患または状態を治療または予防するための式(I):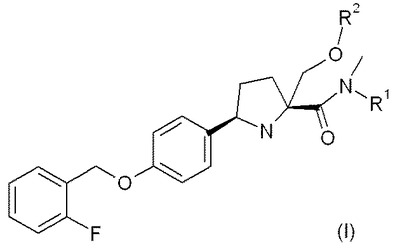
[式中、
R1はHまたはCH3であり;
R2はHまたはCH3である]
で示される第4級α−アミノカルボキシアミド誘導体およびその医薬上許容される塩または溶媒和物に関する。 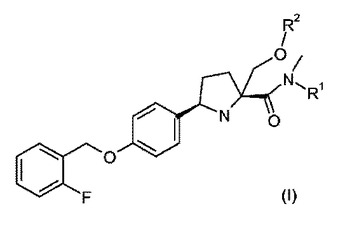 (もっと読む)
(もっと読む)
新規方法
本発明は、薬学的に活性な化合物、特にレニン阻害剤、例えばアリスキレンの合成に有用な新規方法、新規方法工程および新規中間体に関する。とりわけ、本発明は、式(I):
〔式中、R1およびActは、本明細書で定義した通りである。〕の化合物またはその塩の製造方法、およびこの方法におけるこの化合物ならびに中間体の製造工程に関する。 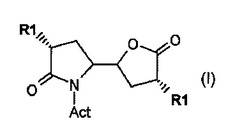 (もっと読む)
(もっと読む)
パーフルオロアルキル基を有する複素環化合物およびその製造方法
【課題】パーフルオロアルキル基を有する複素環化合物の製造方法を開発する。
【解決手段】
パーフルオロアルキル基を有する複素環化合物の製造方法は、
一般式(1)
[式中、Y1は、酸素原子等を示し、Y2、Y3、Y4およびY5は各々独立に、窒素原子、または、炭素数1から4のアルキル基等で置換されていても良い炭素原子を示す。]で表される複素環化合物を、一般式(2) R1aS(=O)R1b [式中、R1aおよびR1bは、炭素数1から12のアルキル基等を示す。]で表されるスルホキシド類、過酸化物、鉄化合物および酸の存在下に、一般式(3) Rf−X [式中、Rfは、炭素数1から6のパーフルオロアルキル基を示し、Xは、ハロゲン原子を示す。]で表されるハロゲン化パーフルオロアルキル類と反応させる。
(もっと読む)
ビシクロアミノアセチルピロリジンカルボニトリル誘導体の製造方法およびその製造中間体
【課題】エステル基を有するアミノアセチルピロリジンカルボニトリル誘導体の安全な製造方法を提供する。
【解決手段】
式1:
【化1】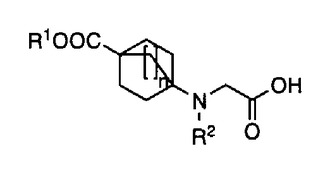
(式中R1は、置換されていてもよいC1〜C6のアルキル基、置換されていてもよいC3〜C6のシクロアルキル基、置換されていてもよいアリールメチル基、置換されていてもよいアリールエチル基、置換されていてもよい芳香族炭化水素、置換されていてもよい芳香族へテロ環、または置換されていてもよい脂肪族へテロ環を示し;
R2は水素原子または窒素原子の保護基を示し;
nは1または2を示す)で表されるビシクロアルキルアミノ酢酸誘導体。
(もっと読む)
ラクタム置換ジカルボン酸およびそれらの使用
本発明は、新規のラクタム置換ジカルボン酸誘導体、それらの製造方法、疾患の処置および/または予防におけるそれらの使用に関する。本発明は、また、疾患の処置および/または予防用の、特に心血管障害の処置および/または予防用の医薬の製造における該物質の使用に関する。 (もっと読む)
P2X7モジュレーターとしてのピロールおよびイソインドールカルボキサミド誘導体
本発明は、式(I):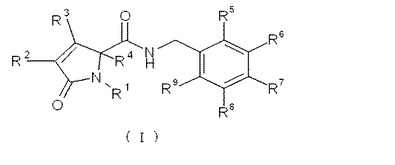
[式中:
R2は、水素、ハロゲン、C1−6アルキル、C6−10アリールメチル−、C2−6アルケニル、C2−6アルキニルまたはC3−6シクロアルキルメチル−を意味し、該C1−6アルキル、C6−10アリールメチル−、C2−6アルケニル、C2−6アルキニルまたはC3−6シクロアルキルメチル−はいずれも、1、2または3個のハロゲン原子により置換されていてもよく;
R3は、水素、フッ素またはメチルを意味し;
あるいは、R2およびR3は、それらが結合している炭素原子と一緒になって、C1−6アルキル、C2−6アルケニルおよびC2−6アルキニルからなる群から選択される、同じでも異なっていてもよい、1、2または3個の置換基により置換されていてもよいベンゼン環を形成する]
で示される化合物またはその医薬上許容される塩に関する。該化合物またはその塩は、P2X7受容体機能をモジュレートし、P2X7受容体でのATP効果に拮抗することができる。また、本発明は、P2X7受容体により介在される障害、例えば疼痛、炎症または神経変性疾患の治療における、かかる化合物またはその塩もしくは医薬組成物の使用を提供する。 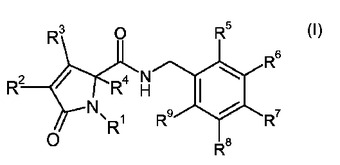 (もっと読む)
(もっと読む)
(メタ)アクリル酸エステルの製造方法
【課題】(メタ)アクリル酸エステルを簡易かつ高収率で得るための製造方法を提供する。
【解決手段】(メタ)アクリル酸またはそのエステルと、炭素数2〜4のアルキレン基を有するN置換ピロリドン誘導体とを、固体触媒の存在下で反応させて、エステル基末端にピロリドン基を有する(メタ)アクリル酸エステルを合成する段階を有する、(メタ)アクリル酸エステルの製造方法である。該固体触媒がイオン交換樹脂であることが好ましい。
(もっと読む)
ピロリルヘプタン酸誘導体の新規な結晶形態
本発明は、[R-(R*,R*)]-2-(4-フルオロフェニル)-β,δ-ジヒドロキ-5-(1-メチルエチル)-3-フェニル-4-[(フェニルアミノ)カルボニル]-1H-ピロール-1-ヘプタン酸ヘミカルシウム塩の結晶形態D1およびD2、およびその水和物を提供する。結晶形態D1およびD2は、それぞれ図1および3に記載のX線粉体回折ピークを有する。さらに、本発明は、結晶形態の製造方法および結晶形態を含んでなる医薬組成物を提供する。結晶形態は商業的規模で生産することができ、優れた安定性を示す。 (もっと読む)
Nrf2活性化剤
【課題】Nrf2の活性化が治療に有効である疾患の治療に用いられる化合物及び組成物の提供。
【解決手段】ブナハリタケ由来の化合物を含んでなる、Nrf2の活性化が治療に有効である疾患の治療に用いられる組成物が提供される。具体的に例示すると次の化合物が挙げられる。4−(1−ヒドロキシ−エチル)−3−メチル−ジヒドロ−フラン−2−オン、5−ヒドロキシ−3,4,5−トリメチル−5−H−フラン−2−オン、酢酸1−(4−メチル−5−オキソ−テトラヒドロ−フラン−3−イル)−エチルエステル、(5−エチル−テトラヒドロ−フラン−2−イル)−酢酸。
(もっと読む)
メルカプトチアゾールの製造方法および製造中間体
【課題】医薬品として有用な化合物の、工業的に有利な製造法および中間体の提供。
【解決手段】式(7)で表される化合物(式中、nは、1または2を表し、X1およびX2は、それぞれ独立して、ハロゲン原子を表す。)の製造方法。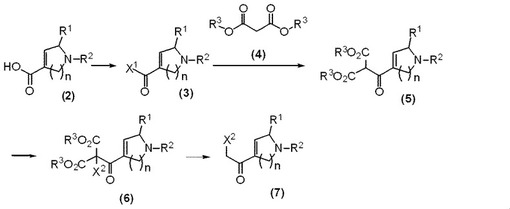 (もっと読む)
(もっと読む)
炎症性腹部疾患のためのカッパ−アヘン製剤作働薬
【課題】 炎症性腹部疾患の治療に適する薬剤調製物を提供する。
【解決手段】 薬剤調製物は、一般式I、即ち
【化1】
[式中、R1、R2、R3、R4、R5、R6、A、Ar、DおよびHalは、請求項1で定義の通りである]
の少なくとも一つの化合物および/または生理学的に容認し得るその塩の一つおよび/またはそのグリコシル化誘導体の一つおよび少なくとも一つの生理学的に容認し得る賦形剤または助剤を含む。
(もっと読む)
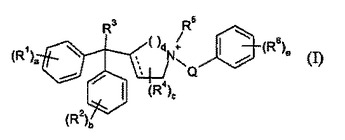
ムスカリン受容体アンタゴニストとして有用な第四級アンモニウムジフェニルメチル化合物
本発明は、塩形態または双性イオン形態の式(I)の化合物であって、式中、R1〜6、a〜eおよびQは本明細書に定義するとおりである、化合物またはその薬学的に許容される塩を提供する。これら化合物は、ムスカリン受容体アンタゴニストである。本発明はまた、そうした化合物を含む医薬組成物、そうした化合物を調製するプロセスおよび、たとえば、慢性閉塞性肺疾患および喘息などの肺障害を処置するためのそうした化合物の使用方法も提供する。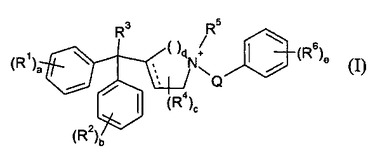
 (もっと読む)
(もっと読む)
新規化合物
新規な置換ベンズアミド系阻害剤、治療におけるそれらの使用、その化合物を含む医薬組成物、薬剤を製造するための前記化合物の使用、及び前記化合物の投与を含む治療法が記載されている。本化合物は、11β−ヒドロキシステロイドデヒドロゲナーゼ1型(11βHSD1)の活性を調節するので、メタボリック症候群などの、調節が効果的である病気の治療に有用である。 (もっと読む)
N−ヒドロキシアルキル化ラクタムの(メタ)アクリル酸エステルの触媒的製造方法
環状N−ヒドロキシアルキル化ラクタム(L)[ここで、R1は、C1〜C5−アルキレンを表すか又は1つ又はそれ以上の酸素原子及び/又は硫黄原子及び/又は1つ又はそれ以上の置換又は非置換のイミノ基により及び/又は1つ又はそれ以上のシクロアルキル−、−(CO)−、−O(CO)O−、−(NH)(CO)O−、−O(CO)(NH)−、−O(CO)−又は−(CO)O−基により中断されたC2〜C20−アルキレンを表し、その際に前記の基はそれぞれ、アリール、アルキル、アリールオキシ、アルキルオキシ、ヘテロ原子及び/又はヘテロ環により置換されていてよく、但し、R1は、炭素原子以外の原子がラクタム−カルボニル基に直接隣接してはならず、R2は、C1〜C20−アルキレン、C5〜C12−シクロアルキレン、C6〜C12−アリーレンを表すか又は1つ又はそれ以上の酸素原子及び/又は硫黄原子及び/又は1つ又はそれ以上の置換又は非置換のイミノ基により及び/又は1つ又はそれ以上のシクロアルキル−、−(CO)−、−O(CO)O−、−(NH)(CO)O−、−O(CO)(NH)−、−O(CO)−又は−(CO)O−基により中断されたC2〜C20−アルキレンを表し、その際に前記の基はそれぞれ、アリール、アルキル、アリールオキシ、アルキルオキシ、ヘテロ原子及び/又はヘテロ環により置換されていてよく、又はR2−OHは式−[Xi]k−Hの基を表し、kは、1〜50の数を表し、かつXiは、各々i=1〜kについて互いに独立して、−CH2−CH2−O−、−CH2−CH2−N(H)−、−CH2−CH2−CH2−N(H)−、−CH2−CH(NH2)−、−CH2−CH(NHCHO)−、−CH2−CH(CH3)−O−、−CH(CH3)−CH2−O−、−CH2−C(CH3)2−O−、−C(CH3)2−CH2−O−、−CH2−CH2−CH2−O−、−CH2−CH2−CH2−CH2−O−、−CH2−CHVin−O−、−CHVin−CH2−O−、−CH2−CHPh−O−及び−CHPh−CH2−O−の群から選択されていてよく、ここで、Phはフェニルを表し、かつVinはビニルを表す]を、アルカリ金属水酸化物、アルカリ土類金属水酸化物及び金属アセチルアセトナートからなる群から選択される少なくとも1つの触媒(K)の存在で、(メタ)アクリル酸(S)でエステル化するか又は少なくとも1つの(メタ)アクリル酸エステル(D)とエステル交換反応することによる、N−ヒドロキシアルキル化ラクタムの(メタ)アクリル酸エステル(F)の製造方法。 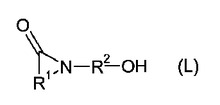 (もっと読む)
(もっと読む)
多量体接合体
本発明は、多量体物質、およびこの多量体物質と生物活性物質とで形成される多量体接合体に関する。前記多量体接合体は、前記非修飾の生物学的物質と比較して、生体内でより長い寿命を持ち、そして、より高い親和性を持つ。さらに本発明は、前記接合体を含む医薬品組成物または診断組成物、およびその製造方法に関する。本発明はさらに、特定の結合パートナーの検出、測定、分離および/または単離のための前記接合体の使用、ならびに、前記特定の結合パートナーが、直接、または、間接的に関与する疾患の診断、予防および治療のための前記接合体の使用を提供する。 (もっと読む)
アセチルチオピロリジン誘導体の製法
【課題】ピロリジルチオカルバペネム誘導体を合成する方法において、ハロゲン含有溶媒を使用しないかもしくは使用を低減させ、ならびに/または極度の高温および/もしくは低温を回避するかもしくは低減する中間体合成工程またはそれらを利用するピロリジルチオカルバペネム誘導体を合成方法を提供すること。
【解決手段】スルファミドを合成する方法であって、以下の工程:a)ハロゲン化スルホニルイソシアナートと、アルコールとを、トルエンまたはCH3CN中で反応させて反応生成物を得る工程;b)工程a)で得られた反応生成物に、ピリジン、置換されたピリジンおよびキノリン類からなる群より選択される化合物を加えて反応生成物を得る工程;およびc)工程b)で得られた反応生成物に、アンモニア水を加えてスルファミドを得る工程、を包含する、方法、ならびにこの方法を合成工程として包含するピロリジルチオカルバペネム誘導体の合成方法。
(もっと読む)
ウレア構造を有する新規N−(2−アミノフェニル)ベンズアミド誘導体
【課題】ウレア構造を有する新規N−(2−アミノフェニル)ベンズアミド誘導体の合成研究及びその誘導体の薬理作用を見出すこと。
【解決手段】一般式(1)で表される化合物又はその塩は線維柱帯細胞に対して、細胞形態変化作用を有し、眼圧が関与するとされる疾患の予防及び/又は治療に有効である。
式中、R1及びR2は水素原子、低級アルキル基等;R3はヒドロキシ基、低級アルコキシ基、低級シクロアルキルオキシ基、アリールオキシ基等;R4及びR5はハロゲン原子、低級アルキル基、ヒドロキシ基、低級アルコキシ基等;Xは低級アルキレン基等;Yは単結合、低級アルキレン基等;l又はmは0、1、2等をそれぞれ示す。
【化1】 (もっと読む)
(もっと読む)
安定性の高いポリイオン液体塩
ポリカチオン分子またはポリアニオン分子を含むポリイオン液体塩を提供する。さらに、1種または2種以上のポリイオン液体塩を含む溶媒、ならびに、このようなポリイオン液体塩の、ガスクロマトグラフィーにおける固定相としての使用、およびエレクトロスプレーイオン化質量分析法(ESI−MS)における試薬としての使用、を提供する。 (もっと読む)
光学的に純粋な4−ヒドロキシ−2−ヨウ素−1−ピロリジンアセトアミドの製造方法
【課題】光学的に純粋なキラル4−ヒドロキシ−2−オキソ−1−ピロリジンアセトアミドの製造方法の提供。
【解決手段】(a)キラルエピクロロヒドリン溶液にシアン化ナトリウムをくえん酸と共に添加して、前記キラルエピクロロヒドリンの開環反応によりキラル3−クロロ−2−ヒドロキシプロピオニトリルを得て、(b)得られた生成物を塩酸ガスの含まれたC1−C4のアルコールと反応させて、キラル4−クロロ−3−ヒドロキシブチル酸エステルを得て、(c)得られた生成物を塩基の存在下でグリシンアミド又はグリシンエステルと反応させた後、アンモノリシスを行うことにより、前記キラル4−ヒドロキシ−2−オキソ−1−ピロリジンアセトアミドを得るステップを含む方法。この方法は、光学的に純粋な4−ヒドロキシ−2−オキソ−1−ピロリジンアセトアミドを高収率及び高純度で製造することができ、大量生産に適している。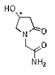
(*はキラルセンター)
(もっと読む)
201 - 220 / 535
[ Back to top ]

