Fターム[4C076EE48]の内容
Fターム[4C076EE48]の下位に属するFターム
Fターム[4C076EE48]に分類される特許
241 - 260 / 832
有機化合物のガレヌス製剤
本出願は、コアおよび外側被覆を有する錠剤形態の経口投与用固形単位剤形であって、前記錠剤のコアは治療有効量のアリスキレンまたはその薬学的に許容される塩を含み、かつ外側被覆は、風味遮蔽特性および/または制御放出機能を有するフィルムコートの形態である固形単位剤形に関する。好ましくは、コア錠剤は、多粒子系、とりわけミニ錠剤の一部である。該固形経口剤形は、小児での使用にとりわけ適している。 (もっと読む)
IL−1結合タンパク質
本発明は、IL−1α結合タンパク質を包含する。具体的には、本発明は、キメラ、CDRグラフトおよびヒト化抗体である抗体に関する。本発明の抗体は、IL−1αについて高い親和性を有し、IL−1α活性を中和する。本発明の抗体は、完全長抗体またはこの抗原結合部分であり得る。本発明の抗体を作製する方法および本発明の抗体を使用する方法も提供する。本発明の抗体、または抗体部分は、例えばIL−1α活性が有害である障害を罹患するヒト対象におけるIL−1αの検出およびIL−1α活性の阻害に有用である。 (もっと読む)
ミルナシプランの持続性放出を伴うガレヌス製剤形態
【課題】多数の微小顆粒が集まったマルチ粒子形態を有し、かつミルナシプランが60ないし140mgの1日1回用量で経口投与される長期放出性ガレヌス製剤形態の提供。
【解決手段】各微顆粒が結合剤ならびに150から1000μgのミルナシプラン含有する粒径200から2000μmのサッカロースおよび/または澱粉核を含む活性微小球を有し、また水不溶性で生理学的液体には浸透性の少なくとも一種のポリマー由来の厚さ20から100μmのフイルムで各微顆粒が被覆されて成り、上記ガレヌス製剤形態が次のパターン:2時間での放出用量が10から55%、4時間での放出用量が40から75%、8時間での放出用量が70から90%、12時間での放出用量80から100%に該当するin vitroでの放出を可能ならしめる、長期放出性ガレヌス製剤形態。
(もっと読む)
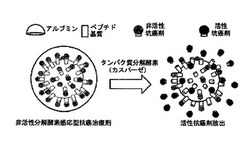
標的タンパク質分解酵素感応型抗癌剤前駆体
【課題】正常細胞の破壊を最小化し、低い抗癌剤の投与及び放射線照射量で高い坑癌治療効果が得られる標的タンパク質分解酵素感応型抗癌剤前駆体を提供する。
【解決手段】本発明は、抗癌剤、癌細胞から過多分泌される標的タンパク質分解酵素によって特異的に分解されるペプチド及び癌部位に特異的に蓄積可能な高分子で結合された標的タンパク質分解酵素感応型抗癌剤前駆体に関するものであって、非活性形態の抗癌剤前駆体を投与すれば、標的部位に蓄積された後、放射線照射によってペプチドが分解されながら活性型の抗癌剤を標的部位から放出することができるために、正常細胞の破壊を最小化し、低い抗癌剤の投与及び放射線照射量で高い坑癌治療効果が得られる。
(もっと読む)
貼付剤および貼付製剤
【課題】粘着面を指で触れずに、剥離ライナーを貼付剤本体から剥離することが容易にでき、貼付時に貼付剤本体が丸まり、または粘着面同士が接着することがなく、かつ貼付時に粘着面を指で触れずに、貼付剤本体を皮膚面に貼付することが容易にできる貼付剤を提供すること。
【解決手段】支持体3および該支持体3の少なくとも片面に積層された粘着剤層2を備える貼付剤本体4と、該貼付剤本体4の該粘着剤層2の該支持体3側とは反対側の面に剥離ライナー1を備える貼付剤であり、貼付剤本体4の平面面積が1.5〜15cm2であり、剥離ライナー1の平面面積の、貼付剤本体4の平面面積に対する比率([剥離ライナー1の平面面積(cm2)]/[貼付剤本体4の平面面積(cm2)])が1.1〜7であり、かつ剥離ライナー1が分割線11を有することを特徴とする、貼付剤。
(もっと読む)
手指消毒剤組成物
【課題】乾き際のべたつき、手洗い時のぬるつきがないだけではなく、乾いた後に白っぽくならず、よれが生じない、使用感に優れた手指消毒剤組成物を提供すること。
【解決手段】(A):エタノール及び/又はイソプロパノールを40〜95重量%、(B):カルボキシビニルポリマー及び/又はアクリル酸・メタクリル酸アルキル共重合体、並びに(C):アスペクト比が10以上である板状粉体を0.02〜2.0重量%含有する手指消毒剤組成物。
(もっと読む)
ナノバブルの形成方法
【課題】超音波造影剤を用いるナノバブルの形成方法の提供。
【解決手段】本発明はナノバブルの形成方法を開示するものであり、前記形成方法は公知技術に使用する油水乳化反応とは異なる特徴を持つ。本発明のナノバブルの形成方法は、無機粒子を中心核として、前記中心核の表面に最低一つの第一高分子をコーティングして有機/無機複合粒子を形成する。次に、第一溶剤によって前記有機/無機複合粒子の中心核を溶解して除去し溶剤型ナノ粒子を形成する。続いて冷凍乾燥プロセスにおいて前記第一溶剤を除去し前記溶剤型ナノ粒子に中空ナノ粒子を形成させる。最後に前記中空ナノ粒子を第二溶剤に溶かして前記ナノバブルを形成する。
(もっと読む)
遅延放出ラサギリン製剤
特定の薬学動態学的性質を維持しながらラサギリンの放出を遅らせるように設計されたラサギリン塩基の製剤を開示する。 (もっと読む)
治療薬の送達のための薬物送達装置
非生体吸収性ポリマー構造と活性剤を含む組成物とを含む薬物送達装置を発見した。この薬物送達装置は、他の疾患および病気の中でも眼の病気を治療するために使用することができる。さらに、薬物送達装置を埋め込むことを含む、眼の病気の治療方法を発見した。この装置は、活性剤をQ=0.001×N×Cの速度で放出する。式中、Cは、活性剤の局所的有効濃度(ミリグラム/mL)であり、エステル、アミド、遊離酸または塩の形態のプロスタグランジンの場合は、N=0.01〜0.5であり、エステル、アミド、遊離酸または塩の形態のプロスタグランジン以外の任意の活性剤の場合は、N=0.5〜5である。 (もっと読む)
可食性フィルムの製造方法
本発明は、成分が実質的に均一に分布している、可食性フィルムの製造方法を提供するものであり、この方法は、水を主体とするフィルム形成ポリマー溶液と、水に対して活性な成分および溶媒を含むスラリー型の混合物とを組み合わせる段階;該ポリマー溶液および該スラリー型の混合物を、約10分間以下の間混合する段階;該混合された溶液およびスラリー型の混合物を供給して、フィルムを形成する段階;および該フィルムを乾燥して、該水および溶媒を蒸発させる段階を含む。本発明は、この方法により作成されたフィルムをも提供する。 (もっと読む)
生体吸収性発泡組織ドレッシング
ガス発生ポロゲン、およびゲルまたはゲル形成溶液を含んでなる、流動性の生体吸収性組織ドレッシングを提供する。上記の組織ドレッシングを調製するためのキットもまた提供する。さらに、哺乳類の組織部位を上記のドレッシングによって治療するための方法を提供する。組織部位に減圧組織治療を適用するための減圧送達システムもまた提供する。 (もっと読む)
水難溶性薬物を含有する高分子ミセル組成物の製造方法
本発明による薬物含有高分子ミセル組成物の製造方法は、薬物と両親媒性ブロック共重合体を有機溶媒に溶解させる段階、及び得られた有機溶媒混合物に水溶液を添加して高分子ミセルを形成する段階を含み、上記方法は、ミセルを形成する段階の前に別途の有機溶媒の除去工程を施さないことを特徴とする。上記薬物含有高分子ミセル組成物の製造方法は、製造工程が単純であり、且つ製造時間を短縮させることができ、大量生産が容易であるという長所がある。 (もっと読む)
感水性の活性成分を含む、局所用医薬組成物
本発明は、医薬活性薬剤として感水性の化合物を、生理学的に許容可能な媒体中に溶解された形態で含む局所用医薬組成物、それを調製するための方法、およびその皮膚への使用に関する。 (もっと読む)
HIV処置用の移植可能デバイス
本発明は、ジメチルスルフォキシド(DMSO)とポリ(ビニルピロリドン)(PVP)との組み合わせ物、ポロキサマーおよびポリソルベートからなる群から選択される1もしくは複数の放出強化剤、およびTMC278と混合された生物適合性の生分解性ポリマーを含んでなる移植可能デバイスに関する (もっと読む)
ポリエーテルとビニルモノマーに基づくコポリマーのエマルションのための安定化剤としての使用
本発明はポリエーテルの存在下における酢酸ビニルとN-ビニルラクタムとの重合により得られる水溶性又は水分散性コポリマーのエマルションのための安定化剤としての使用に関する。 (もっと読む)
ハイドロゲル粒子
【課題】固体粒子及びゲル状成分を含有するハイドロゲル粒子であって、製品の均一性に優れるハイドロゲル粒子を提供すること。
【解決手段】次の(A)成分〜(E)成分:(A)ゾル−ゲルの熱可逆性によってゲル化が生じるゲル化剤、(B)架橋型ポリアクリレート、(C)固体粒子、(D)ゲル状成分、及び(E)水を含む、ハイドロゲル粒子。
(もっと読む)
制御放出組成物
複数の微粒子とマトリックスとを含む制御放出組成物、およびその調製法が開示される。該複数の微粒子は第1の材料を含み、該マトリックスは第2の材料を含む。第1の材料の溶融温度は、第2の材料の溶融温度よりも高い。 (もっと読む)
ポリオルトエステルおよびそれらの製剤の安定性を高めるための方法
活性薬剤およびポリマーを含む除放性医薬組成物の安定性を高める方法ならびに安定性の高いかかる医薬組成物を調製する方法が本明細書で開示される。 (もっと読む)
変性ポリビニルラクタム
変性ポリビニルラクタムおよびその使用。 (もっと読む)
グアニル酸シクラーゼCアゴニストの製剤およびその使用方法
本発明は、グアニル酸シクラーゼ−C(「GCC」)アゴニストペプチドの新規製剤と、消化器癌を含めた、胃腸の疾患および障害の治療における、それらの使用のための方法とを提供する。本発明のGCCアゴニスト製剤は、単独で、または1つまたは複数の追加の治療剤、好ましくは、cGMP依存性ホスホジエステラーゼの阻害剤もしくは緩下剤と併用して投与することができる。一実施形態では、GCCアゴニスト製剤は、十二指腸または空腸にGCCアゴニストを送達するために最適化されており、4.5〜5.5のpH範囲で分解する1つまたは複数のpH依存性ポリマーを含み、このpH依存性ポリマーは、コアの周囲に1つまたは複数の層を形成する。 (もっと読む)
241 - 260 / 832
[ Back to top ]