Fターム[4C084AA16]の内容
蛋白脂質酵素含有:その他の医薬 (348,545) | 発明の種類 (49,201) | 化学的に特定されていない活性成分を含有 (16,769)
Fターム[4C084AA16]の下位に属するFターム
活性成分が1つのもの (6,587)
活性成分が2つのもの (8,706)
活性成分が3つ以上のもの (1,287)
活性成分が互いに結合しているもの (16)
Fターム[4C084AA16]に分類される特許
141 - 160 / 173
炎症関連疾患を予防または治療するためのアルドステロンブロッカー療法
被検者にて、心筋炎、心筋症、脈管炎およびベーチェット病のような炎症関連疾患を予防または治療する方法であって、前記被検者における炎症または心臓リモデリングの調節に直接的または間接的に関係する1つ以上の発現生成物の発現を変化させるのに十分なアルドステロンブロッカーの治療学的に有効な量で前記被検者を処置することを含む方法。 (もっと読む)
マラリア原虫のGPIの生合成を阻害する化合物をスクリーニングする方法
本発明者らは、熱帯熱マラリア原虫のGPI生合成酵素の一つであるGWT1(PfGWT1)の単離に成功した。さらに、本発明者らは、PfGWT1蛋白質をコードするDNAと比較してAT含率が低下した縮重変異DNAがGWT1欠失酵母の表現型を相補できることを見出した。これらの知見に基き、本発明は、マラリア原虫のGWT1蛋白質および抗マラリア剤のスクリーニング方法における該蛋白質の利用法を提供する。また本発明は、もとのGPI生合成蛋白質をコードするDNAと比較して、AT含率が低下したGPI生合成蛋白質をコードする縮重変異DNAを提供する。さらに、本発明は、該縮重変異DNAを利用した抗マラリア剤のスクリーニング方法を提供する。 (もっと読む)
胃食道逆流性疾患を処置するための方法
本発明は、糖質コルチコイドレセプターの生物学的作用を阻害し得る薬剤が、被験体における胃食道逆流性疾患を処置するための方法で使用され得るという知見に関する。本発明の方法は、胃食道逆流性疾患を処置する必要のある被験体における胃食道逆流性疾患を処置する方法であって、該方法は、該被験体における胃食道逆流性疾患を処置するために効果的な量の糖質コルチコイドレセプターアンタゴニストを該被験体に対して投与する工程を包含する。(i)ただし、該被験体は、糖質コルチコイドレセプターアンタゴニストでの処置を他の点では必要としていない。 (もっと読む)
β−アミロイド前駆体タンパク質の細胞プロセッシングをモニターするための方法及び組成物
【課題】β−アミロイド前駆体タンパク質(βAPP)のプロセッシングをモニターするための方法の提供。
【解決手段】β−アミロイド前駆体タンパク質(βAPP)のプロセッシングのモニターは、β−アミロイドペプチドのアミノ末端でのβAPP の切断に起因する可溶性βAPP フラグメントの分泌を検出することによってなされる。βAPP フラグメントの分泌のインビボモニターリングは、アルツハイマー病及び他のβ−アミロイド関連疾病の診断及び進行についてモニターされ、そして培養された細胞からのそのような分泌のインビトロモニターリングは、β−アミロイド生成のインヒビターを同定するためにモニターされ得る。
(もっと読む)
ミルナシプランのパルス型放出組成物
間隔を空けた「パルス」の状態で薬物を放出する、1日1回の経口ミルナシプランパルス型放出処方物が開発された。この投薬形態は、第一投薬単位、第二投薬単位、および必要に応じて第三投薬単位からなり、各投薬単位は、異なる薬物放出プロフィールを有する。この投薬形態は、Cmax約3000ng/mL未満、好ましくは2000ng/mL未満、最も好ましくは1000ng/mL未満を特徴とするインビボ薬物血漿レベルをもたらす。これらのレベルは、CNSに対するコリン作動性作用の刺激を回避することに役立つ。この組成物は、患者に投与した場合に、約24時間にわたってミルナシプランを送達することを可能にし、それによって、一般的なミルナシプラン副作用の発生の減少または強度の減少を生じる。 (もっと読む)
有機化合物
遊離形または塩形態の、式I
【化1】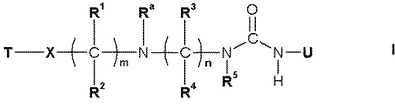
[式中、T、X、R1、R2、Ra、R3、R4、R5およびUは、明細書中に記載の意味を有する。]
で示される化合物は、CCR−3が介在する状態、特に炎症性または閉塞性気道疾患のような炎症性またはアレルギー性状態を処置するために有用である。この化合物を含む医薬組成物およびこの化合物を製造するための方法もまた、記載する。 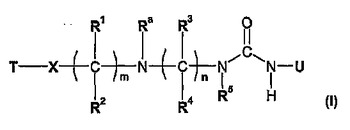 (もっと読む)
(もっと読む)
多発性骨髄腫の処置のためのラクトン誘導体
本発明は、骨髄腫、とりわけ慣用的細胞傷害性化学療法に耐性の骨髄腫を有する温血動物、とりわけヒトの処置方法であって、当該動物に、エポチロンの治療上有効量、好ましくは式(I)
【化1】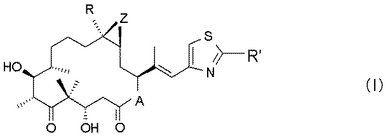
で示されるエポチロンの治療上有効量を投与することを含んでなる方法、同時的、個別的または逐次的使用のためエポチロンを含んでなる組合せ剤;ならびに当該組合せ剤を含んでなる医薬組成物および市販パッケージに関する。 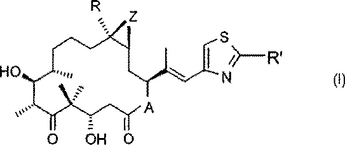 (もっと読む)
(もっと読む)
アスパラギニルヒドロキシラーゼ及びその修飾物質
FIHを模倣するか、それに結合する化学実体を同定、スクリーニング、特性決定又は設計する方法が記載されている。この方法は、FIHの構造モデルと、前記化学実体の構造モデルとを比較することを含み、その際、FIHの前記構造モデルは、FIHを含有する結晶をX線回折測定に掛けることにより決定された構造因子又は構造座標に由来する。このような化学実体は、高いか低いHIFレベル又は活性を伴う状態を治療する際に使用することができる。 (もっと読む)
糖尿病および心血管疾患の治療のためのプロテインキナーゼCαの抑制
本発明は、特に、糖尿病および合併症、例えば糖尿病性腎症、網膜症またはニューロパシーに罹患している患者を治療するための、プロテインキナーゼC−α(PKC−α)の発現および/または活性を妨げる作用物質の使用に関する。  (もっと読む)
(もっと読む)
わずかに溶解性の作用物質用の多粒子の剤形、並びに前記剤形の製造方法
本発明は、a) ペプチド又はタンパク質(その誘導体又は複合体を含める)ではない作用物質と、37℃を超える融点を有する親油性マトリックスと、粘膜付着作用を有するポリマーとを有する内側マトリックス層、b) 場合により製剤学的に通常の助剤で調製されていてもよい、主にアニオン性ポリマー又はコポリマーからなる外側の皮膜形成されたコーティングとから主に構成されている、50〜2500μmの範囲内の平均直径を有する、多数のペレット、粒子、顆粒又はアグロメラートを含有する、胃のpH領域で分解する容器の形の経口の多粒子の剤形において、前記作用物質が、作用物質1質量部に対して水少なくとも30体積部のDAB10による水中での溶解性を示し、かつ親油性マトリックス中に埋め込まれていて、かつこの作用物質含有の親油性マトリックスは粘膜付着作用を有するポリマーからなるマトリックス中に埋め込まれていることを特徴とする、経口の多粒子の剤形に関する。本発明は、更に多粒子の剤形の製造方法に関する。 (もっと読む)
コリンレセプターの薬理活性により腸閉塞を処置する方法
被験体におけるコリンレセプターの活性を高める薬物の有効量を被験体に投与することによる、被験体における腸閉塞を処置する方法。薬物の例には、脳ムスカリンアゴニスト、コリンアゴニストまたはコリンエステラーゼ阻害剤がある。本発明の方法は、腹部手術により引き起こされる腸閉塞を処置するのに、または、例えば、癌の化学療法中での麻酔薬または化学療法薬の投与に使用できる。別の実施態様では、本発明は、被験体における腸閉塞を処置する方法であり、該方法は、該被験体に、コリンアゴニストの有効量を投与する工程を包含する。別の実施態様では、前記コリンアゴニストは、α7ニコチンレセプターである。 (もっと読む)
自己免疫疾患を治療する方法および自己免疫疾患の治療化合物をスクリーニングする方法
本発明は、全身性紅斑性狼瘡のような全身性自己免疫疾患のモデルとして有用であるトランスジェニック動物に関する。そのような動物は、疾患のモデルとして、および疾患を治療または予防する化合物を同定するためのモデルとして有用である。さらに、本発明は、そのような疾患を診断および治療または予防する方法に関する。  (もっと読む)
(もっと読む)
小分子担体としての二又は四グアニジノ−ビフェニル化合物
本発明は、式Iの化合物又はその薬学的に許容される塩に関する:式I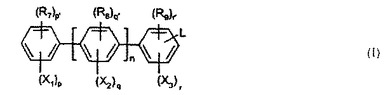
[式中、X1、X2、X3はそれぞれ独立して、
(式中、Yはアルキル、ハロ、CF3、OH、アルコキシ、NH2、CN、NO2及びCOOHから選択される1以上の置換基でそれぞれ任意に置換されていてもよいアルキレン、アルケニレン又はアルキニレン基を示し;Wは存在しないか、又はO、SもしくはNHを示し;R1、R2、R3及びR4はそれぞれ独立してH、アルキル、アリール及び保護基P1から選択される)を示し;R7、R8及びR9はそれぞれ独立してH、アルキル、ハロ、CF3、OH、アルコキシ、NH2、CN、NO2及びCOOHから選択され;q及びrはそれぞれ独立して1、2、3又は4を示し;q’及びr’はそれぞれ独立して0、1、2又は3(q+q’及びr+r’はそれぞれ4に等しい)を示し;pは1、2、3、4又は5を、及びp’は0、1、2、3又は4(p+p’は5である)を示し;nは0、1、2、3....6を示し;Lは(Z)mNR5R6{式中、Zはヒドロカルビル基を示し、mは0又は1を示し;R5及びR6はそれぞれ独立してH、CO(CH2)jQ1又はC=S(NH)(CH2)kQ2(式中、j及びkはそれぞれ独立して0、1、2、3、4又は5を示し、Q1及びQ2はそれぞれ独立してCOOH、発色団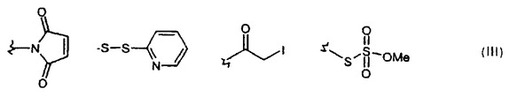

から選択される)を示すか、あるいは、R5、R6及びそれらが結合した窒素が一緒になって
を形成する}を示す]。
(もっと読む)
造血細胞の異常増殖を治療及び/又は予防する方法
本発明は一般的に、造血細胞の異常増殖を治療及び/又は予防する方法に関する。より詳細には、本発明は造血細胞におけるホスホイノシチド3−キナーゼデルタ(PI3Kδ)活性を選択的に阻害することを含む造血細胞の異常増殖を治療及び/又は予防する方法に関する。方法は造血細胞の異常増殖の関与する何れかの適応症を治療するために使用してよい。 (もっと読む)
ポサコナゾールを含む注射用薬学的懸濁液
本発明により、感染の処置に有用な処方物、具体的には、最後の蒸気滅菌の際に安定である、活性のある薬学的成分のポサコナゾールを注射可能な懸濁液中に含む処方物が提供される。ポサコナゾールの水性の注射可能な懸濁液は、リン脂質の助けを借りてビヒクル中に均質になるように懸濁させられている。加えて、熱保護剤が、オートクレーブによって誘導される粒子の大きさの成長を小さくするために使用され、さらに、オートクレーブの間、リン脂質を安定化させるために緩衝システムが使用される。提供される処方物は、121℃で20分間のオートクレーブの後、そしてその後の少なくとも6ヶ月間の4℃から40℃での保存後も安定なままである。  (もっと読む)
(もっと読む)
抗菌剤としての3−{4−(ピリジン−3−イル)フェニル}−5−(1H−1,2,3−トリアゾール−1−イルメチル)−1,3−オキサゾリジン−2−オン
式(I)[式中、R1、R2、R3、及びR4は、本明細書に定義される通りである]の化合物、並びにその医薬的に許容される塩及びプロドラッグを開示する。また開示するのは、式(I)の化合物を作製する方法、並びに、細菌感染症を治療するために式(I)の化合物を使用する方法である。 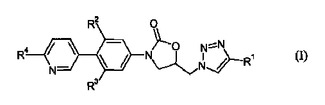 (もっと読む)
(もっと読む)
活性薬剤を送達するための化合物および組成物
活性薬剤の伝達のための化合物および組成物を提供する。投与方法および調製方法も提供する。 (もっと読む)
インドールおよび関連化合物から成るホスホリパーゼ−A2阻害薬を用いた、食事関連疾患の治療
本発明は、ホスホリパーゼ関連疾患の治療のための方法と製薬組成を提示する。特に、本発明は、被験動物のインスリン関連疾患や体重関連疾患、コレステロール関連疾患を治療する方法を提示する。この方法には一般に、ホスホリパーゼA2 阻害薬の投与が含まれ、このホスホリパーゼA2 阻害薬は、例えばインドール含有化合物などの、五員環と六員環を融合した部分を有する置換有機化合物から成る。本発明により治療される疾患としては、例えば、肥満、糖尿病(2型糖尿病など)、インスリン抵抗性、グルコース不耐性、高コレステロール血症、高トリグリセリド血症、これらの組合せがある。 (もっと読む)
消化器官管腔集中性ホスホリパーゼ阻害薬
この分野においては、より有益なホスホリパーゼ阻害薬組成とその使用方法、および治療方法が、依然として必要とされている。本発明は、ホスホリパーゼ関連疾患の治療のための方法と製薬組成を提示する。特に、本発明は、被験動物のインスリン関連疾患や体重関連疾患、コレステロール関連疾患を治療する方法を提示する。方法は全般に、消化器官管腔に集中して留まる、非吸収性または排出性ホスホリパーゼA2阻害薬の投与が関与する。 (もっと読む)
B細胞の白血病及びリンパ腫の治療のためのLTB4インヒビターの使用
本発明は、B細胞慢性リンパ球性白血病(B-CLL)、B細胞前リンパ球性白血病(B-PLL)又はB細胞リンパ腫の治療のための医薬の製造における、LTB4の生合成及び/又は機能のインヒビターの使用に関する。好ましくは、LTB4の生合成及び/又は機能のインヒビターは、5-LOのインヒビターのBWA4C、又はFLAPのインヒビターのMK-886である。 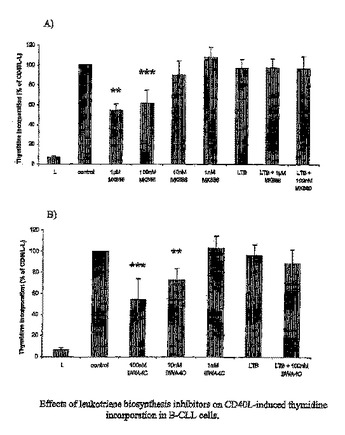 (もっと読む)
(もっと読む)
141 - 160 / 173
[ Back to top ]