Fターム[4H045BA10]の内容
Fターム[4H045BA10]の下位に属するFターム
2 (530)
3 (638)
4〜5 (867)
6〜7 (999)
8〜10 (1,347)
11〜14 (1,219)
15〜23 (1,273)
24〜35 (719)
36〜50 (431)
51〜70 (170)
71〜100 (123)
Fターム[4H045BA10]に分類される特許
1 - 20 / 7,823
血液凝固因子又は細胞接着因子に対する吸着剤及び精製方法
エリスロポエチンの製造方法およびエリスロポエチン産生細胞の単離方法
MPHOSPH1またはDEPDC1ポリペプチドを発現する癌に対するペプチドワクチン
コラーゲンの製造方法
血液がん治療剤
ICAM−1に対するヒト化抗体、それらの生成および使用
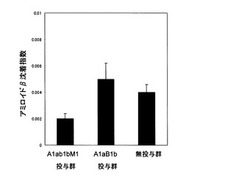
アルツハイマー病の予防および/または治療用ワクチン組成物
【課題】アルツハイマー病の予防および/または治療のためのワクチン組成物を提供すること。
【解決手段】アミロイドβペプチドのN末端部分に由来する5〜15個の連続したアミノ酸配列が、単一もしくは複数個反復して、種子貯蔵タンパクのアミノ酸配列中に挿入されたアミノ酸配列を有する融合タンパク質を含む、アルツハイマー病を予防および/または治療するためのワクチン組成物。
(もっと読む)
抗アクチビンA抗体およびその使用
【課題】抗体を含む抗アクチビンA結合タンパク質に関する、または結合タンパク質に由来する組成物および方法を提供すること。
【解決手段】特定の実施形態においては、本開示は、完全ヒト、ヒト化、およびキメラ抗アクチビンA抗体であって、ヒトアクチビンA、アクチビンA結合性断片、およびそのような抗体の誘導体と、そのような断片を含むアクチビンA結合ポリペプチドとを結合する、完全ヒト、ヒト化、およびキメラ抗アクチビンA抗体を提供する。アクチビンAに対して特異的なヒト抗原結合タンパク質もまた提供され、抗原結合タンパク質は、悪液質の減弱等の、ヒト抗アクチビンA抗体の少なくとも1つの生体内生物活性を保有する。
(もっと読む)
アルツハイマー病に関連する遺伝子配列およびタンパク質、ならびにその使用
【課題】アルツハイマー病に関連する遺伝子配列およびタンパク質、ならびにその使用を提供すること。
【解決手段】本発明は、2つのヒトプレセニリン遺伝子PS-1およびPS-2の同定、単離、配列決定、および特徴付けを記載する。これらの遺伝子の変異は、家族性アルツハイマー病をもたらす。マウス、C.elegans、およびD.melanogasterにおけるプレセニリン遺伝子ホ
モログもまた同定される。プレセニリンを含むかまたはそれに由来する核酸およびタンパク質は、アルツハイマー病のスクリーニングおよび診断、アルツハイマー病の処置のための治療剤の同定および開発、およびアルツハイマー病のモデルとして有用な細胞株およびトランスジェニック動物の産生に有用である。
(もっと読む)
キスペプチン拮抗薬及びその使用
【課題】本発明は、個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療用の薬剤の製造におけるキスペプチンの拮抗薬の使用に関する。本発明はまた、個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療において有用である、キスペプチンの拮抗薬として作用する可能性がある、定義された特定のペプチド分子を提供する。さらに、本発明は、キスペプチンの拮抗薬および/または定義されたペプチドを同定し、かつ/または使用する方法、ならびにその医薬組成物を提供する。
【解決手段】個体におけるキスペプチン活性により誘発され、かつ/または悪化した状態の治療用の薬剤の製造におけるキスペプチンの拮抗薬の使用。
(もっと読む)
ナノ粒子を利用した遺伝子発現調節法
【課題】効率のよく細胞ないし生体を近赤外光を用いて加熱すること。
【解決手段】カーボンナノホーン(CNH)に血清アルブミンが結合した複合体。
(もっと読む)
抗ヒトバンド3モノクローナル抗体
【課題】B3との共結晶化に適した抗B3抗体、又はB3の活性を阻害する抗B3抗体を提供する。
【解決手段】B3の55kDaドメインの細胞外領域に特異的な結合性を有し、且つB3の立体構造を認識する、抗B3抗体。又は、重鎖CDR1、2、及び3が、それぞれ特定の配列のアミノ酸配列を含み、軽鎖CDR1、2、及び3が、それぞれ他の特定の配列のアミノ酸配列を含む、抗B3抗体。この構成を有する抗体は、B3との結晶化リガンドに適する。そのため、この抗体を用いれば、B3の結晶を効率的に生成することができる。又は、高分解能のB3結晶を生成することができる。又は、この構成を有する抗体は、B3の活性を阻害できる。
(もっと読む)
改善された生体内半減期を有する生物学的に活性なタンパク質
【課題】生物学的に活性なタンパク質の半減期を変更する。
【解決手段】2〜約500単位の反復ペプチド・モチーフを含むポリペプチドにペプチド結合を介して結びついた生物学的に活性なポリペプチドを含み、非複合型の生物学的に活性なポリペプチド又はタンパク質の固有の半減期と比較して改善された血漿中半減期を示す。生物学的に活性なポリペプチドは、サイトカイン(例えば、顆粒球コロニー刺激因子(G-CSF))などである。また、主成分としてGly、Asn、及びGlnから選択される1種類のアミノ酸2残基以上、並びに副次成分としてAla、Ser、Thr、Asp、Gln、Glu、His、及びAsnから選択される1種類のアミノ酸1残基以上が、上記アミノ酸が主成分及び副次成分の中に存在しないという条件で含まれる、
(もっと読む)
弱毒化ペスチウイルス
【課題】現場からの病因ペスチウイルスから区別し得る免疫の誘導について高い効力を有する生の弱毒化ワクチンとしての使用のための特異的に弱毒化され、かつ検出可能に標識されたペスチウイルスの提供。
【解決手段】糖タンパク質ERNSにあるRNase活性が不活性化されているペスチウイルスを含む生ワクチン。
(もっと読む)
CD40に対する抗体
【課題】ヒトCD40に特異的に結合してCD40アゴニストとして作用する、単離された抗体またはその抗原結合部分を提供する。
【解決手段】ヒトCD40で免疫化したマウスに由来する抗CD40モノクローナル抗体を産生するハイブリドーマ細胞から重鎖および軽鎖の断片をコードする核酸をクローニングし、配列決定を行い、ヒト抗CD40抗体またはその抗原結合部分の重鎖もしくはその抗原結合部分、または軽鎖もしくはその抗原結合部分をコードする核酸配列を含む、単離された核酸分子からなる。
(もっと読む)
抗−TNFα抗体の投与方法
【課題】TNFα活性が有害となる疾患に関する新規治療方法の提供。
【解決手段】ヒト腫瘍壊死因子α(hTNFα)に特異的に結合するヒト抗体、好ましくは組換えヒト抗体を隔週皮下投与する。メトトレキサートと一緒に投与してもよい。抗体はhTNFαに対して高いアフィニティー(例えば、Kd=10−8M以下)及び遅いhTNFα解離オフレート(Koff=10−3sec−1以下)を有し、インビトロ及びインビボでhTNFα活性を中和する。抗体は完全長抗体またはその抗原結合部分である。
(もっと読む)
EGFRおよびKRAS変異
【課題】EGFR阻害剤での治療に対して非反応性である患者を同定するための方法の提供。
【解決手段】上皮成長因子受容体(EGFR)およびKRASにおける変異ならびに上記変異を検出する。腫瘍試料における変異EGFR遺伝子もしくは変異EGFRタンパク質および/または変異KRAS遺伝子もしくは変異KRASタンパク質の存在を決定することを含む。この変異は、EGFRのエキソン18〜21に位置し、それによって、変異EGFR遺伝子または変異EGFRタンパク質の存在は、腫瘍が治療に対して感受性であることを示す。
(もっと読む)
関心のあるビタミンK依存性タンパク質を含んでなる組成物中におけるタンパク質混入物の量の減少
【課題】非常に少ない、または無視できる量のタンパク質混入物を有するビタミンK依存性タンパク質組成物およびその調製に適用可能な方法を提供する。
【解決手段】ビタミンK依存性タンパク質、特に、因子Xポリペプチド(FX/FXa)、因子IXポリペプチド(FIX/FIXa)、因子VIIポリペプチド(FVII/FVIIa)、および抗凝固性のタンパク質Cから選択される凝固因子、特に因子VIIポリペプチド、と結合することができる固相物質とを接触・回収するステップを含む、前記タンパク質含有組成物中の1以上のタンパク質混入物の量を減少させる方法。
(もっと読む)
腫瘍マーカー、それに対する抗体、その検出キット及びその検出方法
【課題】癌細胞に特異的にみられる糖鎖構造に着目した新たな腫瘍マーカー、それに対する抗体、その検出キット及びその検出方法を提供する。
【解決手段】以下の式(3)で表される糖鎖を有する、腫瘍マーカー。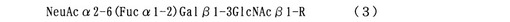
(式中、Rは糖残基を示す)
(もっと読む)
間葉系前駆細胞(MPC)の増殖および/または生存を増強させる方法
【課題】間葉系前駆細胞(MPC)、および/またはそれに由来する子孫の増殖および/または生存をin vitroもしくはin vivoで増強させる方法の提供。
【解決手段】間葉系前駆細胞(MPC)もしくは子孫をケモカイン間質細胞由来因子-1(SDF-1)またはその類似体に曝すことを含む方法。
(もっと読む)
1 - 20 / 7,823
[ Back to top ]