Fターム[4H045BA57]の内容
ペプチド又は蛋白質 (143,989) | 化学構造 (26,018) | 特徴的な構成成分を有するもの (3,792) | 高分子化合物 (636) | ポリアルキレングリコール (498)
Fターム[4H045BA57]に分類される特許
201 - 220 / 498
アシル及びアルキレングリコール部分を有するインスリンアナログ
A21アミノ酸残基のC末端に結合するリジン残基を含むインスリンアナログか又はリジン残基を含む最大4つのアミノ酸残基のペプチド残基がA21アミノ酸残基のC末端に結合するインスリンアナログであるアシル化インスリンアナログであって、アシル部分がA22位置のリジン残基に取り付けられたアルキレングリコール部分又はA21アミノ酸残基のC末端終端に取り付けられたペプチド残基に存在するリジン残基に取り付けられたアルキレングリコール部分を含み、インスリンアナログには単一のリジン(K、Lys)が存在することを特徴とする、都合良く肺に投与されうるアシル化インスリンアナログ。 (もっと読む)
アミノ酸含有アルキレングリコール反復単位を含むアシル部を有するインスリン
アシル部分が親インスリンに取り付けられており、前記アシル部分がアミノ酸含有アルキレングリコール反復単位を含むアシル化インスリンであって、親インスリンにリジン残基(K及びLys)が一つのみあり、肺投与される際に申し分のない特性を有するアシル化インスリンに関する。 (もっと読む)
免疫調節性ペプチド
IgGは、病原体に対する保護の仲介、並びに組織、粘膜、及び皮膚表面への免疫系構成要素の漸増を促進するアレルギー性反応及び炎症性反応の仲介で重要な役割を果たす。本発明は、いくつかの実施形態で、ヒトFcRnに結合し、IgGのFc部分がFcRnに結合するのを阻害し、それにより血清IgG濃度を調節する、親水性ポリマーで誘導体化したペプチドに関する。開示された組成物及び方法は、いくつかの実施形態で、例えば、自己免疫疾患及び炎症障害を治療する際に使用され得る。本発明はまた、更なる実施形態で、本発明のペプチドを使用する方法及び作製する方法に関する。 (もっと読む)
コラーゲン関連ペプチド及びその使用
本発明は、コラーゲン模倣3重らせん及びその原線維に非共有的自己集合できる、N−及びC−末端に疎水性アミノ酸を有するコラーゲン関連ペプチド(CRP)、並びにその合成、使用方法及び組成物に関する。 (もっと読む)
ペグ化ポリペプチドの精製
本発明は、同じ型の陽イオン交換材料を両方の陽イオン交換クロマトグラフィー工程において使用する、2つの陽イオン交換クロマトグラフィー工程を含む、モノペグ化エリスロポエチンの精製のための方法、及び実質的に均質な形態のモノペグ化エリスロポエチンを産生するための方法を含む。 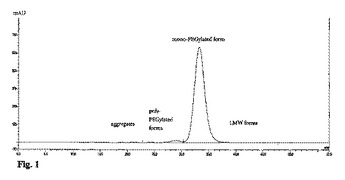 (もっと読む)
(もっと読む)
プロテアーゼに対して安定しているペグ化インスリンアナログ
プロテアーゼに対する耐性を示す新規のペグ化されたインスリンアナログは、効果的に、肺又は口腔に投与することができる。インスリンアナログはB25H及びA14E又はA14Hを含む。B29Kでペグ化されている。  (もっと読む)
(もっと読む)
ヒト膵臓ポリペプチド(HPP)類似体および摂食行動に対するそれらの影響
1つまたは複数の残基におけるアミノ酸置換の点で天然ヒト膵臓ポリペプチドと異なるヒト膵臓ポリペプチドの類似体、また1つまたは複数の前記化合物の使用、1つまたは複数の前記化合物を使用する方法、1つまたは複数の前記化合物を含む組成物、および前記化合物を作製する方法。 (もっと読む)
核酸、アビジン及びポリマーのナノ組織化複合体、その使用並びに調製法
本発明は、核酸とアビジンとの高親和性相互作用によって形成される中心核からなる新規なナノ組織化複合体であって、前記核を水溶液中、生理食塩水中においてさえ安定化し、核自体を全体的または部分的に覆うことが可能な適当なポリマー剤によって更なる非特異的かつ不要な相互作用から核を保護する前記ナノ組織化複合体を開示するものである。得られたナノ複合体は、水溶液中で安定でありナノ粒子の特徴を有することが示された。更に、ナノ複合体はバイオテクノロジー分野及びナノ医療における使用に有用な特性を示した。 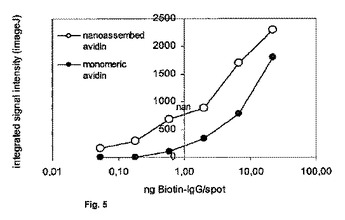 (もっと読む)
(もっと読む)
組織炎症及び発癌を治療するためのグアニル酸シクラーゼ受容体アゴニスト
【課題】哺乳動物被験者の炎症性、前癌性又は癌性組織又はポリープを治療する方法を開示する。
【解決手段】この治療は、グアニル酸シクラーゼ受容体の少なくとも1つのペプチドアゴニストの組成物、及び/又はcGMPの細胞内生成を増大させる他の小分子を投与することを含む。グアニル酸シクラーゼ受容体のこの少なくとも1つのペプチドアゴニストは、単独で、あるいはcGMP依存性ホスホジエステラーゼの阻害剤と組み合わせて投与することができる。該阻害剤は、cGMPの分解を阻害する小分子、ペプチド、タンパク質、又は他の化合物であってよい。特定の作用機構を必要とせずに、この治療は、上皮細胞の被験個体群における増殖とアポトーシスの間の健全なバランスを回復させ、発癌を抑制することもできる。したがって、この方法を使用して、とりわけ、腸の炎症障害、全身性の器官炎症及び喘息を含めた炎症、及び肺、胃腸管、膀胱、精巣、前立腺及び膵臓の発癌、又はポリープを特に治療することができる。
(もっと読む)
MDL−1の使用
本発明は、骨吸収障害をMDL−1のアンタゴニストで治療する方法を提供する。本発明は、MDL−1活性の調節によって骨格および免疫の障害を治療するための方法に関する。例えば、本発明により、対象の骨吸収を調節する方法であって、該対象にMDL−1(配列番号2または4)に特異的に結合する抗体またはその抗体断片の有効量を投与することを含む方法が提供される。本発明により、対象の骨吸収を調節する方法であって、該対象に溶解性のMDL−1タンパク質(配列番号2または4)の有効量を投与することを含む方法もまた提供される。 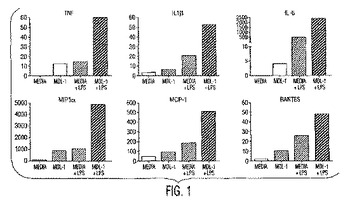 (もっと読む)
(もっと読む)
インフルエンザを阻害する組成物および方法
本発明は、インフルエンザ感染症の治療もしくは予防、またはインフルエンザ感染症の個人間での伝染の予防に有用なペプチド、ペプチド類似体、ペプチド誘導体、および薬学的組成物を提供する。本発明のペプチドは、野生型インフルエンザ血球凝集素2タンパク質の融合開始領域(FIR)のインフルエンザウイルス−細胞融合阻害部分、またはその変異体を含む。好ましい実施形態において、本発明のペプチドは、野生型インフルエンザ血球凝集素2タンパク質の部分の8〜40個の連続したアミノ酸残基、またはその変異体からなり、タンパク質の部分は、タンパク質のFIR、ならびにFIRのアミノ末端側およびカルボキシ末端側にある最大5個のアミノ酸残基を含む。 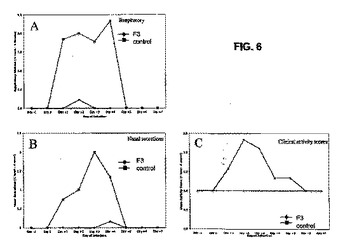 (もっと読む)
(もっと読む)
Apo−2リガンド
【課題】本発明は一般的に哺乳動物細胞アポトーシスを誘導するここで「Apo-2リガンド」として表される新規なサイトカインの同定、単離、及び組換え生産に関し、およびApo-2リガンド抗体と該組成物を用いる方法に関する。
【解決手段】哺乳動物細胞アポトーシスを誘導するApo-2リガンドと名付けられたサイトカインが提供される。該Apo-2リガンドは、TNFサイトカインファミリーのメンバーであると考えられる。Apo-2リガンドキメラ、Apo-2リガンドをコードする核酸、そしてApo-2リガンドに対する抗体を含む組成物もまた提供される。アポトーシスを誘導するための、そしてガンのような病理学上のコンディションを治療するためのApo-2リガンドの使用法もさらに提供される。
(もっと読む)
組換えヒトインターフェロン様タンパク質
本願は組換えヒトインターフェロン様タンパク質に関する。一実施形態では、遺伝子シャッフリング技術により作製された組換えタンパク質は、自然発生的なヒトインターフェロンアルファ2b(HuIFN−α2b)と比較して高い抗ウイルス活性及び抗増殖活性を有する。本発明は、前記タンパク質及び組換えベクターをコードするポリヌクレオチド、及び前記ポリヌクレオチドを有する宿主細胞を包含する。好ましくは、前記ポリヌクレオチドは、それぞれが配列番号1に対して少なくとも93%同一である配列を含むポリヌクレオチドの群より選択され、前記タンパク質は、それぞれが配列番号2に対して少なくとも85%同一であるアミノ酸を含むタンパク質の群より選択される。前記タンパク質及び前記タンパク質からなる組成物は、ウイルス性疾患及び癌のような、インターフェロン療法に対して反応性であるの病気の治療に使用され得る。 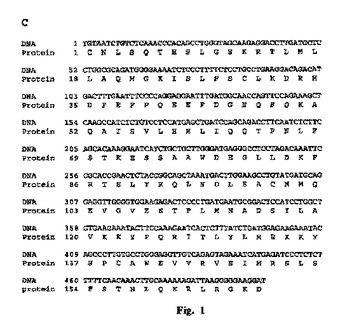 (もっと読む)
(もっと読む)
部位特異的なペグ化をされた直鎖状のサケカルシトニン類似体
本発明は、部位特異的なペグ化をされた直鎖状のサケカルシトニン類似体又はその薬剤的に容認できる塩類、前記類似体又は前記塩類の調製方法、前記類似体又は前記塩類を含んだ医薬組成物、及び、例えば骨粗鬆症等の骨代謝と付随する疾患の治療又は予防に対する薬物の調製のための前記類似体又は前記塩類の使用に関する。 (もっと読む)
免疫グロブリン定常領域Fc受容体結合因子
免疫学的に活性な生体模倣薬の組換えおよび/または生化学的創製によって、IVIG代替化合物を誘導する。次に、これらの代替化合物をin vitroでスクリーニングして、それぞれの代替化合物の免疫機能調節の効率を評価する。さらにin vivoでの確認と投与量/投与の最適化のために、特定の代替化合物を選択する。最後に、この代替化合物を使用して、炎症性疾患や自己免疫疾患を含む多岐にわたる疾患を治療する。 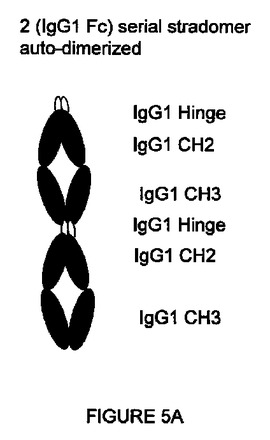 (もっと読む)
(もっと読む)
活性成分を制御放出するための自己沈澱製剤
本発明は、少なくとも一つの活性成分(AP)を数日または数週間の持続期間にわたって放出するための新規の製剤に関するものである。
本発明は、第1態様において、少なくとも一つの活性成分(AP)とポリマー(PO)のコロイド粒子を基にした水性懸濁液とを備える液体製剤に関するものであり、前記製剤は、以下の4つの条件:
(a)ポリマー(PO)が、グルタミン酸残基を含むポリアミノ酸であり、ここで、
一部のグルタミン酸残基は、それぞれがペンダントの陽イオン基(CG)を有し、前記陽イオン基は、互いに同一でも異なっていてもよく、
他のグルタミン酸残基は、それぞれがペンダントの疎水基(GH)を有し、前記疎水基(GH)は、互いに同一でも異なっていてもよいこと、
(b)前記製剤のpHのpHf値が、3.0〜6.5の間であること;
(c)前記pHf値にて、ポリマー(PO)が、活性成分(AP)と自発的に非共有で会合しているコロイド溶液を形成すること;
(d)1mlの前記製剤が、体積1mlのテスト緩衝溶液Tpと混合する間に沈殿すること、
を満たす。
本発明はまた、かかる製剤を調製する方法と、かかる製剤を含む薬剤を調製する方法とに関するものである。
(もっと読む)
癌の処置のための生物学的な標的基の改変
本発明は、ポリマー化学の分野、およびさらに詳細には、クリック官能化標的化合物およびこれを用いる方法に関する。本発明によって提供される標的基は、PEG末端基の反対側に結合されるかまたは薬物担体内にカプセル化されているタンパク質、ウイルス、DNAプラスミド、オリゴヌクレオチド(例えば、siRNA,miRNA、アンチセンス治療剤、アプタマーなど)、薬物、色素、および一次または二次標識の細胞特異的送達のために、PEGの官能化末端基または薬物担体に結合されてもよい。 (もっと読む)
B7様分子およびその使用
【課題】本発明は、B7様(B7−L)ポリペプチドおよびこれをコードする核酸分子ならびにこれらを含有する組成物を提供することを、課題とする。
【解決手段】ATCC寄託番号PTA2481におけるDNA挿入物を提供することによって、上記課題は解決された。本発明はまた、B7−Lポリペプチドを産生するための、選択的結合因子、ベクター、宿主細胞、および方法を提供する。本発明はさらに、B7−Lポリペプチドに関連する疾患、障害、および状態の、診断、処置、改善、および/または予防のための薬学的組成物を提供する。本発明はさらに、B7−Lポリペプチドに関連する疾患、障害、および状態の、診断、処置、改善、および/または予防のための方法を提供する。
(もっと読む)
修飾されたアネキシン蛋白質および血栓症を防ぐための方法
【課題】修飾されたアネキシン蛋白質、好ましくはアネキシンVを用いることにより出血を増加させることなしに血栓症を防ぐ。
【解決手段】血栓症を変調させる修飾アネキシン蛋白質をスクリーニングする方法であって、a)血栓症試験システムを、血栓症を許容する条件下で、少なくとも一つの修飾されたアネキシン蛋白質に接触させ;b)上記試験修飾アネキシン蛋白質の存在下で抗血栓活性を評価し;そしてc)試験修飾アネキシン蛋白質の存在下での抗血栓活性を、試験修飾アネキシン蛋白質の不在下での抗血栓活性と比較し、試験修飾アネキシン蛋白質の存在下での抗血栓活性の変化が血栓症を変調させる修飾アネキシン蛋白質の指標である、上記方法が提供される。
(もっと読む)
ポリ(アミノ酸)ターゲッティング部分
本発明は、概して、ポリマーおよび高分子、特に、ナノ粒子などの粒子中で有用なポリマーに関する。本発明の一態様は、所望の特性を有するナノ粒子を開発する方法を対象とする。実施形態の一セットでは、本方法は、高度に制御された特性を有するナノ粒子のライブラリーを作製するステップを含み、これは、種々の割合の2種以上の高分子を一緒に混合することによって形成できる。1種以上の高分子は、生体適合性ポリマーの一部のポリマーコンジュゲートであり得る。いくつかの場合には、ナノ粒子は、薬物を含み得る。本発明のその他の態様は、ナノ粒子ライブラリーを用いる方法を対象とする。  (もっと読む)
(もっと読む)
201 - 220 / 498
[ Back to top ]



