Fターム[4H045FA61]の内容
Fターム[4H045FA61]に分類される特許
41 - 60 / 112
癌の処置におけるヘミアスタリン誘導体およびその利用法
【課題】種々のヘミアスタリン誘導体を入手しその治療効果を試験するための合成方法論を開発すること。
【解決手段】本発明は、癌の処置における、式(I)を有する化合物:そしてさらに、その合成のための方法およびその使用のための方法を提供し、ここで、R1〜R7、X1、X2、R、Q、およびnは、本明細書中で定義される通りである。新規のヘミアスタリンアナログを開発し、その癌の処置のための治療薬剤としてのその能力を評価する必要が、依然として存在する。本発明は、一般式(I)の新規の化合物を提供し、そしてこれらの合成方法および癌の処置におけるこれらの使用方法をさらに提供し、ここで、R1〜R7、X1、X2、R、Q、およびnは、本明細書中で規定される通りである。本発明の化合物はまた、血管形成術またはステント術のような、外傷を受けがちな血管の再狭窄の予防における用途を見出す。
(もっと読む)
ケージドペプチドの合成法
【課題】ペプチドに関するケージド化合物を提供する。
【解決手段】下記式(I)
(式中、R1はアミノ基の保護基を示す。AはGly,Pro以外のペプチドを構成するαアミノ酸の側鎖を示す。Bはαアミノ酸の側鎖を示す。Raは光解離性保護基を示す。)で表されるN保護ジペプチド化合物を、固相合成においてN保護アミノ酸の代わりに使用することを特徴とする、光解離性保護基を主鎖に導入したペプチドの固相合成法。
(もっと読む)
増殖抑制作用を有するペプチド
本発明は、増殖抑制作用を有する、配列番号1、配列番号2又は配列番号3の配列のペプチドに関するものである。 (もっと読む)
チャネル活性化プロテアーゼ阻害剤である化合物および組成物
本発明は、チャネル活性化プロテアーゼを調節するために有用な式(I)で示される化合物およびその医薬的に許容される塩、水和物、溶媒和物、立体異性体および医薬組成物および、これに限定するものではないが、プロスタシン、PRSS22、TMPRSS11(例えば、TMPRSS11B、TMPRSS11E)、TMPRSS2、TMPRSS3、TMPRSS4(MTSP−2)、マトリプターゼ(MTSP−1)、CAP2、CAP3、トリプシン、カテプシンA、または好中球エラスターゼを含むチャネル活性化プロテアーゼに関連する病状を処置、改善または予防するためにこの化合物を使用する方法を提供する。 (もっと読む)
ポリマー修飾合成タンパク質
【課題】組換えDNA法とは別個のもので、ポリマー修飾が可能なポリマーを形成するために利用できる、生物活性タンパク質の生成法およびポリマー。
【解決手段】ポリマー修飾合成生物活性タンパク質、それらを含む医薬組成物およびそれらの製法及び使用法。ポリマー修飾合成生物活性タンパク質は化学的合成によって形成され、生物学的に産生されたタンパク質とは異なる。具体的には、式 “タンパク質”−n個のU−B−“ポリマー”の分離された合成ポリマー修飾生物活性タンパク質を含有する組成物。上記式中、Uは、1個以上の重なり合わないペプチドセグメントの1個以上のアミノ酸の1から6個の側鎖に共有結合する化学群であり、Bは、同一または異なる、3個以上のアームを有する分岐コアであり“ポリマー”は水溶性ポリアミドポリマーである、合成ポリマー修飾生物活性タンパク質を含有する組成物である。
(もっと読む)
リソバクチン誘導体の製造法
分子内環化による、下記式(I)
【化1】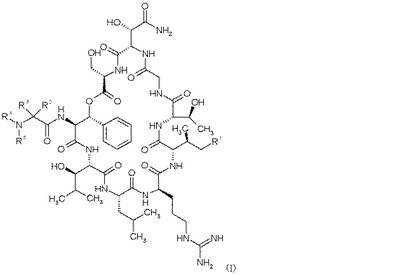
を有する環状デプシペプチドの製造法。 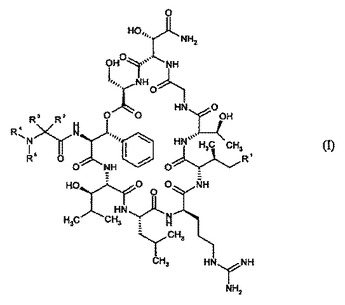 (もっと読む)
(もっと読む)
新規な機能性ペプチド核酸およびその製法
【課題】コストパフォーマンスに優れ、かつ機能性分子を超高速に導入することができる、機能性PNAの新規合成方法およびそれに用いる化合物の提供。
【解決手段】機能性PNAオリゴマーを製造する方法であって、保護基によって保護されたアデニン、グアニン、シトシンまたはチミンを有するPNAモノマーユニットを、Fmoc−ω−アミノ酸−BocPNA−OHと反応させてPNAオリゴマーを合成した後、該PNAオリゴマーに遊離カルボン酸を有する機能性分子を導入し、さらに前記保護基の脱保護を行うことによって、機能性PNAオリゴマーを製造することを含む特徴とする前記方法、該方法によって合成される化合物および前駆体的PNAモノマーユニットとして機能するFmoc−ω−アミノ酸−BocPNA−OH。
(もっと読む)
「擬似」天然型化学的ライゲーション
【課題】アミド結合を介し、より広範なペプチド、ポリペプチド、他のポリマーおよび他の分子のライゲーションを可能にするために天然型化学的ライゲーションの技法を拡大するための方法および組成物の提供。
【解決手段】側鎖が式−S−Raaを有し、該式中、Raaは、表Iの擬似Asp、擬似Gln、擬似Asn、擬似Ser、擬似Thr、擬似Lys、擬似Arg、擬似Met、擬似Phe、擬似Tyr、擬似ホスホtyr、擬似Dopa、擬似Gla、擬似His、擬似Trp、擬似Leu、擬似Val、擬似Ile、擬似N−(エチル)トリフルオロアセトアミド、擬似SBF、及び擬似メチルSBF、から成る群より選択される擬似アミノ酸残基を含有する合成タンパク質。
(もっと読む)
金属イオン結合能およびナノチューブ形成能を有する環状ペプチドと、それを用いたペプチドで構成されるナノチューブ、並びにそれらの製造方法。
【課題】規則的な微細構造で中空構造を有するナノメートルスケールのナノチューブを形成する新規環状ペプチドの配列、当該配列を成す物質のナノチューブ形成条件を提供する。
【解決手段】環状ペプチドの環内部に金属イオンを配位させるため、3残基連続して同じ光学異性体が並んだ領域を2つ連続せずに配置し、それ以外のアミノ酸はL−体とD−体が交互に配された配列を持たせることにより、3残基の真ん中のアミノ酸は環内部を向き、その位置に金属イオンと配位結合するHis、Aspなどのアミノ酸を設定するように設計する。環状ペプチドは特定条件下で自己組織化的に会合し、金属イオンを環内部に配位させながらナノチューブを形成するため、ナノチューブ内に一次元的に金属イオンを配列化させることができることで、機能的なナノ素材、ナノ材料へ応用が可能である。
(もっと読む)
アレルギーを診断するエピトープポリペプチド
【課題】本発明は、簡便で正確なアレルギー疾患の診断法を提供することを目的とする。
【解決手段】本発明は卵アレルギーの診断のために有用なPro-Val-Cys-Gly-Thr-Asp-Gly-Val-Thr、Pro-Ile-Cys-Gly-Thr-Asp-Gly-Val-Thr、またはGly-Gly-Cys-Arg-Lys-Glu-Leu-Ala-Ala-Valで表されるアミノ酸配列のポリペプチドに関する。本発明はまたアレルギー疾患の診断薬のスクリーニング方法であって、診断対象のアレルギー疾患のアレルゲンに特異的なIgEを有し且つアレルギー症状を示す患者の前記IgEにより認識されるエピトープのアミノ酸配列(1)と、診断対象のアレルギー疾患のアレルゲンに特異的なIgEを有し且つアレルギー症状を示さない患者の前記IgEにより認識されるエピトープのアミノ酸配列(2)とを比較し、アミノ酸配列(1)を含むポリペプチドを選択することを特徴とする方法に関する。
(もっと読む)
自己組織化ペプチド
【課題】種々の機械的特性を有する自己組織化ペプチドゲル及び該ゲルの機械的特性を制御する新たな方法を提供すること。
【解決手段】式:A *1 B *2 Cで表される構造を含んでなり、水系媒体中においてβ-シート構造を形成する自己組織化ペプチド(X)[式中、AがN末端側であり、A、B及びCは、それぞれ非極性アミノ酸残基と酸性アミノ酸残基と塩基性アミノ酸残基とを含有するドメインであり、ドメインA、B及びCの両末端は、それぞれ独立して酸性アミノ酸残基又は塩基性アミノ酸残基であり、ドメインA及びCにおいては、酸性アミノ酸残基及び塩基性アミノ酸残基がβ−シート構造の一方の面(a)のみにそれぞれ独立して1個以上配置され、ドメインBにおいては、酸性アミノ酸残基及び塩基性アミノ酸残基がβ−シート構造の他方の面(b)のみにそれぞれ独立して1個以上配置され、*1及び*2は、それぞれ独立してペプチド結合又は非極性アミノ酸残基のみを含有するドメインである]。
(もっと読む)
ペプチド合成におけるマイクロ波により向上されたN−FMOC脱保護
【課題】脱保護反応により簡単にペプチド合成を実施する方法を提供する。
【解決手段】脱保護反応に対してマイクロ波照射を適用すると同時に、Fmoc保護アミノ酸をピペラジンにより脱保護することを含み、固相ペプチド合成方法を用いて、脱保護、活性化、及びカップリングのサイクルを繰り返し、連続するアミノ酸を付加して所望のペプチドを形成する方法。マイクロ波エネルギーを適用することでペプチド及びアミノ酸の分解を防止することができる。
(もっと読む)
連続合成装置および方法
【課題】 原料の成分の濃度を一定にした状態で反応を進行させ、効率よく連続ペプチド合成を行うことができる連続合成装置を提供する。
【解決手段】 この連続合成装置は、水溶性縮合剤と、N保護アミノ酸およびC保護ペプチドの混合液とを連続流れで混合し反応させる混合反応手段5と、合成後の液中から未反応の水相成分を分離し除去する油水分離手段6と、水相成分が除去された有機相成分液中に水素ガスを混合させ、触媒を介して生成したペプチドの脱保護反応を行う気体触媒反応手段7とを有する。
(もっと読む)
フッ素化アミノ酸を含有するタンパク質及びその使用方法
本発明の1つの態様は、少なくとも1つのフッ素化アミノ酸を含むポリペプチドに関する。本発明の別の態様は、第1のポリペプチドを修飾する方法に関し、前記第1のポリペプチド中の少なくとも1つのアミノ酸を、フッ素化アミノ酸で置換することにより、前記第1のポリペプチドに対して増大した安定性を有する第2のポリペプチドを生成することを含む。 (もっと読む)
テンプレート固定ペプチド擬似体
一般式(I)[式中、Zは12個のα−アミノ酸残基のテンプレート固定鎖であり、これらのアミノ酸残基は、鎖中の残基の位置(N末端アミノ酸から開始して数えた位置)に応じて、Gly、もしくはProであるか、または特定のタイプの残基であり、上の式中の残りの記号と同様に、本明細書および特許請求の範囲に定義されている]で表わされるテンプレート固定β−ヘアピンペプチド擬似体およびその塩は、シュードモナス・アエルギノーザ[Pseudomonas aeruginosa](緑膿菌)のような微生物の増殖を選択的に阻害する、またはそれを殺す特質を有する。これらは、食品、化粧品、医薬品、および他の栄養素含有材料用の殺菌薬として、または感染を治療または予防するための医薬として用いることができる。こうしたβ−ヘアピンペプチド擬似体は、混合型固相・液相合成法に基づいた方法により製造することができる。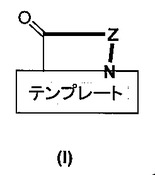 (もっと読む)
(もっと読む)
GLP−1のポリマ複合体
GLP−1部分の複合体は1つ以上の水溶性ポリマと共有結合している場合がある。例えば、GLP−1ポリマ複合体は、N末端で水溶性ポリマに解放可能に付着しているGLP−1部分を含んでいる場合がある。GLP−1ポリマ複合体は、GLP−1部分がN−メチル置換基を保有する水溶性ポリマと共有結合しているGLP−1部分を含む場合がある。GLP−1ポリマ複合体は、GLP−1部分がポリマ付着部位で、ポリマ付着部位から分離した部位でGLP−1部分がグリコシル化された水溶性ポリマと共有結合しているGLP−1部分を含む場合がある。 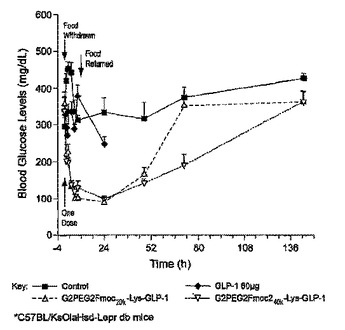 (もっと読む)
(もっと読む)
非天然アミノ酸およびそれらのニューロテンシンアナログ
本発明は、非天然デスアミノアミノ酸化合物、作成方法、およびそれらのN末端部分としてこれらの化合物を含有するペプチドに関する。好ましい一例は、N末端がαデスアミノN,Nジメチルホモリシン残基であるニューロテンシン(8−13)である。 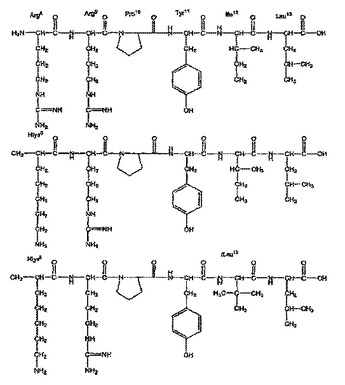 (もっと読む)
(もっと読む)
巨大環状のキレート化剤によるビオチンジアミノ誘導体およびその複合体
各基が明細書に定義されている式(I)の化合物、その調製方法、および、ヒトおよび動物の治療および診断、特に腫瘍などの病状の診断および治療のための放射性核種との複合体の調製のためのその使用を記載する。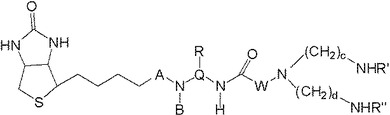
(I) 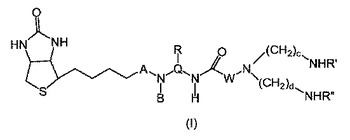 (もっと読む)
(もっと読む)
治療的介入のためのY4選択性レセプターアゴニスト
[Ala30]PP2-36、[Thr30]PP2-36、[Asn30]PP2-36、[Gln30]PP2-36、[Glu10]PP2-36、[Glu10,Leu17,Thr30]PP2-36、[Nle17,Nle30]PP2-36、[Glu10,Nle17,Nle30]PP2-36、それらのPP1-36等価物、並びに本明細書に記載のそれらのアナログ及び誘導体からなる群より選択されるY4レセプターアゴニストペプチドは、Y1レセプター及びY2レセプターよりY4レセプターの選択性アゴニストであり、治療、例えば、肥満及び過体重、これらが主因とされる症状の治療、並びに下痢又は腸の過剰分泌の治療に有用である。 (もっと読む)
特異的に保護された直交ランチオニン技術
本発明は、少なくとも1つの分子内架橋を含む分子内架橋ポリペプチドの合成法を提供する。本発明は、さらに、2つの分子内架橋を含む分子内架橋ポリペプチドの合成法であって、2つの分子内架橋が重なり合う環、連続する2つの環、または2つの埋め込まれている環の形成法を提供する。本発明は、また、ナイシンAを含むランチビオティックの合成法を提供する。さらに、本発明は、本明細書に開示された方法によって合成される分子内架橋ポリペプチド、および特異的に保護された直交ランチオニンを提供する。 (もっと読む)
41 - 60 / 112
[ Back to top ]